文档内容
3.4.1 难溶电解质的沉淀溶解平衡 练习(原卷版)
一.选择题(共14小题)
1.25℃时CaCO 溶于水达饱和,其物质的量浓度为5.0×10﹣5mol•L﹣1,该温度下CaCO 的K 为(
3 3 sp
)
A.5.0×10﹣5 B.2.5×10﹣9 C.5.0×10﹣10 D.1.0×10﹣10
2.已知 相同温度下:K [Zn(OH) ]>K (ZnS),K (MgCO )>K [Mg(OH) ]; 电
sp 2 sp sp 3 sp 2
离出S①2﹣的能力:FeS>H S>CuS.则下列离子方程式错误的是( ) ②
2
A.将FeS加入稀盐酸中:FeS+2H+═Fe2++H S↑
2
B.向CuSO 溶液中通H S气体:Cu2++H S═CuS↓+2H+
4 2 2
C.将ZnCl 溶液和Na S溶液混合:Zn2++S2﹣+2H O═Zn(OH) ↓+H S↑
2 2 2 2 2
D.向少量Mg(HCO ) 溶液中加入足量NaOH溶液:Mg2++2HCO ﹣+4OH﹣═Mg(OH)
3 2 3
↓+2CO 2﹣+2H O
2 3 2
3.某化学兴趣小组进行下列实验:
将0.1mol•L﹣1的MgCl 溶液和0.5mol•L﹣1的NaOH溶液等体积混合得到浊液
2
①取少量 中浊液,滴加0.1mol•L﹣1的FeCl 溶液,出现红褐色沉淀
3
②过滤 ①中浊液,取少量白色沉淀,滴加0.1mol•L﹣1的FeCl 溶液,白色沉淀变为红褐色沉淀
3
③另取①少量白色沉淀,滴加饱和NH
4
Cl溶液,沉淀溶解
④下列说法中错误的是( )
A.将 中浊液过滤,所得滤液中有微量的Mg2+存在
B.实验① 和 均能说明Fe(OH)
3
比Mg(OH)
2
难溶
C. 中②沉淀③转化反应式为:3Mg(OH)
2
(s)+2Fe3+(aq) 2Fe(OH)
3
(s)+3Mg2+(aq)
D.③NH 4 Cl溶液中的NH 4 +水解可能是 中沉淀溶解的原因 ⇌
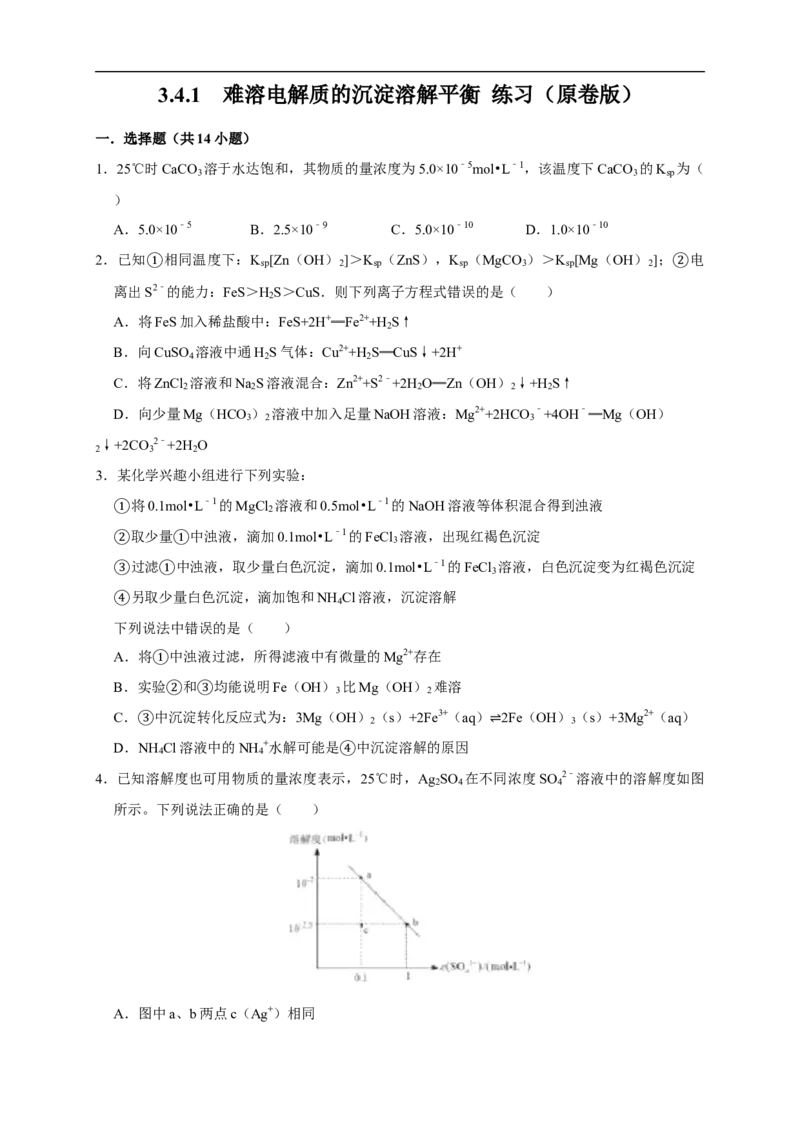
4.已知溶解度也可用物质的量浓度表示④,25℃时,Ag SO 在不同浓度SO 2﹣溶液中的溶解度如图
2 4 4
所示。下列说法正确的是( )
A.图中a、b两点c(Ag+)相同B.把a点的溶液加热蒸发掉一部分水,恢复到室温,可得到b点的溶液
C.该温度下,Ag SO 溶度积的数量级为10﹣5
2 4
D.在c点的溶液中加入少量Na SO 固体,溶液可变为a点
2 4
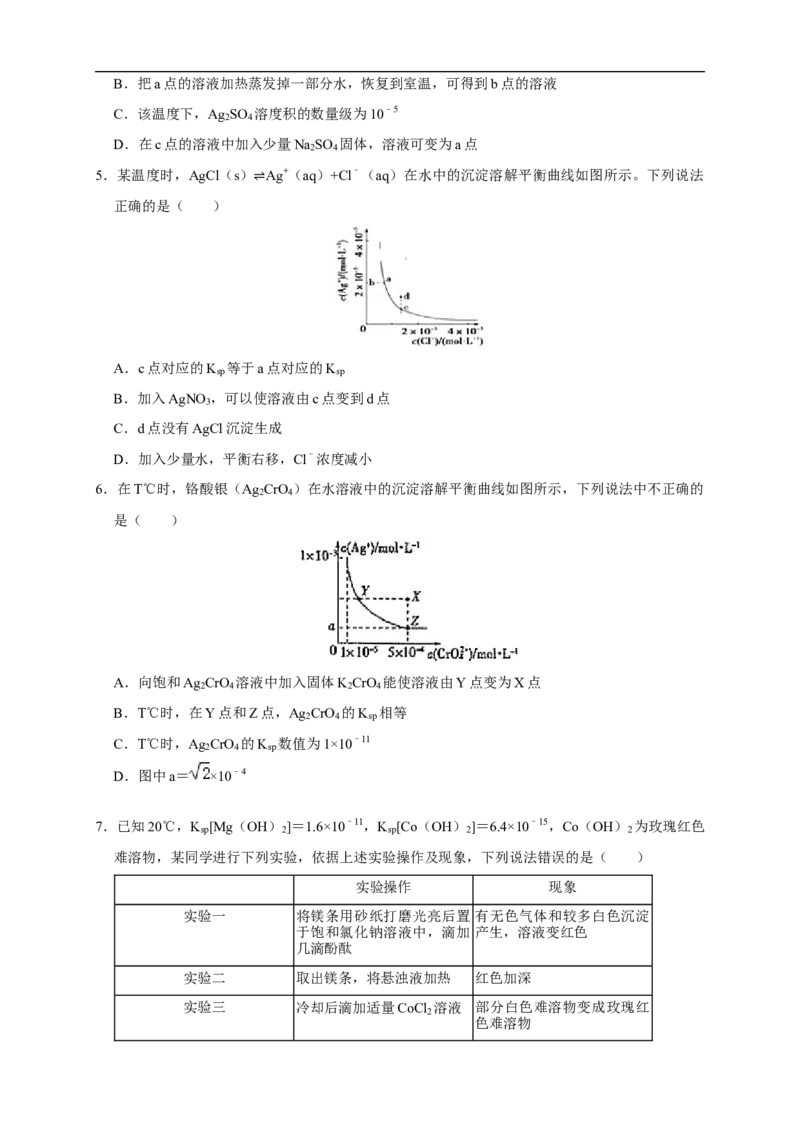
5.某温度时,AgCl(s) Ag+(aq)+Cl﹣(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法
正确的是( ) ⇌
A.c点对应的K 等于a点对应的K
sp sp
B.加入AgNO ,可以使溶液由c点变到d点
3
C.d点没有AgCl沉淀生成
D.加入少量水,平衡右移,Cl﹣浓度减小
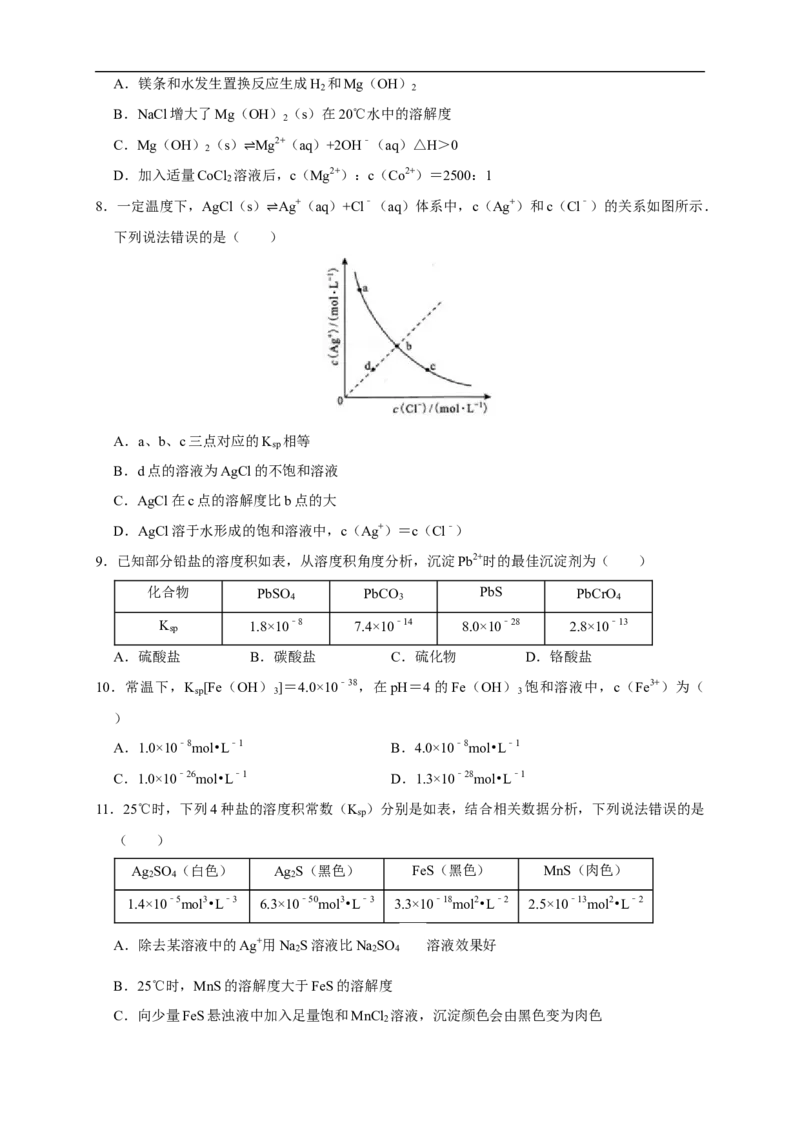
6.在T℃时,铬酸银(Ag CrO )在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的
2 4
是( )
A.向饱和Ag CrO 溶液中加入固体K CrO 能使溶液由Y点变为X点
2 4 2 4
B.T℃时,在Y点和Z点,Ag CrO 的K 相等
2 4 sp
C.T℃时,Ag CrO 的K 数值为1×10﹣11
2 4 sp
D.图中a= ×10﹣4
7.已知20℃,K [Mg(OH) ]=1.6×10﹣11,K [Co(OH) ]=6.4×10﹣15,Co(OH) 为玫瑰红色
sp 2 sp 2 2
难溶物,某同学进行下列实验,依据上述实验操作及现象,下列说法错误的是( )
实验操作 现象
实验一 将镁条用砂纸打磨光亮后置 有无色气体和较多白色沉淀
于饱和氯化钠溶液中,滴加 产生,溶液变红色
几滴酚酞
实验二 取出镁条,将悬浊液加热 红色加深
实验三 冷却后滴加适量CoCl 溶液 部分白色难溶物变成玫瑰红
2
色难溶物A.镁条和水发生置换反应生成H 和Mg(OH)
2 2
B.NaCl增大了Mg(OH) (s)在20℃水中的溶解度
2
C.Mg(OH) (s) Mg2+(aq)+2OH﹣(aq)△H>0
2
D.加入适量CoCl
2
溶⇌液后,c(Mg2+):c(Co2+)=2500:1
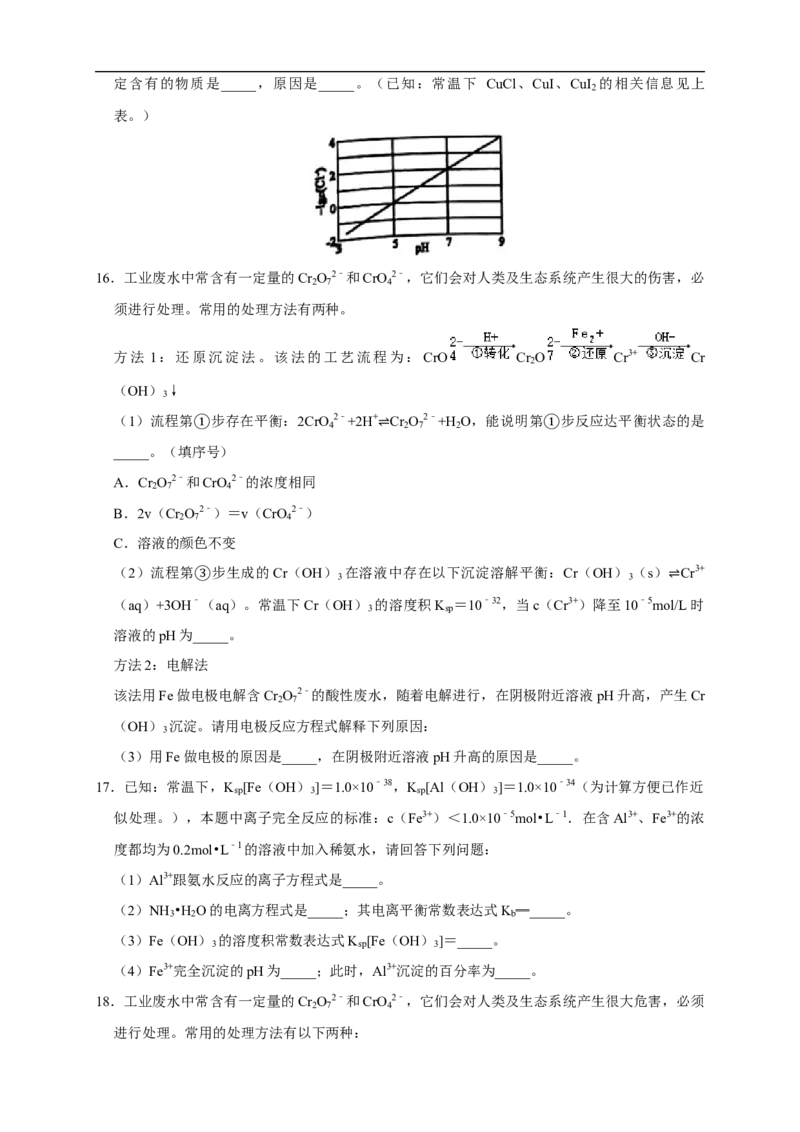
8.一定温度下,AgCl(s) Ag+(aq)+Cl﹣(aq)体系中,c(Ag+)和c(Cl﹣)的关系如图所示.
下列说法错误的是( ⇌)
A.a、b、c三点对应的K 相等
sp
B.d点的溶液为AgCl的不饱和溶液
C.AgCl在c点的溶解度比b点的大
D.AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl﹣)
9.已知部分铅盐的溶度积如表,从溶度积角度分析,沉淀Pb2+时的最佳沉淀剂为( )
化合物 PbSO PbCO PbS PbCrO
4 3 4
K 1.8×10﹣8 7.4×10﹣14 8.0×10﹣28 2.8×10﹣13
sp
A.硫酸盐 B.碳酸盐 C.硫化物 D.铬酸盐
10.常温下,K [Fe(OH) ]=4.0×10﹣38,在pH=4的Fe(OH) 饱和溶液中,c(Fe3+)为(
sp 3 3
)
A.1.0×10﹣8mol•L﹣1 B.4.0×10﹣8mol•L﹣1
C.1.0×10﹣26mol•L﹣1 D.1.3×10﹣28mol•L﹣1
11.25℃时,下列4种盐的溶度积常数(K )分别是如表,结合相关数据分析,下列说法错误的是
sp
( )
Ag SO (白色) Ag S(黑色) FeS(黑色) MnS(肉色)
2 4 2
1.4×10﹣5mol3•L﹣3 6.3×10﹣50mol3•L﹣3 3.3×10﹣18mol2•L﹣2 2.5×10﹣13mol2•L﹣2
A.除去某溶液中的Ag+用Na S溶液比Na SO 溶液效果好
2 2 4
B.25℃时,MnS的溶解度大于FeS的溶解度
C.向少量FeS悬浊液中加入足量饱和MnCl 溶液,沉淀颜色会由黑色变为肉色
2D.向Ag S(s) 2Ag+(aq)+S2﹣(aq)平衡体系中加入少量Na S固体,溶液中c(Ag+)不
2 2
变 ⇌
12.当溶液中离子浓度小于1.0×10﹣5mol•L﹣1时,可视为该离子已完全除去,通过调节溶液 pH的
方法可以除去溶液中的某些杂质离子。常温下,某 0.1mol•L﹣1的NiSO 溶液中含有杂质Al3+和
4
Fe3+,欲将这两种杂质完全除去,需调节溶液pH的范围可以是(不考虑溶液体积变化,已知:
常温时,氢氧化镍K =1×10﹣16、氢氧化铁K =1×10﹣38、氢氧化铝K =1×10﹣33)( )
sp sp sp
A.2~3 B.3~4 C.5~6 D.6~8
13.取1mL 0.1mol•L﹣1AgNO 溶液进行如下实验(实验中所用试剂浓度均为0.1mol•L﹣1),下列
3
说法不正确的是( )
A.实验 白色沉淀是难溶的AgCl
B.若按① 顺序实验,能看到白色沉淀
C.若按②①顺序实验,能看到黑色沉淀
D.由实①验③说明AgI比AgCl更难溶
14.向含有M②gCO
3
固体的浊液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是( )
A.c(Mg2+) B.K (MgCO ) C.c(H+) D.c(CO 2﹣)
sp 3 3
二.解答题(共4小题)
15.向湿法炼锌的电解液中同时加入Cu和CuSO ,可生成CuCl沉淀除去Cl﹣,反应
4
原理如下:
Cu(s)+Cu2++(aq) 2Cu+(aq)△H =ak•mol﹣l
1
Cl﹣(aq)+Cu+(aq)⇌CuCl(s)△H =bkJ•mol﹣l
2
(1)反应Cu(s)+Cu⇌2+(aq)+2Cl﹣(aq)═2CuCl(s)△H=_____。
物质 CuCl CuI Cul
2
K 1.7×10﹣7 1.3×10﹣12 ﹣
sp
颜色 白色 白色 金黄色
(2)实验测得电解液 pH 对溶液中残留(Cl﹣)的影响如图所示。当 pH=7时,溶液中 c
(Cu+)=_____。
(3)兴趣小组在CuCl 溶液中加入过量KI固体,观察到有白色沉淀生成。推测该白色沉淀中一
2定含有的物质是_____,原因是_____。(已知:常温下 CuCl、CuI、CuI 的相关信息见上
2
表。)
16.工业废水中常含有一定量的Cr O 2﹣和CrO 2﹣,它们会对人类及生态系统产生很大的伤害,必
2 7 4
须进行处理。常用的处理方法有两种。
方法 1:还原沉淀法。该法的工艺流程为:CrO Cr O Cr3+ Cr
2
(OH) ↓
3
(1)流程第 步存在平衡:2CrO 2﹣+2H+ Cr O 2﹣+H O,能说明第 步反应达平衡状态的是
4 2 7 2
_____。(填序①号) ⇌ ①
A.Cr O 2﹣和CrO 2﹣的浓度相同
2 7 4
B.2v(Cr O 2﹣)=v(CrO 2﹣)
2 7 4
C.溶液的颜色不变
(2)流程第 步生成的Cr(OH) 在溶液中存在以下沉淀溶解平衡:Cr(OH) (s) Cr3+
3 3
(aq)+3OH﹣③(aq)。常温下Cr(OH) 的溶度积K =10﹣32,当c(Cr3+)降至10﹣5mo⇌l/L时
3 sp
溶液的pH为_____。
方法2:电解法
该法用Fe做电极电解含Cr O 2﹣的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr
2 7
(OH) 沉淀。请用电极反应方程式解释下列原因:
3
(3)用Fe做电极的原因是_____,在阴极附近溶液pH升高的原因是_____。
17.已知:常温下,K [Fe(OH) ]=1.0×10﹣38,K [Al(OH) ]=1.0×10﹣34(为计算方便已作近
sp 3 sp 3
似处理。),本题中离子完全反应的标准:c(Fe3+)<1.0×10﹣5mol•L﹣1.在含Al3+、Fe3+的浓
度都均为0.2mol•L﹣1的溶液中加入稀氨水,请回答下列问题:
(1)Al3+跟氨水反应的离子方程式是_____。
(2)NH •H O的电离方程式是_____;其电离平衡常数表达式K ═_____。
3 2 b
(3)Fe(OH) 的溶度积常数表达式K [Fe(OH) ]=_____。
3 sp 3
(4)Fe3+完全沉淀的pH为_____;此时,Al3+沉淀的百分率为_____。
18.工业废水中常含有一定量的Cr O 2﹣和CrO 2﹣,它们会对人类及生态系统产生很大危害,必须
2 7 4
进行处理。常用的处理方法有以下两种:方法1:还原沉淀法。
该法的工艺流程为:CrO 2﹣ Cr O 2﹣ Cr3+ Cr(OH) ↓。
4 2 7 3
其中第 步存在平衡2CrO 2﹣(黄色)+2H+ Cr O 2﹣(橙色)+H O。
4 2 7 2
(1)若①平衡体系的pH=2,该溶液显_____色⇌。
(2)能说明第 步反应达平衡状态的是_____(填序号)。
A.Cr
2
O
7
2﹣和C①rO
4
2﹣的浓度相同
B.2v(Cr O 2﹣)=v(CrO 2﹣)
2 7 4
C.溶液的颜色不变
(3)第 步中,还原1mol Cr O 2﹣离子,需要_____mol的FeSO •7H O。
2 7 4 2
(4)第②步生成的Cr(OH)
3
在溶液中存在以下沉淀溶解平衡:Cr(OH)
3
(s) Cr3+(aq)
+3OH﹣(③aq),常温下,Cr(OH) 的溶度积 K =c(Cr3+)•c3(OH﹣)=10⇌﹣32,要使c
3 sp
(Cr3+)降至10﹣5mol/L,溶液的pH应调至_____。
方法2:电解法。
该法用Fe做电极电解含Cr O 2﹣的酸性废水,随着电解的进行,在阴极附近溶液pH升高,产生
2 7
Cr(OH) 沉淀。
3
(5)用Fe做电极的原因为_____(用电极反应式解释)。
(6)在阴极附近溶液pH升高,溶液中同时生成的沉淀还有_____。