文档内容
班级 姓名 学号 分数
第 07 单元 有机化合物
(A卷·夯实基础)
(时间:75分钟,满分:100分)
一、选择题(本题共16小题,每小题3分,共48分)
1.下列关于有机物结构特点的说法中,正确的是( )
A.CH 具有正四面体结构 B.碳原子之间只能形成C-C单键
4
C.含碳元素的物质都是有机物 D.碳原子之间只能形成碳链
【答案】A
【解析】A.CH 具有正四面体结构,故A正确;
4
B.碳原子之间能形成碳碳单键,碳碳双键,碳碳三键,故B错误;
C.含碳元素的物质不一定都是有机物,比如CO,故C错误;
D.碳原子之间能形成碳链,也可以形成碳环,故D错误。
综上所述,答案为A。
2.下列化学式及结构式,从成键情况看合理的是
A.CHN: B.CHSO:
3 2
C.CHS: D.CHSi:
4 4
【答案】B
【解析】A.CHN: 中,N原子形成了4个共价键,而C原子只形成3个共价键,与事
3
实不符,A不正确;
B.CHSO: 中,O、S原子的最外层有6个电子,可形成2个共价键,C原子的最外层有
2
4个电子,可形成4个共价键,与事实相符,B正确;
1 / 16
学科网(北京)股份有限公司C.CHS: 中,C原子只形成3个共价键,而S原子却形成了3个共价键,与事实不符,
4
C不正确;
D.CHSi: 中,C、Si的最外层都有4个电子,C、Si原子间应形成双键,D不正确;
4
故选B。
3.以下关于甲烷的说法中,正确的是
①一氯甲烷分子具有四面体结构
②二氯甲烷有两种同分异构体
Cl 1mol H 0.5mol Cl
③甲烷与 2发生光照取代,取代 需 2
④甲烷分子中四个C-H键,任意两个之间的键角均相等
A.②③④ B.②③ C.①④ D.①③
【答案】C
【解析】①一氯甲烷分子为甲烷中一个H原子被Cl取代,C为sp3杂化,但CHCl的结构不对称,为四面
3
体结构,故①正确;
②甲烷为正四面体结构,为立体结构,所以二氯甲烷只有一种,故②错误;
③甲烷与氯气发生一氯取代的方程式为:CH+Cl→CHCl+HCl,取代1molH需要1mol氯气,故③错误;
4 2 3
④甲烷分子中四个碳氢键完全相同,四个C-H键的任意两个之间的键角均相等,故④正确;
故选:C。
4.下列各组有机物中,既不互为同系物,又不互为同分异构体的是
CH CH CH SCH CH CH CH CH CH CH SH
A. 3 2 2 2 3与 3 2 2 2 2
B. 与
CH COOCH CH CH CH COOCH
C. 3 2 3与 3 2 3
CH Cl CCl
D. 2 2与 4
【答案】D
2 / 16
学科网(北京)股份有限公司【解析】A. 两种物质的分子式相同,但结构不同,两者互为同分异构体,A不符合题意;
PH COOH CH
B. 两种物质均含有两种官能团 2和 ,分子组成上相差一个 2原子团,两者互为同系物,
B不符合题意;
C. 两种物质分子式相同,但结构不同,两者互为同分异构体,C不符合题意;
CH
D. 两种物质分子式不同,且分子组成也不是相差若干个 2原子团,两者既不是同系物也不是同分异
构体,D符合题意;
故选D。
5.下列有关简单烷烃的描述,说法错误的是
A.原子间所成的键都是单键
B.都易燃烧,都难溶于水
C.分子组成上满足通式C H (n≥1)
n 2n+2
D.相邻两个烷烃分子组成上相差一个甲基
【答案】D
【解析】烷烃属于饱和烃,碳碳原子间成单键,剩余的价键与氢相连,分子组成上满足通式C H
n 2n+
(n≥1),所有的烷烃均不溶于水,能够燃烧;相邻的两个烷烃分子在组成上相差一个CH 原子团,而不是
2 2
甲基,故A、B、C正确,D错误;
故选D。
6.①②是两种常见烃的球棍模型,下列说法正确的是
A.都能在空气中燃烧 B.都能使酸性高锰酸钾溶液褪色
C.①②所有原子均共平面 D.等质量的①②完全燃烧时,耗氧量相同
【答案】A
【解析】A.①是乙烷、②是乙烯,都能在空气中燃烧生成二氧化碳和水,故A正确;
B.①是乙烷,乙烷不能使酸性高锰酸钾溶液褪色,②是乙烯,乙烯含有碳碳双键,能使酸性高锰酸钾溶
液褪色,故B错误;
C.①是乙烷,其中碳原子是饱和碳原子,形成四面体结构,分子中所有碳原子不可能共平面,故C错误;
D.乙烷、乙烯含碳元素的质量分数不同,等质量的①②完全燃烧时,产生CO 的量不相同,故D错误;
2
3 / 16
学科网(北京)股份有限公司故选A。
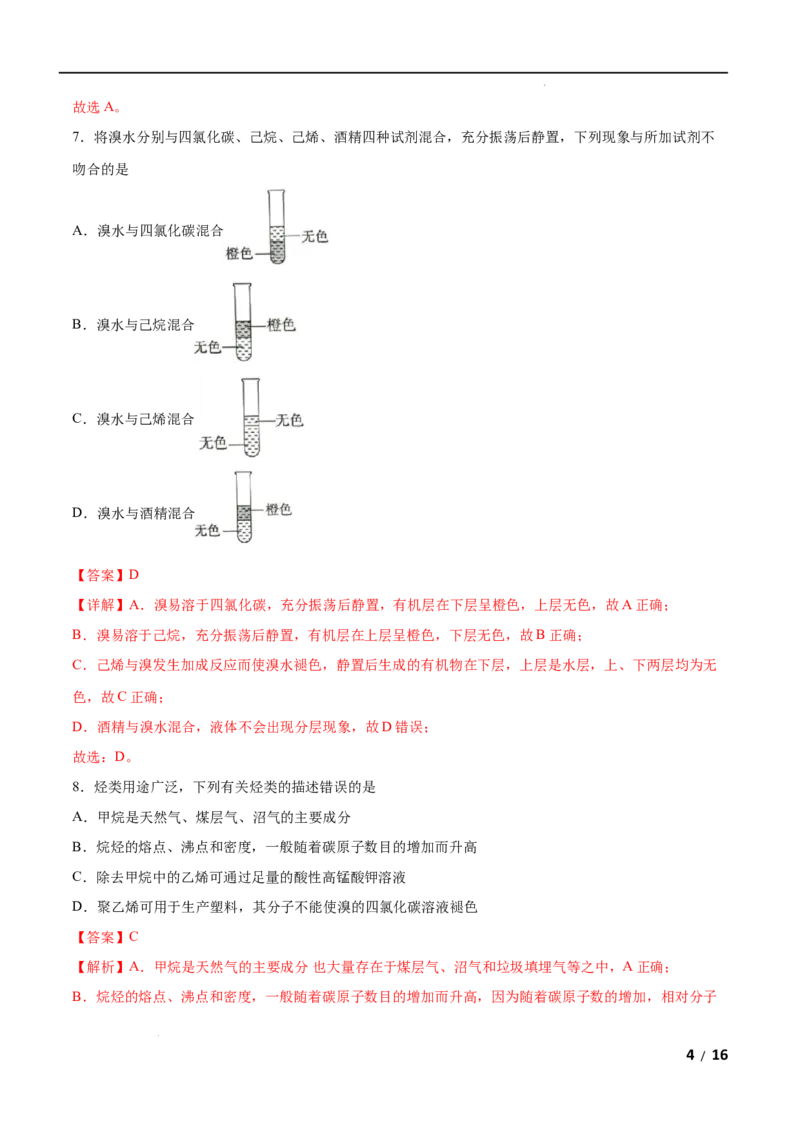
7.将溴水分别与四氯化碳、己烷、己烯、酒精四种试剂混合,充分振荡后静置,下列现象与所加试剂不
吻合的是
A.溴水与四氯化碳混合
B.溴水与己烷混合
C.溴水与己烯混合
D.溴水与酒精混合
【答案】D
【详解】A.溴易溶于四氯化碳,充分振荡后静置,有机层在下层呈橙色,上层无色,故A正确;
B.溴易溶于己烷,充分振荡后静置,有机层在上层呈橙色,下层无色,故B正确;
C.己烯与溴发生加成反应而使溴水褪色,静置后生成的有机物在下层,上层是水层,上、下两层均为无
色,故C正确;
D.酒精与溴水混合,液体不会出现分层现象,故D错误;
故选:D。
8.烃类用途广泛,下列有关烃类的描述错误的是
A.甲烷是天然气、煤层气、沼气的主要成分
B.烷烃的熔点、沸点和密度,一般随着碳原子数目的增加而升高
C.除去甲烷中的乙烯可通过足量的酸性高锰酸钾溶液
D.聚乙烯可用于生产塑料,其分子不能使溴的四氯化碳溶液褪色
【答案】C
【解析】A.甲烷是天然气的主要成分 也大量存在于煤层气、沼气和垃圾填埋气等之中,A正确;
B.烷烃的熔点、沸点和密度,一般随着碳原子数目的增加而升高,因为随着碳原子数的增加,相对分子
4 / 16
学科网(北京)股份有限公司质量增大,分子间作用力越来越大,熔沸点越高,B正确;
C.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,不能除杂,应选溴水洗气,C错误;
D.聚乙烯可用于生产塑料,其分子不能使溴的四氯化碳溶液褪色,因为聚乙烯中没有碳碳双键了,D正
确;
答案选C。
9.下列叙述正确的是
A.高分子材料能以石油、煤等化石燃料为原料进行生产
B.聚乙烯的分子中含有碳碳双键
C.高分子材料中的有机物分子均呈链状结构
D.橡胶硫化的过程中只发生了物理变化
【答案】A
【解析】A.高分子材料能以石油、煤等化石燃料为原料,将其转化成单体,单体再经过聚合反应生产,A
正确;
B.聚乙烯是乙烯的加聚产物,聚乙烯中不含碳碳双键,B错误;
C.高分子材料有三类结构:线型结构、支链型结构和网状结构,网状结构的高分子不是链状结构,C错
误;
D.橡胶硫化过程中通过—S—S—键等把线型结构连接为网状结构,是化学变化,D错误;
答案选A。
10.乙醇能发生如下反应:
①CHCHOH+3O――→2CO+3HO;
3 2 2 2 2
②2Cu+O=====2CuO,CHCHOH+CuO――→CHCHO+HO+Cu。
2 3 2 3 2
由以上反应不能得出的结论是( )
A.由反应①②可知,条件不同,乙醇与O 反应的产物不同
2
B.由反应②可知,Cu是乙醇氧化生成乙醛的催化剂
C.由反应①可知,乙醇燃烧时,碳碳键、碳氢键、氢氧键均断裂
D.由反应②可知,乙醇氧化为乙醛时,只断开氢氧键
【答案】D
【解析】由反应①可知,乙醇在氧气中燃烧生成CO 和HO,由反应②可知,乙醇与O 在铜作催化剂的条
2 2 2
件下生成CHCHO和HO,产物不同,故A正确;由反应②可知,Cu能参与反应,但反应前后质量和化
3 2
学性质不变,是催化剂,故B正确;由反应①可知,乙醇燃烧时,所有的化学键——碳碳键、碳氢键、氢
氧键均断裂,故C正确;由反应②可知,乙醇氧化为乙醛时,断开了氢氧键和一个碳氢键,故D错误。
11.下列有机化学反应方程式及反应类型均正确的是
选项 化学方程式 反应类型
5 / 16
学科网(北京)股份有限公司浓硫酸
A
CHCOOH+CH
CHOHΔ CHCOOC
H
酯化反应
3 3 2 3 2 5
B CH+Cl 光照CHCl+HCl 置换反应
4 2 3
C CH=CH +Cl→CHCHCl 加成反应
2 2 2 3 2
D CHCHOH+3O 点燃2CO+3H O 氧化反应
3 2 2 2 2
【答案】D
浓硫酸
【解析】A.酯化反应还生成水,反应为CHCOOH+CH CHOH
Δ CHCOOCH
CH+H O,A
3 3 2 3 2 3 2
项错误;
光照
B.CH+Cl CHCl+HCl为取代反应,生成物中无单质,不是置换反应,B项错误;
4 2 3
C.乙烯发生加成反应时双键C上均引入Cl原子,则加成反应为CH=CH +Cl→CHClCH Cl,C项错误;
2 2 2 2 2
点燃
D.乙醇燃烧化学方程式为:CHCHOH+3O 2CO+3H O,属于氧化反应,D项正确;
3 2 2 2 2
答案选D。
12.某有机物的结构简式为 ,下列关于该有机物的叙述错误的是
A.能与乙酸在一定条件下发生酯化反应
B.在一定条件下能发生还原反应、氧化反应
C.不能使溴的四氯化碳溶液褪色
D.含有两种官能团
【答案】C
【解析】A.该物质含有羟基,能和乙酸在一定条件下发生酯化反应,A正确;
B.该物质含有碳碳双键,能与氢气反应,可被还原;该物质含有羟基,能与氧气反应,可被氧化,B正
确;
C.该物质含有碳碳双键,能与溴发生加成反应,使之褪色,C错误;
D.该物质含有碳碳双键和羟基这两种官能团,D正确;
故选C。
CH CH 18OH
13.实验室用下图装置制取乙酸乙酯(使用的乙醇的结构简式为 3 2 ),下列有关说法正确的是
6 / 16
学科网(北京)股份有限公司CH CH 18OH CH COOH
A.在甲试管中加入药品的顺序:3mL 3 2 、2mL浓硫酸和2mL 3
B.乙试管中的饱和碳酸钠溶液可以换成氢氧化钠溶液
C.从乙试管中分离得到纯净干燥的乙酸乙酯的操作是:振荡、静置、分液
CH C18OOCH CH
D.生成的乙酸乙酯的结构简式为 3 2 3
【答案】A
【解析】A.加入药品的顺序:先加密度小的液体,再加密度大的液体,有利于混合和热量散失,A正确;
B.乙酸乙酯会与氢氧化钠溶液发生水解反应,B错误;
C.分液后得到的乙酸乙酯中还含有少量的水分,需要加入干燥剂,蒸馏,C错误;
CH CO18OCH CH
D.酯化反应断键的规律是“酸脱羟基醇脱氢”,所以生成的乙酸乙酯的结构简式为 3 2 3,
D错误;
故选A。
14.下列有关糖类的说法正确的是
A.糖类都符合通式C (H O)
n 2 m
B.符合通式C (H O) 的都是糖类
n 2 m
C.纤维素没有甜味,不属于糖类,糖类都有甜味
D.糖类是人类维持生命的六大类营养素之一
【答案】D
【解析】A.不符合C (H O) 这一通式的物质也可能属于糖类,如脱氧核糖C H O、鼠李糖C H O,A
n 2 m 5 10 4 6 12 5
错误;
B.糖类俗称碳水化合物,大都可用C (H O) 来表示,但符合这一通式的不一定都是糖,如乙酸
n 2 m
CHCOOH、甲酸甲酯HCOOCH [C (H O) ]等,B错误;
3 3 2 2 2
C.纤维素没有甜味,但属于糖类,糖不一定有甜味,如多糖:淀粉、纤维素,C错误;
D.人体的六大营养物质是:水、无机盐、蛋白质、油脂、糖类和维生素,糖类是人类维持生命的营养素
7 / 16
学科网(北京)股份有限公司之一,D正确;
答案选D。
15.中国酒文化源远流长,很多地方至今仍用传统工艺来制作米酒。家酿米酒的转化过程为( )
A.淀粉→蔗糖→葡萄糖→酒
B.淀粉→麦芽糖→葡萄糖→酒
C.淀粉→麦芽糖→果糖→酒
D.淀粉→蔗糖→果糖→酒
【答案】B
【解析】家酿米酒是以淀粉类物质为原料在酶的作用下逐步转化而成:淀粉――→麦芽糖――→葡萄
糖――→酒(乙醇)。
16.下列叙述中不正确的是
A.氨基酸分子中既含有羧基又含有氨基
B.向鸡蛋清溶液中加入饱和硫酸铵溶液,有固体析出
C.天然油脂的主要成分是高级脂肪酸甘油酯,没有恒定的熔沸点,属于高分子化合物
D.重金属盐能使蛋白质变性,但吞服钡餐(BaSO)不会引起中毒
4
【答案】C
【解析】A.氨基酸含有的官能团为氨基和羧基,则氨基酸分子中含有羧基和氨基,故A正确;
B.向鸡蛋清溶液中加入饱和硫酸铵溶液,蛋白质发生盐析,有固体析出,故B正确;
C.天然油脂为混合物,混合物没有固定的熔、沸点,油脂不属于高分子化合物,故C错误;
D.重金属盐能使蛋白质变性,钡餐的成分是硫酸钡,硫酸钡不溶于酸,无法生成钡离子,不会引起中毒,
故D正确;
故选:C。
二、非选择题(本题共5小题,共52分)
17.(10分)请解答下列与蛋白质有关的题目:
I.(1)从鸡蛋清溶液中提取蛋白质的方法是___________________________。
(2)鸡蛋腐烂时,常闻到有臭鸡蛋气味的气体,该气体中主要含有_______(填化学式),说明蛋白质中含有
_______(填元素名称)元素。
(3)误食重金属盐会中毒,这是因为___________________________。
(4)浓硝酸溅在皮肤上,使皮肤呈现_______色,这是由于浓硝酸和蛋白质发生了_______反应。
II.(1)下列物质对蛋白质的化学性质具有明显影响的是_______(填字母,下同)。
A.重晶石(BaSO) B.蓝矾 C.碘酒 D.高锰酸钾 E.酒精 F.生牛奶 G.熟鸡蛋
4
8 / 16
学科网(北京)股份有限公司(2)如果你发现有人误服重金属盐而出现了轻微中毒症状,需要你马上对病人进行抢救,你认为上述物质中
可以应用的是_______(写代号)。
(3)当你选择物质对病人进行抢救以后,下一步的打算或做法是_______。
A.建议病人快去医院继续治疗
B.将病人安置于通风处呼吸新鲜的空气
C.建议病人卧床休息
【答案】盐析 HS 硫 重金属盐使蛋白质发生变性 黄 颜色 B、C、D、E F
2
A
【解析】I(1)从鸡蛋清溶液中提取蛋白质可用盐析的方法,故答案为:盐析;
(3)具有臭鸡蛋气味的气体为HS,蛋白质中含有硫元素,故答案为:HS;硫;
2 2
(3)重金属盐会使蛋白质发生变性,使蛋白质失去生理活性,进而造成人体中毒,故答案为:重金属盐使蛋白
质发生变性;
(4)浓硝酸溅到皮肤上,使皮肤显黄色,发生了颜色反应,故答案为:颜色;
II(1)蓝矾、碘酒、高锰酸钾、酒精等物质都能使蛋白质变性,蛋白质的变性属于化学变化。重晶石的主要
成分是硫酸钡,它既不溶于水又不溶于酸,不能使蛋白质变性,对人体无毒,故答案为:B、C、D、E;
(2)生牛奶中含有较多的未变性的蛋白质,熟鸡蛋中蛋白质已经变性了,综上所述F符合题意,故选F;
(3)重金属盐中毒者服用生牛奶能降低重金属盐对人体的伤害,但这种作用是有限的,所以病人去医院做更
有效的治疗是最佳选择,故选A。
18.(10分)已知 可简写为 ,降冰片烯的分子结构可表示为:
(1)降冰片烯属于_______。
a.环烷烃 b.不饱和烃 c.烷烃 d.芳香烃
(2)降冰片烯的分子式为_______;分子中含有官能团_______(填名称)。
(3)降冰片烯不具有的性质_______。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温、常压下为气体
(4)降冰片烯的一氯代物有_______种,二氯代物有_______种。
【答案】b C H 碳碳双键 ad 4 14
7 10
【详解】(1)根据降冰片烯的键线式可知,分子中含碳碳双键和环,没有苯环,所以不属于环烷烃、烷烃和
芳香烃,属于不饱和烃,故选b;
(2)根据图示键线式可知,降冰片烯的不饱和度为3,含碳碳双键,其分子式为C H ,故答案为:C H ;
7 10 7 10
碳碳双键;
(3)降冰片烯分子中含碳碳双键和环,属于烃类,所以难溶于水,具有碳碳双键的化学性质,能发生氧化反
9 / 16
学科网(北京)股份有限公司应和加成反应,碳原子数大于4,常温下不是气体,所以ad错误,故答案为:ad;
(4)降冰片烯的分子结构为: ,根据分子结构的对称性 可知,分子中有4种不同环境
的氢原子,所以一氯代物有4种;二氯代物可以采用定一移一的方式分析如下:总共含4种H,在双键上
取代1个H后再取代1个H情况如图: ,二氯代物有6种;若取代1个H在1号碳上,则再取
代1个H的情况如图: ,剩余4个C上有H,所以有4种情况;如图 取代1号C
上H后有1种情况,在1、2号C上1种,共2种;同理,如图 取代1号C上H后有1种情况,
在1、2号C上1种,共2种;综上分析,总共6+4+2+2=14种,故答案为:4;14。
19.(10分)含有 结构的化合物与CH=CH 一样,可在一定条件下聚合成高分子化合物。
2 2
(1)广泛用作农用薄膜的聚氯乙烯塑料,是由CH=CHCl聚合成的,其化学方程式为______________。
2
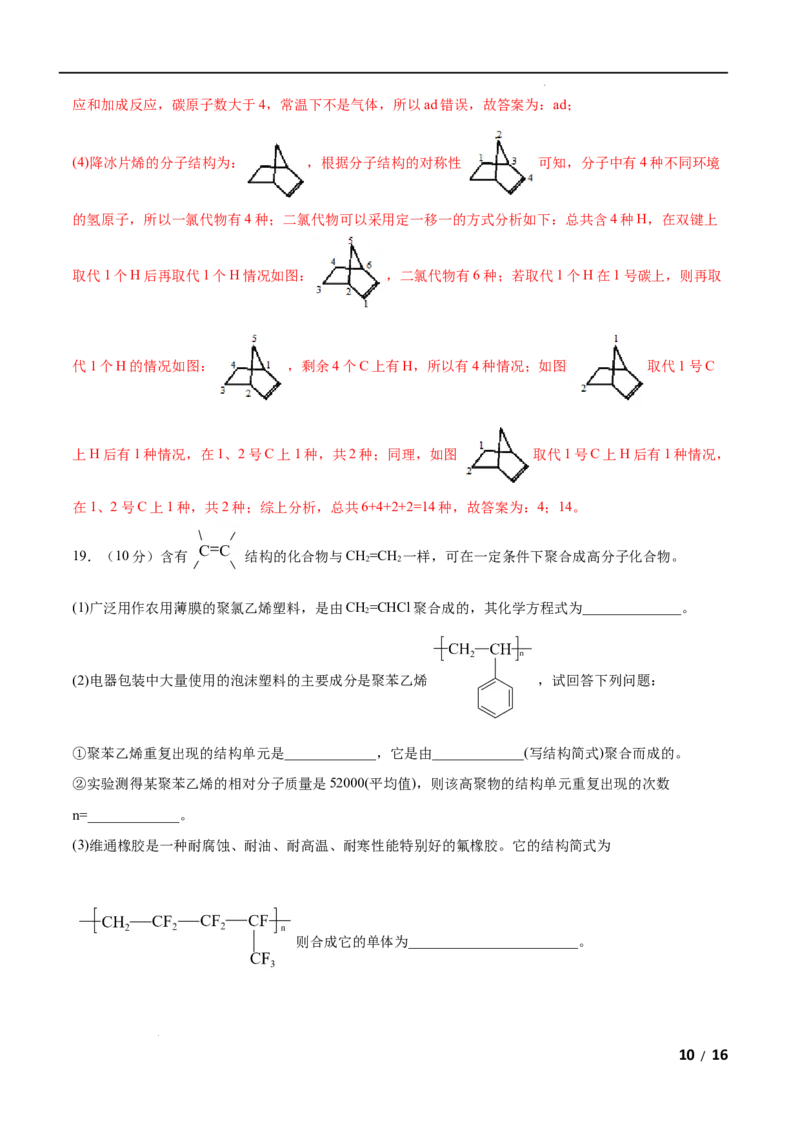
(2)电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯 ,试回答下列问题:
①聚苯乙烯重复出现的结构单元是_____________,它是由_____________(写结构简式)聚合而成的。
②实验测得某聚苯乙烯的相对分子质量是52000(平均值),则该高聚物的结构单元重复出现的次数
n=_____________。
(3)维通橡胶是一种耐腐蚀、耐油、耐高温、耐寒性能特别好的氟橡胶。它的结构简式为
则合成它的单体为________________________。
10 / 16
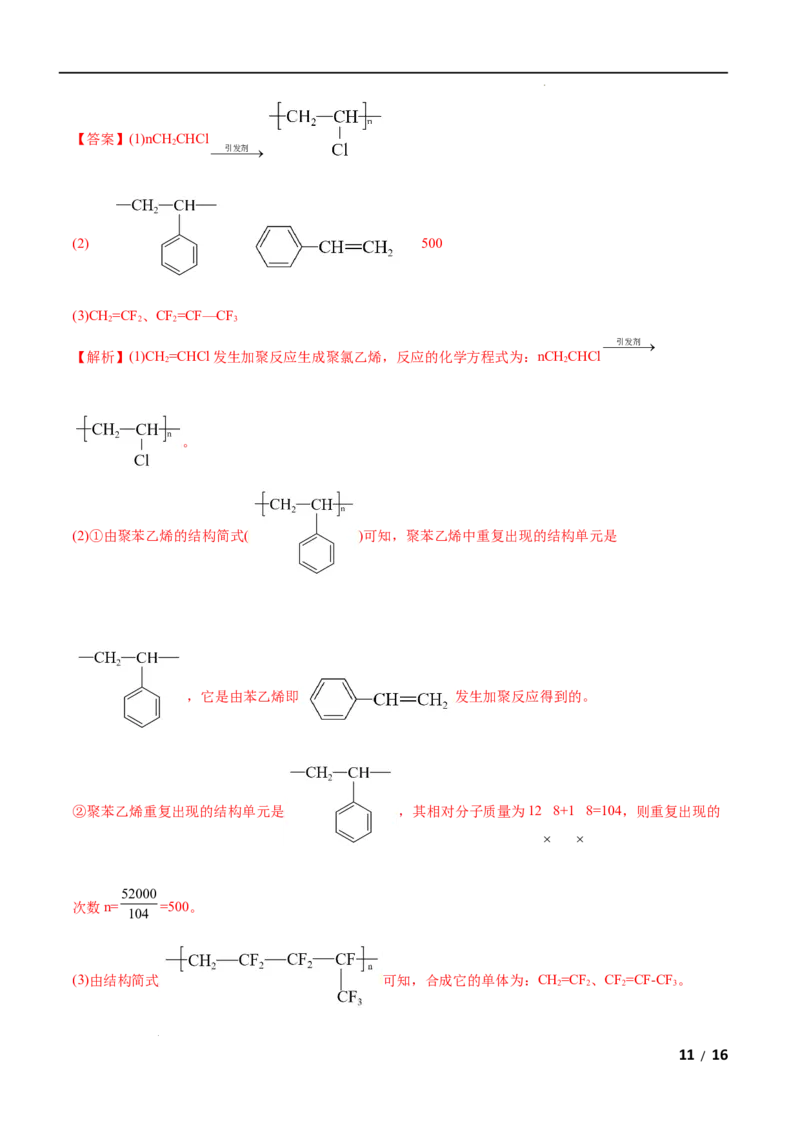
学科网(北京)股份有限公司【答案】(1)nCH CHCl
2
引发剂
(2) 500
(3)CH =CF 、CF=CF—CF
2 2 2 3
引发剂
【解析】(1)CH =CHCl发生加聚反应生成聚氯乙烯,反应的化学方程式为:nCHCHCl
2 2
。
(2)①由聚苯乙烯的结构简式( )可知,聚苯乙烯中重复出现的结构单元是
,它是由苯乙烯即 发生加聚反应得到的。
②聚苯乙烯重复出现的结构单元是 ,其相对分子质量为12 8+1 8=104,则重复出现的
52000
次数n= =500。
104
(3)由结构简式 可知,合成它的单体为:CH=CF 、CF=CF-CF 。
2 2 2 3
11 / 16
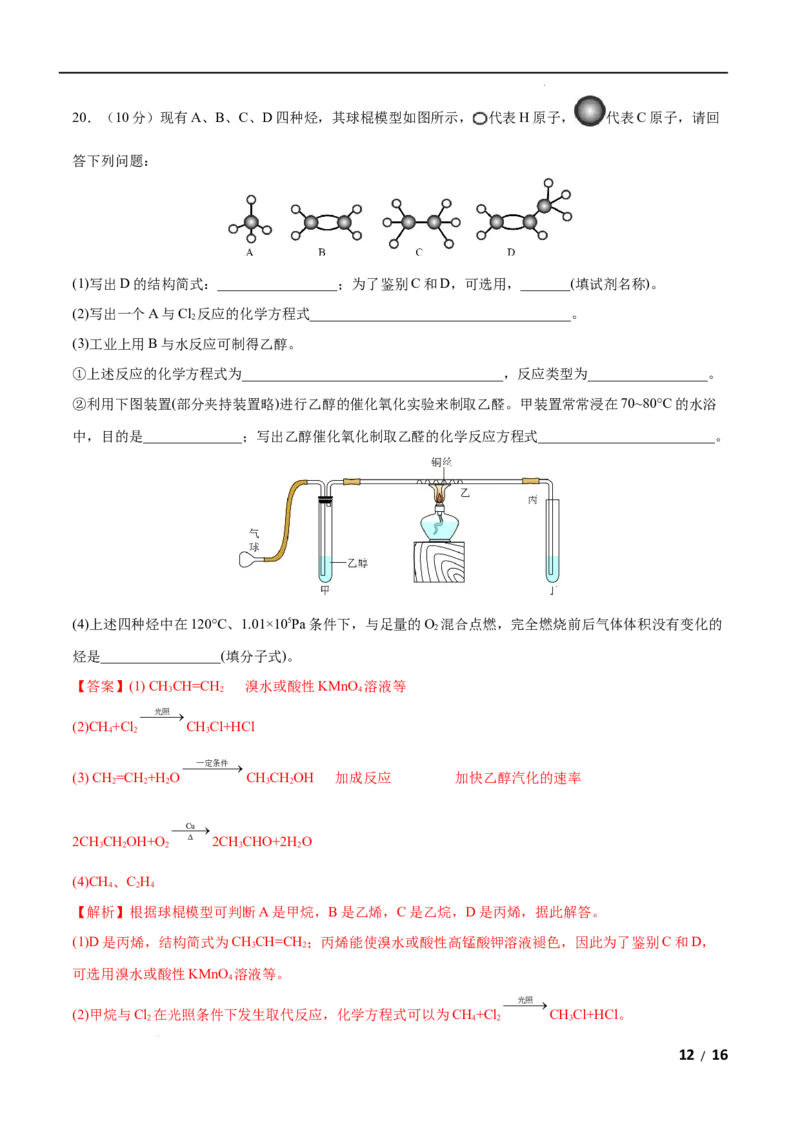
学科网(北京)股份有限公司20.(10分)现有A、B、C、D四种烃,其球棍模型如图所示, 代表H原子, 代表C原子,请回
答下列问题:
(1)写出D的结构简式:_________________;为了鉴别C和D,可选用,_______(填试剂名称)。
(2)写出一个A与Cl 反应的化学方程式_____________________________________。
2
(3)工业上用B与水反应可制得乙醇。
①上述反应的化学方程式为_____________________________________,反应类型为_________________。
②利用下图装置(部分夹持装置略)进行乙醇的催化氧化实验来制取乙醛。甲装置常常浸在70~80°C的水浴
中,目的是______________;写出乙醇催化氧化制取乙醛的化学反应方程式_________________________。
(4)上述四种烃中在120°C、1.01×105Pa条件下,与足量的O 混合点燃,完全燃烧前后气体体积没有变化的
2
烃是_________________(填分子式)。
【答案】(1) CH CH=CH 溴水或酸性KMnO 溶液等
3 2 4
光照
(2)CH +Cl CHCl+HCl
4 2 3
一定条件
(3) CH =CH +H O CHCHOH 加成反应 加快乙醇汽化的速率
2 2 2 3 2
Cu
2CHCHOH+O Δ 2CHCHO+2H O
3 2 2 3 2
(4)CH 、C H
4 2 4
【解析】根据球棍模型可判断A是甲烷,B是乙烯,C是乙烷,D是丙烯,据此解答。
(1)D是丙烯,结构简式为CHCH=CH;丙烯能使溴水或酸性高锰酸钾溶液褪色,因此为了鉴别C和D,
3 2
可选用溴水或酸性KMnO 溶液等。
4
光照
(2)甲烷与Cl 在光照条件下发生取代反应,化学方程式可以为CH+Cl CHCl+HCl。
2 4 2 3
12 / 16
学科网(北京)股份有限公司一定条件
(3)①乙烯和水反应生成乙醇,反应的化学方程式为CH=CH +H O CHCHOH,反应类型为加成
2 2 2 3 2
反应。②乙醇沸点低,易挥发,因此甲装置常常浸在70~80°C的水浴中,目的是加快乙醇汽化的速率;乙
Cu
醇催化氧化制取乙醛的化学反应方程式为2CHCHOH+O Δ 2CHCHO+2H O。
3 2 2 3 2
m m m m
(4)根据C H +(
n
)O →nCO+ HO(g)可知完全燃烧前后气体体积没有变化,说明1+
n
=n+ ,解
n m 4 2 2 2 2 4 2
得m=4,所以符合条件的是甲烷和乙烯,即CH、C H。
4 2 4
21.(11分)(1)下列试剂可用于鉴别乙烷和乙烯的是________________________(填字母)。
a.水 b.四氯化碳 c.酸性KMnO 溶液
4
(2)CH ===CH 、 、CHCHOH、CHCOOCH CH、
2 2 3 2 3 2 3
CHCOOH、葡萄糖,其中:
3
①能通过化学反应使溴水褪色的是_________________。
②能发生水解反应的是___________________。
③能与新制Cu(OH) 反应生成砖红色沉淀的是______________。
2
④能与NaCO 溶液反应有气体生成的是___________________。
2 3
(3)以淀粉为主要原料合成一种具有果香味的物质C的合成路线如图所示。
请回答下列问题:
a.A的结构简式为______________,B分子中的官能团名称为________。
b.上述①~⑤的反应中,属于取代反应的有________(填序号)。
c.写出下列转化的化学方程式:
反应①:_________________________;
反应⑤:_______________________;
(4)乙烯是石油化工的重要基础原料,工业上可由乙烯与水反应制乙醇,其化学方程式为
___________________;
乙烯还可通过加聚反应获得高分子材料聚乙烯,化学方程式为__________________________________。
13 / 16
学科网(北京)股份有限公司【答案】 (1)c
(2)①CH===CH ②CHCOOCH CH ③葡萄糖 ④CHCOOH
2 2 3 2 3 3
(3)a.CHCHO 羧基 b.①⑤
3
c.(C H O)+nHO――→nC H O
6 10 5 n 2 6 12 6
淀粉 葡萄糖
CHCOOH+C HOH CHCOOC H+HO
3 2 5 3 2 5 2
(4)CH ===CH +HO―――――→CHCHOH
2 2 2 3 2
【解析】(1)乙烯含有碳碳双键,可发生加成、氧化反应,可用酸性高锰酸钾溶液鉴别乙烷和乙烯,乙烯能
使酸性高锰酸钾溶液褪色,乙烷不能使酸性高锰酸钾溶液褪色,c正确。
(2)① CH===CH 含有碳碳双键,可以与溴发生加成反应而使溴水褪色;②酯类物质乙酸乙酯
2 2
(CHCOOCH CH)能够发生水解反应生成乙酸和乙醇;③葡萄糖含有醛基,能与新制Cu(OH) 在加热煮沸
3 2 3 2
条件下发生反应生成砖红色沉淀;④乙酸(CHCOOH)含有羧基,具有酸性,且酸性比碳酸强,能与
3
NaCO 溶液反应放出CO 气体。
2 3 2
(3)根据反应条件及转化关系可知A是CHCHO,B是CHCOOH,C是CHCOOCH CH。a.A是乙醛,结
3 3 3 2 3
构简式为CHCHO,B是CHCOOH,分子中官能团(—COOH)的名称为羧基。b.题图①~⑤的反应中,
3 3
①是淀粉的水解反应,属于取代反应,②是葡萄糖的发酵反应,③是乙醇的催化氧化反应,④是乙醛的催
化氧化反应,⑤是乙酸与乙醇的酯化反应,酯化反应属于取代反应,因此属于取代反应的有①⑤。c.反
应①是淀粉在稀硫酸催化作用下发生水解反应,反应的化学方程式为
(C H O)+nHO――→nC H O;
6 10 5 n 2 6 12 6
淀粉 葡萄糖
反应⑤是乙酸与乙醇在浓硫酸、加热条件下发生酯化反应,生成乙酸乙酯和水,反应的化学方程式为
CHCOOH+C HOH CHCOOC H+HO。
3 2 5 3 2 5 2
(4)乙烯是石油化工的重要基础原料,工业上可由乙烯与水通过加成反应制乙醇,该反应的化学方程式为
CH===CH +HO――――→CHCHOH;乙烯还可通过加聚反应获得高分子材料聚乙烯,反应的化学方
2 2 2 3 2
14 / 16
学科网(北京)股份有限公司程式为 。
15 / 16
学科网(北京)股份有限公司16 / 16
学科网(北京)股份有限公司