文档内容
第一章 物质及其变化 B 卷 能力提升—2022-2023 学年高一化学人教
版(2019)必修第一册单元达标测试卷
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1、《新修本草》是我国古代中药学著作之一,其中关于“青矾”的描述为“本来绿色,新出窟未
见风者,正如琉璃……烧之赤色……”。“青矾”的主要成分为 ,其不属于( )
A.碱
B.硫酸盐
C.化合物
D.亚铁盐
2、下列判断正确的是( )
A.由同种元素组成的物质一定是单质
B.两种元素只能组成一种化合物
C.一种元素在同一种化合物中可能显示不同的化合价
D.澄清透明的液体一定是溶液
3、铁是应用最广泛的金属,被誉为“金属之王”。已知:①
,② 。下
列有关说法正确的是( )
A. 溶液与Cu反应的离子方程式为
B.反应②中Cu元素化合价升高,发生还原反应
C.铁与稀硝酸反应中电子转移情况:
D.反应①中硝酸只起氧化剂的作用
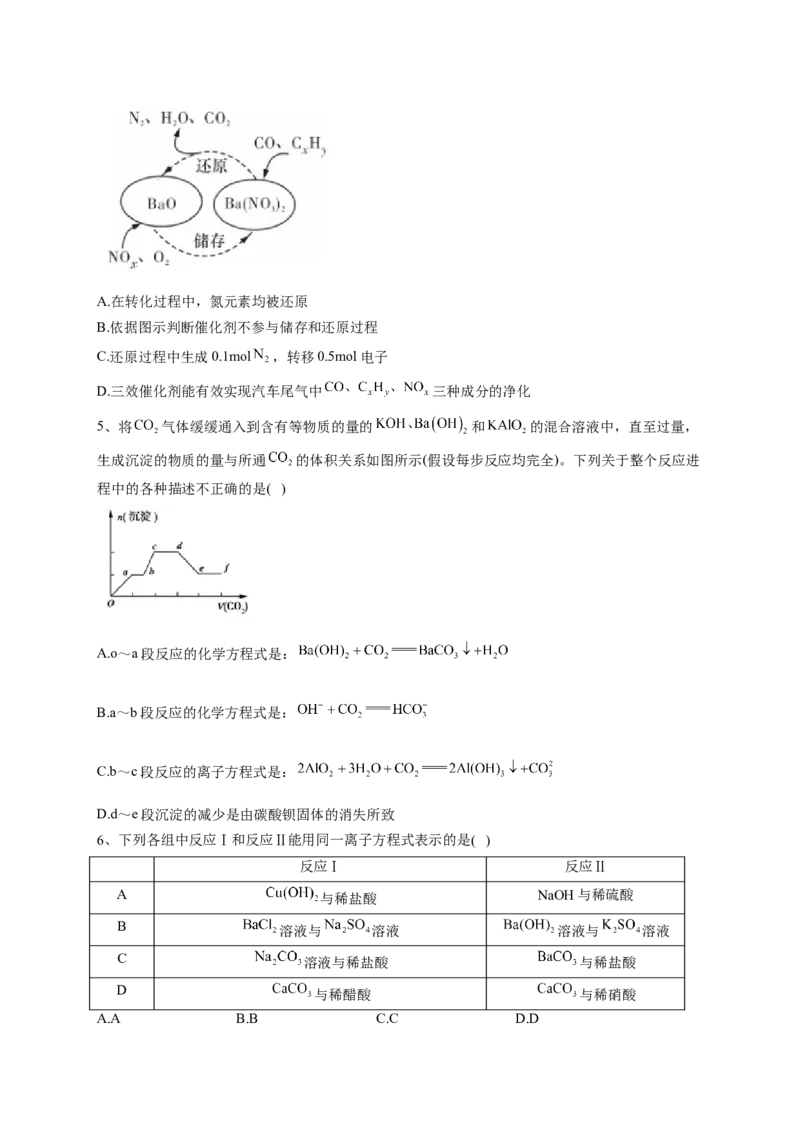
4、三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示。下列说法
正确的是( )A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1mol ,转移0.5mol电子
D.三效催化剂能有效实现汽车尾气中 三种成分的净化
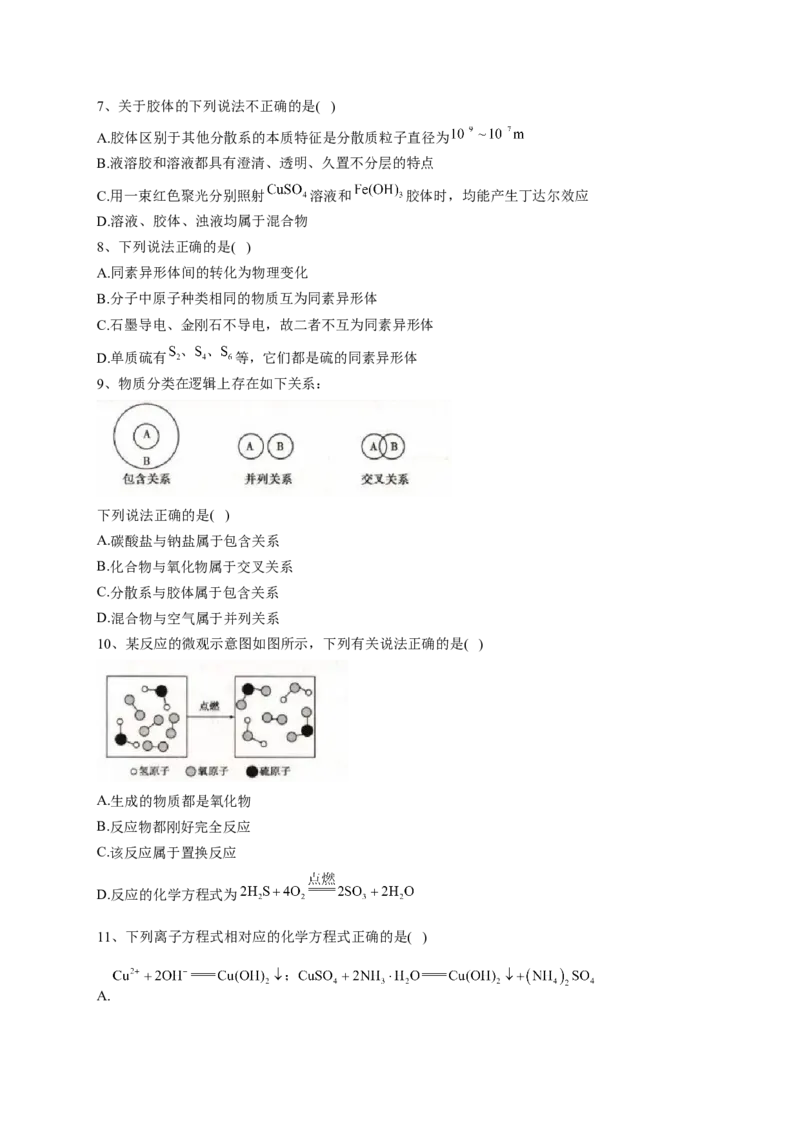
5、将 气体缓缓通入到含有等物质的量的 和 的混合溶液中,直至过量,
生成沉淀的物质的量与所通 的体积关系如图所示(假设每步反应均完全)。下列关于整个反应进
程中的各种描述不正确的是( )
A.o~a段反应的化学方程式是:
B.a~b段反应的化学方程式是:
C.b~c段反应的离子方程式是:
D.d~e段沉淀的减少是由碳酸钡固体的消失所致
6、下列各组中反应Ⅰ和反应Ⅱ能用同一离子方程式表示的是( )
反应Ⅰ 反应Ⅱ
A 与稀盐酸 NaOH与稀硫酸
B 溶液与 溶液 溶液与 溶液
C 溶液与稀盐酸 与稀盐酸
D 与稀醋酸 与稀硝酸
A.A B.B C.C D.D7、关于胶体的下列说法不正确的是( )
A.胶体区别于其他分散系的本质特征是分散质粒子直径为
B.液溶胶和溶液都具有澄清、透明、久置不分层的特点
C.用一束红色聚光分别照射 溶液和 胶体时,均能产生丁达尔效应
D.溶液、胶体、浊液均属于混合物
8、下列说法正确的是( )
A.同素异形体间的转化为物理变化
B.分子中原子种类相同的物质互为同素异形体
C.石墨导电、金刚石不导电,故二者不互为同素异形体
D.单质硫有 等,它们都是硫的同素异形体
9、物质分类在逻辑上存在如下关系:
下列说法正确的是( )
A.碳酸盐与钠盐属于包含关系
B.化合物与氧化物属于交叉关系
C.分散系与胶体属于包含关系
D.混合物与空气属于并列关系
10、某反应的微观示意图如图所示,下列有关说法正确的是( )
A.生成的物质都是氧化物
B.反应物都刚好完全反应
C.该反应属于置换反应
D.反应的化学方程式为
11、下列离子方程式相对应的化学方程式正确的是( )
A.B.
C. ;
D.
12、下列离子组在指定条件下的溶液中,一定能大量共存的是( )
A.含有大量 的溶液:
B.使石蕊变红色的溶液中:
C.加入 固体的溶液中:
D.无色澄清溶液中:
13、在强碱性条件下发生如下反应: (未配平),下列说法
错误的是( )
A. 是氧化产物
B. 的化学计量数之比是3:2
C.配平后X是“ ”
D.每生成1个 就会有3个电子发生转移
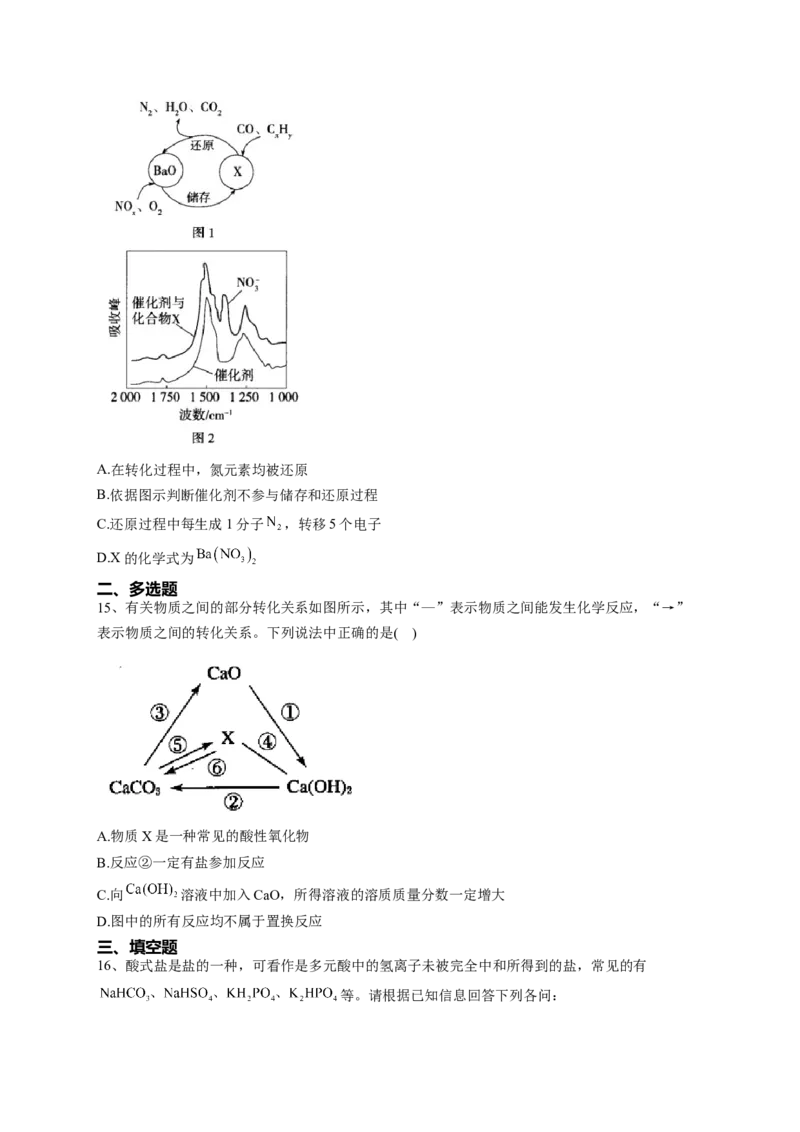
14、三效催化剂能有效实现汽车尾气中 三种成分的净化,其催化剂表面物质转化
的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。下列说法正确的是(
)A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中每生成1分子 ,转移5个电子
D.X的化学式为
二、多选题
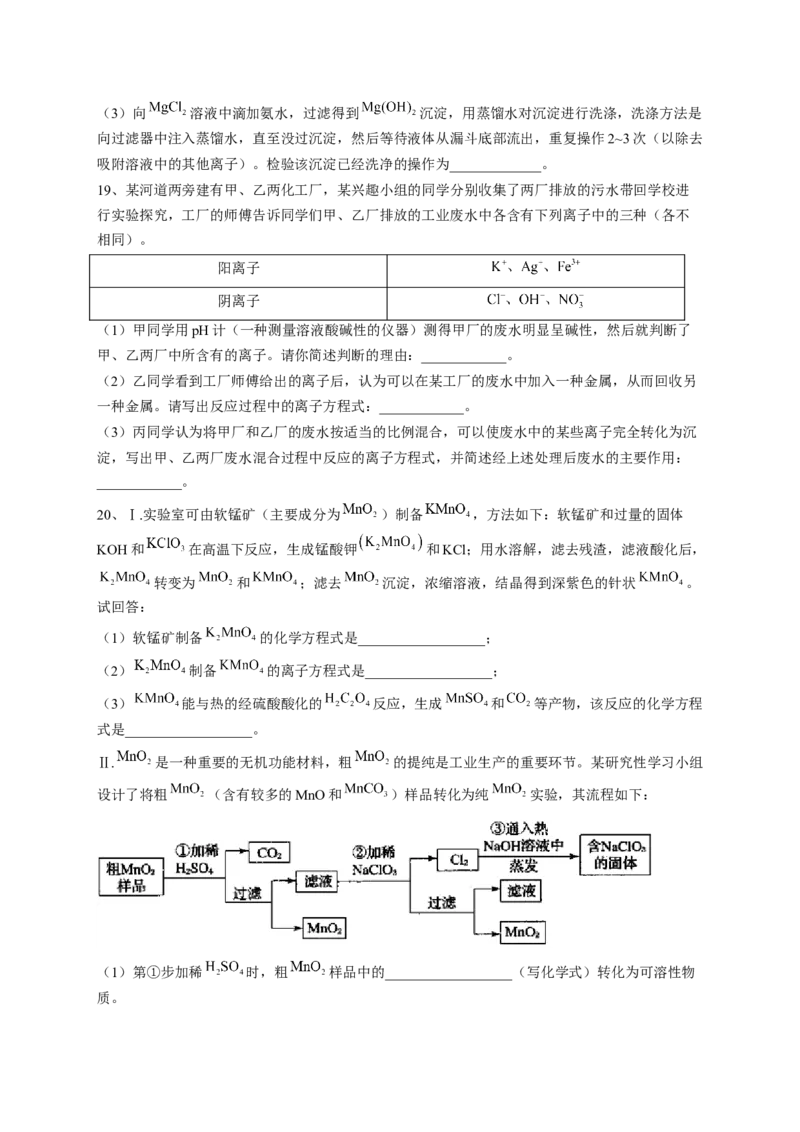
15、有关物质之间的部分转化关系如图所示,其中“—”表示物质之间能发生化学反应,“→”
表示物质之间的转化关系。下列说法中正确的是( )
A.物质X是一种常见的酸性氧化物
B.反应②一定有盐参加反应
C.向 溶液中加入CaO,所得溶液的溶质质量分数一定增大
D.图中的所有反应均不属于置换反应
三、填空题
16、酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有
等。请根据已知信息回答下列各问:Ⅰ.已知 (次磷酸) 与足量的NaOH反应只生成一种盐 , 水溶液中存在
分子。
(1) 属于____________酸; 为___________盐(填序号)
①一元酸,②二元酸,③三元酸,④强 酸,⑤弱 酸,⑥正盐,⑦酸式盐
(2)写出 溶液与足量NaOH溶液反应的离子方程式___________________________。
Ⅱ . 可用作清洁剂、防腐剂等。
(3)下列关于 的说法正确的是_______________。
A. 固体不能导电
B. 溶液的导电性一定强于 溶液
C. 属于电解质
D. 溶液显中性
(4) 溶液与N 溶液反应的离子方程式为_____________________________。
17、铜器久置于空气中会和空气中的水蒸气、 、 作用产生“绿锈”,“绿锈”俗称“铜
绿”[化学式为 ],“铜绿”能跟酸反应生成铜盐和 、 。某同学利用下述系
列反应实现了“铜→铜绿→……→铜”的转化:
(1)从三种不同分类标准回答,“铜绿”属于哪类物质:______。
(2)请写出“铜绿”与盐酸反应的化学方程式:____________。
(3)写出④、⑤的化学方程式:
④_________、⑤_____。
(4)上述转化过程中属于化合反应的是________,属于复分解反应的是________,属于分解反应的
是________。
(5)以Cu为原料,其他试剂自选,设计制备 的实验方案,并用流程图表示出来______。
18、(1)工业上常用氨气为原料制备硝酸,其中有一步非常重要的反应为:
,该反应的氧化剂为______________,还原剂为_____________。用
单线桥法表示该氧化还原反应电子转移的方向和数目。
(2)写出下列反应的离子方程式。
①铝片与硝酸汞溶液反应:_____________。
②向 溶液中滴加氨水 生成 沉淀:_____________。(3)向 溶液中滴加氨水,过滤得到 沉淀,用蒸馏水对沉淀进行洗涤,洗涤方法是
向过滤器中注入蒸馏水,直至没过沉淀,然后等待液体从漏斗底部流出,重复操作2~3次(以除去
吸附溶液中的其他离子)。检验该沉淀已经洗净的操作为_____________。
19、某河道两旁建有甲、乙两化工厂,某兴趣小组的同学分别收集了两厂排放的污水带回学校进
行实验探究,工厂的师傅告诉同学们甲、乙厂排放的工业废水中各含有下列离子中的三种(各不
相同)。
阳离子
阴离子
(1)甲同学用pH计(一种测量溶液酸碱性的仪器)测得甲厂的废水明显呈碱性,然后就判断了
甲、乙两厂中所含有的离子。请你简述判断的理由:____________。
(2)乙同学看到工厂师傅给出的离子后,认为可以在某工厂的废水中加入一种金属,从而回收另
一种金属。请写出反应过程中的离子方程式:____________。
(3)丙同学认为将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子完全转化为沉
淀,写出甲、乙两厂废水混合过程中反应的离子方程式,并简述经上述处理后废水的主要作用:
____________。
20、Ⅰ.实验室可由软锰矿(主要成分为 )制备 ,方法如下:软锰矿和过量的固体
KOH和 在高温下反应,生成锰酸钾 和KCl;用水溶解,滤去残渣,滤液酸化后,
转变为 和 ;滤去 沉淀,浓缩溶液,结晶得到深紫色的针状 。
试回答:
(1)软锰矿制备 的化学方程式是__________________;
(2) 制备 的离子方程式是__________________;
(3) 能与热的经硫酸酸化的 反应,生成 和 等产物,该反应的化学方程
式是__________________。
Ⅱ. 是一种重要的无机功能材料,粗 的提纯是工业生产的重要环节。某研究性学习小组
设计了将粗 (含有较多的MnO和 )样品转化为纯 实验,其流程如下:
(1)第①步加稀 时,粗 样品中的__________________(写化学式)转化为可溶性物
质。(2)完成第②步反应的离子方程式并配平: _______+ _______=
_______。(“1”也要填写在 内)参考答案
1、答案:A
解析:根据物质的交叉分类法可知, 属于亚铁盐、硫酸盐,也属于化合物,阴离子
并不是氢氧根离子,所以不属于碱,A项符合题意;故选A。
2、答案:C
解析:由同种元素组成的纯净物一定是单质,但由同种元素组成的物质有可能是混合物,如氧气
和臭氧的混合物;两种元素可以组成多种化合物,如H元素和O元素可以组成 和 ;一
种元素在同一种化合物中可能显示不同的价态,如硝酸铵中的氮元素;澄清透明的液体有可能是
纯净物,如水;故选C。
3、答案:C
解析:根据反应②可写出其离子方程式为 ,A项错误;反
应②中Cu元素化合价升高,发生氧化反应,B项错误;该反应中Fe元素由0价升高
至+3价,硝酸中N元素由+5价降低至+2价,反应中转移电子数为3,可用单线桥法表
示,C项正确;反应①中硝酸既是氧化剂,又起酸的作用,D项错误。
4、答案:D
解析:A.根据图示可知, 与BaO、 转化成 的过程中,N元素化合价升高被氧化,
故A错误;B.根据图示可知,BaO为催化剂, 与BaO、 转化成 时,BaO参与储
存N元素,故B错误;C.还原过程中生成0.1mol ,转移电子的物质的量为:
,故C错误;D.整个过程中,CO、 、 转化成 。
说明三效催化剂能有效实现汽车尾气中CO、 、 三种成分的净化,故D正确。故选:
D。
5、答案:B
解析: A.由上述分析可知, o-a段发生反应: ,故A正确;
B.由上述分析可知, a~ b段发生反应 ,故B错误;C.由上述分析
可知,b-c段反应的离子方程式是: , 故C正确;
D.d - e段发生反应 ,导致沉淀的减少,故D正确;故选:B。
6、答案:B解析:A项,离子方程式分别为 和 ;B项,离
子方程式均为 ,符合题意;C项,离子方程式分别为
和 ;D项,离子方程式分别为
和 。
7、答案:C
解析:胶体区别于其他分散系的本质是胶体分散质粒子直径为1~100nm,A正确;液溶胶属于介稳
体系,液溶胶与溶液都具有澄清、透明、久置不分层的特点,B正确; 溶液不具有丁达尔
效应,C错误;溶液、胶体、浊液都是一种(或多种)物质分散到另一种(或多种)物质中形成的
混合物,D正确。
8、答案:D
解析:由同种元素组成的不同单质互为同素异形体,比如 与 ,因此同素异形体之间的相互转
化是化学变化;分子中原子种类相同的物质如 与 ,均为化合物,不互为同素异形体;石
墨和金刚石互为同素异形体; 都是硫的单质,属于硫的同素异形体;故选D。
9、答案:C
解析:钠盐有的是碳酸盐,如碳酸钠,有的是硫酸盐,如硫酸钠,钠盐和碳酸盐不属于包含关系;
化合物包括氧化物,二者属于包含关系;分散系包括胶体,二者属于包含关系;混合物包括固体
混合物、气体混合物液体混合物等,混合物与空气属于包含关系;故选C。
10、答案:A
解析:根据题图可以看出,该反应的化学方程式为 ,生成的物质都是
氧化物,A项正确,D项错误;由题图可知, 过量,有剩余,B项错误;置换反应是一种单质
和一种化合物反应生成另一种单质和另一种化合物的反应,该反应不属于置换反应,C项错误;故
选A。
11、答案:C
解析:一水合氨是难电离的物质,应写成化学式,离子方程式为
,A错误; 与 反应的离子方程式为
,B错误; 只能拆成 和 ,故离子方程式为 ,C正确;氯化银不溶于水,金属铜不能与氯化银反应得到
金属银,D错误。
12、答案:B
解析:A项, 与 反应生成沉淀不能大量共存;B项,溶液呈酸性,
之间不发生任何反应,能大量共存;C项, 与水反应
生成NaOH, 与 反应生成沉淀不能大量共存;D项, 不能大量存在于无
色溶液中。
13、答案:B
解析:根据得失电子守恒和质量守恒可配平该反应:
,则 的化学计量数之比是2:3,B项
错误。
14、答案:D
解析:本题结合图示转化考查氧化还原反应知识的综合应用。解答关键是结合图示转化确定物质X
的化学式和分析反应中元素的化合价变化。分析图示转化:
结合图2可知X中含有 ,且BaO X BaO,故X中一定含 ,即X的化学式
为 。
储存时发生反应: ;
还原时发生反应: 。
由图示可知BaO为催化剂, 为中间产物,通过储存和还原过程能将汽车尾气成分净化,
最终得到 和 的混合物。
结合上述分析可知,在还原过程中,氮元素被还原,而储存过程中氧元素被还原,则氮元素被氧
化,A错误;结合图示储存和还原过程,可知催化剂BaO均参与化学反应,B错误;还原过程中
转化为 ,由化合价变化可知每生成1个 分子,将转移10个电子,C错误;结合上述分析可知X的化学式为 ,D正确。
15、答案:AD
解析:由于二氧化碳、碳酸钙之间能相互转化,二氧化碳能与氢氧化钙反应,X为二氧化碳,二氧
化碳属于酸性氧化物,A项正确;由于氢氧化钙能与二氧化碳反应生成碳酸钙,二氧化碳不属于盐,
B项错误;向 溶液中加入CaO,若是饱和溶液,溶液的质量分数不会增大,C项错误;由
题图中物质之间的反应可知,所有反应均不属于置换反应,D项正确。
16、答案:(1) ①⑤;⑥
(2)
(3)AC
(4)
解析:
17、答案:(1)盐、铜盐、碱式盐(或碳酸盐)
(2)
(3) ;
(4)① ;②③ ;④
(5)
解析:(1)铜绿的成分是 ,属于盐类,也属于碱式盐或碳酸盐等。
(2)铜绿不溶于水,若将铜绿转化成 ,必首先将铜绿转化成易溶于水的铜盐,而易溶的铜
盐与NaOH溶液反应生成 沉淀,故反应②的方程式为
(3) 不溶于水,受热能分解,故④的反应方程式为 ,反应⑤是
还原CuO,反应方程式为 。
(4)反应①是指Cu与 、 和 的化合生成碱式碳酸铜;反应②是铜绿与盐酸反应生成A(成分是 ),是复分解反应;反应③是A与NaOH反应生成 ,是复分解反应;反应④是
受热分解生成B(成分是CuO),是分解反应;反应⑤是B与 反应生成Cu,是置换反应。
(5)注意Cu与 (稀)不能直接反应。先将Cu转化为CuO,再用CuO与 反应制 。
18、答案:(1)
(2)①
②
(3)取最后一次洗涤液放入试管中,向该溶液中滴加 溶液,若无沉淀产生则证明沉淀已洗
净
解析: (1)反应中O素的化合价由氧气中的0价降至NO和 中的-2价,所以 为氧化剂;
反应中N元素的化合价由 中的-3价升至NO中的+2价, 为还原剂。1个 分子失去5
个电子,则该反应中转移电子数为20,用单线桥表示该反应电子转移的方向和数目为:
。
(2)①铝与硝酸汞溶液发生置换反应,反应的化学方程式为:
,离子方程式为: 。
② 溶液与氨水反应生成 沉淀的化学方程式为:
,离子方程式为:
。
(3)洗涤沉淀的目的是洗涤沉淀上吸附的可溶性杂质, 沉淀上吸附的可溶性杂质为
,检验沉淀是否洗净即检验洗涤液中是否含 。检验该沉淀已经洗净的操作为取最后
一次洗涤液放入试管中,向该溶液中滴加 溶液,若无沉淀产生则证明沉淀已洗净。
19、答案:(1) 只能和三种阴离子中的 共存,二者存在于同一个工厂的废水中,而
与 不能大量共存,所以 只能和 存在于同一个工厂的废水中。由于甲厂排放的废
水显碱性,所以甲厂废水中含有 ,而乙厂废水中含有(2)
(3)混合后生成沉淀的反应的离子方程式是 ,
反应后经过滤的废水主要含 ,可以用作化肥,用来浇灌农田,也可以提取 固体作为工
业原料
解析:
20、答案:Ⅰ.(1)
(2)
(3)
Ⅱ.(1)MnO、
(2)5 2 4 5 1 8
解析: