文档内容
第一章第二节离子反应小题训练--人教版(2019)必修第一
册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列各组离子在溶液中能大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
2.常温下,下列各组中的离子,能在溶液中大量共存的是
A. B.
C. D.
3.下列离子一定能大量存在于含 的酸性溶液中的是
A. B. C. D.
4.下列离子方程式书写正确的是
A.铁屑与盐酸的反应:
B. 与KI溶液混合:
C.氢氧化钡溶液与稀硫酸混合:
D.碳酸氢钠溶液和氢氧化钠溶液混合:
5.下列物质属于电解质的是
A.Al B. C.HCl D.
6.下列关于物质的分类组合正确的是
纯净
混合物 电解质 碱
物
A 生铁 碘伏 HSO 纯碱
2 4
B 液氯 碱石灰 HClO NaOH
4C 铝 冰水混合物 浓硫酸 Cu (OH) CO
2 2 3
D 青铜 云雾 稀盐酸 NH
3
A.A B.B C.C D.D
7.向一定量硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与
加入锌粉的质量关系如下图所示。下列说法正确的是
A.a点所得固体为银和铁
B.b点所得溶液中的溶质为硝酸银、硝酸亚铁和硝酸锌
C.c点所得溶液中的溶质为硝酸亚铁和硝酸锌
D.d点所得固体为银、铁和锌
8.下列表示对应化学反应的离子方程式正确的是
A.Cl 通入氢氧化钠溶液:Cl + 2OH- = Cl- + ClO- + H O
2 2 2
B.用FeCl 溶液腐蚀铜箔制造印刷电路板:3Cu + 2Fe3+= 3Cu2+ + 2Fe
3
C.NaO 与水反应: NaO + 2H O=2Na+ + 2OH-+ O ↑
2 2 2 2 2 2
D.向CaCl 溶液中通入CO:Ca2+ + H O + CO = CaCO + 2H+
2 2 2 2 3
9.常温下,下列各组离子在指定溶液中能大量共存的是
A.强酸性溶液中: 、 、
B.强碱性溶液中: 、 、
C.含有 的溶液中:OH-、 、
D.澄清透明的溶液中: 、Na+、 、
10.下列反应的离子方程式正确的是
A.Na与水反应:Na+HO=Na++OH-+H ↑
2 2
B.Al O 与NaOH溶液反应:Al O+2OH-= +H O
2 3 2 3 2
试卷第2页,共3页C.Ag CO 与稀硝酸反应:
2 3
D. 溶液与稀硫酸反应: ↓
11.下列叙述中,正确的是
A. 固体不导电,所以 不是电解质
B.石墨均能导电,所以它是电解质
C. 溶于水能导电,所以 是电解质
D.熔融的KCl能导电,所以KCl是电解质
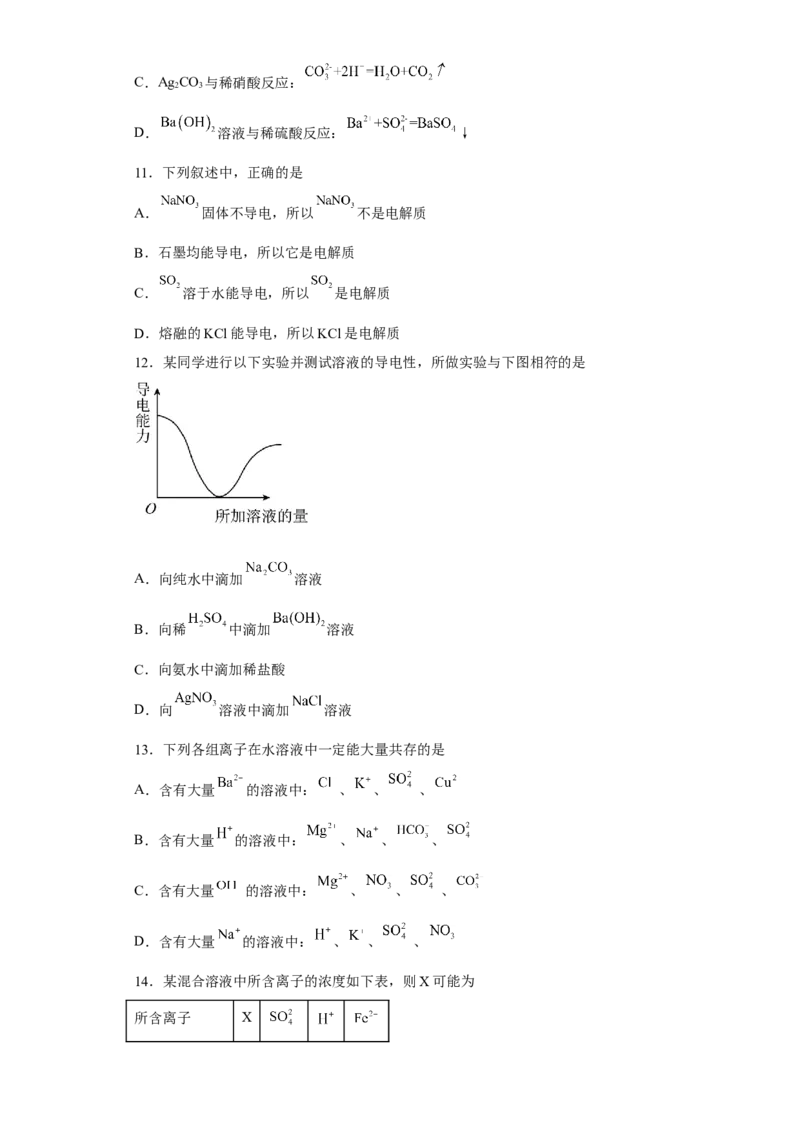
12.某同学进行以下实验并测试溶液的导电性,所做实验与下图相符的是
A.向纯水中滴加 溶液
B.向稀 中滴加 溶液
C.向氨水中滴加稀盐酸
D.向 溶液中滴加 溶液
13.下列各组离子在水溶液中一定能大量共存的是
A.含有大量 的溶液中: 、 、 、
B.含有大量 的溶液中: 、 、 、
C.含有大量 的溶液中: 、 、 、
D.含有大量 的溶液中: 、 、 、
14.某混合溶液中所含离子的浓度如下表,则X可能为
所含离子 X浓度/( ) 2 1 2 1
A. B. C. D.
15.分类是科学研究的重要方法,下列物质分类错误的是
A.化合物:干冰、冰水混合物、烧碱 B.电解质:熔融氯化钠、 、硫酸
C.碱:烧碱、纯碱、熟石灰 D.混合物:漂白粉、纯净矿泉水、盐酸
二、填空题
16.某实验小组用到了如下的化学物质:①用饱和 溶液制备好的胶体 ②食用白
酒 ③ ④ ⑤饱和 溶液 ⑥ ⑦液氯 ⑧烧碱溶液 ⑨
⑩ 溶液
(1)一小组成员将①②⑤⑧⑩归为一类,他的分类依据是__________。
A.都是混合物 B.都是溶液
(2)以上物质属于非电解质的有__________,能导电的有__________(填编号)。
(3)向⑤中加入足量铁粉后过滤,随即向所得的滤液中加入足量 溶液,观察到滤
液中先有白色絮状沉淀生成,然后迅速转变成灰绿色,一段时间后最终变为红褐色,
写出白色絮状沉淀变成红褐色的化学反应方程式__________。
(4)向①中逐滴加入⑩至过量,可以观察到的现象是__________,写出反应的离子方程
式__________。
(5)向③中加入少量的⑧,发生反应的离子方程式为__________。
(6)检验⑩中含有 的实验方法为__________。
(7)向⑩中滴加 溶液至不再产生沉淀,反应的离子方程式为__________。
17.现有下列几种物质:① 、② 、③ 、④ 、⑤ 、⑥
、⑦稀硫酸。回答下列问题:
(1)上述物质中属于碱性氧化物的是_________(填序号,下同),属于两性氧化物的是
_________,属于混合物的是_________。
试卷第4页,共3页(2)上述物质在水中能电离出三种离子的是_________(填序号);写出④的电离方程式:
__________________。
(3)写出①与⑦反应的离子方程式:___________________________________;加热条件
下,⑤在⑥的溶液中发生自身的氧化还原反应生成两种含氯元素的盐,其中一种是
,则另一种为_________(填化学式)。
18.从① ②HCl③Zn④ ⑤ 中选出合适的物质,按下列各题要求,
写出反应的离子方程式。
(1)实验室制取 的反应_______。
(2)盐与金属的置换反应_______。
(3)酸碱之间的中和反应_______。
(4)实验室制取 的反应_______。
19.阅读下列材料。
人类对墨水的使用有着悠久的历史。中国古代流传最多的是一种由①炭黑、松烟、胶
等制成的松烟墨。公元前5世纪至20世纪,欧洲主要使用的是铁胆墨水,其中一种配
方用到的原料有:鞣酸、②硫酸亚铁、③水等。为了防止生成的鞣酸亚铁与水反应产
生沉淀,还会加入④稀硫酸等物质。鞣酸早期通过发酵和水解产生,同时生成⑤葡萄
糖等物质。至今墨水仍被广泛使用。神舟十四号三名宇航员携带了红墨水返回地球,
一旦宇航员落入海域就可以染红海水,便于搜救人员发现。
回答下列问题:
(1)属于有机物的是_______(填标号,下同);属于电解质的是_______;属于单质的是
_______。
(2)能与碱溶液反应的是_______;可用于治疗缺铁性贫血症的是_______;可为人体提
供能量的是_______。
20.有下列物质:①胆矾②氨水③氯气④铜⑤氯化氢⑥蔗糖⑦液氨⑧ ⑨
⑩
(1)属于电解质的是_______(填序号,下同),
(2)能导电的是_______。参考答案:
1.C
【详解】A.酸性条件下 、 发生氧化还原反应而不能大量共存,A错误;
B. 、 反应不能大量共存,B错误;
C. 、 、 、 互不反应,可以大量共存,C正确;
D. 、 反应生成沉淀不能大量共存,D错误;
故选C。
2.D
【详解】A.H+与 反应生成二氧化碳和水,不能大量共存,A不符合题意;
B.Ca2+与 反应生成沉淀,不能大量共存,B不符合题意;
C.Mg2+与OH-反应生成沉淀,不能大量共存,C不符合题意;
D.各个离子间可以大量共存,D符合题意;
故答案为:D。
3.A
【详解】A. 在含 的酸性溶液中大量共存,故A符合题意;
B. 与酸性溶液中氢离子反应生成二氧化碳和水而不共存,故B不符合题意;
C. 与 反应生成硫酸钡沉淀而不共存,故C不符合题意;
D. 与酸性溶液中氢离子反应生成水而不共存,故D不符合题意。
综上所述,答案为A。
4.D
【详解】A.不符合客观事实,正确的为: ,故A错误;
B.不符合电荷守恒,正确的为: ,故B错误;
C.不符合化学式配比,正确的为: ,故C错误;
D.碳酸氢钠溶液和氢氧化钠溶液混合反应生成碳酸钠: ,故D
正确;
故选:D。
5.C
【详解】电解质的定义是在水溶液中或熔融状态下能够导电的化合物。
A.Al是单质,因此Al不是电解质,A项错误;
B. 自身不能电离出离子,在水溶液中之所以能导电是因为与水反应生成了新物质
, 能在水溶液中电离出离子导电,因此 不是电解质,B项错误;
C.HCl的水溶液能导电,HCl是电解质,C项正确;
D. 在水中或熔融状态下不能导电,CH 不是电解质,D项错误;
4
答案选C。
6.B
【详解】A.生铁属于合金,属于混合物,纯碱是碳酸钠,属于碱,故A错误;
B.液氯是液态的氯气,属于纯净物;碱石灰是氧化钙和氢氧化钠的混合物;高氯酸属于
酸,NaOH属于碱,故B正确;
C.冰水混合物是水的两种不同状态,属于纯净物,Cu (OH) CO 属于盐,故C错误;
2 2 3
D.稀盐酸是电解质溶液;NH 是碱性气体,不属于碱,故D错误。
3
综上所述,答案为B。
7.D
【分析】向一定量硝酸银和硝酸亚铁的混合溶液中加入锌粉,锌粉先与硝酸银反应,溶液
质量减少,a点是溶液中还有硝酸银,b点硝酸银反应完全,b点后开始与硝酸亚铁反应,c
点硝酸亚铁恰好反应完全,d点锌粉过量,沉淀的固体有银、铁和锌。
【详解】A.a点溶液中还有硝酸银,所得固体只有银,A错误;
B.b点溶液中硝酸银反应完全,溶液中不含有硝酸银,B错误;
C.c点溶液中硝酸银和硝酸亚铁都反应完全,溶液的溶质只有硝酸锌,C错误;
D.d点溶液中硝酸银和硝酸亚铁反应完全,固体有银和铁,d点锌粉过量,固体还有锌粉,
D正确;
答案第2页,共2页故答案为:D。
8.A
【详解】A.Cl 气通入氢氧化钠溶液生成氯化钠、次氯酸钠和水,其离子方程式为Cl +
2 2
2OH- = Cl- + ClO- + H O,故A正确;
2
B.FeCl 溶液腐蚀铜箔制造印刷电路板,Fe3+被还原成Fe2+,其正确的离子方程式为Cu +
3
2Fe3+= Cu2+ + 2 Fe2+,故B错误;
C.NaO + 2H O=2Na+ + 2OH-+ O ↑,此离子方程式质量不守恒,正确的是2NaO +
2 2 2 2 2 2
2HO=4Na+ + 4OH-+ O ↑,故C错误;
2 2
D.向CaCl 溶液中通入CO 不能生成碳酸钙和盐酸,因为酸和盐反应,不能用弱酸制强酸,
2 2
故D错误;
答案A。
9.D
【详解】A.强酸性溶液中 具有强氧化性能和 发生氧化还原反应,不能大量共存,
故A不选;
B.强碱性溶液中 会生成氢氧化铁沉淀,不能大量存在,故B不选;
C.含有 的溶液中,OH-会和 发生反应,不能大量共存,故C不选;
D.澄清透明的溶液中 、Na+、 、 之间不发生反应,可以大量共存,故D选;
故选D。
10.B
【详解】A.原离子方程式质量不守恒,故Na与水反应的离子方程式为:2Na+2HO=2Na+
2
+2OH-+H ↑,A错误;
2
B.Al O 与NaOH溶液反应方程式为:Al O+2NaOH=2NaAlO +H O,故其离子方程式为:
2 3 2 3 2 2
Al O+2OH-= +H O,B正确;
2 3 2
C.Ag2CO3是沉淀,故Ag CO 与稀硝酸反应的离子方程式为:
2 3
,C错误;D.原离子方程式漏写了生成HO的离子方程式,故 溶液与稀硫酸反应的离子方
2
程式为: ,D错误;
故答案为:B。
11.D
【详解】电解质是指溶于水或熔融状态下能导电的化合物,非电解质是指溶于水和熔融状
态下都不能导电的化合物;
A.NaNO 固体溶于水和熔融状态下均能导电,故 NaNO 属于电解质,电解质本身不能导
3 3
电,故A错误;
B.石墨能导电,但石墨属于单质,既不是电解质,也不是非电解质,故B错误;
C.SO 溶于水能导电是因为和水反应生成了亚硫酸, SO 属于非电解质,故C错误;
2 2
D.熔融的 KCl 能导电,且 KCl 属于化合物,故 KCl 属于电解质,故D正确;
故选 D。
12.B
【详解】A.向纯水中滴加 溶液,离子浓度逐渐增大所以导电性依次增强,A错误;
B.向稀 中滴加 溶液 ,离子浓度降低,导电
能力减小,当 过量时导电能力增强,B正确;
C.向氨水中滴加稀盐酸,两者反应生成盐导电性增强,C错误;
D.向 溶液中滴加 溶液, 会生成相同量的硝酸钠,导电性变化不大,D
错误;
故选B 。
13.D
【详解】A.含有大量 的溶液中 不能共存,A错误;
B.含有大量 的溶液中 不能共存,B错误;
答案第4页,共2页C.大量 、CO 与 不能共存,C错误;
D.含有大量 的溶液中 、 、 、 均可共存,D正确;
故选D。
14.A
【详解】A.假设溶液体积为1L, 所带负电荷的物质的量为2mol, 和 所带正
电荷总量为4mol,溶液呈电中性,可得需要加入阴离子。又X离子浓度为2mol/L,那么阴
离子需带一个单位负电荷,A正确;
B. 、 与 会发生氧化还原反应,不能共存,B正确;
C.由A可知溶液中需加入阴离子,C错误;
D. 、 与 会发生氧化还原反应,不能共存,D正确;
故选A。
15.C
【详解】A.干冰是二氧化碳固体是纯净的化合物,冰水混合物成分为水是纯净的化合物,
烧碱是氢氧化钠属于纯净的化合物,故 A不符合题意;
B.熔融氯化钠、 、硫酸在熔融或溶于水时可以导电,都属于电解质,故B不符合题
意;
C.纯碱属于盐,不属于碱,故C符合题意;
D.漂白粉、纯净矿泉水、盐酸都属于混合物,故D符合题意;
故选C。
16.(1)A
(2) ⑥ ①⑤⑧⑩
(3)4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
(4) 先生成红褐色沉淀,然后红褐色沉淀溶解 Fe(OH) +3H+=Fe3++3H O
3 2
(5) +2OH-=AlO +H O
2
(6)首先在试液中加入盐酸酸化,再加入BaCl 溶液,若有BaSO 白色沉淀产生,则证明有
2 4SO
(7)Ba2++H++OH-+SO ═BaSO ↓+H O
4 2
【详解】(1)①用饱和 溶液制备好的胶体、②食用白酒、⑤饱和 溶液、⑧烧
碱溶液、⑩ 溶液都是多种物质构成的,都属于混合物,故选A。
(2)在水溶液或熔融状态下都不能导电的化合物是非电解质,以上物质属于非电解质的有
⑥,能导电的有①⑤⑧⑩。
(3)Fe(OH) 白色絮状在空气中被氧气氧化为Fe(OH) 变成红褐色,该反应的化学方程式
2 3
为:4Fe(OH) +O +2H O=4Fe(OH) 。
2 2 2 3
(4)向Fe(OH) 胶体中逐滴加入 溶液至过量, 电离出的 SO
3
使 Fe(OH) 胶体发生聚沉,生成红褐色沉淀;氢氧化铁胶体聚沉后会产生 Fe(OH) 沉淀,
3 3
继续加入硫酸,会发生酸碱中和反应,红褐色沉淀溶解,生成 FeCl 和水,此反应的离子
3
方程式是
Fe(OH) +3H+=Fe3++3H O。
3 2
(5)向 中加入少量的NaOH溶液生成偏铝酸钠和水,离子方程式为 +2OH-
=AlO +H O。
2
(6)首先在试液中加入盐酸酸化,再加入BaCl 溶液,若有BaSO 白色沉淀产生,则证明
2 4
有SO 。
(7)向NaHSO 中滴加 溶液至不再产生沉淀,生成硫酸钡沉淀和水,离子方程式
4
为:Ba2++H++OH-+SO ═BaSO ↓+H O。
4 2
17.(1) ② ① ⑦
(2) ③
答案第6页,共2页(3)
【详解】(1) 属于碱性氧化物, 属于两性氧化物,溶液均是混合物。故答案为:
②;①;⑦;
(2) 在水中能电离出 、 、 三种离子; 的电离方程式为
。故答案为:③; ;
(3) 与稀硫酸反应生成 与水,离子方程式为 ;
由于 发生自身氧化还原反应时,氯的化合价一部分升高、一部分降低,故另一种产物
中氯的化合价低于0价,产物为 。故答案为: ; 。
18.(1)CaCO+2H+=Ca2++H O+CO↑
3 2 2
(2)Zn+Cu2+=Zn2++Cu
(3)OH-+H+=H O
2
(4)Zn+2H+=Zn2++H ↑
2
【详解】(1)验室利用⑤②制取二氧化碳,发生的离子反应为CaCO +2H+=Ca2+
3
+H O+CO↑。
2 2
(2)③⑤发生金属与盐溶液的置换反应,发生的离子反应为Zn+Cu2+=Zn2++Cu。
(3)①②发生酸碱中和反应,离子反应为OH-+H+=H O。
2
(4)实验室利用②③制取氢气,发生的离子反应为Zn+2H+=Zn2++H ↑。
2
19.(1) ⑤ ②③ ①
(2) ②④ ② ⑤
【分析】①炭黑是碳元素形成的单质;②硫酸亚铁是盐,属于电解质;③水是化合物,属
于电解质;④稀硫酸为混合物,不属于电解质;⑤葡萄糖是有机物,属于非电解质。
【详解】(1)有机物的是指含碳元素的一类化合物,以上物质中属于有机物的是葡萄糖,故填标号⑤;电解质是在水溶液中或熔融状态下能导电的化合物,常见的酸、碱、盐大多
是电解质,水也属于电解质,故填标号②③;单质是只由一种元素组成的纯净物,故填标
号①;
(2)盐和碱反应生成另一种盐和另一种碱,酸和碱反应生成盐和水,以上物质能与碱溶液
反应的是硫酸亚铁、稀硫酸,故填标号②④;人体缺铁,就会患缺铁性贫血,硫酸亚铁可
用于治疗缺铁性贫血,故填标号②;葡萄糖能提供人体所需的能量,故填标号⑤。
20.(1)①⑤⑨⑩
(2)②④
【详解】(1)在水溶液或熔融状态下能够导电的化合物是电解质,可知①胆矾、⑤氯化氢、
⑨NaHCO 、⑩ 为电解质。
3
(2)电解质的水溶液、熔融状态下的电解质和一些单质均能导电,故②氨水、④铜均能导
电。
答案第8页,共2页