文档内容
绝密★启用前
化学参考答案
7.【答案】A
【解析】医学上硫酸钡常用作“钡餐”,主要是因为其难溶于稀盐酸。
8.【答案】D
【解析】灼烧实验一般是在坩埚中进行,不需要石棉网(或陶土网)和铁架台,需要泥三角和三脚架等,A
项错误;Fe(OH) 胶体和FeCl 溶液的溶质都可以通过滤纸,不能用过滤方式分离,B项错误;生成的三溴苯酚
3 3
在苯中可溶,不能通过过滤的方法分离,C项错误;不要误以为生成的H 可能会跑到恒压漏斗中就不能测H
2 2
体积,根据反应前后气压相等原理,该装置可以测定生成H 的体积,D项正确。
2
9.【答案】D
【解析】根据结构可知:X、Y、Z、W分别为C、N、O、F。Y、Z、W的简单离子核外电子排布相同,半径
关系:Y>Z>W,A项正确;由于N原子的2p轨道半满结构,稳定性较强,其第一电离能比O大,但是比F
小,第一电离能的关系:Z(O)<Y(N)<W(F),B项正确;C原子杂化类型有sp2、sp3,C项正确;HF
的沸点高于CH,是因为HF分子之间可以形成氢键,使其沸点升高,但是HF分子之间形成的不是直线形氢键
4
(锯齿形),D项错误。
10.【答案】C
【解析】1mol该物质与NaOH溶液反应,最多消耗3molNaOH,A项错误;含3种含氧官能团:酯基、羟基和
醚键,B项错误;溴水褪色是C=C键发生加成反应,酸性KMnO 溶液褪色是与分子中的还原性基团发生氧化
4
反应,C项正确;该分子中C=C键两个C原子连接不同的原子或原子团,存在顺反异构体,D项错误。
11.【答案】C
【解析】碳棒b上发生氧化反应,碳棒b为原电池的负极,碳棒a为原电池的正极,在外电路,电子从负极移
动到正极,A项正确;碳棒b上(负极)S生成SO 2-的电极反应式:S-6e-+4H O=SO 2-+8H+,B项正确;负极
4 2 4
上每生成1molSO 2-,电路中转移7mol电子,理论上消耗39.2LO (标准状况下),C项错误;根据负极的电
4 2
极反应可以判断,工作一段时间后,生成了H SO ,酸性增强,氧硫化菌失去活性,电池效率降低,D项正确。
2 4
12.【答案】B
【解析】过程中只有极性键的断裂和形成,A项错误;中间体A的结构简式为 ,得一个质子变成B,则B
的结构为 ,B项正确;根据最终各产物的百分比可以判断,用C原子吸附在复合金属上的CO 的量为90%,
2
化学参考答案 第 1 页 (共 5 页)
{#{QQABRYQAogCAAIBAAQgCAQWCCEEQkAACCIoOBAAMIAAASRNABAA=}#}用O原子吸附在复合金属上的CO 的量为10%,C项错误;0.1molCO →0.1molHCOOH(转移0.2mol电子),
2 2
0.6molCO →0.6molCH OH(转移3.6mol电子),0.3molCO →0.3molCH (转移2.4mol电子),共转移6.2mol
2 3 2 4
电子,D项错误。
13.【答案】C
【解析】由-lgK 〔N(OH) 〕=-lgc(N2+)c2(OH-)=-lgc(N2+)-2lgc(OH-)=pN+2pR得关系式①pN=-2pR-lgK 〔N(OH)
sp 2 sp
〕;由-lgK (NCO )=-lgc(N2+)c(CO 2-)=-lgc(N2+)-lgc(CO 2-)=pN+pR,得关系式②pN=-pR-lgK (NCO )。从关系
2 sp 3 3 3 sp 3
式可知:①的斜率的绝对值大于②的,故曲线XY对应的物质是N(OH) ,曲线XZ对应的物质是NCO ,A项
2 3
错误。B项,X点时,pR=5.7,pN=0,由关系式①pN=-2pR-lgK 〔N(OH) 〕得lgK 〔N(OH) 〕=-2pR-pN=-2
sp 2 sp 2
×5.7=-11.4,则K〔N(OH) 〕=10-11.4,其数量级为10-12,B项错误。曲线XY中X点表示饱和N(OH) 溶液,
s 2 2
向其中通入HCl后,c(OH-)减小(即pR增大),c(N2+)增大(即pN减小),所以能使溶液从X点变成Y点,
C项正确。向N(OH) 饱和溶液中加入一定量NaOH,会产生沉淀N(OH) ,但是c(OH-)变大,D项错误。
2 2
27.(14分)
(1)FeS (2分) 不同(2分)
2
(2)FeS +2Fe3+=3Fe2++2S(2分)
2
(3)1∶1(2分)
5cV
(4)酚酞(2分,甲基橙也给分) (2分) 硫酸溶液中含有盐酸(2分)
V
0
【解析】
(1)硫铁矿的主要成分为二硫化亚铁(FeS );“操作1”包含萃取和分液,“操作2”为分液操作。
2
(2)“浸取”过程中,饱和的FeCl 溶液和硫铁矿粉发生的主要反应的离子方程式为FeS +2Fe3+=3Fe2++2S。
3 2
(3)NaClO+2HCl=Cl ↑+H O+NaCl,参加反应的HCl只有一半做还原剂。
2 2
(4)用氢氧化钠标准溶液滴定强酸溶液,指示剂可选用酚酞或甲基橙;量取的25mL配制的硫酸溶液,其溶质
的物质的量为5cV×10-4mol,250mL配制的硫酸溶液中溶质的物质的量为5cV×10-3mol,则该硫酸溶液的浓度为
5cV 103mol 5cV
= mol/L。经过3次平行实验,发现测得的结果高于实际浓度,其原因可能是硫酸溶液中含
V 103L V
0 0
有未除净的盐酸。
化学参考答案 第 2 页 (共 5 页)
{#{QQABRYQAogCAAIBAAQgCAQWCCEEQkAACCIoOBAAMIAAASRNABAA=}#}28.(15分)
(1)+6(1分)
(2)过滤(2分) 玻璃棒 漏斗(2分,每个1分,顺序可换)
(3)20(1分) 170(1分)
(4)NiMoO +2Na CO +H O Na MoO +2NaHCO +NiO(2分)
4 2 3 2 2 4 3
(5)(R N) MoO +2HCO -=2R NHCO +MoO 2-(2分)
4 2 4 3 4 3 4
(6)C(2分)
(7)(R N) CO Na CO (2分,每个1分,顺序可换)
4 2 3 2 3
【解析】
(1)Ni为+2价,O为-2价,则Mo为+6价。
(1)“操作1”后有“浸出渣”和“浸出液”,则“操作1”是过滤。过滤实验用到的玻璃仪器有烧杯、玻璃棒
和漏斗。
(3)图1,Na CO 最佳添加量为20wt%-60wt%时,Mo和Al浸出率变化量很小,则Na CO 最佳添加量为20wt%;
2 3 2 3
图2,当浸出温度≥170℃时,Mo和Al浸出率较高,且再继续升温后,Mo和Al浸出率变化不大,则最佳浸出温
度为170℃。
(4)NiMoO 在碱浸时有Na MoO 和NaHCO 生成,根据已知②判断生成物还有NiO;则NiMoO 在碱浸时的化
4 2 4 3 4
学方程式为NiMoO +2Na CO +H O Na MoO +2NaHCO +NiO。
4 2 3 2 2 4 3
(5)由一些离子被R N+萃取的先后顺序可知,加入NH HCO 反萃取发生反应为(R N) MoO +2NH HCO =
4 4 3 4 2 4 4 3
2R NHCO +(NH ) MoO ,其离子方程式为(R N) MoO +2HCO -=2R NHCO +MoO 2-。
4 3 4 2 4 4 2 4 3 4 3 4
(6)下口倾斜向上,旋转下口的活塞放气。
(7)根据(5)中信息可知,采用碳酸根类型的N263萃取钼的反应产物有Na CO ;萃取后有机相为HCO -型(如
2 3 3
R NHCO ),加入NaOH处理后可实现萃取剂(R N) CO 再生。流程中可以循环利用的物质有Na CO 和(R N) CO 。
4 3 4 2 3 2 3 4 2 3
29.(14分)
(1)2CO (g)+6H (g) CH CH OH(g)+3H O(g) ΔH=-173.4kJ/mol(2分)
2 2 3 2 2
5
①A(2分) ②0.4(2分) (2分)
96
(2)300℃之前,反应未达到平衡,随温度升高,反应速率加快,CH CH OH选择性增大;300℃之后,生成C
3 2
H CH OH反应的催化活性降低,反应速率减慢,CH CH OH选择性减小(或其他合理答案)(2分)
3 2 3 2
化学参考答案 第 3 页 (共 5 页)
{#{QQABRYQAogCAAIBAAQgCAQWCCEEQkAACCIoOBAAMIAAASRNABAA=}#}486
(3)12(2分) (2分,其他合理形式也可给分)
N (a107)3
A
【解析】
(1)Ⅰ×2+Ⅱ即为所求的热化学方程式2CO (g)+6H (g) CH CH OH(g)+3H O(g) ΔH=-173.4kJ/mol。
2 2 3 2 2
①A.容器内压强不变,说明容器内所有气体的物质的量都不再变化,则反应Ⅰ和Ⅱ都达到化学平衡状态,A项正
确;B.容积固定,平衡时向容器中充入稀有气体,各气体分压不变,平衡不移动,B项错误;C.平衡时向容器
中充入一定量H ,反应Ⅰ和Ⅱ均正向移动,但是H 的转化率降低,C项错误。
2 2
②根据原子守恒来解此题,只考虑起始和平衡时各组分的物质的量,忽略反应过程,分析如下:
起始 转化 平衡 备注
1molCO (1-0.1-2x)molCO 根据C原子守恒写CO 的物质的量
2 2 2
1molH 转化率40% 0.6molH 根据转化率可求
2 2
0.1molCO 已知
(0.4-3x)molH O 根据H原子守恒写H O的物质的量
2 2
xmolCH CH OH 设的未知数
3 2
根据O原子守恒列式为2(1-0.1-2x)+0.1+(0.4-3x)+x=2,解方程得x=0.05。平衡时,体系中各气态物质的
物质的量分别为:0.8molCO ,0.6molH ,0.1molCO,0.25molH O,0.05molCH CH OH,故总的气体的物质的
2 2 2 3 2
p(CO) p(H O)
量为 1.8mol,平衡时容器内混合气体的压强为 0.9pMPa。反应Ⅰ的分压平衡常数 K = 2 =
P
p(CO ) p(H )
2 2
0.1 0.25
0.9pMPa 0.9pMPa
1.8 1.8 5 0.8mol
= 。平衡时,CO (g)的物质的量浓度为= =0.4mol/L。
2
0.8 0.6 96 2L
0.9pMPa 0.9pMPa
1.8 1.8
(2)300℃之前,反应未达到平衡,随温度升高,反应速率加快,CH CH OH选择性增大;300℃之后,生成
3 2
CH CH OH反应的催化活性降低,反应速率减慢,CH CH OH选择性减小。300℃之后,还是速率因素,不是平
3 2 3 2
衡原因。因为总反应是放热反应,且CO 的转化率是增大的,如果是平衡原因,则二者矛盾。
2
1 1
(3)1个砷化硼的晶胞结构中,顶点:8 1,面心:6 3,故含有4个B原子,离硼原子最近的硼原
8 2
2 486
子有12个,且最近距离为 anm,该晶胞中有4个BAs,晶体密度可表示为 g/cm3。
2 N (a107)3
A
30.(15分)
(1)对氨基苯酚或4-氨基苯酚(2分) 酯基、羧基(2分,每个1分)
化学参考答案 第 4 页 (共 5 页)
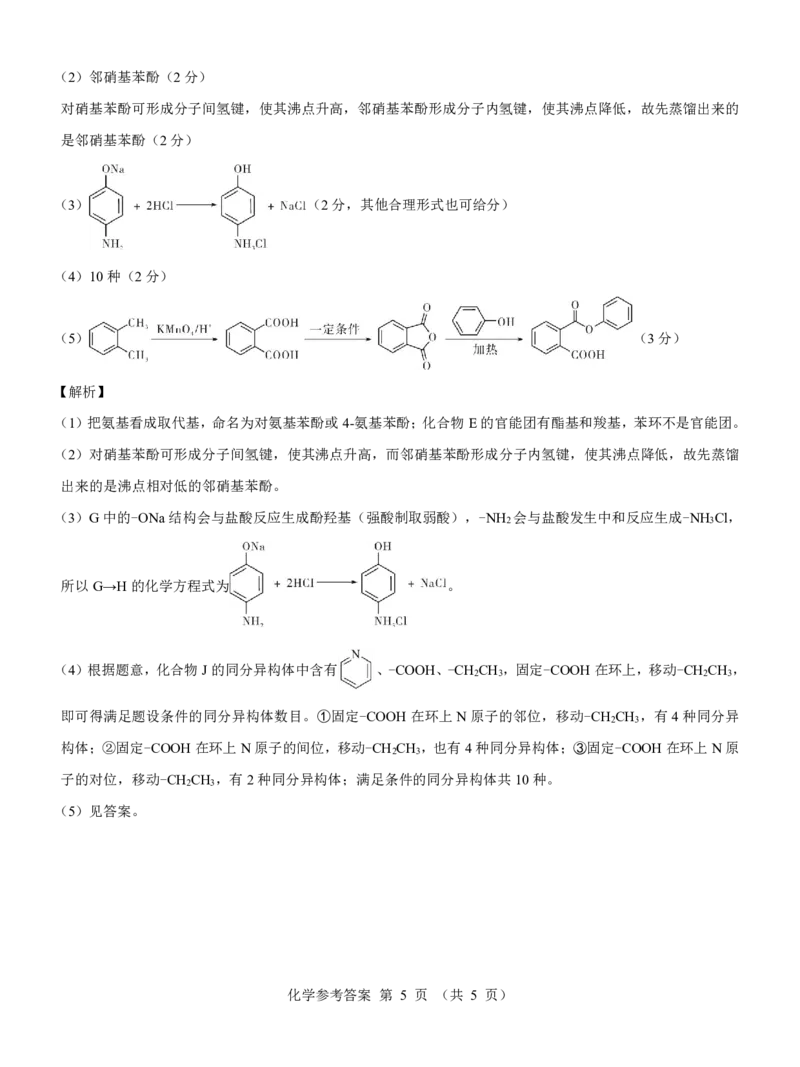
{#{QQABRYQAogCAAIBAAQgCAQWCCEEQkAACCIoOBAAMIAAASRNABAA=}#}(2)邻硝基苯酚(2分)
对硝基苯酚可形成分子间氢键,使其沸点升高,邻硝基苯酚形成分子内氢键,使其沸点降低,故先蒸馏出来的
是邻硝基苯酚(2分)
(3) (2分,其他合理形式也可给分)
(4)10种(2分)
(5) (3分)
【解析】
(1)把氨基看成取代基,命名为对氨基苯酚或4-氨基苯酚;化合物E的官能团有酯基和羧基,苯环不是官能团。
(2)对硝基苯酚可形成分子间氢键,使其沸点升高,而邻硝基苯酚形成分子内氢键,使其沸点降低,故先蒸馏
出来的是沸点相对低的邻硝基苯酚。
(3)G中的-ONa结构会与盐酸反应生成酚羟基(强酸制取弱酸),-NH 会与盐酸发生中和反应生成-NH Cl,
2 3
所以G→H的化学方程式为 。
(4)根据题意,化合物J的同分异构体中含有 、-COOH、-CH CH ,固定-COOH在环上,移动-CH CH ,
2 3 2 3
即可得满足题设条件的同分异构体数目。①固定-COOH在环上N原子的邻位,移动-CH CH ,有4种同分异
2 3
构体;②固定-COOH在环上N原子的间位,移动-CH CH ,也有4种同分异构体;③固定-COOH在环上N原
2 3
子的对位,移动-CH CH ,有2种同分异构体;满足条件的同分异构体共10种。
2 3
(5)见答案。
化学参考答案 第 5 页 (共 5 页)
{#{QQABRYQAogCAAIBAAQgCAQWCCEEQkAACCIoOBAAMIAAASRNABAA=}#}