文档内容
宜春一中 2024-2025 学年第二学期高二年级期中考试 5.下列仪器是实验室常见仪器,对相关实验中使用到的部分仪器选择合理的是( )
A.中和热的测定:③⑤
化学试卷
B.用标准盐酸测定NaOH溶液的浓度:③⑥
C.蒸馏法分离CHCl 和CCl :②③④
注意事项: 2 2 4
1. 考查范围:选择性必修3第一章至第三章第四节。 D.重结晶法纯化苯甲酸(含少量泥沙、NaCl):①⑦
2. 答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
3. 回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目上的答案标号涂黑。回
答非选择题时,将答案写在答题卡上,写在本试卷上无效。 6. 一种抗血小板聚集药物X的结构如下图所示。下列说法正确的是( )
4. 考试结束后,请将答题卡交回。 A.X的分子式为C H O
19 20 6
可能用到的相对原子质量:H 1 C 12 O 16 B.X中存在4种含氧官能团
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一项是符合题目要求的。 C.X遇FeCl 溶液显紫色
3
1.生活处处有化学,下列说法错误的是( ) D.1mol X最多能与2mol NaOH发生反应
A.浸有酸性高锰酸钾溶液的硅藻土可用于鲜花保鲜
B.电阻率低、热导率高的石墨烯可用于制作超级导电材料
7.N 代表阿伏加德罗常数的值,下列说法中正确的是( )
C.天然气、液化石油气、汽油、柴油、凡士林、甘油和石蜡的主要成分都是烷烃 A
A.B NH (无机苯)的结构与苯相似,1mol无机苯中π键数目为3N
D.氯乙烷可与其他药物制成气雾剂,用于运动中的急性损伤,其在汽化时有冷冻麻醉作用 3 3 6 A
B.1mol CaC 含有阴离子的数目为2N
2.下列有关有机化合物的化学用语表述正确的是( ) 2 A
C.48g正丁烷和10g异丁烷的混合物中共价键数目为13N
A
A.2-丁烯的键线式: B.丙炔的球棍模型:
D.1mol环戊二烯( )分子中含有的σ键数目为5N
A
C.异丁酸正丁酯的结构简式:(CH)CHCOO(CH )CH D.乙醇钠的电子式:
3 2 2 3 3 8.由1-氯环己烷( )制备1,2-环己二醇( )时,需要经过下列哪几步反应( )
A.加成→消去→取代 B.消去→加成→取代
3.乙醇和二甲醚属于同分异构体,其结构简式分别为: ,在下列哪种检
C.取代→消去→加成 D.取代→加成→消去
测仪上显示出的信号是完全相同的( ) 9.对下列事实的描述,所给化学方程式或离子方程式正确的是( )
A.质谱仪 B.李比希元素分析仪 C.红外光谱仪 D. 核磁共振仪
A.制备乙二酸乙二酯:
4.下列有机化合物的命名正确的是( )
B.乙醇与酸性 溶液反应:
A. :2,2-二甲基-2-丙醛 B. :2-乙基-3-戊醇
C.溴乙烷与氢氧化钠水溶液共热:C HBr + OH- CH=CH ↑ +Br-+H O
2 5 2 2 2
C. :2-乙基-1,3-丁二烯 D.
D.用小苏打溶解水杨酸: +2 → +2CO +2H O
2 2
:间-苯二甲酸
10. 利用下列装置(夹持装置略)或操作进行实验,能达到实验目的的是( )A.操作I为萃取、分液,萃取剂为苯
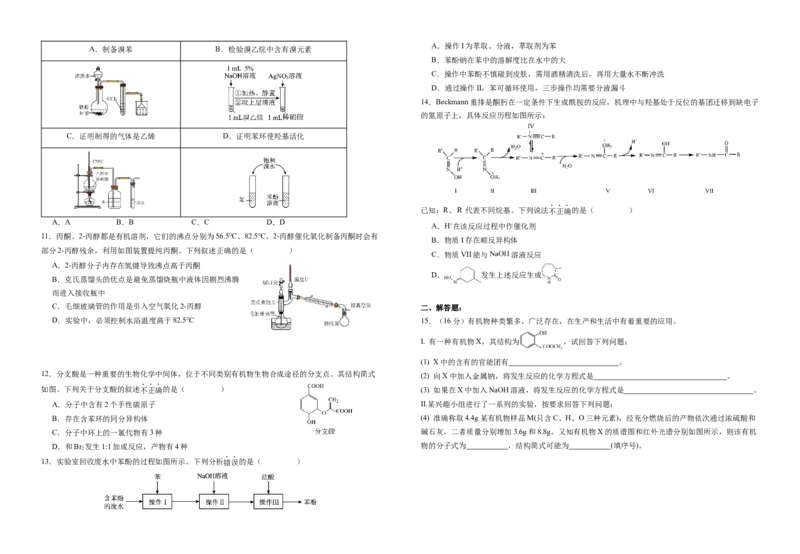
A.制备溴苯 B.检验溴乙烷中含有溴元素
B.苯酚钠在苯中的溶解度比在水中的大
C.操作中苯酚不慎碰到皮肤,需用酒精清洗后,再用大量水不断冲洗
D.通过操作II,苯可循环使用,三步操作均需要分液漏斗
14.Beckmann重排是酮肟在一定条件下生成酰胺的反应,机理中与羟基处于反位的基团迁移到缺电子
的氮原子上,具体反应历程如图所示:
C.证明制得的气体是乙烯 D.证明苯环使羟基活化
已知:R、 代表不同烷基。下列说法不正确的是( )
A.A B.B C.C D.D
A.H+在该反应过程中作催化剂
11.丙酮、2-丙醇都是有机溶剂,它们的沸点分别为56.5℃、82.5℃。2-丙醇催化氧化制备丙酮时会有
B.物质I存在顺反异构体
部分2-丙醇残余,利用如图装置提纯丙酮。下列叙述正确的是( )
C.物质VII能与 溶液反应
A.2-丙醇分子内存在氢键导致沸点高于丙酮
D. 发生上述反应生成
B.克氏蒸馏头的优点是避免蒸馏烧瓶中液体因剧烈沸腾
而进入接收瓶中
C.毛细玻璃管的作用是引入空气氧化2-丙醇 二、解答题:
D.实验中,必须控制水浴温度高于82.5℃ 15.(16分)有机物种类繁多,广泛存在,在生产和生活中有着重要的应用。
Ⅰ. 有一种有机物X,其结构为 ,试回答下列问题:
(1) X中的含有的官能团有 。
12.分支酸是一种重要的生物化学中间体,位于不同类别有机物生物合成途径的分支点。其结构简式 (2) 向X中加入金属钠,将发生反应的化学方程式是 。
如图。下列关于分支酸的叙述不正确的是( ) (3) 如果在X中加入NaOH溶液,将发生反应的化学方程式是 。
A.分子中含有2个手性碳原子 Ⅱ.某兴趣小组进行了一系列的实验,按要求回答下列问题:
B.存在含苯环的同分异构体 (4) 准确称取4.4g某有机物样品M(只含C、H、O三种元素),经充分燃烧后的产物依次通过浓硫酸和
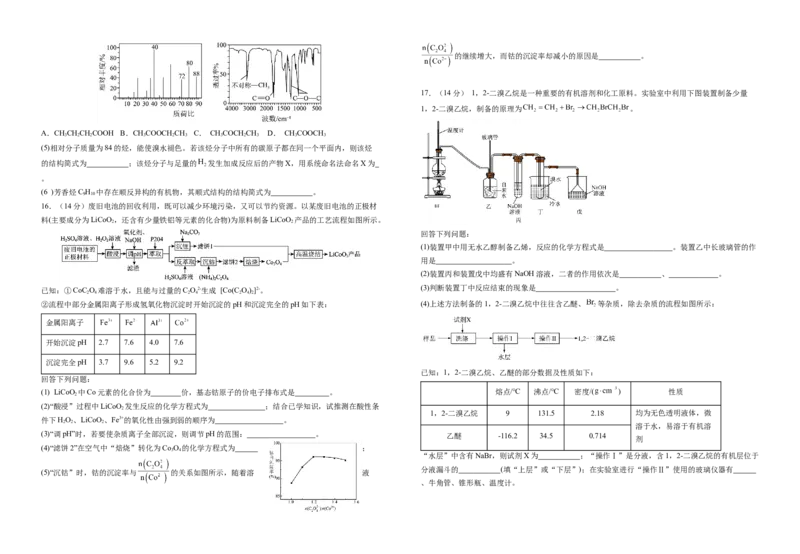
C.分子中环上的一氯代物有3种 碱石灰,二者质量分别增加3.6g和8.8g。又知有机物X的质谱图和红外光谱分别如图所示,则该有机
D.和Br 发生1:1加成反应,产物有4种 物的分子式为 ,结构简式可能为 (填序号)。
2
13.实验室回收废水中苯酚的过程如图所示。下列分析错误的是( )的继续增大,而钴的沉淀率却减小的原因是 。
17.(14分) 1,2-二溴乙烷是一种重要的有机溶剂和化工原料。实验室中利用下图装置制备少量
1,2-二溴乙烷,制备的原理为 。
A.CHCHCHCOOH B.CHCOOCH CH C. CHCOCH CH D. CHCOOCH
3 2 2 3 2 3 3 2 3 3 3
(5)相对分子质量为84的烃,能使溴水褪色。若该烃分子中所有的碳原子都在同一个平面内,则该烃
的结构简式为 ;该烃分子与足量的 发生加成反应后的产物X,用系统命名法命名X为
。
(6 )芳香烃C H 中存在顺反异构的有机物,其顺式结构的结构简式为 。
9 10
16.(14分)废旧电池的回收利用,既可以减少环境污染,又可以节约资源。以某废旧电池的正极材
料(主要成分为LiCoO ,还含有少量铁铝等元素的化合物)为原料制备LiCoO 产品的工艺流程如图所示。
2 2
回答下列问题:
(1)装置甲中用无水乙醇制备乙烯,反应的化学方程式是 。装置乙中长玻璃管的作
用是 。
(2)装置丙和装置戊中均盛有NaOH溶液,二者的作用依次是 、 。
已知:①CoC O 难溶于水,且能与过量的C O2-生成 [Co(C O)]2-。 (3)判断装置丁中反应结束的现象是 。
2 4 2 4 2 4 2
②流程中部分金属阳离子形成氢氧化物沉淀时开始沉淀的pH和沉淀完全的pH如下表: (4)上述方法制备的1,2-二溴乙烷中往往含乙醚、 等杂质,除去杂质的流程如图所示:
金属阳离子
开始沉淀pH 2.7 7.6 4.0 7.6
沉淀完全pH 3.7 9.6 5.2 9.2
已知:1,2-二溴乙烷、乙醚的部分数据及性质如下:
回答下列问题:
(1) LiCoO 中Co元素的化合价为 价,基态钴原子的价电子排布式是 。 熔点/℃ 沸点/℃ 密度/( ) 性质
2
(2)“酸浸”过程中LiCoO 发生反应的化学方程式为 ;结合已学知识,试推测在酸性条
2
1,2-二溴乙烷 9 131.5 2.18 均为无色透明液体,微
件下HO、LiCoO 、Fe3+的氧化性由强到弱的顺序为 。
2 2 2
溶于水,易溶于有机溶
(3)“调pH”时,若要使杂质离子全部沉淀,则调节pH的范围: 。 乙醚 -116.2 34.5 0.714
剂
(4)“滤饼2”在空气中“焙烧”转化为Co O 的化学方程式为 ;
3 4
“水层”中含有NaBr,则试剂X为 ;“操作Ⅰ”是分液,含1,2-二溴乙烷的有机层位于
分液漏斗的 (填“上层”或“下层”);在实验室进行“操作Ⅱ”使用的玻璃仪器有
(5)“沉钴”时,钴的沉淀率与 的关系如图所示,随着溶 液
、牛角管、锥形瓶、温度计。18.(14分)有机化合物G可用于辅助治疗高血压。一种制备G的合成路线如图所示:
回答下列问题:
(1)反应①除生成B外,还生成的有机产物为 (填结构简式);B中含有的官能团名称是
。
(2)反应②的反应类型是 。
(3)反应③所需要的试剂X通常为 。
(4)E的结构简式是 。
(5)F生成G的化学方程式是 。
(6)甲是A的同分异构体,除A外,满足下列条件的甲的结构有 种(不考虑立体异构)。
a.属于芳香族化合物 b.含有—NH 、—Cl基团
2
其中核磁共振氢谱有4组峰且峰面积之比为2∶2∶2∶2的同分异构体的结构简式是 (填一种)。