文档内容
标准学术能力诊断性测试2024年12月测试
化学试卷
本试卷共100分
可能用到的相对原子质量:H 1 Be 9 B 11 C 12 O 16 F 19 K 39
一、单项选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一个选项
是符合题意的。
1.中华文化绚丽灿烂,源远流长。对下列珍贵文物的主要化学成分说法错误的是
青铜器何尊 甲骨文龟甲 睡虎地秦简 五代倒流壶
A B C D
A.国宝西周青铜器何尊主要是铜锡合金
B.记载甲骨文的龟甲的化学成分主要是碳酸钙
C.睡虎地秦简简片的化学成分主要是纤维素
D.五代瓷器耀州提梁倒流壶的化学成分主要是硅酸盐
2.化学与航天科技发展密切相关,下列说法错误的是
A.火箭隔热层所用的新型陶瓷材料Si N 熔点高、难氧化
3 4
B.问天实验舱使用的石墨烯属于新型无机非金属材料
C.飞船返回舱表层用的玻璃纤维和酚醛树脂复合烧蚀材料属于有机高分子材料
D.返回舱用的降落伞材质是高强度芳纶纤维,可由间苯二胺和间苯二甲酸缩聚合成
3.中国战机歼-20上用到的氮化镓材料。以含镓废料[主要成分为Ga(CH ) ]制备半导体材料GaN
3 3
的工艺流程如图所示。已知:Ga和Al的性质相似。下列说法错误的是
第1页 共12页 第2页 共12页
废 料
盐
酸
酸
溶 G a C l
3
溶 液 操 作 X G a C l
3
· n H
2
O 加
S
气
O
热
C
脱
体
l
2
水
a
G a C l
3
气
N
合
体
H
成
3
b
G a N
A.“操作X”是蒸发、结晶、过滤、洗涤、干燥
B.气体a是SO ,可用品红溶液来检验
2
C.“加热脱水”可用HCl气体代替SOCl
2
D.GaN是共价晶体,“合成”产生的气体b可循环利用
4.学好化学,学会感恩。美国杜克大学的 P.Murali Doraiswamy 教授研究发现,当向别人表达
感谢时,人体内会释放出一类“奖励”性化学物质,包括:多巴胺、5-羟色胺、皮质醇等。
它们的分子结构依次如图所示,下列说法不正确的是
多巴胺 5-羟色胺 皮质醇
A.多巴胺和5-羟色胺既能和盐酸反应,又能和碳酸钠溶液反应
B.5-羟色胺分子中的碳原子、氮原子、氧原子可以共平面
C.1mol皮质醇最多可与2mol H 、1mol NaOH反应
2
D.1mol多巴胺和1mol 5-羟色胺与浓溴水反应,反应掉一样多的溴
5.锂电池、新能源汽车、光伏是我国出口三大拳头产品。其中锂电池的制备原理如图所示,下列有
关说法错误的是
{#{QQABKQIEogCIQBBAARhCAwWwCgOQkgCCCagGBBAAIAABSQNABAA=}#}A.制备组装时,安全起见,正极材料是LiCoO ,负极材料是石墨,并未用到单质金属锂
2
B.组装好后开始充电,正极发生反应为:LiCoO →Li CoO + xLi+ + xe-,负极发生反应为:
2 1-x 2
6C + xLi+ + xe-→Li C
x 6
C.图中所示正在充电,锂离子电池比能量高
D.石墨是混合型晶体,图中所示的LiCoO 是一个晶胞
2
6.适度食用洋葱有益健康。洋葱中对身体有益的主要化学成分的结构式如图所示,下列有关
说法不正确的是
对香豆酸
阿魏酸
A.由图示可知:由CH → CH OH、HCOOH的过程是自发的过程
4 3
B.CN负载的W单原子光催化剂(W-SA-PCN)比纳米级催化剂有更高的催化剂利用效率
a
槲皮素 山奈酚 C.金属钨晶胞(如下图)的棱长为a pm,则钨原子半径是 3
4
pm
A.它们都有抗氧化作用
B.槲皮素和山奈酚互为同分异构体
C.对香豆酸分子中,所有原子可以共平面
D.阿魏酸能发生加聚反应,也能发生缩聚反应
7.张涛院士、李亚栋院士因“单原子催化”理论及应用而荣获“2024 年未来科技大奖”。金属钨单
D.催化过程中只有极性键的断裂和形成
原子W在H O蒸汽中光催化CH 转化CH OH、HCOOH等产物,下列有关该催化过程的说法中
2 4 3
8.钛是一种重要的航天航空材料,也是一种重要的医用金属材料。陕西省宝鸡市有全国乃至世界最
错误的是
大的钛业基地。从高钛渣(主要为TiO )中提炼海绵钛的流程如图所示。
2
第3页 共12页 第4页 共12页
{#{QQABKQIEogCIQBBAARhCAwWwCgOQkgCCCagGBBAAIAABSQNABAA=}#}氯化后的粗TiCl 中含有FeCl 、SiCl 、AlCl 等杂质,相关物质的沸点如下表:
4 3 4 3
化合物 TiCl FeCl SiCl AlCl
4 3 4 3
沸点/℃ 136 310 56.5 180
下列说法不正确的是
高温
A.“氯化”时发生的主要反应是:TiO +2C+2Cl =TiCl +2CO
2 2 4
B.“分馏”得到的低沸点物为SiCl ,可用于制备高纯硅
4
C.已知“除铝”的方法是用水湿润的活性炭加入到粗TiCl 中,目的是将AlCl 转化为Al(OH)
4 3 3
而除去
D.“还原”过程中还原剂选择金属镁,气氛还可以选择N
2
9.下列物质之间不能通过一步反应实现如图所示转化关系的是
X Y Z
A HCl Cl HClO
2
B C CO CO 2
C Fe FeCl FeCl
3 2
D Si SiO H SiO
2 2 3
10.下列方程式或离子方程式与所给事实不相符的是
A.少量的SO 通入NaClO溶液中:SO +3NaClO +H O=NaCl + Na SO + 2HClO
2 2 2 2 4
B.在10mL0.1mol/L (NH ) Fe(SO ) 溶液中滴加10mL0.1mol/L的Ba(OH) 溶液:
4 2 4 2 2
2NH
第5页 共12页 第6页 共12页
+4 +SO 24 −
A.该离子是一种配位离子,且配体数是2,配位数是4
B.同周期第一电离能比Z大的还有两种元素
C.该离子中的σ键数是22
D.X Z-YX -YX -ZX 的沸点比X Y-YX -YX -YX 的沸点高
2 2 2 2 3 2 2 3
12.钴和镍在军工和新能源工业必不可少。从钴镍渣(主要含CoO、NiO和少量FeO、Cu)中回收Co
和Ni的流程如图所示。
已知:①Co2+ + 6NH ·H O = [Co(NH ) ]2+ + 6H O K=105;②K [Ni(OH) ]=1.0×10−15,完全沉淀
3 2 3 6 2 sp 2
时c(Ni2+)≤10−5mol·L−1;③K (NH ·H O) = 10−5。
b 3 2
下列说法正确的是
A.滤渣1是Cu,滤渣2是Fe(OH)
2
B.氧化性:H O >Co3+>Fe3+
2 2
C.“氧化沉钴”中氧化剂、还原剂的物质的量之比为2:1
c([Co(NH ) ]2+)
3 6
D.若“沉镍”完全后滤液中c(NH 4 +)=10−3mol·L−1,则 c(Co2+) ≥10−13
13.2024年7月22日报道:我国科学家在嫦娥五号带回的月球样本中,发现了一种富含水分子和铵
的未知矿物晶体——ULM-1。该矿物的化学式为(NH ,K,Cs,Rb) MgCl ·6H O。月球上发现水
4 3 2
意义重大。下列有关说法错误的是
A.晶体具有各向异性,有固定的熔沸点,可以通过 x-射线衍射鉴定晶体
B.由化学式看,该矿物相当于一种复盐,属于离子晶体
C.(NH ,K,Cs,Rb) MgCl ·6H O 是一种超分子。其中 N、O 都是 sp3杂化
4 3 2
+Ba2++2OH-=BaSO ↓+2NH +H O
4 3 2
D.Mg、K、Rb、Cs(镁、钾、铷、铯)的金属性依次增强,其最高价氧化物的水化物
C.侯氏制碱法的原理:NaCl+NH +H O+CO =NaHCO ↓+NH Cl、
3 2 2 3 4 的碱性依次增强
2NaHCO =Na CO +H O+CO ↑
3 2 3 2 2
14.2024 年巴黎奥运会上,中国运动员在 50 米步枪三姿项目比赛中夺冠。这是他们首次身
D.海水提溴工艺中,用纯碱溶液富集Br :3Br +3CO 2-=BrO -+5Br-+3CO ↑
2 2 3 3 2
穿中国自主研发的射击服装(皮服)。制作皮服用到了帆布、牛皮、橡胶片、聚酯纤维、
11.X、Y、Z、W四种原子序数依次增大的前四周期元素,其中Y原子的最外层电子数是内层电子数
尼龙、氨纶等等材料。下列有关说法错误的是
的2倍,Z和Y位于同一周期且第一电离能大于同周期相邻元素,W位于ds区,其+1价阳离子
A.帆布一般由棉、麻织成,棉、麻主要成分是纤维素,是一种多糖
没有成单电子。四种元素可形成一种离子如图所示,下列有关说法错误的是
{#{QQABKQIEogCIQBBAARhCAwWwCgOQkgCCCagGBBAAIAABSQNABAA=}#}B.牛皮的主要成分是蛋白质,可以通过灼烧或颜色反应来鉴别
C.天然橡胶又名聚异戊二烯,能被溴水、酸性高锰酸钾溶液腐蚀
D.聚酯纤维、尼龙、氨纶等都是人造纤维,是人造高分子材料
15.下列有关化学反应速率或化学平衡的说法,正确的是
A.锌粒和稀硫酸反应制氢气,为了使反应加快,可以多滴加硫酸铜溶液
回答下列问题:
B.实验室可以用 0.1mol/L、0.2mol/L 的酸性 KMnO 溶液分别与 0.1mol/L H C O 的溶液
4 2 2 4
(1)为了提高“焙烧”过程的效率,可以采取的措施为 (回答任意两点)。“焙烧”过
反应,探究浓度对反应速率的影响
程加入生石灰,有效解决了SO 的危害,则ReS 转化为Ca(ReO ) 的方程式为 。
2 2 4 2
C.实验证明:向同浓度的 H O 溶液中分别滴加同浓度同滴数的 CuSO 溶液、KMnO 溶
2 2 4 4
(2)“萃取”机理为:R N+H++ReO -=R N·HReO ,则“反萃取”所用试剂X为 。
3 4 3 4
液,后者产生 O 快。这说明 MnO -的催化效果优于 Cu2+
2 4
“反萃取”后萃取剂可 。
D.催化剂虽然不能改变化学平衡的转化率,但是能提高化工生成效率
(3)右图表示萃取液流速与铼吸附率关系,萃取剂流速宜选用
二、非选择题:本题共5小题,共55分。 的范围是6~8BV/h,选择此范围的原因是 。
16.(13分)中国科学家研发的晶体材料氟代硼铍酸钾晶体KBBF(KBe BO F )是一种非线性光学晶
2 3 2 (4)已知高铼酸铵微溶于冷水,易溶于热水。提纯粗高铼酸铵
体材料,广泛应用于激光、光刻录等领域,领先世界。回答下列问题:
固体的方法是 。
(1)钾原子的最外能层符号是 ,氟原子核外电子运动的空间状态有 种,硼原子
(5)经过上述反应后制备的铼粉中含有少量碳粉和铁粉(其熔沸点见下表),在3500℃下,利用
的价层电子排布式是 。
氢气提纯可得到纯度达99.995%的铼粉,请分析原因 。
(2)KBBF晶体中Be、B、O、F、K五种元素的原子半径自大到小的顺序是 ,第一电离
能自小到大的顺序是 ,电负性自大到小的顺序是 。
物质 熔点(℃) 沸点(℃)
(3)Be、B、O、F、K五种元素的单质形成的晶体类型有 种,五种单质晶体的熔点最高
的是 。 Re 3180 5900
(4)K O 的阴阳离子比为 ,BF 分子中硼原子的杂化类型是 ,BF 分子空间构型
2 2 3 3 C 3652 4827
为 。
Fe 1535 2750
(5)KBBF晶体晶胞结构如图甲所示(钾的元素符号K已给,氧的元素符
号未标示),晶胞中代表硼(B)的字母是 。该KBBF晶体的
18.(11分)路透社2024年8月28日报道,根据美国政府发布的数据,今年上半年,美国从中国进
晶胞参数分别为a nm和c nm,则晶体密度为 g·cm-3(N 表示
A 口餐废油脂(俗称“地沟油”)约 600000 吨用以生产航空生物柴油。某实验室模拟酯交换法生
阿伏加德罗常数的值)。
产生物柴油流程如图所示。
17.(10分)我国战机歼-20的单晶涡轮叶片要用到比黄金还要贵重的稀有金属铼。陕西省华州秦岭
山中产铼矿。铼可通过还原高铼酸铵(NH ReO )制备。以钼精矿(主要成分为钼的硫化物和少量
4 4
铼的硫化物)制取高铼酸铵的流程如图所示。
第7页 共12页 第8页 共12页
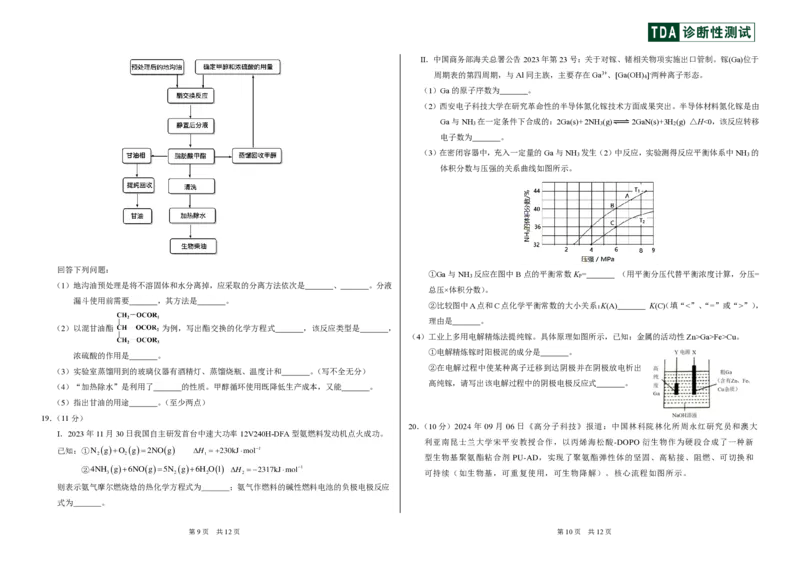
{#{QQABKQIEogCIQBBAARhCAwWwCgOQkgCCCagGBBAAIAABSQNABAA=}#}Ⅱ.中国商务部海关总署公告2023年第23号:关于对镓、锗相关物项实施出口管制。镓(Ga)位于
周期表的第四周期,与Al同主族,主要存在Ga3+、[Ga(OH) ]-两种离子形态。
4
(1)Ga的原子序数为 。
(2)西安电子科技大学在研究革命性的半导体氮化镓技术方面成果突出。半导体材料氮化镓是由
Ga与NH 在一定条件下合成的:2Ga(s)+ 2NH (g) 2GaN(s)+3H (g) △H<0,该反应转移
3 3 2
电子数为 。
(3)在密闭容器中,充入一定量的Ga与NH 发生(2)中反应,实验测得反应平衡体系中NH 的
3 3
体积分数与压强的关系曲线如图所示。
回答下列问题:
①Ga与NH 反应在图中B点的平衡常数K = (用平衡分压代替平衡浓度计算,分压=
3 P
(1)地沟油预处理是将不溶固体和水分离掉,应采取的分离方法依次是 、 。分液
总压×体积分数)。
漏斗使用前需要 ,其方法是 。
②比较图中A点和C点化学平衡常数的大小关系:K(A) K(C() 填“<”、“=”或“>”),
理由是 。
(2)以混甘油酯 为例,写出酯交换的化学方程式 ,该反应类型是 ,
(4)工业上多用电解精炼法提纯镓。具体原理如图所示,已知:金属的活动性Zn>Ga>Fe>Cu。
①电解精炼镓时阳极泥的成分是 。
浓硫酸的作用是 。
②在电解过程中使某种离子迁移到达阴极并在阴极放电析出
(3)实验室蒸馏用到的玻璃仪器有酒精灯、蒸馏烧瓶、温度计和 。(写不全无分)
高纯镓,请写出该电解过程中的阴极电极反应式 。
(4)“加热除水”是利用了 的性质。甲醇循环使用既降低生产成本,又能 。
(5)指出甘油的用途 。(至少两点)
19.(11分)
20.(10分)2024 年 09 月 06 日《高分子科技》报道:中国林科院林化所周永红研究员和澳大
I.2023年11月30日我国自主研发首台中速大功率12V240H-DFA型氨燃料发动机点火成功。
利亚南昆士兰大学宋平安教授合作,以丙烯海松酸-DOPO 衍生物作为硬段合成了一种新
已知:①
型生物基聚氨酯粘合剂 PU-AD,实现了聚氨酯弹性体的坚固、高粘接、阻燃、可切换和
②
可持续(如生物基,可重复使用,可生物降解)。核心流程如图所示。
则表示氨气摩尔燃烧焓的热化学方程式为 ;氨气作燃料的碱性燃料电池的负极电极反应
式为 。
第9页 共12页 第10页 共12页
N
2
( g ) + O
2
( g ) = 2 N O ( g ) H =+230kJmol−1
1
4NH (g)+6NO(g)=5N (g)+6H O(l) H =−2317kJmol−1
3 2 2 2
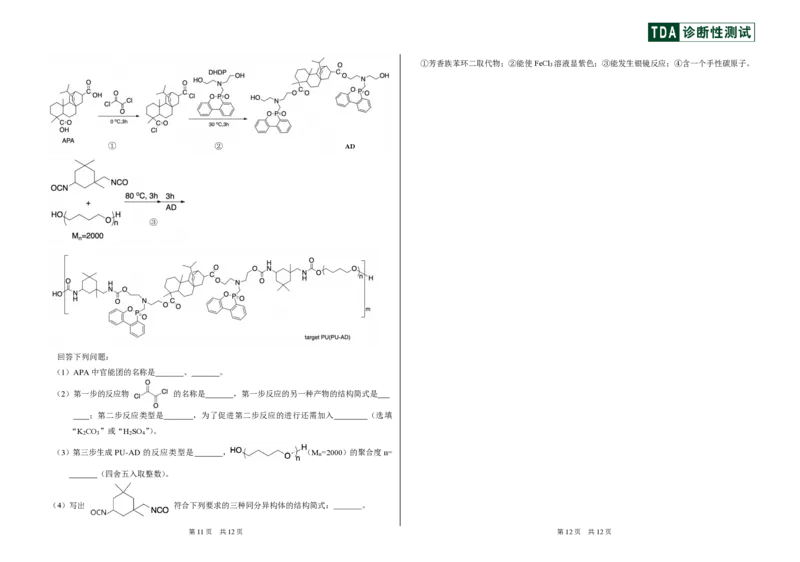
{#{QQABKQIEogCIQBBAARhCAwWwCgOQkgCCCagGBBAAIAABSQNABAA=}#}①芳香族苯环二取代物;②能使FeCl 溶液显紫色;③能发生银镜反应;④含一个手性碳原子。
3
① ② AD
③
回答下列问题:
(1)APA中官能团的名称是 、 。
(2)第一步的反应物 的名称是 ,第一步反应的另一种产物的结构简式是
;第二步反应类型是 ,为了促进第二步反应的进行还需加入 (选填
“K CO ”或“H SO ”)。
2 3 2 4
(3)第三步生成PU-AD 的反应类型是 , (M =2000)的聚合度n=
n
(四舍五入取整数)。
(4)写出 符合下列要求的三种同分异构体的结构简式: 。
第11页 共12页 第12页 共12页
{#{QQABKQIEogCIQBBAARhCAwWwCgOQkgCCCagGBBAAIAABSQNABAA=}#}标准学术能力诊断性测试 2024 年 12 月测试
化学参考答案
一、单项选择题:本题共 15 小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只
有一个选项是符合题意的。
1 2 3 4 5 6 7 8 9 10
B C A C D B D D D B
11 12 13 14 15
C D C D D
二、非选择题:本题共5小题,共55分。
16.(13分)
(1)N(1分) 5(1分) 2s22p1(1分)
(2)K>Be>B>O>F(1分) KO>B>Be>K(1分)
(3)3(1分) 硼(1分)
(4)1:2(1分) sp2(1分) 平面正三角形(答平面三角形也可给分)(1分)
(5) Z(1分)(154×2)/(N a2c×10-21) (1分)
A
17.(10分)
(1)适当升高温度,将钼精矿粉碎,增大空气通入量(2分)
高温
4ReS +10CaO+19O 2Ca(ReO ) +8CaSO (2分)
2 2 4 2 4
(2)氨水(1分) 循环利用 (1分)
(3)萃取液流速小于 6BV/h,萃取时间太长,会降低生产效率;萃取液流速大于 8BV/h,铼
吸附率下降太多(2分)
(4)重结晶或用热水溶解再降温结晶,过滤,再洗涤干燥(1分)
(5)3500℃时,Fe已气化去除;固态碳与H 完全反应,形成了气态物质(1分)
2
18.(11分)
(1)过滤(1分) 分液(1分) 检漏(1分)
关闭旋(活)塞,注入少量蒸馏水,观察旋塞处是否漏水;再塞上玻璃塞(凹槽和小孔
错开),摁住玻璃塞倒立,观察玻璃塞处是否漏水,将玻璃塞旋转180度,再如是检查。
(1分)
第 1 页 共2页
{#{QQABKQIEogCIQBBAARhCAwWwCgOQkgCCCagGBBAAIAABSQNABAA=}#}(2)
取代反应(水解反应)(1分) 催化剂(1分)
(3)水冷凝管、接液管(牛角管)、锥形瓶(1分,少写不得分)
(4)脂肪酸甲酯的沸点比水的沸点高得多的性质(1分) 提高甲醇的转化率(1分)
(5)润肤用品,制硝化甘油(1分,少于两点无分)
19.(11分)
3 1 3
Ⅰ.NH (g)+ O (g)= N (g)+ H O(l)H =−406.75kJmol−1(1分)
3 4 2 2 2 2 2
(1分)
Ⅱ.(1)31(1分)
(2) 6N (1分)
A
(3)①8.1MPa(2分)
②<(1分) 该反应为放热反应,同压条件下,温度升高平衡左移,NH 的体积分数
3
增大,K减小,故T >T 且K(A)