文档内容
工作秘密
严禁泄露
自贡市普高 2025 届第一次诊断性考试
化学
注意事项:
考试时间共75分钟。试卷共6页,满分100分。
考生作答客观题时,必须使用2B铅笔在答题卡上将所选答案对应的标号涂黑。
考生作答主观题时,须将答案答在答题卡上,在本试题卷、草稿纸上答题无效。考试结束后,
将本试题卷和答题卡一并交回。
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.千年盐都、南国灯城、恐龙之乡,自贡是一座历史悠久的中国文化名城。对下列自贡文化遗产的说法错误
的是( )
富顺豆花 荣县大佛 恐龙化石 彩灯制作
A.富顺豆花是四川省第一批非物质文化遗产,豆花制作中需要煮豆浆,豆浆属于液溶胶
B.荣县大佛是世界第二大石刻佛,荣县大佛的主要成分是高分子化合物
C.自贡恐龙博物馆是世界上展示侏罗纪恐龙化石最多、最全的地方,可以用 断代法来测定化石所处的年
代
D.自贡彩灯是国家级非物质文化遗产,在立体扎丝工艺中,使用的铁丝是合金
2.化学用语是表达化学思想的专门语言,包括符号语言、文字语言和图表语言。下列化学用语表达错误的是
( )
A. 的 模型: B.水合氯离子的示意图:C. 的结构式: D.“钠与水反应”实验有关图标:
3.自贡市怀德镇素有“桂圆之乡”的美称,中医认为桂圆肉有滋补养血、安神补脑等功效,其富含的铁元素
可经过以下步骤完成检验:①桂圆肉剪碎研磨;②用适量稀 溶液溶解;③过滤取滤液;④滴加试剂检
测其中的铁元素。上述操作中,未用到的仪器为( )
A. B. C. D.
4.在人体中,大概含有60多种元素,其中含量前10的元素分别是氧、碳、氢、氮、钙、磷、硫、钾、钠、
氯。下列说法正确的是( )
A.酸性: B. 通入紫色石蕊溶液中,溶液先变红后褪色
C.金属性: D. 均属于酸性氧化物
5.下列实验设计或操作能达成对应实验目的的是( )
选项 A B C D
实验装置
实验目的 碱式滴定管排气泡
分离苯与 溶液
干燥 实验室制
A.A B.B C.C D.D
6.下列离子方程式与所给事实不相符的是( )
A.海水提溴过程中,将溴吹入 吸收塔:
B.某主要成分为苛性钠和铝粉的管道疏通剂:
C.用 溶液能有效除去误食的
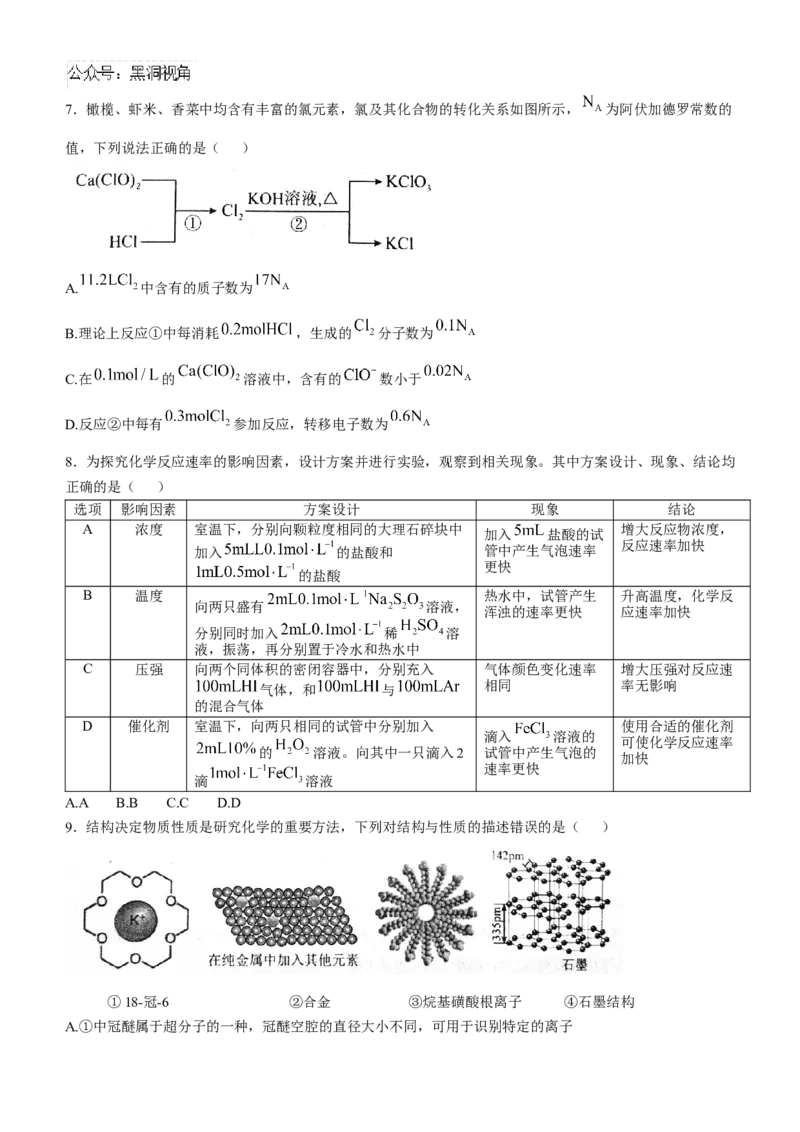
D.用草酸标准溶液测定高锰酸钾溶液浓度:7.橄榄、虾米、香菜中均含有丰富的氯元素,氯及其化合物的转化关系如图所示, 为阿伏加德罗常数的
值,下列说法正确的是( )
A. 中含有的质子数为
B.理论上反应①中每消耗 ,生成的 分子数为
C.在 的 溶液中,含有的 数小于
D.反应②中每有 参加反应,转移电子数为
8.为探究化学反应速率的影响因素,设计方案并进行实验,观察到相关现象。其中方案设计、现象、结论均
正确的是( )
选项 影响因素 方案设计 现象 结论
A 浓度 室温下,分别向颗粒度相同的大理石碎块中 增大反应物浓度,
加入 盐酸的试
反应速率加快
加入 的盐酸和 管中产生气泡速率
更快
的盐酸
B 温度 热水中,试管产生 升高温度,化学反
向两只盛有 溶液,
浑浊的速率更快 应速率加快
分别同时加入 稀 溶
液,振荡,再分别置于冷水和热水中
C 压强 向两个同体积的密闭容器中,分别充入 气体颜色变化速率 增大压强对反应速
相同 率无影响
气体,和 与
的混合气体
D 催化剂 室温下,向两只相同的试管中分别加入 使用合适的催化剂
滴入 溶液的
可使化学反应速率
的 溶液。向其中一只滴入2 试管中产生气泡的
加快
速率更快
滴 溶液
A.A B.B C.C D.D
9.结构决定物质性质是研究化学的重要方法,下列对结构与性质的描述错误的是( )
①18-冠-6 ②合金 ③烷基磺酸根离子 ④石墨结构
A.①中冠醚属于超分子的一种,冠醚空腔的直径大小不同,可用于识别特定的离子B.②中在纯金属中加入其它元素,使原子层之间的相对滑动变得困难导致合金的硬度变大
C.③中烷基磺酸根离子在水中会形成亲水基向内疏水基向外的胶束,而用作表面活性剂
D.④中石墨晶体是层状结构,每个碳原子的配位数为3,属于混合晶体,熔沸点高
10.如图所示的化合物是一种重要化工原料,X、Y、Z、W、E是原子序数依次增大的短周期主族元素,其
中Z、E同族,基态Y原子的核外有3个未成对电子。下列说法正确的是( )
A.键角:
B. 的空间结构均为平面三角形
C.Z的第一电离能比同周期相邻元素的第一电离能都大
D.共价键极性:
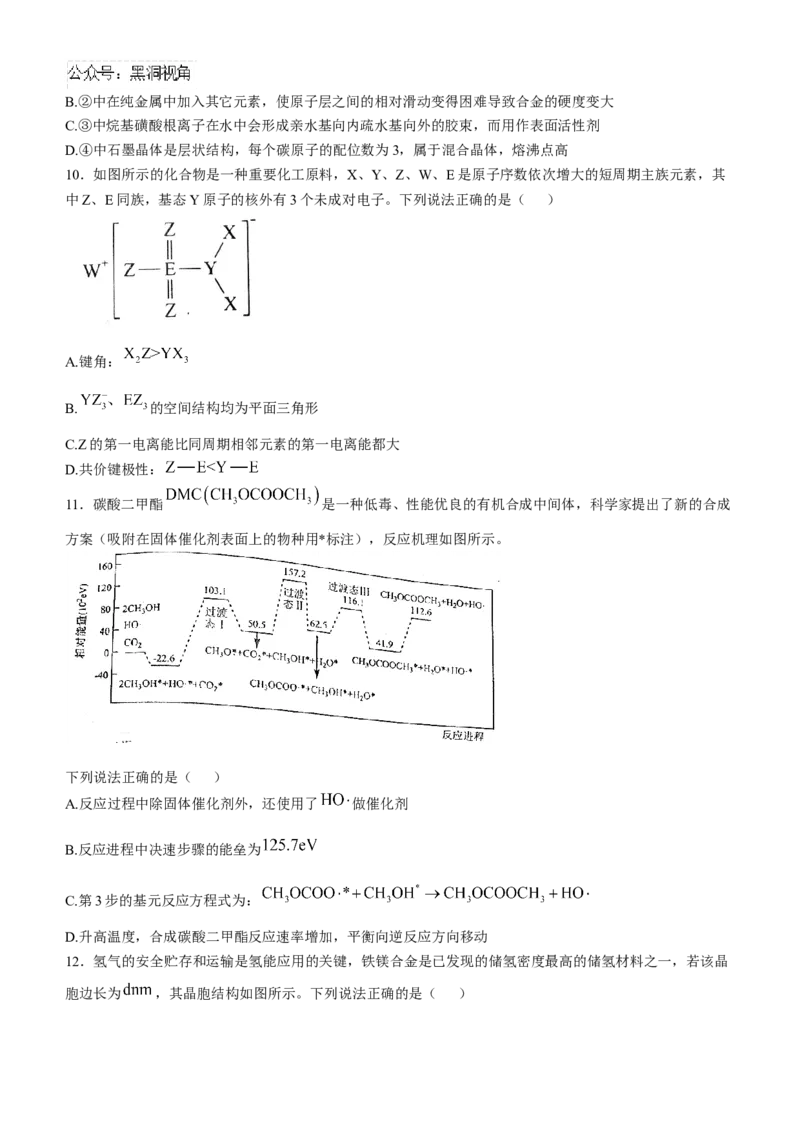
11.碳酸二甲酯 是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成
方案(吸附在固体催化剂表面上的物种用*标注),反应机理如图所示。
下列说法正确的是( )
A.反应过程中除固体催化剂外,还使用了 做催化剂
B.反应进程中决速步骤的能垒为
C.第3步的基元反应方程式为:
D.升高温度,合成碳酸二甲酯反应速率增加,平衡向逆反应方向移动
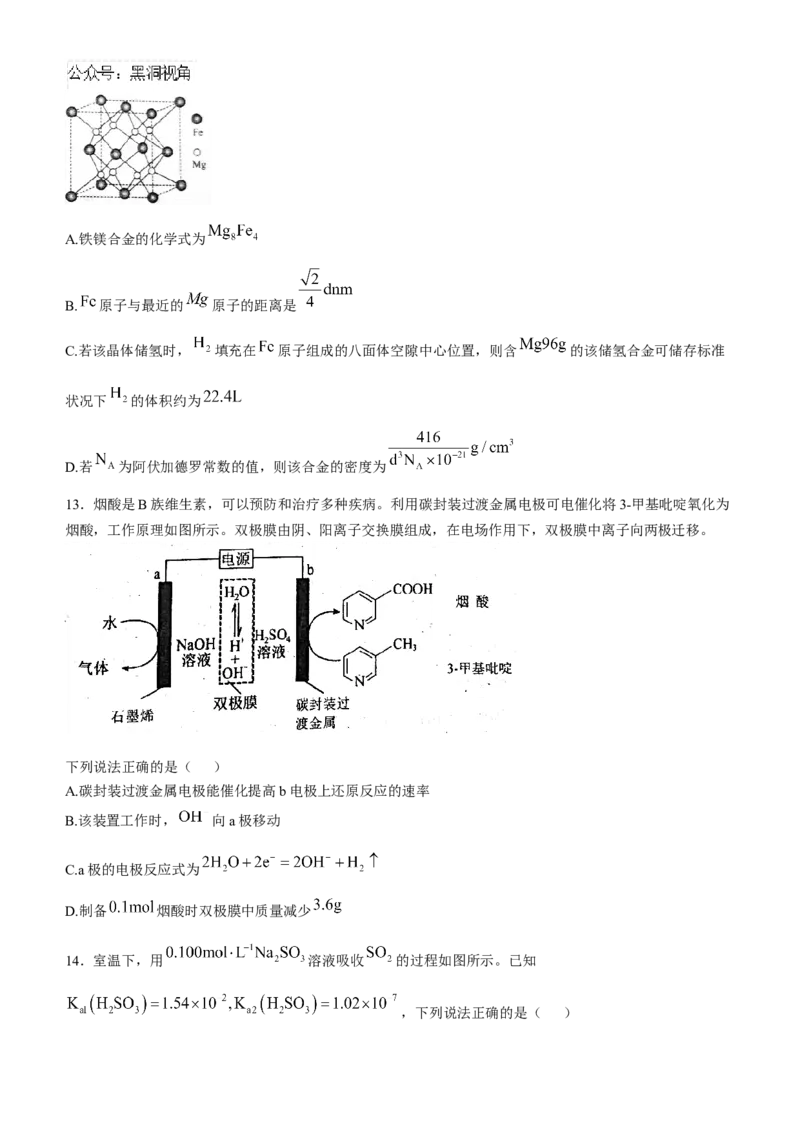
12.氢气的安全贮存和运输是氢能应用的关键,铁镁合金是已发现的储氢密度最高的储氢材料之一,若该晶
胞边长为 ,其晶胞结构如图所示。下列说法正确的是( )A.铁镁合金的化学式为
B. 原子与最近的 原子的距离是
C.若该晶体储氢时, 填充在 原子组成的八面体空隙中心位置,则含 的该储氢合金可储存标准
状况下 的体积约为
D.若 为阿伏加德罗常数的值,则该合金的密度为
13.烟酸是B族维生素,可以预防和治疗多种疾病。利用碳封装过渡金属电极可电催化将3-甲基吡啶氧化为
烟酸,工作原理如图所示。双极膜由阴、阳离子交换膜组成,在电场作用下,双极膜中离子向两极迁移。
下列说法正确的是( )
A.碳封装过渡金属电极能催化提高b电极上还原反应的速率
B.该装置工作时, 向a极移动
C.a极的电极反应式为
D.制备 烟酸时双极膜中质量减少
14.室温下,用 溶液吸收 的过程如图所示。已知
,下列说法正确的是( )A. 溶液中存在:
B.将 溶液稀释到 几乎不变
C.吸收烟气后的溶液中:
D.沉淀得到的上层清液中:
二、非选择题:本题共4小题,共58分。
15.(14分)对物质进行分类是进行性质研究的基本方法。按照一定的分类标准进行分类(如下图),相连
的物质可以归为一类,相交部分以A\B\C\D为分类代码。
(1)相连的两种物质都属于强电解质的是__________(填分类代码);请写出相连两种物质反应生成白色沉
淀的离子反应方程式__________。
(2)铜单质室温下与稀硫酸不反应,利用图中某种物质可以使铜常温下反应生成 ,请写出该反应的
化学方程式__________;向生成的 溶液中加入稀氨水会生成蓝色浑浊,继续滴加变为深蓝色溶液,加
入95%的乙醇溶液会有深蓝色晶体析出,经__________(填操作名称)可得到纯净的
晶体。
(3) 俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在。 可看作是 中
的一个O原子被S原子取代的产物。
①基态S的价层电子轨道表达式为__________, 的中心原子杂化类型为__________。
② 中各元素的简单离子半径由大到小的顺序为__________。
③利用 标准溶液定量测定某硫代硫酸钠样品的纯度。测定步骤如下:
i.溶液配制:取 硫代硫酸钠晶体 样品,用新煮沸并冷却的蒸馏
水在烧杯中溶解,完全溶解后,全部转移至 的容量瓶中,加蒸馏水至刻度线。蒸馏水煮沸的目的是__________。
ii.滴定:取 的 标准溶液 ,硫酸酸化后加入过量 ,发生反应:
。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:
。加入淀粉溶液作为指示剂,继续滴定,当溶液__________,即为滴定终
点。平行滴定3次,样品溶液的平均用量为 ,则样品纯度为__________%(保留1位小数)
16.(15分)蛇纹石矿的主要成分为 等,一种综合利用
蛇纹石矿回收镁资源的工艺流程如下:
已知:
①当溶液中被沉淀离子 时,认为该离子沉淀完全。
② ,氢硫酸的两步电离常数分别为 。
(1) 位于元素周期表第__________周期第__________族,其原子核外价层电子排布式为__________。
(2)“加压酸浸”中,滤渣1的主要成分除S外还有__________。
(3)“氧化”中空气的作用是__________, 发生反应的离子方程式为__________。
(4)“除铁”过程中生成难溶于水的、大颗粒、沉降速率快的黄钠铁矾 晶体,相较
于传统的通过调节 生成 沉淀,其它金属阳离子损失更少,理由是__________, 溶液需
缓慢加入,原因是__________。
(5)“沉镍”中,当 恰好完全沉淀时,若溶液中 ,则此时溶液的 约为
__________。
17.(14分) 导电玻璃广泛用于液晶显示屏、光催化、薄膜太阳能电池基底等,实验室可用无水四氯
化锡 制作 ,制备 的装置如图所示。有关信息如下表:
化学式
熔点/℃ 232 246
沸点/℃ 2260 652 114
其他性质 银白色固体金属
无色晶体, 易被 等氧化为 无色液体,易水解生成
(1) 位于元素周期表__________区(填“s”、“p”、“d”、“ ”、“f”)。
(2)仪器A的名称为__________,浓盐酸的作用为__________。
(3)将如图装置连接好,先检查装置的气密性,再慢慢滴入浓盐酸,待观察到__________现象后,开始加热
装置丁。
(4) 和 的反应产物可能会有 和 ,为加快反应速率并防止产品中带入 ,除了通入
过量氯气外,应控制的最佳温度在__________(填序号)范围内。
A. B. C. D.
(5)若将制得的 少许溶于水中得到白色沉淀 ,其反应的化学方程式为__________。
(6)实际制备的产品中往往含有 ,实验测定 的含量:准确称取 产品溶解,用 酸性高
锰酸钾标准溶液滴定,滴定终点时消耗酸性高锰酸钾标准溶液 。由此计算得出的产品中 的质量分
数严重偏高,理由是__________。
18.(15分)随着我国2060年实现碳中和目标的提出, 的资源化利用对于碳中和目标的实现具有非常
重要的现实意义。回答下列问题:
Ⅰ.上将 和 在催化剂作用下实现二氧化碳甲烷化是有效利用 资源的途径之一:
①
②③
(1)经计算,反应③在__________(填“高温”、“低温”、“任何条件”)下可自发进行。
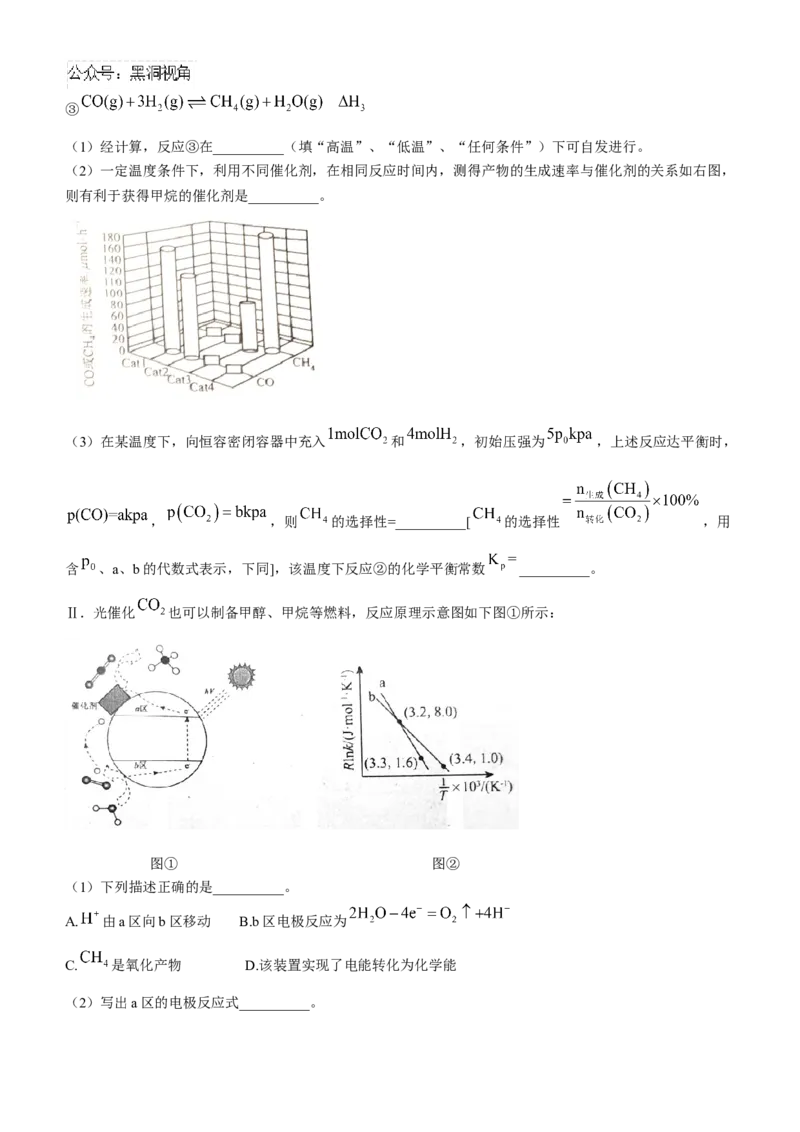
(2)一定温度条件下,利用不同催化剂,在相同反应时间内,测得产物的生成速率与催化剂的关系如右图,
则有利于获得甲烷的催化剂是__________。
(3)在某温度下,向恒容密闭容器中充入 和 ,初始压强为 ,上述反应达平衡时,
, ,则 的选择性=__________[ 的选择性 ,用
含 、a、b的代数式表示,下同],该温度下反应②的化学平衡常数 __________。
Ⅱ.光催化 也可以制备甲醇、甲烷等燃料,反应原理示意图如下图①所示:
图① 图②
(1)下列描述正确的是__________。
A. 由a区向b区移动 B.b区电极反应为
C. 是氧化产物 D.该装置实现了电能转化为化学能
(2)写出a区的电极反应式__________。(3)以 催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为
。该反应 经验公式的实验数据如图②中自线a所示,已知
经验公式 ,( 为活化能,k为速率常数。R和C为常数)。当改变外界条件
时,实验数据如图②中的曲线b所示,则实验可能改变的外界条件是__________。