文档内容
第I卷(选择题 共42分)
相对原子质量(原子量):H-1 C-12 N-14 O-16 Na-23 S-32
一、选择题(本大题共7小题,每小题6分,共42分。在每小题给出的四个备选项中,只有一项符合题目
要求)
1.化学与生活密切相关。下列说法不正确的是
A.乙烯可作水果的催熟剂
B.硅胶可作袋装食品的干燥剂
C.福尔马林可作食品的保鲜剂
D.氢氧化铝可作胃酸的中和剂
2.下列关于物质分类的说法正确的是
A.金刚石、白磷都属于单质
B.漂白粉、石英都属于纯净物
C.氯化铵、次氯酸都属于强电解质
D.葡萄糖、蛋白质都属于高分子化合物
第1页 | 共13页确,答案选A。
3.能正确表示下列反应的离子方程式是
A.Cl 通入NaOH溶液:Cl +OH-=Cl-+ClO-+H O
2 2 2
B.NaHCO 溶液中加入稀HCl:CO 2-+2H+=CO ↑+H O
3 3 2 2
C.AlCl 溶液中加入过量稀氨水:Al3++4NH ·H O=AlO -+4NH ++2H O
3 3 2 2 4 2
D.Cu溶于稀HNO :3Cu+8H++2NO -=3Cu2++2NO↑+4H O
3 3 2
4.下列实验方案中,不能达到实验目的的是
选项 实验目的 实验方案
[来源:学科网]
检验CH CH Br在NaOH 将CH CH Br与NaOH溶液共热。冷却后,取出上层水溶液
3 2 3 2
A
溶液中是否发生水解 用稀HNO 酸化加入AgNO 溶液,观察是否产生淡黄色沉淀
3 3
检验Fe(NO ) 晶体是否已 将Fe(NO ) 样品溶于稀H SO 后,滴加KSCN溶液,观察溶
3 2 3 2 2 4
B
氧化变质 液是否变红
验证Br 的氧化性强于I 将少量溴水加入KI溶液中,再加入CCl ,振荡,静置。可观
2 2 4
C
察到下层液体呈紫色
验证Fe(OH) 的溶解度小 将FeCl 溶液加入Mg(OH) 悬浊液中,振荡,可观察到沉淀
3 3 2
D
于Mg(OH) 由白色变为红褐色
2
第2页 | 共13页5.设N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.高温下,0.2molFe与足量水蒸气反应,生成的H 分子数目为0.3N
2 A
B.室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1N
A
C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2N
A
△
D.5NH NO =====2HNO +4N ↑+9H O反应中,生成28g N 时,转移的电子数目为3.75N
4 3 3 2 2 2 A
第3页 | 共13页6.下列溶液中粒子的物质的量浓度关系正确的是
A.0.1mol/LNaHCO 溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:
3
c(Na+)>c(CO 2-)>c(HCO -)>c(OH-)
3 3
B.20ml0.1mol/LCH COONa溶液与10ml0.1mol/LHCl溶液混合后呈酸性,所得溶液中:
3
c(CH COO-)>c(Cl-)>c(CH COOH)>c(H+)
3 3
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:
c(Cl-)>c(H+)>c(NH +)>c(OH-)
4
D.0.1mol/LCH COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:
3
c(OH-)>c(H+)+c(CH COOH)
3
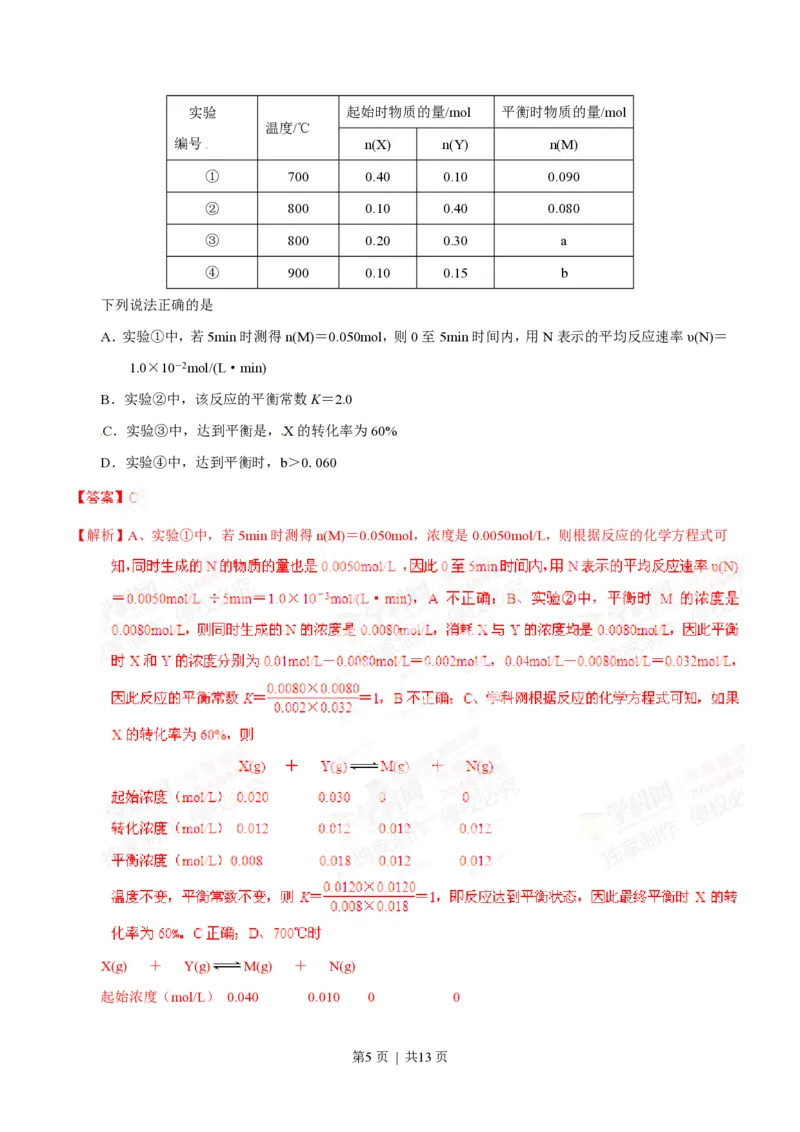
7.在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) M(g)+N(g),所得实验数据如下表:
第4页 | 共13页实验 起始时物质的量/mol 平衡时物质的量/mol
[来源:Zxxk.Com] [来源:学科网]
温度/℃
[来源:Z|xx|k.Com]
编号 n(X) n(Y) n(M)
[来源:Zxxk.Com][来源:学|科|网Z|X|X|K]
① 700 0.40 0.10 0.090
② 800 0.10 0.40 0.080
③ 800 0.20 0.30 a
④ 900 0.10 0.15 b
下列说法正确的是
A.实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率υ(N)=
1.0×10-2mol/(L·min)
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡是,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
【解析】A、实验①中,若5min时测得n(M)=0.050mol,浓度是0.0050mol/L,则根据反应的化学方程式可
X(g) + Y(g) M(g) + N(g)
起始浓度(mol/L) 0.040 0.010 0 0
第5页 | 共13页第Ⅱ卷 (非选择题 共58分)
8.(13分)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY 是红棕色气体;X与氢元素可形成
2
XH ;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。请回答下列问题:
3
(1)Y基态原子的电子排布式是________;Z所在周期中第一电离能最大的主族元素是_____。
(2)XY -离子的立体构型是_______;R2+的水合离子中,提供孤电子对的是原子是______。
2
(3)Z与某元素形成的化合物的晶胞如右图所示,晶胞中阴离子与阳离子的个数之比是___________。
(4)将R单质的粉末加入XH 的浓溶液中,通入Y ,充分反应后溶液呈深蓝色,该反应的离子方程
3 2
式是___ _________。
第6页 | 共13页素是Cl元素。
9.(13分)硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na S O ·5H O)。
2 2 3 2
I.[查阅资料]
(1)Na S O ·5H O是无色透明晶体,易溶于水。其稀溶液与BaCl 溶液混合无沉淀生成。
2 2 3 2 2
(2)向Na CO 和Na S混合液中通入SO 可制得Na S O ,所得产品中常含有少量Na SO 和Na SO 。
2 3 2 2 2 2 3 2 3 2 4
(3)Na SO 易被氧化;BaSO 难溶于水,可溶于稀HCl。
2 3 3
Ⅱ.[制备产品]
实验装置如图所示(省略夹持装置)
实验步骤:
(1)检查装置气密性,按图示加入试剂。仪器a的名称是____;E中的试剂是___(选填下列字母编
第7页 | 共13页号)。
A.稀H SO B.NaOH溶液 C.饱和NaHSO 溶液
2 4 3
(2)先向C中烧瓶加入Na S和Na CO 混合溶液,再向A中烧瓶滴加浓H SO 。
2 2 3 2 4
(3)待Na S和Na CO 完全消耗后,结束反应。过滤C中混合液,滤液经____(填写操作名称)、结
2 2 3
晶、过滤、洗涤、干燥、得到产品。
Ⅲ.[探究与反思]
(1)为验证产品中含有Na SO 和Na SO ,该小组设计了以下实验方案,请将方案补充完整。(所需
2 3 2 4
试剂从稀HNO 、稀H SO 、稀HCl、蒸馏水中选择)
3 2 4
取适量产品配成稀溶液,滴加足量BaCl 溶液,有白色沉淀生成,_____,若沉淀未完全溶解,并
2
有刺激性气味的气体产生,则可确定产品中含有Na SO 和Na SO 。
2 3 2 4
(2)为减少装置C中生成的Na SO 的量,在不改变原有装置的基础上对原有实验步骤(2)进行了改
2 4
进,改进后的操作是_______。
(3)Na S O ·5H O的溶解度随温度升高显著增大,所得产品通过_____方法提纯。
2 2 3 2
【解析】Ⅱ.[制备产品]
第8页 | 共13页(3)由于Na S O ·5H O的溶解度随温度升高显著增大,因此所得产品通过重结晶方法提纯。
2 2 3 2
【命题意图】本题主要是考查物质制备实验方案设计与评价,涉及仪器识别、物质的分离与提纯、尾气处
理、物质检验、实验方案设计等化学基础知识,意在考查学生的实验技能和综合分析问题的能力。
10.(16分)A是一种有机合成中间体,其结构简式为: 。A的
合成路线如下图,其中B~H分别代表一种有机物。
已知:
请回答下列问题:
(1)A中碳原子的杂化轨道类型有_____;A的名称(系统命名)是____;第⑧步反应类型是___。
(2)第①步反应的化学方程式是________。
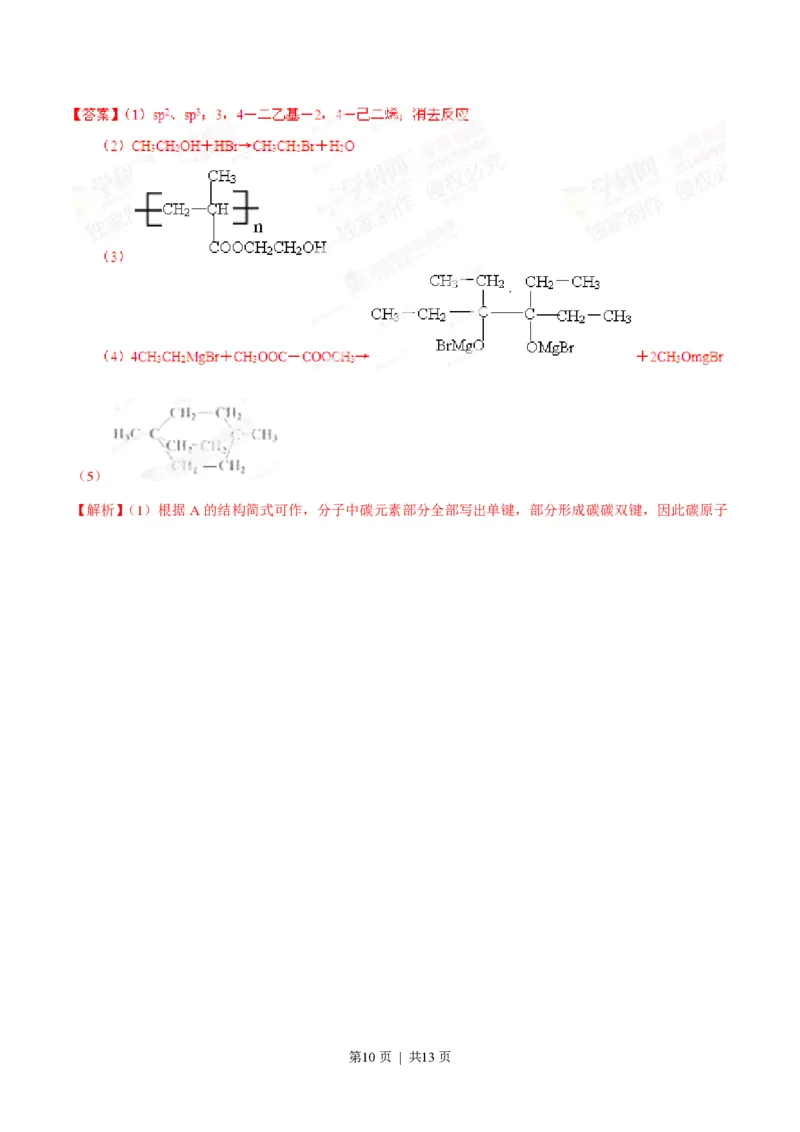
(3)C物质与CH =C(CH )COOH按物质的量之比1:1反应,其产物经加聚得到可作隐形眼镜的镜片
2 3
材料I。I的结构简式是_______________。
(4)第⑥步反应的化学方程式是________________。
(5)写出含有六元环,且一氯代物只有2种(不考虑立体异构)的A的同分异构体的结构简式____。
第9页 | 共13页(5)
【解析】(1)根据A的结构简式可作,分子中碳元素部分全部写出单键,部分形成碳碳双键,因此碳原子
第10页 | 共13页【命题意图】本题主要是考查有机物推断、命名、碳原子杂化轨道类型、有机反应类型、同分异构体判断
以及方程式书写等,是有机化学的综合考查,旨在考查学生对已知信息的获取能力、知识的迁移能力
以及灵活应用基础知识解决实际问题的能力的综合考查。
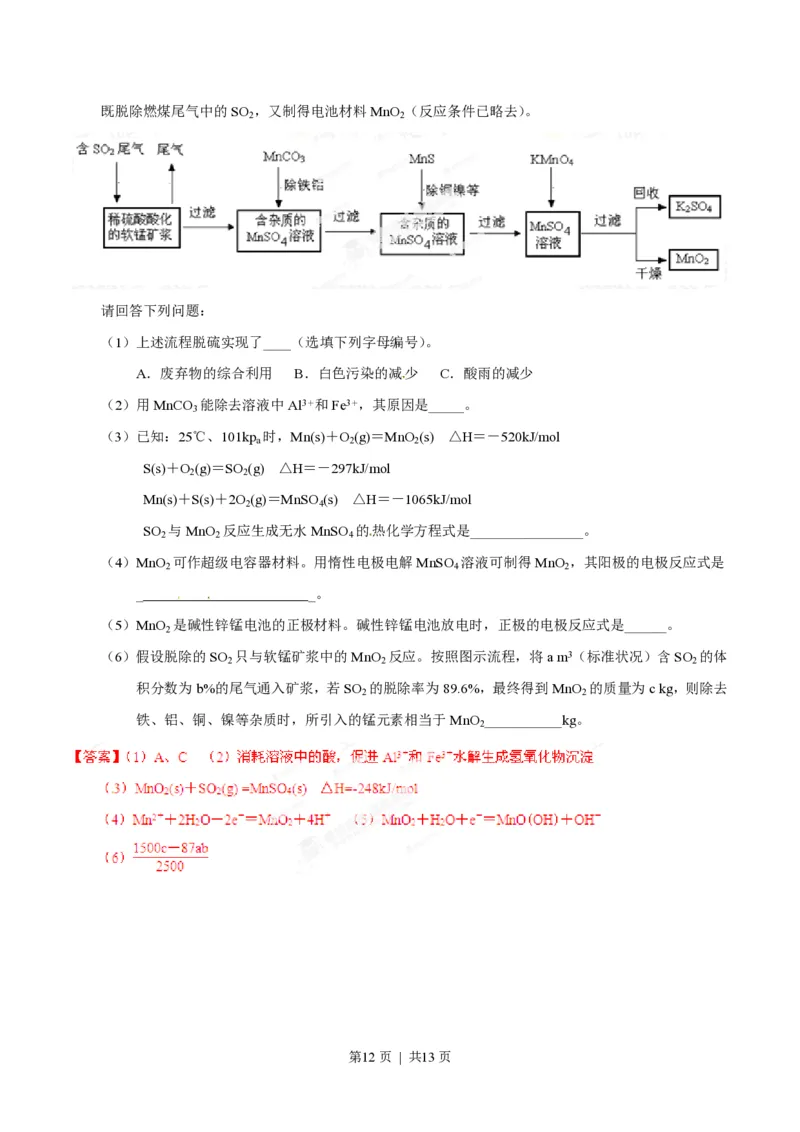
11.(16分)污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某化学研究小组利用软
锰矿(主要成分为MnO ,另含有少量头铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程
2
第11页 | 共13页既脱除燃煤尾气中的SO ,又制得电池材料MnO (反应条件已略去)。
2 2
请回答下列问题:
(1)上述流程脱硫实现了____(选填下列字母编号)。
A.废弃物的综合利用 B.白色污染的减少 C.酸雨的减少
(2)用MnCO 能除去溶液中Al3+和Fe3+,其原因是_____。
3
(3)已知:25℃、101kp 时,Mn(s)+O (g)=MnO (s) △H=-520kJ/mol
a 2 2
S(s)+O (g)=SO (g) △H=-297kJ/mol
2 2
Mn(s)+S(s)+2O (g)=MnSO (s) △H=-1065kJ/mol
2 4
SO 与MnO 反应生成无水MnSO 的热化学方程式是________________。
2 2 4
(4)MnO 可作超级电容器材料。用惰性电极电解MnSO 溶液可制得MnO ,其阳极的电极反应式是
2 4 2
_ _。
(5)MnO 是碱性锌锰电池的正极材料。碱性锌锰电池放电时,正极的电极反应式是______。
2
(6)假设脱除的SO 只与软锰矿浆中的MnO 反应。按照图示流程,将a m3(标准状况)含SO 的体
2 2 2
积分数为b%的尾气通入矿浆,若SO 的脱除率为89.6%,最终得到MnO 的质量为c kg,则除去
2 2
铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO ___________kg。
2
第12页 | 共13页第13页 | 共13页