文档内容
高二年级 12 月考试化学试题
可能用到的相对原子质量: N14 O16 Ca40 Cu64
一、单选题(本题包括15小题,每小题3分,共45分)
1.水解原理在生产、生活科研中都具有重要的应用。下列事实与盐类的水解无关的是
A.用热的纯碱溶液清洗油污
B.实验室保存和配制 溶液时,加入少量
C. 水溶液应存放在塑料瓶中,而不能存放于玻璃瓶中
D.实验室保存 溶液时,常在溶液中加入适量铁粉
2.常温下,下列各组离子一定能在指定溶液中大量共存的是
A.由水电离出的 的溶液: 、 、 、
B.使甲基橙变红的溶液中: 、 、 、
C.澄清透明的溶液中: 、 、 、
D. 的 溶液中: 、 、 、
3.提供几组常见的实验装置示意图,下列有关叙述正确的是
A.装置①中阳极上有红色物质析出
B.装置②中的铜片应与直流电源的负极相连
C.装置③中,若电解液为KOH溶液,则电极a的反应式:H-2e-+2OH-=2H O
2 2
D.装置④中,CuSO 溶液的浓度始终不变
4
4.在化学学习过程中要树立“变化观念与平衡思想”。已知 2SO (g)+O(g)
2 2
2SO (g) ΔH=-196 kJ/mol,下列相关说法正确的是
3
A.恒温恒容密闭容器中充入2 mol SO 和1 mol O ,充分反应后,放出196 kJ的热量
2 2
B.密闭容器中该反应达到平衡后,缩小容器体积,V 减小,V 增大,平衡正向移动
逆 正
C.加入催化剂,可加快反应速率,同时提高SO 的平衡转化率
2
D.升高温度,V 增大的程度比V 增大的程度更显著
逆 正
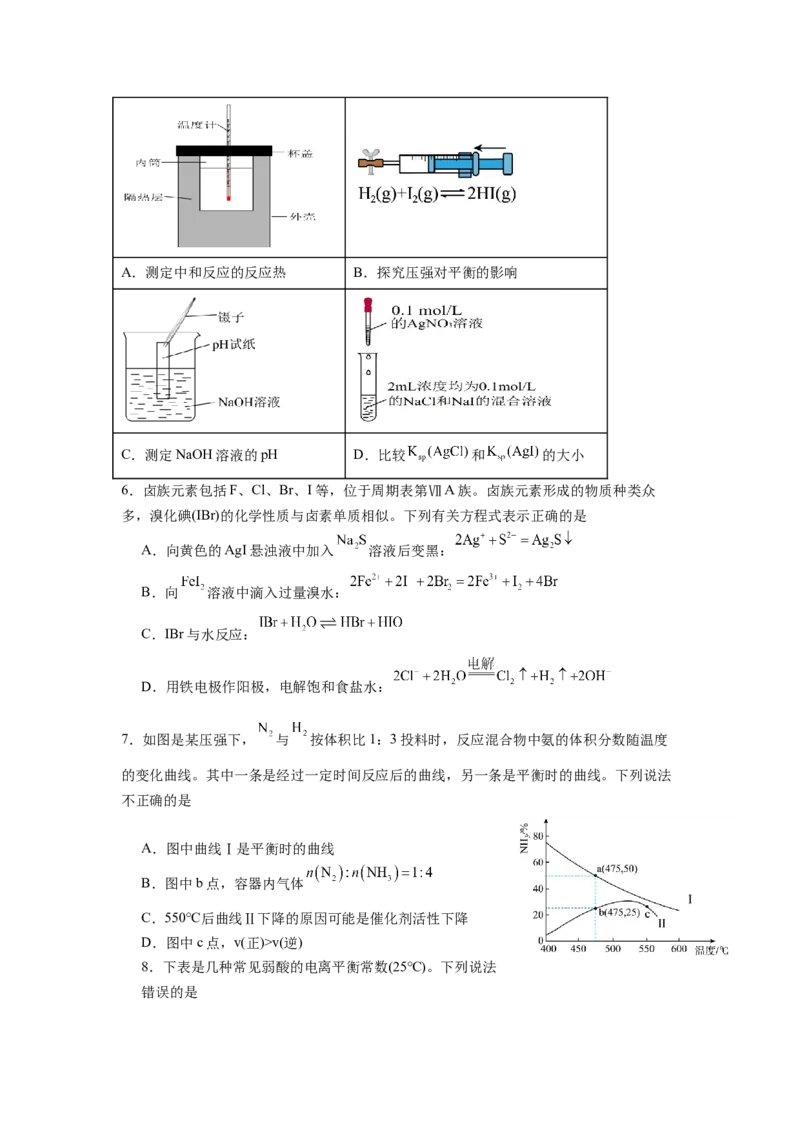
5.下列实验装置能达到实验目的的是A.测定中和反应的反应热 B.探究压强对平衡的影响
C.测定NaOH溶液的pH D.比较 和 的大小
6.卤族元素包括F、Cl、Br、I等,位于周期表第ⅦA族。卤族元素形成的物质种类众
多,溴化碘(IBr)的化学性质与卤素单质相似。下列有关方程式表示正确的是
A.向黄色的AgI悬浊液中加入 溶液后变黑:
B.向 溶液中滴入过量溴水:
C.IBr与水反应:
D.用铁电极作阳极,电解饱和食盐水:
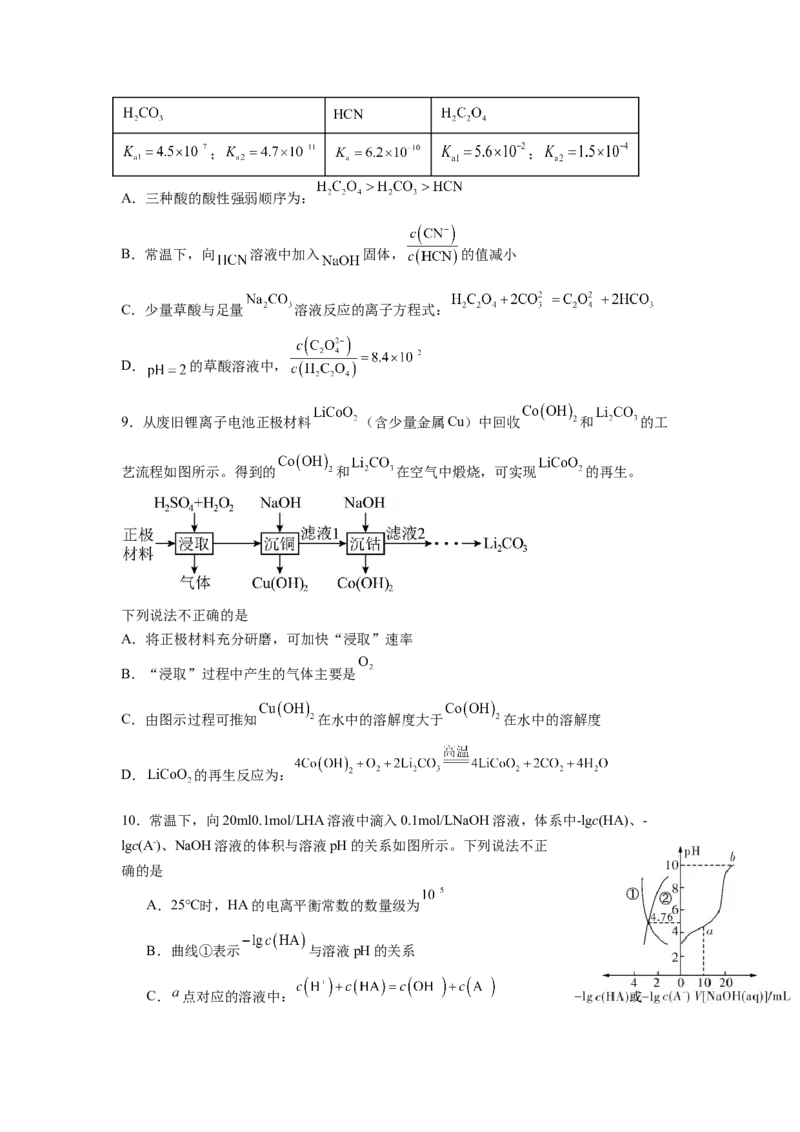
7.如图是某压强下, 与 按体积比1:3投料时,反应混合物中氨的体积分数随温度
的变化曲线。其中一条是经过一定时间反应后的曲线,另一条是平衡时的曲线。下列说法
不正确的是
A.图中曲线Ⅰ是平衡时的曲线
B.图中b点,容器内气体
C.550℃后曲线Ⅱ下降的原因可能是催化剂活性下降
D.图中c点,v(正)>v(逆)
8.下表是几种常见弱酸的电离平衡常数(25℃)。下列说法
错误的是HCN
; ;
A.三种酸的酸性强弱顺序为:
B.常温下,向 溶液中加入 固体, 的值减小
C.少量草酸与足量 溶液反应的离子方程式:
D. 的草酸溶液中,
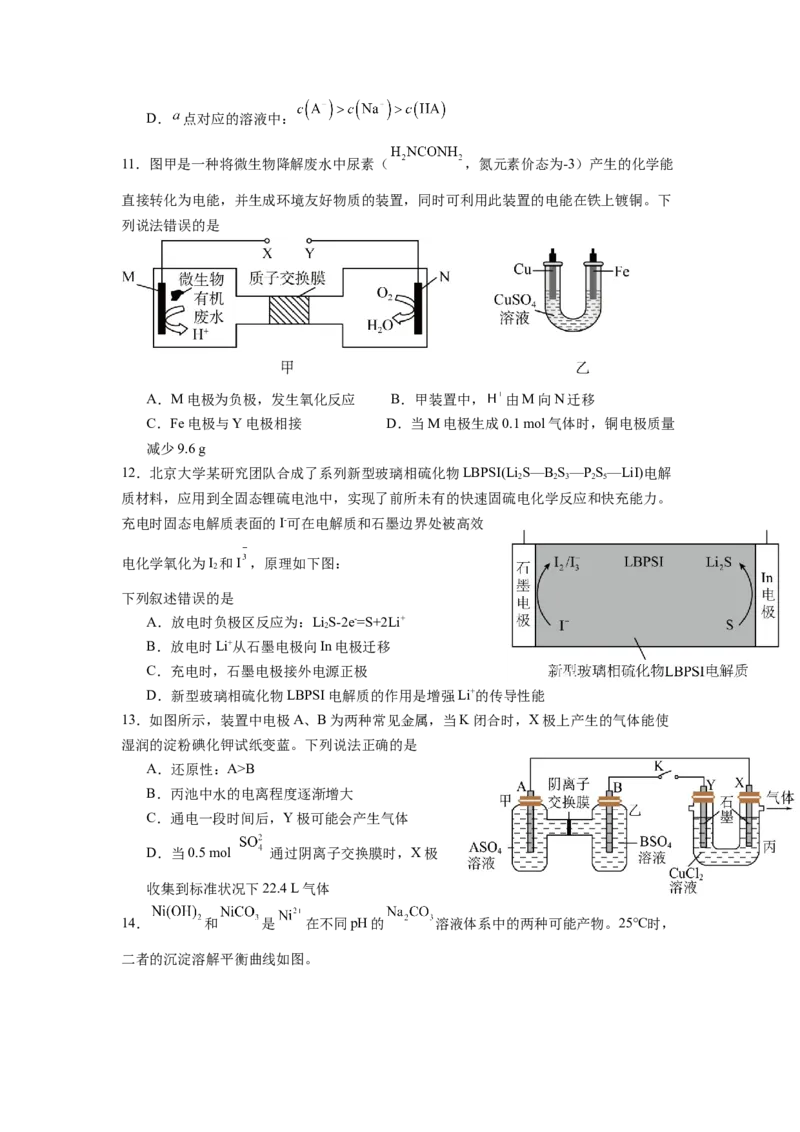
9.从废旧锂离子电池正极材料 (含少量金属Cu)中回收 和 的工
艺流程如图所示。得到的 和 在空气中煅烧,可实现 的再生。
下列说法不正确的是
A.将正极材料充分研磨,可加快“浸取”速率
B.“浸取”过程中产生的气体主要是
C.由图示过程可推知 在水中的溶解度大于 在水中的溶解度
D. 的再生反应为:
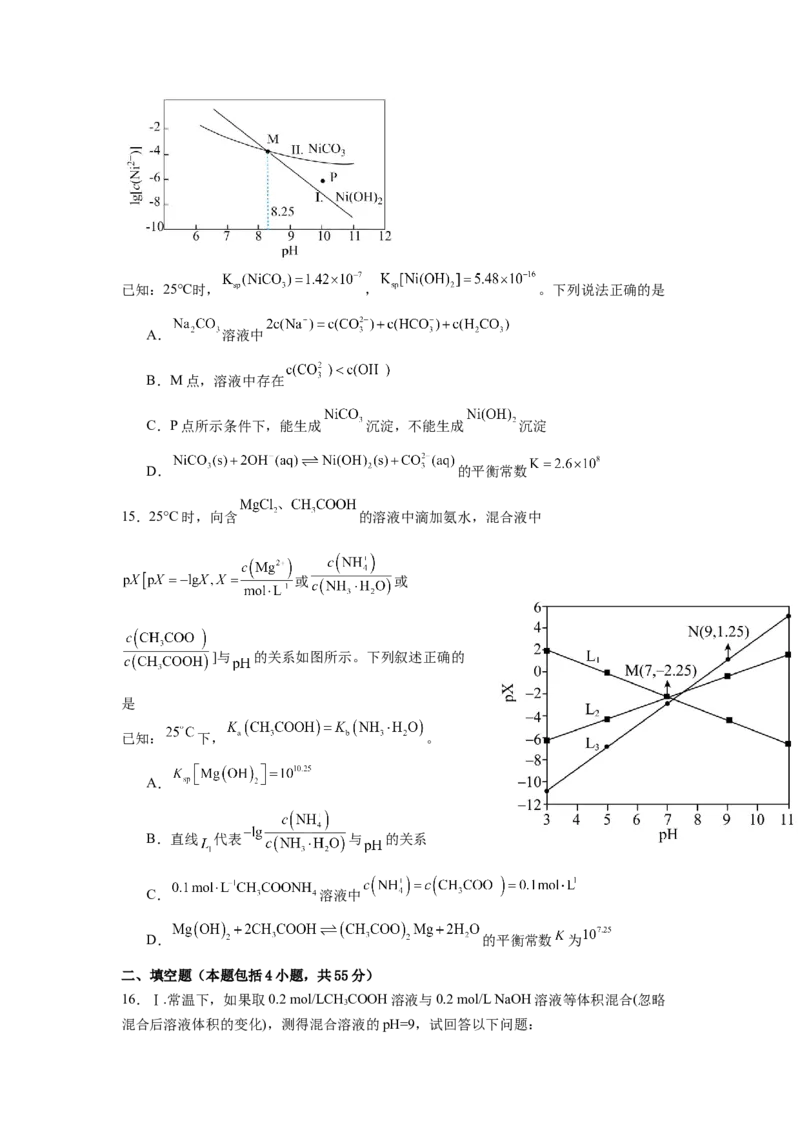
10.常温下,向20ml0.1mol/LHA溶液中滴入0.1mol/LNaOH溶液,体系中-lgc(HA)、-
lgc(A-)、NaOH溶液的体积与溶液pH的关系如图所示。下列说法不正
确的是
A.25℃时,HA的电离平衡常数的数量级为
B.曲线①表示 与溶液pH的关系
C. 点对应的溶液中:D. 点对应的溶液中:
11.图甲是一种将微生物降解废水中尿素( ,氮元素价态为-3)产生的化学能
直接转化为电能,并生成环境友好物质的装置,同时可利用此装置的电能在铁上镀铜。下
列说法错误的是
A.M电极为负极,发生氧化反应 B.甲装置中, 由M向N迁移
C.Fe电极与Y电极相接 D.当M电极生成0.1 mol气体时,铜电极质量
减少9.6 g
12.北京大学某研究团队合成了系列新型玻璃相硫化物LBPSI(Li S—B S—PS—LiI)电解
2 2 3 2 5
质材料,应用到全固态锂硫电池中,实现了前所未有的快速固硫电化学反应和快充能力。
充电时固态电解质表面的I-可在电解质和石墨边界处被高效
电化学氧化为I 和I ,原理如下图:
2
下列叙述错误的是
A.放电时负极区反应为:LiS-2e-=S+2Li+
2
B.放电时Li+从石墨电极向In电极迁移
C.充电时,石墨电极接外电源正极
D.新型玻璃相硫化物LBPSI电解质的作用是增强Li+的传导性能
13.如图所示,装置中电极A、B为两种常见金属,当K闭合时,X极上产生的气体能使
湿润的淀粉碘化钾试纸变蓝。下列说法正确的是
A.还原性:A>B
B.丙池中水的电离程度逐渐增大
C.通电一段时间后,Y极可能会产生气体
D.当0.5 mol 通过阴离子交换膜时,X极
收集到标准状况下22.4 L气体
14. 和 是 在不同pH的 溶液体系中的两种可能产物。25℃时,
二者的沉淀溶解平衡曲线如图。已知:25℃时, , 。下列说法正确的是
A. 溶液中
B.M点,溶液中存在
C.P点所示条件下,能生成 沉淀,不能生成 沉淀
D. 的平衡常数
15.25°C时,向含 的溶液中滴加氨水,混合液中
或 或
]与 的关系如图所示。下列叙述正确的
是
已知: 下, 。
A.
B.直线 代表 与 的关系
C. 溶液中
D. 的平衡常数 为
二、填空题(本题包括4小题,共55分)
16.Ⅰ.常温下,如果取0.2 mol/LCH COOH溶液与0.2 mol/L NaOH溶液等体积混合(忽略
3
混合后溶液体积的变化),测得混合溶液的pH=9,试回答以下问题:(1)混合溶液的pH=9的原因是:(用离子方程式表示) 。
(2)该混合溶液中由水电离出的c(H+)和pH=9的NaOH溶液中由水电离出c(H+)的比值为
。
(3)求该混合溶液中下列算式的计算结果:
c(Na+)-c(CHCOO-)= mol/L(代入数据,列出算式即可,)
3
c(OH-)-c(CHCOOH)= moL/L。
3
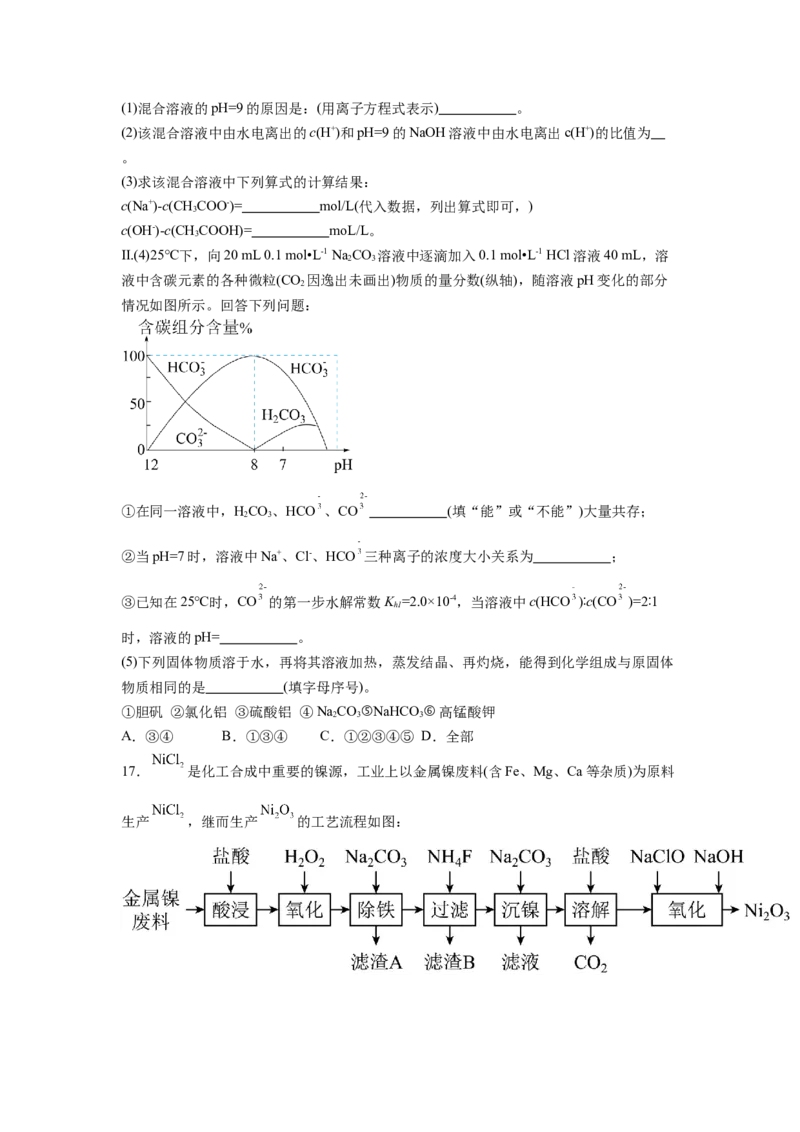
Ⅱ.(4)25℃下,向20 mL 0.1 mol•L-1 NaCO 溶液中逐滴加入0.1 mol•L-1 HCl溶液40 mL,溶
2 3
液中含碳元素的各种微粒(CO 因逸出未画出)物质的量分数(纵轴),随溶液pH变化的部分
2
情况如图所示。回答下列问题:
①在同一溶液中,HCO、HCO 、CO (填“能”或“不能”)大量共存;
2 3
②当pH=7时,溶液中Na+、Cl-、HCO 三种离子的浓度大小关系为 ;
③已知在25℃时,CO 的第一步水解常数K =2.0×10-4,当溶液中c(HCO )∶c(CO )=2∶1
h1
时,溶液的pH= 。
(5)下列固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体
物质相同的是 (填字母序号)。
①胆矾 ②氯化铝 ③硫酸铝 ④NaCO⑤NaHCO ⑥高锰酸钾
2 3 3
A.③④ B.①③④ C.①②③④⑤ D.全部
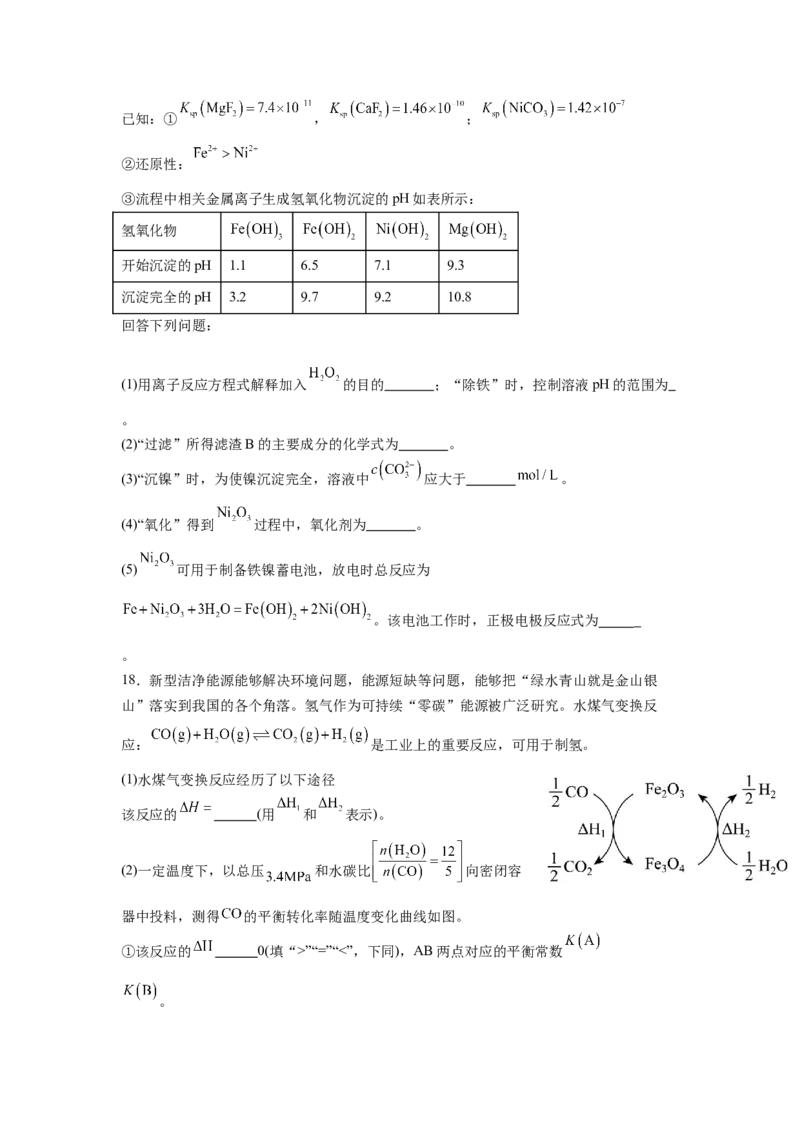
17. 是化工合成中重要的镍源,工业上以金属镍废料(含Fe、Mg、Ca等杂质)为原料
生产 ,继而生产 的工艺流程如图:已知:① , ;
②还原性:
③流程中相关金属离子生成氢氧化物沉淀的pH如表所示:
氢氧化物
开始沉淀的pH 1.1 6.5 7.1 9.3
沉淀完全的pH 3.2 9.7 9.2 10.8
回答下列问题:
(1)用离子反应方程式解释加入 的目的 ;“除铁”时,控制溶液pH的范围为
。
(2)“过滤”所得滤渣B的主要成分的化学式为 。
(3)“沉镍”时,为使镍沉淀完全,溶液中 应大于 。
(4)“氧化”得到 过程中,氧化剂为 。
(5) 可用于制备铁镍蓄电池,放电时总反应为
。该电池工作时,正极电极反应式为
。
18.新型洁净能源能够解决环境问题,能源短缺等问题,能够把“绿水青山就是金山银
山”落实到我国的各个角落。氢气作为可持续“零碳”能源被广泛研究。水煤气变换反
应: 是工业上的重要反应,可用于制氢。
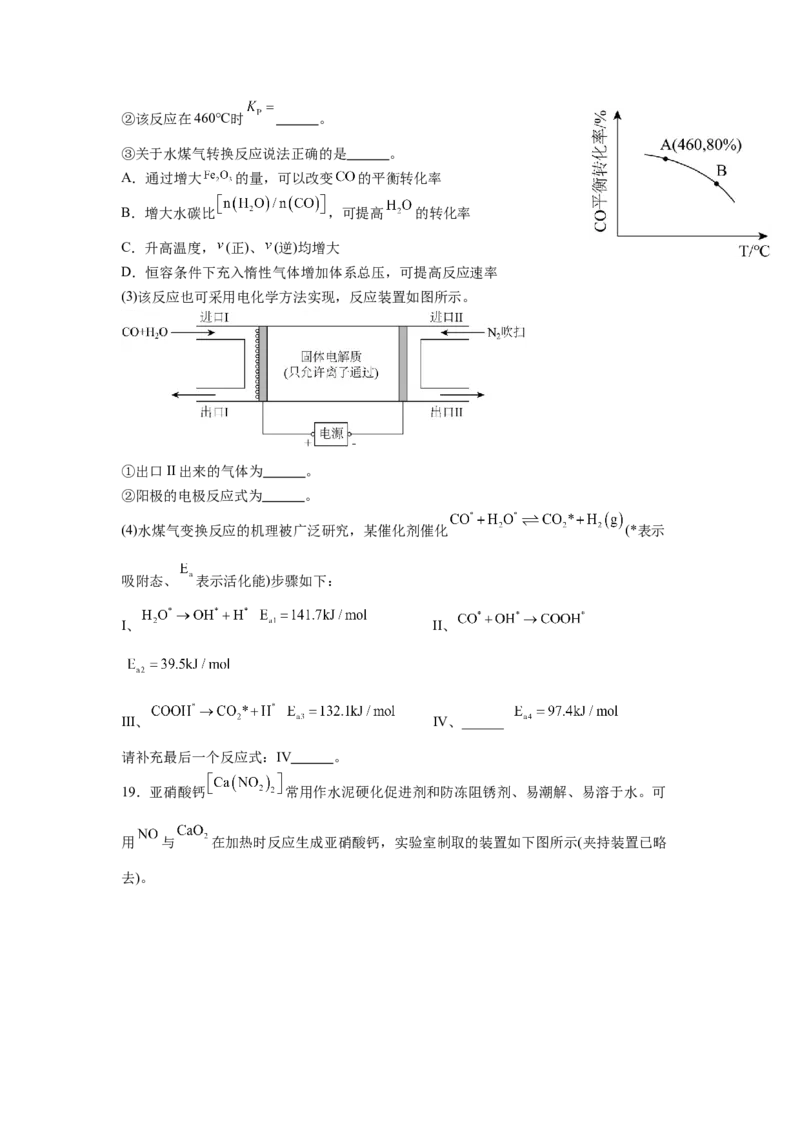
(1)水煤气变换反应经历了以下途径
该反应的 (用 和 表示)。
(2)一定温度下,以总压 和水碳比 向密闭容
器中投料,测得 的平衡转化率随温度变化曲线如图。
①该反应的 0(填“>”“=”“<”,下同),AB两点对应的平衡常数
。②该反应在460℃时 。
③关于水煤气转换反应说法正确的是 。
A.通过增大 的量,可以改变 的平衡转化率
B.增大水碳比 ,可提高 的转化率
C.升高温度, (正)、 (逆)均增大
D.恒容条件下充入惰性气体增加体系总压,可提高反应速率
(3)该反应也可采用电化学方法实现,反应装置如图所示。
①出口II出来的气体为 。
②阳极的电极反应式为 。
(4)水煤气变换反应的机理被广泛研究,某催化剂催化 (*表示
吸附态、 表示活化能)步骤如下:
I、 II、
III、 IV、______
请补充最后一个反应式:IV 。
19.亚硝酸钙 常用作水泥硬化促进剂和防冻阻锈剂、易潮解、易溶于水。可
用 与 在加热时反应生成亚硝酸钙,实验室制取的装置如下图所示(夹持装置已略
去)。(1)仪器a的名称是 ;装置B的作用是 。
(2)滴入稀硝酸之前需通入一段时间的 ,目的是 。
(3)滴入稀硝酸后,装置A中三颈烧瓶内的现象是 。(写至少两条现象)
(4)常温下,测得亚硝酸钙溶液的 ,则水电离出的 mol/L。
(5)装置E用来吸收未反应的 ,在该装置中 中的N元素被氧化成 价,则其反应的
离子方程式为 。
(6)测定所得亚硝酸钙产品中硝酸钙含量的步骤:
Ⅰ.称量ag产品溶于水,加入足量 固体充分搅拌后过滤;
Ⅱ.将滤液全部注入锥形瓶,加入足量饱和 溶液,煮沸3~4分钟,再冷却(目的是除去
)。
Ⅲ.再向锥形瓶中加入 溶液和适量硫酸,发生反应:
。
Ⅳ.加入4滴指示剂,用 标准液滴定过量的 至终点,消耗 溶液
的体积5.00mL(发生的反应为: )。
①步骤Ⅰ中加入足量 的目的是 。
②所得产品中 的质量分数为 %。(用含a、 、 的式子表示)《高二年级12月考试化学试题》参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 D C C D C D C C B C
题号 11 12 13 14 15
答案 C B C D D
1.D
【详解】A.加热促进碳酸根离子的水解,溶液碱性增强,热的溶液可以增强清洗油污的
效果,和盐类的水解有关,A不符合题意;
B.保存和配制 溶液时,加入少量 ,增大氢氧根离子浓度,可以抑制硫离子的水
解,B不符合题意;
C.氟离子水解生成的HF会和玻璃中成分反应,故 水溶液应存放在塑料瓶中,而不
能存放于玻璃瓶中,和盐类的水解有关,C不符合题意;
D.亚铁离子容易被氧化为铁离子,铁和铁离子生成亚铁离子,实验室保存 溶液时,
常在溶液中加入适量铁粉,是防止亚铁离子被氧化,与盐类的水解无关,D符合题意;
故选D。
2.C
【详解】A.由水电离出的 的溶液,该溶液可能显酸性或碱性,
在酸性中要反应不能共存 ,A不符合题意;
B.使甲基橙变红的溶液显酸性,酸性溶液中 与 不能共存
,B不符合题意;
C.澄清透明的溶液中,该组离子都不反应,能共存,C符合题意;
D.该组离子中 与 要反应不能共存 ,D不符合题意;
故答案为:C。
3.C
【详解】A.装置①中用惰性电极电解CuCl 溶液,在阳极上Cl-失去电子被氧化变为Cl,
2 2
阳极的电极反应式为:2Cl--2e-=Cl↑;在阴极上Cu2+得到电子被还原为单质Cu,阴极的电
2极反应式为:Cu2++2e-=Cu,故电解时在阴极上有红色物质析出,A错误;
B.在装置②电镀铜时,应该使镀层金属铜片与直流电源的正极相连,作阳极;镀件与直
流电源的负极连接作阴极,B错误;
C.在装置③的氢氧燃料电池中,通入燃料H 的电极a为负极,通入O 的电极b为正极,
2 2
若电解液为KOH溶液,溶液显碱性,则电极a的反应式:H-2e-+2OH-=2H O,C正确;
2 2
D.在装置④的金属铜的精炼中,粗铜作阳极,精铜作阴极。阳极上Cu及活动性比Cu强
金属如Zn、Fe等会失去电子变为金属阳离子进入电解质溶液;在阴极上只有Cu2+得到电子
被还原变为单质Cu。由于同一闭合回路中电子转移数目相等,因此电解一段时间后,溶液
中CuSO 的浓度会逐渐降低,D错误;
4
故选C。
4.D
【详解】A.图中缺少玻璃搅拌器,无法准确测定中和反应的反应热,A错误;
B.该可逆反应是气体分子数保持不变的反应,通过压缩针筒体积增大压强,虽然气体颜
色变深,但平衡不移动,该装置只是增大压强使气体浓度增大而已,不能达到探究目的,
B错误;
C.用pH试纸测定溶液的pH时,不能直接将pH试纸插入溶液中,C错误;
D.把AgNO 溶液滴加到NaCl和NaI的混合溶液中,先产生黄色的AgI沉淀,后产生白色
3
沉淀,说明AgI的溶解度比AgCl小,D正确;
故选D。
5.C
【详解】A.向黄色的AgI悬浊液中加入 溶液后变黑,反应的离子方程式为
,A错误;
B.碘化亚铁溶液与过量溴水反应生成溴化铁和碘,反应的离子方程式为
,B错误;
C.溴化碘(IBr)的化学性质与卤素相似,Br的化合价为 价,I的化合价为+1价,IBr与水
发生复分解反应生成HBr和HIO,化学方程式为 ,C正确;D.用铁电极作阳极电解饱和食盐水,Fe在阳极会失去电子生成 ,总反应方程式为
,D错误;
故选C。
6.D
【详解】A.热化学方程式2SO (g)+O(g) 2SO (g) ΔH=-196 kJ/mol表示每有2 mol SO 与
2 2 3 2
O 反应产生SO 气体,放出196 kJ的热量。在恒温恒容密闭容器中充入2 mol SO 和1 mol
2 3 2
O 时,由于该反应是可逆反应,反应物不能完全转化为生成物,故充分反应后,放出的热
2
量小于196 kJ,A错误;
B.密闭容器中该反应达到平衡后,缩小容器体积,导致体系的压强增大,反应速率都加
快,因此V 增大,V 也增大,由于正反应是气体体积减小的反应,增大压强后,导致正
逆 正
反应速率增大的程度大于逆反应速率,故化学平衡向正向移动,B错误;
C.加入催化剂,可加快反应速率。由于催化剂使正、逆反应速率增大的倍数相同,使用
催化剂,化学平衡不移动,因此不能提高SO 的平衡转化率,C错误;
2
D.升高温度,化学反应速率加快,V 、V 都增大。由于该反应的正反应是放热反应,
正 逆
温度改变对吸热反应影响更大,因此升高温度后,逆反应速率增大的倍数大于正反应速率
增大的倍数,即V 的程度比V 增大的程度更显著,所以化学平衡向吸热的逆反应方向移
逆 正
动,D正确;
故合理选项是D。
7.C
【分析】条件相同的情况下,平衡状态时氨气的体积分数应该是最大的,因此I表示平衡
时的曲线,II表示经过一定时间反应后的曲线。
【详解】A.根据分析可知,曲线I表示平衡时的曲线,A正确;
B.从图中可知,c点温度下,氨气的体积分数小于该温度下平衡状态时的体积分数,说明
此时反应还在正向进行,v(正)>v(逆),B正确;
C.图中b点氨气的体积分数为25%,不妨令开始时氮气和氢气的物质的量为1mol和
3mol,设反应消耗氮气xmol,则消耗氢气3xmol,生成氨气2xmol,平衡时气体总物质的
量为(4-2x)mol,氨气的体积分数为2x÷(4-2x)=0.25,解得x=0.4mol,此时容器中氮气和氨
气的物质的量之比为3:4,C错误;D.550℃以后曲线II下降,可能的原因高温导致催化剂活性降低,使得反应速率减小,氨
气的体积分数减小,D正确;
故答案选C。
8.B
【详解】A.电离平衡常数 越大,酸性越强,因此根据表中数据得到酸性强弱关系为
,A正确;
B.向HCN溶液中加入NaOH固体,会消耗HCN电离出的 ,导致溶液中 降低,
根据公式 ,温度不变 不变,但 减小,比值会增大,B错误;
C.由于酸性 ,足量 可与草酸的两个H+反应,生成 和 ,
离子方程式正确,C正确;
D.根据 的电离常数得到 ,当pH=2时,
, 代入数据得
,D正确;
故答案选B。
9.C
【分析】正极材料 (含少量金属Cu)中加入 、 , 被还原为 ,
同时生成 , 与 、 作用转化为 ,将反应后的溶液中加入NaOH溶液
沉铜, 转化为 沉淀,过滤后,往滤液中继续加入 溶液沉钴,此时转化为 沉淀;将滤液2经过一系列操作,最后制得 。
【详解】A.将正极材料充分研磨,增大反应物接触面积,可加快“浸取”速率,A正确;
B.“浸取”过程中在酸性条件下, 被 还原为 ,同时生成 ,B正确;
C.由图示过程可知,加入 溶液过程中,先生成 沉淀,后生成 沉
淀,则表明沉淀 时,所需 大,所以 在水中的溶解度小于 在
水中的溶解度,C错误;
D.根据题意, 和 在空气中煅烧,可实现 的再生,反应为:
,D正确。
故答案选C。
10.C
【分析】未加NaOH溶液时,0.1mol/LHA溶液的pH>2,则表明HA为弱酸,随着NaOH
溶液的不断加入。HA不断发生电离, 不断减小, 不断增大,溶液的pH不断
增大,则曲线①表示 ,曲线②)表示 。
【详解】A.25℃时, , ,HA的电离平衡常数为
,所以HA的电离平衡常数的数量级为 ,A正确;
B.由分析可知,曲线①表示 与溶液pH的关系,B正确;
C. 点对应的溶液中,加入NaOH的物质的量刚好为HA物质的量的一半,溶质为等物质
的量的NaA和HA的混合溶液,所以溶液中存在两个守恒:物料守恒,电荷守恒 ,从而得出:
,且此时溶液呈酸性, ,C不正确;
D. 点时溶质为等物质的量的NaA和HA的混合溶液,溶液呈酸性,说明HA的电离程度
大于NaA的水解程度,因此 ,D正确;
故选C。
11.C
【分析】由图可知,N电极的电极反应为 ,该极发生还原反应为正极。M
电极为负极,发生氧化反应,电极反应为 。根据
已知条件,装置乙可用于给铁镀铜,则Fe极的电极反应为 ,该极发生还原
反应为阴极。Cu极为阳极,电极反应为 。据此分析;
【详解】A.M电极为负极,发生氧化反应,A正确;
B.原电池电解质中的正离子由负极向正极迁移,B正确;
C.电解池的阴极与原电池的负极相连,在该题中即为Fe电极通过X与M极相连,C错误;
D.由M电极反应可知,该电极生成的气体是 和 的等物质的量混合物。因此,每生
成0.1 mol气体会转移0.3 mol电子。结合Cu电极反应可知,若转移0.3 mol电子会消耗
0.15 mol Cu,则电极质量减少量 ,D正确;
故答案选C。
12.B
【分析】充电时,固态电解质表面的I-可在电解质和石墨边界处被高效电化学氧化为I 和I
2
,石墨电极为阳极,In电极为阴极,放电时,In电极为负极,LiS发生氧化反应生成硫,
2
电极反应式为:LiS-2e-=S+2Li+,石墨电极为正极。
2【详解】A.据分析,放电时负极区反应为:LiS-2e-=S+2Li+,A不符合题意;
2
B.放电时阳离子向正极移动,则Li+从In电极向石墨电极迁移,B符合题意;
C.充电时,石墨电极为阳极、则接外电源正极,C不符合题意;
D.已知:新型玻璃相硫化物LBPSI(Li S—B S—PS—LiI)电解质材料,应用到全固态锂
2 2 3 2 5
硫电池中,实现了前所未有的快速固硫电化学反应和快充能力。则新型玻璃相硫化物
LBPSI电解质的作用是增强Li+的传导性能,D不符合题意;
故选B。
13.C
【分析】X极上产生能使湿润的淀粉碘化钾试纸变蓝的气体,则该气体为Cl,X极为阳极,
2
Y极为阴极,A极为正极,B极为负极。
【详解】A.由分析可知,A极为正极,B极为负极,故还原性:B>A,A错误;
B.Cu2+促进水的电离,丙池中消耗Cu2+,水的电离程度逐渐减小,B错误;
C.通电一段时间后,Cu2+可能被消耗完,则Y极上H+放电,产生H,C正确;
2
D.0.5 mol 通过阴离子交换膜时,电路中转移电子的物质的量为1 mol,X极生成0.5
mol Cl,标准状况下的体积为11.2 L,D错误;
2
故答案选C。
14.D
【详解】A. 溶液中 ,因此元素守恒为
,故A项错误;
B.M点 ,曲线上的点均为饱和溶液,因此
,
,因此 ,
故B项错误;C.P点位于 溶度积曲线之上、 溶度积曲线之下,纵坐标越往上,
越大,因此P点为 的过饱和状态,为 的不饱和溶液,故C项错误;
D. 的平衡常数
,故D项正确
综上所述,正确的是D项。
15.D
【分析】随着pH增大, 增大, 逐渐减小,则 逐渐增大;
,随着pH增大, 增大, 不变,则
减小, 逐渐增大; ,随着
pH增大, 减小, 不变, 增大, 减
小,则 代表 。 , 时,
,则 代表 , 代表 ,据
此分析;
【详解】A. 代表p(Mg2+),由N点坐标可知,当pH=9时即c(H+)=10-9mol/L,c(OH-)=10-5mol/L,此时c(Mg2+)=10-1.25mol/L, = =
,A错误;
B.由分析可知, 代表 ,即 与pH的关系,B错误;
C. 溶液中, 和CHCOO-相互促进水解,导致离子浓度减小,
3
又因 ,则 和CHCOO-水解程度相同,因此
3
,C错误;
D. 的平衡常数
= =
,结合M点坐标可知pH=7时, ,
,则 ,D正确;
故选D。
16. CHCOO-+H O CHCOOH+OH- 104:1 10-5-10-9 10-9 不能
3 2 3
⇌
c(Na+)>c(Cl-)>c(HCO ) 10 A
【详解】Ⅰ. (1)等体积等浓度混合,恰好生成CHCOONa,离子反应为CHCOOH+OH-
3 3
=CH COO-+H O,混合后pH=9,则CHCOO-离子水解显碱性,离子反应为CHCOO-
3 2 3 3
+H O CHCOOH+OH-,故答案为:CHCOO-+H O CHCOOH+OH-;
2 3 3 2 3
(2)混合⇌溶液中由水电离出的c(H+)为10-5mol/L,pH=⇌9的NaOH溶液中由水电离出c(H+)为10-9mol/L,则比值为10-5:10-9=104:1,故答案为:104:1;
(3)由电荷守恒可知c(Na+)-c(CHCOO-)=c(OH-)-c(H+)=10-5mol/L-10-9mol/L,物料守恒为
3
c(Na+)=c(CHCOO-)+c(CHCOOH),则c(OH-)-c(CHCOOH)=c(H+)=10-9mol/L,故答案为:
3 3 3
10-5-10-9;10-9;
Ⅱ.(4)①由图可知,在同一溶液中,三种HCO、HCO 、CO 不能大量共存,CO 减少时
2 3
HCO 的浓度逐渐增大,HCO 逐渐减少时HCO 的浓度增大;故答案为:不能;
2 3
②由图可知,当pH=7时,部分碳酸氢根离子转化为碳酸,溶液中含碳元素的主要微粒为
HCO 、HCO,此时溶液中的溶质为碳酸氢钠、碳酸、氯化钠,且氯化钠的物质的量大于
2 3
碳酸氢钠的物质的量,因为溶液呈中性,则c(H+)=c(OH-),所以溶液中各离子的浓度关系
为c(Na+)>c(Cl-)>c(HCO )>c(H+)=c(OH-);故答案为:c(Na+)>c(Cl-)>c(HCO );
③当溶液中c(HCO )∶c(CO )=2∶1时,根据K = =2.0×10-4可得c(OH
h1
-)=1.0×10-4mol·L-1,则c(H+)=1.0×10-10mol·L-1,所以溶液pH=10,故答案为:10;
(5)①胆矾溶于水后,将溶液蒸发结晶再灼烧得到硫酸铜而不是胆矾,所以得不到原物质,
故①错误;
②氯化铝溶于水后,将溶液蒸发结晶时促进氯化铝水解,氯化氢具有挥发性,所以蒸发结
晶得到的固体是氢氧化铝,再灼烧氢氧化铝得到氧化铝,所以得不到原物质,故②错误;
③硫酸铝溶于水后,蒸发过程中硫酸铝水解得到硫酸和氢氧化铝,但硫酸没有挥发性,所
以蒸发结晶得到的固体是硫酸铝,硫酸铝较稳定,在灼烧时不分解,所以最终得到的固体
是原物质,故③正确;
④纯碱溶于水后,蒸发结晶过程中得到的固体是碳酸钠,碳酸钠较稳定,加热时不分解,
所以最终得到原物质,故④正确;
⑤小苏打溶于水后,蒸发结晶过程中得到的固体是碳酸钠,所以得不到原物质,故⑤错误;
⑥高锰酸钾溶于水后,蒸发结晶,固体高锰酸钾不稳定,受热分解得到的固体是锰酸钾、
二氧化锰、氧气,所以最终得到的固体不是原物质,故⑥错误;
综上③④正确,答案选A。17.(1) 分液漏斗 吸收挥发的硝酸酸雾
(2)排尽装置内的空气,防止 与 反应生成 ,增加杂质含量
(3)铜片上有气泡、铜片逐渐溶解、溶液变蓝
(4)
(5)
(6) 除去
【分析】实验开始前先通氮气是为了排除装置内的空气,在装置A中由铜和稀硝酸反应制
取一氧化氮,产生的气体中混有少量的HNO,可用B装置进行除杂,则B装置中盛放的
3
试剂为蒸馏水,吸收挥发的硝酸酸雾,装置C为干燥装置,通过D中与过氧化钙反应生成
亚硝酸钙,装置E为尾气吸收装置,据此答题。
【详解】(1)根据实验装置图可知,仪器a为分液漏斗;由于硝酸具有挥发性,这样会干
扰实验结果,可以在B洗气瓶中盛放蒸馏水,除去硝酸蒸气;
(2)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N,排除装置中的空气,
2
防止生成的NO被空气中的O 氧化为NO ,发生反应2NO +CaO =Ca(NO),造成产品纯度
2 2 2 2 3 2
降低;
(3)滴入稀硝酸后,装置A中三颈烧瓶内发生反应:
,可观察到的现象是铜片上有气泡、铜片逐渐
溶解、溶液变蓝;
(4)亚硝酸钙溶液中氢离子和氢氧根离子均来自水的电离,亚硝酸根水解促进水的电离,
则 的亚硝酸钙溶液,水电离出的 mol/L。
(5)装置E中NO被酸性高锰酸钾氧化为硝酸根离子,结合电子得失守恒以及元素守恒得
反应的离子方程式: ;
(6)①步骤Ⅰ中加入足量 的目的是除去 ;② 溶液中硫酸亚铁铵物质的量为 ,过量的
的物质的量n(Fe2+) =6n( )= ,则与硝酸根反应的n(Fe2+)
过量 硝酸根
= ;则n( )= n(Fe2+) =
消耗 硝酸根消耗
,产品中 的质量分数为
。
18.(1)粉碎废料,搅拌等
(2)
(3) 、
(4)
(5)
(6) 22.4
【分析】金属镍废料(含Fe、Mg、Ca等杂质)盐酸酸浸后的酸性溶液中含有Ni2+、Cl-,另含
有Fe2+、Mg2+、Ca2+等;加入过氧化氢氧化亚铁离子为铁离子;加入碳酸钠溶液调节溶液的
pH,使铁离子全部沉淀,滤渣A为Fe(OH) ;过滤后的滤液中再加入氟化铵沉淀Ca2+、
3
Mg2+,则滤渣B为MgF 、CaF ;再次过滤后向滤液中加入碳酸钠沉淀镍离子得NiCO;将
2 2 3
NiCO 再溶于盐酸,得氯化镍溶液;向其中加入次氯酸钠和氢氧化钠溶液可得 ,据此
3
分析作答。
【详解】(1)为了提高镍元素的浸出率,在“酸浸”时还可采取的措施有粉碎废料,搅拌
等,故答案为:粉碎废料,搅拌等。
(2)过氧化氢氧化亚铁离子为铁离子,则离子方程式为 ;“除铁”三价铁离子要沉淀完全,而镍离子不能产生沉淀,所以溶液的pH值控制在
,故答案为: ; 。
(3)滤液中再加入氟化铵的目的是沉淀Ca2+、Mg2+,则滤渣B为 、 ,故答案为:
、 。
(4) ,镍离子完全沉淀时,溶液中 ,应保
持溶液中 > ,故答案为: 。
(5)“氧化”得到 过程中,Ni元素由+2价升高到+3价,则NiCO 为还原剂,
3
中Cl元素由+1价降低到-1价,则氧化剂为 ,故答案为: 。
(6) 可用于制备铁镍蓄电池,放电时总反应为
,该反应中Ni元素由+3价降到+2价,得到电子,
则 为原电池的正极,正极电极反应式为: ;
根据 ,可知消耗56gFe,转移电子2mol,电解饱
和食盐水阴极电极反应式为: ,理论转移电子2mol,产生氢气为
1mol,标准状况下气体体积为22.4L,故答案为: ;
22.4。
19.(1)
(2) < > 2 C(3)
(4)
【详解】(1)由图,反应1: ,
反应2: ,由盖斯定律得:目标反应=
,即 ,故答案为: ;
(2)①由图像可知,温度升高,CO的平衡转化率降低,说明升高温度平衡逆向移动,根
据勒夏特列原理,逆反应吸热,则正反应放热,因此 ;平衡常数只与温度有关,该
反应正反应放热,A到B,温度升高,平衡逆向移动,平衡常数减小,因此 > ,
故答案为:<;>;
②由图可知,460℃时CO转化率为80%,以水碳比 进行反应,假设投入的
、 ,可列三段式:
,则各物质的分压分别为
, ,
, ,压强平衡常数
,故答案为:2;③A. 是固体,改变 的量,不能改变 的平衡转化率,A错误;
B.增大水碳比 ,相当于增加 的量,可以提高CO的转化率,但
自身的转化率降低,B错误;
C.升高温度,增大活化分子百分比, (正)、 (逆)均增大,C正确;
D.恒容条件下充入惰性气体增加体系总压,参与反应的气体浓度未变,反应速率也不变,
D错误;
故答案选C。
(3)分析:由图,右侧接电源负极,则右侧电极为阴极,得电子,发生还原反应;左侧通
入CO和水,接电源正极,失电子,发生氧化反应;结合总反应:
中物质变化可得,阳极为CO失电子生成 ,电极反
应式为 ;因固体电解质只允许离子通过,因此阴极电极反应为
。
①由分析可知,出口II出来的气体为 ,故答案为: ;
②由分析可知,阳极的电极反应式为 ,故答案为:
;
(4)根据反应I、II、III以及总反应 ,产物中有 ,根据原
子守恒及盖斯定律可得反应IV为 ,故答案为: 。