文档内容
辽宁省辽西重点高中2025-2026学年高二上学期11月期中化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
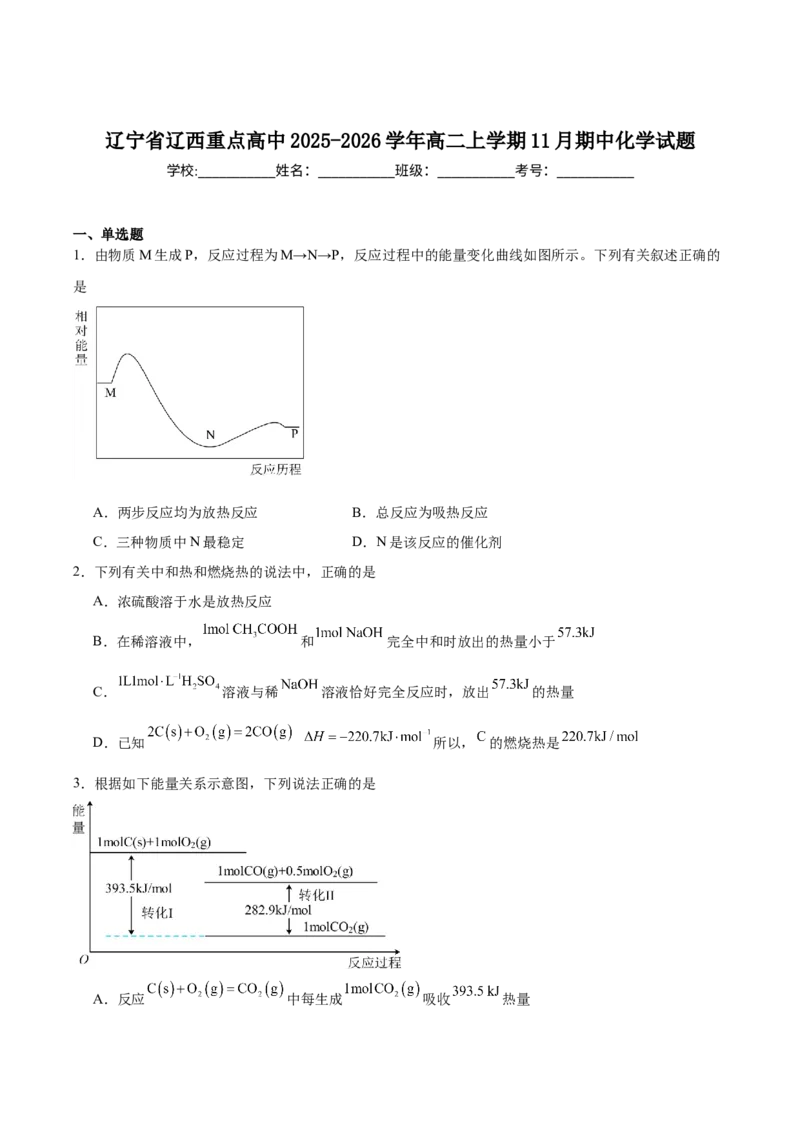
1.由物质M生成P,反应过程为M→N→P,反应过程中的能量变化曲线如图所示。下列有关叙述正确的
是
A.两步反应均为放热反应 B.总反应为吸热反应
C.三种物质中N最稳定 D.N是该反应的催化剂
2.下列有关中和热和燃烧热的说法中,正确的是
A.浓硫酸溶于水是放热反应
B.在稀溶液中, 和 完全中和时放出的热量小于
C. 溶液与稀 溶液恰好完全反应时,放出 的热量
D.已知 所以, 的燃烧热是
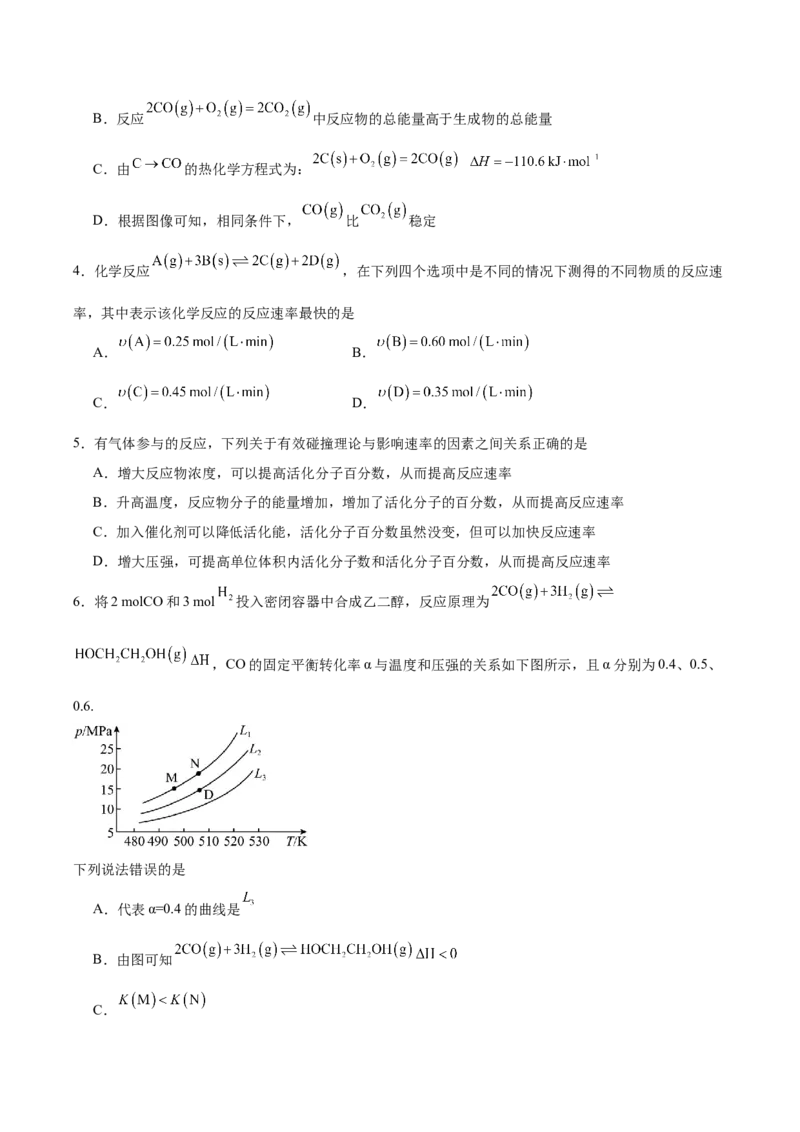
3.根据如下能量关系示意图,下列说法正确的是
A.反应 中每生成 吸收 热量B.反应 中反应物的总能量高于生成物的总能量
C.由 的热化学方程式为:
D.根据图像可知,相同条件下, 比 稳定
4.化学反应 ,在下列四个选项中是不同的情况下测得的不同物质的反应速
率,其中表示该化学反应的反应速率最快的是
A. B.
C. D.
5.有气体参与的反应,下列关于有效碰撞理论与影响速率的因素之间关系正确的是
A.增大反应物浓度,可以提高活化分子百分数,从而提高反应速率
B.升高温度,反应物分子的能量增加,增加了活化分子的百分数,从而提高反应速率
C.加入催化剂可以降低活化能,活化分子百分数虽然没变,但可以加快反应速率
D.增大压强,可提高单位体积内活化分子数和活化分子百分数,从而提高反应速率
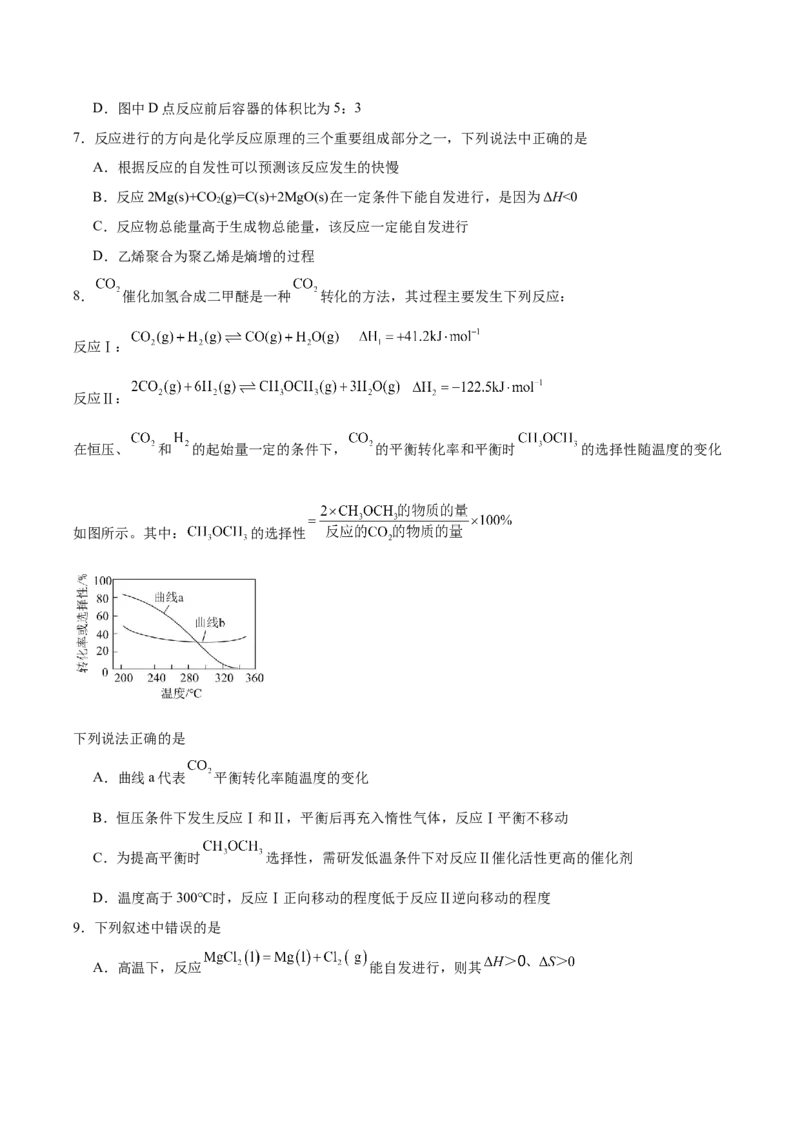
6.将2 molCO和3 mol 投入密闭容器中合成乙二醇,反应原理为
,CO的固定平衡转化率α与温度和压强的关系如下图所示,且α分别为0.4、0.5、
0.6.
下列说法错误的是
A.代表α=0.4的曲线是
B.由图可知
C.D.图中D点反应前后容器的体积比为5:3
7.反应进行的方向是化学反应原理的三个重要组成部分之一,下列说法中正确的是
A.根据反应的自发性可以预测该反应发生的快慢
B.反应2Mg(s)+CO (g)=C(s)+2MgO(s)在一定条件下能自发进行,是因为ΔH<0
2
C.反应物总能量高于生成物总能量,该反应一定能自发进行
D.乙烯聚合为聚乙烯是熵增的过程
8. 催化加氢合成二甲醚是一种 转化的方法,其过程主要发生下列反应:
反应Ⅰ:
反应Ⅱ:
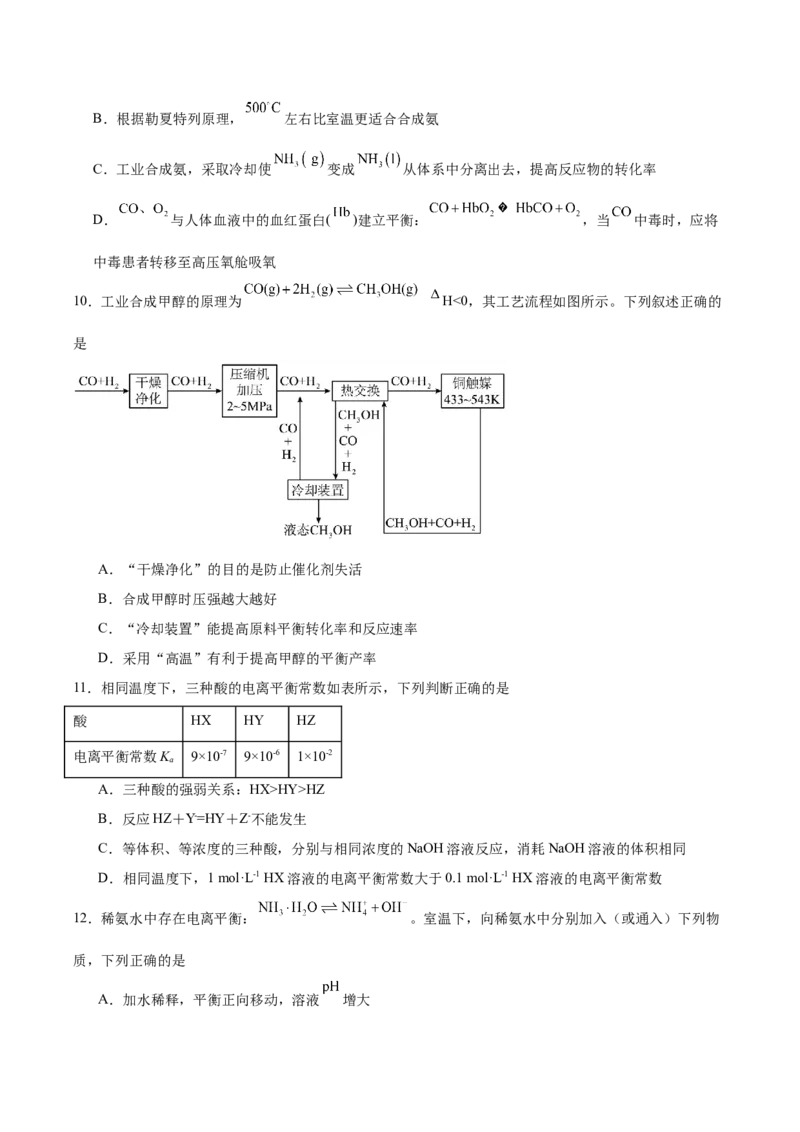
在恒压、 和 的起始量一定的条件下, 的平衡转化率和平衡时 的选择性随温度的变化
如图所示。其中: 的选择性
下列说法正确的是
A.曲线a代表 平衡转化率随温度的变化
B.恒压条件下发生反应Ⅰ和Ⅱ,平衡后再充入惰性气体,反应Ⅰ平衡不移动
C.为提高平衡时 选择性,需研发低温条件下对反应Ⅱ催化活性更高的催化剂
D.温度高于300℃时,反应Ⅰ正向移动的程度低于反应Ⅱ逆向移动的程度
9.下列叙述中错误的是
A.高温下,反应 能自发进行,则其B.根据勒夏特列原理, 左右比室温更适合合成氨
C.工业合成氨,采取冷却使 变成 从体系中分离出去,提高反应物的转化率
D. 与人体血液中的血红蛋白( )建立平衡: ,当 中毒时,应将
中毒患者转移至高压氧舱吸氧
10.工业合成甲醇的原理为 H<0,其工艺流程如图所示。下列叙述正确的
是
A.“干燥净化”的目的是防止催化剂失活
B.合成甲醇时压强越大越好
C.“冷却装置”能提高原料平衡转化率和反应速率
D.采用“高温”有利于提高甲醇的平衡产率
11.相同温度下,三种酸的电离平衡常数如表所示,下列判断正确的是
酸 HX HY HZ
电离平衡常数K 9×10-7 9×10-6 1×10-2
a
A.三种酸的强弱关系:HX>HY>HZ
B.反应HZ+Y-=HY+Z-不能发生
C.等体积、等浓度的三种酸,分别与相同浓度的NaOH溶液反应,消耗NaOH溶液的体积相同
D.相同温度下,1 mol·L-1 HX溶液的电离平衡常数大于0.1 mol·L-1 HX溶液的电离平衡常数
12.稀氨水中存在电离平衡: 。室温下,向稀氨水中分别加入(或通入)下列物
质,下列正确的是
A.加水稀释,平衡正向移动,溶液 增大B.通入 ,平衡正向移动, 的电离程度增大,恢复至室温电离平衡常数不变
C.通入 ,平衡正向移动,溶液中 和 均增大
D.加入 固体,平衡逆向移动,恢复至室温, 减小
13.我国科学家在一颗距离地球100光年的行星上发现了不可思议的“水世界”,引起了全球科学界的轰
动。下列有关说法正确的是
A.温度升高,水的电离平衡正向移动,c(H+)增大,酸性增强
B.SO 溶于水后导电,所以 是电解质
3
C.室温下,pH=4的盐酸溶液中,
D.向水中加入NaHSO 固体后(溶液温度不变),水的电离程度减小
4
14.常温时,向 溶液中滴加 溶液,滴定曲线如下图所示。下列说
法错误的是
A.该滴定过程第一滴定终点应该选择甲基橙溶液作指示剂
B.反应 的平衡常数
C.W点到X点发生的主要反应的离子方程式为:
D.Y点对应的溶液中
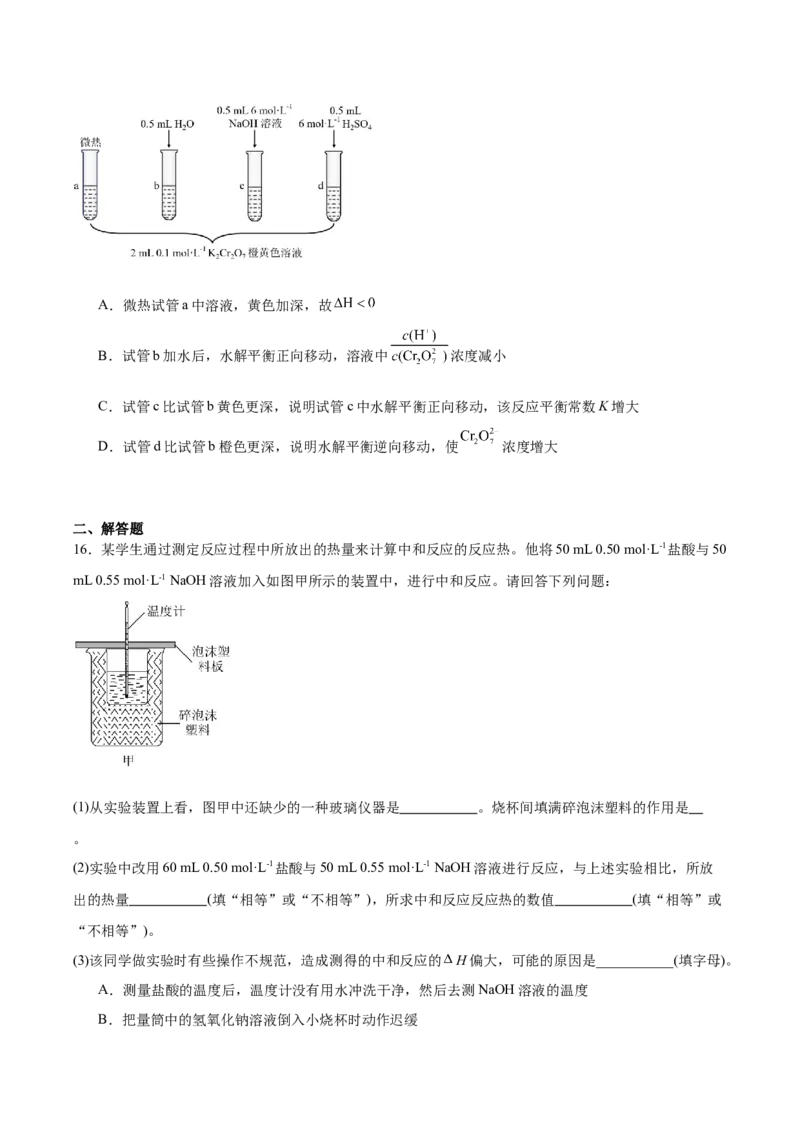
15.为探究温度、浓度对化学平衡的影响,利用 的水解反应 取四支
试管,按下图进行实验,下列说法正确的是A.微热试管a中溶液,黄色加深,故
B.试管b加水后,水解平衡正向移动,溶液中 浓度减小
C.试管c比试管b黄色更深,说明试管c中水解平衡正向移动,该反应平衡常数K增大
D.试管d比试管b橙色更深,说明水解平衡逆向移动,使 浓度增大
二、解答题
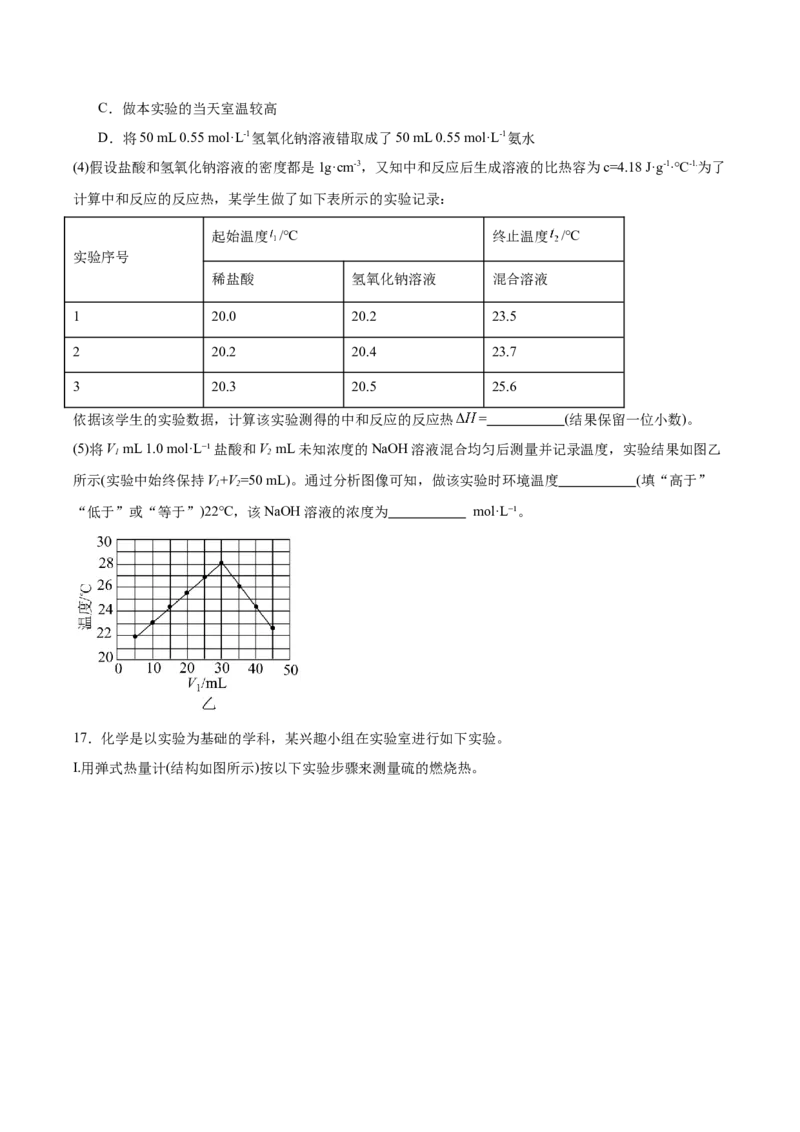
16.某学生通过测定反应过程中所放出的热量来计算中和反应的反应热。他将50 mL 0.50 mol·L-1盐酸与50
mL 0.55 mol·L-1 NaOH溶液加入如图甲所示的装置中,进行中和反应。请回答下列问题:
(1)从实验装置上看,图甲中还缺少的一种玻璃仪器是 。烧杯间填满碎泡沫塑料的作用是
。
(2)实验中改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放
出的热量 (填“相等”或“不相等”),所求中和反应反应热的数值 (填“相等”或
“不相等”)。
(3)该同学做实验时有些操作不规范,造成测得的中和反应的 H偏大,可能的原因是___________(填字母)。
A.测量盐酸的温度后,温度计没有用水冲洗干净,然后去测NaOH溶液的温度
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓C.做本实验的当天室温较高
D.将50 mL 0.55 mol·L-1氢氧化钠溶液错取成了50 mL 0.55 mol·L-1氨水
(4)假设盐酸和氢氧化钠溶液的密度都是1g·cm-3,又知中和反应后生成溶液的比热容为c=4.18 J·g-1·℃-1.为了
计算中和反应的反应热,某学生做了如下表所示的实验记录:
起始温度 /℃ 终止温度 /℃
实验序号
稀盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.2 23.5
2 20.2 20.4 23.7
3 20.3 20.5 25.6
依据该学生的实验数据,计算该实验测得的中和反应的反应热 = (结果保留一位小数)。
(5)将V mL 1.0 mol·L⁻¹盐酸和V mL未知浓度的NaOH溶液混合均匀后测量并记录温度,实验结果如图乙
1 2
所示(实验中始终保持V+V=50 mL)。通过分析图像可知,做该实验时环境温度 (填“高于”
1 2
“低于”或“等于”)22℃,该NaOH溶液的浓度为 mol·L⁻¹。
17.化学是以实验为基础的学科,某兴趣小组在实验室进行如下实验。
Ⅰ.用弹式热量计(结构如图所示)按以下实验步骤来测量硫的燃烧热。称量 纯水,倒入内筒中;称量 硫固体装入氧弹内,用氧气排净空气后再注满高纯氧气;打开搅拌
器开关,读取纯水温度,当温度不再改变时,记为初始温度;当纯水温度保持不变时,打开引燃电极,读
取并记录内筒最高水温;重复实验 次,测得内筒温度改变的平均值为 。通过已知燃烧热的物质利
用此装置在相同条件下测定,内筒每克水升高 时,需要反应放热 。
请回答下列问题:
(1)搅拌器和氧弹适宜的材质分别为 、 (填“不锈钢”或“玻璃纤维”);氧弹内注
满过量高纯氧气的目的是 。
(2)用相关字母表示硫的燃烧热 为 ;若测得的 比实际数据偏高,则可能原因是
(填字母)。
a.硫未充分燃烧 b.称取硫时质量偏高 c.测得纯水的初始温度偏高
Ⅱ.利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素,设计如下系列实验:
稀硫酸 浓度
实验 反应温
序号 度/℃
1 20 0.50 10.0 0.10 10.0 0
2 20 0.50 10.0 0.10 5.0
3 40 0.50 0.10 10.0
(3)写出硫代硫酸钠与稀硫酸反应的离子方程式: 。
(4)该实验1和2可探究 对反应速率的影响,因此 mL。实验3比实验1反应速率快,因为升高温度增加了 (填字母)。
a.单位体积离子总数 b.单位体积活化离子数 c.单位体积活化离子百分数
18.某学习小组欲利用 平衡体系探究影响平衡的因素,将
溶液和 溶液混合,得血红色溶液X,进行下列实验:
实验I.改变 等离子浓度对平衡的影响
(1)取 溶液X,加入5滴 溶液,观察到溶液红色变浅,产生该现象的原因可能是:
① 对平衡产生了影响;
②不直接参与平衡体系的 或 对平衡产生了影响。
实验II.为了探究对 平衡体系的影响某学习小组同学进行如下探究:
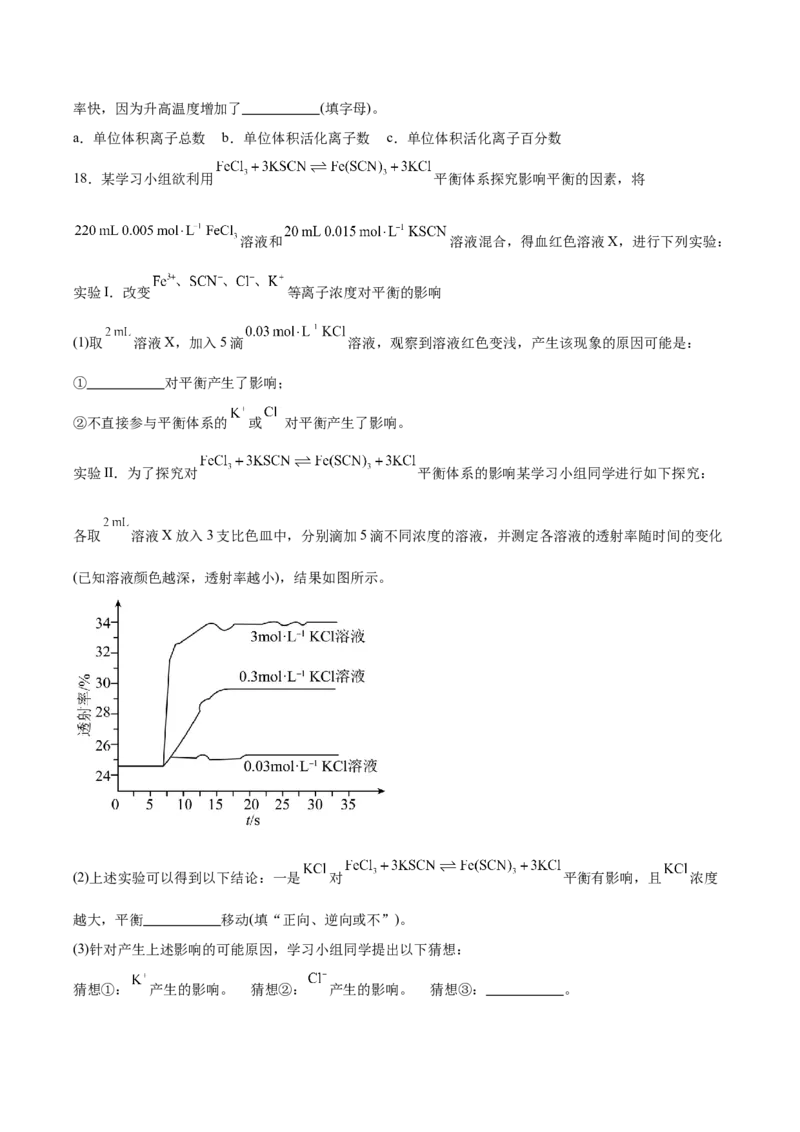
各取 溶液X放入3支比色皿中,分别滴加5滴不同浓度的溶液,并测定各溶液的透射率随时间的变化
(已知溶液颜色越深,透射率越小),结果如图所示。
(2)上述实验可以得到以下结论:一是 对 平衡有影响,且 浓度
越大,平衡 移动(填“正向、逆向或不”)。
(3)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①: 产生的影响。 猜想②: 产生的影响。 猜想③: 。实验III.探究盐对 和 平衡体系产生的影响资料信息:
a.溶液中的 离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐
效应。
b.在 溶液中存在反应 。
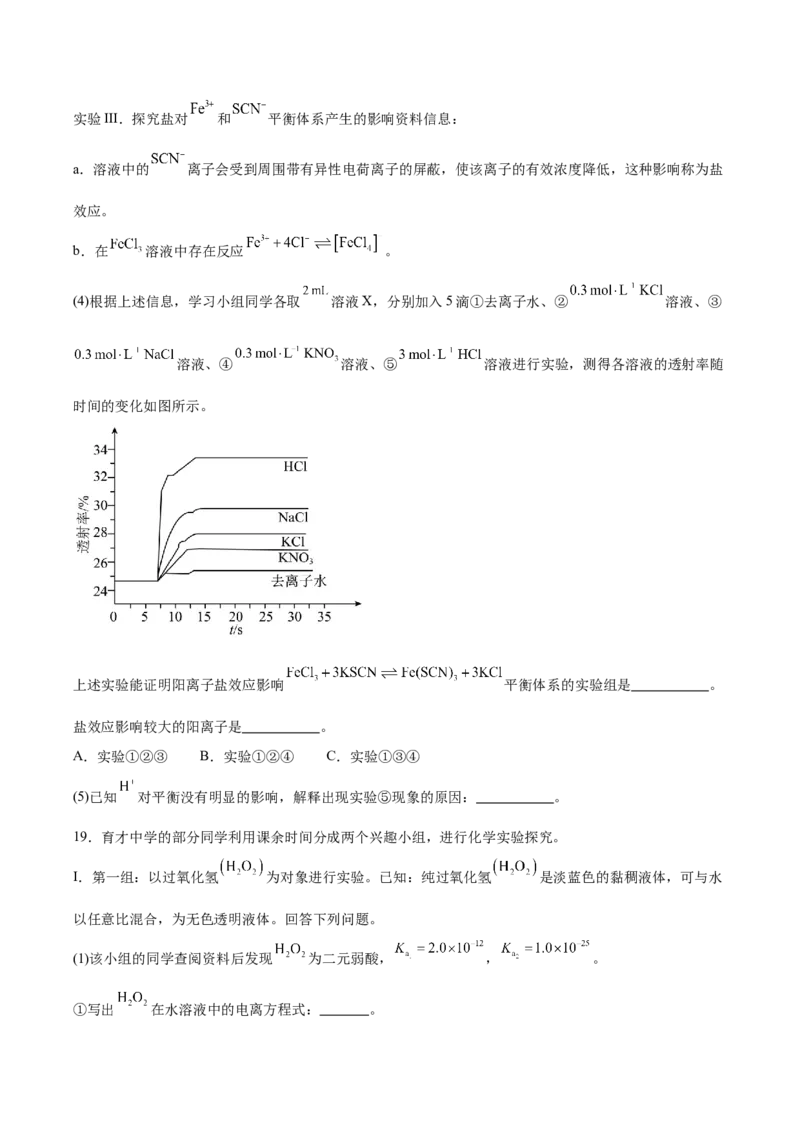
(4)根据上述信息,学习小组同学各取 溶液X,分别加入5滴①去离子水、② 溶液、③
溶液、④ 溶液、⑤ 溶液进行实验,测得各溶液的透射率随
时间的变化如图所示。
上述实验能证明阳离子盐效应影响 平衡体系的实验组是 。
盐效应影响较大的阳离子是 。
A.实验①②③ B.实验①②④ C.实验①③④
(5)已知 对平衡没有明显的影响,解释出现实验⑤现象的原因: 。
19.育才中学的部分同学利用课余时间分成两个兴趣小组,进行化学实验探究。
I.第一组:以过氧化氢 为对象进行实验。已知:纯过氧化氢 是淡蓝色的黏稠液体,可与水
以任意比混合,为无色透明液体。回答下列问题。
(1)该小组的同学查阅资料后发现 为二元弱酸, , 。
①写出 在水溶液中的电离方程式: 。②如果常温下 溶液 , 的酸式酸根离子与 的浓度比为 。
(2)测定某瓶过氧化氢溶液中 的含量。
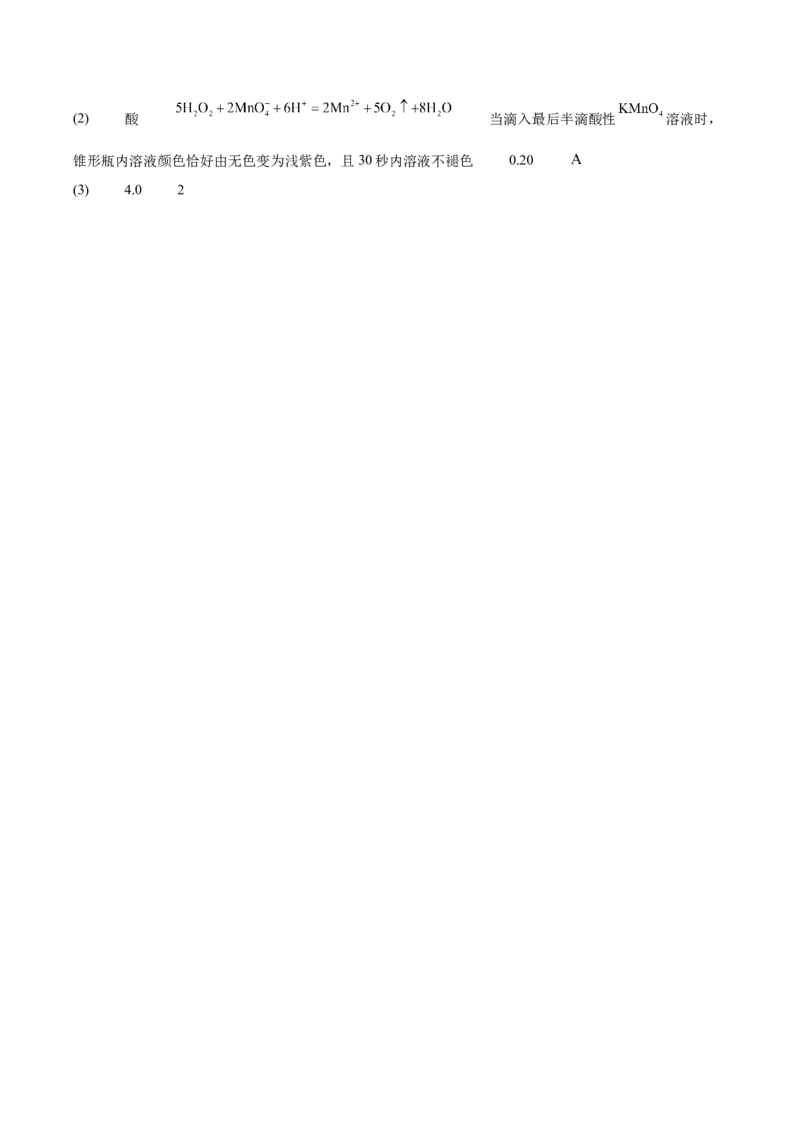
①取 试样置于锥形瓶中,用装有 的酸性 标准溶液的棕色 式滴定管滴
定。反应的离子方程式为 。
②滴定达到终点的现象为 ,记录数据。重复滴定两次,每次消耗的酸性 标准溶液体积如下
表所示:
实验次数 第一次 第二次 第三次
体积 16.10 16.05 16.15
则试样中过氧化氢的浓度为 。(保留两位有效数字,下同)
③若实验测得的浓度比该瓶试剂标签上的数据低,下列哪些是造成偏低的可能原因: 。
A.滴定终点读数时俯视读数
B.滴定管水洗后直接倒入 溶液进行滴定
C.锥形瓶水洗后未干燥
D.滴定时有几滴 溶液溅落在锥形瓶外
Ⅱ.第二组:已知 溶液和 溶液可发生反应: 。为探究
反应速率与 的关系,该组同学设计下表进行四组实验,排水法收集 用秒表测量收集
所需的时间。实验数据如下表所示:
/mL
实验编号 /s
溶液 溶液 醋酸 水
1 4.0 4.0 8.0 334
2 4.0 4.0 6.0 150
3 8.0 4.0 4.0 4.0 834 12.0 4.0 4.0 0.0 38
(3)① 。
②该反应的速率方程为 , 为反应速率常数。利用实验数据计算得
(填整数)。
《辽宁省辽西重点高中2025-2026学年高二上学期11月期中化学试题》参考答案
1.C
2.B
3.B
4.A
5.B
6.C7.B
8.C
9.B
10.A
11.C
12.D
13.D
14.B
15.D
16.(1) 环形玻璃搅拌棒 减少反应体系和环境之间的热交换
(2) 不相等 相等
(3)ABD
(4)-56.8 kJ/mol
(5) 低于 1.50
17.(1) 玻璃纤维 不锈钢 确保可燃物完全燃烧
(2) ac
(3)
(4) 硫代硫酸钠溶液的浓度 5.0 bc
18.(1)溶液被稀释
(2)逆向
(3) 和 共同产生的影响
(4) A
(5)实验⑤中增大 浓度, 平衡正向移动, 浓度降低,
平衡逆向移动,溶液透射率增大明显
19.(1) 、(2) 酸 当滴入最后半滴酸性 溶液时,
锥形瓶内溶液颜色恰好由无色变为浅紫色,且30秒内溶液不褪色 0.20
(3) 4.0 2