文档内容
2025-2026 学年上学期高二期中考试
化学
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:人教版必修第一册、必修第二册、选择性必修1第一章至第三章第
二节。
5.可能用到的相对原子质量:H 1 C 12 N 14 O 16
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学与生产、生活密切相关。下列物质的主要成分属于金属的是
A.《论语》书本 B.玉手镯
C.一次性塑料碗 D.铜鼎
A. A B. B C. C D. D
【答案】D
第1页/共17页
学科网(北京)股份有限公司【解析】
【详解】A.书本的主要成分是纤维素,不属于金属,A不符合题意;
B.玉手镯的主要成分是硅酸盐,不属于金属,B不符合题意;
C.一次性塑料碗主要成分是合成有机高分子材料,不属于金属,C不符合题意;
D.铜鼎是铜合金,属于金属,D符合题意;
故选D。
2. 下列变化中没有发生熵增的是
A. 气态水变成冰 B. 煅烧石灰石
C. 蔗糖溶解在水中 D. 氯化铵固体受热分解成氯化氢和氨气
【答案】A
【解析】
【详解】A.气态水变成冰是从较无序的气态变为较有序的固态,混乱度降低,熵减小,属于熵减过程,
A正确;
B.煅烧石灰石生成了 气体,气体熵值显著高于固体,系统总熵增加,B不符合题意;
C.蔗糖溶解后分子分散到水中,混乱度增大,熵增,C不符合题意;
D.氯化铵分解生成氨气和HCl气体,气体熵值远高于固体,熵增,D不符合题意;
故选A。
3. 催化加氢可制取乙烯: 。反应过程中, (g)与
(g)的反应速率之比为
A. 1:3 B. 2:1 C. 3:2 D. 1:4
【答案】C
【解析】
【详解】化学反应速率通常用单位时间内反应物浓度的减少量或生成物浓度的增加量来表示,则各物质的
反应速率之比等于其化学计量数之比。反应方程式中, (g)与 (g)化学计量数分别为6、4,则H 与
2
HO的速率之比为6:4,化简为3:2,故选C。
2
4. 下列物质属于非电解质的是
A. Cu B. C. KOH D.
【答案】D
第2页/共17页
学科网(北京)股份有限公司【解析】
【详解】A.非电解质是指在水溶液里和熔融状态下都不能自身电离出阴阳离子而导电的化合物,Cu是金
属单质,不是化合物,不属于非电解质,A不符合题意;
B.Al O 在熔融状态下能自身电离出离子,属于电解质,B不符合题意;
2 3
C.KOH在水溶液和熔融状态下均可电离出阴阳离子,属于电解质,C不符合题意;
D.C HOH(乙醇)在水溶液和熔融状态下均不能自身电离,属于非电解质,D符合题意;
2 5
故选D。
的
5. 盐酸和醋酸是生活中经常用到 酸。下列说法错误的是
A. 盐酸和醋酸溶液均不属于电解质
B. 适当升高温度有利于 增大
C. HCl在水溶液中的电离方程式为:
D. 浓度均为0.1 的盐酸和醋酸溶液中,所含的 均为0.1
【答案】D
【解析】
【详解】A.盐酸和醋酸溶液均为混合物,而电解质必须是化合物,A正确;
B.醋酸的电离是吸热过程,升高温度促进电离,导致其电离平衡常数增大,B正确;
C.HCl在水中完全电离,电离方程式通常写作: ,选项中的电离方程式表示HCl分子与
水分子结合而得到水合氢离子和氯离子,也是一种正确的表达方式,C正确;
D.盐酸为强酸,HCl在水中完全电离,0.1 mol/L盐酸中 为0.1 mol/L,而醋酸为弱酸,部分电离,
醋酸溶液中的 小于0.1 mol/L,D错误;
故选D。
6. 下列说法正确的是
A. 所有放热的自发过程均为熵减过程
B. 常温常压下 大于0的反应一定不能自发进行
C. 其他条件不变,升高温度,吸热反应的反应速率加快,放热反应的反应速率减慢
D. (g)与 (g)生成 (g)的反应中,催化剂能减小该反应的焓变
第3页/共17页
学科网(北京)股份有限公司【答案】B
【解析】
【详解】A.ΔG=ΔH-TΔS<0时,反应能够自发进行,放热反应的ΔH<0,若该反应的ΔS>0,该反应能够
自发进行,则放热的自发过程不一定是熵减过程,A错误;
B.ΔG>0时反应非自发,常温常压下ΔG>0确实无法自发进行,B正确;
C.升高温度会加快所有反应的正、逆反应速率,无论是吸热反应还是放热反应,C错误;
D.催化剂仅降低活化能,不影响焓变ΔH,D错误;
故选B。
7. 下列有关氢硫酸( )的说法正确的是
A. 氢硫酸溶液中,不存在 分子
B. 25℃时,电离平衡常数:
C. 的第二步电离平衡常数
D. 由反应 可知,酸性:
【答案】C
【解析】
【详解】A.氢硫酸是弱酸,部分电离,溶液中存在未电离的HS分子,A错误;
2
B.多元弱酸的第一步电离平衡常数K 远大于第二步电离平衡常数K ,故K (H S) > K (H S),B错误;
a1 a2 a1 2 a2 2
C.HS的第二步电离方程式为HS- H+ + S2-,电离平衡常数表达式正确,C正确;
2
D.该反应因生成极难溶的CuS沉淀而进行,不能说明HS酸性强于HSO (事实上HS的酸性弱于
2 2 4 2
HSO ),D错误;
2 4
故选C。
8. 在某恒温恒压密闭容器中,当反应 , 达到平衡时,下列措施不能
提高 平衡转化率的是(每次仅改变一个条件)
A. 充入少量的He B. 适当降低温度 C. 及时抽走部分 (g) D. 增大 (g)的浓度
第4页/共17页
学科网(北京)股份有限公司【答案】A
【解析】
【详解】A.该反应正向气体分子数减少,恒温恒压密闭容器中,充入少量的He,容器的体积增大,相当
于减压,该平衡逆向移动, 的平衡转化率降低,A符合题意;
B.该反应的 ,正向为放热反应,降低温度可使平衡正向移动, 的平衡转化率升高,B不符合题
意;
C.及时抽走部分 (g),则氨气的浓度降低,平衡正向移动, 的平衡转化率升高,C不符合题意;
D.增大 (g)的浓度,平衡正向移动, 的平衡转化率升高,D不符合题意;
故选A。
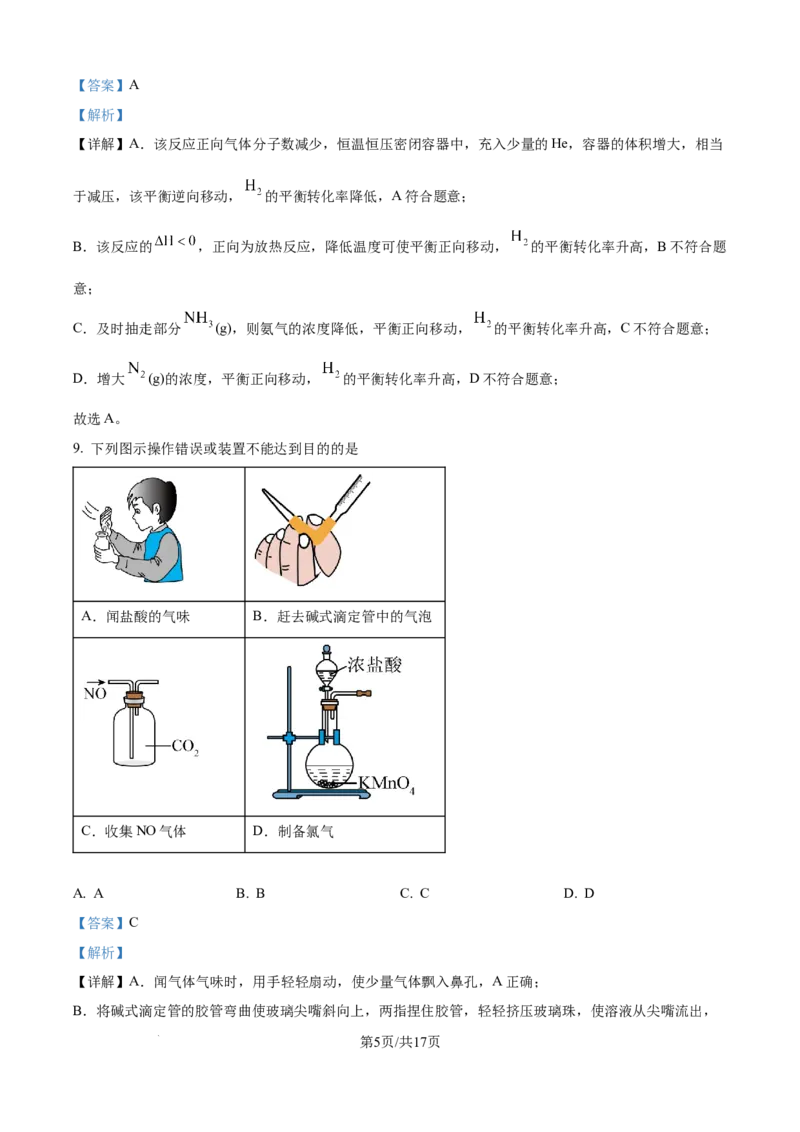
9. 下列图示操作错误或装置不能达到目的的是
A.闻盐酸的气味 B.赶去碱式滴定管中的气泡
C.收集NO气体 D.制备氯气
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.闻气体气味时,用手轻轻扇动,使少量气体飘入鼻孔,A正确;
B.将碱式滴定管的胶管弯曲使玻璃尖嘴斜向上,两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出,
第5页/共17页
学科网(北京)股份有限公司可排出气泡,该操作能达到实验目的,B正确;
C.NO气体的密度与空气相近,且NO会与空气中的氧气反应生成NO ,不能用排空气法收集,可用排水
2
法,C错误;
D.常温下浓盐酸和高锰酸钾发生氧化还原反应生成氯气,可以用于制取氯气,D正确;
故选C。
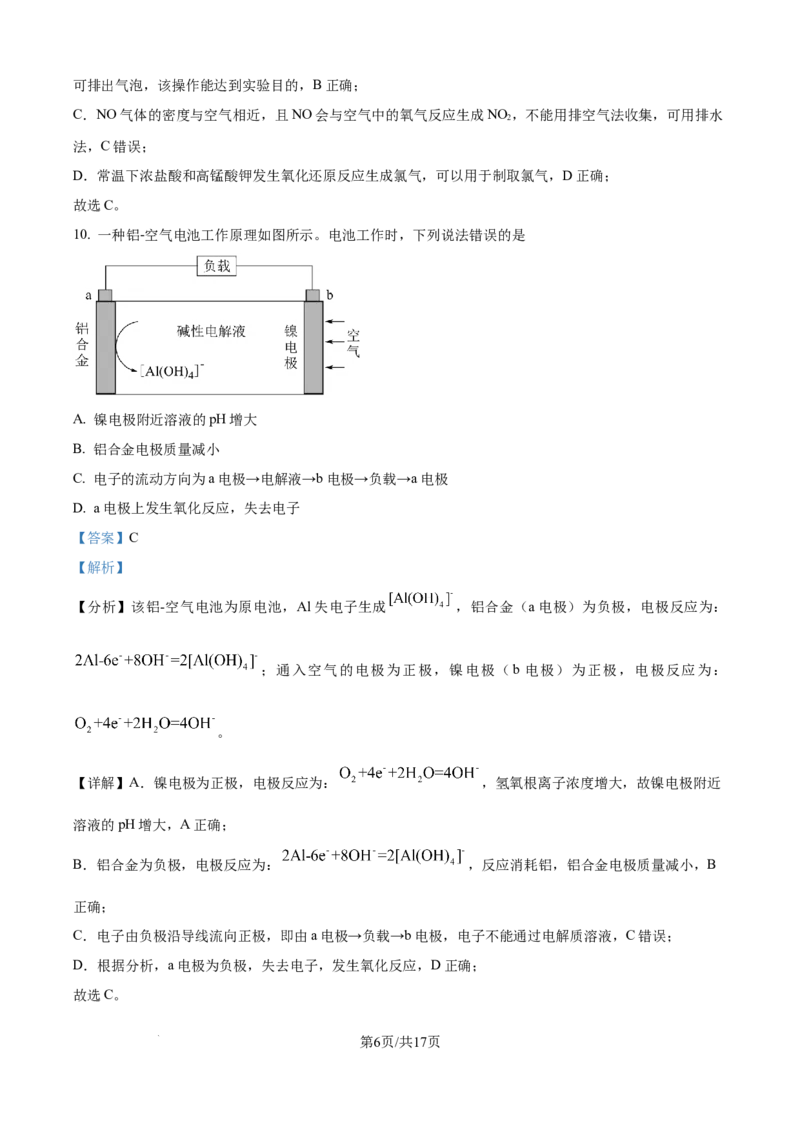
10. 一种铝-空气电池工作原理如图所示。电池工作时,下列说法错误的是
A. 镍电极附近溶液的pH增大
B. 铝合金电极质量减小
C. 电子的流动方向为a电极→电解液→b电极→负载→a电极
D. a电极上发生氧化反应,失去电子
【答案】C
【解析】
【分析】该铝-空气电池为原电池,Al失电子生成 ,铝合金(a电极)为负极,电极反应为:
;通入空气的电极为正极,镍电极(b 电极)为正极,电极反应为:
。
【详解】A.镍电极为正极,电极反应为: ,氢氧根离子浓度增大,故镍电极附近
溶液的pH增大,A正确;
B.铝合金为负极,电极反应为: ,反应消耗铝,铝合金电极质量减小,B
正确;
C.电子由负极沿导线流向正极,即由a电极→负载→b电极,电子不能通过电解质溶液,C错误;
D.根据分析,a电极为负极,失去电子,发生氧化反应,D正确;
故选C。
第6页/共17页
学科网(北京)股份有限公司11. 工业上采用 催化氧化法处理HCl废气: 。下列说法错误的是
A. 最外层电子数:Cl>O B. 稳定性: >HCl
C. 酸性: D. 氧是第二周期第ⅣA族元素
【答案】D
【解析】
【详解】A.氯原子的最外层有7个电子,氧原子的最外层有6个电子,则最外层电子数:Cl>O,A正确;
B.非金属元素的非金属性越强,其对应的最简单氢化物的稳定性越强,氧元素的非金属性强于氯元素,
则稳定性: >HCl,B正确;
C.同种元素的含氧酸,可表示为 ,非羟基氧原子数n越大,酸的酸性越强,高氯酸的非羟基
氧数目为3,氯酸的非羟基氧数目为2,则酸性: ,C正确;
D.氧元素的原子序数为8,最外层电子数为6,位于元素周期表第二周期第ⅥA族, D错误;
故选D。
12. 下列反应的化学方程式书写正确的是
A. 少量的 通入次氯酸钠溶液中:
B. 少量 通入氯化钡溶液中:
C. 少量NaOH溶液滴入 中:
D. 少量醋酸滴入碳酸钠溶液中:
【答案】A
【解析】
【详解】A.少量的SO 与NaClO的氧化还原反应中,SO 将ClO-还原为Cl-,而自身被氧化为 ,根
2 2
据得失电子守恒、电荷守恒和原子守恒,反应的离子方程式为: ,
第7页/共17页
学科网(北京)股份有限公司化学方程式为: ,A正确;
B.HCO 酸性弱于HCl,CO 与BaCl 不反应,B错误;
2 3 2 2
C.少量NaOH优先中和NH HSO 电离产生的H+,故NaOH和NH HSO 按照物质的量之比1:1反应,反应
4 4 4 4
的化学方程式为: ,C错误;
D.醋酸酸性强于碳酸,少量醋酸与碳酸钠反应生成醋酸钠和碳酸氢钠,化学方程式应为:
,D错误;
故选A。
13. 某温度下,0.1 的NaOH溶液的pH是12,在此温度下,将pH=a的盐酸 L与pH=b的
NaOH溶液 L混合(忽略溶液混合时体积和温度的变化),所得混合溶液呈中性。若a+b=11,则 为
A. 1:10 B. 10:1 C. 1:100 D. 100:1
【答案】C
【解析】
【详解】0.1 mol/L NaOH的pH=12,则c(H+)=10-12mol/L,由于c(OH-)=0.1mol/L,故K =10-12×0.1=10-13;此
w
温度下,pH=a的盐酸中c(H+)=10-amol/L,pH=b的NaOH溶液中c(OH-)= ,将
pH=a的盐酸 L与pH=b的NaOH溶液 L混合(忽略溶液混合时体积和温度的变化),所得混合溶液呈
中性,则 ×10-a=V×10b-13,即 =10a+b-13,若a+b=11,则 为1:100,故选C。
2
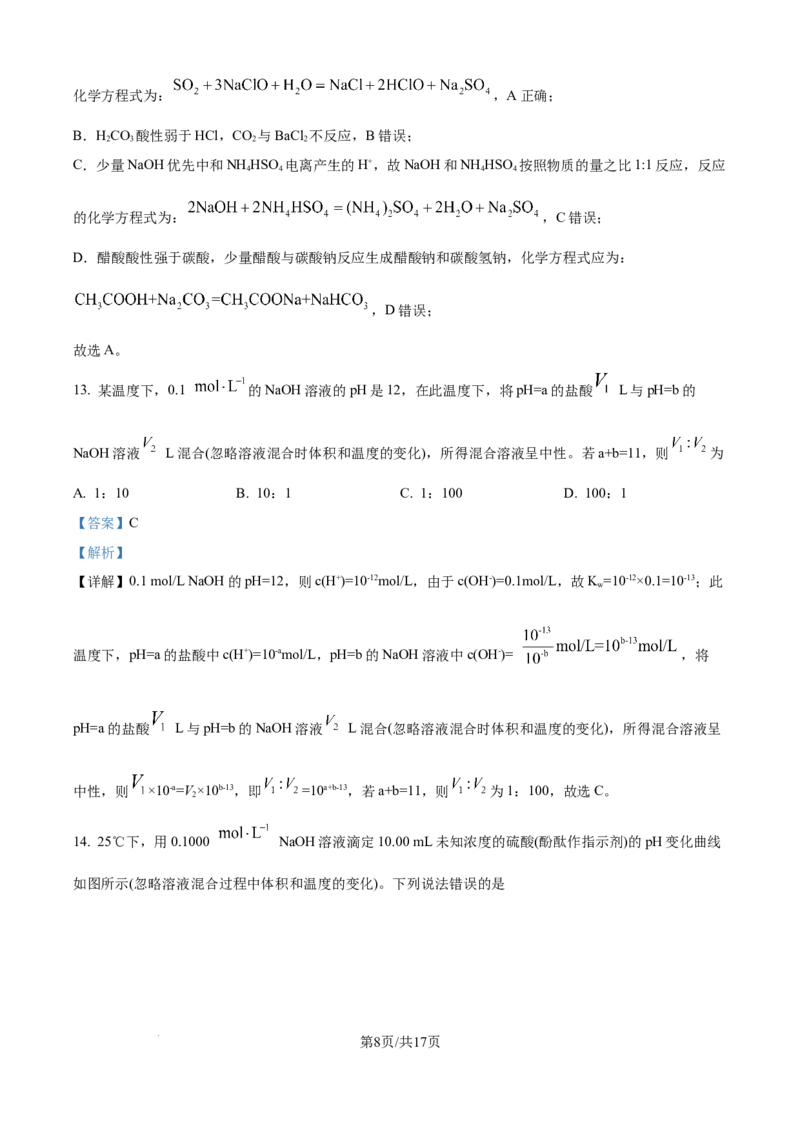
14. 25℃下,用0.1000 NaOH溶液滴定10.00 mL未知浓度的硫酸(酚酞作指示剂)的pH变化曲线
如图所示(忽略溶液混合过程中体积和温度的变化)。下列说法错误的是
第8页/共17页
学科网(北京)股份有限公司A. 该硫酸中 浓度为0.2
B. b点溶液中,由水电离出的 和 的浓度为
C. c点溶液中所含的分子有 、 和NaOH
D. 该温度下,a、b、c三点溶液中 均为
【答案】C
【解析】
【详解】A.氢氧化钠为强碱,硫酸为强酸,图中滴加20.00 mL NaOH溶液时,溶液呈中
性,即恰好中和,则 ,即 ,故该硫酸
中 浓度为 ,A正确;
B. b点溶液恰好为中性,溶质为硫酸钠,则 ,B正确;
C. c点时,所加的NaOH溶液已过量,溶液中的溶剂为 ,溶质为 和NaOH,由于 和
NaOH均为强电解质,在水中完全电离,故所含的分子只有 ,C错误;
D.常温下, 只受温度影响,故该温度下,a、b、c三点溶液中 均为 ,D正确;
故选C。
二、非选择题:本题共4小题,共58分。
15. 用 与硫酸(足量)反应制取 气体,实验过程中产生 的体积(已换算成标准状况下且气体
第9页/共17页
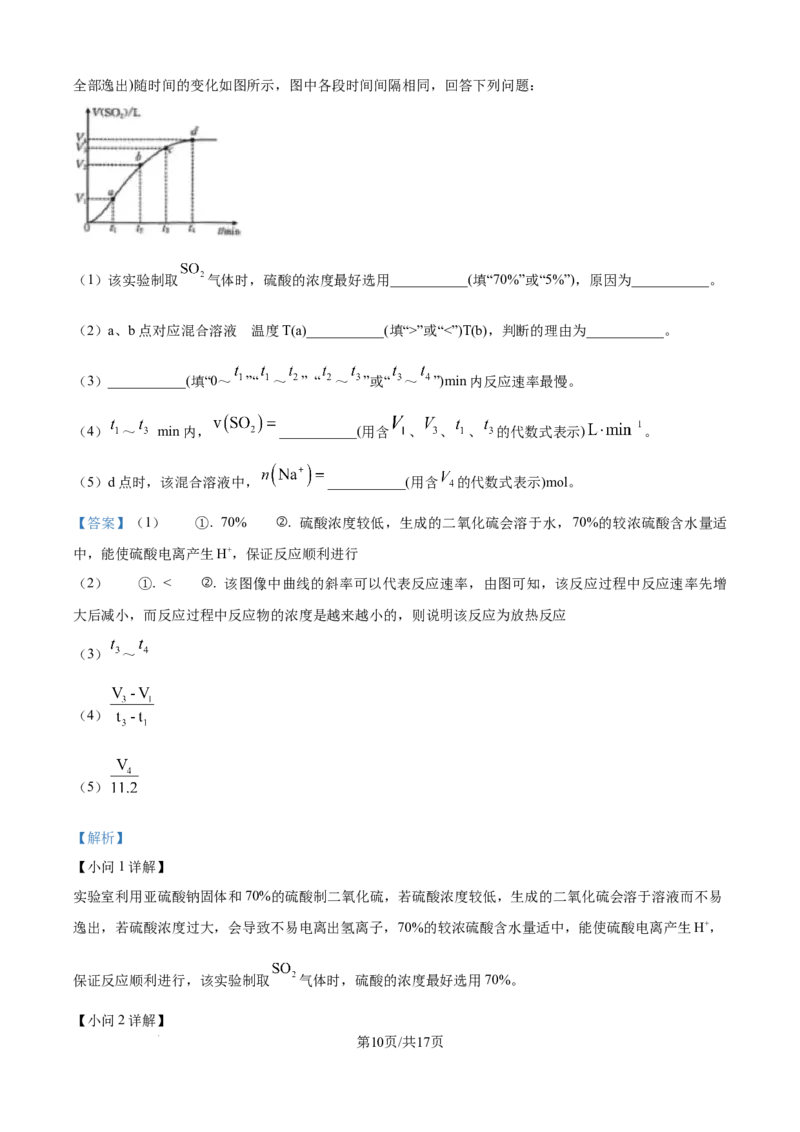
学科网(北京)股份有限公司全部逸出)随时间的变化如图所示,图中各段时间间隔相同,回答下列问题:
(1)该实验制取 气体时,硫酸的浓度最好选用___________(填“70%”或“5%”),原因为___________。
的
(2)a、b点对应混合溶液 温度T(a)___________(填“>”或“<”)T(b),判断的理由为___________。
(3)___________(填“0~ ”“ ~ ” “ ~ ”或“ ~ ”)min内反应速率最慢。
(4) ~ min内, ___________(用含 、 、 、 的代数式表示) 。
(5)d点时,该混合溶液中, ___________(用含 的代数式表示)mol。
【答案】(1) ①. 70% ②. 硫酸浓度较低,生成的二氧化硫会溶于水,70%的较浓硫酸含水量适
中,能使硫酸电离产生H+,保证反应顺利进行
(2) ①. < ②. 该图像中曲线的斜率可以代表反应速率,由图可知,该反应过程中反应速率先增
大后减小,而反应过程中反应物的浓度是越来越小的,则说明该反应为放热反应
(3) ~
(4)
(5)
【解析】
【小问1详解】
实验室利用亚硫酸钠固体和70%的硫酸制二氧化硫,若硫酸浓度较低,生成的二氧化硫会溶于溶液而不易
逸出,若硫酸浓度过大,会导致不易电离出氢离子,70%的较浓硫酸含水量适中,能使硫酸电离产生H+,
保证反应顺利进行,该实验制取 气体时,硫酸的浓度最好选用70%。
【小问2详解】
第10页/共17页
学科网(北京)股份有限公司该图像中曲线的斜率可以代表反应速率,由图可知,相同时间段内产生的气体量先增多后减少,说明该反
应过程中反应速率先增大后减小,而反应过程中反应物的浓度是越来越小的,则说明该反应为放热反应,
反应放热使溶液温度升高,从而使反应速率加快,因此a、b点对应混合溶液的温度T(a) ”或“<”)0。
第11页/共17页
学科网(北京)股份有限公司④下列反应的能量变化与反应Ⅲ的能量变化相符的是___________(填标号)。
a.生石灰溶于水 b.金属钠溶于水
c.稀盐酸与碳酸氢钠的反应 d.氯化铵固体与 的反应
(3)已知反应: 。相关化学键键能数据如表所示。
化学键 C-H C-F H-F F-F
键能/( ) x y z q
① ___________(用含x、y、z、q的代数式表示) 。
②该反应中,每生成0.2 mol HF(g),转移电子的数目为___________ 。
【答案】(1)
(2) ①. 放热 ②. 大于 ③. < ④. ab
(3) ①. ②. 0.4
【解析】
【小问1详解】
燃烧热是在101 kPa时,1 mol纯物质完全燃烧生成指定产物时所放出的热量;表示 (g)燃烧热的热化学
方程式为 ;
【小问2详解】
①反应Ⅰ焓变小于0,属于放热反应。
②反应Ⅱ焓变小于0,属于放热反应,则反应物的能量总和大于生成物的能量总和。
③由盖斯定律,反应Ⅰ +反应Ⅱ得到反应Ⅲ:
;
④反应Ⅲ焓变小于0,为放热反应;
a.生石灰溶于水并与水反应生成氢氧化钙,同时放热,a符合题意;
第12页/共17页
学科网(北京)股份有限公司b.金属钠溶于水并与水反应生成氢氧化钠和氢气,同时放出大量热,b符合题意;
c.稀盐酸与碳酸氢钠的反应为吸热反应,c不符合题意;
d.氯化铵固体与 的反应为吸热反应,d不符合题意;
故选ab;
【小问3详解】
①反应焓变=反应物键能总和-生成物键能总和;则
;
②该反应中,氟元素化合价由0变为-1,F 为氧化剂,则存在关系: ,结合反应方程式知,每生
2
成0.2 mol HF(g),转移0.4mol电子,电子的数目为0.4 。
17. 某温度下,向2L的某恒容密闭容器中仅充入 气体 和 气体 ,在一定条件下发生反应:
。反应 时,测得 的物质的量减少了 ,B的物质的量减少
了 ,有 生成,平均反应速率 。回答下列问题:
(1) 时, _______(用含 、 的代数式表示) ,D的物质的量分数为_______(用含
、 的代数式表示)。
(2)若 为 ,B为 ,D为 ,则上述反应的化学方程式为_______。该反应中,每转移
电子,生成 的体积为_______ (标准状况下)。
(3) 时,该反应达到平衡,此时测得 的物质的量为 。
①B的平衡转化率为_______%(用含 、 的代数式表示,写出计算式即可)。
第13页/共17页
学科网(北京)股份有限公司② 内, _______(用含 的代数式表示) 。
③该反应的平衡常数为_______(用含 、 的代数式表示,写出计算式即可)。
④保持其他条件不变,仅增大压强,此时该反应的平衡常数将_______(填“增大”“减小”或“不变”)。
【答案】(1) ①. ②.
(2) ①. ②. 2.24
(3) ① ②. 0.025a ③. ④. 不变
.
【解析】
【小问1详解】
,向2 L的某恒容密闭容器中仅充入 气体 和 气体 ,反应 时,,B的物质的量减少
了 , , 。
反应 时,测得 的物质的量减少了 ,B的物质的量减少了 ,有 生成,平均反应速
率 。则有 ,方程式表示为 ,反应
时, 的物质的量为 ,B的物质的量 ,D的物质的量为 生成,C
的物质的量为 ,生成
第14页/共17页
学科网(北京)股份有限公司D的物质的量分数为
【小问2详解】
若 为 ,B为 ,D为 ,则上述反应氯元素化合价降低故 的化合价升高生成氮气,化学
方程式为 。
化合物C为 ,按照 ,则每转移 电子,生成 的物质的量为0.1 mol,标况
下的体积为2.24L。
【小问3详解】
时,该反应达到平衡,此时测得 的物质的量为 。以此列三段式:
①B的平衡转化率为 。
② 内, 。
③该反应的平衡常数 。
④平衡常数只与温度有关,保持其他条件不变,仅增大压强,此时该反应的平衡常数不变。
18. 氨水为实验室常用的化学试剂,回答下列问题:
(1) 的电离方程式为 。
① ___________(填“>”或“<”)0。
②适当升高温度, ___________(填“增大”“减小”或“不变”)。
第15页/共17页
学科网(北京)股份有限公司(2)25℃时,将0.2 氨水加水稀释至0.02 。
①稀释过程中, ___________(填“增大”“减小”或“不变”,下同) 。
②稀释过程中,所含氮元素的质量___________。
(3)已知:25℃下, 。
①查阅资料可知,25℃下, 溶液呈中性。 ___________(填“>”“<”或
“=”) 。
②0.2 的氨水中, 约为___________ 。
(4)将3.36 L(标准状况下)氨气溶于水配制成1 L溶液,则溶液中_________。
+___________+___________=0.15 mol。
【答案】(1) ①. > ②. 增大
(2) ①. 减小 ②. 不变
(3) ①. = ②.
(4) +
【解析】
【小问1详解】
①一水合氨的电离过程为吸热过程,则 >0。
②适当升高温度,促进一水合氨的电离,使得电离常数 增大;
【小问2详解】
①稀释过程中,一水合氨的电离平衡正向移动,但是溶液体积变大的影响大于电离平衡正向移动的影响,
使得电离出的铵根离子浓度减小;
②根据氮元素守恒,稀释过程中,所含氮元素 的质量不变;
【小问3详解】
①查阅资料可知,25℃下, 溶液呈中性,则醋酸根离子和铵根离子的水解程度相当,那么
第16页/共17页
学科网(北京)股份有限公司= ;
② ,0.2 的氨水中
, 。
【小问4详解】
将3.36 L(标准状况下)氨气(为0.15mol NH )溶于水配制成1 L溶液,根据氮元素守恒,则溶液中
3
+ + =0.15 mol。
第17页/共17页
学科网(北京)股份有限公司