文档内容
工业流程(分离提纯产物——萃取与反萃取)
【重点知识】
一、萃取与反萃取
(一)萃取:利用物质在两种互不相溶的溶剂中的溶解度不同,将物质从一种溶剂转移到另一种溶剂的过程。如用CCl 萃取溴水中的
4
Br。(水相→有机相)
2
(二)反萃取:反萃取是利用反萃取剂使被萃取物从负载有机相返回水相的过程,为萃取的逆过程。(有机相→水相)
(三)原理:Mx++xRH⇋RxM+xH+ [例如:Ce3+(水层)+3HA(有机层)⇋Ce(A)
3
(有机层)+3H+(水层) ]
①金属离子的萃取:有机萃取剂将金属离子从水溶液中萃取出来,使其进入有机层:Mx++xRH→RxM+xH+
②金属离子的反萃取:向有机层加入反萃取剂(HCl、HSO、HNO 等无机酸),使有机层中的金属离子转移到水层:RxM+xH+→Mx++xRH
2 4 3
(四)目的:除去杂质离子,富集主要元素xxx。
(五)装置:
(六)提高萃取率的措施:
①适当增加萃取剂的量
②分多次萃取
(七)萃取中的条件控制:
1. pH:若pH过高会生成xx(如水解),pH过低会使萃取平衡逆向移动,导致萃取率下降。
2. 温度:低于xx℃时,xx的萃取率不高;高于xx℃时,xx的萃取率提高不明显,(另一个)yy的萃取率增大。
(八)萃取中的循环物质:萃取剂
(九)萃取率计算:分配系数Kd=c(有机相)/c(水相)
萃取率= c(有机相)·V(萃取剂)×100%
c(有机相)·V(萃取剂)+c(水相)·V(溶液)
残留率= c(水相)·V(溶液)×100%
c(有机相)·V(萃取剂)+c(水相)·V(溶液)
【典例1】某锂离子二次电池的正极材料主要为LiCoO,还含有少量Al、Fe、Mn、Ni的化合物。通过如下流程利用废旧锂离子电池制
2
取CoO。该工艺设计萃取、反萃取的目的是___________________________________.
3 4
答:分离钴和镍锂,富集Co2+,提高产物纯度。
分析:在“酸浸还原”中都能与硫酸反应,“水解净化”除铝,“氧化沉铁锰”除铁、锰,剩余钴、锂、镍在滤液中,后续萃取除去。
【典例2】以粗NiSO 溶液(含Cu2+、Ca2+等杂质)为原料制备NiSO·6HO的部分过程如下:
4 4 2
已知:Ni2+、Ca2+能被有机萃取剂(简称HR)萃取,其萃取原理:
Ni2+(水层)+2HR(有机层)� NiR(有机层)+2H+(水层)
2
学科网(北京)股份有限公司Ca2+(水层)+2HR(有机层)� CaR(有机层)+2H+(水层)
2
(2)“萃取”时,用一定量的HR充分萃取,能实现Ni2+与Ca2+的分离,原因是 。
(3)“反萃取”时,加入稀HSO,水层中Ni2+物质的量迅速增多的原因是 。
2 4
答:(2)Ni2+与HR结合的能力大于Ca2+与HR结合的能力 (3)随着c(H+)的增大,平衡向逆反应方向移动,且NiR 转化为Ni2+的速率加
2
快,转化程度迅速增大
分析:“萃取”时用一定量的HR充分萃取,能实现Ni2+ 与Ca2+
的分离,说明Ca2+与HR结合的能力小于Ni2+与HR结合的能力;“反
Ni2++2HR � NiR +2H+
萃取”时,加入稀硫酸,溶液中氢离子浓度增大,反应 2 的平衡向逆反应方向移动,且反应速率加快,使
得NiR 转化为Ni2+的转化程度迅速增大。
2
【典例3】萃取Cu2+后,为进行“反萃取”应往有机相中加入___________(填化学式)
答:HSO
2 4
分析:根据反萃取后产物形式,可知为加入硫酸,即可平衡逆移,得到CuSO 溶液。
4
【典例4】一种阳极泥的主要成分为Cu、Ag、Pt、Au、Ag Se和Cu S,从中回收Se和贵重金属的工艺流程如下图所示。
2 2
(4)萃取后得到有机相的操作方法是 (填操作名称),“反萃取剂”最好选用 (填化学式)溶液。
答:分液 HNO
3
分析:萃取后得到有机相的操作方法是分液。反萃取即使萃取平衡逆向移动,此时可向体系中加酸,由于最终是获得硝酸铜,所以为
了不引入新杂质,最好选用HNO 。
3
【典例5】浸-反萃取-电积法是一种高效、环保的湿法冶金工艺,广泛应用于从低品位锌矿中提取锌。用该方法从锌矿(主要成分为ZnS,
含有FeS 、CuS、NiS、SiO 等杂质)中获得锌的流程如下图所示:
2 2
(4)
为提高Zn2+
的萃取率,“萃取”时需要 (填“一次萃取”或“多次萃取”),分离含锌有机相和含镍萃余液的操作
学科网(北京)股份有限公司为 。(操作名称)
答:多次萃取 分液
分析:为提高 Zn2+的萃取率,“萃取”时需要多次萃取;含锌有机相与含镍萃余液为互不相溶的液体混合物,分离含锌有机相和含镍
萃余液的操作为:分液。
【典例6】稀土是一种重要的战略资源,铈是地壳中含量最多的稀土元素。由氟碳铈矿(主要成分CeFCO ,含少量SiO、Fe O、CaF
3 2 2 3 2
等杂质)提取铈的一种工艺流程如下:
(3)已知有机物HR能将Ce3+从水溶液中萃取出来,该过程可表示为:Ce3+(水层)+3HR(有机层)� CeR (有机层)+3H+(水层)。
3
在分离有机相和水相时,打开分液漏斗活塞放出下层液体前,应先 (填具体操作)。
答:打开分液漏斗上口活塞(或使活塞上的凹槽对准漏斗口的小孔)
分析:分液时打开分液漏斗活塞放出下层液体前,应先打开分液漏斗上口活塞(或使活塞上的凹槽对准漏斗口的小孔)。
【典例7】利用稀有金属镍、钴制造的合金是航天领域重要材料之一、以含镍废料(主要成分为NiO,含少量FeO、Fe O 、CoO、BaO
2 3
和SiO )为原料制备Ni和Co(OH) 的工艺流程如下。
2 2
(4)“萃取”和“反萃取”可简单表示为:2HX+Ni2+���� 萃�取 ����� NiX +2H+。
2
①“萃取”时需充分振荡,目的 。
②“反萃取”后水层为NiSO 溶液,需要往有机层中加入的试剂1为 (填化学式)。
4
答:增大有机溶剂与溶液的接触面积,提高Ni2+的萃取率 H SO
2 4
分析:①“萃取”时需充分振荡,目的是增大有机溶剂与溶液的接触面积,提高Ni2+
的萃取率;
②“萃取”和“反萃取”可简单表示为:2HX+Ni2+���� 萃�取 ����� NiX
2
+2H+,在含NiSO
4
的有机层反萃取得到NiSO
4
溶液,故加入的
试剂1为H SO ;
2 4
学科网(北京)股份有限公司【典例8】从某铜镍矿(主要含有Cu、Ni单质,还含有Fe O 、FeO、MgO、CuO等杂质)资源中提取Cu和Ni的一种工艺流程如下:
2 3
(3)“萃取”时发生反应:Cu2++2HR � CuR +2H+,“反萃取”时使用的试剂a最合适的为 。
2
A.NaOH B.H SO C.HCl
2 4
从平衡角度解释试剂a的作用:
答:B 增大c(H+),萃取反应逆向移动,使Cu2+进入水相。
分析:整个流程中用到的都是硫酸,根据萃取方程式,反萃取使平衡逆向移动,因此需要增大 c(H+),不引入杂质,因此采用 HSO,
2 4
c
( H+)
故选B;a的作用为增大 ,萃取反应逆向移动,使Cu2+进入水相。
【典例9】利用炼锌矿渣获得3种金属盐,并进一步利用镓盐制备氮化镓(GaN),已知矿渣主要含铁酸镓Ga (Fe O ) 、铁酸锌ZnFe O 、
2 2 4 3 2 4
二氧化硅等,部分工艺流程如下:
常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在该工艺条件下萃取率(进入有机层中金属离子的百分数)如下表:
金属离子 Fe2+ Fe3+ Zn2+ Ga3+
开始沉淀pH 8.0 1.7 5.5 3.0
沉淀完全pH 9.6 3.2 8.0 4.9
萃取率(%) 0 99 0 97~98.5
(3)“萃取”前加入铁粉还原Fe3+的作用是 ,Ga性质与Al相似,反萃取后水溶液中镓元素以
形式存在。
Ga(OH) − NaGa(OH)
答:铁离子和镓离子萃取率相近,避免铁离子被萃取 4 或 4
分析:根据题中表格数据可知,Fe3+ 萃取率与Ga3+
相近,为避免铁离子被萃取,所以将其还原为亚铁离子。Ga的性质与 Al相似,
学科网(北京)股份有限公司Ga(OH) − NaGa(OH)
反萃取后水溶液中镓元素以 4 或 4 形式存在。
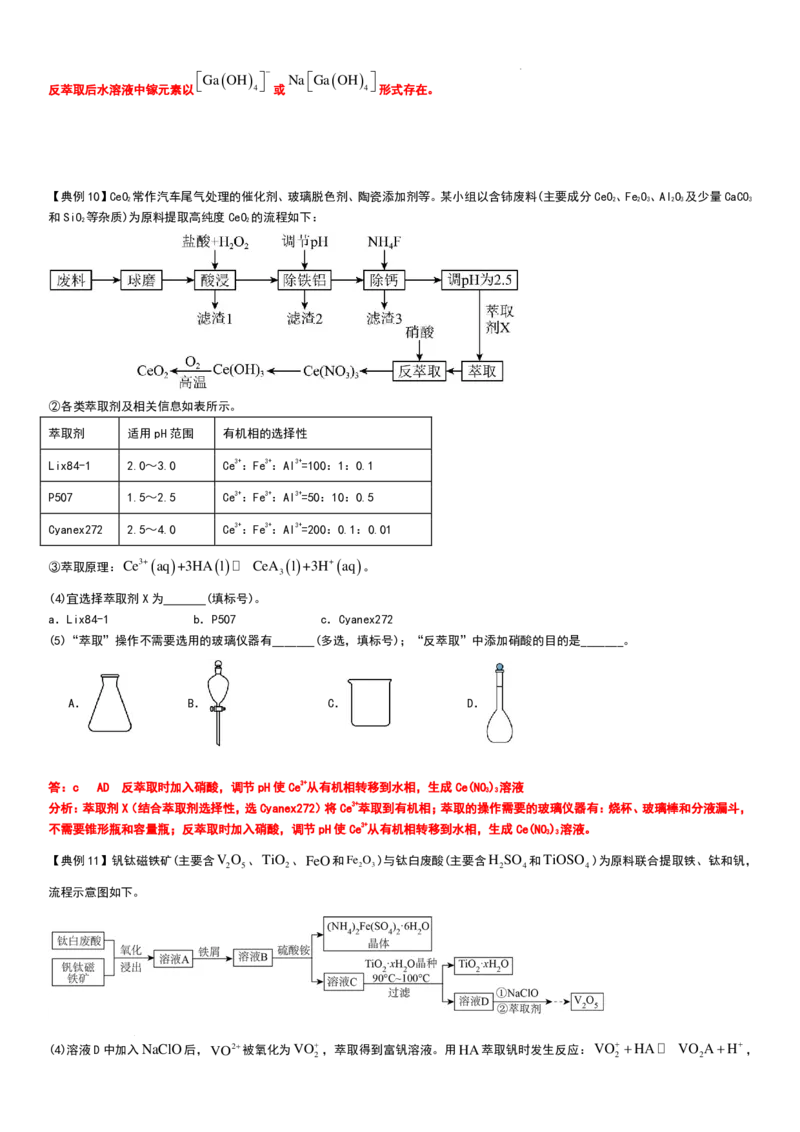
【典例10】CeO 常作汽车尾气处理的催化剂、玻璃脱色剂、陶瓷添加剂等。某小组以含铈废料(主要成分CeO、FeO、AlO 及少量CaCO
2 2 2 3 2 3 3
和SiO 等杂质)为原料提取高纯度CeO 的流程如下:
2 2
②各类萃取剂及相关信息如表所示。
萃取剂 适用pH范围 有机相的选择性
Lix84-1 2.0~3.0 Ce3+:Fe3+:Al3+=100:1:0.1
P507 1.5~2.5 Ce3+:Fe3+:Al3+=50:10:0.5
Cyanex272 2.5~4.0 Ce3+:Fe3+:Al3+=200:0.1:0.01
③萃取原理:Ce3+(aq)+3HA(l)� CeA (l)+3H+(aq) 。
3
(4)宜选择萃取剂X为 (填标号)。
a.Lix84-1 b.P507 c.Cyanex272
(5)“萃取”操作不需要选用的玻璃仪器有_______(多选,填标号);“反萃取”中添加硝酸的目的是_______。
A. B. C. D.
答:c AD 反萃取时加入硝酸,调节pH使Ce3+从有机相转移到水相,生成Ce(NO) 溶液
3 3
分析:萃取剂X(结合萃取剂选择性,选Cyanex272)将Ce3+萃取到有机相;萃取的操作需要的玻璃仪器有:烧杯、玻璃棒和分液漏斗,
不需要锥形瓶和容量瓶;反萃取时加入硝酸,调节pH使Ce3+从有机相转移到水相,生成Ce(NO) 溶液。
3 3
【典例11】钒钛磁铁矿(主要含VO 、TiO 、FeO和Fe O )与钛白废酸(主要含H SO 和TiOSO )为原料联合提取铁、钛和钒,
2 5 2 2 3 2 4 4
流程示意图如下。
(4)溶液D中加入NaClO后,VO2+被氧化为VO+,萃取得到富钒溶液。用HA萃取钒时发生反应:VO+ +HA� VO A+H+,
2 2 2
学科网(北京)股份有限公司分液后得到含VO A的有机溶液。由有机溶液重新得到含VO+的水溶液的操作是
2 2
。
答:将有机溶液注入分液漏斗中,加入较浓的硫酸,振荡后静置,分液
分析:由有机溶液重新得到含VO+的水溶液,使VO+ +HA� VO A+H+平衡逆向移动,则应增大c ( H+) ,故反萃取操作为将
2 2 2
有机溶液注入分液漏斗中,加入较浓的硫酸,振荡后静置,分液。
【典例12】钪(Sc)是一种高度分散的微量元素,赤泥(主要成分为Al O、SiO、Fe O 、CaO、Na O、Sc O 等)是提取这类稀有
2 3 2 2 3 2 2 3
贵金属的潜在资源。从赤泥中回收钪元素的流程图如下,回答下列问题。
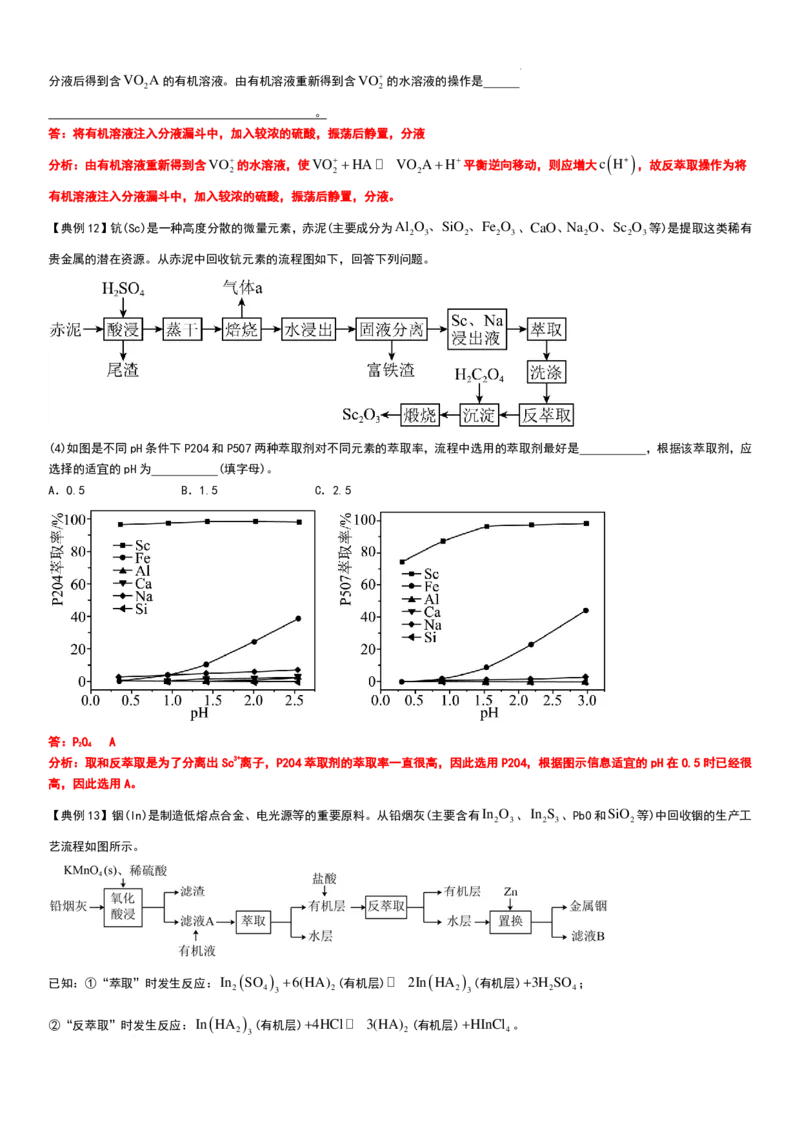
(4)如图是不同pH条件下P204和P507两种萃取剂对不同元素的萃取率,流程中选用的萃取剂最好是 ,根据该萃取剂,应
选择的适宜的pH为 (填字母)。
A.0.5 B.1.5 C.2.5
答:P0 A
2 4
分析:取和反萃取是为了分离出Sc3+离子,P204萃取剂的萃取率一直很高,因此选用P204,根据图示信息适宜的pH在0.5时已经很
高,因此选用A。
【典例13】铟(In)是制造低熔点合金、电光源等的重要原料。从铅烟灰(主要含有In O 、In S 、PbO和SiO 等)中回收铟的生产工
2 3 2 3 2
艺流程如图所示。
已知:①“萃取”时发生反应:In (SO ) +6(HA) (有机层)� 2In(HA ) (有机层)+3H SO ;
2 4 3 2 2 3 2 4
②“反萃取”时发生反应:In(HA ) (有机层)+4HCl� 3(HA) (有机层)+HInCl 。
2 3 2 4
学科网(北京)股份有限公司(5)“萃取”和“反萃取”的目的是 ;“萃取”时,控制溶液的pH为1.5,铟萃取率最大,原因是 。
答:富集In元素并除去杂质 pH小,
c
( H+)
大,不利于萃取正向进行,萃取率减小,pH过大,In3+
会转化为
In(OH)
3沉淀,萃取
率减小
【典例14】某矿石中富含Cu (OH) CO 和Ni(OH) ,还含有Fe、Al、Si、Ca的氧化物。以该矿石为原料制备
2 2 3 2
Ni(OH) ?2NiCO ?nH O的流程如图所示,请回答下列问题:
2 3 2
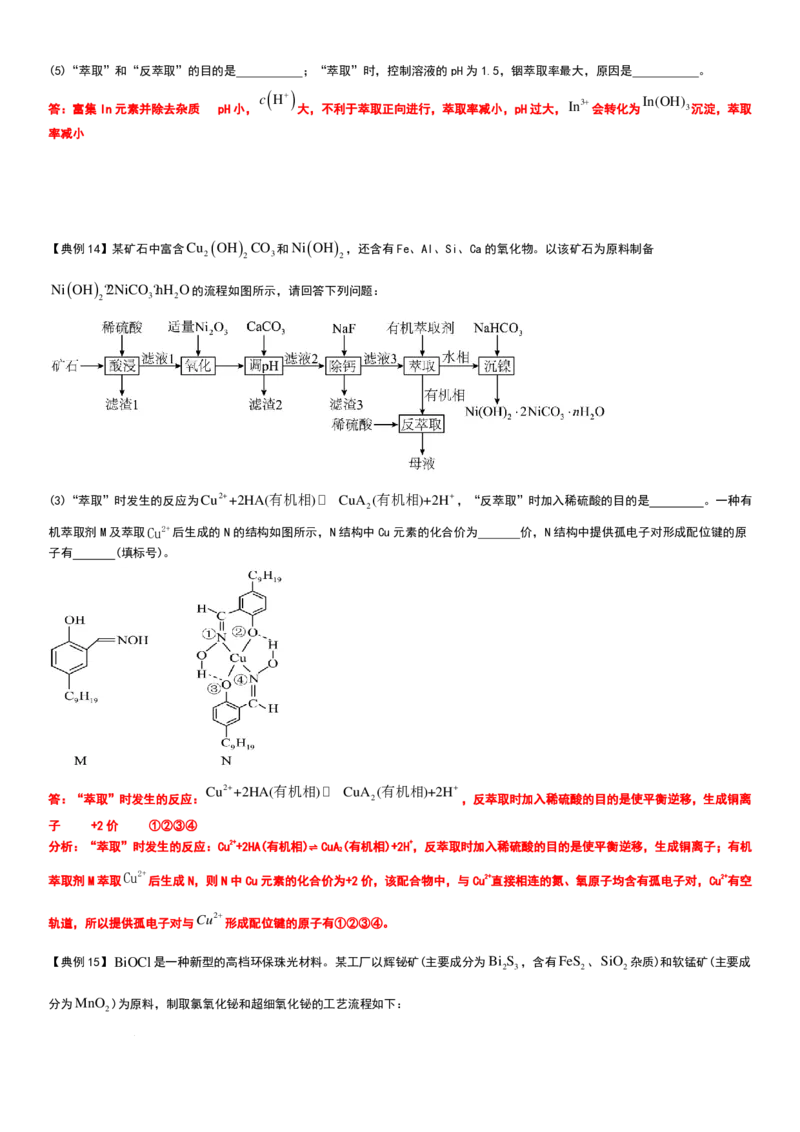
(3)“萃取”时发生的反应为Cu2++2HA(有机相)� CuA (有机相)+2H+,“反萃取”时加入稀硫酸的目的是 。一种有
2
机萃取剂M及萃取Cu2+后生成的N的结构如图所示,N结构中Cu元素的化合价为 价,N结构中提供孤电子对形成配位键的原
子有 (填标号)。
Cu2++2HA(有机相)� CuA (有机相)+2H+
答:“萃取”时发生的反应: 2 ,反萃取时加入稀硫酸的目的是使平衡逆移,生成铜离
子 +2价 ①②③④
分析:“萃取”时发生的反应:Cu2++2HA(有机相)⇌CuA
2
(有机相)+2H+,反萃取时加入稀硫酸的目的是使平衡逆移,生成铜离子;有机
萃取剂M萃取
Cu2+
后生成N,则N中Cu元素的化合价为+2价,该配合物中,与Cu2+直接相连的氮、氧原子均含有孤电子对,Cu2+有空
轨道,所以提供孤电子对与Cu2+
形成配位键的原子有①②③④。
【典例15】BiOCl是一种新型的高档环保珠光材料。某工厂以辉铋矿(主要成分为Bi S ,含有FeS 、SiO 杂质)和软锰矿(主要成
2 3 2 2
分为MnO )为原料,制取氯氧化铋和超细氧化铋的工艺流程如下:
2
学科网(北京)股份有限公司已知:Bi3+易与Cl-
形成
BiCl3
6
-
,
pH
大于2时,
BiCl3
6
-
易水解。
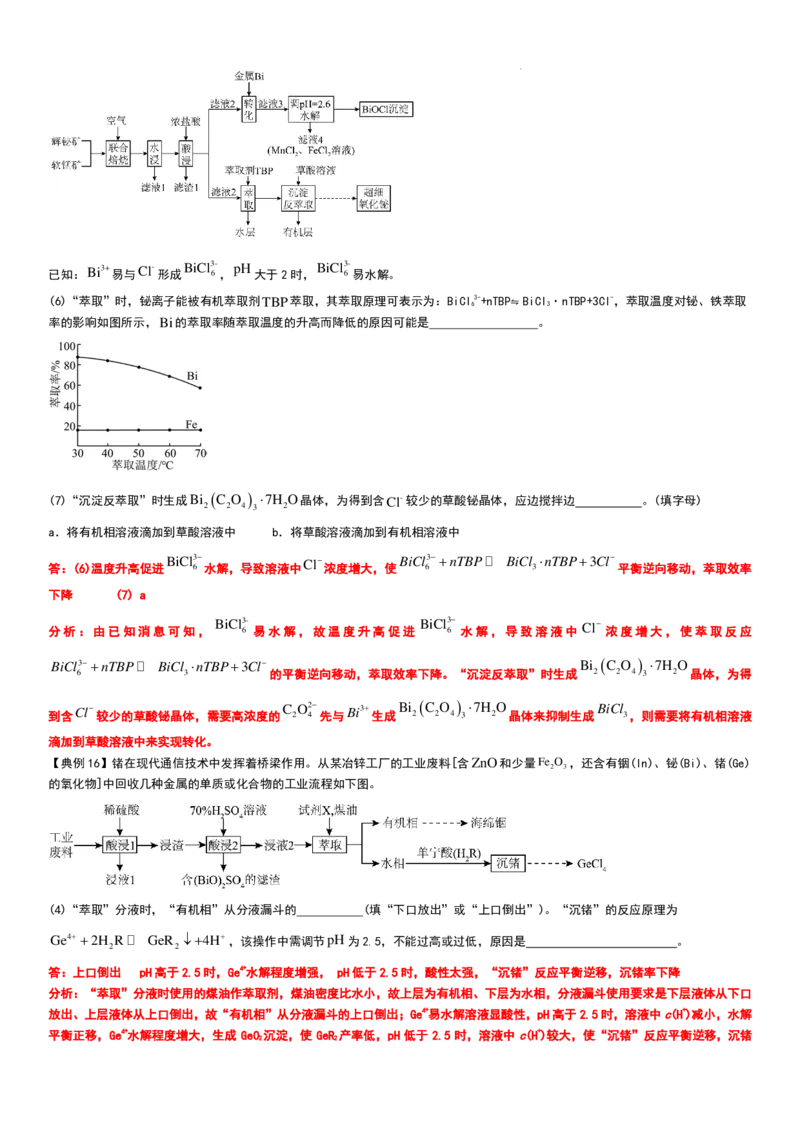
(6)“萃取”时,铋离子能被有机萃取剂TBP萃取,其萃取原理可表示为:BiCl
6
3-+nTBP⇋BiCl
3
·nTBP+3Cl-,萃取温度对铋、铁萃取
率的影响如图所示,Bi的萃取率随萃取温度的升高而降低的原因可能是 。
(7)“沉淀反萃取”时生成Bi (C O ) ⋅7H O晶体,为得到含Cl-较少的草酸铋晶体,应边搅拌边 。(填字母)
2 2 4 3 2
a.将有机相溶液滴加到草酸溶液中 b.将草酸溶液滴加到有机相溶液中
答:(6)温度升高促进
BiCl3
6
− 水解,导致溶液中Cl−
浓度增大,使
BiCl
6
3−+nTBP� BiCl
3
⋅nTBP+3Cl−
平衡逆向移动,萃取效率
下降 (7) a
分析:由已知消息可知,
BiCl3
6
-
易水解,故温度升高促进
BiCl3
6
−
水解,导致溶液中
Cl−
浓度增大,使萃取反应
BiCl3−+nTBP� BiCl ⋅nTBP+3Cl− Bi (C O ) ⋅7H O
6 3 的平衡逆向移动,萃取效率下降。“沉淀反萃取”时生成 2 2 4 3 2 晶体,为得
到含Cl−
较少的草酸铋晶体,需要高浓度的
C
2
O
4
2− 先与Bi3+
生成
Bi
2
(C
2
O
4
)
3
⋅7H
2
O
晶体来抑制生成
BiCl
3,则需要将有机相溶液
滴加到草酸溶液中来实现转化。
【典例16】锗在现代通信技术中发挥着桥梁作用。从某冶锌工厂的工业废料[含ZnO和少量Fe O ,还含有铟(In)、铋(Bi)、锗(Ge)
2 3
的氧化物]中回收几种金属的单质或化合物的工业流程如下图。
(4)“萃取”分液时,“有机相”从分液漏斗的 (填“下口放出”或“上口倒出”)。“沉锗”的反应原理为
Ge4+ +2H R � GeR ↓+4H+,该操作中需调节pH为2.5,不能过高或过低,原因是 。
2 2
答:上口倒出 pH高于2.5时,Ge4+水解程度增强, pH低于2.5时,酸性太强,“沉锗”反应平衡逆移,沉锗率下降
分析:“萃取”分液时使用的煤油作萃取剂,煤油密度比水小,故上层为有机相、下层为水相,分液漏斗使用要求是下层液体从下口
放出、上层液体从上口倒出,故“有机相”从分液漏斗的上口倒出;Ge4+易水解溶液显酸性,pH高于2.5时,溶液中c(H+)减小,水解
平衡正移,Ge4+水解程度增大,生成 GeO 沉淀,使 GeR 产率低,pH低于 2.5时,溶液中c(H+)较大,使“沉锗”反应平衡逆移,沉锗
2 2
学科网(北京)股份有限公司率降低。
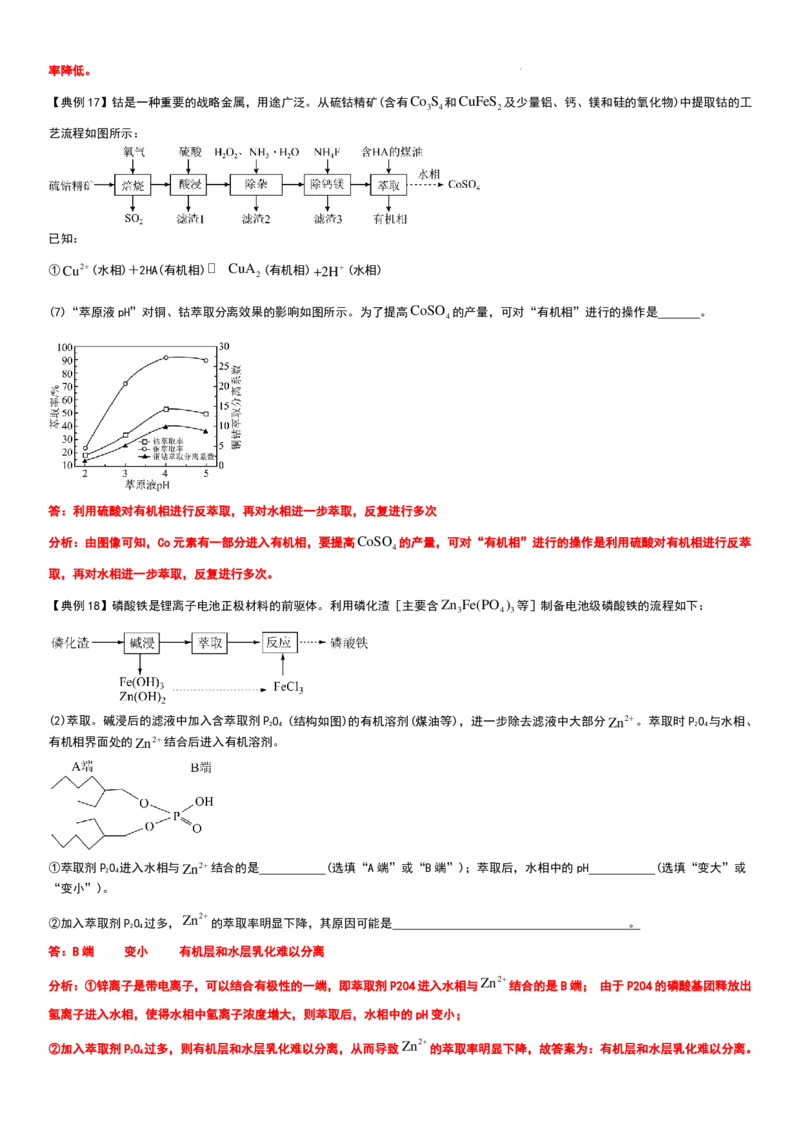
【典例17】钴是一种重要的战略金属,用途广泛。从硫钴精矿(含有Co S 和CuFeS 及少量铝、钙、镁和硅的氧化物)中提取钴的工
3 4 2
艺流程如图所示:
已知:
①Cu2+(水相)+2HA(有机相)� CuA (有机相)+2H+(水相)
2
(7)“萃原液pH”对铜、钴萃取分离效果的影响如图所示。为了提高CoSO 的产量,可对“有机相”进行的操作是 。
4
答:利用硫酸对有机相进行反萃取,再对水相进一步萃取,反复进行多次
分析:由图像可知,Co元素有一部分进入有机相,要提高CoSO 的产量,可对“有机相”进行的操作是利用硫酸对有机相进行反萃
4
取,再对水相进一步萃取,反复进行多次。
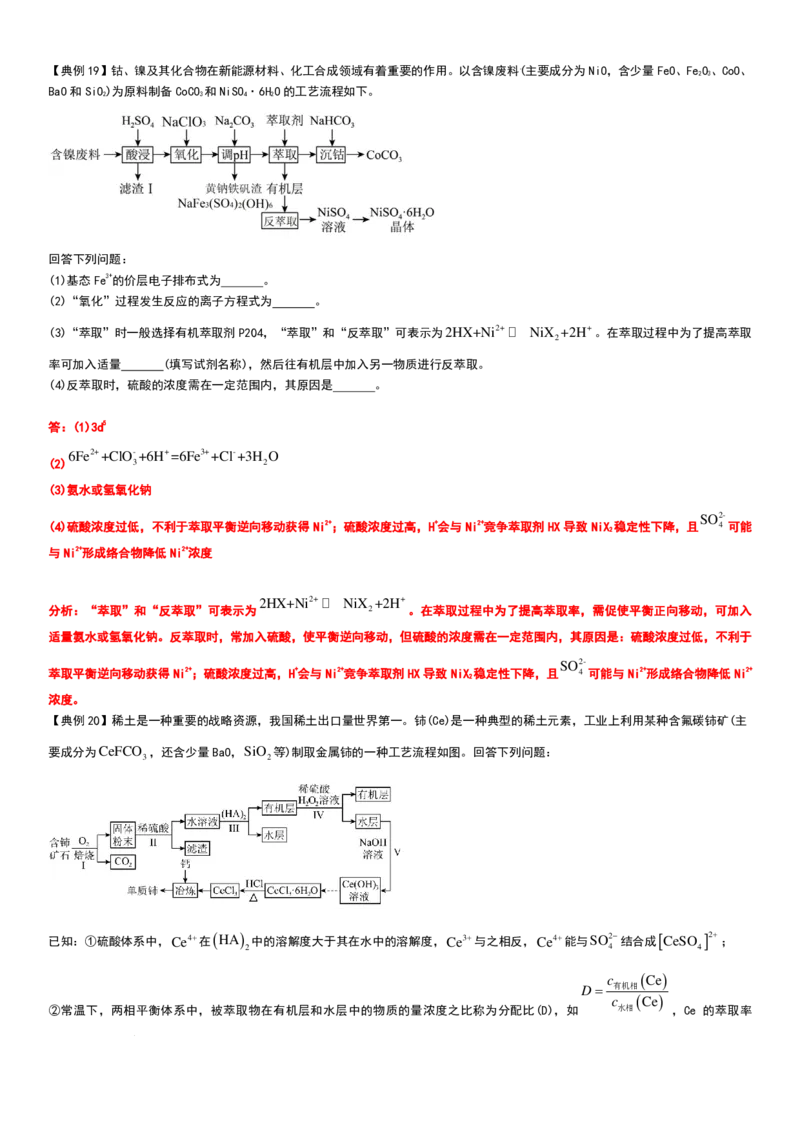
【典例18】磷酸铁是锂离子电池正极材料的前驱体。利用磷化渣[主要含Zn Fe(PO ) 等]制备电池级磷酸铁的流程如下:
3 4 3
(2)萃取。碱浸后的滤液中加入含萃取剂P
2
O
4
(结构如图)的有机溶剂(煤油等),进一步除去滤液中大部分Zn2+。萃取时P
2
O
4
与水相、
有机相界面处的Zn2+结合后进入有机溶剂。
①萃取剂P
2
O
4
进入水相与Zn2+结合的是 (选填“A端”或“B端”);萃取后,水相中的pH (选填“变大”或
“变小”)。
②加入萃取剂PO
过多,Zn2+
的萃取率明显下降,其原因可能是 。
2 4
答:B端 变小 有机层和水层乳化难以分离
分析:①锌离子是带电离子,可以结合有极性的一端,即萃取剂P2O4进入水相与Zn2+
结合的是B端; 由于P2O4的磷酸基团释放出
氢离子进入水相,使得水相中氢离子浓度增大,则萃取后,水相中的pH变小;
②加入萃取剂PO
过多,则有机层和水层乳化难以分离,从而导致Zn2+
的萃取率明显下降,故答案为:有机层和水层乳化难以分离。
2 4
学科网(北京)股份有限公司【典例19】钴、镍及其化合物在新能源材料、化工合成领域有着重要的作用。以含镍废料(主要成分为NiO,含少量FeO、FeO、CoO、
2 3
BaO和SiO)为原料制备CoCO 和NiSO·6HO的工艺流程如下。
2 3 4 2
回答下列问题:
(1)基态Fe3+的价层电子排布式为 。
(2)“氧化”过程发生反应的离子方程式为 。
(3)“萃取”时一般选择有机萃取剂P204,“萃取”和“反萃取”可表示为2HX+Ni2+ � NiX +2H+。在萃取过程中为了提高萃取
2
率可加入适量 (填写试剂名称),然后往有机层中加入另一物质进行反萃取。
(4)反萃取时,硫酸的浓度需在一定范围内,其原因是 。
答:(1)3d5
6Fe2++ClO-+6H+=6Fe3++Cl-+3H O
(2) 3 2
(3)氨水或氢氧化钠
SO2-
(4)硫酸浓度过低,不利于萃取平衡逆向移动获得Ni2+;硫酸浓度过高,H+会与Ni2+竞争萃取剂HX导致NiX 稳定性下降,且 4 可能
2
与Ni2+形成络合物降低Ni2+浓度
2HX+Ni2+ � NiX +2H+
分析:“萃取”和“反萃取”可表示为 2 。在萃取过程中为了提高萃取率,需促使平衡正向移动,可加入
适量氨水或氢氧化钠。反萃取时,常加入硫酸,使平衡逆向移动,但硫酸的浓度需在一定范围内,其原因是:硫酸浓度过低,不利于
SO2-
萃取平衡逆向移动获得Ni2+;硫酸浓度过高,H+会与Ni2+竞争萃取剂HX导致NiX 稳定性下降,且 4 可能与Ni2+形成络合物降低Ni2+
2
浓度。
【典例20】稀土是一种重要的战略资源,我国稀土出口量世界第一。铈(Ce)是一种典型的稀土元素,工业上利用某种含氟碳铈矿(主
要成分为CeFCO ,还含少量BaO,SiO 等)制取金属铈的一种工艺流程如图。回答下列问题:
3 2
已知:①硫酸体系中,Ce4+在 (HA) 中的溶解度大于其在水中的溶解度,Ce3+与之相反,Ce4+能与SO2−结合成[CeSO ]2+ ;
2 4 4
c (Ce)
D= 有机相
c (Ce)
②常温下,两相平衡体系中,被萃取物在有机层和水层中的物质的量浓度之比称为分配比(D),如 水相 ,Ce 的萃取率
学科网(北京)股份有限公司n (Ce)
E= 有机相 ×100%
n (Ce)
总
(3)步骤III萃取时存在反应Ce4+ +n(HA) � Ce⋅(H A )+4H+,萃取Ce4+最适宜的条件:温度为75~85℃,硫酸浓度为
2 2n−4 2n
2.5mol⋅L−1;当硫酸浓度过大时,萃取率降低的原因是 。
(4)步骤IV反萃取中,在稀硫酸和H O 的作用下Ce4+转化为Ce3+,反应的离子方程式为 。该步骤通常控制温度为40~50℃
2 2
的原因是 。
(5)某工厂取1000L含Ce4+
浓度为
50mg⋅L−1 的溶液,加入500L某萃取剂,若D=10,则单次萃取率E=
%(保留一位小数)。
若要提高萃取率,需优化的工艺条件为 (写一条即可)。
答:(3)随着硫酸根浓度增大,Ce4+
与硫酸根结合生成
[CeSO
4
]2+
,氢离子浓度增大,萃取平衡逆向移动
2Ce4+ +H O =2Ce2+ +2H+ +O ↑
(4) 2 2 2 有利于加快反应速率,还可以防止双氧水分解
(5)83.3 增大D(调节 pH 或更换萃取剂)、增大有机相体积或者多级萃取(合理即可)
分析:(3)随着硫酸根浓度增大,Ce4+
与硫酸根结合生成
[CeSO
4
]2+
,氢离子浓度增大,萃取平衡逆向移动,导致萃取率降低。(4)
步骤IV 加入 H 2 O 2,将Ce4+ 转化为Ce3+ 进入水层,发生反应的离子方程式为: 2Ce4+ +H 2 O 2 =2Ce3+ +O 2 ↑+2H+ 。过氧化氢受
热易分解,反应时控制温度为40−50℃
之间既有利于加快反应速率,又可以防止温度过高导致双氧水分解。 (5)根据题给公式整
D?V 10×500
E= 有机 ×100%= ×100%=83.3%
理得萃取率 D?V 有机 +V 水 10×500+1000 。若要提高萃取率,需优化的工艺条件为增大D(调节 pH
或更换萃取剂)、增大有机相体积或者多级萃取。
【典例21】钪(Sc)是一种在国防、航空航天、核能等领域具有重要作用的稀土元素。以钛白酸性废水(主要含TiO2+、Fe3+、Sc3+)
为原料制备Sc及TiO 的工艺流程如图所示。
2
K Fe(OH) =2.8×10-39,K Sc(OH) =1.0×10-30
已知:①25℃时,
sp
3
sp
3
c (Sc)
(5)常温下,两相平衡体系中,被萃取物在有机层和水层中的物质的量浓度之比称为分配比(D),D= 有机物 ,Sc的萃取率=
c (Sc)
水相
n (Sc)
有机物 ×100%。某工厂取1000L含Sc3+的废酸溶液,加入500L某有机萃取剂进行萃取,则单次萃取率为 (用含D的式子
n (Sc)
总
表示)。
学科网(北京)股份有限公司D
×100%
答:D+2
n (Sc) DV 500D D
有机物 ×100%= 有机物 ×100%= ×100%= ×100%
n (Sc) DV +1×V 500D+1000 D+2
分析:萃取率= 总 有机物 水 。
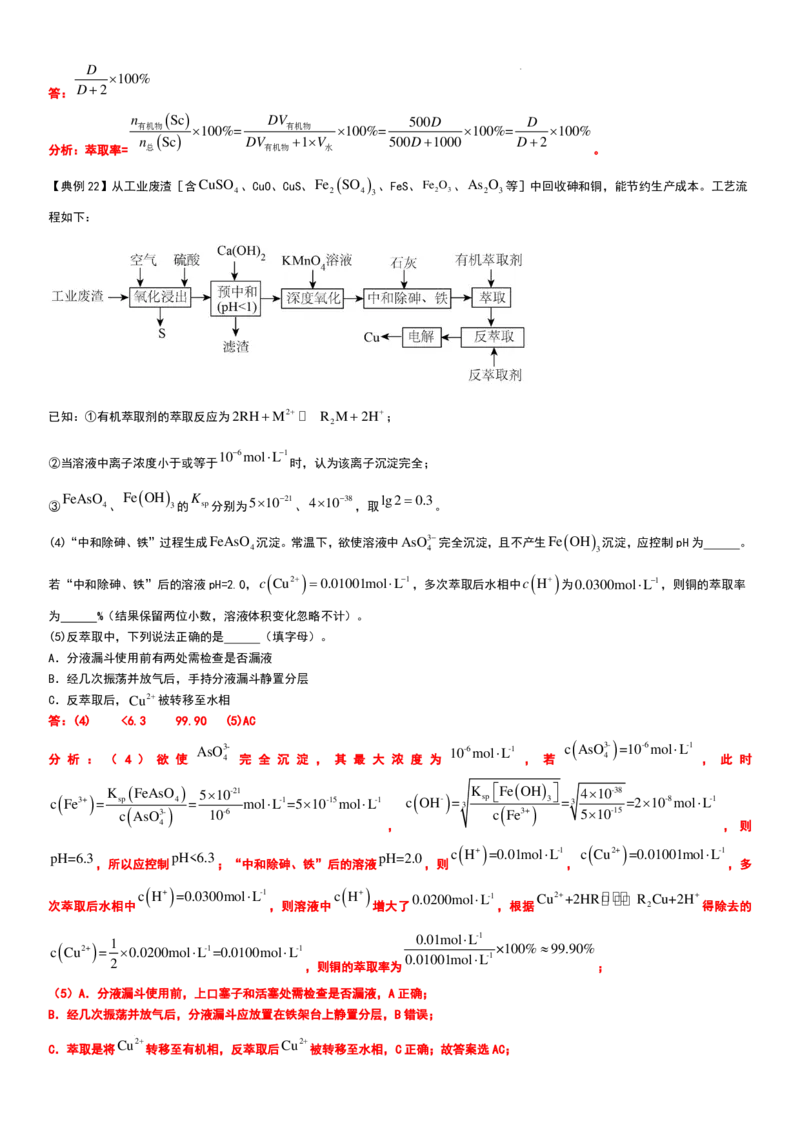
【典例22】从工业废渣[含CuSO 、CuO、CuS、Fe (SO ) 、FeS、Fe O 、As O 等]中回收砷和铜,能节约生产成本。工艺流
4 2 4 3 2 3 2 3
程如下:
已知:①有机萃取剂的萃取反应为2RH+M2+ � R M+2H+;
2
10−6mol⋅L−1
②当溶液中离子浓度小于或等于 时,认为该离子沉淀完全;
③
FeAsO
4、
Fe(OH)
3的
K sp分别为5×10−21 、4×10−38
,取
lg2=0.3
。
(4)“中和除砷、铁”过程生成FeAsO 沉淀。常温下,欲使溶液中AsO3−完全沉淀,且不产生Fe(OH) 沉淀,应控制pH为 。
4 4 3
若“中和除砷、铁”后的溶液pH=2.0,c ( Cu2+) =0.01001mol⋅L−1,多次萃取后水相中c ( H+) 为0.0300mol⋅L−1,则铜的萃取率
为 %(结果保留两位小数,溶液体积变化忽略不计)。
(5)反萃取中,下列说法正确的是 (填字母)。
A.分液漏斗使用前有两处需检查是否漏液
B.经几次振荡并放气后,手持分液漏斗静置分层
C.反萃取后,Cu2+被转移至水相
答:(4) <6.3 99.90 (5)AC
AsO3- 10-6mol⋅L-1 c ( AsO3-) =10-6mol⋅L-1
分 析 : ( 4 ) 欲 使 4 完 全 沉 淀 , 其 最 大 浓 度 为 , 若 4 , 此 时
c ( Fe3+) = K s
c
p
(
(
A
Fe
s
A
O
s
3-
O
)
4 ) = 5×
1
1
0
0
-6
-21 mol⋅L-1=5×10-15mol⋅L-1 c ( OH-) =3 K sp
c
F
( F
e
e
(O
3+
H
)
) 3 =3
5
4
×
×
1
1
0
0
-
-
1
3
5
8 =2×10-8mol⋅L-1
4 , , 则
pH=6.3 pH<6.3 pH=2.0 c ( H+) =0.01mol⋅L-1 c ( Cu2+) =0.01001mol⋅L-1
,所以应控制 ;“中和除砷、铁”后的溶液 ,则 , ,多
c ( H+) =0.0300mol⋅L-1 c ( H+) 0.0200mol⋅L-1 Cu2++2HR������ R Cu+2H+
次萃取后水相中 ,则溶液中 增大了 ,根据 2 得除去的
c ( Cu2+) = 1 ×0.0200mol⋅L-1=0.0100mol⋅L-1
0.01mol⋅L-1
×100%≈99.90%
2 ,则铜的萃取率为
0.01001mol⋅L-1
;
(5)A.分液漏斗使用前,上口塞子和活塞处需检查是否漏液,A正确;
B.经几次振荡并放气后,分液漏斗应放置在铁架台上静置分层,B错误;
C.萃取是将Cu2+ 转移至有机相,反萃取后Cu2+
被转移至水相,C正确;故答案选AC;
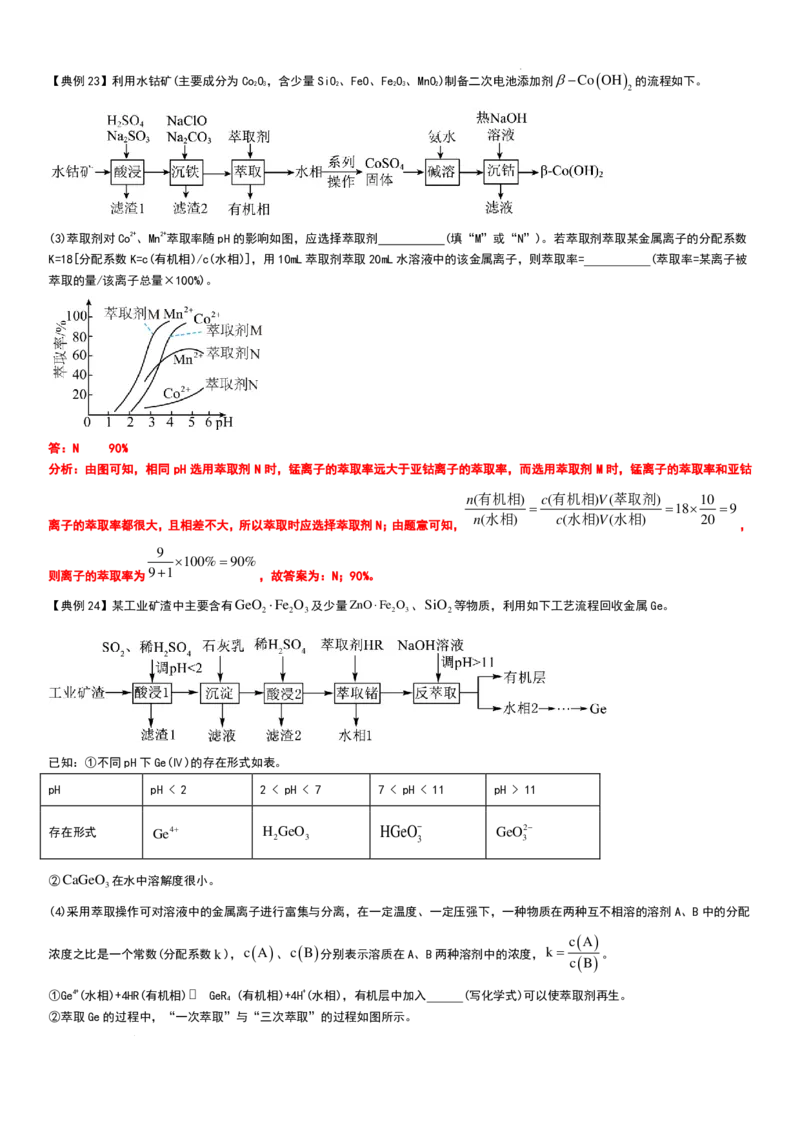
学科网(北京)股份有限公司【典例23】利用水钴矿(主要成分为CoO,含少量SiO、FeO、FeO、MnO)制备二次电池添加剂β−Co(OH)
的流程如下。
2 3 2 2 3 2 2
(3)萃取剂对Co2+、Mn2+萃取率随pH的影响如图,应选择萃取剂 (填“M”或“N”)。若萃取剂萃取某金属离子的分配系数
K=18[分配系数K=c(有机相)/c(水相)],用10mL萃取剂萃取20mL水溶液中的该金属离子,则萃取率= (萃取率=某离子被
萃取的量/该离子总量×100%)。
答:N 90%
分析:由图可知,相同pH选用萃取剂 N时,锰离子的萃取率远大于亚钴离子的萃取率,而选用萃取剂M时,锰离子的萃取率和亚钴
n(有机相) c(有机相)V(萃取剂) 10
= =18× =9
n(水相) c(水相)V(水相) 20
离子的萃取率都很大,且相差不大,所以萃取时应选择萃取剂N;由题意可知, ,
9
×100%=90%
则离子的萃取率为9+1 ,故答案为:N;90%。
【典例24】某工业矿渣中主要含有GeO ⋅Fe O 及少量ZnO⋅Fe O 、SiO 等物质,利用如下工艺流程回收金属Ge。
2 2 3 2 3 2
已知:①不同pH下Ge(Ⅳ)的存在形式如表。
pH pH < 2 2 < pH < 7 7 < pH < 11 pH > 11
存在形式 Ge4+ H GeO HGeO− GeO2−
2 3 3 3
②CaGeO 在水中溶解度很小。
3
(4)采用萃取操作可对溶液中的金属离子进行富集与分离,在一定温度、一定压强下,一种物质在两种互不相溶的溶剂A、B中的分配
c(A)
浓度之比是一个常数(分配系数k),c(A) 、c(B) 分别表示溶质在A、B两种溶剂中的浓度,k= 。
c(B)
①Ge4+(水相)+4HR(有机相)� GeR (有机相)+4H+(水相),有机层中加入 (写化学式)可以使萃取剂再生。
4
②萃取Ge的过程中,“一次萃取”与“三次萃取”的过程如图所示。
学科网(北京)股份有限公司n (X)
已知:萃取率有机相总= 有机相 ×100%,用20mL萃取剂萃取时每一次萃取率为60%。
n (X)
总
加入60mL萃取剂“一次萃取”时Ge的萃取率为 %(保留整数),有机相1比有机相2中Ge的残留率 (填“高”或“低”) %。
答: HSO 82 高 24
2 4
�
分析:①Ge4+(水相)+4HR(有机相) GeR (有机相)+4H+(水相),原来水相中就含有硫酸,为使萃取剂再生,可使平衡逆向移动,则有
4
机层中加入HSO 可以使萃取剂再生。
2 4
nmol×60%
②设100 mL含锗溶液中Ge的总物质的量为n mol,用20 mL萃取剂第一次萃取时萃取率是60%,有机相中c(Ge)= 0.02L =30n mol/L,
nmol×40% 30nmol/L
水相中c(Ge)= 0.1L =4n mol/L,则分配系数k= 4nmol/L =7.5。一次萃取中,设有机相中Ge的浓度为7.5 mol/L,则水相
60×7.5mol/L
×100%
中Ge的浓度为1 mol/L,加入60 mL萃取剂“一次萃取”时萃取率为60×7.5mol/L+100×1mol/L ≈82%。有机相1中Ge
的残留率为1-60%=40%,有机相2中Ge的残留率为40%(1-60%)=16%,故有机相1中Ge的残留率比有机相2中Ge的残留率高40%-16%=24%。
【典例25】以铟砷烟灰(含In O 、In S 、As O 、PbO等)为主要原料提取铟的流程如下:
2 3 2 3 2 3
已知:I.水相中含有强电解质FeS O 。
4 6
II.H A 在酸性溶液中只萃取三价金属离子,3H A +M3+ � M+(HA ) +3H+。
2 2 2 2 2 3
III.常温下,FeAsO 难溶于水,K
[
In(OH)
]=1.0×10−34。
4 sp 3
(3)反萃取后得到含[InCl ]− 的溶液,X的化学式为 。置换前需先中和再加入Zn粉,已知常温下反萃取后溶液中In3+的浓度
4
为0.0115g⋅L−1,则中和时可调节溶液pH的最大值为 。
答:HCl 4
3H A +M3+ � M+(HA ) +3H+
分析:根据信息 2 2 2 3 ,上述平衡逆向移动可提高铟的反萃取率,故需引入氢离子,为防止引入杂质,
则 X 的化学式为 HCl 。置换前需先中和再加入 Zn 粉,已知常温下反萃取后溶液中 In3+ 的浓度为 0.0115g⋅L−1 ,即
0.0115g⋅L−1 K [ In(OH) ]
=10−4mol⋅L−1 c(OH-)=
3
sp 3 =1.0×10−10
115g⋅mol−1 c(In3+) c(H+)=1.0×10−4 pH
, ,则 ,故中和时可调节溶液 的最大值
学科网(北京)股份有限公司为4。
【典例26】废弃电池电极材料的再利用可缓解全球对锂、钴等重要金属的供需矛盾。以废钴酸锂正极材料(主要含LiCoO 和Al)和
2
废磷酸亚铁锂正极材料(主要含LiFePO 和Al)为原料联合提取钴和锂的一种流程示意图如下:
4
(4)萃取过程中使用的P507用HR表示,发生萃取的反应可表示为Co2+ +2HR CoR +2H+。
2
①若滤液F中c
( Co2+)
=0.011mol/L,多次萃取后水相c
( H+)
=0.036mol/L,则Co的萃取率为 (保留两位有效数字,
10−1.8 ≈0.016)。
②为回收Co,可用一定浓度的硫酸将有机相中的Co反萃取到水相中,其原理是 。
答: 91% 加入硫酸,
c(H+)
增大,使萃取反应
Co2++2HR � CoR
2
+2H+
平衡逆向移动,
CoR 2转化为Co2+
进入水相;
分 析 : 已 知 滤 液 F 的
PH≈1.8
, 滤 液 F 中 的
c(H+)=10-1.8mol/L≈0.016mol/L
, 则 生 成 的
c(H+) =(0.036-0.016)mol/L=0.020mol/L Co2++2HR � CoR +2H+
生成 , 由 萃 取 反 应 2 , 消 耗
1 0.020mol/L 0.010
c(Co2+)= c(H+) = =0.010mol/L η= ×100%≈91%
2
生成
2 ,萃取率 0.011 ;加入硫酸,
c(H+)
增大,使萃取反应
Co2++2HR � CoR
2
+2H+
平衡逆向移动,
CoR 2转化为Co2+
进入水相。
学科网(北京)股份有限公司