文档内容
化学参考答案
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
题号 1 2 3 4 5 6 7
答案 D B B C B A C
题号 8 9 10 11 12 13 14
答案 B D C C D D C
【解析】
1.P O 有强烈的吸水性和腐蚀性,不能用作食品干燥,A错误。SiO 不具有导电性,B错误。
2 5 2
碳纤维是一种碳单质,不是有机高分子材料,C错误。用过碳酸钠漂白衣物,是利用Na CO
2 4
的强氧化性,D正确。
2.中子数为 18 的氯原子为35Cl,A错误。2−丁炔的键线式为 ,B正确。NF 的价层电
17 3
子对为4,VSEPR模型为四面体形,C错误。H PO 为三元弱酸,在水溶液中分步电离,电
3 4
离方程式分步书写,D错误。
3.NH 中含有3个N—H键,NH 与Ag+间有2个配位键,因此1mol [Ag(NH ) ]+中含σ键
3 3 3 2
数目为8N ,A 错误。0.5mol XeF 中氙的价层电子对数为3N ,B 正确。Na Cr O 溶液
A 4 A 2 2 7
存在平衡状态CrO2 H O 2CrO2 2H,0.1molL1Na CrO 溶液中含Cr元素微
2 7 2 4 2 2 7
粒浓度之和介于0.1mol·L−1~0.2mol·L−1,C错误。Li与O 反应生成Li O,1.4g Li与足
2 2
量O 充分反应,转移的电子数为0.2N ,D错误。
2 A
4.使甲基橙呈红色的溶液显酸性,同时存在 NO ,与I−不共存,A错误。由水电离的
3
c(H+)1×10−13mol/L的溶液可能显酸性或碱性,HCO不能共存,B错误。澄清透明溶液中:
3
NH、K+、MnO、SO2能大量共存,C正确。遇苯酚变紫的溶液中含Fe3+,与CO2发生
4 4 4 3
完全双水解而不共存,D错误。
5.CCl 不能与氢氧化钠溶液反应,溴能与氢氧化钠溶液反应生成溴化钠、次溴酸钠和水,但
4
CCl 密度比水大,应在下层,A错误。乙酸乙酯的收集用饱和碳酸钠溶液,能降低其溶解
4
度,B 正确。氨气极易溶于水,则题给装置不能达到用排水法测量氨气体积的实验目的,
C 错误。CH 和 Cl 的取代反应需在光照条件下进行,用铝箔套遮光后,反应不发生,无
4 2
油状液滴,D错误。
化学参考答案·第1页(共6页)6.侯氏制碱法:NaCl+NH +CO +H O=NaHCO ↓+NH Cl,碳酸氢钠受热分解制得纯碱碳
3 2 2 3 4
酸钠,A正确。制备金属镁需要电解熔融氯化镁,B错误。硫在足量氧气中燃烧也只能生成
SO ,C错误。NO和H O不能直接反应生成HNO ,D错误。
2 2 3
7.“乙→丙”羟基氧化成了羰基,发生了氧化反应,A错误。香茅醛中碳碳双键和醛基都能
使溴水褪色,B错误。一个甲分子中有4个手性碳 ,C正确。香茅醛中有醛基,醛基中的
氧原子可以和其他的—OH等的氢原子之间形成氢键,但不能形成分子内氢键,D错误。
8.根据题目所给信息:X、Y、Z、M、Q原子序数依次增大,M、Q的价电子数相等以及在化
合物中成键情况,可推出几种元素依次为H、C、N、O、S。第ⅤA、ⅥA族元素的第一电
离能存在反常:N>O,A错误。相对分子量:H O>NH >CH ,且H O和NH 存在分子
2 3 4 2 3
间氢键,故沸点:H O>NH >CH ,B正确。NO的空间结构为平面三角形,而SO2为三
2 3 4 3 3
角锥形,C错误。除H外,S也不满足8电子稳定结构,D错误。
9.H H H H ,A 错误。Ca2+的半径比 Mg2+大,则 CaCO 电离时需要的能量比
1 2 3 3
MgCO 小,且电离过程是吸热过程,则ΔH (MgCO )>ΔH (CaCO )>0,B错误。MgCO 和
3 1 3 1 3 3
CaCO 中CO2(g)=O2−(g)+CO (g)所需要的能量相等,则ΔH (MgCO )=ΔH (CaCO )>0,
3 3 2 2 3 2 3
C 错误。电离和断裂化学键是吸热过程,则 ΔH +ΔH >0,形成化学键是放热过程,ΔH <
1 2 3
<0,则ΔH +ΔH >ΔH ,D正确。
1 2 3
10. Na+的配位数即离Na+最近的且等距离的BH个数,由晶胞示意图可知,Na+的配位数是8,
4
A正确。B最外层有3个单电子,与3个氢原子形成3个普通共价键,另提供一个空轨道
与H−形成 1 个配位键,B正确。已知硼氢化钠晶体的密度为ρ g·cm−3,N 代表阿伏加德
A
罗常数的值,由晶胞示意图可知,每个晶胞的体积为a2×2a×10−21cm3=2a3×10−21cm3,一个
1 1 1 1
晶胞中含有Na+个数为4 6 4,含有BH个数为8 4 14,则一个晶胞
4 2 4 8 2
438
g
438 m N 76
的 质 量 为 g , 故 有 A 1021gcm3 , 即 得
N V 2a31021cm3 N a3
A A
3 76
a 107nm ,而Na+与 BH 之间的最近距离为底面对角线的一半,故为
N 4
A
2 3 76
107nm, C错误。若该晶胞四个棱心处的Na+被K+取代,得到晶体中一个晶
2 N
A
化学参考答案·第2页(共6页)1 1 1 1
胞中含有Na+个数为6 3,含有BH个数为8 4 14,K+数目为4 1,
2 4 8 2 4
该晶体的化学式为KNa (BH ) ,D正确。
3 4 4
11.等物质的量的 FeBr 和 Cl 反应,Fe2+先被氧化,剩余 Cl 与 Br−反应生成 Br ,无法验证
2 2 2 2
还原性 Br−>Fe2+,A 错误。一种沉淀易转化为比它更难溶的沉淀,向 BaSO 固体中加入
4
过量饱和Na CO 溶液有BaCO 生成,不能证明K (BaSO )②,D正确。
化学参考答案·第3页(共6页)K Co(OH) K Co(OH) c2(H+)
14.常温下,pColg sp 2 lg sp 2 2pHlgK Co(OH) 28、
c2(OH) K2 sp 2
w
K Pb(OH) K Pb(OH) c2(H+)
pPblg sp 2 lg sp 2 2pHlgK Pb(OH) 28 , 由 于
c2(OH) K2 sp 2
w
K Co(OH) K Pb(OH) 可知,X代表lgc(Pb2+)与 pH 的关系,Y代表lgc(Co2+)与
sp 2 sp 2
c(R)
pH 的 关 系 , Z 代 表 lg 与 pH 的 关 系 , A 正 确 。
c(HR)
c(R) K(HR)
lg lg pHlgK(HR),取Z中点(5,0)带入得,K(HR)1105,
c(HR) c(H+)
K c(R)
K W 1109 ,B 正确。a 点存在关系 c(Pb2) ,两边同乘 c(H) 得
h K c(HR)
HR
c(R)
c(H) c(Pb2)c(H) ; 即 K(HR)c(Pb2)c(H) , 再 两 边 同 乘 c2(OH) 得
c(HR)
c2(OH)K(HR)c(Pb2)c2(OH)c(H);即c2(OH)K(HR)K [Pb(OH )]c(H);再两边
sp 2
同乘c(OH)得c3(OH)K(HR)K [Pb(OH) ]K ,代入B,C数据可求得c3(OH)1029,
sp 2 w
解 得 pH4.33 , C 错 误 。 X 代 表 lgc(Pb2) 与 pH 的 关 系 ,
pPb2pHlgK [Pb(OH) ]28,取 X 中点(10,12)带入得K [Pb(OH) ]11020,
sp 2 sp 2
Y代表lgc(Co2)与 pH 的关系,pCo2pHlgK [Co(OH) ]28,取Y中点(10,7)
sp 2
带 入 得 K [Co(OH) ]11015 , 常 温 下 , Co(OH) 和 Pb(OH) 共 存 时 :
sp 2 2 2
c(Pb2)∶c(Co2)K Pb(OH) ∶K Co(OH) 1∶105,D正确。
sp 2 sp 2
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空2分,共14分)
(1)粉碎铝钴膜、适当提高NaOH溶液的浓度、适当升高浸取温度(1分,合理即可)
(2) 正四面体形(1分)
(3)2LiCoO +H O +3H SO =Li SO +2CoSO +4H O+O ↑
2 2 2 2 4 2 4 4 2 2
(4)2.4×10−9mol·L−1
(5)焰色试验
煅烧
(6)4Co O +6Li CO +O =====12LiCoO +6CO
3 4 2 3 2 2 2
(7)Co O
2 3
化学参考答案·第4页(共6页)【解析】(4)当 Co2+恰好沉淀完全时,溶液中剩余 Co2+浓度为 1×10−5mol·L−1。根据
c(C O2)c2(H)
K (CoC O )可求得溶液中c(C O2)=6×10−3 mol·L−1。由于 2 4 =K ×K ,所
sp 2 4 2 4 c(H C O ) a1 a2
2 2 4
以c(H C O )2.4109molL1。
2 2 4
5.9 2.4
(7)C点时剩余Co的质量为5.9g,剩余O的质量为2.4g,所以n(Co)∶n(O)= ∶ =2∶
59 16
3,所以剩余固体的化学式为Co O 。
2 3
16.(除特殊标注外,每空2分,共14分)
(1)球形冷凝管(1分) 冷凝、回流、平衡气压
(2)在球形冷凝管上增加一个干燥装置
(3)分液漏斗、烧杯
(4)重结晶(1分)
(5)取最后一次洗涤液,加入硝酸酸化的硝酸银,无明显现象则洗净
(6)BD
(7)69.11%
【解析】(2)由于AlCl 容易与水反应,反应过程中防止空气中的水蒸气进入三颈烧瓶中,
3
降低产率。
(4)固体粗品分离提纯的方法为重结晶。
(5)晶体洗涤过程中,除去晶体表面的HCl,证明是否洗净,主要检验Cl−的存在。
(6)A项,毛细管的作用是防止暴沸。B项,减压蒸馏是降低物质的沸点。C项,实验结
束时,先打开止水夹G,使瓶内压强与大气压强相等,再关闭水泵电源。D项,固体颗粒
不能通过滤纸。
123.7
(7)产率= 100%69.11%。
179
17.(除特殊标注外,每空2分,共15分)
K2 K
(1)①低温(1分) 1 3 ②BC
K2
2
(2)T 2∶1
(3)①C ②C H −12e−+4H O=2CO +12H+ 36
2 4 2 2
化学参考答案·第5页(共6页)【解析】(1)①该反应H<0,S<0,根据G=H−T·S<0可知,该反应低温下
可以自发进行。
②A项,该反应是得氧的氧化反应,且生成物只有环氧乙烷,所以原子利用率为100%。B
项,移出环氧乙烷可以提高产率,但是生成物浓度减小,反应速率减小。C项,恒温恒容
条件下,充入氩气,反应物浓度不变,平衡不移动,乙烯的转化率不变。D项,银单质作
为催化剂,可以提高单位体积内活化分子百分数。
(2)根据反应过程图示,物质T为催化剂。为了生成等物质的量的E和G,需要提供2份A,
生成2份物质B,将生成的物质B均分后,一份与物质C反应,最后生成1份物质F与1份
物质B反应生成1份物质G。
(3)①工业生成短链烃类物质选用裂解的化学工艺。②根据化合价变化可以判断装置左边
电极为负极,其电极反应为C H −12e−+4H O=2CO +12H+。若消耗5.6g乙烯气体,转
2 4 2 2
移 2.4mol e−。负极室减少的质量 m =0.2×2×44−5.6+2.4×1=14.4g,正极室增加的质量
1
m =32×0.6+2.4×1=21.6g,所以|m m |7.2g。
1 1 2
18.(除特殊标注外,每空2分,共15分)
(1)氯乙烯 醚键、酰胺基(答对1个得1分)
(2)sp2、sp(答对1个得1分) 加成反应(1分)
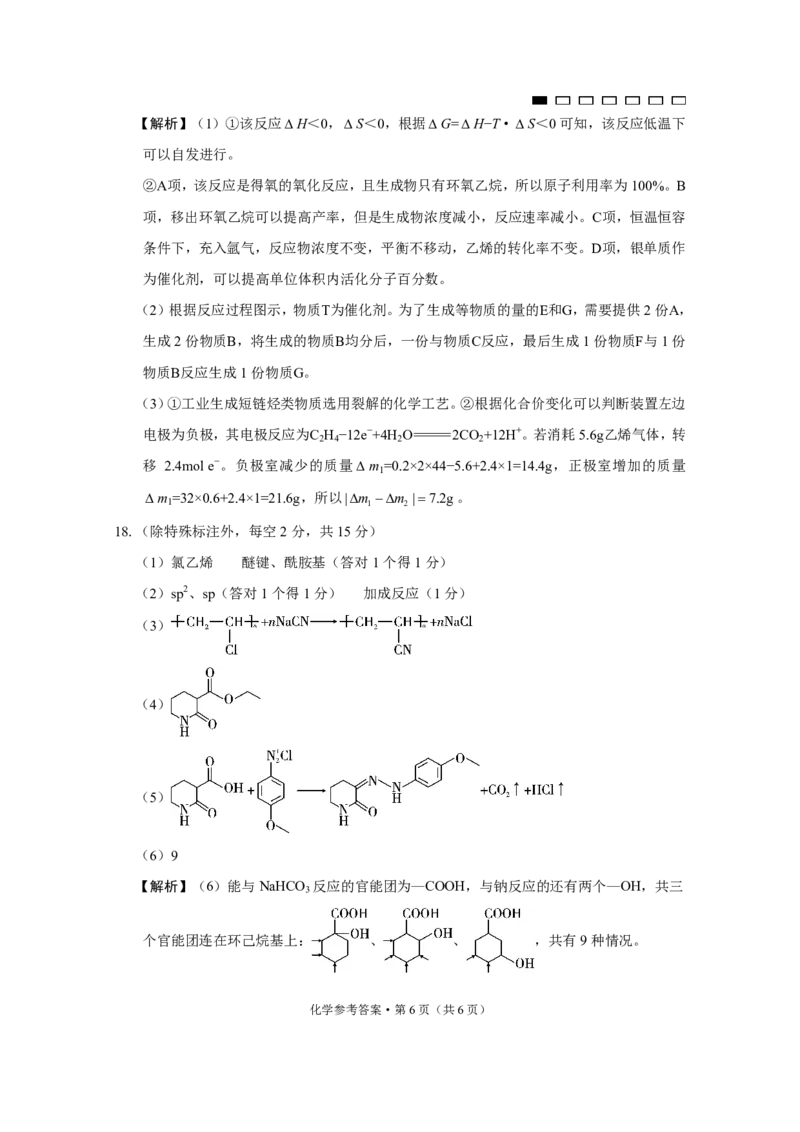
(3)
(4)
(5)
(6)9
【解析】(6)能与NaHCO 反应的官能团为—COOH,与钠反应的还有两个—OH,共三
3
个官能团连在环己烷基上: 、 、 ,共有9种情况。
化学参考答案·第6页(共6页)