文档内容
遂宁市高中 2026 届高三一诊考试
化 学 试 题
本试卷分第I卷(选择题)和第II卷(非选择题)两部分。总分100分。考试时间75分
钟。
注意事项:
1.答题前,考生务必将自己的姓名、班级、考号用0.5毫米的黑色墨水签字笔填写在答题卡上。并检查条形码粘贴是否
正确。
2.选择题使用2B铅笔填涂在答题卡对应题目标号的位置上,非选择题用0.5毫米黑色墨水签字笔书写在答题卡对应
框内,超出答题区域书写的答案无效;在草稿纸、试题卷上答题无效。
3.考试结束后,将答题卡收回。
可能用到的相对原子质量: H—1 N—14 Cl—35.5 Cr—52
第Ⅰ卷
(选择题,满分45分)
一、单选题(共45分,每题3分)
1.化学是美好生活的催化剂,衣食住行皆化学,下列说法正确的是
A.我国研制的超级钢具有优异的强度和延展性,其中含碳量大于生铁中的含碳量
B.低压法聚乙烯支链较多,无毒,较柔软,常用于生产食品包装袋等
C.苏打属于大宗化学品,可用作食用碱
D.冰敷袋中的主要成分为硝酸铵和水合碳酸钠,主要是借助其物理变化中的吸热来实现降温、
保鲜等用途
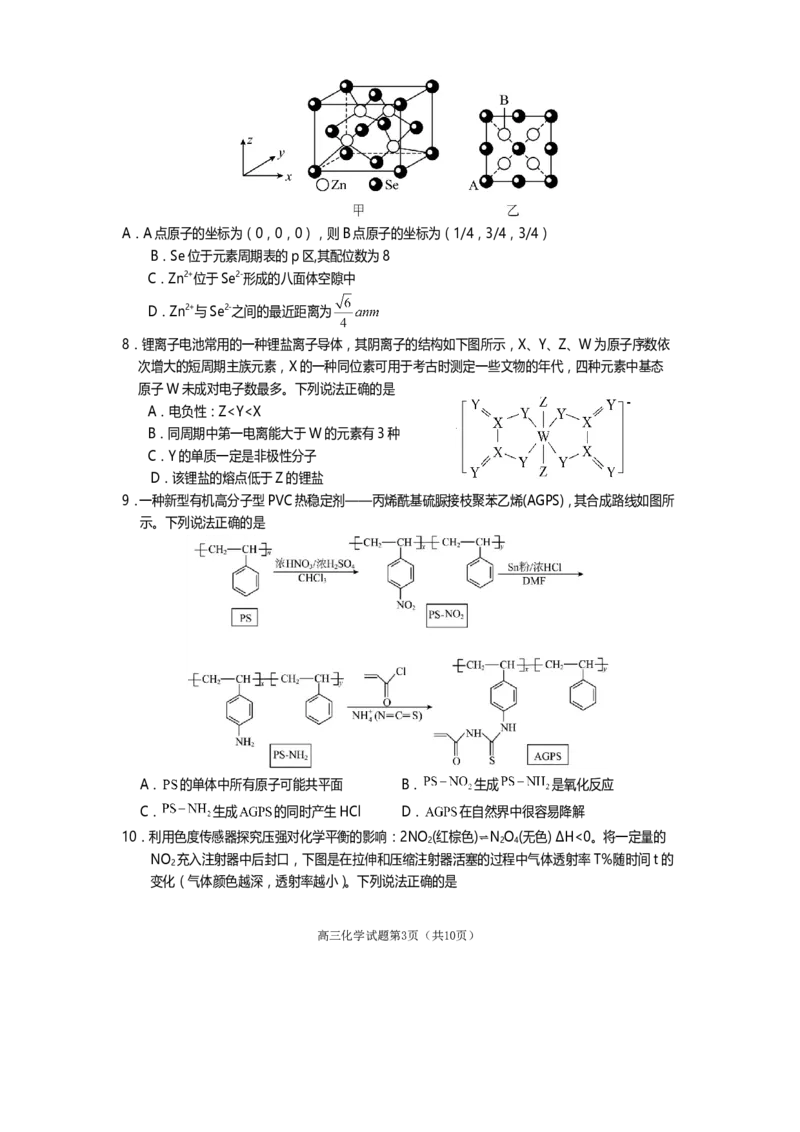
2.下列化学用语或图示错误的是
A.用电子云轮廓图示意 键的形成:
B.sp2杂化轨道示意图:
C.用电子式表示 的形成过程:
D.SO 的VSEPR模型:
2
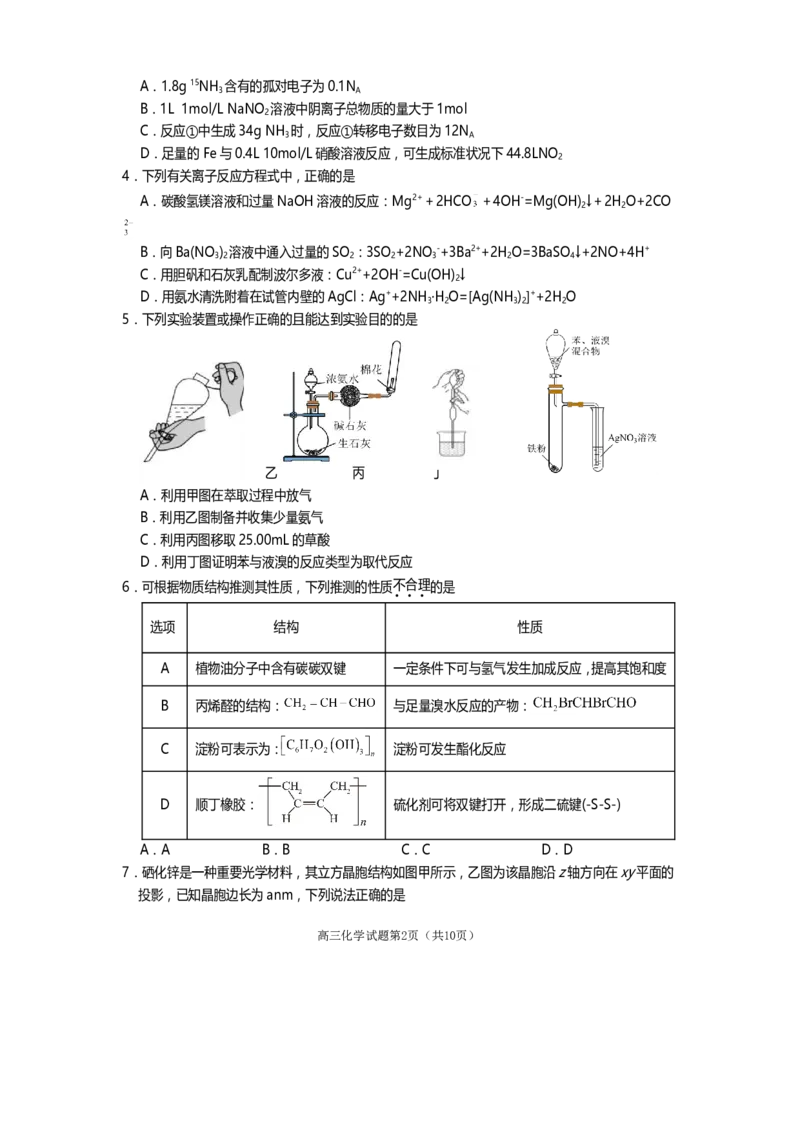
3.发蓝工艺是将钢铁浸入热的NaNO 碱性
2
溶液中,在其表面形成一层四氧化三铁
薄膜,其中铁经历了如图所示的转化(假
设NaNO 的还原产物均为NH ),下列说
2 3
法错误的是(设N 为阿伏伽德罗常数)
A
高三化学试题第1页(共10页)A.1.8g 15NH 含有的孤对电子为0.1N
3 A
B.1L 1mol/L NaNO 溶液中阴离子总物质的量大于1mol
2
C.反应①中生成34g NH 时,反应①转移电子数目为12N
3 A
D.足量的 Fe与0.4L 10mol/L硝酸溶液反应,可生成标准状况下44.8LNO
2
4.下列有关离子反应方程式中,正确的是
A.碳酸氢镁溶液和过量NaOH溶液的反应:Mg2++2HCO +4OH-=Mg(OH) ↓+2H O+2CO
2 2
B.向Ba(NO ) 溶液中通入过量的SO :3SO +2NO -+3Ba2++2H O=3BaSO ↓+2NO+4H+
3 2 2 2 3 2 4
C.用胆矾和石灰乳配制波尔多液:Cu2++2OH-=Cu(OH) ↓
2
D.用氨水清洗附着在试管内壁的AgCl:Ag++2NH ·H O=[Ag(NH ) ]++2H O
3 2 3 2 2
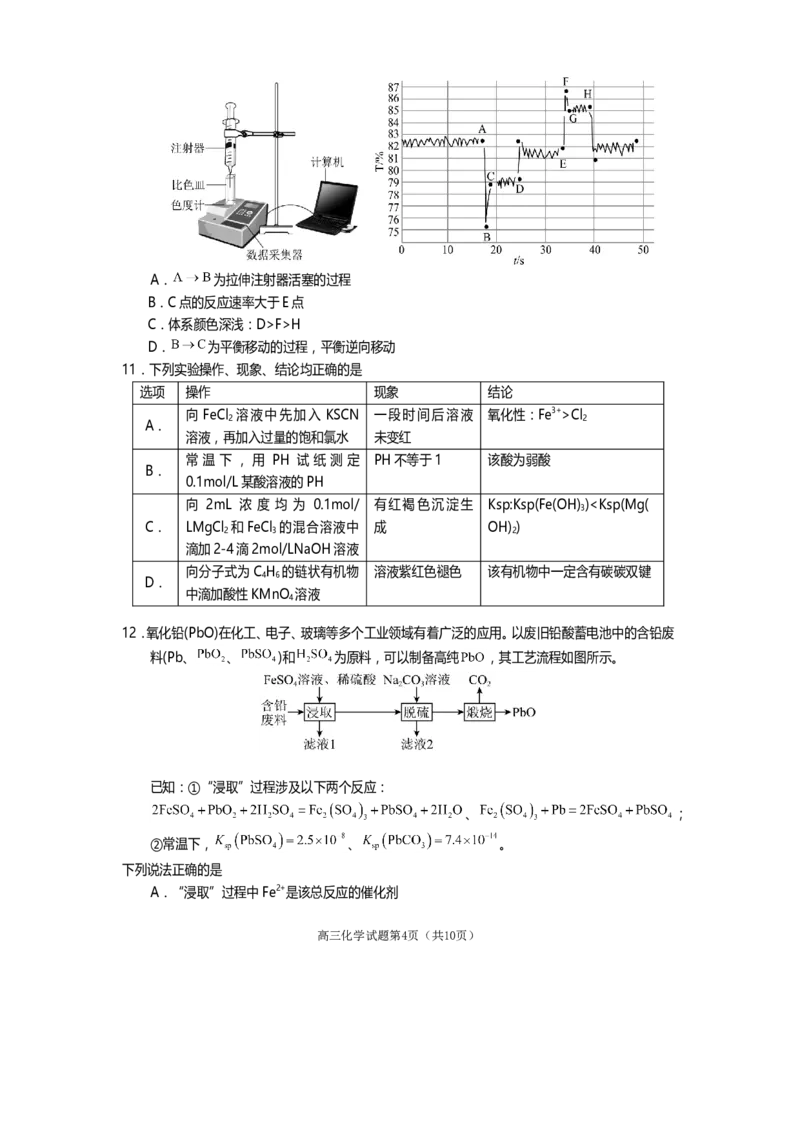
5.下列实验装置或操作正确的且能达到实验目的的是
甲 乙 丙 丁
A.利用甲图在萃取过程中放气
B.利用乙图制备并收集少量氨气
C.利用丙图移取25.00mL的草酸
D.利用丁图证明苯与液溴的反应类型为取代反应
6.可根据物质结构推测其性质,下列推测的性质不合理的是
选项 结构 性质
A 植物油分子中含有碳碳双键 一定条件下可与氢气发生加成反应,提高其饱和度
B 丙烯醛的结构: 与足量溴水反应的产物:
C 淀粉可表示为: 淀粉可发生酯化反应
D 顺丁橡胶: 硫化剂可将双键打开,形成二硫键(-S-S-)
A.A B.B C.C D.D
7.硒化锌是一种重要光学材料,其立方晶胞结构如图甲所示,乙图为该晶胞沿z轴方向在xy平面的
投影,已知晶胞边长为anm,下列说法正确的是
高三化学试题第2页(共10页)A.A点原子的坐标为(0,0,0),则B点原子的坐标为(1/4,3/4,3/4)
B.Se位于元素周期表的p区,其配位数为8
C.Zn2+位于Se2-形成的八面体空隙中
D.Zn2+与Se2-之间的最近距离为
8.锂离子电池常用的一种锂盐离子导体,其阴离子的结构如下图所示,X、Y、Z、W为原子序数依
次增大的短周期主族元素,X的一种同位素可用于考古时测定一些文物的年代,四种元素中基态
原子W未成对电子数最多。下列说法正确的是
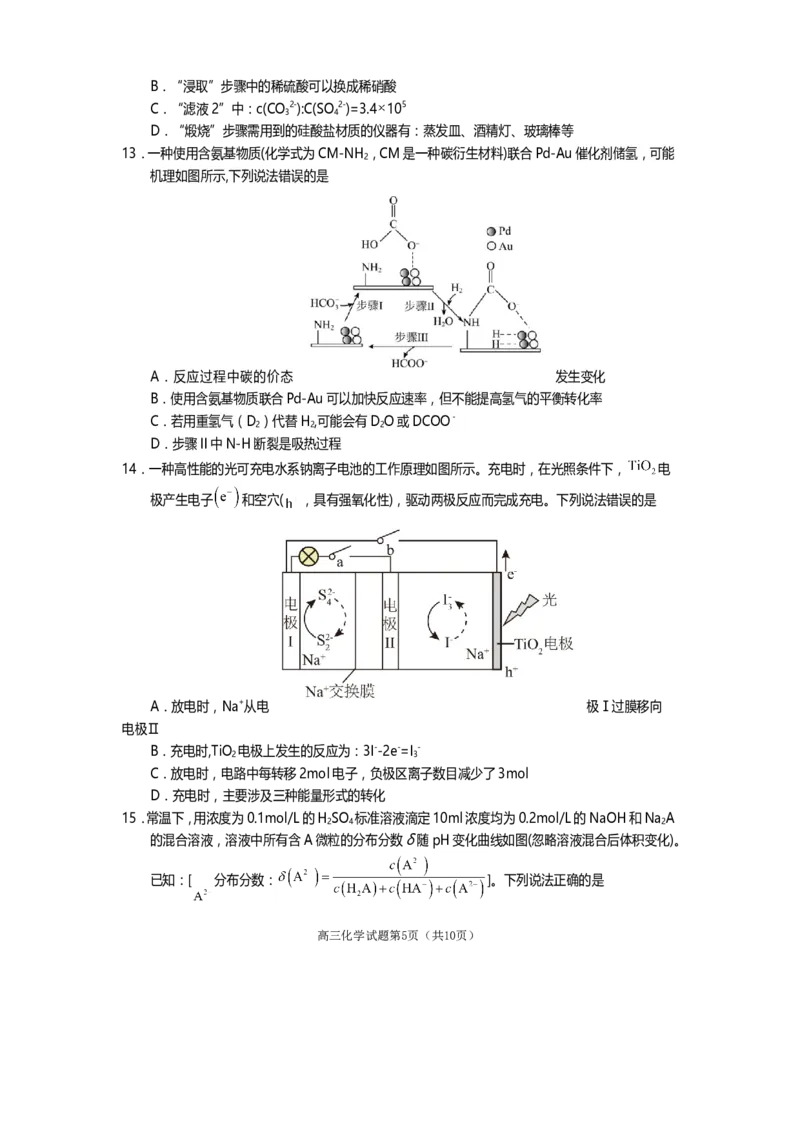
A.电负性:ZF>H
D. 为平衡移动的过程,平衡逆向移动
11.下列实验操作、现象、结论均正确的是
选项 操作 现象 结论
向 FeCl 溶液中先加入 KSCN 一段时间后溶液 氧化性:Fe3+>Cl
2 2
A.
溶液,再加入过量的饱和氯水 未变红
常 温 下 , 用 PH 试 纸 测 定 PH不等于1 该酸为弱酸
B.
0.1mol/L某酸溶液的PH
向 2mL 浓 度 均 为 0.1mol/ 有红褐色沉淀生 Ksp:Ksp(Fe(OH) )0.2mol/L
第Ⅱ卷
(非选择题,共55分)
注意事项:
1.请用蓝黑钢笔或圆珠笔在第Ⅱ卷答题卡上作答,不能答在此试卷上。
2.试卷中横线及框内注有“▲”的地方,是需要你在第Ⅱ卷答题卡上作答。
二、非选择题(本题共4题,共55分)
16.(14分)某研究小组以 为原料探究制备无水 并进一步制备新型CrN电子陶瓷的流程
如下。
已知:① 熔点为83℃,易潮解,易升华,高温下易被 氧化。
②光气( )沸点为8.2℃,有毒,易水解; 沸点为76.8℃;CrN熔点为1650℃。
回答下列问题:
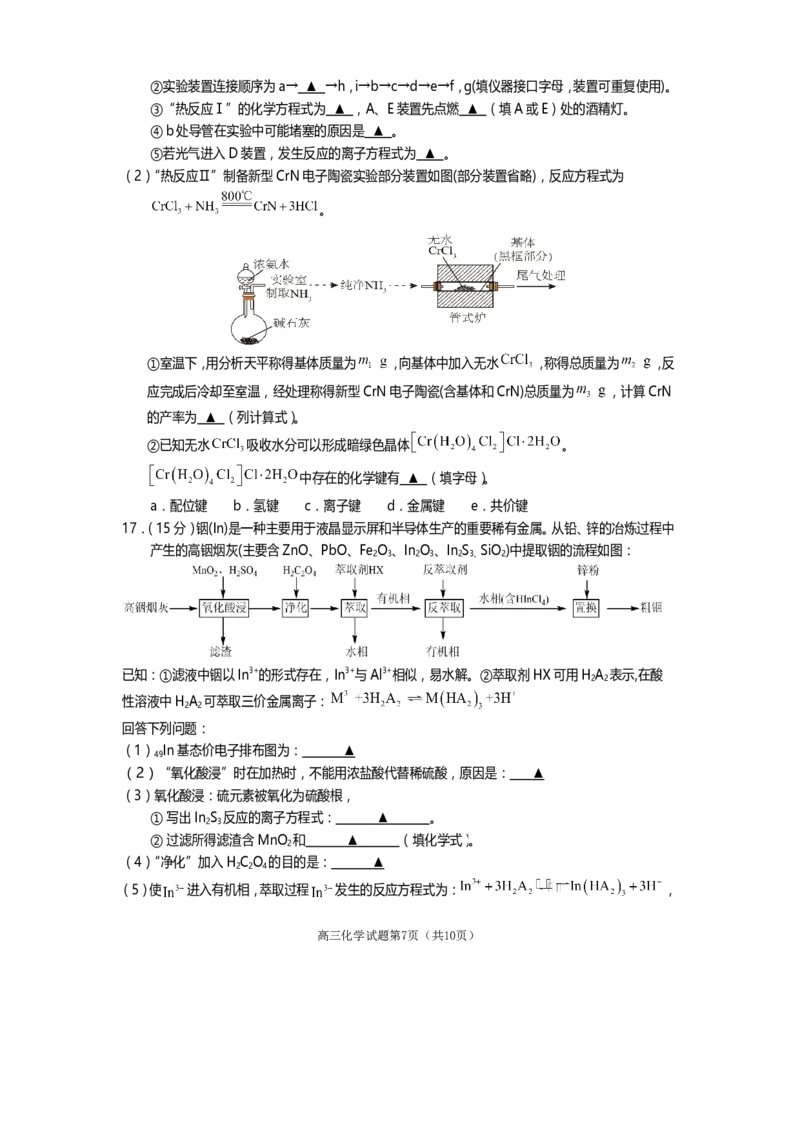
(1)“热反应Ⅰ”制备无水 的实验装置如图(夹持及A、E、F中加热装置省略)。
①A装置用于制取 ,反应时需通 的目的是 ▲ 。
高三化学试题第6页(共10页)②实验装置连接顺序为a→ ▲ →h,i→b→c→d→e→f,g(填仪器接口字母,装置可重复使用)。
③“热反应Ⅰ”的化学方程式为 ▲ ,A、E装置先点燃 ▲ (填A或E)处的酒精灯。
④b处导管在实验中可能堵塞的原因是 ▲ 。
⑤若光气进入D装置,发生反应的离子方程式为 ▲ 。
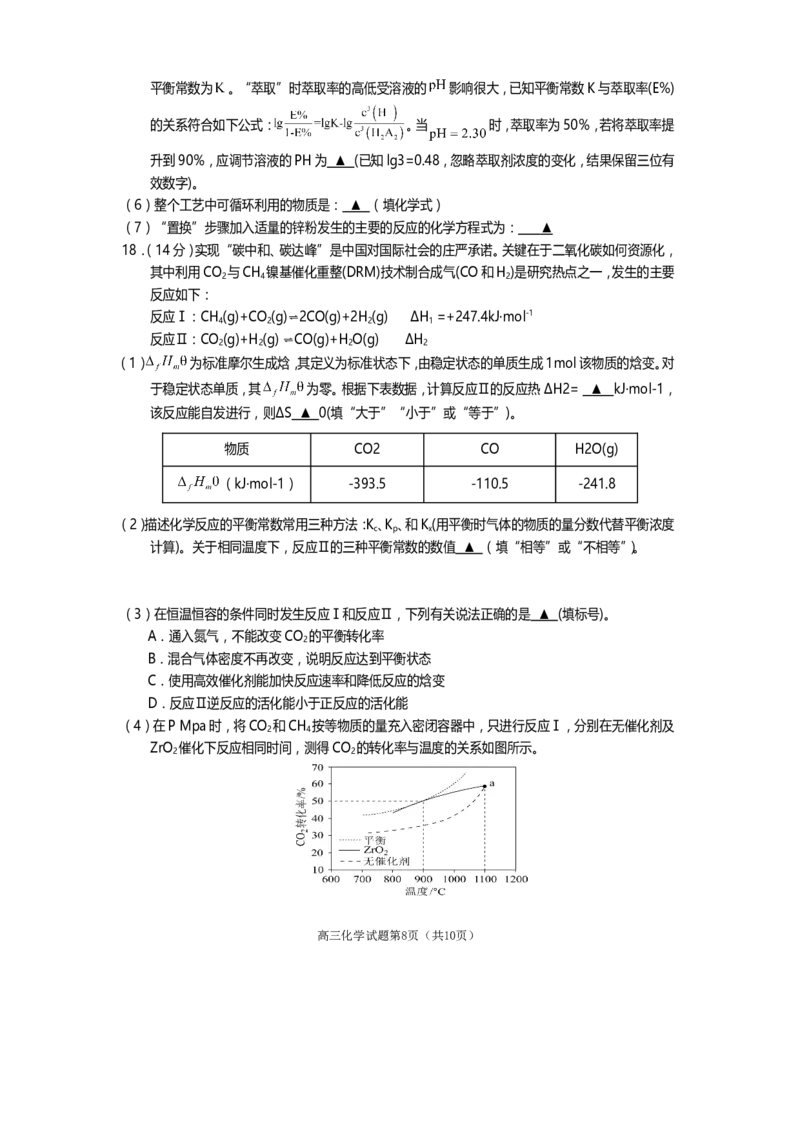
(2)“热反应Ⅱ”制备新型CrN电子陶瓷实验部分装置如图(部分装置省略),反应方程式为
。
①室温下,用分析天平称得基体质量为 ,向基体中加入无水 ,称得总质量为 ,反
应完成后冷却至室温,经处理称得新型CrN电子陶瓷(含基体和CrN)总质量为 ,计算CrN
的产率为 ▲ (列计算式)。
②已知无水 吸收水分可以形成暗绿色晶体 。
中存在的化学键有 ▲ (填字母)。
a.配位键 b.氢键 c.离子键 d.金属键 e.共价键
17.(15分)铟(In)是一种主要用于液晶显示屏和半导体生产的重要稀有金属。从铅、锌的冶炼过程中
产生的高铟烟灰(主要含ZnO、PbO、Fe O 、In O 、In S SiO )中提取铟的流程如图:
2 3 2 3 2 3、 2
已知:①滤液中铟以In3+的形式存在,In3+与Al3+相似,易水解。②萃取剂HX可用H A 表示,在酸
2 2
性溶液中H A 可萃取三价金属离子:
2 2
回答下列问题:
(1) In基态价电子排布图为: ▲
49
(2)“氧化酸浸”时在加热时,不能用浓盐酸代替稀硫酸,原因是: ▲
(3)氧化酸浸:硫元素被氧化为硫酸根,
① 写出In S 反应的离子方程式: ▲ 。
2 3
② 过滤所得滤渣含MnO 和 ▲ (填化学式)。
2
(4)“净化”加入H C O 的目的是: ▲
2 2 4
(5)使 进入有机相,萃取过程 发生的反应方程式为: ,
高三化学试题第7页(共10页)平衡常数为 。“萃取”时萃取率的高低受溶液的 影响很大,已知平衡常数K与萃取率(E%)
的关系符合如下公式: 。当 时,萃取率为50%,若将萃取率提
升到90%,应调节溶液的PH为 ▲ (已知lg3=0.48,忽略萃取剂浓度的变化,结果保留三位有
效数字)。
(6)整个工艺中可循环利用的物质是: ▲ (填化学式)
(7)“置换”步骤加入适量的锌粉发生的主要的反应的化学方程式为: ▲
18.(14分)实现“碳中和、碳达峰”是中国对国际社会的庄严承诺。关键在于二氧化碳如何资源化,
其中利用CO 与CH 镍基催化重整(DRM)技术制合成气(CO和H )是研究热点之一,发生的主要
2 4 2
反应如下:
反应Ⅰ:CH
4
(g)+CO
2
(g)⇌2CO(g)+2H
2
(g) ∆H
1
=+247.4kJ·mol-1
反应Ⅱ:CO
2
(g)+H
2
(g) ⇌CO(g)+H
2
O(g) ∆H
2
(1) 为标准摩尔生成焓,其定义为标准状态下,由稳定状态的单质生成1mol该物质的焓变。对
于稳定状态单质,其 为零。根据下表数据,计算反应Ⅱ的反应热 ∆H2= ▲ kJ·mol-1,
该反应能自发进行,则∆S ▲ 0(填“大于”“小于”或“等于”)。
物质 CO2 CO H2O(g)
(kJ·mol-1) -393.5 -110.5 -241.8
(2)描述化学反应的平衡常数常用三种方法:K、K 、和K(用平衡时气体的物质的量分数代替平衡浓度
c p x
计算)。关于相同温度下,反应Ⅱ的三种平衡常数的数值 ▲ (填“相等”或“不相等”)。
(3)在恒温恒容的条件同时发生反应Ⅰ和反应Ⅱ,下列有关说法正确的是 ▲ (填标号)。
A.通入氮气,不能改变CO 的平衡转化率
2
B.混合气体密度不再改变,说明反应达到平衡状态
C.使用高效催化剂能加快反应速率和降低反应的焓变
D.反应Ⅱ逆反应的活化能小于正反应的活化能
(4)在P Mpa时,将CO 和CH 按等物质的量充入密闭容器中,只进行反应Ⅰ,分别在无催化剂及
2 4
ZrO 催化下反应相同时间,测得CO 的转化率与温度的关系如图所示。
2 2
高三化学试题第8页(共10页)①a点时有催化剂和无催化剂的CO 转化率相等的原因是 ▲ 。
2
②在P MPa、900℃、ZrO 催化条件下,将CO 、CH 、Ar按物质的量之比1:1:2充入密闭容器,
2 2 4
CO 的平衡转化率ɑ大于50%,解释说明原因: ▲ ,此时平衡常数
2
Kp= ▲ (以各气体的分压代替浓度计算;列出含ɑ、p的计算式)。
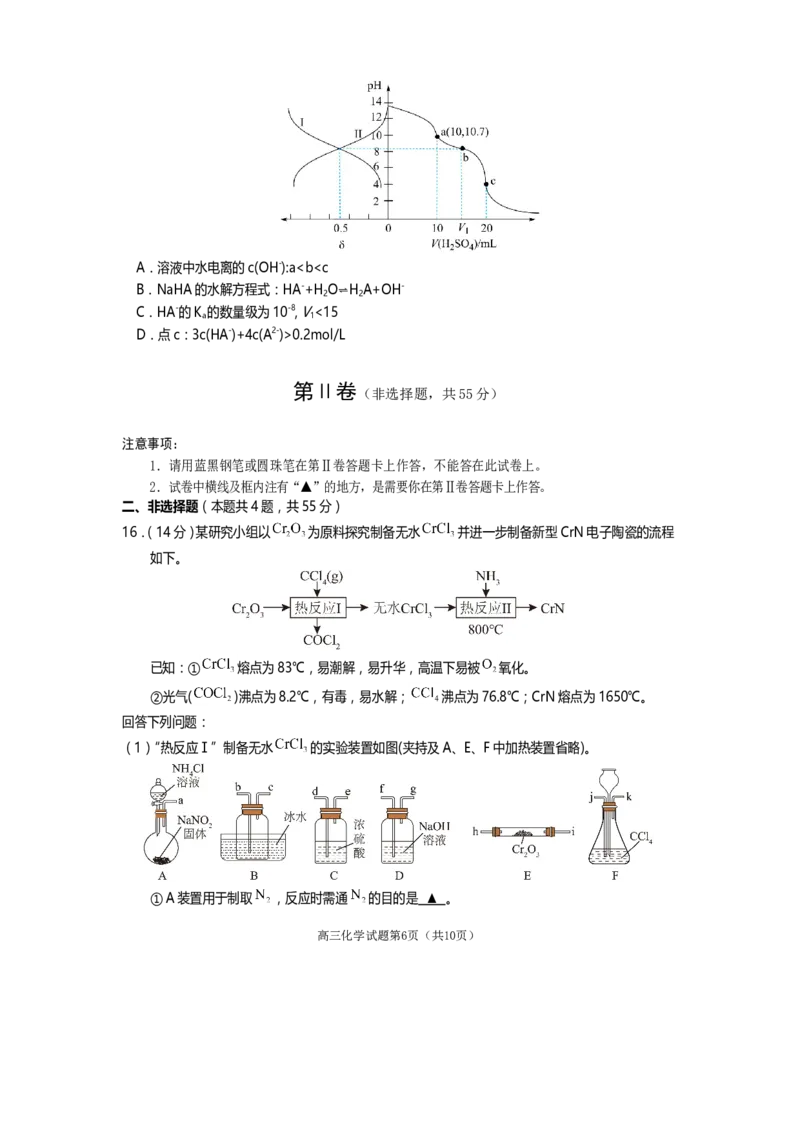
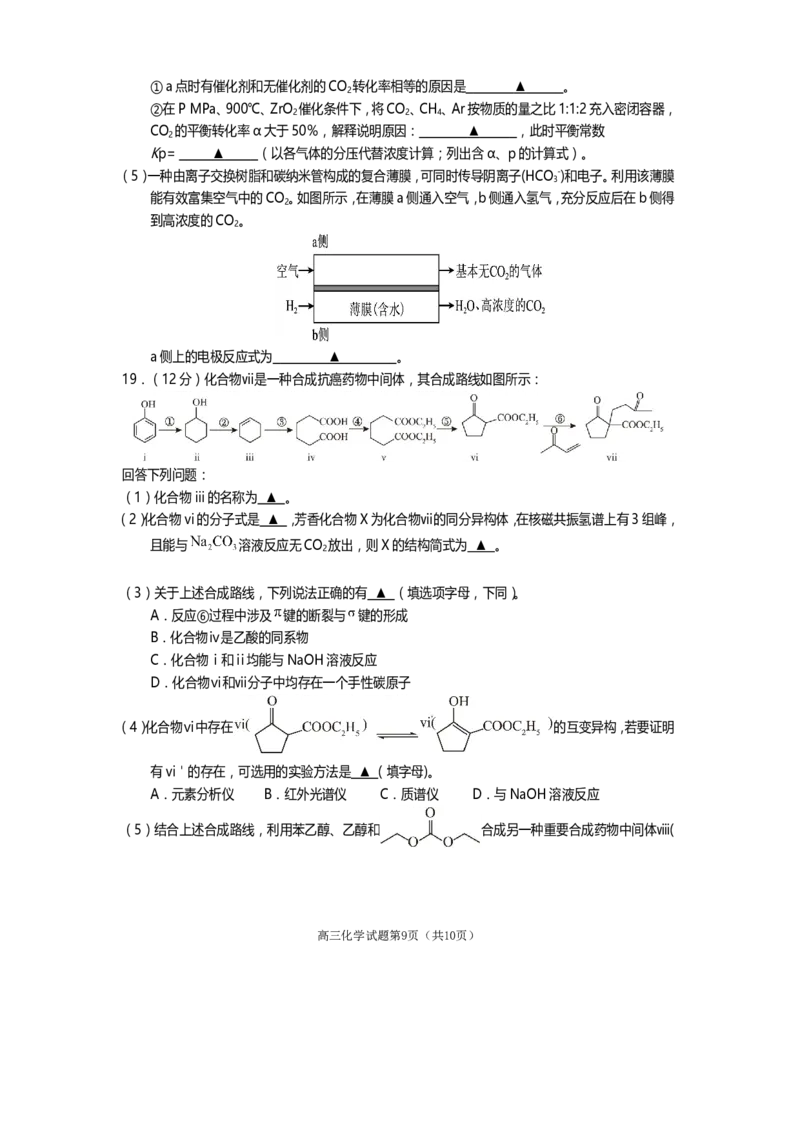
(5)一种由离子交换树脂和碳纳米管构成的复合薄膜,可同时传导阴离子(HCO -)和电子。利用该薄膜
3
能有效富集空气中的CO 。如图所示,在薄膜a侧通入空气,b侧通入氢气,充分反应后在b侧得
2
到高浓度的CO 。
2
a侧上的电极反应式为 ▲ 。
19.(12分)化合物ⅶ是一种合成抗癌药物中间体,其合成路线如图所示:
回答下列问题:
(1)化合物iii的名称为 ▲ 。
(2)化合物vi的分子式是 ▲ ,芳香化合物X为化合物ⅶ的同分异构体,在核磁共振氢谱上有3组峰,
且能与 溶液反应无CO 放出,则X的结构简式为 ▲ 。
2
(3)关于上述合成路线,下列说法正确的有 ▲ (填选项字母,下同)。
A.反应⑥过程中涉及 键的断裂与 键的形成
B.化合物ⅳ是乙酸的同系物
C.化合物ⅰ和ⅱ均能与NaOH溶液反应
D.化合物ⅵ和ⅶ分子中均存在一个手性碳原子
(4)化合物ⅵ中存在 的互变异构,若要证明
有vi'的存在,可选用的实验方法是 ▲ ( 填字母)。
A.元素分析仪 B.红外光谱仪 C.质谱仪 D.与NaOH溶液反应
(5)结合上述合成路线,利用苯乙醇、乙醇和 合成另一种重要合成药物中间体ⅷ(
高三化学试题第9页(共10页)),最后一步反应的化学方程式为 ▲ 。
高三化学试题第10页(共10页)