文档内容
黑龙江省实验中学高三上学期10月月考化学试卷
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5 Cu-64
考试时间:75分钟 总分:100分
第Ⅰ卷
一﹑单项选择题(共45分,15题,每题3分)
1.月饼作为中秋节的传统食品,承载着丰富的文化意义。下列关于月饼的叙述,正确的是
A.月饼中的油脂属于有机高分子
B.月饼包装中有个装有铁粉的小包,是吸氧剂,能防止油脂被氧化
C.某些月饼中加入的木糖醇属于糖类
D.脱氢乙酸钠是保存月饼常用的防腐剂,因其低毒,所以,可以放心的大量添加
2.N 为阿伏加德罗常数的值。下列说法的正确的是
A
A.92 g NO 与NO 的混合气体中含有的原子总数一定为6N
2 2 4 A
B.等物质的量的氮气和CO气体中均分别含有2N 个原子
A
C.0.1 mol·L-1的NaHSO 溶液中,Na+数目为0.1N
4 A
D.用电解粗铜的方法精炼铜,当阳极减重64 g时,电路中通过的电子数为2N
A
3.下列溶液中离子一定能大量共存的是
A.强碱溶液:Na+、K+、AlO、CO
B.使紫色石蕊溶液变红的溶液:Fe2+、Mg2+、NO、Cl-
C.含大量Fe3+的溶液:NH、Na+、Cl-、SCN-
D.c(H+)∶c(OH-)=1∶10-2的溶液:K+、Ba2+、ClO-、CO
4.下列离子方程式中,正确的是
A.食醋溶解鸡蛋皮中的CaCO :CaCO +2H+===Ca2++HO+CO↑
3 3 2 2
B.明矾溶液通入过量的氨气:Al3++4NH +2HO===AlO+4NH
3 2
C.澄清石灰水与过量的碳酸氢钙溶液反应:OH-+Ca2++HCO===CaCO ↓+HO
3 2
D.电解氯化镁溶液:2Cl-+2H+=====Cl↑+H↑
2 2
5.实验室用氢氧化钠固体配制0.1mol/L、 500ml的氢氧化钠溶液,下列说法错误的是
A.称量氢氧化钠固体要用小烧杯,不能直接放到滤纸上称量
B.如果把氢氧化钠和砝码放反了,会导致所配溶液浓度偏低
C.如果没有冷却至室温就进行定容,会导致所配溶液浓度偏高
D.某同学仰视定容,会导致所配溶液浓度偏低
6.科学家发现某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将海洋中的NO转化为N 进入
2大气层,反应过程如图所示。下列说法错误的是
A.过程Ⅰ中NO被还原
B.NO是该转化过程的一种中间产物
C.过程Ⅱ中参与反应的n(NO)∶n(NH)=1∶4
D.过程Ⅰ→Ⅲ的总反应为NO+NH===N ↑+2HO
2 2
7.利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法正确的是
A.a处不腐蚀,b处发生析氢腐蚀
B.a、b两处具有相同的电极反应式:Fe-3e-===Fe3+
C.左侧的溶液pH增大,右侧的溶液pH减小
D.一段时间后,左侧液面高于右侧液面
8.党的二十大报告指出:持续深入打好蓝天、碧水、净土保卫战。二氧化硫作为空气的一种主要污染
物,消除其污染势在必行。二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的
结合,原理如图所示。下列说法正确的是
A.该电池放电时电流从Pt1电极经过外电路流向Pt2电极
B.Pt1电极电势高于Pt2电极
C.Pt2电极附近发生的反应为O+4e-+4H+===2H O
2 2
D.相同条件下,放电过程中消耗的SO 和O 的体积比为1∶2
2 2
9.下列叙述中错误的有几项
①CO、NO 、SiO 均为酸性氧化物
2 2 2
②牺牲阳极法属于电解原理
③30 mL 1 mol·L-1盐酸与锌片反应,加入适量的氯化钠溶液,反应速率不变
④碳与二氧化碳的反应、Ba(OH) •8H O与NH Cl固体的反应均是吸热反应
2 2 4
⑤下列过程均需要通电才可进行:电离、电解、电镀、吸氧腐蚀
⑥苛性钠、次氯酸、氯气的分类依次为:强电解质、弱电解质、非电解质
⑦ΔH<0,ΔS>0的反应在温度低时不能自发进行
A. 4 B. 5 C. 6 D. 全部
10.氢能是公认的清洁能源,蓝氢是通过化石燃料制氢,同时配合碳捕捉和碳封存技术。一种制备蓝氢
的原理是CH(g)+CO (g) 2CO(g)+2H(g)。向体积为1L的恒容密闭容器中充入1mol CH(g)和2mol
4 2 2 4CO(g),在一定条件下发生上述反应,测得 的物质的量与时间的关系如表所示。下列叙述正确的是
2
t/min 0 5 10 15 20 25
n (H )/mol 0 0.5 0.75 0.85 0.9 0.9
2
A.0~10min,
B.当2v(CO) =v(CO) 时,反应达到平衡状态
(逆) 2 (正)
C.上述反应中, 的平衡转化率等于 的平衡转化率
D.其他条件不变,若加入高效催化剂,则 的转化率达到45%时所用时间小于20min
11.一种锌钒(Zn/V O))水性混合离子电池的结构示意图如图,放电时正极发生的反应为
2 5
xLi++xe-+V O=Li VO。下列说法错误的是
2 5 x 2 5
A.放电时,内电路中的电流方向为锌极到VO 极
2 5
B.充电时,溶液中Li+浓度不断增大
C.充电时,电极B上的电势比电极A的高
D.放电时,电极A每减少6.5g,有0.2x mol Li+嵌入电极B
12.下列装置能达到对应实验目的的是
A.可根据最终气球的大小判断反应速率的大小
B.探究温度对[Cu(H O) ]2++4Cl- [CuCl ]2-+4H O平衡的影响
2 4 4 2
C.探究KMnO 浓度对化学反应速率的影响
4
D.探究浓度对Fe3++3SCN- Fe(SCN) 平衡的影响
313.Cu基催化剂是 技术脱除NO中性能较为优异的新型催化剂,但烟气中的 会造成Cu基
催化剂的催化性能下降。加入 可抑制 对Cu基催化剂的影响,其作 用
机理如下图所示,下列说法错误的是
A.①②③均涉及氧化还原反应
B. Ce O 的化学式为
m n
C. 总反应中的还原剂是
D.从整个反应机理来看 作为催化剂,在反应过程中有参与反应
14.电渗析法制取八钼酸铵[ ]的工作原理如图所示(装置进出口未标明),已知当溶液的
pH为2~4时,溶液中的Mo元素主要以 形态存在,下列说法不正确的是
A.b极上的电极反应为:
B.III室中发生反应:
C.电解完成后,可从II室中回收氨水
D.生成0.1mol ,IV室溶液质量理论上增加21.6g
15.在体积为2L的恒容密闭容器中充入一定量的HS气体,发生反应 ,平衡
2
时三种组分的物质的量与温度的关系如图所示,下列说法正确的是
A.反应 的Δ
B. 时,向 点容器中再充入3molH S和3molH ,
2 2上述反应平衡不移动
C. 点和 点气体的压强之比为15 :16
D. 时,若起始时向容器中充入8mol HS气体,
2
则平衡时HS的转化率大于
2
第Ⅱ卷(非选择题 共55分)
16.回答下列问题:
(1)甲装置发生的化学反应方程式为 。
阴极收集到标况下2.24L气体时,阳极溶液质量减轻 g。
(2)乙装置是一种家用环保型消毒液发生器,外接电源b为 (填“正”或“负”)极,外接电源a
连接的石墨电极的电极反应式为 。
(3)一氧化氮-空气质子交换膜燃料电池将化学能转化为电能。如图所示,某同学设计用该电池探究将雾
霾中的SO 、NO转化为(NH )SO 的原理和电镀的原理。
2 4 2 4
①燃料电池放电过程中负极的电极反应式 。
②乙装置中物质A是 (填化学式),若在标准状况下,甲装置有5.6L O 参加反应,则乙装置
2
中通入的物质A的物质的量为 mol。
③丙装置为铜表面镀银装置,电极D为 ,电镀一段时间后,溶液中AgNO 溶液浓度
3
(填“变大”、“变小”或“不变”)。
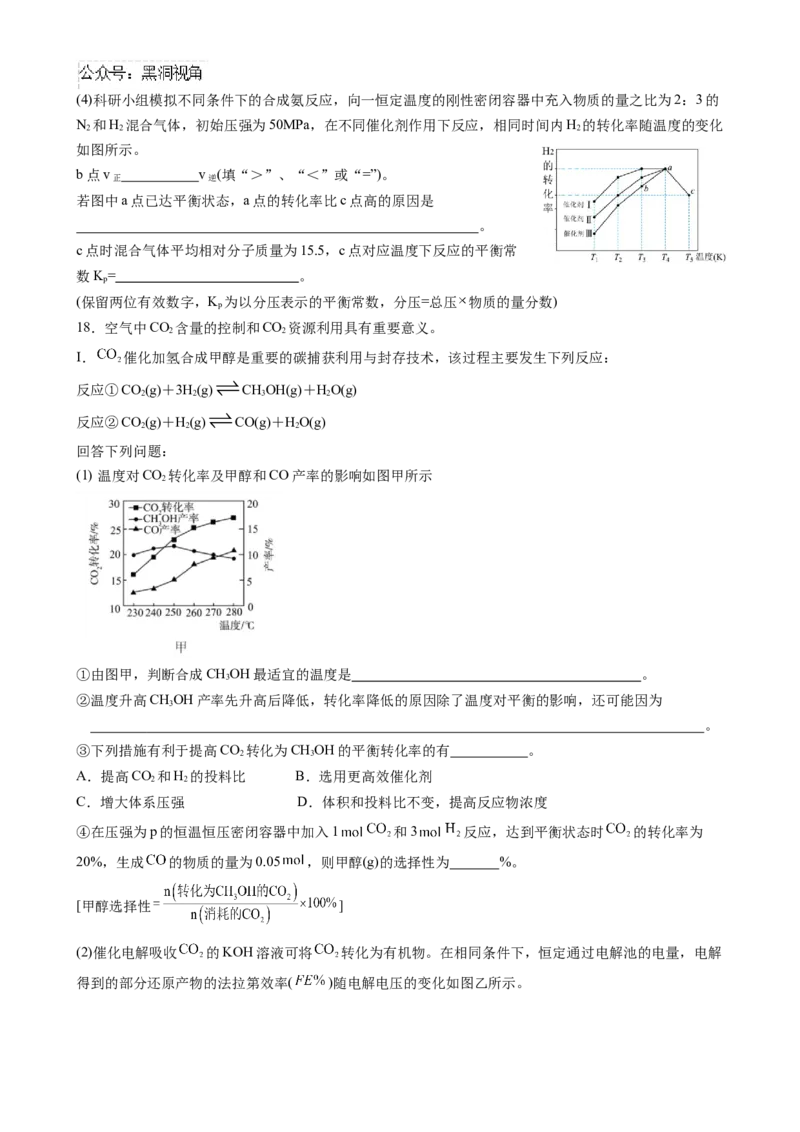
(4)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。飞船在光照区运
行时,太阳能电池帆板将太阳能转化为电能(工作原理图1),除供给飞船使用外,多余部分用镉镍蓄电池
储存起来。当飞船运行到阴影区时,镉镍蓄电池开始为飞船供电,镉镍蓄电池工作原理为Cd+2NiO(OH)
+2H O Cd(OH) +2Ni(OH) 。
2 2 2飞船在光照区运行时,N极链接镉镍蓄电池 极(填“m”或“n”)。飞船运行到阴影区时,b室中
发生的电极反应反应式为 。
17.合成氨是人类科学技术上的一项重大突破,一种工业合成氨的简式流程图如下:
(1) 步骤 可以使用湿法脱硫。
科研人员把铁的配合物 (L为配体)溶于弱碱性的海水中,制成吸收液,将气体 转化为单质硫。
步骤 总反应的热化学方程式为 (a,b>0)
该工艺包含两个阶段:
①第一阶段: 的吸收氧化:
;
②第二阶段 的再生,写出反应的热化学方程式
。
(2)步骤 中制氢气的原理如下:
①
②
反应①能自发进行的条件是 (选填“高温”、“低温”或“任何温度”)。若在恒容绝热容器
中加入2mol CO和1mol 只进行反应②,可以判定反应达到平衡的是 。
a.相同时间段内CO消耗的物质的量与 生成的物质的量相同
b.CO分压保持不变
c.体系总压保持不变
d.混合气体平均摩尔质量保持不变
e.CO与 转化率一样
f.体系温度保持不变
(3)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是 (填序号)。(4)科研小组模拟不同条件下的合成氨反应,向一恒定温度的刚性密闭容器中充入物质的量之比为2:3的
N 和H 混合气体,初始压强为50MPa,在不同催化剂作用下反应,相同时间内H 的转化率随温度的变化
2 2 2
如图所示。
b点v v (填“>”、“<”或“=”)。
正 逆
若图中a点已达平衡状态,a点的转化率比c点高的原因是
。
c点时混合气体平均相对分子质量为15.5,c点对应温度下反应的平衡常
数K= 。
p
(保留两位有效数字,K 为以分压表示的平衡常数,分压=总压 物质的量分数)
p
18.空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
I. 催化加氢合成甲醇是重要的碳捕获利用与封存技术,该过程主要发生下列反应:
反应①CO(g)+3H(g) CHOH(g)+HO(g)
2 2 3 2
反应②CO(g)+H(g) CO(g)+HO(g)
2 2 2
回答下列问题:
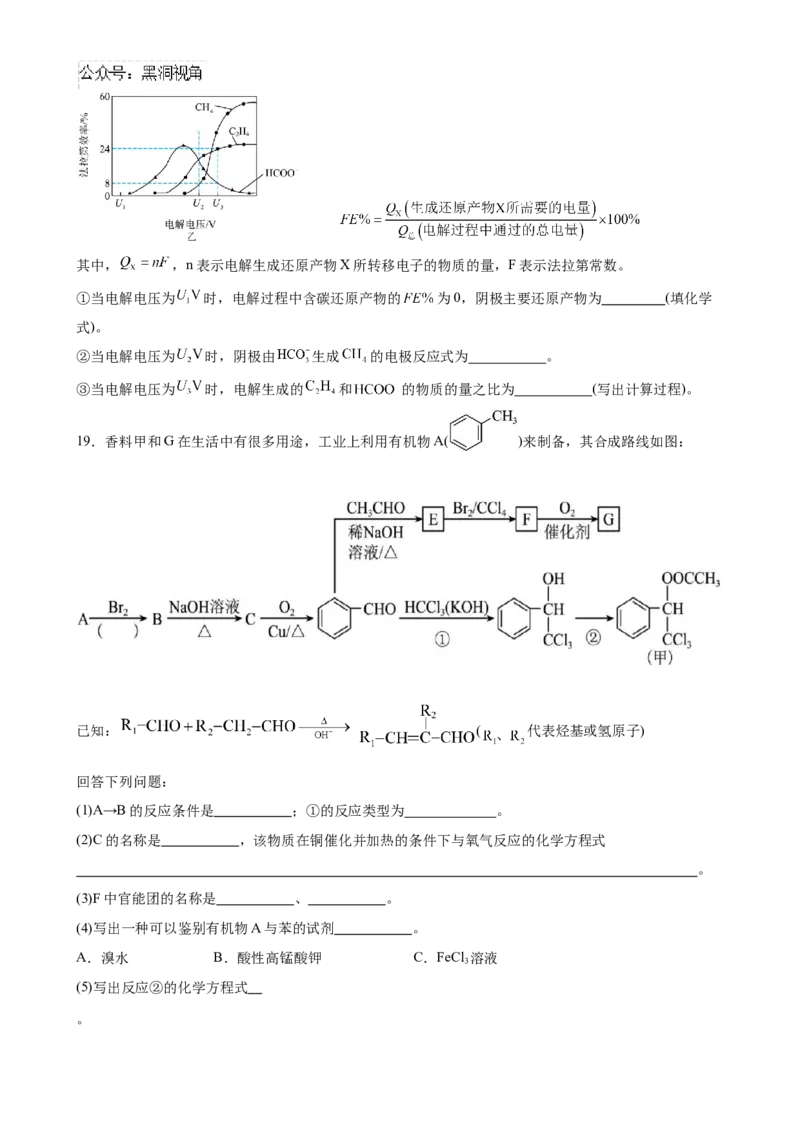
(1) 温度对CO 转化率及甲醇和CO产率的影响如图甲所示
2
①由图甲,判断合成CHOH最适宜的温度是 。
3
②温度升高CHOH产率先升高后降低,转化率降低的原因除了温度对平衡的影响,还可能因为
3
。
③下列措施有利于提高CO 转化为CHOH的平衡转化率的有 。
2 3
A.提高CO 和H 的投料比 B.选用更高效催化剂
2 2
C.增大体系压强 D.体积和投料比不变,提高反应物浓度
④在压强为p的恒温恒压密闭容器中加入1 和3 反应,达到平衡状态时 的转化率为
20%,生成 的物质的量为0.05 ,则甲醇(g)的选择性为 %。
[甲醇选择性 ]
(2)催化电解吸收 的KOH溶液可将 转化为有机物。在相同条件下,恒定通过电解池的电量,电解
得到的部分还原产物的法拉第效率( )随电解电压的变化如图乙所示。其中, ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
①当电解电压为 时,电解过程中含碳还原产物的 为0,阴极主要还原产物为 (填化学
式)。
②当电解电压为 时,阴极由 生成 的电极反应式为 。
③当电解电压为 时,电解生成的 和 的物质的量之比为 (写出计算过程)。
19.香料甲和G在生活中有很多用途,工业上利用有机物A( )来制备,其合成路线如图:
已知: ( 代表烃基或氢原子)
回答下列问题:
(1)A→B的反应条件是 ;①的反应类型为 。
(2)C的名称是 ,该物质在铜催化并加热的条件下与氧气反应的化学方程式
。
(3)F中官能团的名称是 、 。
(4)写出一种可以鉴别有机物A与苯的试剂 。
A.溴水 B.酸性高锰酸钾 C.FeCl 溶液
3
(5)写出反应②的化学方程式
。黑龙江省实验中学高三上学期10月月考化学答案
第Ⅰ卷
一﹑单项选择题(共45分,15题,每题3分)
1 2 3 4 5
B A A C B
6 7 8 9 10
C D C C D
11 12 13 14 15
D B A D B
第Ⅱ卷(非选择题 共55分)
16.(17分)
(1)2NaCl+2HO=====2NaOH+H↑+Cl↑ (2分) 11.7g (2分)
2 2 2
(2) 正 (1分) 2HO+2e-===H +OH- (2分)
2 2
(3) ①NO+2HO-3e-===NO+4H+ (2分) ②NH (1分) 0.8mol (2分)
2 3
③Cu (1分) 不变 (1分)
(4) m (1分) NiO(OH) + e- + H O === Ni(OH) + OH— (2分)
2 2
17.(14分)
(1) (2分)
(2)高温 (2分) bcf (2分)
(3)V (2分)
(4) > (2分) 该反应为放热反应,温度升高,平衡逆向移动,a点的转化率高于c点 (2分)
0.0020 (2分)
18. (14分)
(1)①250℃ (2分)
②升高温度,催化剂活性降低,导致反应速率下降,产率降低。 (2分) ③ CD (2分) ④75 (2分)
(2) ①H (2分) ② 或 (2分)
2
③ 1:2 (2分)
19.(10分)每个方程式2分,其他空均1分
(1)光照 加成反应 (2) 苯甲醇 方程式略
(3) 碳溴键 醛基
(4)B (5) + CHCOOH +H O
3 2