文档内容
2021 年初中学业水平考试试卷
理科综合
注意事项:
1.本试卷共10页,满分100分。考试时间90分钟。
2.答题前,考生务必先将自己的考生号、姓名、座位号等信息填写在试卷和答题卡的指定位置。请认真核对
条形码上的相关信息后,将条形码粘贴在答题卡的指定位置上。
3.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑,修改时用橡皮擦干净,再选涂其他答
案。
4.答非选择题时,必须使用0.5毫米的黑色字迹签字笔书写,作图时可用2B铅笔或0.5毫米的黑色字迹签字
笔。要求字迹工整,笔迹清晰。严格按题号所示的答题区域作答,超出答题区域的答案无效;在试卷、草槁
纸上答题无效。
5.保持答题卡清洁、完整,严禁折叠、损坏。严禁在答题卡上做任何标记,严禁使用涂改液、胶带纸、修正
带。考试结柬后,将本试卷和答题卡一并交回。
化学(40 分)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 S-32 Cl-35.5
Ca-40 Fe-56 Cu-64 Zn-65
一、选择题(本题包括6个小题,每小题2分,共12分。每小题只有一个选项符合题意请将答
题卡上对应题目的答案标号涂黑)
1.(2021·包头)中国政府承诺“努力争取2060年前实现碳中和”,“碳中和”是使碳排放与碳吸收达平衡,
实现二氧化碳相对“零排放”。为了实现碳中和,从实际出发,以下措施不可行的是
A.鼓励拼车或乘坐公共交通出行
B.推广垃圾分类处理,加强资源回收利用
C.禁止使用煤、石油等化石能源
D.采用物理或化学方法,捕集或吸收废气中的二氧化碳
【考点】化学与环境
【答案】C
【解析】现阶段,禁止使用煤、石油等化石能源不现实,只能够合理使用。
2.(2021·包头)手机使用的锂(Li)电池是新型的高能电池,以质量轻、电容量大而受到重视。某种锂电池
的总反应可表示为 ,下列说法正确的是
A.该反应属于化合反应 B.反应前后锂元素的化合价不变
C.MnO 中含有氧分子 D. LiMnO 属于氧化物
2 2
【考点】化学方程式的意义
【答案】A
【解析】该反应中反应前后锂元素的化合价是0,反应后化合价是+1价,发生了改变;MnO 的分子中只含有
2
锰原子和氧原子,不含有氧分子; LiMnO 中含有三种元素,不属于氧化物。
23.(2021·包头)推理是化学学习中常用的思维方法,下列推理正确的是
A.离子是带电的粒子,所以带电的粒子一定是离子
B.置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
C.化学变化伴随有能量变化,所以有能量变化的一定是化学变化
D.化合物含有不同种元素,所以由不同种元素组成的纯净物一定是化合物
【考点】归纳与推理
【答案】D
【解析】离子是带电的粒子,所以带电的粒子一定是离子,如电子带负电荷;置换反应有单质和化合物生成,
有单质和化合物生成的反应一定是置换反应,如一氧化碳还原氧化铁就不属于置换反应;化学变化伴随有能
量变化,有能量变化的一定是化学变化,如摩擦生热就不属于化学变化。
4.(2021·包头)下列实验操作能达到实验目的的是
选项 实验目的 实验操作
A 除去NaOH溶液中混有的NaCO 加过量的Ca(OH) 溶液,过滤
2 3 2
B 检验CH 中是否混有H 点燃,在火焰上方罩一干冷烧杯
4 2
C 分离CaCl 和CaCO 的固体混合物 加足量的水溶解、过滤
2 3
D 比较黄铜片(铜锌合金)和铜片的硬度 黄铜片和铜片相互刻划
【考点】实验设计与评价
【答案】D
【解析】除去NaOH溶液中混有的NaCO,应该加入适量的Ca(OH) 溶液;CH 燃烧也生成水,点燃后在
2 3 2 4
火焰上方罩一干冷烧杯,不可行;分离CaCl 和CaCO 的固体混合物,加足量的水溶解、过滤、蒸发。
2 3
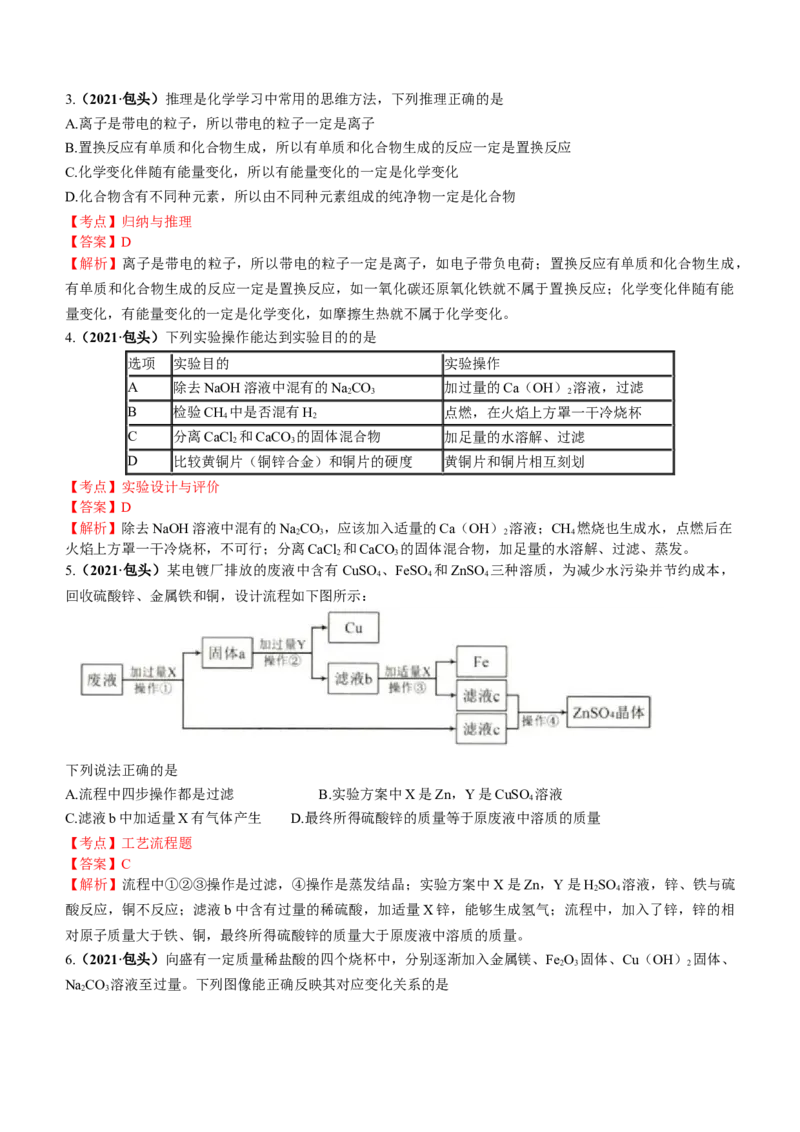
5.(2021·包头)某电镀厂排放的废液中含有CuSO 、FeSO 和ZnSO 三种溶质,为减少水污染并节约成本,
4 4 4
回收硫酸锌、金属铁和铜,设计流程如下图所示:
下列说法正确的是
A.流程中四步操作都是过滤 B.实验方案中X是Zn,Y是CuSO 溶液
4
C.滤液b中加适量X有气体产生 D.最终所得硫酸锌的质量等于原废液中溶质的质量
【考点】工艺流程题
【答案】C
【解析】流程中①②③操作是过滤,④操作是蒸发结晶;实验方案中X是Zn,Y是HSO 溶液,锌、铁与硫
2 4
酸反应,铜不反应;滤液b中含有过量的稀硫酸,加适量X锌,能够生成氢气;流程中,加入了锌,锌的相
对原子质量大于铁、铜,最终所得硫酸锌的质量大于原废液中溶质的质量。
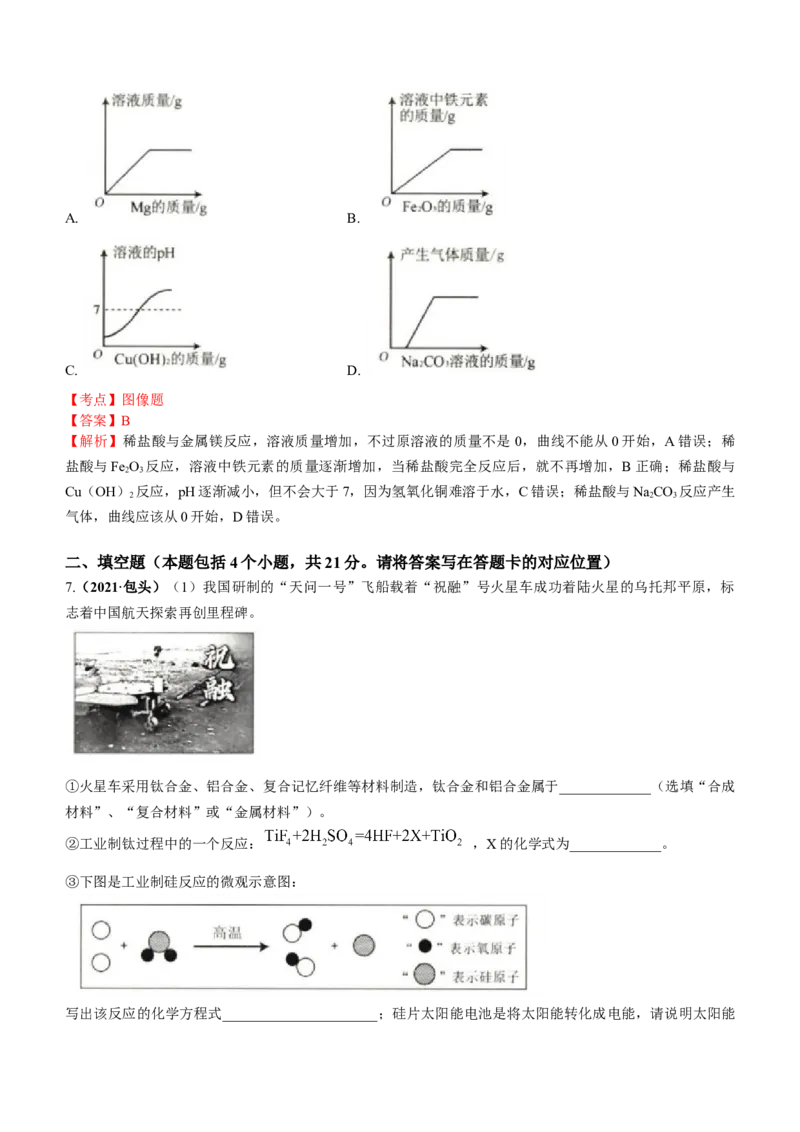
6.(2021·包头)向盛有一定质量稀盐酸的四个烧杯中,分别逐渐加入金属镁、Fe O 固体、Cu(OH) 固体、
2 3 2
NaCO 溶液至过量。下列图像能正确反映其对应变化关系的是
2 3A. B.
C. D.
【考点】图像题
【答案】B
【解析】稀盐酸与金属镁反应,溶液质量增加,不过原溶液的质量不是 0,曲线不能从0开始,A错误;稀
盐酸与Fe O 反应,溶液中铁元素的质量逐渐增加,当稀盐酸完全反应后,就不再增加,B正确;稀盐酸与
2 3
Cu(OH) 反应,pH逐渐减小,但不会大于7,因为氢氧化铜难溶于水,C错误;稀盐酸与NaCO 反应产生
2 2 3
气体,曲线应该从0开始,D错误。
二、填空題(本题包括4个小题,共21分。请将答案写在答题卡的对应位置)
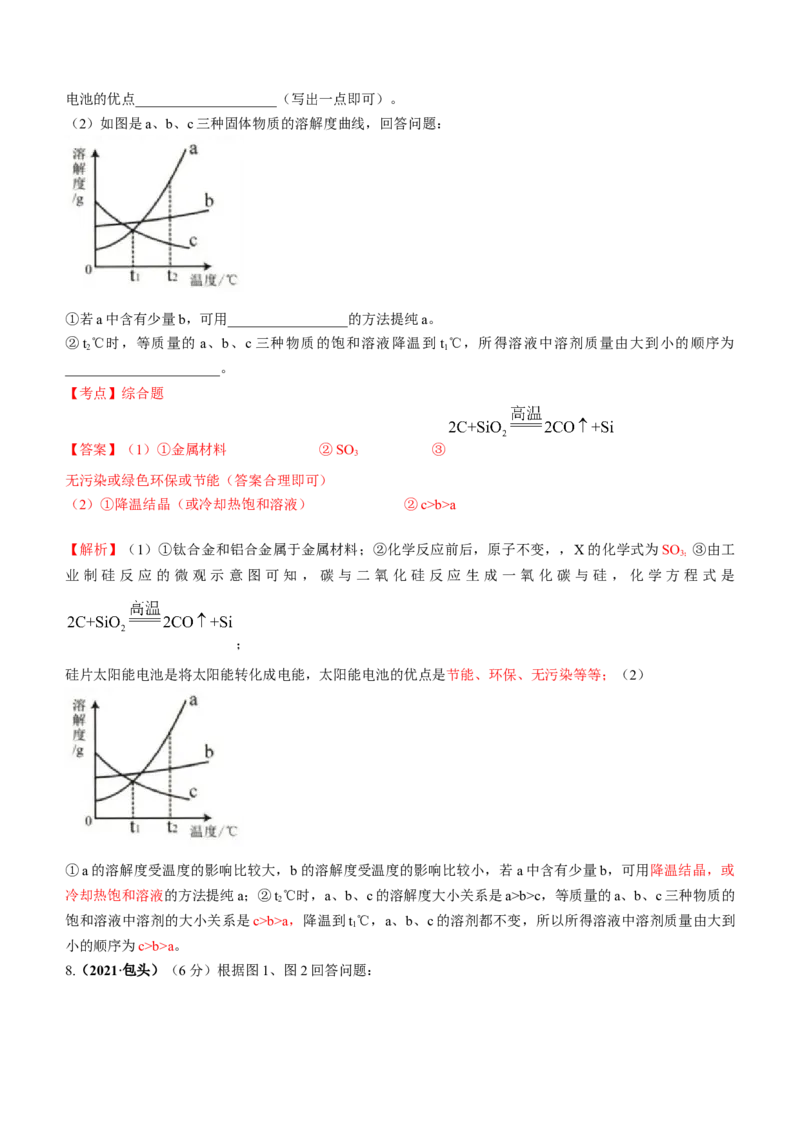
7.(2021·包头)(1)我国研制的“天问一号”飞船载着“祝融”号火星车成功着陆火星的乌托邦平原,标
志着中国航天探索再创里程碑。
①火星车采用钛合金、铝合金、复合记忆纤维等材料制造,钛合金和铝合金属于_____________(选填“合成
材料”、“复合材料”或“金属材料”)。
②工业制钛过程中的一个反应: ,X的化学式为_____________。
③下图是工业制硅反应的微观示意图:
写出该反应的化学方程式______________________;硅片太阳能电池是将太阳能转化成电能,请说明太阳能电池的优点____________________(写出一点即可)。
(2)如图是a、b、c三种固体物质的溶解度曲线,回答问题:
①若a中含有少量b,可用_________________的方法提纯a。
②t℃时,等质量的 a、b、c三种物质的饱和溶液降温到 t℃,所得溶液中溶剂质量由大到小的顺序为
2 1
______________________。
【考点】综合题
【答案】(1)①金属材料 ②SO ③
3
无污染或绿色环保或节能(答案合理即可)
(2)①降温结晶(或冷却热饱和溶液) ②c>b>a
【解析】(1)①钛合金和铝合金属于金属材料;②化学反应前后,原子不变,,X的化学式为SO ③由工
3;
业 制 硅 反 应 的 微 观 示 意 图 可 知 , 碳 与 二 氧 化 硅 反 应 生 成 一 氧 化 碳 与 硅 , 化 学 方 程 式 是
;
硅片太阳能电池是将太阳能转化成电能,太阳能电池的优点是节能、环保、无污染等等;(2)
①a的溶解度受温度的影响比较大,b的溶解度受温度的影响比较小,若a中含有少量b,可用降温结晶,或
冷却热饱和溶液的方法提纯a;②t℃时,a、b、c的溶解度大小关系是a>b>c,等质量的a、b、c三种物质的
2
饱和溶液中溶剂的大小关系是c>b>a,降温到t℃,a、b、c的溶剂都不变,所以所得溶液中溶剂质量由大到
1
小的顺序为c>b>a。
8.(2021·包头)(6分)根据图1、图2回答问题:(1)实验室用一种物质制取氧气,从图1中应选用的发生装置是_____________(填字母),该反应的化学
方 程 式 为 ________________________ ; 若 用 F 装 置 且 采 用 排 水 法 收 集 氧 气 , 简 述 操 作 步 骤
___________________。
(2)某同学将图2中G装置产生的气体通入H中,若试剂X是新制澄清石灰水,H中一直未出现浑浊现象,
其原因是_______________________;若Ⅰ中干燥的紫色石蕊纸花没有变红,则 X可能是下列选项中的
_______________(填标号)。
a.浓硫酸 b.饱和 NaHCO 溶液 c.CaCl 溶液 d.NaOH浓溶液
3 2
【考点】气体的制取
【答案】(1)B; (2分)
先将集气瓶装满水,再将氧气从m端管口通入。
(2)浓盐酸挥发,使生成的二氧化碳中混有较多的氯化氢而不能生成碳酸钙沉淀;ad
【解析】(1)实验室可用高锰酸钾这一种物质制取氧气,从图1中应选用的发生装置是塞有棉花的装置B,
化学方程式为 ;若用F装置且采用排水法收集氧气,操作步骤是先将集
气瓶装满水,再将氧气从m端管口通入;(2)某同学将图2中G装置产生的气体通入H中,若试剂X是新
制澄清石灰水,H中一直未出现浑浊现象,其原因是浓盐酸挥发,使生成的二氧化碳中混有较多的氯化氢而
不能生成碳酸钙沉淀;二氧化碳不显酸性,不能使干燥的紫色石蕊纸花变红色,浓硫酸能够吸收气体中的水
分,纸花不会变红; NaOH浓溶液可以吸收水,也可以吸收二氧化碳、浓盐酸挥发出的氯化氢气体,纸花
不会变红。
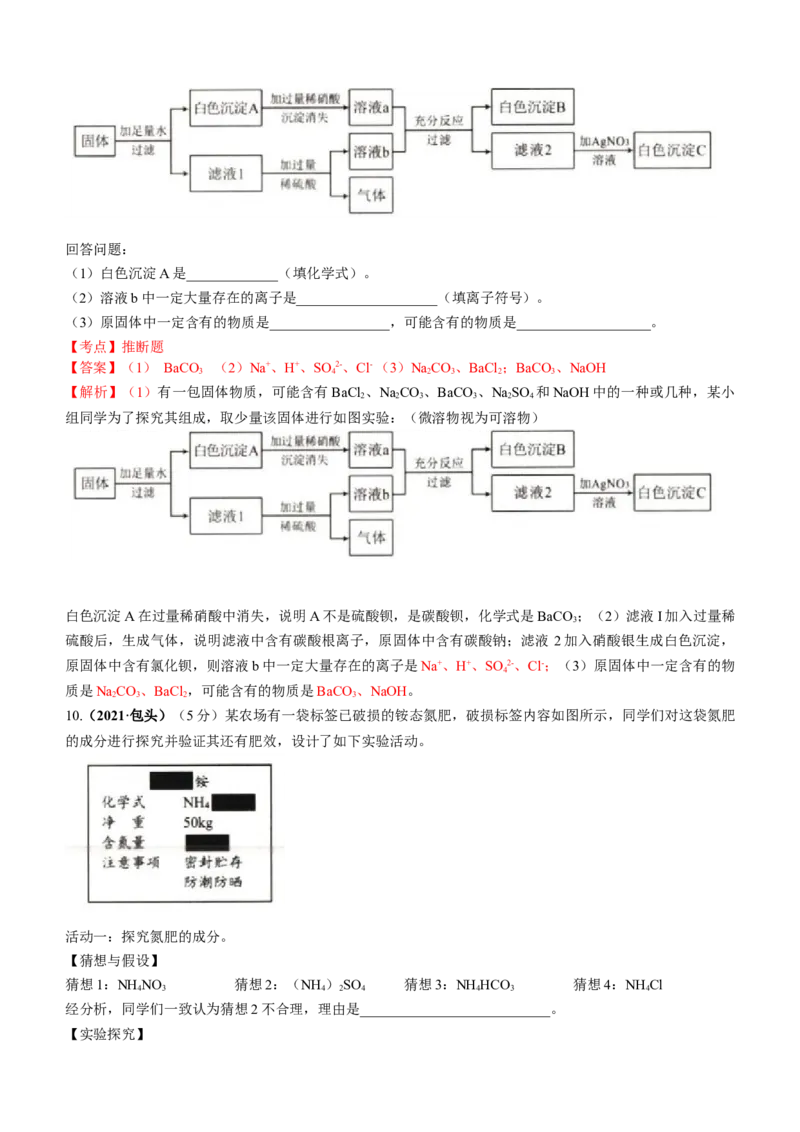
9.(2021·包头)(4分)有一包固体物质,可能含有BaCl 、NaCO、BaCO 、NaSO 和NaOH中的一种或几
2 2 3 3 2 4
种,某小组同学为了探究其组成,取少量该固体进行如图实验:(微溶物视为可溶物)回答问题:
(1)白色沉淀A是_____________(填化学式)。
(2)溶液b中一定大量存在的离子是____________________(填离子符号)。
(3)原固体中一定含有的物质是_________________,可能含有的物质是___________________。
【考点】推断题
【答案】(1) BaCO (2)Na+、H+、SO 2-、Cl-(3)NaCO、BaCl ;BaCO 、NaOH
3 4 2 3 2 3
【解析】(1)有一包固体物质,可能含有BaCl 、NaCO 、BaCO 、NaSO 和NaOH中的一种或几种,某小
2 2 3 3 2 4
组同学为了探究其组成,取少量该固体进行如图实验:(微溶物视为可溶物)
白色沉淀A在过量稀硝酸中消失,说明A不是硫酸钡,是碳酸钡,化学式是BaCO ;(2)滤液I加入过量稀
3
硫酸后,生成气体,说明滤液中含有碳酸根离子,原固体中含有碳酸钠;滤液 2加入硝酸银生成白色沉淀,
原固体中含有氯化钡,则溶液b中一定大量存在的离子是Na+、H+、SO 2-、Cl-;(3)原固体中一定含有的物
4
质是NaCO、BaCl ,可能含有的物质是BaCO 、NaOH。
2 3 2 3
10.(2021·包头)(5分)某农场有一袋标签已破损的铵态氮肥,破损标签内容如图所示,同学们对这袋氮肥
的成分进行探究并验证其还有肥效,设计了如下实验活动。
活动一:探究氮肥的成分。
【猜想与假设】
猜想1:NH NO 猜想2:(NH )SO 猜想3:NH HCO 猜想4:NH Cl
4 3 4 2 4 4 3 4
经分析,同学们一致认为猜想2不合理,理由是___________________________。
【实验探究】(1)取少量样品于试管中,滴加稀盐酸,观察到无气泡产生,则该氮肥的成分一定不是________________
(填化学式)。
(2)为了确定该氮肥究竟是剩余两种中的哪一种,写出实验操作、现象及结论________________。
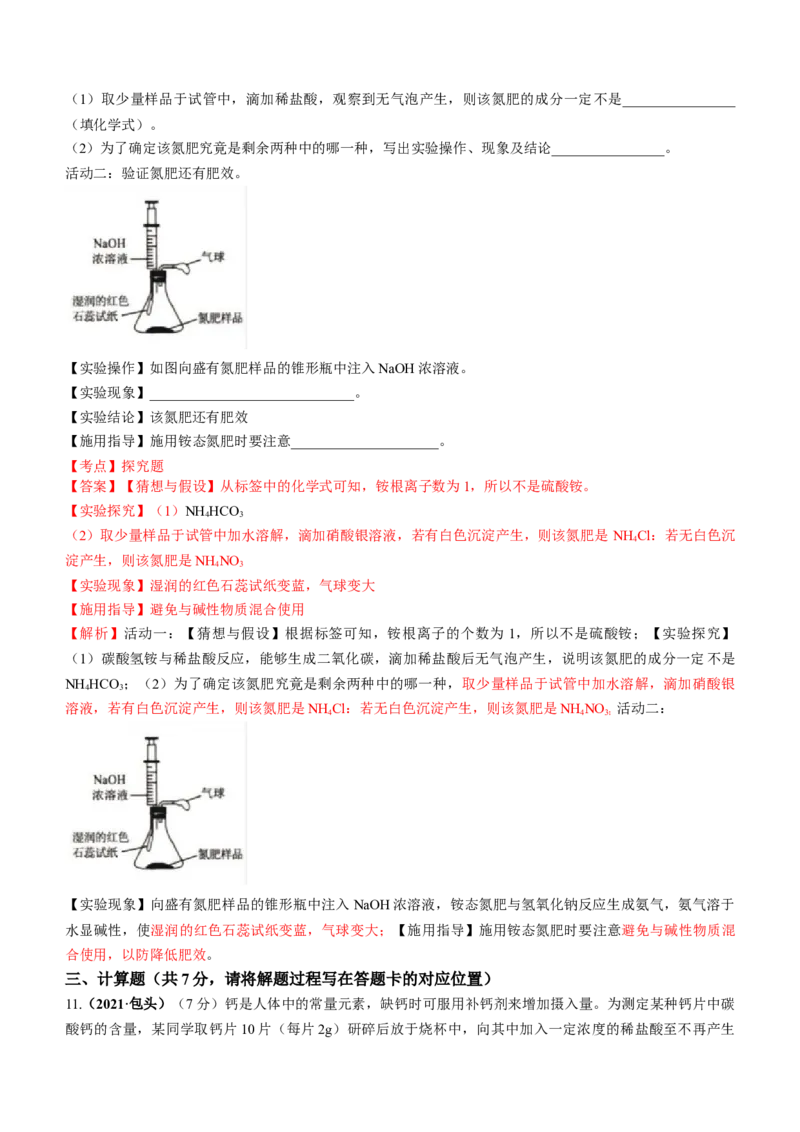
活动二:验证氮肥还有肥效。
【实验操作】如图向盛有氮肥样品的锥形瓶中注入NaOH浓溶液。
【实验现象】_____________________________。
【实验结论】该氮肥还有肥效
【施用指导】施用铵态氮肥时要注意_____________________。
【考点】探究题
【答案】【猜想与假设】从标签中的化学式可知,铵根离子数为1,所以不是硫酸铵。
【实验探究】(1)NH HCO
4 3
(2)取少量样品于试管中加水溶解,滴加硝酸银溶液,若有白色沉淀产生,则该氮肥是 NH Cl:若无白色沉
4
淀产生,则该氮肥是NH NO
4 3
【实验现象】湿润的红色石蕊试纸变蓝,气球变大
【施用指导】避免与碱性物质混合使用
【解析】活动一:【猜想与假设】根据标签可知,铵根离子的个数为 1,所以不是硫酸铵;【实验探究】
(1)碳酸氢铵与稀盐酸反应,能够生成二氧化碳,滴加稀盐酸后无气泡产生,说明该氮肥的成分一定不是
NH HCO ;(2)为了确定该氮肥究竟是剩余两种中的哪一种,取少量样品于试管中加水溶解,滴加硝酸银
4 3
溶液,若有白色沉淀产生,则该氮肥是NH Cl:若无白色沉淀产生,则该氮肥是NH NO 活动二:
4 4 3;
【实验现象】向盛有氮肥样品的锥形瓶中注入NaOH浓溶液,铵态氮肥与氢氧化钠反应生成氨气,氨气溶于
水显碱性,使湿润的红色石蕊试纸变蓝,气球变大;【施用指导】施用铵态氮肥时要注意避免与碱性物质混
合使用,以防降低肥效。
三、计算题(共7分,请将解题过程写在答题卡的对应位置)
11.(2021·包头)(7分)钙是人体中的常量元素,缺钙时可服用补钙剂来增加摄入量。为测定某种钙片中碳
酸钙的含量,某同学取钙片10片(每片2g)研碎后放于烧杯中,向其中加入一定浓度的稀盐酸至不再产生气泡,过滤后得到不溶物的质量为10g,再向滤液中加入55.4g水,此时溶液中溶质的质量分数为10%(钙片
中主要成分为碳酸钙,假设其他成分不溶于水,也不与盐酸反应)。计算:
(1)该种钙片中碳酸钙的质量分数。
(2)加入稀盐酸的质量。
(3)若配制200g上述浓度的稀盐酸,需用36.5%的浓盐酸的质量。
【考点】计算题
【解析】解:(1)该种钙片中碳酸钙的质量分数
(2)设反应所消耗的氯化氢的质量为x,生成氯化钙的质量为y,二氧化碳的质量为z
设加入稀盐酸质量为M。
(3)设需用36.5%的浓盐酸的质量为N。
N=80g
(或: )
答:(略)
(其它解法合理均给分)