文档内容
秘密★启用前
2021 年广州市初中学业水平考试
化学
本试卷共8页,20小题,满分90分。考试时间60分钟。
注意事项:
1.答题前,考生务必在答题卡第1面和第3面上用黑色字迹的钢笔或签字笔填写自己的
考生号、姓名;并将自己的条形码粘贴在答题卡的“条形码粘贴处”。
2.选择题每小题选出答素后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号;答案不能写在试卷上。
3.非选择题答案必须写在答题卡各题目指定区域内的相应位置上;如需改动,先划掉
原来的答案,然后再写上新的答案,改动后的答案也不能超出指定的区域;除作图
可用2B铅笔外,其他都必须用黑色字迹的钢笔或签字笔作答。不准使用圆珠笔和涂
改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束时,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Ca 40 Fe 56
一、选择题:本题包括14小题,每小题3分,共42分。每小题给出的四个选项中,只有一
项最符合题意。错选、不选、多选或涂改不清的,均不给分。
1.中国的科技发展举世瞩日。2020年“嫦娥五号”成功登月,2021年“天问一号”着陆火
星,它们都是由以液氢为燃料的“长征五号”火箭搭载升空。“嫦娥五号”携带了特种
芳纶材质的五星红旗,“天问一号”应用了我国研发的新型镁锂合金以及锂氟化碳电池。
下列说法不正确的是
A.液氢燃烧只生成水 B.芳纶属于合成纤维
C.镁锂合金是氧化物 D.氟属于非金属元素
2.“劳动创造幸福,实干成就伟业。”下列劳动所涉及的化学知识正确的是
选项 劳动项目 化学知识
A 用明矾处理较浑浊的天然水 明矾主要起杀菌消毒作用
B 煮水时,若水的硬度大,易结垢 硬水中含有较多可溶性钙、镁化合物
C 在盐田中晾晒海水,得到粗盐 粗盐除去泥沙即可得到纯净的氯化钠
D 用含小苏打的发酵粉焙制糕点 小苏打(NaHCO )的化学名称是碳酸钠
3
3.虾饺是一种有名的广州美食,下列制作虾饺的原料中富含糖类的是
化 学 试 卷 第1页 共8页A.米粉 B.虾仁
C.食盐 D.植物油
4.空气是多种气体的混合物,下列生产生活中用到的气体来自空气的是
A.填充气球用到的氦气 B.制硝酸用到的二氧化氮
C.炼铁用到的一氧化碳 D.做饭用到的天然气
5.在生产、运输、使用和贮存化学药品时,应注意安全。浓硫酸运输车须张贴的标志是
A B C D
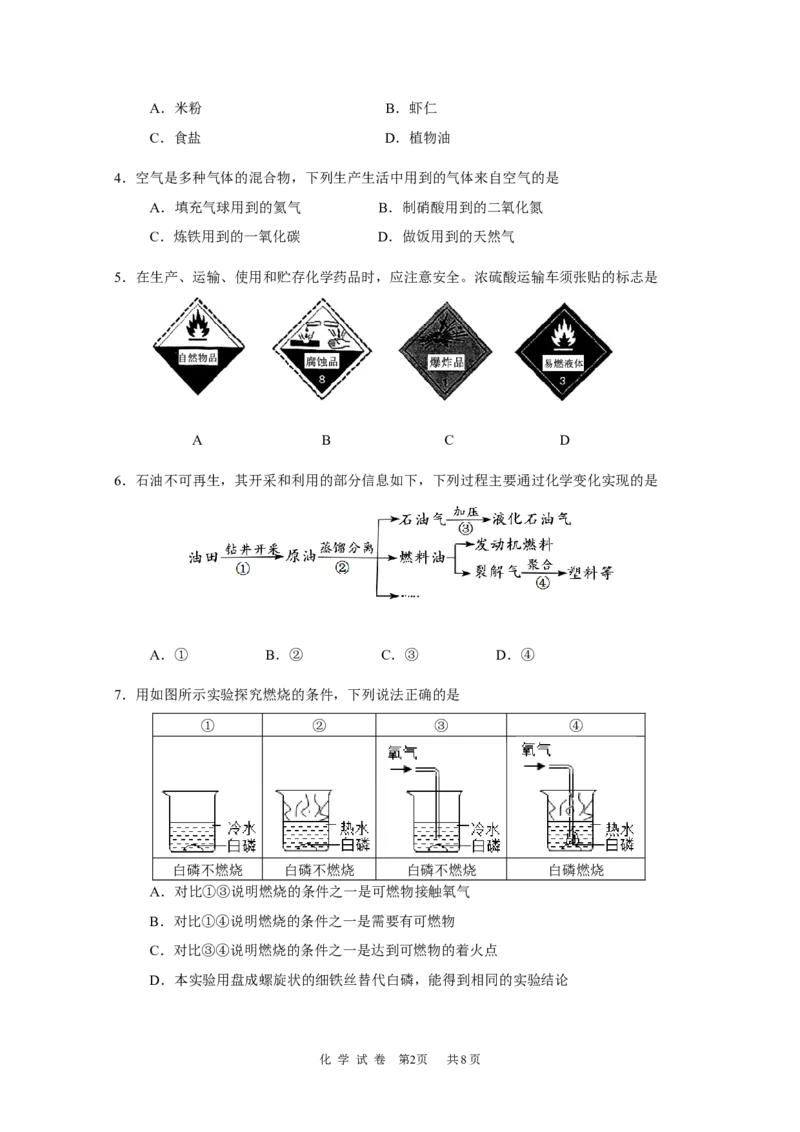
6.石油不可再生,其开采和利用的部分信息如下,下列过程主要通过化学变化实现的是
A.① B.② C.③ D.④
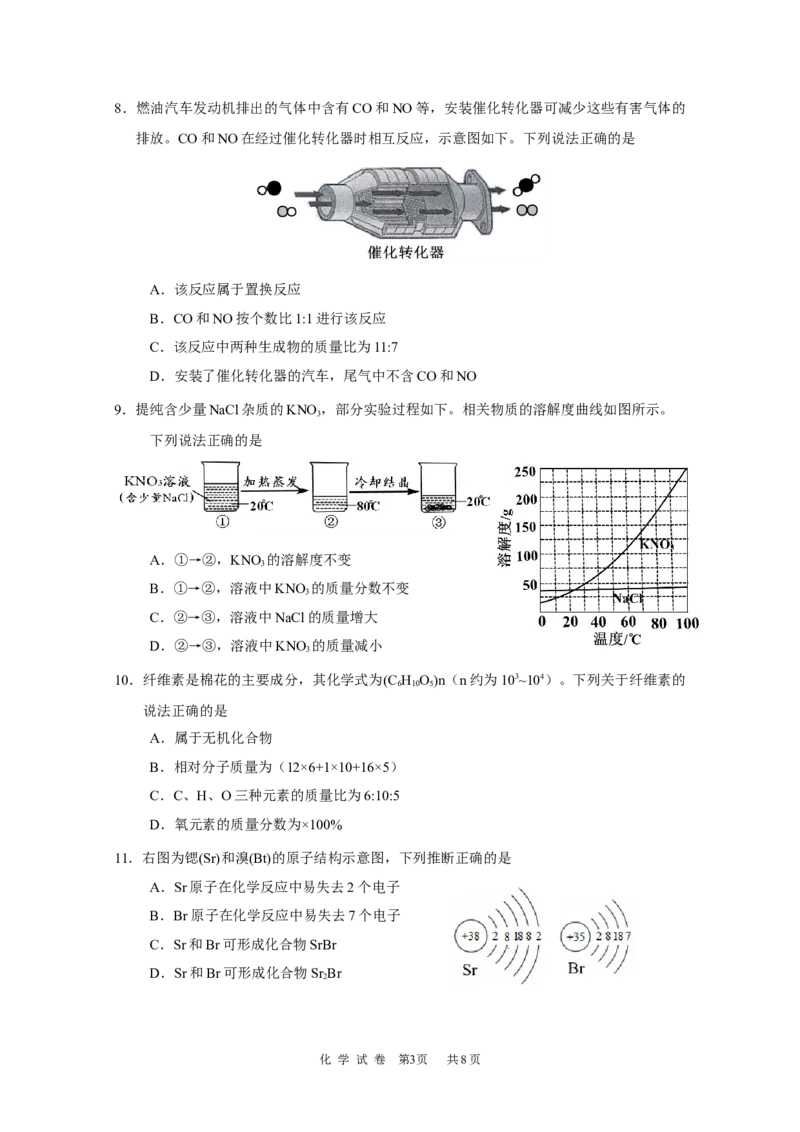
7.用如图所示实验探究燃烧的条件,下列说法正确的是
① ② ③ ④
白磷不燃烧 白磷不燃烧 白磷不燃烧 白磷燃烧
A.对比①③说明燃烧的条件之一是可燃物接触氧气
B.对比①④说明燃烧的条件之一是需要有可燃物
C.对比③④说明燃烧的条件之一是达到可燃物的着火点
D.本实验用盘成螺旋状的细铁丝替代白磷,能得到相同的实验结论
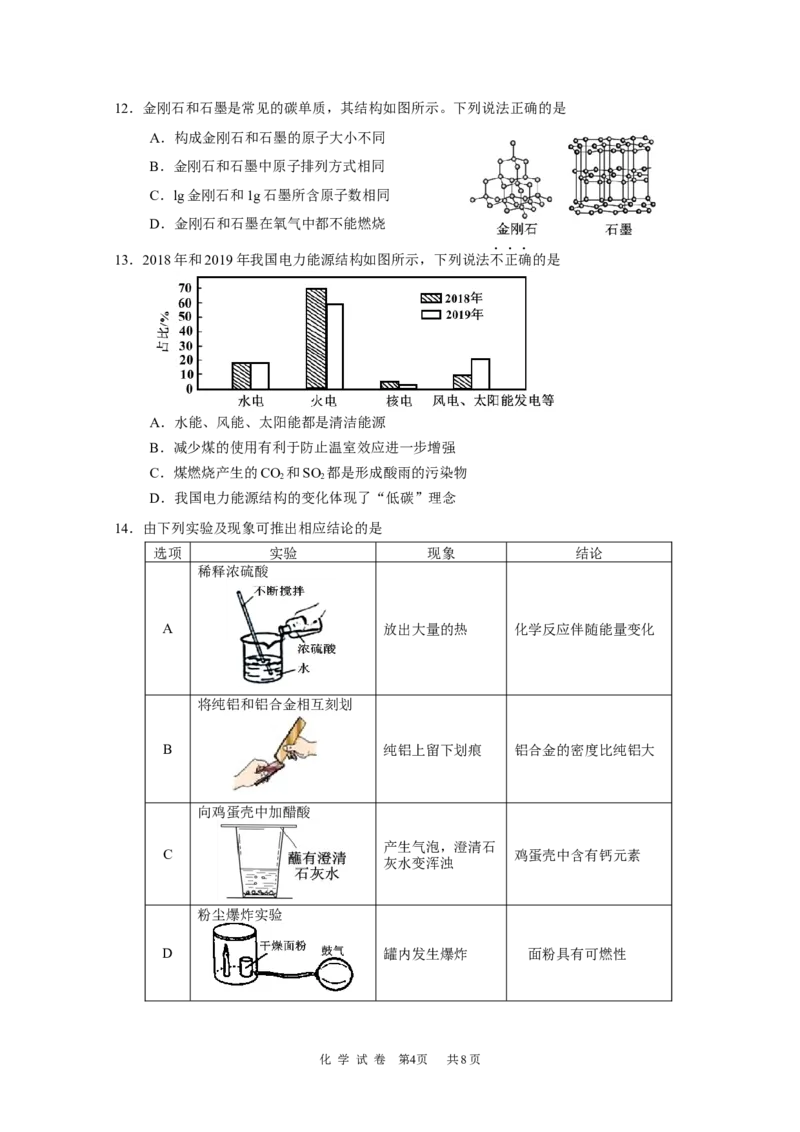
化 学 试 卷 第2页 共8页8.燃油汽车发动机排出的气体中含有CO和NO等,安装催化转化器可减少这些有害气体的
排放。CO和NO在经过催化转化器时相互反应,示意图如下。下列说法正确的是
A.该反应属于置换反应
B.CO和NO按个数比1:1进行该反应
C.该反应中两种生成物的质量比为11:7
D.安装了催化转化器的汽车,尾气中不含CO和NO
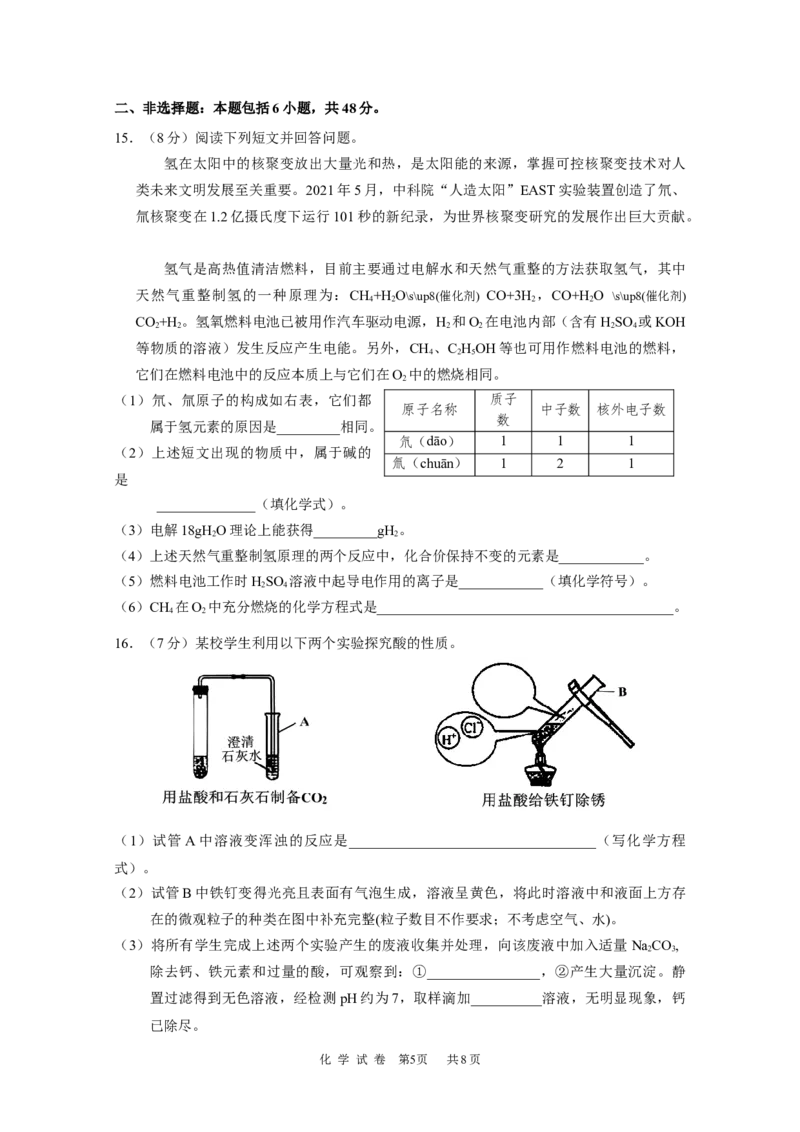
9.提纯含少量NaCl杂质的KNO,部分实验过程如下。相关物质的溶解度曲线如图所示。
3
下列说法正确的是
A.①→②,KNO 的溶解度不变
3
B.①→②,溶液中KNO 的质量分数不变
3
C.②→③,溶液中NaCl的质量增大
D.②→③,溶液中KNO 的质量减小
3
10.纤维素是棉花的主要成分,其化学式为(C H O)n(n约为103~104)。下列关于纤维素的
6 10 5
说法正确的是
A.属于无机化合物
B.相对分子质量为(12×6+1×10+16×5)
C.C、H、O三种元素的质量比为6:10:5
D.氧元素的质量分数为×100%
11.右图为锶(Sr)和溴(Bt)的原子结构示意图,下列推断正确的是
A.Sr原子在化学反应中易失去2个电子
B.Br原子在化学反应中易失去7个电子
C.Sr和Br可形成化合物SrBr
D.Sr和Br可形成化合物Sr Br
2
化 学 试 卷 第3页 共8页12.金刚石和石墨是常见的碳单质,其结构如图所示。下列说法正确的是
A.构成金刚石和石墨的原子大小不同
B.金刚石和石墨中原子排列方式相同
C.lg金刚石和1g石墨所含原子数相同
D.金刚石和石墨在氧气中都不能燃烧
13.2018年和2019年我国电力能源结构如图所示,下列说法不正确的是
A.水能、风能、太阳能都是清洁能源
B.减少煤的使用有利于防止温室效应进一步增强
C.煤燃烧产生的CO 和SO 都是形成酸雨的污染物
2 2
D.我国电力能源结构的变化体现了“低碳”理念
14.由下列实验及现象可推出相应结论的是
选项 实验 现象 结论
稀释浓硫酸
A 放出大量的热 化学反应伴随能量变化
将纯铝和铝合金相互刻划
B 纯铝上留下划痕 铝合金的密度比纯铝大
向鸡蛋壳中加醋酸
产生气泡,澄清石
C 鸡蛋壳中含有钙元素
灰水变浑浊
粉尘爆炸实验
D 罐内发生爆炸 面粉具有可燃性
化 学 试 卷 第4页 共8页二、非选择题:本题包括6小题,共48分。
15.(8分)阅读下列短文并回答问题。
氢在太阳中的核聚变放出大量光和热,是太阳能的来源,掌握可控核聚变技术对人
类未来文明发展至关重要。2021年5月,中科院“人造太阳”EAST实验装置创造了氘、
氚核聚变在1.2亿摄氏度下运行101秒的新纪录,为世界核聚变研究的发展作出巨大贡献。
氢气是高热值清洁燃料,目前主要通过电解水和天然气重整的方法获取氢气,其中
天然气重整制氢的一种原理为:CH+H O\s\up8(催化剂) CO+3H ,CO+HO \s\up8(催化剂)
4 2 2 2
CO+H 。氢氧燃料电池已被用作汽车驱动电源,H 和O 在电池内部(含有HSO 或KOH
2 2 2 2 2 4
等物质的溶液)发生反应产生电能。另外,CH 、C HOH等也可用作燃料电池的燃料,
4 2 5
它们在燃料电池中的反应本质上与它们在O 中的燃烧相同。
2
(1)氘、氚原子的构成如右表,它们都 质子
原子名称 中子数 核外电子数
数
属于氢元素的原因是_________相同。
氘(dāo) 1 1 1
(2)上述短文出现的物质中,属于碱的
氚(chuān) 1 2 1
是
______________(填化学式)。
(3)电解18gHO理论上能获得_________gH。
2 2
(4)上述天然气重整制氢原理的两个反应中,化合价保持不变的元素是____________。
(5)燃料电池工作时HSO 溶液中起导电作用的离子是____________(填化学符号)。
2 4
(6)CH 在O 中充分燃烧的化学方程式是__________________________________________。
4 2
16.(7分)某校学生利用以下两个实验探究酸的性质。
(1)试管A中溶液变浑浊的反应是___________________________________(写化学方程
式)。
(2)试管B中铁钉变得光亮且表面有气泡生成,溶液呈黄色,将此时溶液中和液面上方存
在的微观粒子的种类在图中补充完整(粒子数目不作要求;不考虑空气、水)。
(3)将所有学生完成上述两个实验产生的废液收集并处理,向该废液中加入适量 NaCO,
2 3
除去钙、铁元素和过量的酸,可观察到:①________________,②产生大量沉淀。静
置过滤得到无色溶液,经检测pH约为7,取样滴加__________溶液,无明显现象,钙
已除尽。
化 学 试 卷 第5页 共8页(4)若处理废液时共消耗NaCO212g,则实验室为本次探究实验至少准备了_________g盐
2 3
酸。(已知盐酸的质量分数为7.3%)
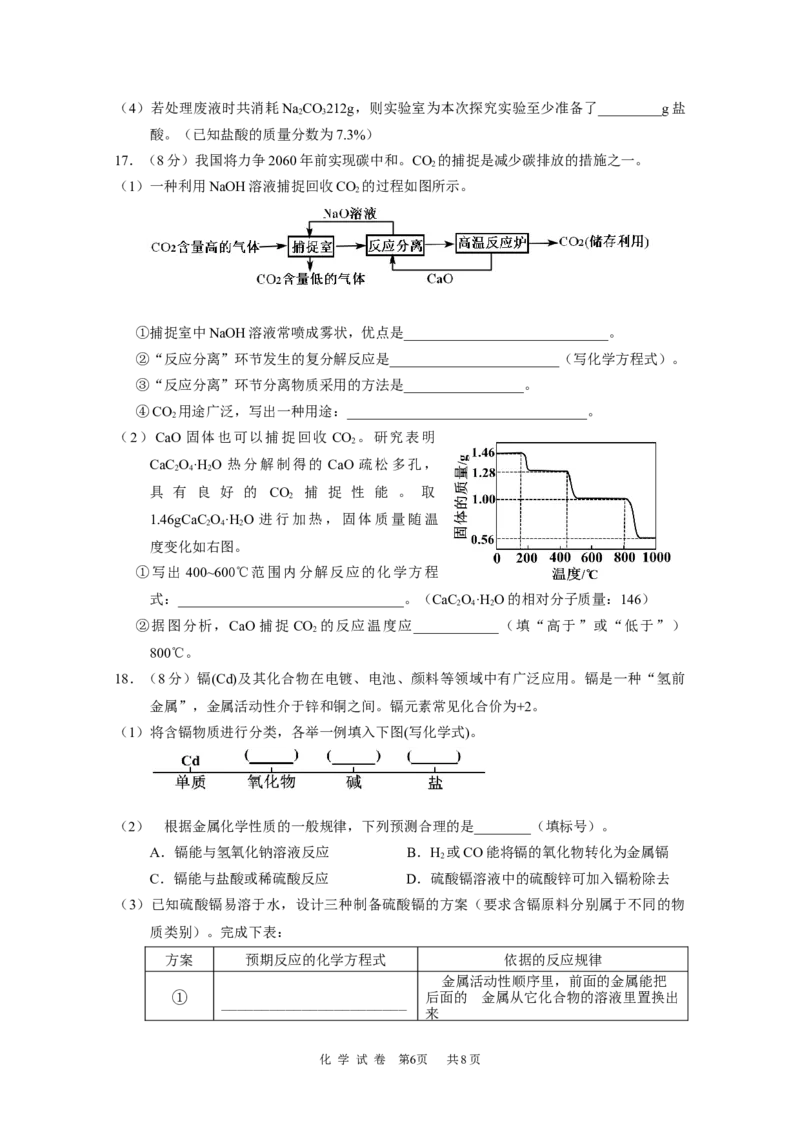
17.(8分)我国将力争2060年前实现碳中和。CO 的捕捉是减少碳排放的措施之一。
2
(1)一种利用NaOH溶液捕捉回收CO 的过程如图所示。
2
①捕捉室中NaOH溶液常喷成雾状,优点是_____________________________。
②“反应分离”环节发生的复分解反应是________________________(写化学方程式)。
③“反应分离”环节分离物质采用的方法是_________________。
④CO 用途广泛,写出一种用途:__________________________________。
2
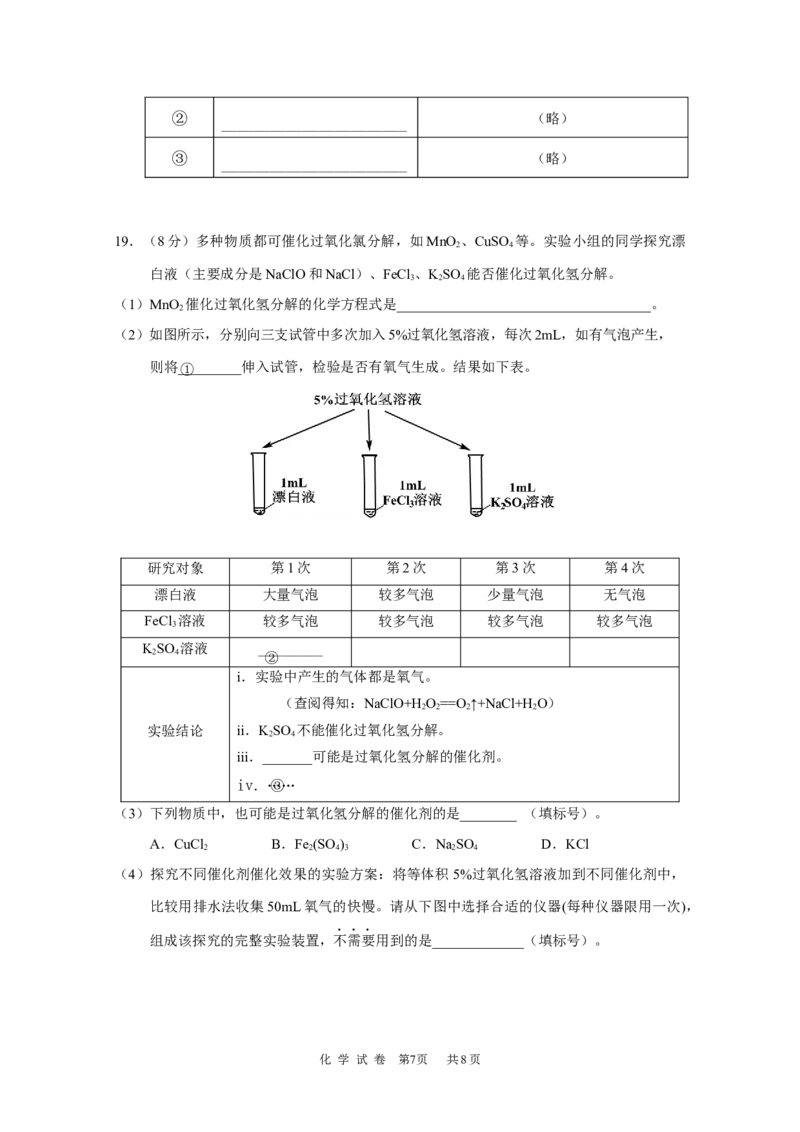
(2)CaO 固体也可以捕捉回收 CO 。研究表明
2
CaC O·H O 热分解制得的 CaO 疏松多孔,
2 4 2
具 有 良 好 的 CO 捕 捉 性 能 。 取
2
1.46gCaC O·H O 进行加热,固体质量随温
2 4 2
度变化如右图。
①写出 400~600℃范围内分解反应的化学方程
式:________________________________。(CaC O·H O的相对分子质量:146)
2 4 2
②据图分析,CaO 捕捉 CO 的反应温度应____________(填“高于”或“低于”)
2
800℃。
18.(8分)镉(Cd)及其化合物在电镀、电池、颜料等领域中有广泛应用。镉是一种“氢前
金属”,金属活动性介于锌和铜之间。镉元素常见化合价为+2。
(1)将含镉物质进行分类,各举一例填入下图(写化学式)。
(2) 根据金属化学性质的一般规律,下列预测合理的是________(填标号)。
A.镉能与氢氧化钠溶液反应 B.H 或CO能将镉的氧化物转化为金属镉
2
C.镉能与盐酸或稀硫酸反应 D.硫酸镉溶液中的硫酸锌可加入镉粉除去
(3)已知硫酸镉易溶于水,设计三种制备硫酸镉的方案(要求含镉原料分别属于不同的物
质类别)。完成下表:
方案 预期反应的化学方程式 依据的反应规律
金属活动性顺序里,前面的金属能把
① 后面的 金属从它化合物的溶液里置换出
_______________________
来
化 学 试 卷 第6页 共8页② (略)
_______________________
③ (略)
_______________________
19.(8分)多种物质都可催化过氧化氯分解,如MnO 、CuSO 等。实验小组的同学探究漂
2 4
白液(主要成分是NaClO和NaCl)、FeCl 、KSO 能否催化过氧化氢分解。
3 2 4
(1)MnO 催化过氧化氢分解的化学方程式是____________________________________。
2
(2)如图所示,分别向三支试管中多次加入5%过氧化氢溶液,每次2mL,如有气泡产生,
则将_①________伸入试管,检验是否有氧气生成。结果如下表。
研究对象 第1次 第2次 第3次 第4次
漂白液 大量气泡 较多气泡 少量气泡 无气泡
FeCl 溶液 较多气泡 较多气泡 较多气泡 较多气泡
3
KSO 溶液 ________
2 4 ②
i.实验中产生的气体都是氧气。
(查阅得知:NaClO+HO==O ↑+NaCl+H O)
2 2 2 2
实验结论 ii.KSO 不能催化过氧化氢分解。
2 4
iii._______可能是过氧化氢分解的催化剂。
iv.…③…
(3)下列物质中,也可能是过氧化氢分解的催化剂的是________ (填标号)。
A.CuCl B.Fe (SO ) C.NaSO D.KCl
2 2 4 3 2 4
(4)探究不同催化剂催化效果的实验方案:将等体积5%过氧化氢溶液加到不同催化剂中,
比较用排水法收集50mL氧气的快慢。请从下图中选择合适的仪器(每种仪器限用一次),
组成该探究的完整实验装置,不需要用到的是_____________(填标号)。
化 学 试 卷 第7页 共8页A B C D E F G H
20.(9分)随着世界人口的增长,人类对农产品需求量增大,增施化肥逐渐成为农作物增
产的最有力措施。NH HCO 、NH Cl、KSO 、KC1都是常见的化肥。
4 3 4 2 4
(1)化肥能为农作物补充的营养元素主要有三种,上述化肥含有的两种营养元素是_______。
(2)有一包用剩的肥料,可能含有上述四种化肥中的一种或几种,为确定其成分,进行了
如下实验:
a.取少量肥料样品于研钵中,加入少量熟石灰混合研磨,有刺激性气味。
b.取少量肥料样品于烧杯中,加水溶解,得到无色溶液A。
c.取少量溶液A于试管中,滴加AgNO 溶液,有白色沉淀产生。
3
d.取少量溶液A于试管中,滴加BaCl 溶液,无明显现象。
2
e.取少量溶液A于试管中,滴加稀盐酸,无明显现象。
①分析上述实验过程,关于该肥料的成分可以得到的结论是_________________________。
②实验a~e中,不必要进行的一项是___________(填标号)。
③设计实验方案进一步确定该肥料的成分,完成下表。
(已知:NH Cl\s\up7(△) NH ↑+ HCl↑)
4 3
实验操作 预期现象与结论
若_______________,则该肥料的成分是
__________。
_____________________
_
若_______________,则该肥料的成分是
__________。
化 学 试 卷 第8页 共8页化 学 试 卷 第9页 共8页