文档内容
第二单元 海水中的重要元素——钠和氯
第一节 钠及其化合物(二)
一、基础巩固
1.某同学结合所学知识探究Na O 与H 能否反应,设计装置如图,下列说法正确的是( )
2 2 2
A.装置A中锌粒可用铁粉代替
B.装置B中盛放碱石灰,目的是除去A中挥发出来的少量水蒸气
C.装置C加热前,必须先用试管在干燥管管口处收集气体,检验气体纯度
D.装置A也可直接用于MnO 与浓盐酸反应制取Cl
2 2
【答案】C
【解析】A.装置A为简易启普发生器,固体应使用不溶于水的颗粒固体,所以锌粒不可用铁粉代替,
故A错误;
B.盐酸易挥发,B装置中应为碱石灰,目的是除去A中挥发出来的HCl和水蒸气,故B错误;
C.氢气具有可燃性,不纯时加热易发生爆炸,则加热试管前,必须先用试管在干燥管管口处收集气体,
检验气体纯度,应先收集气体并点燃,通过爆鸣声判断气体的纯度,故C正确;
D.二氧化锰和浓盐酸应在加热条件下反应制备氯气,A装置不能加热,故D错误。
故选:C。
2.下列钠及其化合物的叙述中正确的是( )
A.Na O与Na O 都能和水反应生成碱,他们都是化合反应
2 2 2
B.Na CO 和NaHCO 都不稳定,受热容易分解
2 3 3
C.Na O 可以作为呼吸面具或潜水艇里的氧气来源
2 2
D.将Na O加到酚酞溶液中,溶液先变色后褪色
2【答案】C
【解析】A、过氧化钠与水反应生成氢氧化钠和氧气,不是化合反应,故A错误;
B、碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,碳酸钠稳定受热不分解,碳酸氢钠不稳定,受热分
解,故B错误;
C.过氧化钠可以和二氧化碳及水反应生成氧气,可用于呼吸面具或潜水艇中作为氧气的来源,故 C正
确;
D.氧化钠与水反应生成氢氧化钠,溶液呈碱性,所以将Na O加到酚酞溶液中,溶液变红色,故D错
2
误;
故选:C。
3.下列物质的变化,不能通过一步化学反应完成的是( )
A.Na
2
O
2
→Na
2
CO
3
B.SO
2
→H
2
SO
4
C.SiO →Na SiO D.SiO →H SiO
2 2 3 2 2 3
【答案】D
【解析】A、过氧化钠与二氧化碳反应生成碳酸钠和氧气,则Na O →Na CO 可以一步转化,故A正
2 2 2 3
确;
B、二氧化硫与过氧化氢反应生成硫酸,则SO →H SO 可以一步转化,故B正确;
2 2 4
C、二氧化硅与碳酸钠的高温条件下反应生成硅酸钠,则SiO →Na SiO 可以一步转化,故C正确;
2 2 3
D、二氧化硅不与水反应,则反应SiO →H SiO 不能一步转化,故D错误;
2 2 3
故选:D。
4.下列叙述中不正确的是( )
A.NaOH、Na CO 、NaHCO 的溶液均呈碱性,所以可以共存
2 3 3
B.Na O 用于呼吸面具,活性炭用于防毒面具,两者原理不同
2 2
C.合金的熔点一般低于成分金属,硬度高于成分金属
D.62g Na O和78g Na O 分别溶于等量且足量的水中,所得溶液中溶质的质量分数相等
2 2 2
【答案】A
【解析】A.NaOH、NaHCO 反应生成Na CO ,不能共存,故A错误;
3 2 3
B.过氧化钠反应生成氧气,则Na O 用于呼吸面具,而活性炭具有吸附性,活性炭用于防毒面具,两
2 2
者原理不同,故B正确;
C.合金是金属和金属或金属和非金属形成具有特征性质的混合物,合金的熔点一般低于成分金属,硬
度要高于成分金属,故C正确;
D.62g Na O和78g Na O 分别溶于等量且足量的水中,溶质均为 2molNaOH,过氧化钠反应生成氧气,
2 2 2增加质量为78g﹣16g=62g,溶液质量相同,则所得溶液中溶质的质量分数相等,故D正确;
故选:A。
5.下列有关焰色反应的理解正确的是( )
只有金属化合物才有焰色反应
①只有某些金属或其化合物才有焰色反应
②铂丝做焰色反应实验,每次做完后都需要用盐酸洗涤,再用自来水洗净后使用
③铂丝做焰色反应实验,每次做完后都需要用盐酸洗涤,在灼烧至酒精灯火焰颜色相同后 再使用
④A. B. C. D.
【答①案③】D ①④ ②③ ②④
【解析】 焰色反应是一种金属元素的性质,不一定是化合物,故错误;
只有某①些金属或其化合物才有焰色反应,非金属元素没有,故正确;
②由于自来水中含矿物质离子,故铂丝做焰色反应实验,每次做完后都需要用盐酸洗涤,再用自来水
③洗净后使用会对实验造成干扰,但也不需用蒸馏水洗涤,故错误;
铂丝做焰色反应实验,每次做完后都需要用盐酸洗涤,在灼烧至酒精灯火焰颜色相同后 再使用,不
④需用蒸馏水洗涤,故正确。
故选:D。
6.白色固体 Na
2
S
2
O
4
常用于织物的漂白,也能将污水中的某些重金属离子还原为单质除去。下列关于
Na
2
S
2
O
4
说法不正确的是( )
A.可以使品红溶液褪色
B.其溶液可用作分析化学中的吸氧剂
C.其溶液可以和 Cl
2
反应,但不能和 AgNO
3
溶液反应
D.已知隔绝空气加热 Na
2
S
2
O
4
分解可生成 SO
2
,则其残余固体产物中可能有 Na
2
S
2
O
3
【答案】C
【解析】A、白色固体 Na
2
S
2
O
4
常用于织物的漂白,说明具有漂白性,可以使品红溶液褪色,故A正
确;
B、也能将污水中的某些重金属离子还原为单质除去,说明具有还原性,则可用作分析化学中的吸氧剂,
故B正确;
C、也能将污水中的某些重金属离子还原为单质除去,说明具有还原性,则可以和 Cl
2
反应,也能和
AgNO
3
溶液发生氧化还原反应,故C错误;
D、由隔绝空气加热 Na
2
S
2
O
4
分解可生成 SO
2
,则硫元素化合价升高,则必有降低的产物,则其残余
固体产物中可能有 Na S O ,故D正确;
2 2 3故选:C。
7.(1)Na O (填“是”或“否”)属于碱性氧化物,Na O 是 色固体粉末。向包有Na O 固
2 2 2 2 2 2
体的棉花上滴几滴水,棉花很快燃烧起来,原因是该反应有氧气生成且该反应为 (填”吸热”或
者“放热”)反应;
(2)Na O 作为在潜水艇和消防员呼吸面具中的供氧剂,写出其中一个反应的化学方程式
2 2
,某潜水艇中有50人,若每人每小时消耗O 在标准状况下的体积为44.8L,(标准状况下O 的密度
2 2
1.429g/L),假设所需要的O 全由Na O 所提供,则每小时所需Na O 的质量为 Kg。
2 2 2 2 2
(3)3.1 g Na O溶于水配成1L溶液,溶液中Na+离子物质的量浓度为 。
2
(4)制备Fe(OH) 胶体:用洁净的烧杯取一定量蒸馏水,用酒精灯加热至沸腾,向烧杯中加入几滴
3
饱和FeCl 溶液继续加热至液体呈透明的红褐色。
3
写出制备Fe(OH) 胶体反应的离子方程式 ,
3
①验证制得的分散系是胶体的方法为 。
②【答案】(1)否; 淡黄(或者“黄”); 放热;
(2)2Na O +2CO =2Na CO +O 、2Na O +2H O=4NaOH+O ↑;15.6;
2 2 2 2 3 2 2 2 2 2
(3)0.1mol•L﹣1;
(4) Fe3++3H O Fe(OH) (胶体)+3H+;
2 3
①
利用丁达尔效应实验或“用一束可见光照射是否看到一条光亮的通路。
②【解析】(1)过氧化钠与硫酸反应的方程式为:2Na
2
O
2
+2H
2
SO
4
=2Na
2
SO
4
+2H
2
O+O
2
↑,生成物中除
盐和水外还有氧气,不是碱性氧化物,Na O 是淡黄色固体粉末,棉花能燃烧,说明Na O 与H O的反
2 2 2 2 2
应属于放热反应,过氧化钠和水反应生成氢氧化钠和氧气,方程式为2Na O +2H O=4NaOH+O ↑,
2 2 2 2
故答案为:否; 淡黄(或者“黄”); 放热;
(2)过氧化钠,用于呼吸面具,则主要是与CO 、H O反应,生成O ,化学方程式为:2Na O +2CO
2 2 2 2 2 2
=2Na CO +O 、2Na O +2H O=4NaOH+O ↑,潜水艇中有50人,若每人每小时消耗O 在标准状况下
2 3 2 2 2 2 2 2
的体积为44.8L,(标准状况下O 的密度1.429g/L),潜水艇中有50人,若每人每小时消耗O 在标准
2 2
状况下的体积为44.8L,(标准状况下O 的密度1.429g/L),所需要的O 的物质的量为2mol×50=
2 2
100mol,假设所需要的 O 全由 Na O 所提供,根据 2Na O ~O 、需过氧化钠 200mol,质量为
2 2 2 2 2 2
200mol×78g/mol=15600g=15.6kg,
故答案为:2Na O +2CO =2Na CO +O 、2Na O +2H O=4NaOH+O ↑;15.6;
2 2 2 2 3 2 2 2 2 2
(3)Na O 溶于水生成氢氧化钠,Na O+2H O=2NaOH,3.1 g Na O 溶于水生成 n(NaOH)=
2 2 2 2×2=0.1mol,C= = =0.1mol/L,
故答案为:0.1mol•L﹣1;
(4) 实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即
①
停止加热,反应的化学方程式为:FeCl +3H O Fe(OH) +3HCl,离子方程式为:Fe3++3H O
3 2 3 2
Fe(OH) (胶体)+3H+,
3
故答案为:Fe3++3H O Fe(OH) (胶体)+3H+;
2 3
可以用可见光束照射胶体和溶液,出现光亮的通道的是胶体,否则是溶液,验证制得的分散系是胶
②体的方法为利用丁达尔效应实验或“用一束可见光照射是否看到一条光亮的通路,
故答案为:利用丁达尔效应实验或“用一束可见光照射是否看到一条光亮的通路。
二、拓展提升
8.现有 Al O Fe O Na O CuO NaCl NaHCO Na SiO 七种物质。请你根据已有的知识,
2 3 2 3 2 2 3 2 3
选择合①适的物质②,用数③字序号填④空: ⑤ ⑥ ⑦
(1)海水中主要含有的电解质是 ;
(2)常作为潜水艇和呼吸面具中氧气来源的淡黄色固体是 ;
(3)常用于焙制糕点的是 ;
(4)可用于制备硅胶和木材防火剂的是 ;
(5)属于两性氧化物的是 ;
(6)可用作油漆和涂料的红棕色固体是 。
【答案】(1) ;
(2) ; ⑤
(3)③;
(4)⑥;
(5)⑦;
(6)①。
【解析②】(1)海水中主要含有的电解质是氯化钠,故答案为: ;
(2)常作为潜水艇和呼吸面具中氧气来源的淡黄色固体是过氧⑤化钠,故答案为: ;
(3)常用于焙制糕点的是碳酸氢钠,故答案为: ; ③
(4)可用于制备硅胶和木材防火剂的是硅酸钠,⑥故答案为: ;
⑦(5)属于两性氧化物的是氧化铝,故答案为: ;
(6)可用作油漆和涂料的红棕色固体是氧化铁①,故答案为: 。
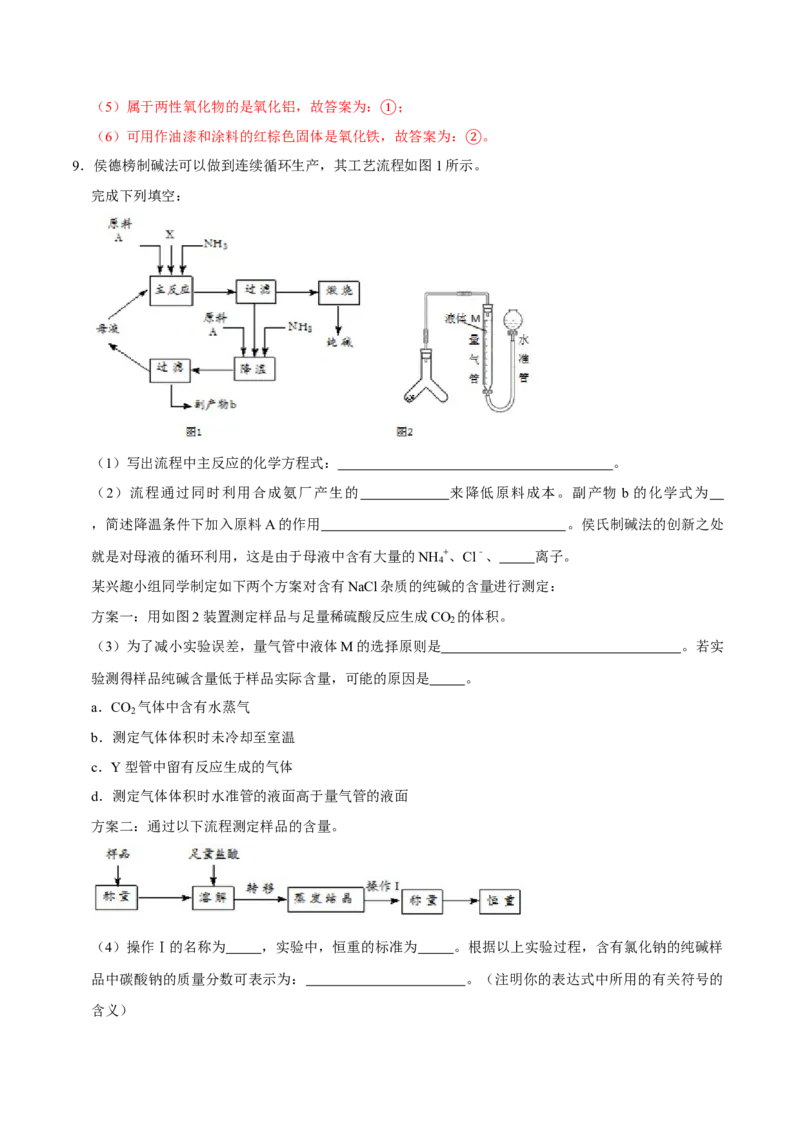
9.侯德榜制碱法可以做到连续循环生产,其工艺流程如图1所示②。
完成下列填空:
(1)写出流程中主反应的化学方程式: 。
(2)流程通过同时利用合成氨厂产生的 来降低原料成本。副产物 b的化学式为
,简述降温条件下加入原料A的作用 。侯氏制碱法的创新之处
就是对母液的循环利用,这是由于母液中含有大量的NH +、Cl﹣、 离子。
4
某兴趣小组同学制定如下两个方案对含有NaCl杂质的纯碱的含量进行测定:
方案一:用如图2装置测定样品与足量稀硫酸反应生成CO 的体积。
2
(3)为了减小实验误差,量气管中液体M的选择原则是 。若实
验测得样品纯碱含量低于样品实际含量,可能的原因是 。
a.CO 气体中含有水蒸气
2
b.测定气体体积时未冷却至室温
c.Y型管中留有反应生成的气体
d.测定气体体积时水准管的液面高于量气管的液面
方案二:通过以下流程测定样品的含量。
(4)操作Ⅰ的名称为 ,实验中,恒重的标准为 。根据以上实验过程,含有氯化钠的纯碱样
品中碳酸钠的质量分数可表示为: 。(注明你的表达式中所用的有关符号的
含义)【答案】(1)NaCl+CO +NH +H O=NaHCO ↓+NH Cl;
2 3 2 3 4
(2)NH 、CO ;NH Cl;Cl﹣浓度提高有利于NH Cl析出;Na+、CO 2﹣;
3 2 4 4 3
(3)CO 不溶解于液体M且不与之反应;d;
2
(4冷却;连续两次称量质量差小于等于0.001g; ,m ﹣﹣样品的质量,m ﹣﹣
1 2
恒重后样品的质量。
【解析】(1)候德榜制碱法中是利用NaCl、CO 、NH 为原料制取NaHCO ,同时得到NH Cl,再煅
2 3 3 4
烧NaHCO 得到纯碱,所以主反应方程式为NaCl+CO +NH +H O=NaHCO ↓+NH Cl,
3 2 3 2 3 4
故答案为:NaCl+CO +NH +H O=NaHCO ↓+NH Cl;
2 3 2 3 4
(2)流程通过同时利用合成氨厂产生的NH 、CO 来降低原料成本,通过以上分析知,b为NH Cl;
3 2 4
降温条件下加入原料A(NaCl)能增大氯离子浓度,有利于NH Cl析出;侯氏制碱法的母液中含有大
4
量溶质中的离子,所以母液中含有大量NH +、Cl﹣、Na+、CO 2﹣,
4 3
故答案为:NH 、CO ;NH Cl;Cl﹣浓度提高有利于NH Cl析出;Na+、CO 2﹣;
3 2 4 4 3
(3)实验目的是测定二氧化碳体积,所以二氧化碳不能溶解与 M液体且不能和M液体反应,所以量
气管中液体M的选择原则是CO 不溶解于液体M且不与之反应;
2
a.CO 气体中含有水蒸气,水蒸气看作二氧化碳,导致二氧化碳体积偏大,则实验测得样品纯碱含量
2
高于样品实际含量,故错误;
b.测定气体体积时未冷却至室温,气体有热胀冷缩的性质,导致二氧化碳体积偏大,则实验测得样品
纯碱含量高于样品实际含量,故错误;
c.Y型管中留有反应生成的气体,原来Y型管中含有气体,所以测量气体体积不变,则实验测得样品
纯碱含量等于样品实际含量,故错误;
d.测定气体体积时水准管的液面高于量气管的液面,导致左侧气体压强增大,二氧化碳气体体积偏小,
则实验测得样品纯碱含量低于样品实际含量,故正确;
故答案为:CO 不溶解于液体M且不与之反应;d;
2
(4)样品称量后加入水溶解,然后和足量稀盐酸反应,转移至蒸发皿中蒸发结晶得到NaCl固体,冷
却至室温后称量固体,所以操作I为冷却; 连续两次称量质量差小于等于0.001g时为恒重;设样品质
量为m g,恒重后样品的质量m g,根据Na原子守恒得关系式为Na CO ~2NaCl,反应前后固体质量
1 2 2 3
差为(m ﹣m )g,
2 1
设碳酸钠实际质量为x,
Na CO ~2NaCl 二者之差
2 3106 117 11
x (m ﹣m )g
2 1
106:11=x:(m ﹣m )g
2 1
x= ×106
样品中碳酸钠质量分数= ×100%= ×100%= ,
故答案为:冷却;连续两次称量质量差小于等于0.001g; ,m ﹣﹣样品的质量,
1
m ﹣﹣恒重后样品的质量。
2
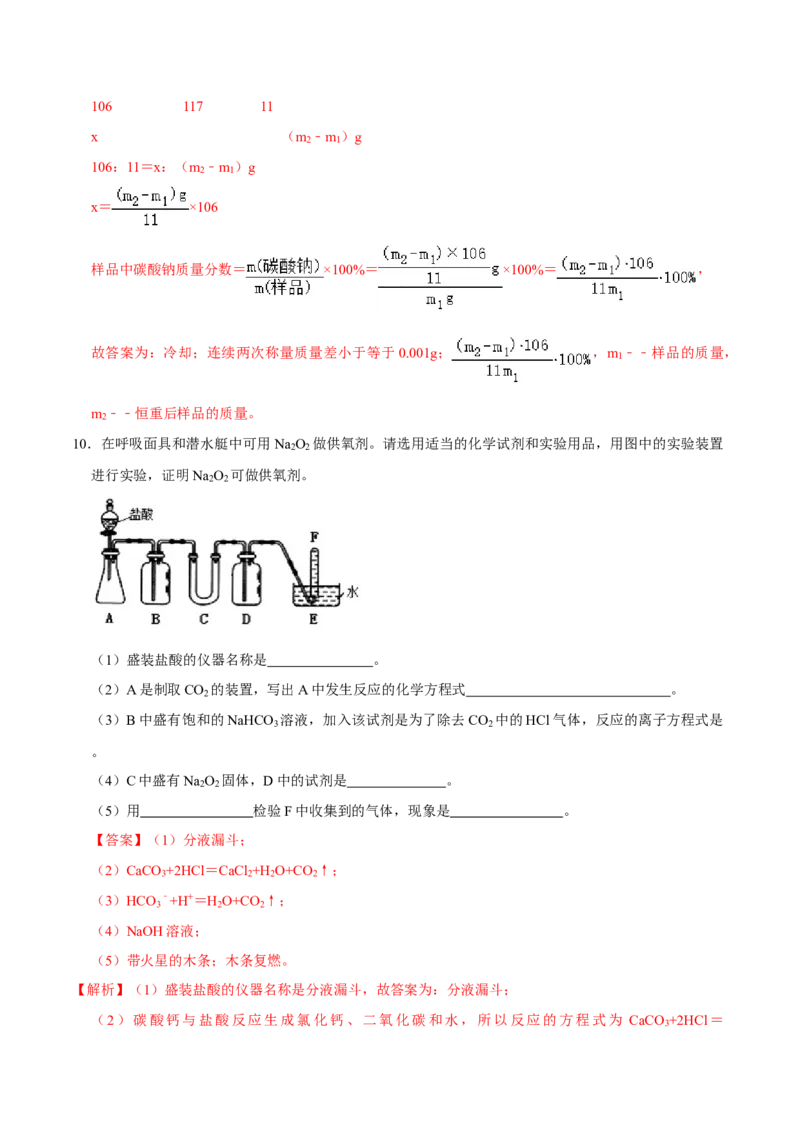
10.在呼吸面具和潜水艇中可用Na O 做供氧剂。请选用适当的化学试剂和实验用品,用图中的实验装置
2 2
进行实验,证明Na O 可做供氧剂。
2 2
(1)盛装盐酸的仪器名称是 。
(2)A是制取CO 的装置,写出A中发生反应的化学方程式 。
2
(3)B中盛有饱和的NaHCO 溶液,加入该试剂是为了除去CO 中的HCl气体,反应的离子方程式是
3 2
。
(4)C中盛有Na O 固体,D中的试剂是 。
2 2
(5)用 检验F中收集到的气体,现象是 。
【答案】(1)分液漏斗;
(2)CaCO +2HCl=CaCl +H O+CO ↑;
3 2 2 2
(3)HCO ﹣+H+=H O+CO ↑;
3 2 2
(4)NaOH溶液;
(5)带火星的木条;木条复燃。
【解析】(1)盛装盐酸的仪器名称是分液漏斗,故答案为:分液漏斗;
(2)碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,所以反应的方程式为 CaCO +2HCl=
3CaCl +H O+CO ↑,故答案为:CaCO +2HCl=CaCl +H O+CO ↑;
2 2 2 3 2 2 2
(3)碳酸氢钠与盐酸反应生成氯化钠、二氧化碳和水,离子反应方程式为:HCO ﹣+H+=
3
H O+CO ↑,故答案为:HCO ﹣+H+=H O+CO ↑;
2 2 3 2 2
(4)D中的试剂是氢氧化钠吸收未反应的二氧化碳气体,所以D中的试剂是NaOH溶液,故答案为:
NaOH溶液;
(5)用带火星的木条检验F中收集到的气体,如果木条复燃证明气体是氧气,故答案为:带火星的木
条;木条复燃。