文档内容
2016 年 10 月浙江省普通高校招生选考考试
A.氯化钠的电子式:
B.二氧化碳的结构式:O—C—O
化学试题
C.S2-的结构示意图:
D.葡萄糖的分子式:C H O
一、选择题(本大题共25小题,每小题2分,共50分。每小题列出的四个备选项中只有一个是符合题目要求的, 6 12 6
不选、多选、错选均不得分) 8.下列能使品红溶液褪色的是( )
1.下列属于酸的是( )
A.SO
2
B.BaSO
4
A.HSO B.CO
C.KCl D.CO
2
2 4 2
C.NaCl D.NaOH 9.下列属于可再生能源的是( )
2.下列仪器名称为“分液漏斗”的是( )
A.氢能 B.石油
C.煤 D.天然气
10.下列说法正确的是( )
A.用过滤的方法可以除去食盐水中的泥沙
B.酒精灯加热烧瓶时不用垫石棉网
3.下列属于电解质的是( ) C.氯化氢气体能使干燥的蓝色石蕊试纸变红
A.酒精 B.蔗糖 D.盛放氢氧化钠溶液的玻璃瓶,可以使用橡胶塞或玻璃塞
C.硝酸钾 D.铜丝 11.下列说法不正确的是( )
4.下列反应中,水作氧化剂的是( ) A.6C表示质子数为6、中子数为8的核素
A.C+HO=====CO+H
2 2
B.H 2 +CuO=====Cu+H 2 O B.甲醇(CH 3 OH)和甘油( )互为同系物
C.Cl 2 +H 2 O HCl+HClO C.C 5 H 12 的同分异构体有3种,其沸点各不相同
D.SO 3 +H 2 O===H 2 SO 4 D.CH 3 CH 2 CH 2 CH(CH 3 ) 2 的名称是2甲基戊烷
5.下列物质的水溶液因水解而呈酸性的是( ) 12.在一定条件下,可逆反应X(g)+2Y(g) 2Z(g) ΔH=-a kJ·mol-1,达到化学平衡时,下列说法一定正
A.NaOH B.(NH )SO 确的是 ( )
4 2 4
C.NaCO D.NaCl A.反应放出a kJ热量
2 3
6.下列说法不正确的是( ) B.X和Y的物质的量之比为1∶2
A.氯化钠可用于配制生理盐水 C.反应物和生成物的浓度都不再发生变化
B.二氧化硅可用于制造玻璃 D.X的正反应速率等于Z的逆反应速率
C.海水中的钠元素以单质存在
13.下列离子方程式正确的是( )
D.氧化镁(熔点2 800 ℃)是优良的耐高温材料
A.金属钠和水反应:Na+2HO===Na++2OH-+H↑
7.下列表示正确的是( ) 2 2
B.用氢氧化钠溶液吸收少量二氧化硫气体:SO +2OH-===SO+HO
2 2C.硫酸铵溶液和氢氧化钡溶液反应:Ba2++SO===BaSO↓ D.铁片里的铁和碳与食盐水形成无数微小原电池,发生了电化学腐蚀
4
D.碳酸氢钠溶液和过量的澄清石灰水混合: 18.为证明醋酸是弱电解质,下列方法不正确的是( )
2HCO+Ca2++2OH-===CaCO ↓+2HO+CO A.测定0.1 mol·L-1醋酸溶液的pH
3 2
14.W、X、Y、Z四种短周期元素,它们在周期表中位置如图所示,下列说法不正确的是( ) B.测定0.1 mol·L-1CHCOONa溶液的酸碱性
3
C.比较浓度均为0.1 mol·L-1盐酸和醋酸溶液的导电能力
D.比较相同物质的量浓度的NaOH溶液和醋酸溶液恰好反应完全时消耗两溶液的体积
19.根据能量变化示意图,下列热化学方程式正确的是( )
A.W、Y、X三种元素的原子半径依次减小
B.Z元素的气态氢化物的热稳定性比Y的高
C.W元素与氢元素可能会形成WH
2 6
D.Y元素的单质能从NaZ溶液中置换出Z元素的单质
15.下列说法正确的是( )
A.N(g)+3H(g)===2NH (g) ΔH=-(b-a) kJ·mol-1
2 2 3
A.甲烷分子的比例模型为 ,其二氯取代物有2种结构 B.N(g)+3H(g)===2NH (g) ΔH=-(a-b) kJ·mol-1
2 2 3
B.苯和乙烯都能使溴水褪色,其褪色原理相同 C.2NH (l)===N(g)+3H(g) ΔH=2(a+b-c) kJ·mol-1
3 2 2
C.相同质量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的物质的量相同 D.2NH (l)===N(g)+3H(g) ΔH=2(b+c-a) kJ·mol-1
3 2 2
D.在一定条件下,苯与氯气生成氯苯的反应类型是加成反应 20.下列说法不正确的是( )
16.下列说法正确的是( ) A.Cl、Br 、I 的分子间作用力依次减小
2 2 2
A.油脂、糖类和蛋白质均为高分子化合物 B.石英是由硅原子和氧原子构成的原子晶体,加热熔化时需破坏共价键
B.植物秸秆的主要成分是纤维素,纤维素在催化剂作用下经水解可得葡萄糖,葡萄糖在酒化酶的作用下能转化 C.氢氧化钠在熔融状态下离子键被削弱,形成自由移动的离子,具有导电性
为酒精 D.水电解生成氢气和氧气,有化学键的断裂和形成
C.往含硫酸的淀粉水解液中加入银氨溶液,水浴加热后无银镜产生,说明淀粉未水解
21.为研究某溶液中溶质R的分解速率的影响因素,分别用三份不同初始浓度的R溶液在不同温度下进行实验,
D.向鸡蛋清的溶液中加入甲醛溶液,可观察到蛋白质发生凝聚,再加入蒸馏水,振荡后蛋白质又发生溶解
c(R)随时间变化如图。下列说法不正确的是( )
17.在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片上有铁锈出现。铁片腐蚀过程中发生的总化
学方程式:2Fe+2HO+O===2Fe(OH) ,Fe(OH) 进一步被氧气氧化为Fe(OH) ,再在一定条件下脱水生成铁锈,
2 2 2 2 3
其原理如图。下列说法正确的是( )
A.铁片发生还原反应而被腐蚀
A.25 ℃时,在10~30 min内,R的分解平均速度为0.030 mol·L-1·min-1
B.铁片腐蚀最严重区域应该是生锈最多的区域
B.对比30 ℃和10 ℃曲线,在50 min时,R的分解百分率相等
C.铁片腐蚀中负极发生的电极反应:2HO+O+4e-===4OH-
2 2
C.对比30 ℃和25 ℃曲线,在0~50 min内,能说明R的分解平均速度随温度升高而增大D.对比30 ℃和10 ℃曲线,在同一时刻,能说明R的分解速率随温度升高而增大 二、非选择题(本大题共7小题,共50分)
22.设N 为阿伏加德罗常数的值,下列说法正确的是( ) 26.(6分)烃A是一种重要的化工原料。已知A在标准状况下的密度为1.25 g·L-1,B可发生银镜反应。它们之间
A
A.2.8 g铁粉与50 mL 4 mol·L-1盐酸反应转移电子的数目为0.15N 的转化关系如图:
A
B.常温下1 L pH=13的氢氧化钠溶液中由水电离出的H+的数目为0.1N
A
C.标准状况下,8.96 L氢气、一氧化碳的混合气体完全燃烧,消耗氧分子的数目为0.2N
A
D.1.2 g金刚石与石墨的混合物中含有碳碳单键的数目为0.4N
A
23.常温下,用浓度为0.100 mol·L-1的NaOH溶液分别逐滴加入到20.00 mL 0.100 0 mol·L-1的HX、HY溶液中,
pH随NaOH溶液体积的变化如图。下列说法正确的是( )
请回答:
(1)有机物B中含有的官能团名称是________。
(2)第⑤步发生加成反应,该反应的化学方程式是____________________________________。
(3)将金属钠与有机物 D 反应所得的少量产物溶于水,滴加 2 滴酚酞溶液,水溶液显红色,其原因是
____________________________(用化学方程式表示)。
(4)下列说法正确的是______。
A.V(NaOH)=10.00 mL时,两份溶液中c(X-)>c(Y-) A.有机物A与D在一定条件下可反应生成乙醚[(CH CH)O]
3 2 2
B.V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) B.用新制碱性氢氧化铜悬浊液无法区分有机物B、C和D
C.V(NaOH)=20.00 mL时,c(OH-)>c(H+)>c(Na+)>c(X-) C.通过直接蒸馏乙酸乙酯和有机物C的混合物,可分离得到纯的乙酸乙酯
D.pH=7时,两份溶液中c(X-)=c(Na+)=c(Y-) D.相同条件下乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全
24.已知还原性:SO >I-。向含a mol KI和a mol KSO 的混合液中通入b mol Cl 充分反应(不考虑Cl 与I 之 27.(6分)为探究不溶性盐X(仅含四种元素)的组成和性质,设计并完成如下实验:
2 3 2 2 2
间的反应)。下列说法不正确的是 ( )
A.当a≥b时,发生的离子反应为SO+Cl+HO===SO+2H++2Cl-
2 2
B.当5a=4b时,发生的离子反应为4SO+2I-+5Cl+4HO===4SO+I+8H++10Cl-
2 2 2
C.当a≤b≤a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol
请回答:
D.当a<b<时,溶液中SO、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b
(1)X的组成元素为H、O和______(用元素符号表示),化学式为________。
25.已知:Ag SO 微溶于水,可溶于硝酸。溶液X中可能含有Na+、Ca2+、Fe2+、Cl-、Br-、CO、SiO、SO中
2 4 (2)写出经一步反应能得到X的化学方程式(要求非氧化还原反应)_______________________。
的几种离子。为了确定其组成,某同学进行了如下实验:
28.(4分)用无水NaCO 固体配制250 mL 0.100 0 mol·L-1的溶液。
2 3
请回答:
(1)在配制过程中不必要的玻璃仪器是________。
A.烧杯 B.量筒 C.玻璃棒 D.胶头滴管 E.容量瓶
下列说法正确的是( )
(2)定容时的操作:当液面接近容量瓶刻度线时,______________________________________,再将容量瓶塞盖
A.溶液X中一定含有Na+、Cl-和SiO
好,反复上下颠倒,摇匀。
B.溶液X中一定不含Ca2+、Br-
(3)下列操作会使配得的NaCO 溶液浓度偏低的是________。
2 3
C.为确定溶液X中是否含有SO,可取溶液2,加入BaCl 溶液
2 A.称取相同质量的NaCO ·10H O固体进行配制
3 2
D.在溶液X中依次滴入盐酸、双氧水和硫氰化钾溶液后,溶液将变成血红色
B.定容时俯视容量瓶的刻度线
C.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线D.转移洗涤液时洒到容量瓶外,继续用该未清洗的容量瓶重新配制 __________________________________________________________________。
29.(4分)为确定NaCO 和NaHCO 混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度盐酸 31.(加试题)(10分)某研究小组在实验室以含铁的铜屑为原料制备Cu(NO )·3H O晶体,并进一步探究用SOCl
2 3 3 3 2 2 2
30.0 mL,充分反应,产生CO 的体积(已折算成标准状况下的体积,不考虑CO 在水中的溶解)如下表: 制备少量无水Cu(NO )。设计的合成路线如下:
2 2 3 2
实验序号 Ⅰ Ⅱ Ⅲ Ⅳ
盐酸体积(mL) 30.0 30.0 30.0 30.0
样品质量(g) 2.96 3.70 5.18 6.66
CO 体积(mL) 672 840 896 672
2
已知:Cu(NO )·3H O――→Cu(NO )·Cu(OH) ――→CuO
(1)样品中的物质的量之比n(Na CO)∶n(NaHCO )=________。 3 2 2 3 2 2
2 3 3
SOCl 熔点-105 ℃、沸点76 ℃、遇水剧烈水解生成两种酸性气体。
(2)盐酸的物质的量浓度c(HCl)=________。 2
请回答:
30.(加试题)(10分)氯及其化合物在生活和生产中应用广泛。
(1)第②步调pH适合的物质是____________(填化学式)。
(1)已知:900 K时,4HCl(g)+O(g) 2Cl (g)+2HO(g),反应自发。
2 2 2
(2) 第 ③ 步 包 括 蒸 发 浓 缩 、 冷 却 结 晶 、 抽 滤 等 步 骤 , 其 中 蒸 发 浓 缩 的 具 体 操 作 是
①该反应是放热还是吸热,判断并说明理由__________________________________________。
_________________________________________________。为得到较大颗粒的Cu(NO )·3H O晶体,可采用的方
②900 K时,体积比为4∶1的HCl和O 在恒温恒容的密闭容器中发生反应,HCl的平衡转化率α(HCl)随压强(p) 3 2 2
2
法是____________________(填一种)。
变化曲线如图,保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在1.5×105~4.5×105 Pa范围
(3)第④步中发生的反应化学方程式是_____________________________________________。
内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。
(4)第④步,某同学设计的实验装置示意图(夹持及控温装置省略,如图1)有一处不合理,请提出改进方案并说明
理由________________________________________。
(2)已知:Cl(g)+2NaOH(aq)===NaClO(aq)+NaCl(aq)+HO(l) ΔH=-102 kJ·mol-1
2 2 1
3Cl(g)+6NaOH(aq)===5NaCl(aq)+NaClO(aq)+3HO(l) ΔH=-422 kJ·mol-1
2 3 2 2
①写出在溶液中NaClO分解生成NaClO 的热化学方程式:_____________________________。 图1
3
②用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO),此时ClO-的浓度为c mol·L-1;加热时 装置改进后,向仪器A中缓慢滴加SOCl 时,需打开活塞________(填“a”、“b”或“a和b”)。
3 0 2
NaClO转化为NaClO ,测得t时刻溶液中ClO-浓度为c mol·L-1,写出该时刻溶液中Cl-浓度的表达式:c(Cl-) (5)为测定无水Cu(NO ) 产品的纯度,可用分光光度法。
3 1 3 2
=________(用c、c 表示)mol·L-1。 已知:4NH ·H O+Cu2+===Cu(NH )+4HO;Cu(NH )对特定波长光的吸收程度(用吸光度A表示)与Cu2+在一定
0 1 3 2 3 2 3
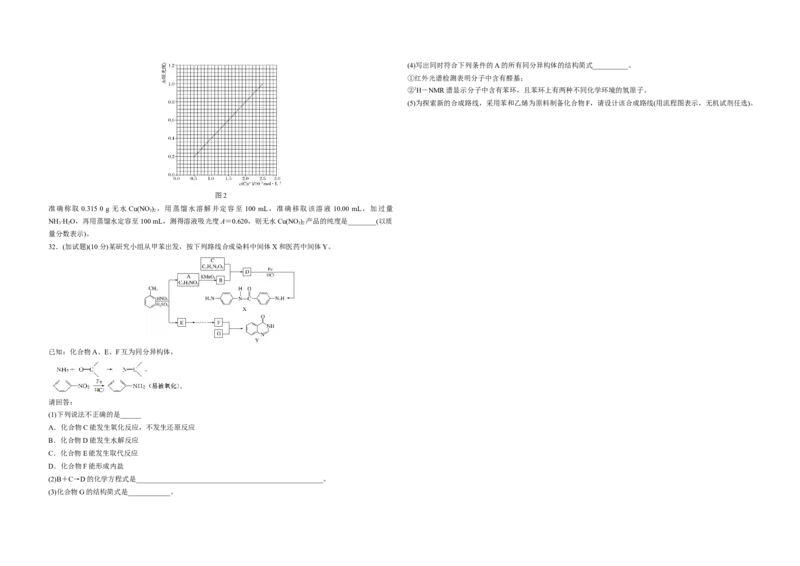
③有研究表明,生成NaClO 的反应分两步进行: 浓度范围内成正比。现测得Cu(NH )的吸光度A与Cu2+标准溶液浓度关系如图2所示:
3 3
Ⅰ.2ClO-===ClO+Cl-
Ⅱ.ClO+ClO-===ClO+Cl-
常温下,反应Ⅱ能快速进行,但氯气与 NaOH 溶液反应很难得到 NaClO ,试用碰撞理论解释其原因:
3
______________________________________________________。
(3)电解NaClO 水溶液可制备NaClO 。在电解过程中由于阴极上吸附氢气,会使电解电压升高,电解效率下降。
3 4
为 抑 制 氢 气 的 产 生 , 可 选 择 合 适 的 物 质 ( 不 引 入 杂 质 ) , 写 出 该 电 解 的 总 化 学 方 程 式(4)写出同时符合下列条件的A的所有同分异构体的结构简式__________。
①红外光谱检测表明分子中含有醛基;
②1H-NMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子。
(5)为探索新的合成路线,采用苯和乙烯为原料制备化合物F,请设计该合成路线(用流程图表示,无机试剂任选)。
图2
准确称取 0.315 0 g 无水 Cu(NO ) ,用蒸馏水溶解并定容至 100 mL,准确移取该溶液 10.00 mL,加过量
3 2
NH ·H O,再用蒸馏水定容至100 mL,测得溶液吸光度A=0.620,则无水Cu(NO ) 产品的纯度是________(以质
3 2 3 2
量分数表示)。
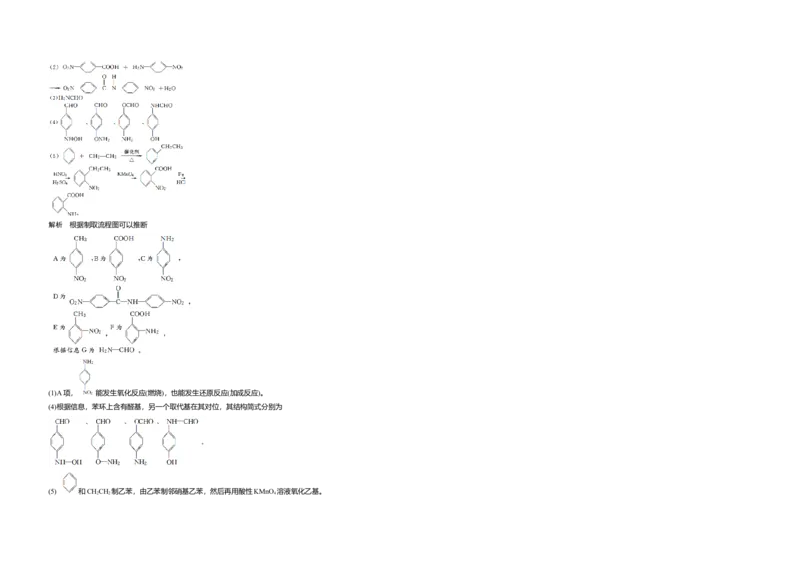
32.(加试题)(10分)某研究小组从甲苯出发,按下列路线合成染料中间体X和医药中间体Y。
已知:化合物A、E、F互为同分异构体,
请回答:
(1)下列说法不正确的是______
A.化合物C能发生氧化反应,不发生还原反应
B.化合物D能发生水解反应
C.化合物E能发生取代反应
D.化合物F能形成内盐
(2)B+C→D的化学方程式是_____________________________________________________。
(3)化合物G的结构简式是____________。化学参考答案
,其名称为2甲基戊烷。
12.C
1.A
解析 A项,由于该反应为可逆反应,且没给出反应物物质的量,所以反应放出热量不确定;B项,达到平衡时,
解析 酸是电离时生成的阳离子全部是H+的化合物,CO 为酸性氧化物,NaCl属于盐,NaOH属于碱。
2
X、Y的物质的量之比不一定为1∶2,它和起始量、转化率均有关系;D项,达到平衡时,X的正反应速率与Z
2.B
的逆反应速率应符合其化学计量数之比。
解析 A为烧杯,C为容量瓶,D为烧瓶。
13.B
3.C
解析 A项,不符合电子守恒,应为2Na+2HO===2Na++2OH-+H↑;C项,应为2NH+SO+Ba2++2OH-
解析 酒精、蔗糖属于非电解质,铜丝属于单质,既不是电解质,也不是非电解质。 2 2
===BaSO↓+2NH ·H O;D项,应为HCO+Ca2++OH-===CaCO ↓+HO。
4.A 4 3 2 3 2
14.D
解析 B项,H 还原CuO,H 作还原剂,HO是氧化产物;C项,Cl 和HO反应,Cl 既是氧化剂又是还原剂;
2 2 2 2 2 2
解析 根据元素在周期表中的位置,可以推断,X为O,Y为S,Z为Cl,W为Si。A项,同周期原子半径逐渐
D项,SO 和HO反应不是氧化还原反应。
3 2
减小,同族元素从上到下,随电子层数增多,原子半径增大;B项,稳定性HCl>HS;C项,由于C可形成
5.B 2
C H,Si和C是同主族元素,所以Si也可能形成Si H;D项,Cl+NaS===S↓+2NaCl,反过来不能进行。
解析 A项,NaOH水溶液显碱性是因为NaOH的电离;C项,NaCO 的水溶液因为CO的水解呈碱性;D项, 2 6 2 6 2 2
2 3
15.C
NaCl的水溶液呈中性。
解析 A项,由于甲烷是正四面体结构,所以它的二氯代物只有一种;B项,苯使溴水褪色因为萃取,而乙烯使
6.C
溴水褪色是因为发生加成反应;C项,由于乙炔和苯的最简式相同,所以当质量相同时,其耗氧量也相同;D项,
解析 配制生理盐水用的是食盐;工业上利用SiO 、NaCO 、CaCO 在高温下制造普通玻璃;MgO的熔点很高,
2 2 3 3
苯与氯气反应生成氯苯,发生取代反应。
所以可用作耐高温材料;在海水中钠元素是以Na+形式存在。
16.B
7.D
解析 A项,油脂、糖类中的单糖、二糖均不是高分子化合物;C项,在加银氨溶液之前,应加入NaOH溶液中
解析 A项,NaCl的电子式应为Na+[Cl]-;B项,二氧化碳的结构式应为OCO;C项,S2-的结构示意图:
和硫酸;D项,甲醛能使蛋白质变性。
17.D
。
解析 A项,在铁的吸氧腐蚀过程中,铁片发生氧化反应而被腐蚀;B项,铁片负极腐蚀最严重,由于离子的移动,
8.A
在正极区域生成铁锈最多;C项,铁片负极反应式应为Fe-2e-===Fe2+。
解析 SO 和品红发生化合反应而使品红溶液褪色,但褪色不稳定,加热会恢复红色。
2 18.D
9.A
解析 A项,若0.1 mol·L-1醋酸溶液的pH>1,则证明醋酸是弱电解质;B项,若0.1 mol·L-1 CHCOONa溶液
3
解析 石油、煤、天然气属于传统能源,均不能再生。
呈碱性,则证明CHCOO-发生水解,从而证明CHCOOH是弱电解质;C项,比较浓度均为0.1 mol·L-1的盐酸
3 3
10.A
和醋酸溶液的导电能力,若前者强,则证明醋酸是弱电解质;D项,当NaOH溶液和醋酸溶液的物质的量浓度
解析 B项,烧瓶不能用酒精灯直接加热,应垫石棉网;C项,氯化氢在水中才能发生电离,所以氯化氢气体不
相同时,恰好完全反应时,消耗两溶液的体积也相同,无法证明醋酸是弱电解质。
能使干燥的蓝色石蕊试纸变红;D项,由于玻璃中的SiO 能和NaOH反应,所以盛放NaOH的试剂瓶不能用玻
2
19.D
璃塞,应用橡胶塞。
解析 根据图示,N(g)+3H(g) 2NH (g) ΔH=-2(b-a) kJ·mol-1,所以,A、B两项错误,根据图示:
2 2 3
11.B
2NH (l)===N(g)+3H(g) ΔH=2(b+c-a) kJ·mol-1,所以C项错误,D项正确。
3 2 2
解析 A项,6C中质子数为6,中子数为8;B项,CHOH是一元醇,而甘油是三元醇,所以它们不是同系物;
3
20.A
C 项 , C H 的 同 分 异 构 体 有 正 戊 烷 、 异 戊 烷 和 新 戊 烷 , 它 们 的 沸 点 各 不 相 同 ; D 项 ,
5 12解析 A项,对于组成结构相似的物质,相对分子质量越大,分子间作用力越大,错误;B项,由于石英(SiO) Ba(NO ) ,不能加入BaCl ,因为Ag+干扰SO的检验,错误;D项,溶液中不含Fe2+,所以不会发生该现象,
2 3 2 2
是原子晶体,所以加热熔化时需破坏共价键;C项,NaOH加热熔化时,电离成自由移动的OH-和Na+,所以 错误。
具有导电性,正确;D项,水分解破坏氢氧键,生成H 和O,形成共价键,正确。 26.(1)醛基
2 2
21.D (2)CH
2
CH
2
+CH
3
COOH――→CH
3
COOCH
2
CH
3
解析 A项,v(R)==0.030 mol·L-1·min-1,正确;B项,在50 min时,两个温度下R全部分解,分解率均为 (3)CH 3 CH 2 ONa+H 2 O―→CH 3 CH 2 OH+NaOH
(4)AD
100%,正确;C项,在50 min时,30 ℃时,R分解了1.6 mol·L-1,而在25 ℃时,R分解了1.3 mol·L-1,所以
解析 A的摩尔质量为1.25 g·L-1×22.4 L·mol-1=28 g·mol-1,应为C H ,根据转化关系,B为CHCHO,C为
在0~50 min内,R的平均分解速率随温度升高而增大,正确;D项,对比30 ℃和10 ℃的曲线,不能在同一时 2 4 3
CHCOOH,D为C HOH。(3)Na与C HOH反应生成C HONa,C HONa强烈水解生成C HOH和NaOH,所
刻,应指明在同一段时间内R的分解速率随温度升高而增大,错误。 3 2 5 2 5 2 5 2 5 2 5
以滴入酚酞溶液呈红色。(4)A项,CHCH +HOC H――→C HOC H ,正确;B项,CHCHO与Cu(OH) 反应
22.C 2 2 2 5 2 5 2 5 3 2
生成砖红色沉淀,CHCOOH能使Cu(OH) 溶解,而C HOH和Cu(OH) 不反应,所以用新制Cu(OH) 悬浊液能
解析 A项,铁与盐酸反应生成Fe2+,所以转移电子数应为0.1N ,错误;B项,在pH=13的NaOH溶液中, 3 2 2 5 2 2
A
区分B、C、D,错误;C项,分离乙酸乙酯和乙酸的混合液,应加入饱和NaCO 溶液,再分液,错误;D项,
c(H+) =10-13mol·L-1,所以 1 L pH=13 NaOH 溶液中,n(H+) =10-13mol,错误;C 项,根据 2H + 2 3
水 水 2
CHCOOC H+HO CHCOOH+C HOH,当加入NaOH时,由于CHCOOH和NaOH反应,平衡右移,所
O===2HO、2CO+O===2CO ,标准状况,8.96 L(即0.4 mol)该混合气体完全燃烧,消耗氧分子数目为0.2N , 3 2 5 2 3 2 5 3
2 2 2 2 A
以乙酸乙酯在NaOH溶液中水解较在稀硫酸中更完全。
正确;D项,1.2 g金刚石中含有碳碳单键的数目为0.2N ,而1.2 g的石墨中含有碳碳单键的数目为0.15N ,所
A A
27.(1)S、Cu
以1.2 g的该混合物中,含有碳碳单键的数目应在0.15N ~0.2N 之间,错误。
A A
Cu (OH) SO 或者2Cu(OH) ·CuSO
23.B 3 4 4 2 4
(2)4NaOH+3CuSO ===Cu (OH) SO ↓+2NaSO
解析 根据加入的NaOH溶液体积和混合溶液pH变化曲线可知,HY为强酸,HX为弱酸。A项,由于HY为强 4 3 4 4 2 4
解析 (1)根据反应流程,白色沉淀为BaSO ,其物质的量为0.01 mol,黑色固体为CuO,其物质的量为0.01
酸,所以c(X-)<c(Y-),错误;B项,当V(NaOH)=10.00 mL时,HX、HY均反应一半,根据pH,此时溶液呈 4
mol,所以X中除H、O外,还有S、Cu。固体中有CuSO ,其物质的量为0.01 mol,其质量为1.60 g,1.60 g的黑
酸性,说明HX的电离大于X-的水解,所以c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-),正确;C项,当V(NaOH) 4
色固体应为CuO,其物质的量为0.02 mol,所以Cu2+共有0.03 mol, OH-共有0.04 mol,SO共有0.01 mol,X的
=20.00 mL时,正好完全反应生成NaX,溶液呈碱性,此时c(Na+)>c(X-)>c(OH-)>c(H+),错误;D项,当
化学式为Cu (OH) SO 或2Cu(OH) ·CuSO 。(2)若用非氧化还原反应制取X,可用NaOH溶液与CuSO 溶液反应
pH=7时,c(Na+)=c(Y-)>c(X-),错误。 3 4 4 2 4 4
制取。
24.C
28.(1)B
解析 由于还原性SO>I-,所以通入Cl 发生的反应依次为
2
(2)用胶头滴管滴加蒸馏水至溶液凹面正好与刻度线相切
SO+Cl+HO===SO+2H++2Cl-①
2 2
(3)AC
2I-+Cl===I+2Cl-②
2 2
解析 (1)在配制一定物质的量浓度溶液时,量筒可用也可不用。
A项,当a≥b时,Cl 不足,只发生反应①,正确;B项,当5a=4b时,即=时,既发生反应①,又发生反应
2
(3)A项,若称取相同质量的NaCO·10H O,造成NaCO 的质量偏小,所配溶液浓度偏低;B项,定容时俯视刻
2 3 2 2 3
②,正确;C项,当b=a时,只发生反应①,转移电子数为2a,当b=a时,转移电子数为2a+a=3a mol,所
度线,溶液体积偏小,所配溶液浓度偏高;C项,摇匀后,发现液面低于刻度线,若此时再加水,造成溶液体
以当a≤b≤a时,转移电子数为2a≤n(e-)≤3a,错误;D项,当a<b<a时,此时,n(SO)=a mol,I-为[a-
积偏大,所配溶液浓度偏低;D项,未清洗容量瓶,造成溶液有残留,所配溶液浓度偏高。
2(b-a)]=(3a-2b) mol,Cl-为2b mol,正确。
29.(1)2∶1(或2)
25.B
(2)2.50 mol·L-1
解析 根据向溶液X中加入过量稀盐酸有气体放出,可以推断 X中含有CO,根据离子共存原则,没有Ca2+、
解析 (1)根据表中数据分析,第Ⅰ组实验,NaCO 、NaHCO 完全反应,设NaCO 、NaHCO 的物质的量分别
2 3 3 2 3 3
Fe2+,根据电荷守恒,一定有Na+;根据沉淀,X中一定有SiO,根据向溶液1中加入过量AgNO 溶液产生的现
3
为x、y,
象,一定没有Br-,因为没有产生黄色沉淀,可能有 SO、Cl-,综上所述,A错误,B正确;C项,应加入解得 ②Cl+2NaOH===NaCl+NaClO+HO
2 2
Na
2
CO
3
、NaHCO
3
的物质的量之比为2∶1。 c
0
c
0
(2)设NaHCO 3 的物质的量为x,则Na 2 CO 3 的物质的量为2x, 3NaClO===2NaCl+NaClO 3
实验Ⅱ:106 g·mol-1×2x+84 g·mol-1×x=3.70 g c 0 -c 1
x=0.012 5 mol, 所以c(Cl-)=c 0 +。
实验Ⅲ:106 g·mol-1×2x+84 g·mol-1×x=5.18 g (3)电极反应式为
阳极:ClO-2e-+HO===ClO+2H+
2
x=0.017 5 mol, 阴极:2H++2e-===H 2
实验Ⅳ:106 g·mol-1×2x+84 g·mol-1×x=6.66 g 利用O 2 把生成H 2 除去,2H 2 +O 2 ===2H 2 O,
x=0.022 5 mol 总反应式为2NaClO 3 +O 2 =====2NaClO 4 。
实验Ⅳ中,Na
2
CO
3
为0.045 mol,NaHCO
3
为0.022 5 mol,Na
2
CO
3
完全反应生成NaHCO
3
,而NaHCO
3
反应了0.03 31.(1)Cu(OH)
2
或Cu
2
(OH)
2
CO
3
mol,所以消耗HCl的物质的量为0.045 mol+0.03 mol=0.075 mol,
(2)将溶液转移到蒸发皿中,控制温度加热至溶液表面形成一层晶膜 减慢冷却结晶的速度
(3)Cu(NO )·3H O+3SOCl ===Cu(NO )+3SO ↑+6HCl↑
c(HCl)==2.5 mol·L-1。 3 2 2 2 3 2 2
(4)在A、B之间增加干燥装置,防止B中水蒸气进入反应器A b
(注:用实验Ⅲ数据也可以计算)
(5)92.5%
30.(1)①放热反应,ΔS<0且反应自发
解析 (1)第②步调节pH的目的是通过水解除去Fe3+,为了不引入杂质离子,应选用Cu(OH) 或Cu (OH) CO。
② 2 2 2 3
(2)蒸发浓缩所用的主要仪器是蒸发皿。
(3)根据信息,SOCl 和水反应生成SO 和HCl。
2 2
(4)因为需制得无水Cu(NO ),所以应在A、B之间加干燥装置。
3 2
(5)当A=0.620时,Cu2+浓度为1.55×10-3mol·L-1
设Cu(NO ) 的质量分数为x,
3 2
(2)①3NaClO(aq)===2NaCl(aq)+NaClO(aq) ΔH=-116 kJ·mol-1(其他合理答案均可) ×=1.55×10-3mol·L-1
3
②c+或 x≈92.5%。
0
③反应Ⅰ的活化能高,活化分子百分数低,不利于ClO-向ClO转化 32.(1)A
(3)2NaClO+O=====2NaClO(其他合理答案均可)
3 2 4
解析 (1)该反应为放热反应,反应自发进行即ΔG=ΔH-TΔS<0,又因ΔS<0,所以ΔH<0为放热反应。
(2)①NaClO分解生成NaClO 的化学方程式为
3
3NaClO===2NaCl+NaClO
3
3NaClO(aq)+3NaCl(aq)+3HO(l)===3Cl(g)+6NaOH(aq) ΔH=306 kJ·mol-1
2 2
3Cl(g)+6NaOH(aq)===5NaCl(aq)+NaClO(aq)+3HO(l) ΔH=-422 kJ·mol-1
2 3 2 2
上述两式相加得
3NaClO(aq)===2NaCl(aq)+NaClO(aq) ΔH=-116 kJ·mol-1
3解析 根据制取流程图可以推断
(1)A项, 能发生氧化反应(燃烧),也能发生还原反应(加成反应)。
(4)根据信息,苯环上含有醛基,另一个取代基在其对位,其结构简式分别为
(5) 和CHCH 制乙苯,由乙苯制邻硝基乙苯,然后再用酸性KMnO 溶液氧化乙基。
2 2 4