文档内容
2018 年全国统一高考化学试卷(新课标Ⅰ) C.92.0g甘油(丙三醇)中含有羟基数为 1.0N A
D.1.0molCH 与Cl 在光照下生成CH Cl 的分子数为 1.0N
一、选择题(共 7小题,每小题 6分,满分 42分) 4 2 3 A
1.(6分)磷酸亚铁锂(LiFePO
4
)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废 5.(6分)环之间共用一个碳原子的化合物称为螺环化合物,螺(2,2)戊烷( )是最简
旧磷酸亚铁锂电池正极片中的金属,其流程如下: 单的一种,下列关于该化合物的说法错误的是( )
A.与环戊烯互为同分异构体 B.二氯化物超过两种
C.所有碳原子均处同一平面 D.生成1molC H ,至少需要2molH
5 12 2
6.(6分)主族元素 W、X、Y、Z 的原子序数依次增加,且均不大于 20.W、X、Z 最外层电子数
下列叙述错误的是( )
之和为 10;W与 Y 同族;W与 Z 形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。下列
A.合理处理废旧电池有利于保护环境和资源再利用
说法正确的是( )
B.从“正极片”中可回收的金属元素有Al、Fe、Li
A.常温常压下 X 的单质为气态
C.“沉淀”反应的金属离子为 Fe3+
B.Z 的氢化物为离子化合物
D.上述流程中可用硫酸钠代替碳酸钠
C.Y 和Z 形成的化合物的水溶液呈碱性
2.(6分)下列说法错误的是( )
D.W与Y 具有相同的最高化合价
A.蔗糖、果糖和麦芽糖均为双糖
7.(6分)最近我国科学家设计了一种 CO +H S 协同转化装置,实现对天然气中 CO 和 H S 的高
2 2 2 2
B.酶是一类具有高选择催化性能的蛋白质
效去除。示意图如右所示,其中电极分别为 ZnO@石墨烯(石墨烯包裹的 ZnO)和石墨烯,石
C.植物油含不饱和脂肪酸酯,能使Br /CCl 褪色
2 4 墨烯电极区发生反应为:
D.淀粉和纤维素水解的最终产物均为葡萄糖
①EDTA﹣Fe2+﹣e﹣=EDTA﹣Fe3+
3.(6分)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是( )
②2EDTA﹣Fe3++H S=2H++S+2EDTA﹣Fe2+该装置工作时,下列叙述错误的是( )
2
A. B. C. D.
4.(6分)N 是阿伏加德罗常数的值,下列说法正确的是( )
A
A.16.25gFeCl ,水解形成的 Fe(OH) 为胶体粒子数为0.1N
3 3 A
B.22.4L(标准状况)氩气含有的质子数为18N A.阴极的电极反应:CO +2H++2e﹣═CO+H O
A 2 2
第1页(共5页)B.协同转化总反应:CO +H S═CO+H O+S
2 2 2
C.石墨烯上的电势比 ZnO@石墨烯上的低
D.若采用Fe3+/Fe2+取代EDTA﹣Fe3+/EDTA﹣Fe2+,溶液需为酸性
①pH=4.1时,Ⅰ中为 溶液(写化学式)。
二、解答题(共 3小题,满分 43分)
②工艺中加入Na CO 固体,并再次充入SO 的目的是 。
2 3 2
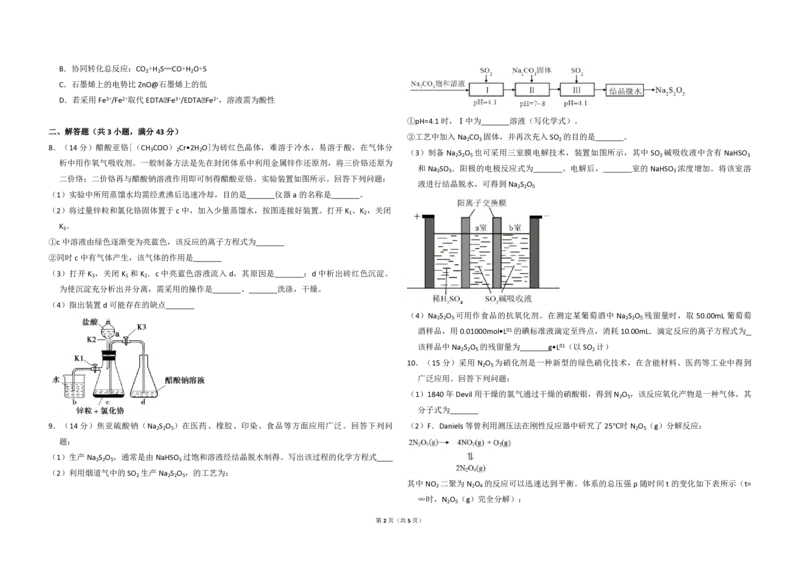
8.(14分)醋酸亚铬[(CH COO) Cr•2H O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分
3 2 2 (3)制备 Na S O 也可采用三室膜电解技术,装置如图所示,其中 SO 碱吸收液中含有 NaHSO
2 2 5 2 3
析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为
和 Na SO .阳极的电极反应式为 。电解后, 室的 NaHSO 浓度增加。将该室溶
2 3 3
二价络;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示。回答下列问题:
液进行结晶脱水,可得到 Na S O
2 2 5
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是 仪器a的名称是 。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开K 、K ,关闭
1 2
K 。
3
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为
②同时c中有气体产生,该气体的作用是
(3)打开 K ,关闭 K 和 K .c中亮蓝色溶液流入 d,其原因是 ;d 中析出砖红色沉淀。
3 1 2
为使沉淀充分析出并分离,需采用的操作是 、 洗涤,干燥。
(4)指出装置d 可能存在的缺点
(4)Na S O 可用作食品的抗氧化剂。在测定某葡萄酒中 Na S O 残留量时,取 50.00mL 葡萄萄
2 2 5 2 2 5
酒样品,用 0.01000mol•L﹣1的碘标准液滴定至终点,消耗 10.00mL.滴定反应的离子方程式为
该样品中Na S O 的残留量为 g•L﹣1(以SO 计)
2 2 5 2
10.(15分)采用 N O 为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到
2 5
广泛应用。回答下列问题:
(1)1840年 Devil 用干燥的氯气通过干燥的硝酸银,得到 N O ,该反应氧化产物是一种气体,其
2 5
分子式为
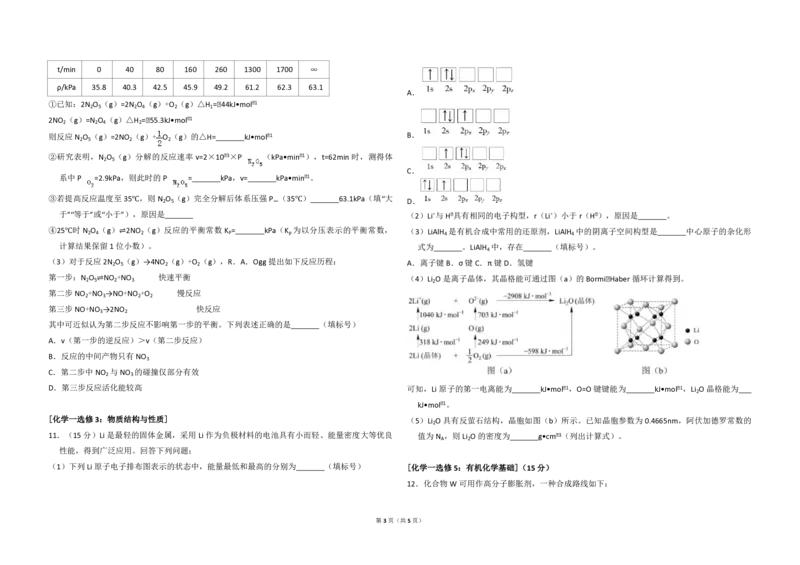
9.(14分)焦亚硫酸钠(Na S O )在医药、橡胶、印染、食品等方面应用广泛。回答下列问 (2)F.Daniels 等曾利用测压法在刚性反应器中研究了25℃时N O (g)分解反应:
2 2 5 2 5
题:
(1)生产Na S O ,通常是由NaHSO 过饱和溶液经结晶脱水制得。写出该过程的化学方程式
2 2 5 3
(2)利用烟道气中的SO 生产Na S O ,的工艺为:
2 2 2 5
其中 NO 二聚为 N O 的反应可以迅速达到平衡。体系的总压强 ρ随时间 t的变化如下表所示(t=
2 2 4
∞时,N O (g)完全分解):
2 5
第2页(共5页)t/min 0 40 80 160 260 1300 1700 ∞
ρ/kPa 35.8 40.3 42.5 45.9 49.2 61.2 62.3 63.1
A.
①已知:2N O (g)=2N O (g)+O (g)△H =﹣44kJ•mol﹣1
2 5 2 4 2 1
2NO (g)=N O (g)△H =﹣55.3kJ•mol﹣1
2 2 4 2
则反应N O (g)=2NO (g)+ O (g)的△H= kJ•mol﹣1
B.
2 5 2 2
②研究表明,N O (g)分解的反应速率 v=2×10﹣3×P (kPa•min﹣1),t=62min 时,测得体
2 5
C.
系中P =2.9kPa,则此时的 P = kPa,v= kPa•min﹣1。
③若提高反应温度至 35℃,则 N 2 O 5 (g)完全分解后体系压强 P ∞ (35℃) 63.1kPa(填“大 D.
于”“等于”或“小于”),原因是 (2)Li+与H﹣具有相同的电子构型,r(Li+)小于r(H﹣),原因是 。
④25℃时 N
2
O
4
(g)⇌2NO
2
(g)反应的平衡常数 K
P
= kPa(K
p
为以分压表示的平衡常数, (3)LiAlH
4
是有机合成中常用的还原剂,LiAlH
4
中的阴离子空间构型是 中心原子的杂化形
计算结果保留1位小数)。 式为 。LiAlH 中,存在 (填标号)。
4
(3)对于反应2N
2
O
5
(g)→4NO
2
(g)+O
2
(g),R.A.Ogg提出如下反应历程: A.离子键 B.σ键C.π键D.氢键
第一步:N 2 O 5 ⇌NO 2 +NO 3 快速平衡 (4)Li 2 O 是离子晶体,其晶格能可通过图(a)的Bormi﹣Haber循环计算得到。
第二步NO +NO →NO+NO +O 慢反应
2 3 2 2
第三步NO+NO →2NO 快反应
3 2
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是 (填标号)
A.v(第一步的逆反应)>v(第二步反应)
B.反应的中间产物只有NO
3
C.第二步中 NO
2
与NO
3
的碰撞仅部分有效
D.第三步反应活化能较高 可知,Li 原子的第一电离能为 kJ•mol﹣1,O=O 键键能为 kJ•mol﹣1,Li O 晶格能为
2
kJ•mol﹣1。
[化学一选修 3:物质结构与性质] (5)Li O 具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为 0.4665nm,阿伏加德罗常数的
2
11.(15分)Li 是最轻的固体金属,采用 Li 作为负极材料的电池具有小而轻、能量密度大等优良 值为N ,则Li O 的密度为 g•cm﹣3(列出计算式)。
A 2
性能,得到广泛应用。回答下列问题:
(1)下列Li 原子电子排布图表示的状态中,能量最低和最高的分别为 (填标号) [化学一选修 5:有机化学基础](15分)
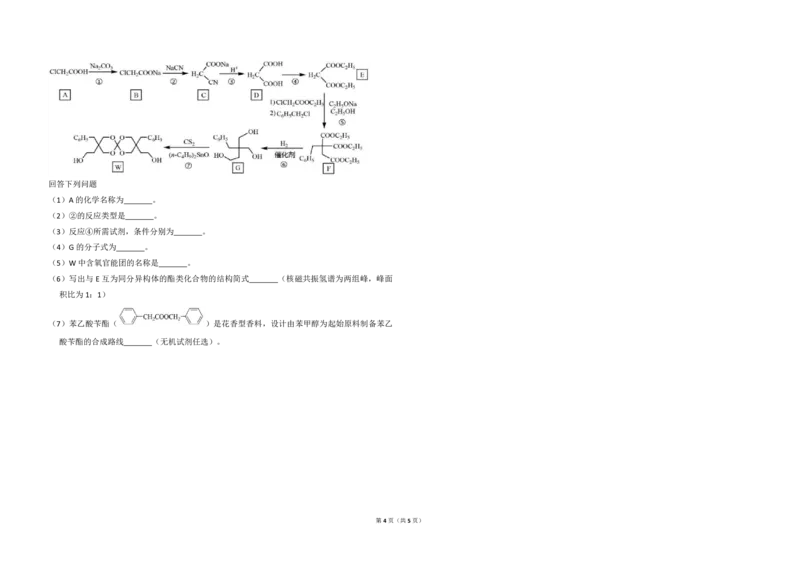
12.化合物 W可用作高分子膨胀剂,一种合成路线如下:
第3页(共5页)回答下列问题
(1)A的化学名称为 。
(2)②的反应类型是 。
(3)反应④所需试剂,条件分别为 。
(4)G的分子式为 。
(5)W中含氧官能团的名称是 。
(6)写出与 E 互为同分异构体的酯类化合物的结构简式 (核磁共振氢谱为两组峰,峰面
积比为1:1)
(7)苯乙酸苄酯( )是花香型香料,设计由苯甲醇为起始原料制备苯乙
酸苄酯的合成路线 (无机试剂任选)。
第4页(共5页)第5页(共5页)