文档内容
辽宁省 2022 年普通高等学校招生选择性考试
化学
注意事项:
1、答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。答非选择题时,将答案写在答题卡上。写在本试卷
上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 Cr 52 Fe 56 Cu 64 Zn 65
Bi 209
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项符合题目要求。
的
1. 北京冬奥会备受世界瞩目。下列说法错误 是
A. 冰壶主材料花岗岩属于无机非金属材料
B. 火炬“飞扬”使用的碳纤维属于有机高分子材料
C. 冬奥会“同心”金属奖牌属于合金材料
D. 短道速滑服使用的超高分子量聚乙烯属于有机高分子材料
2. 下列符号表征或说法正确的是
A. 电离: B. 位于元素周期表p区
C. 空间结构:平面三角形 D. 电子式:
3. 设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的中子数为
的
B. 分子中含有 键数目为
C. 标准状况下, 气体中 数目为
D. 的 溶液中 数目为4. 下列关于苯乙炔( )的说法正确的是
A. 不能使酸性 溶液褪色 B. 分子中最多有5个原子共直线
C. 能发生加成反应和取代反应 D. 可溶于水
5. 短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电子,W简单离子在
同周期离子中半径最小,Q与Z同主族。下列说法错误的是
A. X能与多种元素形成共价键 B. 简单氢化物沸点:
C. 第一电离能: D. 电负性:
6. 镀锌铁钉放入棕色的碘水中,溶液褪色;取出铁钉后加入少量漂白粉,溶液恢复棕色;加入 ,振
荡,静置,液体分层。下列说法正确的是
A. 褪色原因为 被 还原 B. 液体分层后,上层呈紫红色
C. 镀锌铁钉比镀锡铁钉更易生锈 D. 溶液恢复棕色的原因为 被氧化
7. 理论化学模拟得到一种 离子,结构如图。下列关于该离子的说法错误的是
A. 所有原子均满足8电子结构 B. N原子的杂化方式有2种
C. 空间结构为四面体形 D. 常温下不稳定
8. 下列类比或推理合理的是
已知 方法 结论
A 沸点: 类比 沸点:
B 酸性: 类比 酸性:
C 金属性: 推理 氧化性:
D : 推理 溶解度:A. A B. B C. C D. D
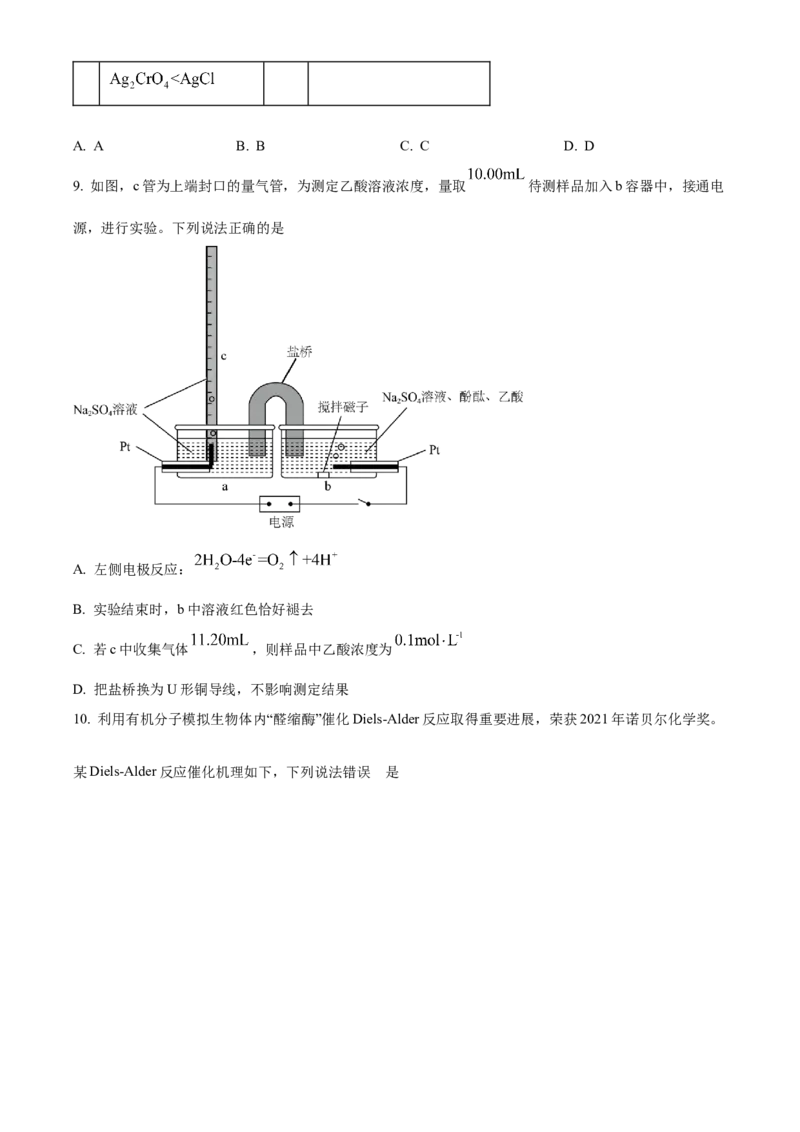
9. 如图,c管为上端封口的量气管,为测定乙酸溶液浓度,量取 待测样品加入b容器中,接通电
源,进行实验。下列说法正确的是
A. 左侧电极反应:
B. 实验结束时,b中溶液红色恰好褪去
C. 若c中收集气体 ,则样品中乙酸浓度为
D. 把盐桥换为U形铜导线,不影响测定结果
10. 利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得重要进展,荣获2021年诺贝尔化学奖。
的
某Diels-Alder反应催化机理如下,下列说法错误 是A. 总反应为加成反应 B. Ⅰ和Ⅴ互为同系物
C. Ⅵ是反应的催化剂 D. 化合物X为
11. 、 均可自耦电离: 、 。下列反
应与 CHCHOH+HBr原理不同的是
3 2
A.
B.
C.
D.
12. 某温度下,在 恒容密闭容器中 发生反应 ,有关数据如下:
时间段/ 产物Z的平均生成速率/
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是A. 时,Z的浓度大于
B. 时,加入 ,此时
C. 时,Y的体积分数约为33.3%
D. 时,X的物质的量为
13. 下列实验能达到目的的是
实验目的 实验方法或操作
A 测定中和反应的反应热 酸碱中和滴定的同时,用温度传感器采集锥形瓶内溶液的温度
探究浓度对化学反应速率 量取同体积不同浓度的 溶液,分别加入等体积等浓度的
B
的影响
溶液,对比现象
将 溶液与 溶液混合,反应后静置,向上层清液中再加
判断反应后 是否沉
C
淀完全 1滴 溶液
D 检验淀粉是否发生了水解 向淀粉水解液中加入碘水
A. A B. B C. C D. D
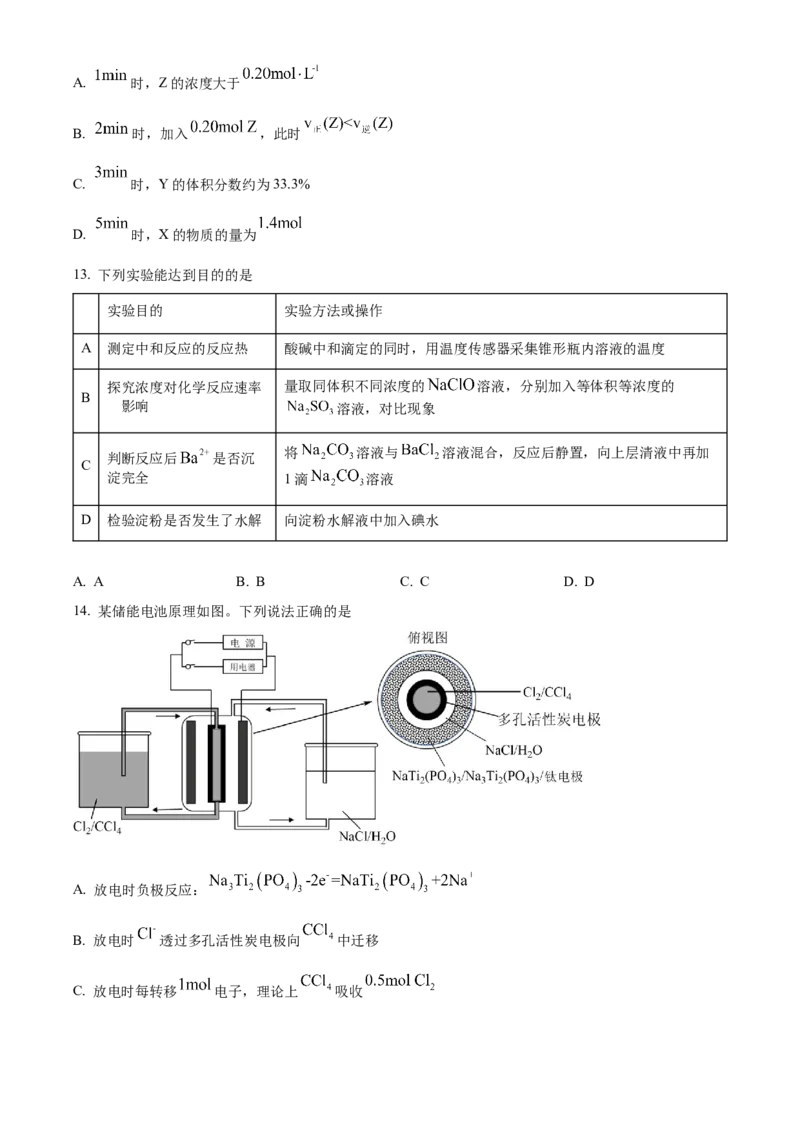
14. 某储能电池原理如图。下列说法正确的是
A. 放电时负极反应:
B. 放电时 透过多孔活性炭电极向 中迁移
C. 放电时每转移 电子,理论上 吸收D. 充电过程中, 溶液浓度增大
15. 甘氨酸 是人体必需氨基酸之一、在 时, 、
和 的分布分数【如 】与溶液 关系如图。下列说
法错误的是
A. 甘氨酸具有两性
B. 曲线c代表
C. 的平衡常数
D.
二、非选择题:本题共4小题,共55分。
16. 某工厂采用辉铋矿(主要成分为 ,含有 、 杂质)与软锰矿(主要成分为 )联合焙烧
法制各 和 ,工艺流程如下:
已知:①焙烧时过量的 分解为 , 转变为 ;②金属活动性: ;
③相关金属离子形成氢氧化物的 范围如下:
开始沉淀
完全沉淀
6.5 8.3
1.6 2.8
8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为_______。
a.进一步粉碎矿石 b.鼓入适当过量的空气 c.降低焙烧温度
(2) 在空气中单独焙烧生成 ,反应的化学方程式为_______。
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出 和 ;②_______。
(4)滤渣的主要成分为_______(填化学式)。
(5)生成气体A的离子方程式为_______。
(6)加入金属Bi的目的是_______。
(7)将100kg辉铋矿进行联合焙烧,转化时消耗1.1kg金属Bi,假设其余各步损失不计,干燥后称量
产品质量为32kg,滴定测得产品中Bi的质量分数为78.5%。辉铋矿中Bi元素的质量分数为
_______。
17. 工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为:
。回答下列问题:
(1)合成氨反应在常温下_______(填“能”或“不能”)自发。
(2)_______温(填“高”或“低”,下同)有利于提高反应速率,_______温有利于提高平衡转化率,综合考虑
催化剂(铁触媒)活性等因素,工业常采用 。
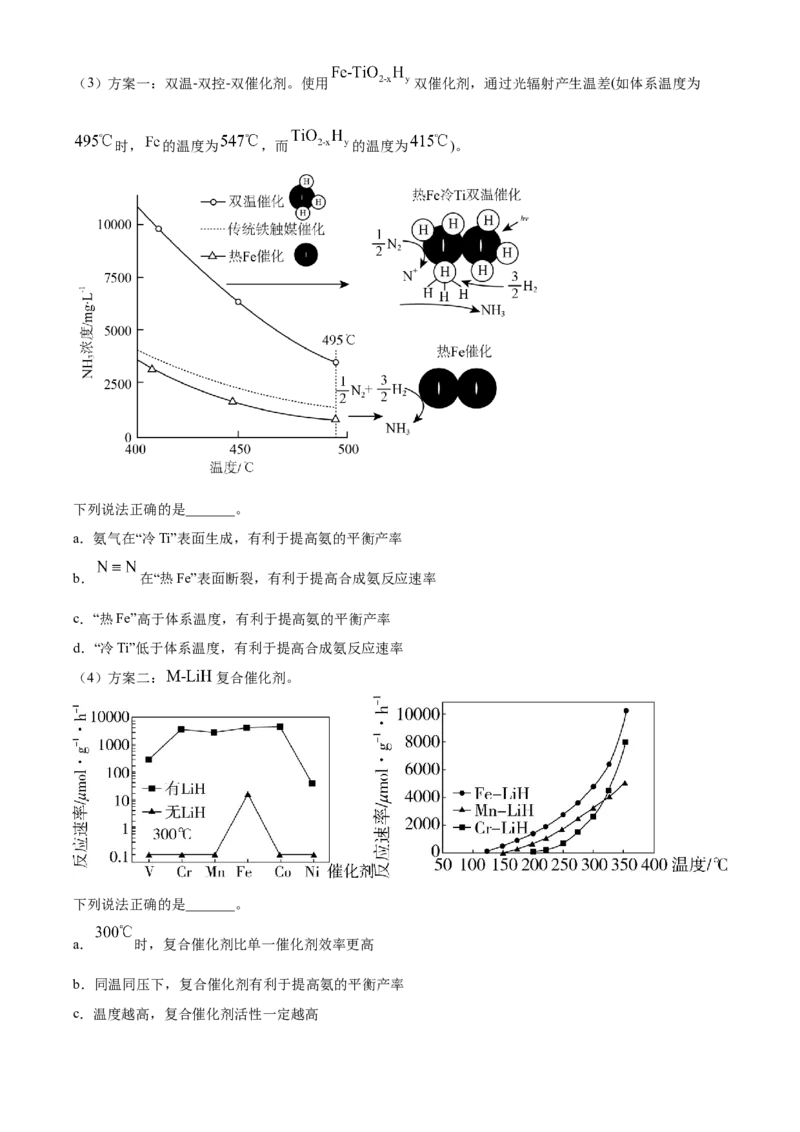
针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。(3)方案一:双温-双控-双催化剂。使用 双催化剂,通过光辐射产生温差(如体系温度为
时, 的温度为 ,而 的温度为 )。
下列说法正确的是_______。
a.氨气在“冷Ti”表面生成,有利于提高氨的平衡产率
b. 在“热Fe”表面断裂,有利于提高合成氨反应速率
c.“热Fe”高于体系温度,有利于提高氨的平衡产率
d.“冷Ti”低于体系温度,有利于提高合成氨反应速率
(4)方案二: 复合催化剂。
下列说法正确的是_______。
a. 时,复合催化剂比单一催化剂效率更高
b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高(5)某合成氨速率方程为: ,根据表中数据, _______;
实
验
1 m n p q
2 2m n p 2q
3 m n 0.1p 10q
4 m 2n p 2.828q
在合成氨过程中,需要不断分离出氨的原因为_______。
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
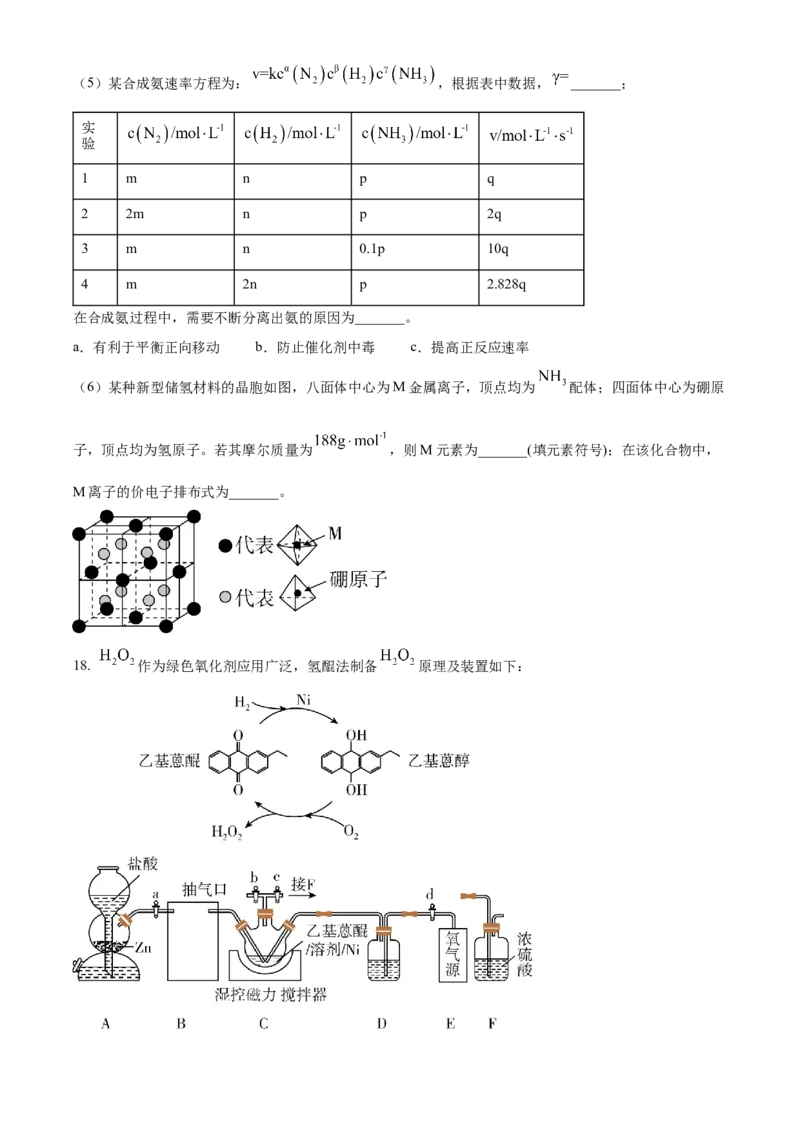
(6)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为 配体;四面体中心为硼原
子,顶点均为氢原子。若其摩尔质量为 ,则M元素为_______(填元素符号);在该化合物中,
M离子的价电子排布式为_______。
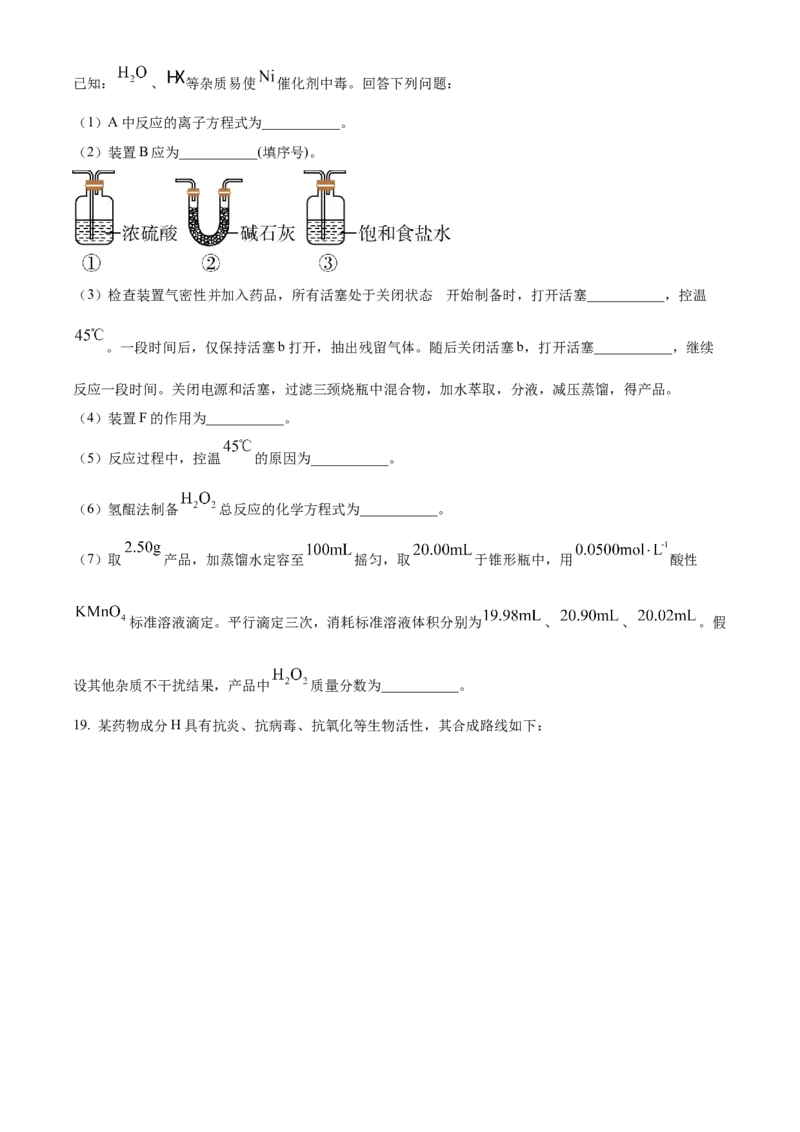
18. 作为绿色氧化剂应用广泛,氢醌法制备 原理及装置如下:已知: 、 等杂质易使 催化剂中毒。回答下列问题:
(1)A中反应的离子方程式为___________。
(2)装置B应为___________(填序号)。
(3)检查装置气密性并加入药品,所有活塞处于关闭状态 。开始制备时,打开活塞___________,控温
。一段时间后,仅保持活塞b打开,抽出残留气体。随后关闭活塞b,打开活塞___________,继续
反应一段时间。关闭电源和活塞,过滤三颈烧瓶中混合物,加水萃取,分液,减压蒸馏,得产品。
(4)装置F的作用为___________。
(5)反应过程中,控温 的原因为___________。
(6)氢醌法制备 总反应的化学方程式为___________。
(7)取 产品,加蒸馏水定容至 摇匀,取 于锥形瓶中,用 酸性
标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为 、 、 。假
设其他杂质不干扰结果,产品中 质量分数为___________。
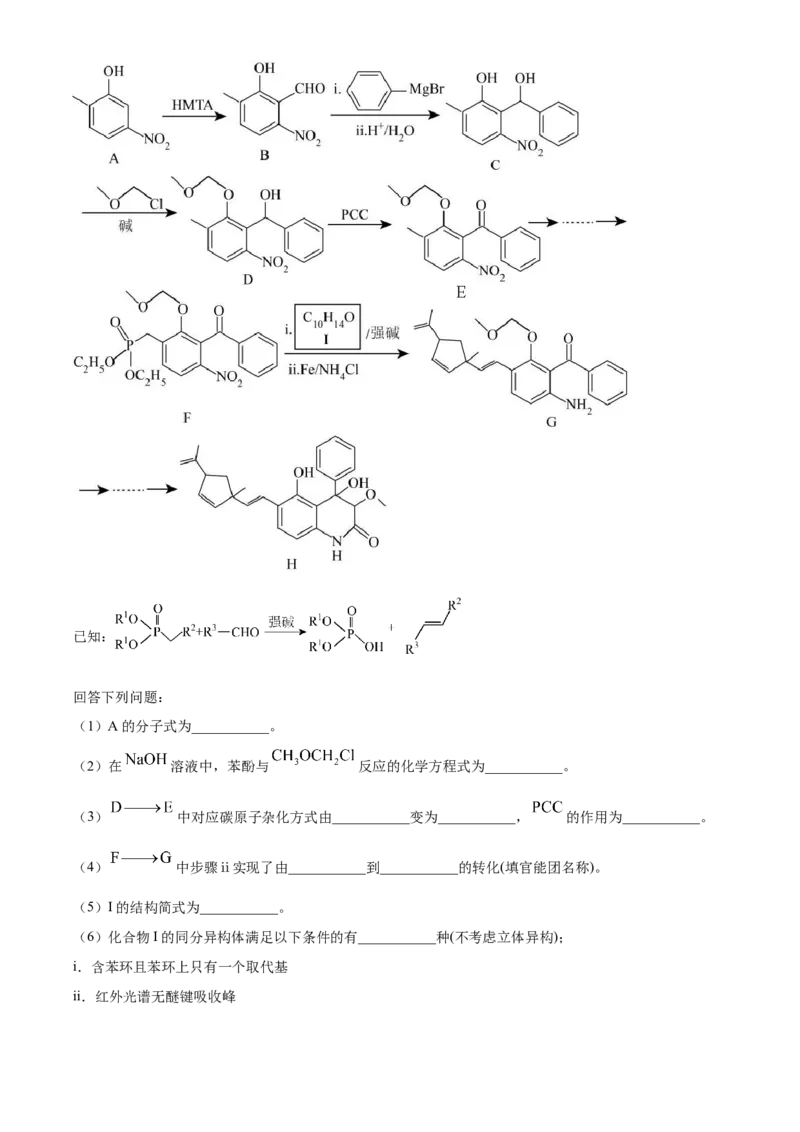
19. 某药物成分H具有抗炎、抗病毒、抗氧化等生物活性,其合成路线如下:已知:
回答下列问题:
(1)A的分子式为___________。
(2)在 溶液中,苯酚与 反应的化学方程式为___________。
(3) 中对应碳原子杂化方式由___________变为___________, 的作用为___________。
(4) 中步骤ⅱ实现了由___________到___________的转化(填官能团名称)。
(5)I的结构简式为___________。
(6)化合物I的同分异构体满足以下条件的有___________种(不考虑立体异构);
i.含苯环且苯环上只有一个取代基
ii.红外光谱无醚键吸收峰其中,苯环侧链上有3种不同化学环境的氢原子,且个数比为6∶2∶1的结构简式为___________(任写一
种)。