文档内容
2025年上海市高考化学试卷
参考答案与试题解析
一、碳酸丙烯酯的合成(20分)
1.(20分)碳酸丙烯酯(PC)是一种重要的有机化合物,在工业上有广泛应用。
(1) 中电负性最大的元素是 C 。
A.C
B.H
C.O
(2)1mol 分子中σ键的数目为 C 。
A.7N
A
B.12N
A
C.13N
A
D.14N
A
环氧丙烷与CO 催化合成法是生产碳酸丙烯酯(PC)的常用方法:
2
反应Ⅰ: (g)+CO (g)═ (l)ΔH =﹣125kJ•mol﹣1
2 1
反应Ⅱ:C(s)+O (g)═CO (g)ΔH =﹣393.5kJ•mol﹣1
2 2 2
反应Ⅲ:3H (g)+3C(s)+0.5O (g)═ (g)ΔH =﹣94.7kJ•mol﹣1
2 2 3
(3)反应Ⅳ:3H (g)+4C(s)+1.5O (g)═ (l)的热效应为ΔH = A kJ•mol﹣1。
2 2 4
A.﹣613.2
B.613.2
C.395.2
第1页(共22页)D.﹣395.2
(4)下列关于反应Ⅰ的ΔH﹣TΔS(kJ•mol﹣1)随温度T(K)的变化趋势正确的是 C 。
A B C D
环氧丙烷在反应生成碳酸丙烯酯时,会发生副反应。已知:
①碳酸丙烯醋的选择性= ×100%;
②M(环氧丙烷)=58gmol﹣1; (环氧丙烷)=1.2g•mL﹣1。
向含有过量CO
2
的体积为25mLρ的恒压容器中充入一定量环氧丙烷,反应4h后,容器体积缩小为
10mL,其中碳酸丙烯酯的选择性为95%。
(5)以环氧丙烷表示的化学反应速率v= 4. 0 mol•L﹣1•h﹣1(保留两位小数)。
(6)下列操作中可使活化分子百分数变大的有 A 。
A.升高温度
B.增大CO 浓度
2
C.压缩容器
D.恒容充入惰性气体
(7)碳酸丙烯酯在单位时间内的产率随温度变化如图所示。产率随温度先变大后变小的原因是 T
< 140 ℃,反应未达到平衡,温度越高反应速率越快,产率越高, T > 140 ℃,正反应放热,温度越高 ,
平衡逆向移动,产率降低 。
(8)能作为反应Ⅰ达到化学平衡的标志是 CD 。(不定项)
A.v正 (CO
2
)=v正 (碳酸丙烯酯)
B.物质总质量不变
第2页(共22页)C.气体体积不变
D.混合气体平均摩尔质量不变
(9)用光气COCl 与丙二醇反应也可以用于制备碳酸丙烯酯,从绿色化学角度写出三点传统环氧丙烷
2
与CO 催化合成法的优势 光气有毒,传统方法更安全;用光气 COC l 与丙二醇反应还有副产物 HC l
2 2
产生,原子利用率低;传统方法用二氧化碳做原料,可以帮助完成碳中和,减缓温室效应 。
【分析】
(1) 中含有C、H、O元素;
(2)单键是σ键,双键中含有1个σ键;
(3)根据盖斯定律进行解答;
(4)反应Ⅰ中的ΔH<0,ΔS<0;
(5)根据反应速率v= 进行解答;
(6)使活化分子百分数变大的方法可以使降低反应的活化能或者让更多分子变为活化分子;
(7)碳酸丙烯酯在单位时间内的产率随温度变化先变大后减小是因为开始反应未达到平衡;
(8)化学反应达到化学平衡的标志是正逆反应速率相等,各物质的浓度不再变化;
(9)绿色化学角度是指源头上减少污染、原子利用率大、绿色环保。
【解答】
解:(1) 中含有C、H、O元素,电负性O>C>H,故电负性最大的是O,
故答案为:C;
(2) 分子中含有13个σ键,则1mol 分子中含有13N 个σ键,
A
故答案为:C;
(3)已知反应Ⅰ: (g)+CO (g)═ (l)ΔH =﹣125kJ•mol﹣1;
2 1
反应Ⅱ:C(s)+O (g)═CO (g)ΔH =﹣393.5kJ•mol﹣1;
2 2 2
第3页(共22页)反应Ⅲ:3H (g)+3C(s)+0.5O (g)═ (g)ΔH =﹣94.7kJ•mol﹣1;
2 2 3
反应Ⅳ:3H (g)+4C(s)+1.5O (g)═ (l);
2 2
反应Ⅰ+反应Ⅱ+反应Ⅲ=反应Ⅳ,则热效应为ΔH = ΔH +ΔH +ΔH =﹣613.2kJ•mol﹣1,故A正确,
4 1 2 3
故答案为:A;
(4)反应Ⅰ中的ΔH<0,ΔS<0,ΔH﹣TΔS(kJ•mol﹣1)随温度T(K)的变化是一次函数的变化,
斜率k=﹣ΔS>0,与y轴的截距b= <0,故C正确,
故答案为:C;
(5)由反应 (g)+CO (g)═ 可知, 与CO (g)的反应比为1:1,反应4h后,容
2 2
器体积缩小为10mL,则 与CO (g)的体积各减少7.5mL,n( )= =
2
mol,产生 的物质的量= mol,碳酸丙烯醋的选择性= =95%,则n
(消耗环氧丙烷的物质的量)=0.16mol,根据反应速率v= = =4.0mol•L﹣1•h﹣1,
故答案为:4.0;
(6)
A.升高温度,分子能量升高,活化分子百分数增大,A正确;
B.增大浓度,增大活化分子数,活化分子百分数不变,B错误;
C.压缩容器,即增大压强,针对有气体的反应,增大单位体积活化分子数,活化分子百分数不变 ,
C错误;
第4页(共22页)D.充入惰性气体,若体积不变,浓度不变,活化分子百分数不变,D错误;
答案选A
(7)碳酸丙烯酯在单位时间内的产率随温度变化先变大后减小是因为开始反应未达到平衡,温度越高
反应速率越快,产率越高,T>140℃,正反应放热,温度越高,平衡逆向移动,产率降低,
故答案为:T<140℃,反应未达到平衡,温度越高反应速率越快,产率越高,T>140℃,正反应放热,
温度越高,平衡逆向移动,产率降低;
(8)A.v正 (CO
2
)=v正 (碳酸丙烯酯)都表示正反应速率,故不能表示反应达到平衡状态,故 A错
误;
B.根据质量守恒定律,物质总质量不变,故不能说明反应达到平衡状态,故B错误;
C.该反应前后气体系数不同,故气体体积不变时,各物质的量浓度不变,可以说明反应达到平衡状态,
故C正确;
D.该反应前后气体系数不同,混合气体平均摩尔质量不变时,则说明各物质的量不再变化,可以说明
反应达到平衡状态,故D正确;
故答案为:CD;
(9)用光气COCl 与丙二醇反应也可以用于制备碳酸丙烯酯,光气有毒,传统方法更安全,用光气
2
COCl 与丙二醇反应还有副产物HCl产生,原子利用率低,环氧丙烷与CO 催化合成原子利用率达到
2 2
百分之百,传统方法用二氧化碳做原料,可以帮助完成碳中和,减缓温室效应,
故答案为:光气有毒,传统方法更安全;用光气 COCl 与丙二醇反应还有副产物HCl产生,原子利用
2
率低;传统方法用二氧化碳做原料,可以帮助完成碳中和,减缓温室效应。
二、“重石头元素”——钨(20分)
2.(20分)钨属于有色金属,在高温下可以发出亮光。
(1)钨作灯丝与钨的 C 性质有关。
A.延展性
B.导电性
C.高熔点
D.高密度
(2)请从微观角度解释钨有金属光泽的原因: 钨是金属晶体,含有金属阳离子和自由电子,当可见
光照射到金属表面时,自由电子能够吸收所有频率的光跃迁到高能级,不稳定,又会跃迁到低能级轨
道,以光子的形式释放出来,使得金属不透明并具有金属光泽 。
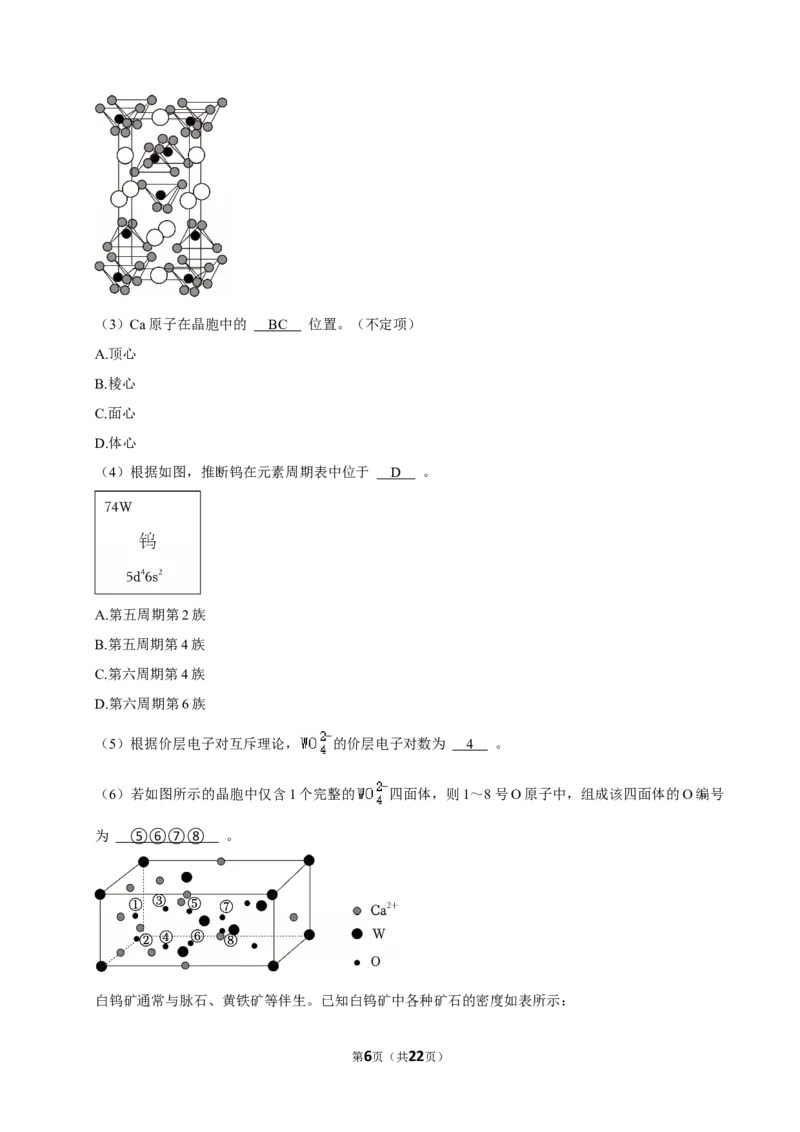
钨的矿石在古代被称为“重石头”。最早由瑞典化学家舍勒发现白钨矿,白钨矿的主要成分是钨酸钙,
化学式为CaWO ,属于四方晶系,晶胞结构如图所示:
4
第5页(共22页)(3)Ca原子在晶胞中的 BC 位置。(不定项)
A.顶心
B.棱心
C.面心
D.体心
(4)根据如图,推断钨在元素周期表中位于 D 。
A.第五周期第2族
B.第五周期第4族
C.第六周期第4族
D.第六周期第6族
(5)根据价层电子对互斥理论, 的价层电子对数为 4 。
(6)若如图所示的晶胞中仅含1个完整的 四面体,则1~8号O原子中,组成该四面体的O编号
为 ⑤⑥⑦⑧ 。
白钨矿通常与脉石、黄铁矿等伴生。已知白钨矿中各种矿石的密度如表所示:
第6页(共22页)矿石 脉石 黄铁矿 萤石 磷灰石
密度 (g•cm﹣3) 2.65 4.95 3.18 3.13
(7)已知ρM(CaWO )=288g•mol﹣1、V(CaWO )=3.12×10﹣22cm3,则 (CaWO )= 6.13
4 4 4
g•cm﹣3。 ρ
结合数据说明钨酸钙矿石被称为“重石头”的原因: 钨酸矿的密度比脉石、黄铁矿的更大,同体积
时钨酸钙矿石重量更大 。
CaWO 具有良好的光学性质,被广泛应用于光电陶瓷材料中,工业上可用电解法制备,电解装置如图
4
所示:
已知:K (CaWO )=8.7×10﹣9,K (CaCO )=2.7×10﹣8。
sp 4 sp 3
(8)写出电解池阳极的反应式: W ﹣ 6 e ﹣ +8OH ﹣ +C a 2 + = CaWO +4H O 。
4 2
(9)为获取高纯产物,制备时需要不断通入N 的原因是 通入氮气隔绝空气中的 CO ,防止生成
2 2
CaCO 。
3
【分析】
(1)钨的熔点高,可以承受灯丝发光时的高温;
(2)金属晶体中含有金属阳离子和自由电子,自由电子能吸收光;
(3)由晶胞结构图可知,黄球为Ca;
(4)由图可知,钨的价层电子排布式为5d46s2;
(5)根据价层电子对互斥理论计算 的价层电子对数;
(6) 四面体中W位于四面体中心,O位于四面体四个顶点上;
(7)根据 = 计算密度并进行解释;
ρ
(8)由电解装置图可知,W为阳极,失电子生成 ,与Ca2+反应CaWO ;
4
(9)K (CaWO )=8.7×10﹣9与K (CaCO )=2.7×10﹣8相差不大,Ca(OH) 易与空气中的CO
sp 4 sp 3 2 2
第7页(共22页)反应生成CaCO 。
3
【解答】
(1)电流在通过钨丝时,以产生足够的热量使灯丝达到白热化状态,钨的熔点高,可以承受灯丝发光
时的高温,故可做灯丝的最佳选择,
故答案为:C;
(2)钨有金属光泽的原因是:金属晶体中有自由电子,所以当可见光照射到金属晶体表面时,晶体中
的自由电子可以吸收光能而呈现能量较高的状态。但是这种状态不稳定,电子跃迁回到低能量状态时
会将吸收的各种波长的光辐射出来,使得金属不透明并具有金属光泽;
故答案为:金属晶体中有自由电子,所以当可见光照射到金属晶体表面时,晶体中的自由电子可以吸
收光能而呈现能量较高的状态。但是这种状态不稳定,电子跃迁回到低能量状态时会将吸收的各种波
长的光辐射出来,使得金属不透明并具有金属光泽;
(3)由晶胞结构图可知,黄球为Ca,位于面心和棱上,
故答案为:BC;
(4)74号W元素在56号Xe元素和86号Rn元素之间,所以W在第六周期第ⅥB族,故答案为D;
(5)根据价层电子对互斥理论, 的价层电子对数为4+ =4,
故答案为:4;
(6) 四面体是由1个W原子和4个O原子构成的,其中W原子位于四面体的中心,4个O原子
位于四面体的4个顶点。从图1-8中可以看到晶胞的结构,当W原子与5、6、7、8号O原子相邻时,
能组成一个四面体,故答案为:5、6、7、8;
(7)Ca位于棱上和面上,个数为6× +4× =4,相当于1个晶胞中含有4个“CaWO ”,晶胞质量
4
为 g, (CaWO )= = g•cm﹣3≈6.13g•cm﹣3,比脉石、黄铁矿的密度都大,
4
ρ
同体积时钨酸钙矿石重量更大,故钨酸钙矿石被称为“重石头”,
故答案为:6.13;钨酸矿的密度比脉石、黄铁矿的更大,同体积时钨酸钙矿石重量更大;
(8)W与电源正极相连,所以是电解池的阳极,故电极反应式为:
,故答案为: ;
(9)制备时需要不断通入的原因是:减少 CO2,避免生成CaCO3;故答案为:减少CO2,避免生成
CaCO3;故答案为:通入氮气隔绝空气中的CO ,防止生成CaCO 。
2 3
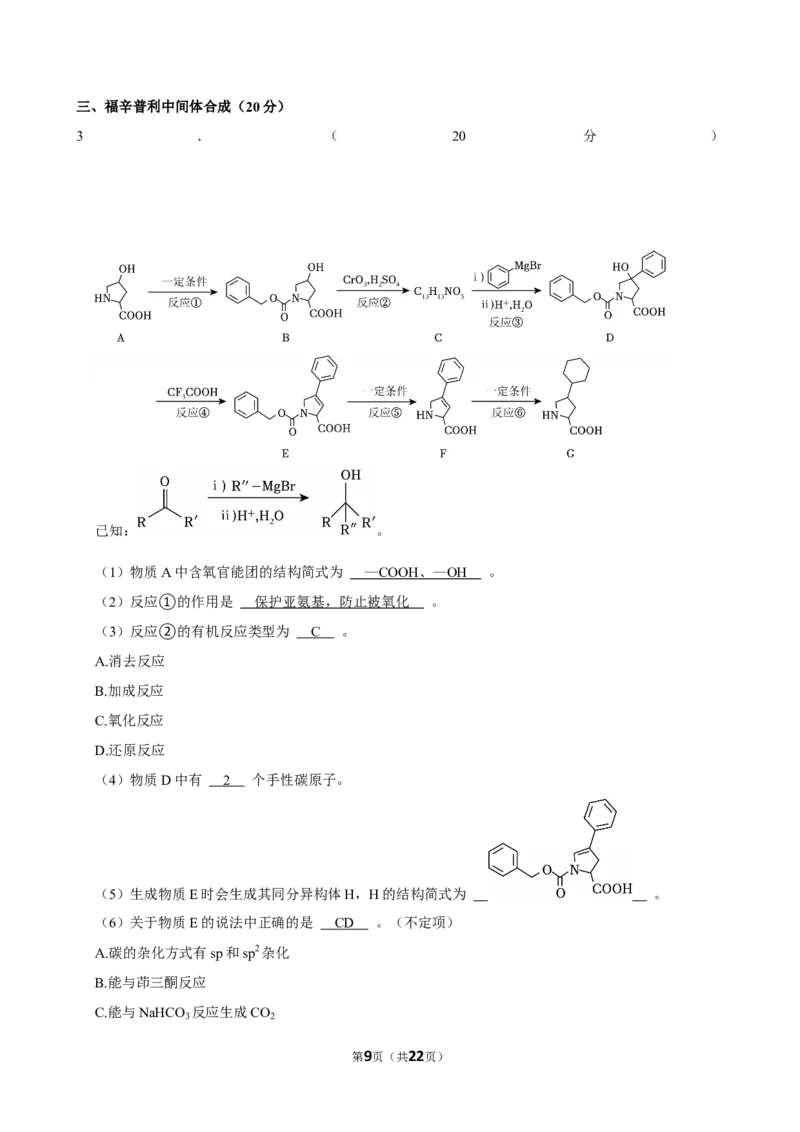
第8页(共22页)三、福辛普利中间体合成(20分)
3 . ( 20 分 )
已知: 。
(1)物质A中含氧官能团的结构简式为 — COOH 、— OH 。
(2)反应①的作用是 保护亚氨基,防止被氧化 。
(3)反应②的有机反应类型为 C 。
A.消去反应
B.加成反应
C.氧化反应
D.还原反应
(4)物质D中有 2 个手性碳原子。
(5)生成物质E时会生成其同分异构体H,H的结构简式为 。
(6)关于物质E的说法中正确的是 CD 。(不定项)
A.碳的杂化方式有sp和sp2杂化
B.能与茚三酮反应
C.能与NaHCO 反应生成CO
3 2
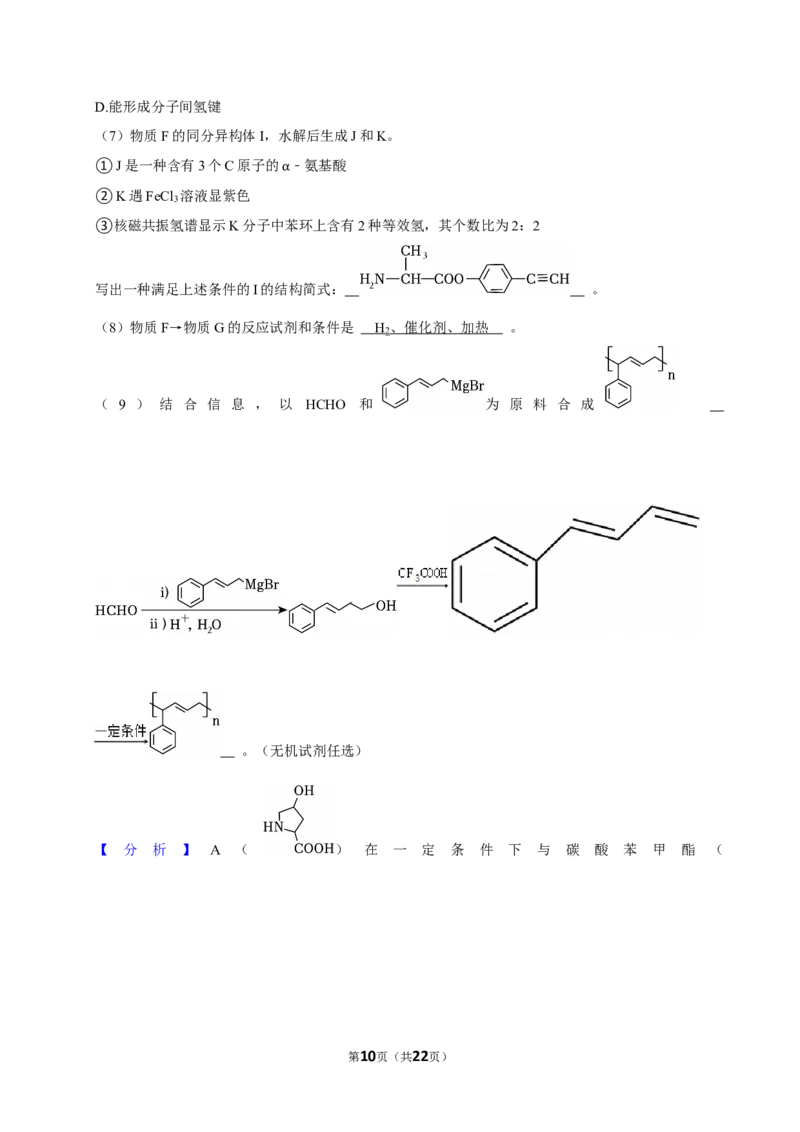
第9页(共22页)D.能形成分子间氢键
(7)物质F的同分异构体I,水解后生成J和K。
①J是一种含有3个C原子的 ﹣氨基酸
②K遇FeCl 3 溶液显紫色 α
③核磁共振氢谱显示K分子中苯环上含有2种等效氢,其个数比为2:2
写出一种满足上述条件的I的结构简式: 。
(8)物质F→物质G的反应试剂和条件是 H 、催化剂、加热 。
2
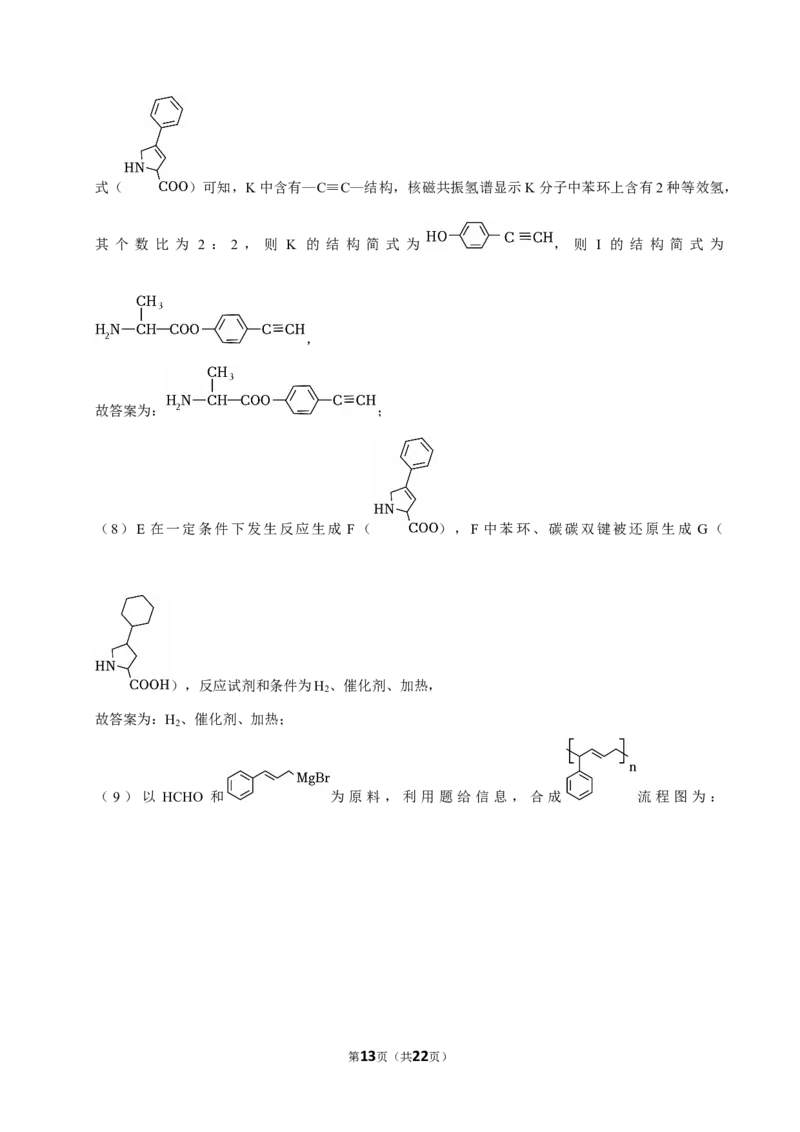
( 9 ) 结 合 信 息 , 以 HCHO 和 为 原 料 合 成
。(无机试剂任选)
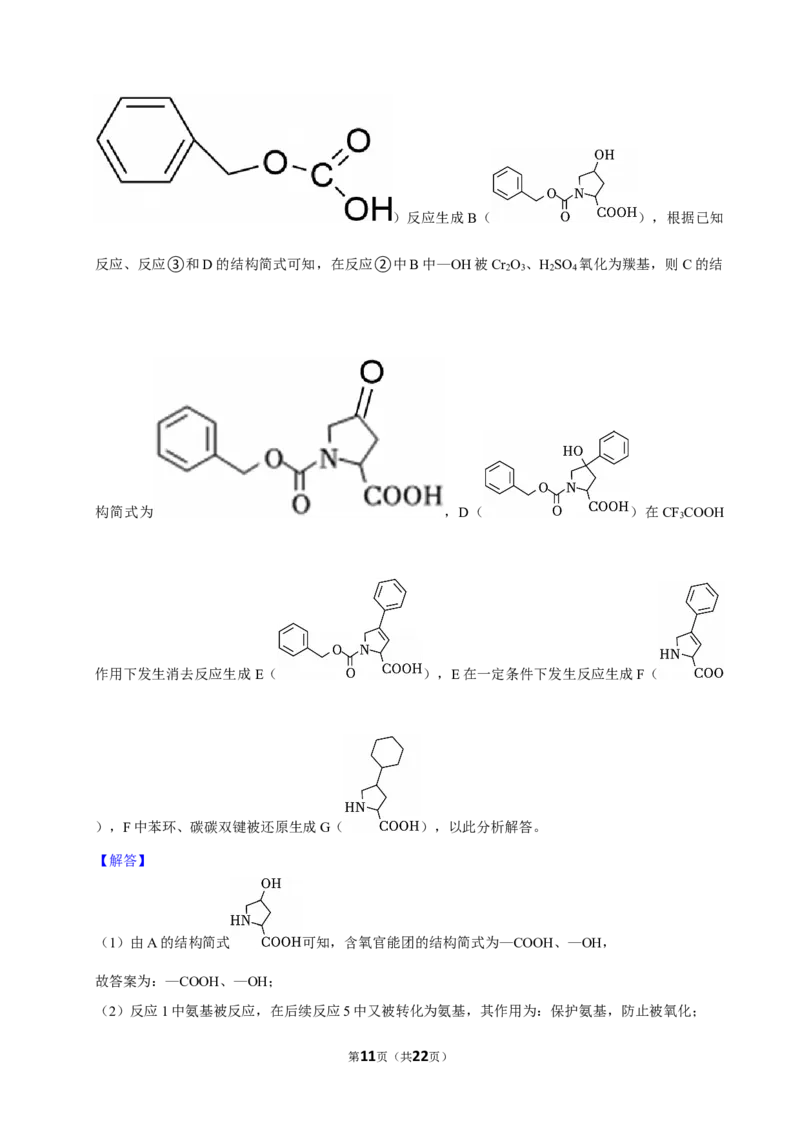
【 分 析 】 A ( ) 在 一 定 条 件 下 与 碳 酸 苯 甲 酯 (
第10页(共22页))反应生成B( ),根据已知
反应、反应③和D的结构简式可知,在反应②中B中—OH被Cr O 、H SO 氧化为羰基,则C的结
2 3 2 4
构简式为 ,D( )在CF COOH
3
作用下发生消去反应生成E( ),E在一定条件下发生反应生成F(
),F中苯环、碳碳双键被还原生成G( ),以此分析解答。
【解答】
(1)由A的结构简式 可知,含氧官能团的结构简式为—COOH、—OH,
故答案为:—COOH、—OH;
(2)反应1中氨基被反应,在后续反应5中又被转化为氨基,其作用为:保护氨基,防止被氧化;
第11页(共22页)(3)由分析,B中羟基被氧化为羰基,为氧化反应;
(4)手性碳原子是连有四个不同基团的碳原子; 中含有2个手性碳原
子,
(5)发生消去反应时,—OH与相邻碳原子上的H结合生成水和碳碳双键,生成物质E时会生成其同
分异构体H,H的结构简式为 ,
故答案为: ;
(6)
A.苯环碳、羰基碳为 杂化,饱和碳为sp3杂化,错误;
B.茚三酮反应是一种化学反应,是指在加热条件及弱酸环境下,氨基酸或肽与茚三酮作用生成有特
殊颜色的化合物及相应的醛和二氧化碳的反应。由E结构可知其不能与茚三酮反应,错误;
C.分子中含羧基,能与 反应产生 ,正确;
D.当氢原子连接在电负性大且原子半径小的原子(例如氟、氧、氮)上时,可以形成氢键;分子中
含有N、羧基,则能形成分子间氢键,正确;
故选CD;
(7)J是一种含有3个C原子的 ﹣氨基酸,则J的结构简式为 ;K遇FeCl 溶液
3
α
显紫色,则K中含有含有酚羟基与苯环,物质F的同分异构体I,水解后生成J和K,根据F的结构简
第12页(共22页)式( )可知,K中含有—C≡C—结构,核磁共振氢谱显示K分子中苯环上含有2种等效氢,
其 个 数 比 为 2 : 2 , 则 K 的 结 构 简 式 为 , 则 I 的 结 构 简 式 为
,
故答案为: ;
(8)E 在一定条件下发生反应生成 F( ),F 中苯环、碳碳双键被还原生成 G(
),反应试剂和条件为H 、催化剂、加热,
2
故答案为:H 、催化剂、加热;
2
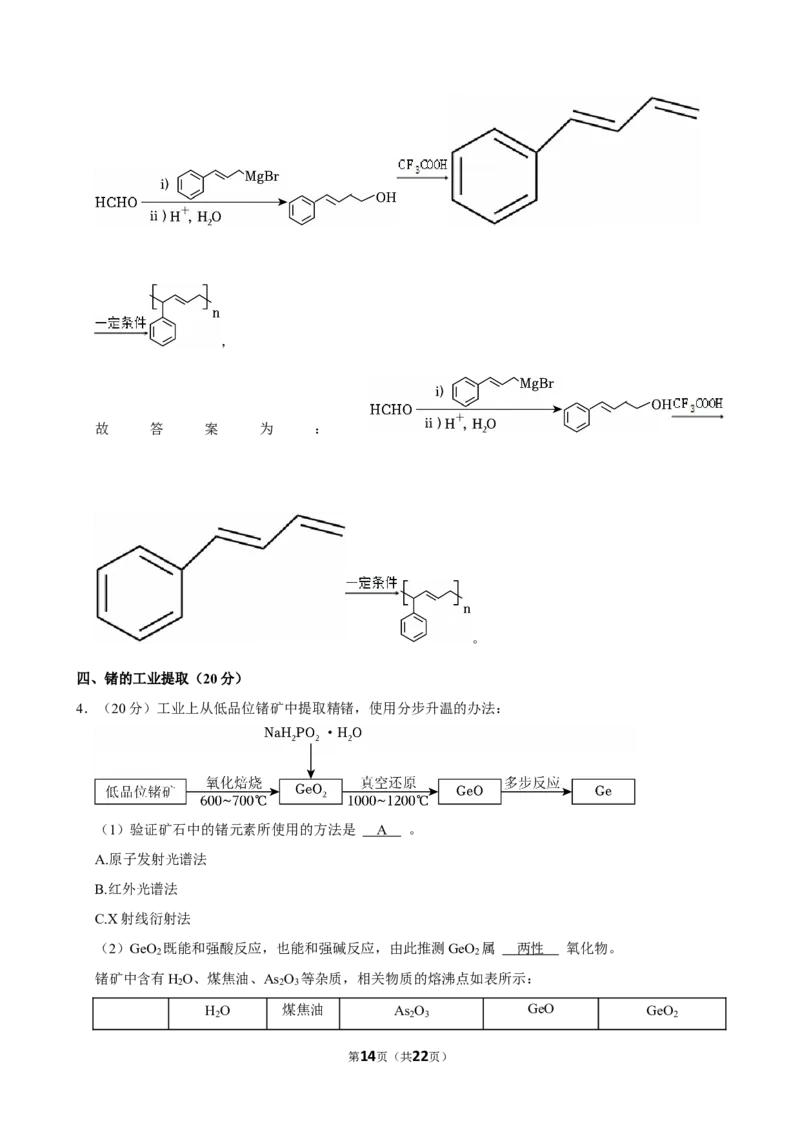
(9)以 HCHO 和 为原料,利用题 给信息,合成 流程图为:
第13页(共22页),
故 答 案 为 :
。
四、锗的工业提取(20分)
4.(20分)工业上从低品位锗矿中提取精锗,使用分步升温的办法:
(1)验证矿石中的锗元素所使用的方法是 A 。
A.原子发射光谱法
B.红外光谱法
C.X射线衍射法
(2)GeO 既能和强酸反应,也能和强碱反应,由此推测GeO 属 两性 氧化物。
2 2
锗矿中含有H O、煤焦油、As O 等杂质,相关物质的熔沸点如表所示:
2 2 3
H O 煤焦油 As O GeO GeO
2 2 3 2
第14页(共22页)熔点/℃ 0 20~30 312 710℃时升华 1100℃时升华
沸点/℃ 100 70~80 465 / /
(3)使用分步升温的原因是 可以将煤焦油、 A s O 等杂质分步蒸,分离,在 71 0 ℃~ 110 0 ℃之间可
2 3
以将 GeO 、 GeO 分步分离出来,再将 GeO 还原为 GeO ,从而得到更纯的 G e 。
2 2
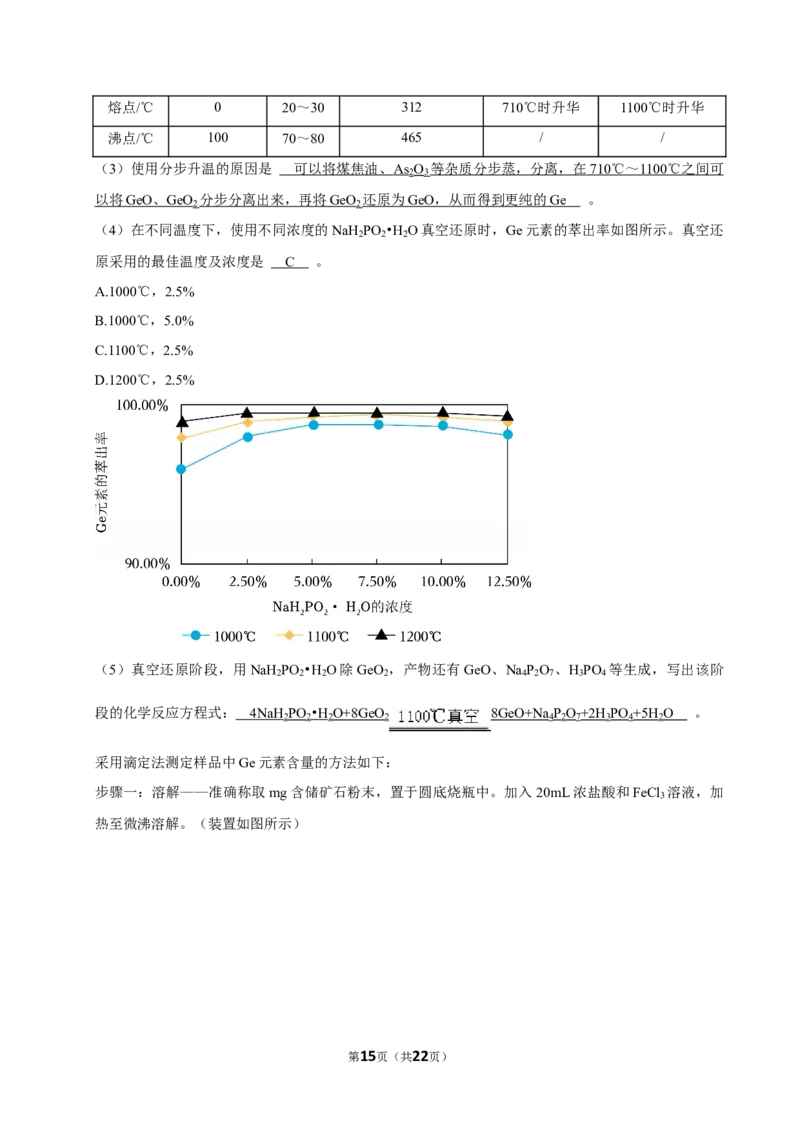
(4)在不同温度下,使用不同浓度的NaH PO •H O真空还原时,Ge元素的萃出率如图所示。真空还
2 2 2
原采用的最佳温度及浓度是 C 。
A.1000℃,2.5%
B.1000℃,5.0%
C.1100℃,2.5%
D.1200℃,2.5%
(5)真空还原阶段,用NaH PO •H O除GeO ,产物还有GeO、Na P O 、H PO 等生成,写出该阶
2 2 2 2 4 2 7 3 4
段的化学反应方程式: 4NaH PO • H O+8GeO 8GeO+Na P O +2H PO +5H O 。
2 2 2 2 4 2 7 3 4 2
采用滴定法测定样品中Ge元素含量的方法如下:
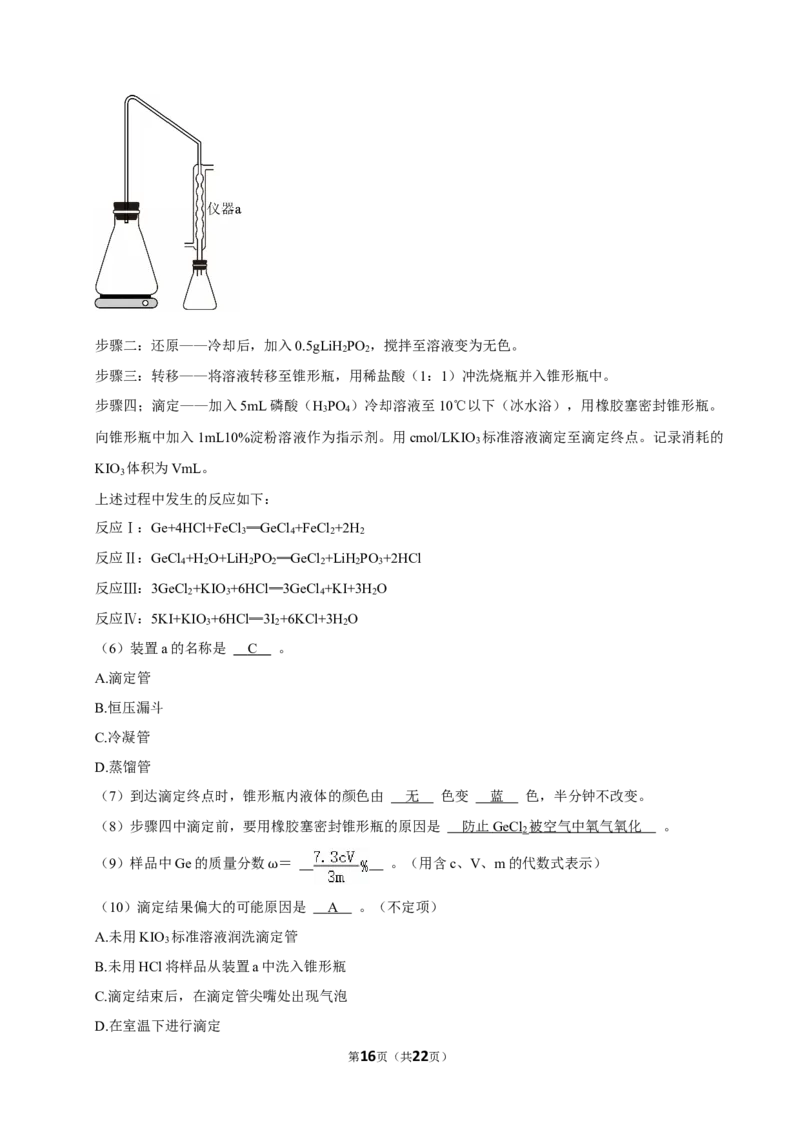
步骤一:溶解——准确称取mg含储矿石粉末,置于圆底烧瓶中。加入20mL浓盐酸和FeCl 溶液,加
3
热至微沸溶解。(装置如图所示)
第15页(共22页)步骤二:还原——冷却后,加入0.5gLiH PO ,搅拌至溶液变为无色。
2 2
步骤三:转移——将溶液转移至锥形瓶,用稀盐酸(1:1)冲洗烧瓶并入锥形瓶中。
步骤四;滴定——加入5mL磷酸(H PO )冷却溶液至10℃以下(冰水浴),用橡胶塞密封锥形瓶。
3 4
向锥形瓶中加入1mL10%淀粉溶液作为指示剂。用cmol/LKIO 标准溶液滴定至滴定终点。记录消耗的
3
KIO 体积为VmL。
3
上述过程中发生的反应如下:
反应Ⅰ:Ge+4HCl+FeCl ═GeCl +FeCl +2H
3 4 2 2
反应Ⅱ:GeCl +H O+LiH PO ═GeCl +LiH PO +2HCl
4 2 2 2 2 2 3
反应Ⅲ:3GeCl +KIO +6HCl═3GeCl +KI+3H O
2 3 4 2
反应Ⅳ:5KI+KIO +6HCl═3I +6KCl+3H O
3 2 2
(6)装置a的名称是 C 。
A.滴定管
B.恒压漏斗
C.冷凝管
D.蒸馏管
(7)到达滴定终点时,锥形瓶内液体的颜色由 无 色变 蓝 色,半分钟不改变。
(8)步骤四中滴定前,要用橡胶塞密封锥形瓶的原因是 防止 GeC l 被空气中氧气氧化 。
2
(9)样品中Ge的质量分数 = 。(用含c、V、m的代数式表示)
ω
(10)滴定结果偏大的可能原因是 A 。(不定项)
A.未用KIO 标准溶液润洗滴定管
3
B.未用HCl将样品从装置a中洗入锥形瓶
C.滴定结束后,在滴定管尖嘴处出现气泡
D.在室温下进行滴定
第16页(共22页)【分析】
(1)不同元素的原子发射光谱是不同的;
(2)两性氧化物既能和强酸反应,也能和强碱反应;
(3)分步升温可以将煤焦油、As O 等杂质分步蒸,分离,在710℃~1100℃之间可以将GeO、GeO
2 3 2
分步分离出来,再将GeO 还原为GeO,从而得到更纯的Ge;
2
(4)由图可知,真空还原采用的最佳温度及浓度是1100℃,2.5%,此时锗的萃出率较高,若温度过
高,需要的能耗高,且GeO 易升华;
2
(5)根据化合价升降守恒、原子守恒书写该阶段的化学反应方程式;
(6)根据a的构造判断其名称;
(7)到达滴定终点时,过量的KIO 会与反应Ⅲ生成的KI发生反应Ⅳ,生成I ,I 遇到淀粉显蓝色;
3 2 2
(8)GeCl 易被空气中氧气氧化;
2
(9)根据题意有关系式:3Ge~KIO ,进一步计算样品中Ge的质量分数;
3
(10)根据关系式:3Ge~KIO ,若导致KIO 标准溶液消耗的体积偏大,则测定结果偏大,反之偏小
3 3
或不变。
【解答】
(1)
A.原子发射光谱法可以测元素的种类,故A正确;
B.红外光谱法可以测有机物的结构,故B错误;
C.X射线衍射法可以测晶体的结构,故C错误;
故选:A;
(2)既能和酸又能和碱反应生成盐和水的氧化物属于两性氧化物;既能和强酸反应,也能与强碱反应,
由此推测是两性氧化物;
(3)在 焙烧可除去矿石中的 、煤焦油、 等杂质,将 元素氧化为 ;
②真空还原阶段,升温到 , 升华蒸出;使用分段升温,可以除去杂质,能得到较
纯的 ;
(4)由图, ,使用2.5%的 真空还原时, 元素的萃出率几乎为100%,此
时能节约能源和原料;
(5)真空还原阶段,用NaH PO •H O除GeO ,产物还有GeO、Na P O 、H PO 等生成,根据化合
2 2 2 2 4 2 7 3 4
第17页(共22页)价升降守恒、原子守恒可得该阶段的化学反应方程式为:4NaH PO •H O+8GeO
2 2 2 2
8GeO+Na P O +2H PO +5H O,
4 2 7 3 4 2
故答案为:4NaH PO •H O+8GeO 8GeO+Na P O +2H PO +5H O;
2 2 2 2 4 2 7 3 4 2
(6)由图,装置a名称为球形冷凝管,故选C;
(7)到达滴定终点时,过量的KIO 会与反应Ⅲ生成的KI发生反应Ⅳ,生成I ,I 遇到淀粉显蓝色,
3 2 2
故锥形瓶内液体的颜色由无色变蓝色,半分钟不改变,
故答案为:无;蓝;
(8)空气中氧气具有氧化性,实验盖紧塞子防止 被氧化(或绝氧气,避免 被氧化为
,否则导致滴定结果偏低),从而产生滴定误差;
( 9 ) 根 据 题 意 有 关 系 式 : 3Ge ~ KIO , 样 品 中 Ge 的 质 量 分 数 =
3
ω
×100%= ,
故答案为: ;
(10)A.未用KIO 标准溶液润洗滴定管,导致KIO 标准溶液浓度降低,测定时,消耗的KIO 标准溶
3 3 3
液的体积偏大,测定结果偏大,故A正确;
B.未用HCl将样品从装置a中洗入锥形瓶,导致GeCl 减少,最终消耗的KIO 标准溶液的体积偏小,
4 3
测定结果偏小,故B错误;
C.滴定结束后,在滴定管尖嘴处出现气泡,最终消耗的KIO 标准溶液的体积偏小,测定结果偏小,故
3
C错误;
D.在室温下进行滴定,对测定结果没有影响,故D错误;
故答案为:A。
五、铁及其化合物(20分)
5.(20分)铁红是一种红色颜料。
(1)铁红的主要成分是 D 。
A.Fe S
2 3
B.Fe O
3 4
第18页(共22页)C.FeS
D.Fe O
2 3
(2)下列关于饱和FeCl 溶液的说法中正确的是 C 。
3
A.常温显中性
B.加铁粉变红褐色
C.遇沸水得到胶体
D.加氨水出现白色沉淀
(3)下列有关基态Fe的说法中正确的是 C 。(不定项)
A.电子处在4个不同能级
B.核外有5个未成对电子
C.核外电子占用15个原子轨道
D.核外有26种能量不同的电子
(4)混合铁粉和硫粉,在试管中加热,那么 A 。(不定项)
A.移开酒精灯后,固体仍保持红热
B.S作还原剂
C.主要的气体副产物是SO
3
D.最终得到黑色的Fe S
2 3
(5)配合物[Fe(SCN)(H O) ]Cl 内界为 ,配体有 2 种。
2 5 2
(6)在FeCl 溶液中存在平衡:Fe3+(aq)+xCl﹣(aq) [FeCl]3﹣x(aq)(x=1、2、3、4)。若加水
3
稀释溶液到原体积的两倍,则m(Fe3+) 变大 ;(⇌填“变大”、“不变”或“变小”)
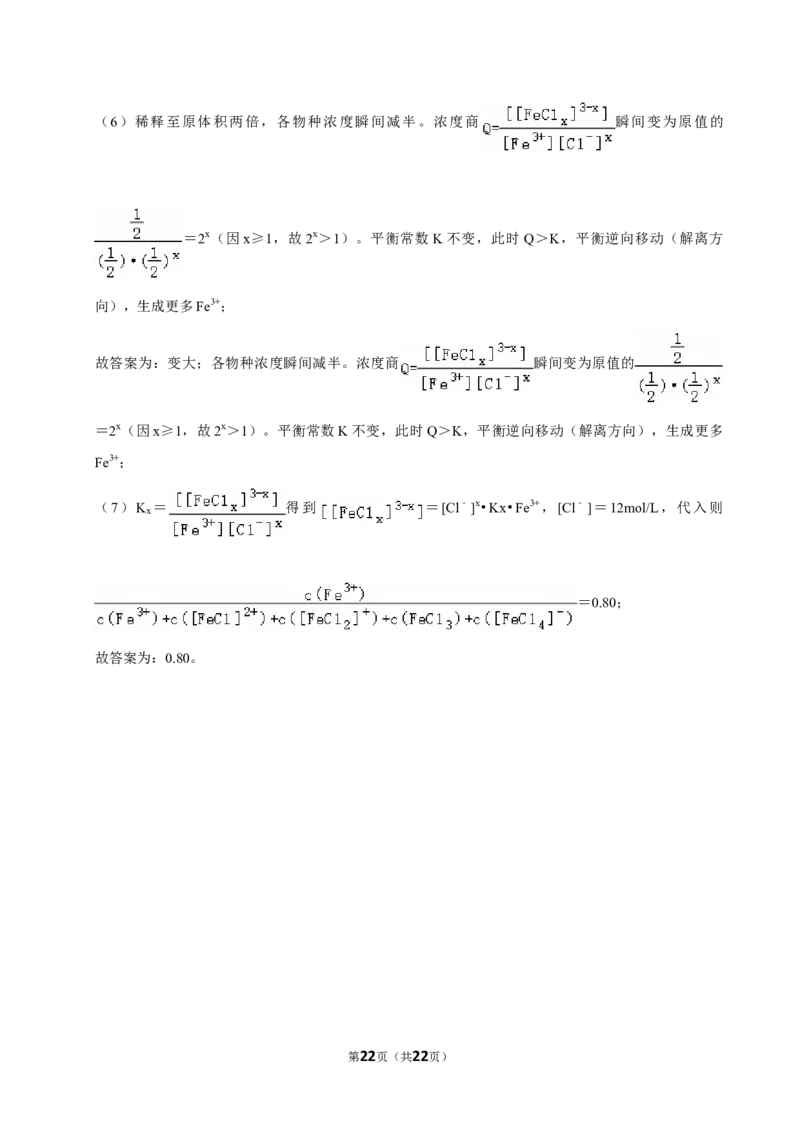
请从浓度商 Q、平衡常数 K 的大小关系角度解释原因 各物种浓度瞬间减半。浓度商
瞬间变为原值的 = 2 x (因 x ≥ 1 ,故 2 x > 1 )。平衡常数 K 不变,此
时 Q > K ,平衡逆向移动(解离方向),生成更多 F e 3 + 。
(7)已知Fe3+(aq)+xCl﹣(aq) [FeCl ]3﹣x(aq)的平衡常数K 如表所示。
x x
x 1 ⇌ 2 3 4
K 30.2 134.9 97.72 1.02
x
若 溶 液 中 [Cl﹣ ] = 12mol• L﹣ 1 , 则
第19页(共22页)= 0.80 。(保留
两位小数)
【分析】
(1)铁红是一种红色颜料,其主要成分为氧化铁(Ⅲ),化学式为Fe O ;
2 3
(2)A.常温显中性:FeCl 是强酸弱碱盐,水解显酸性;
3
B.加铁粉变红褐色:加铁粉发生反应2FeCl +Fe→3FeCl ,溶液由黄褐色变为浅绿色,不是红褐色;
3 2
C.遇沸水得到胶体:FeCl 溶液在沸水中水解生成Fe(OH) 胶体;
3 3
D.加氨水出现白色沉淀:加氨水生成红褐色Fe(OH) 沉淀,不是白色;
3
(3)A.电子处在4个不同能级:实际能级包括1s,2s,2p,3s,3p,4s,3d共7个;
B.核外有5个未成对电子:3d6轨道有4个未成对电子(洪特规则),4s2全成对,共4个;
C.核外电子占用15个原子轨道:轨道分布为1s(1),2s(1),2p(3),3s(1),3p(3),4s
(1),3d(5),总和1+1+3+1+3+1+5=15;
D.核外有26种能量不同的电子:电子能量由能级决定,共有7个不同能级,能量不同的电子最多7种;
(4)A.移开酒精灯后,固体仍保持红热:反应放热,可持续红热;
B.S作还原剂:S从0价降至﹣2价,作氧化剂;
C.主要的气体副产物是SO :反应无气体产物,SO 需氧化剂;
3 3
D.最终得到黑色的Fe S :产物为FeS,Fe S 不稳定;
2 3 2 3
(5)内界:配离子部分,为 配体:提供孤对电子的分子或离子,有SCN﹣
(异硫氰酸根)和H O(水)两种;
2
(6)稀释至原体积两倍,各物种浓度瞬间减半。浓度商 瞬间变为原值的
=2x(因x≥1,故2x>1)。平衡常数K不变,此时Q>K,平衡逆向移动(解离方
向),生成更多Fe3+;
(7)K = 得到 =[Cl﹣]x•Kx•Fe3+,[Cl﹣]=12mol/L,代入则
x
第20页(共22页)=0.80;
【解答】
(1)铁红是一种红色颜料,其主要成分为氧化铁(Ⅲ),化学式为Fe O ;
2 3
A.Fe S 为硫化铁,不是红色;
2 3
B.Fe O 为四氧化三铁,黑色;
3 4
C.FeS为硫化亚铁,黑色;
D.Fe O 为三氧化二铁,红色;
2 3
故答案为:D;
(2)
A.饱和氯化铁溶液中铁离子水解使得溶液显酸性,A错误;
B.铁和铁离子生成亚铁离子,溶液变为浅绿色,B错误;
C.制取 红褐色胶体应该向煮沸的蒸馏水中滴加饱和氯化铁溶液至溶液变红褐色,C正确;
D.加氨水生成红褐色氢氧化铁沉淀,D错误;
故选C。
(3)
铁为26号元素原子,基态Fe原子核外电子排布为1s22s22p63s23p63d64s2;
A.有7个不同能级的电子,错误;
B.有4个未成对电子,错误;
C.占据15个原子轨道,正确;
D.同一能级能量相同,有7种能量不同的电子,错误;
故选C;
(4)
A.铁和硫反应为放热反应,移开酒精灯后固体保持红热,正确;
B.反应生成FeS,S化合价降低,做氧化剂,错误;
C.主要产生的气体附产物为二氧化硫,而非,错误;
D.最终得到黑色的FeS,错误;
故选A;
(5)内界:配离子部分,为 配体:提供孤对电子的分子或离子,有SCN﹣
(异硫氰酸根)和H O(水)两种;
2
故答案为: ;2;
第21页(共22页)(6)稀释至原体积两倍,各物种浓度瞬间减半。浓度商 瞬间变为原值的
=2x(因x≥1,故2x>1)。平衡常数K不变,此时Q>K,平衡逆向移动(解离方
向),生成更多Fe3+;
故答案为:变大;各物种浓度瞬间减半。浓度商 瞬间变为原值的
=2x(因x≥1,故2x>1)。平衡常数K不变,此时Q>K,平衡逆向移动(解离方向),生成更多
Fe3+;
(7)K = 得到 =[Cl﹣]x•Kx•Fe3+,[Cl﹣]=12mol/L,代入则
x
=0.80;
故答案为:0.80。
第22页(共22页)