文档内容
(3)无机非金属材料—高一化学人教版暑假作业本
1.下列说法正确的是( )
A. 既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
B.稀硝酸和锌反应产生的氢气可为工业制氨提供原料
C. 是空气中的主要成分之一,雷雨时可直接转化为
D. 和NO都不是酸性氧化物
2.下列关于硅及其化合物的叙述正确的是( )
A.硅晶体可用于制造光导纤维
B.陶瓷、玻璃、水泥都是硅酸盐产品
C.二氧化硅在电子工业中是重要的半导体材料
D.二氧化硅与氢氟酸和氢氧化钠均能反应,属于两性氧化物
3.接触法制硫酸、氨氧化法制硝酸、工业制备高纯硅分别经过下列主要变化:
下列说法符合事实的是( )
A.第8、9两步互为可逆反应
B.第3、6步都是直接用水吸收
C.第7步 过量,会发生:
D.第9步反应发生前,首先要对第8步反应产物进行蒸馏,得到纯净的
4.下列叙述正确的有( )
① 、 均能使品红溶液褪色,说明二者均有氧化性
② 、 均不能用浓硫酸干燥
③常温下,通常用铝制容器盛放浓硫酸,是因为铝与浓硫酸不反应
④ 是两性氧化物
⑤实验室中用加热 分解来制取氨气⑥由 可推知碳的非金属性比硅强
⑦燃煤加入生石灰能有效减少酸雨的形成及温室气体的排放
⑧化石燃料和植物燃料燃烧释放出的能量均来源于太阳能
A.2项 B.3项 C.4项 D.5项
5.作为全球最大的电子产品制造国,中国却有着“芯”病。我国国产芯片自给率不到30%,
产值不足全球的7%,市场份额不到10%。下列说法正确的是( )
A.水晶和陶瓷都是硅酸盐制品
B.CPU半导体芯片与光导纤维是同种材料
C.高纯硅、碳化硅(SiC)属于新型无机非金属材料
D.粗硅制备单晶硅涉及反应之一:
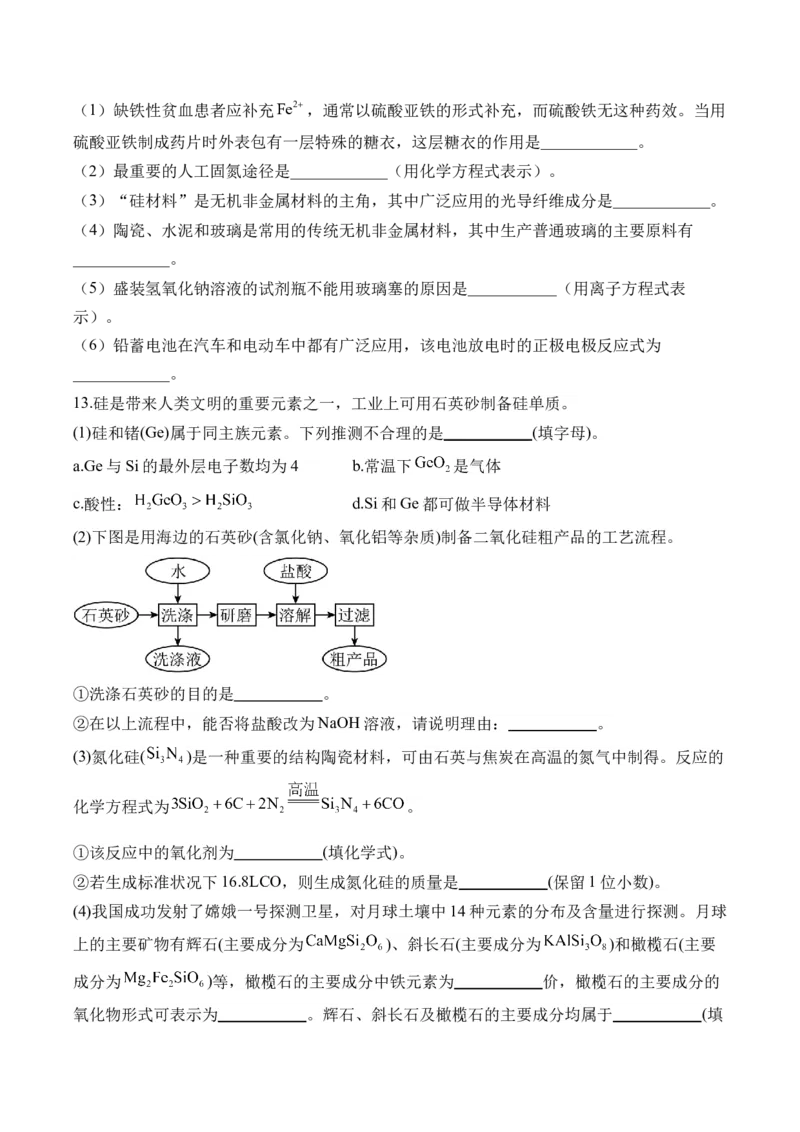
6.高纯单晶硅是重要的半导体材料,在各种集成电路、芯片和CPU的制作中有不可替代的作
用。实验室中模拟 制备高纯硅的装置如图所示(夹持装置略去),下列说法错误的是(
)(已知:电负性 , 的沸点为31.8℃,熔点为-126.5℃,在空气中易自燃,
遇水会剧烈反应)
A.实验过程中,加热石英管前应先对 进行验纯
B.实验开始时,排尽装置中的空气是为了防止 自燃和水解
C.尾气通入NaOH溶液中, 发生反应的化学方程式为
D.为提高装置Ⅳ中 的利用率,装置Ⅲ应使用冷水浴
7.“中国芯”的主要原料是单晶硅,制取纯硅的过程如图所示。下列说法正确的是( )A.步骤①中的反应为
B.二氧化硅是酸性氧化物,能与水反应生成硅酸
C.步骤②和③均属于置换反应
D.28g纯硅中含有4molSi-Si键
8.在给定条件下,能顺利实现下列所示物质间直接转化的是( )
A.S
B.
C.
D.Fe
9.硫元素和氮元素与人类生活息息相关。下列有关说法正确的是( )
A.氮化硅陶瓷属于传统无机非金属材料,可用于制作高温电极材料
B.硫代硫酸钠( )是一种常用的解毒剂,可通过硫酸钠与二氧化硫反应来制得
C.汽油不充分燃烧产生的NO是产生硝酸型酸雨的重要原因
D.食品中添加适量 可起到漂白、防腐和抗氧化作用
10.2023年5月21日世界级重大考古发现:在我国南海发现明代的沉船,“沉没的历史”逐
渐浮出水面,一号沉船遗物以外销的瓷器为主、二号沉船遗物以海外输入的木材为主。下列
说法错误的是( )
A.陶瓷是以粘土为主要原料,经过复杂的物理、化学变化高温烧结而成的
B.SiC、 、 等新型陶瓷具有新的特性和功能,进一步拓展了陶瓷的应用领域
C.木材的主要化学成分是纤维素,食物中的纤维素能够为人体提供能量
D.纤维素和淀粉分子式均为 ,都能发生水解,且最终产物都是葡萄糖
11.许多无机非金属材料含有硅元素,具有耐高温、抗腐蚀、硬度高等特点,以及特殊的光
学、电学等性能。以下为制备高纯硅、氮化硅的主要工艺流程图:已知: ,沸点31.5℃,且能与 剧烈反应,并在空气中易自燃。
回答下列问题:
(1)Si在元素周期表中的位置为________。
(2)若用如图所示装置证明非金属性: ,从以下所给物质中选出合适的物质:①稀盐
酸;②稀硫酸;③碳酸钠;④ 溶液。试剂A为________(填序号,下同),试剂C
为________。
(3)反应①常伴有副反应: 。若产物中硅与碳化硅的物质的量
之比为10:3,则参与反应的 和C的物质的量之比为________。
(4)该工艺中制备 的化学方程式为________。
(5)若在实验室中完成 与过量 制备纯硅,其装置如图(热源及夹持装置已略
去)。
装置B中的试剂是________(填名称),实验中先让稀硫酸与锌粒反应一段时间后,再加热
C、D装置的目的是________。
(6)该工艺中制备氮化硅的同时会生成一种可燃性有毒气体,反应⑤的化学方程式为
________。
(7)上述制备高纯硅、氮化硅的工艺流程中可以循环利用的物质是________(填化学式)。
12.化学就在我们身边,它与我们的日常生活密切相关。按要求回答以下问题:(1)缺铁性贫血患者应补充Fe2,通常以硫酸亚铁的形式补充,而硫酸铁无这种药效。当用
硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是____________。
(2)最重要的人工固氮途径是____________(用化学方程式表示)。
(3)“硅材料”是无机非金属材料的主角,其中广泛应用的光导纤维成分是____________。
(4)陶瓷、水泥和玻璃是常用的传统无机非金属材料,其中生产普通玻璃的主要原料有
____________。
(5)盛装氢氧化钠溶液的试剂瓶不能用玻璃塞的原因是___________(用离子方程式表
示)。
(6)铅蓄电池在汽车和电动车中都有广泛应用,该电池放电时的正极电极反应式为
____________。
13.硅是带来人类文明的重要元素之一,工业上可用石英砂制备硅单质。
(1)硅和锗(Ge)属于同主族元素。下列推测不合理的是___________(填字母)。
a.Ge与Si的最外层电子数均为4 b.常温下 是气体
c.酸性: d.Si和Ge都可做半导体材料
(2)下图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。
①洗涤石英砂的目的是___________。
②在以上流程中,能否将盐酸改为NaOH溶液,请说明理由:___________。
(3)氮化硅( )是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气中制得。反应的
化学方程式为 。
①该反应中的氧化剂为___________(填化学式)。
②若生成标准状况下16.8LCO,则生成氮化硅的质量是___________(保留1位小数)。
(4)我国成功发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球
上的主要矿物有辉石(主要成分为 )、斜长石(主要成分为 )和橄榄石(主要
成分为 )等,橄榄石的主要成分中铁元素为___________价,橄榄石的主要成分的
氧化物形式可表示为___________。辉石、斜长石及橄榄石的主要成分均属于___________(填“氧化物”“混合物”或“硅酸盐”)。
14.Ⅰ.已知:金属钠和空气可以制备纯度较高的 , 易与空气中 、水蒸气反
应。现用金属钠和空气制备纯度较高的 ,可利用的装置如图所示。回答下列问题:
(1)装置Ⅳ中盛放的试剂是______。
(2)若规定气体的气流方向从左到右,则组合实验装置时各接口的连接顺序为
______→a→b→c。
Ⅱ.某实验小组设计了如下装置对焦炭还原二氧化硅的气体产物的成分进行探究。
已知: 溶液可用于检验CO,反应的化学方程式为
(产生黑色金属钯粉末,使溶液变浑浊)。
(3)装置B的作用是______,若装置C、D中溶液均变浑浊,且经检测两种气体产物的物质
的量相等,则该反应的化学方程式为______。
(4)该装置的缺点是______。
Ⅲ.在恒容密闭容器中,用 还原 ,生成S的反应分两步完成(如图所示),请分析并回
答如下问题:
(5)分析可知X为______(填化学式)。
(6)环保监测部门为了测定某硫酸厂周围空气中的 含量进行了如下实验:取标准状况下
1.000L空气(含 、 、 、 ),缓慢通过足量碘水。在所得溶液中加入稍过量的溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为0.233g。则空气样品中
的体积分数为______。
答案以及解析
1.答案:D
解析:A项, 是酸性氧化物,错误;
B项,稀硝酸和锌反应产生的是NO,错误;
C项,雷雨时 可直接转化为NO,错误;
D项, 和NO都不是酸性氧化物,正确。
2.答案:B
解析:二氧化硅晶体可用于制造光导纤维,故A错误;玻璃的主要原料是纯碱、石灰石、石
英,水泥的主要原料是黏土、石灰石,陶瓷主要原料是黏土,石英主要成分是二氧化硅、黏
土属于硅酸盐,故都属于硅酸盐产品,故B正确;晶体硅是半导体的材料,而不是二氧化
硅,故C错误;二氧化硅既能与氢氟酸反应,又能与烧碱反应,但二氧化硅和HF反应生成
四氟化硅而不是盐,所以它是酸性氧化物而不是两性氧化物,故D错误;故选B。
3.答案:D
4.答案:A
解析:①二氧化硫与品红化合生成无色物质,与氧化性无关,而 能使品红溶液褪色,与
HClO的氧化性有关,故错误;
②硫化氢为酸性且有还原性的气体,能被浓硫酸氧化,不能用浓硫酸干燥;氨气为碱性气
体,不能用浓硫酸干燥,故正确;
③常温下能用铝制容器盛放浓硫酸,是因为反应生成了致密的氧化膜阻止进一步反应,故错
误;
④二氧化硅与氢氟酸反应生成物为四氟化硅和水,不符合两性氧化物的概念,不是两性氧化
物,二氧化硅属于酸性氧化物,故错误;
⑤ 受热分解生成的氨气和氯化氢遇冷又会重新结合生成氯化铵,故不能用加热
分解来制取氨气,故错误;⑥根据反应 分析,高温下碳的还原性比硅强,但不能说明C、Si的
非金属性强弱,故错误;
⑦燃煤中含有少量硫元素,燃烧时生成大量 和少量 。高温下,生石灰能与 、
反应生成硫酸钙,从而减少酸雨的形成,但不能与二氧化碳反应,不能减少温室气体的排
放,故错误;
⑧化石燃料和植物燃料燃烧时放出的能量均来源于太阳能,故正确;
综上,正确的有②⑧,共2项;
答案选A。
5.答案:C
解析:A.水晶主要成分为二氧化硅,陶瓷的主要成分是硅酸盐,A不正确;
B.CPU半导体芯片用的是晶体硅,光导纤维用的是二氧化硅,两者所用的材料不同,B不正
确;
C.高纯硅、碳化硅(SiC)都属于新型无机非金属材料,C正确;
D.粗硅制备单晶硅涉及反应之一: ,D错误。
故选C。
6.答案:D
解析:A.实验过程中,应先对 进行验纯再加热石英管,防止氢气不纯导致实验失败,故A
正确;
B. 在空气中易自燃,遇水会剧烈反应,实验开始时,排尽装置中的空气是为了防止
自燃和水解,故B正确;
C.电负性 中H为-1价,具有还原性,可与氢氧化钠溶液发生归中反应化学
方程式为: ,故C正确;
D.Ⅳ中是为了使 气化,使得气化后的 与氢气在石英管中反应,不可使用冷水
浴,故D错误;
故选D。
7.答案:C
解析:A.步骤①中的反应为 和焦炭在高温条件生成粗硅和CO,,故A错误;
B.二氧化硅是酸性氧化物,但其不溶于水也不能与水反应,故B错误;
1380K
C.步骤② ,属于置换反应,③SiHCl H Si3HCl也属
3 2
于置换反应,故C正确;
D.硅晶体中1molSi与另外4molSi形成Si-Si键,但是这个Si只占每个键的一半,所以1mol
纯硅含有2molSi-Si键,即28g纯硅中含有2molSi-Si键,故D错误;
故答案为:C。
8.答案:D
解析:A.S与 在点燃时反应产生 ,不能反应产生 ,A不符合题意;
B. 难溶于水,不能发生反应产生 ,B不符合题意;
C. 与 在催化剂存在条件下反应产生NO,不能直接反应产生 ,C不符合题意;
D.Fe与 发生氧化还原反应产生 , 与NaOH发生复分解反应产生 ,能
够实现物质之间的转化关系,D符合题意;
故合理选项是D。
9.答案:D
解析:A.氮化硅陶瓷属于新型无机非金属材料,故A错误;
B.硫酸钠中硫元素的化合价为+6,二氧化硫中硫元素的化合价为+4,而Na S O 中硫元素的
2 2 3
化合价为+2,故不能由硫酸钠与二氧化硫反应来制得硫代硫酸钠(Na S O ),故B错误;
2 2 3
C.产生氮氧化物的主要原因是空气中的氮气在气缸中被氧化,故C错误;
D.二氧化硫具有还原性,能与氧气反应,葡萄酒中添加微量二氧化硫作抗氧化剂,抑制细菌
滋生,起到保质作用,故D正确;
故选D。
10.答案:C
11.答案:(1)第三周期第ⅣA族
(2)②;④
(3)13:29
(4) )(5)浓硫酸;让 排尽装置中的空气,防止 与水反应和自燃
(6)
(7) 、
12.答案:(1)防止硫酸亚铁被氧化
(2)
(3)
(4)纯碱、石英、石灰石
(5)
(6)
解析:(1)由于二价铁容易被氧化成三价铁,故亚铁盐药片需外包糖衣,故此处填:防止硫
酸亚铁被氧化;
(2)最重要的人工固氮是合成氨反应,故此处填: ;
(3)由于 对光的传导能力强,故可以用来生产光导纤维,故此处填 ;
(4)工业上以纯碱、石灰石、石英为原料,在玻璃回转窑中高温煅烧生产玻璃,故此处填:
纯碱、石灰石、石英;
(5)由于NaOH溶液会与玻璃中的 反应生成具有黏性的 ,从而将塞子和瓶体粘
在一起,所以保存NaOH溶液不能用玻璃塞,对应离子方程式为:
;
(6)铅蓄电池负极为Pb,正极为 ,电解质为硫酸溶液,放电时,Pb失电子转化为
, 在正极得电子转化为 ,对应电极反应为:
。
13.答案:(1)bc
(2)除去石英砂表面的NaCl杂质;不能,二氧化硅能与NaOH溶液反应(3) ;17.5g
(4)+2; ;硅酸盐
解析:(1)a.Ge和Si是同主族元素,最外层电子数均为4,故a正确;
b.同主族元素具有相似的性质,常温下 是固体,故 也是固体,故b错误;
c.同主族元素从上到下非金属性逐渐减弱,最高价氧化物对应水化物的酸性逐渐减弱,因此
酸性: ,故c错误;
d.Si和Ge在金属与非金属的交界处,既有金属性,也由非金属性,导电性介于导体和绝缘体
之间,故都可做半导体材料,故d正确。
故选bc;
(2)①石英石不溶于水,氯化钠易溶于水,氧化铝难溶于水,因此洗涤石英砂的目的是除去
石英砂表面的NaCl杂质;②在以上流程中,用盐酸讲氧化铝溶解,而二氧化硅与盐酸不反
应,因此溶解后过滤得到二氧化硅,由于二氧化硅能和氢氧化钠反应,故不能将盐酸改为氢
氧化钠;
(3)①在 反应中,C的化合价由0升高到+2,被氧化,N
的化合价由0价降低到-3价,被还原,故氧化剂为 ;②若生成标准状况下16.8LCO,即物
质的量为 ,根据化学方程式即可得到氮化硅的质量为
;
(4)橄榄石中Mg的化合价为+2价,Si是+4价,O为-2价;根据化合价代数和为0可判断
铁为+2价;根据原子守恒可知橄榄石(主要成分为 )的氧化物形式可表示为
;根据辉石、斜长石及橄榄石的化学式,可判断均为硅酸盐。
14.答案:(1)NaOH溶液
(2)g→h→e→f
(3)作安全瓶,防止倒吸
(4)无尾气处理装置
(5)
(6)2.24%