文档内容
2016 年全国统一高考化学试卷(新课标Ⅰ)
一、选择题(共 7小题,每小题 6分,满分 42分)
1.(6分)化学与生活密切相关,下列有关说法错误的是( )
A.用灼烧的方法可以区分蚕丝和人造纤维
B.食用油反复加热会产生稠环芳香烃等有害物质
C.加热能杀死流感病毒是因为蛋白质受热变性
D.医用消毒酒精中乙醇的浓度为95%
2.(6分)设N 为阿伏加德罗常数值.下列有关叙述正确的是( )
A
A.14g 乙烯和丙烯混合气体中的氢原子数为2N
A
B.1mol N 与4mol H 反应生成的NH 分子数为2N
2 2 3 A
C.1mol Fe溶于过量硝酸,电子转移数为2N
A
D.标准状况下,2.24L CCl 含有的共价键数为0.4N
4 A
3.(6分)下列关于有机化合物的说法正确的是( )
A.2﹣甲基丁烷也称异丁烷
B.由乙烯生成乙醇属于加成反应
C.C H Cl 有3种同分异构体
4 9
D.油脂和蛋白质都属于高分子化合物
4.(6分)下列实验操作能达到实验目的是( )
A.用长颈漏斗分离出乙酸与乙醇反应的产物
B.用向上排空气法收集铜粉与稀硝酸反应产生的NO
C.配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释
D.将Cl 与HCl 混合气体通过饱和食盐水可得到纯净的Cl
2 2
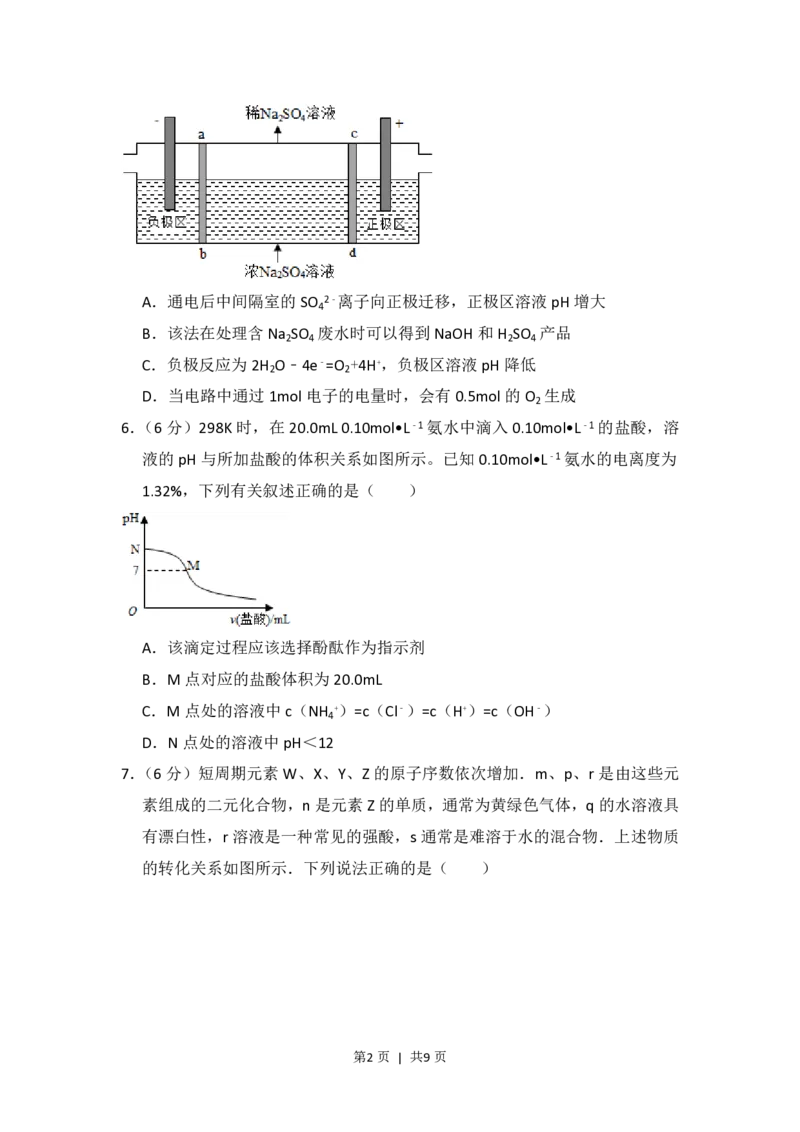
5.(6 分)三室式电渗析法处理含 Na SO 废水的原理如图所示,采用惰性电极,
2 4
ab、cd 均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO 2﹣可通
4
过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确
的是( )
第1页 | 共9页A.通电后中间隔室的SO 2﹣离子向正极迁移,正极区溶液pH增大
4
B.该法在处理含Na SO 废水时可以得到NaOH和H SO 产品
2 4 2 4
C.负极反应为2H O﹣4e﹣=O +4H+,负极区溶液pH降低
2 2
D.当电路中通过1mol 电子的电量时,会有0.5mol的O 生成
2
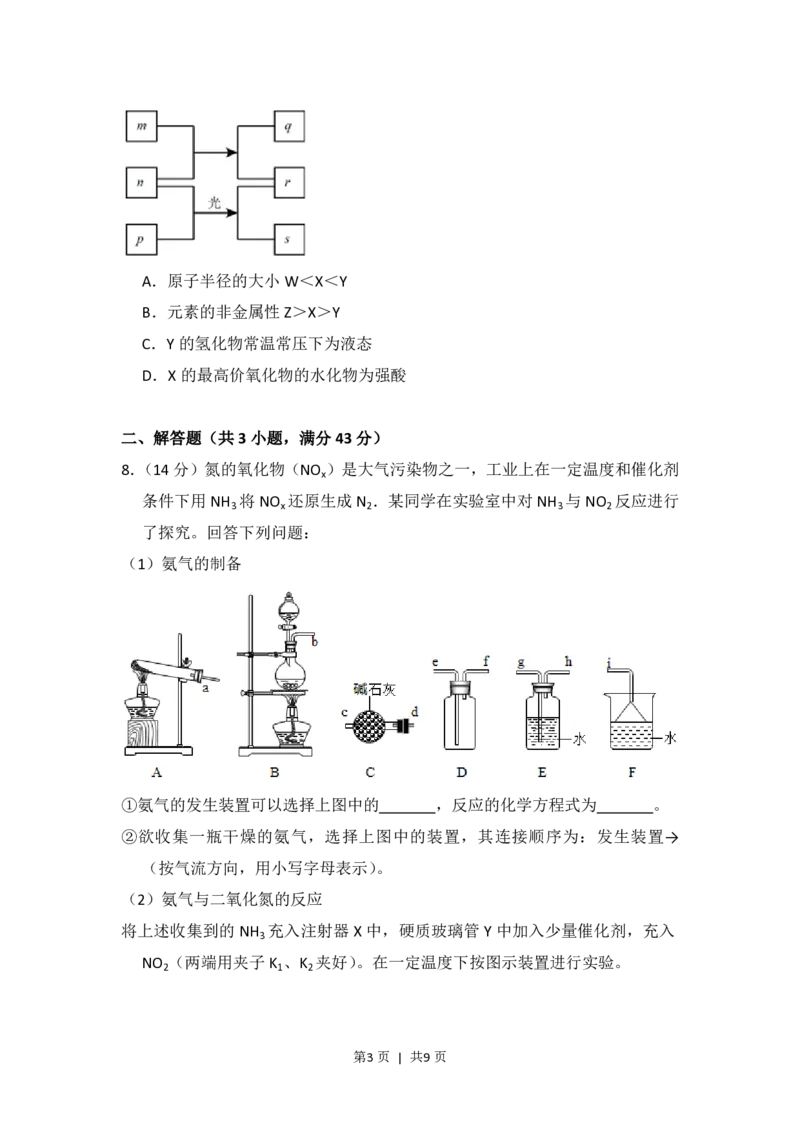
6.(6 分)298K 时,在 20.0mL 0.10mol•L﹣1氨水中滴入 0.10mol•L﹣1的盐酸,溶
液的pH与所加盐酸的体积关系如图所示。已知0.10mol•L﹣1氨水的电离度为
1.32%,下列有关叙述正确的是( )
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0mL
C.M点处的溶液中c(NH +)=c(Cl﹣)=c(H+)=c(OH﹣)
4
D.N点处的溶液中pH<12
7.(6 分)短周期元素 W、X、Y、Z 的原子序数依次增加.m、p、r 是由这些元
素组成的二元化合物,n是元素Z 的单质,通常为黄绿色气体,q的水溶液具
有漂白性,r 溶液是一种常见的强酸,s 通常是难溶于水的混合物.上述物质
的转化关系如图所示.下列说法正确的是( )
第2页 | 共9页A.原子半径的大小W<X<Y
B.元素的非金属性Z>X>Y
C.Y 的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
二、解答题(共 3小题,满分 43分)
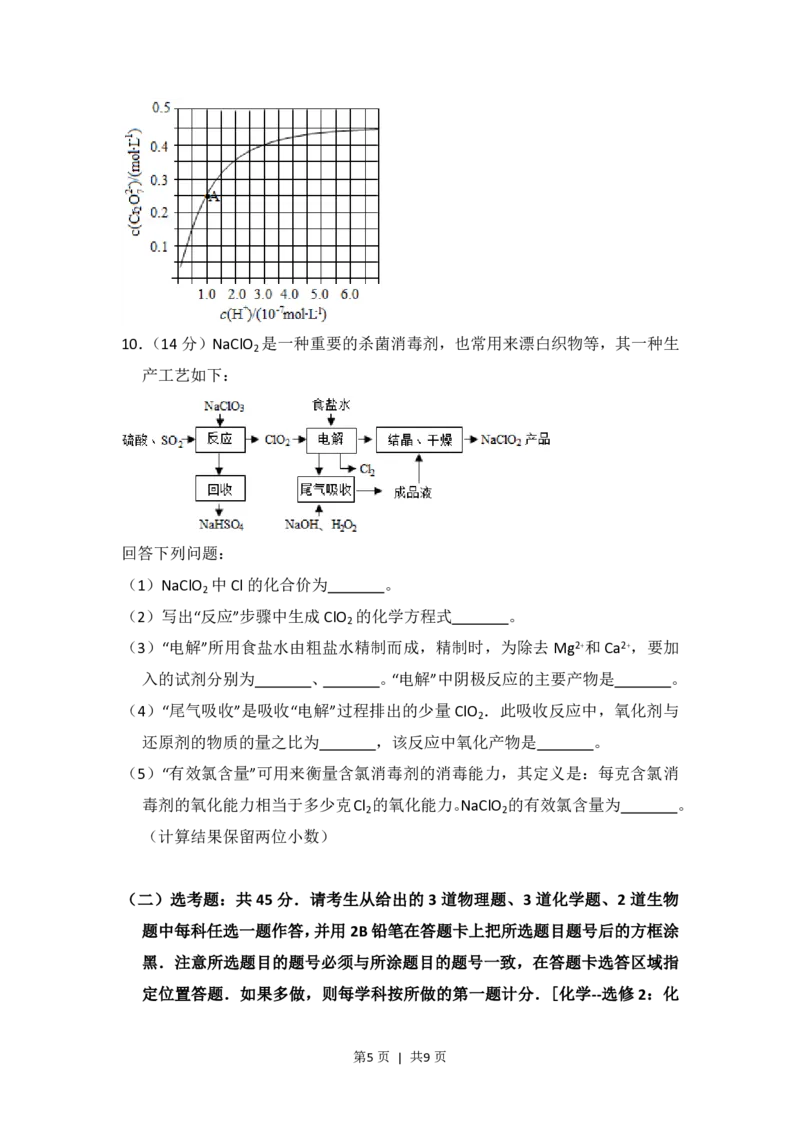
8.(14分)氮的氧化物(NO )是大气污染物之一,工业上在一定温度和催化剂
x
条件下用NH 将NO 还原生成N .某同学在实验室中对NH 与NO 反应进行
3 x 2 3 2
了探究。回答下列问题:
(1)氨气的制备
①氨气的发生装置可以选择上图中的 ,反应的化学方程式为 。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→
(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应
将上述收集到的 NH 充入注射器 X 中,硬质玻璃管 Y 中加入少量催化剂,充入
3
NO (两端用夹子K 、K 夹好)。在一定温度下按图示装置进行实验。
2 1 2
第3页 | 共9页操作步骤 实验现象 解释原因
打开K ,推动注射器活塞,使 ①Y管中 ②反应的化学方程式
1
X中的气体缓慢充入Y管中
将注射器活塞退回原处并固 Y管中有少量水珠 生成的气态水凝聚
定,待装置恢复到室温
打开K ③ ④
2
9.(15 分)元素铬(Cr)在溶液中主要以 Cr3+(蓝紫色)、Cr(OH) ﹣(绿色)、
4
Cr O 2﹣(橙红色)、CrO 2﹣(黄色)等形式存在,Cr(OH) 为难溶于水的灰
2 7 4 3
蓝色固体,回答:
(1)Cr3+与Al3+的化学性质相似,往Cr (SO ) 溶液中滴入NaOH溶液直至过量,
2 4 3
可观察到的现象是 。
(2)CrO 2﹣和Cr O 2﹣在溶液中可相互转化。室温下,初始浓度为1.0mol•L﹣1的
4 2 7
Na CrO 溶液中c(Cr O 2﹣)随c(H+)的变化如图所示。
2 4 2 7
①用离子方程式表示Na CrO 溶液中的转化反应 。
2 4
②由图可知,溶液酸性增强,CrO 2﹣的平衡转化率 (填“增大“减小”或“不
4
变”)。
根据A 点数据,计算出该转化反应的平衡常数为 。
(3)用 K CrO 为指示剂,以 AgNO 标准液滴定溶液中的 Cl﹣,Ag+与 CrO 2﹣生成
2 4 3 4
砖红色沉淀时到达滴定终点。当溶液中Cl﹣恰好完全沉淀(浓度等于1.0×10﹣
5mol•L﹣1)时,溶液中 c (Ag+)为 mol•L﹣1,此时溶液中 c(CrO 2﹣)
4
等于 mol•L﹣1.(K (Ag CrO )=2.0×10﹣12、K (AgCl)=2.0×10﹣10)。
sp 2 4 sp
(4)+6 价铬的化合物毒性较大,常用 NaHSO 将废液中的 Cr O 2﹣还原成 Cr3+,
3 2 7
反应的离子方程式为 。
第4页 | 共9页10.(14分)NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生
2
产工艺如下:
回答下列问题:
(1)NaClO 中Cl 的化合价为 。
2
(2)写出“反应”步骤中生成ClO 的化学方程式 。
2
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 Mg2+和 Ca2+,要加
入的试剂分别为 、 。“电解”中阴极反应的主要产物是 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 ClO .此吸收反应中,氧化剂与
2
还原剂的物质的量之比为 ,该反应中氧化产物是 。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消
毒剂的氧化能力相当于多少克Cl 的氧化能力。NaClO 的有效氯含量为 。
2 2
(计算结果保留两位小数)
(二)选考题:共 45 分.请考生从给出的 3 道物理题、3 道化学题、2 道生物
题中每科任选一题作答,并用 2B铅笔在答题卡上把所选题目题号后的方框涂
黑.注意所选题目的题号必须与所涂题目的题号一致,在答题卡选答区域指
定位置答题.如果多做,则每学科按所做的第一题计分.[化学--选修 2:化
第5页 | 共9页学与技术]
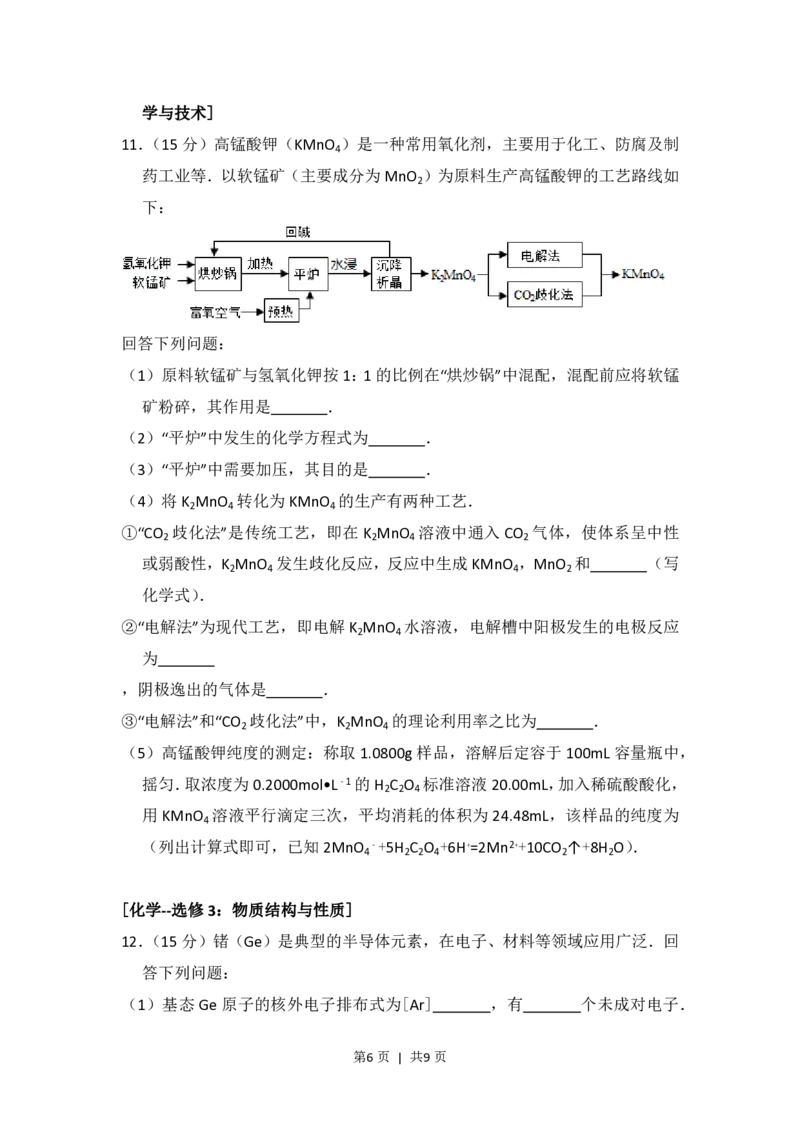
11.(15分)高锰酸钾(KMnO )是一种常用氧化剂,主要用于化工、防腐及制
4
药工业等.以软锰矿(主要成分为MnO )为原料生产高锰酸钾的工艺路线如
2
下:
回答下列问题:
(1)原料软锰矿与氢氧化钾按1:1的比例在“烘炒锅”中混配,混配前应将软锰
矿粉碎,其作用是 .
(2)“平炉”中发生的化学方程式为 .
(3)“平炉”中需要加压,其目的是 .
(4)将K MnO 转化为KMnO 的生产有两种工艺.
2 4 4
①“CO 歧化法”是传统工艺,即在 K MnO 溶液中通入 CO 气体,使体系呈中性
2 2 4 2
或弱酸性,K MnO 发生歧化反应,反应中生成KMnO ,MnO 和 (写
2 4 4 2
化学式).
②“电解法”为现代工艺,即电解 K MnO 水溶液,电解槽中阳极发生的电极反应
2 4
为
,阴极逸出的气体是 .
③“电解法”和“CO 歧化法”中,K MnO 的理论利用率之比为 .
2 2 4
(5)高锰酸钾纯度的测定:称取 1.0800g 样品,溶解后定容于 100mL 容量瓶中,
摇匀.取浓度为0.2000mol•L﹣1的H C O 标准溶液20.00mL,加入稀硫酸酸化,
2 2 4
用 KMnO 溶液平行滴定三次,平均消耗的体积为 24.48mL,该样品的纯度为
4
(列出计算式即可,已知2MnO ﹣+5H C O +6H+=2Mn2++10CO ↑+8H O).
4 2 2 4 2 2
[化学--选修 3:物质结构与性质]
12.(15分)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛.回
答下列问题:
(1)基态 Ge 原子的核外电子排布式为[Ar] ,有 个未成对电子.
第6页 | 共9页(2)Ge 与 C 是同族元素,C 原子之间可以形成双键、叁键,但 Ge 原子之间难
以形成双键或叁键.从原子结构角度分析,原因是 .
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因 .
GeCl GeBr GeI
4 4 4
熔点/℃ ﹣49.5 26 146
沸点/℃ 83.1 186 约400
(4)光催化还原 CO 制备 CH 反应中,带状纳米 Zn GeO 是该反应的良好催化
2 4 2 4
剂.Zn、Ge、O 电负性由大至小的顺序是 .
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为 微粒之间存
在的作用力是 .
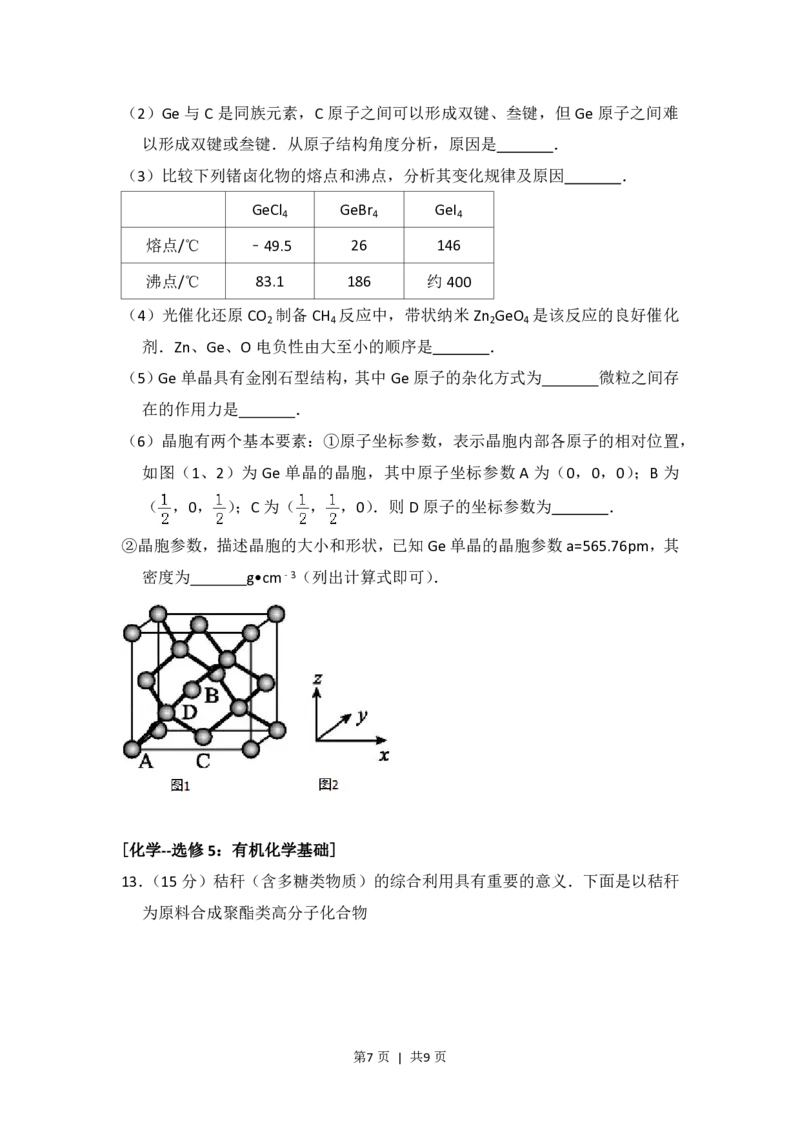
(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,
如图(1、2)为 Ge 单晶的晶胞,其中原子坐标参数 A 为(0,0,0);B 为
( ,0, );C为( , ,0).则D原子的坐标参数为 .
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76pm,其
密度为 g•cm﹣3(列出计算式即可).
[化学--选修 5:有机化学基础]
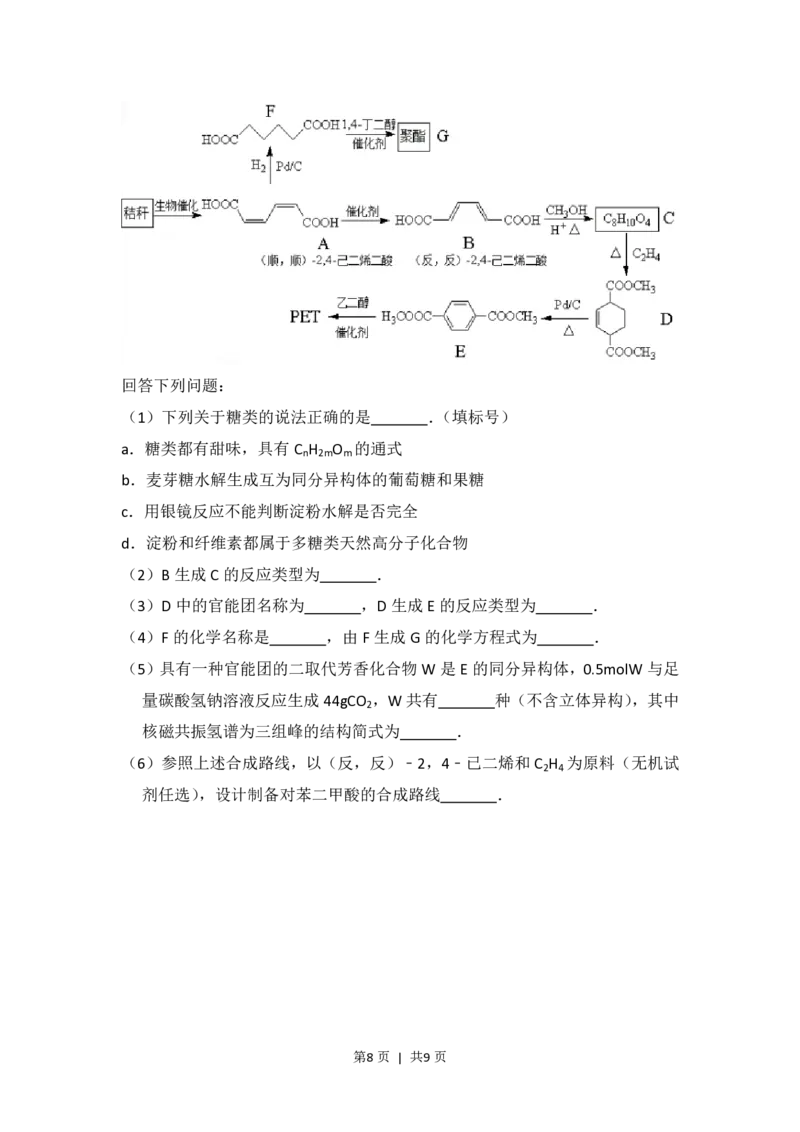
13.(15分)秸秆(含多糖类物质)的综合利用具有重要的意义.下面是以秸秆
为原料合成聚酯类高分子化合物
第7页 | 共9页回答下列问题:
(1)下列关于糖类的说法正确的是 .(填标号)
a.糖类都有甜味,具有C H O 的通式
n 2m m
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为 .
(3)D中的官能团名称为 ,D生成E 的反应类型为 .
(4)F的化学名称是 ,由F 生成G的化学方程式为 .
(5)具有一种官能团的二取代芳香化合物W是E的同分异构体,0.5molW与足
量碳酸氢钠溶液反应生成44gCO ,W共有 种(不含立体异构),其中
2
核磁共振氢谱为三组峰的结构简式为 .
(6)参照上述合成路线,以(反,反)﹣2,4﹣已二烯和C H 为原料(无机试
2 4
剂任选),设计制备对苯二甲酸的合成路线 .
第8页 | 共9页第9页 | 共9页