文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
第三单元 物质构成的奥秘
中考知识点归纳
知识点一 分子和原子
1.构成物质的微粒:_______等微粒。
(1)由分子构成的物质:例如___________________等物质;
(2)由原子构成的物质:___________________等物质;
(3)由离子构成的物质:___________________等物质。
【名师点睛】物质构成的描述:物质由××分子(或原子)构成。例如:铁由铁原子构成;氧气由氧分子构
成。
2.分子与原子的区别和联系
分子 原子
都是构成物质的一种粒子;_________、_________都非常小,彼此之间有间隔,
相同点 总是在不停地_________,同种分子(或原子)性质_________,不同种分子(或
原子)性质_________。
在_________中,分子可以再分 在化学反应中,原子不可以再分为,是
不同点
为_________ _________中最小的粒子。
分子由原子构成的,在_________中,分子可以再分为原子,原子可以_________
相互关系
为新分子
①物理变化只是构成物质的__________________发生了变化;
②化学变化是生成了__________________;
应用
③混合物是__________________构成的;
④纯净物是__________________构成的
【易错警示】①分子是保持物质化学性质的“最小粒子”,不是“唯一粒子”;
② “保持”的含义是指构成该物质的每一个分子与该物质的化学性质是一致的;
③分子只能保持物质的化学性质,而物质的物理性质需要大量的集合体一起来共同体现,单个分子无法体
现物质的物理性质。
④ “最小”不是绝对意义上的最小,而是“保持物质化学性质的最小”。
知识点二 微粒的性质和应用
1.用微粒的性质解释常见现象
分子的性质 解释 举例(以水为例)
分子的_______ 常用来解释质量或体积很小的物质中所含 1个水分子的质量约是3×10-26 kg,1
和_________都 分子的数目巨大或一个分子的质量或体积 滴水中大约有1.67×1021个水分子
很小 非常小等
分子在永不停 无规则 指速度大小、运动方向等物理量水分子都在_________,但分子运动
息地做无规则 不同且无规律 的速率并不一样
________ 运动 a.温度升高,分子运动的速率加 水蒸发成水蒸气,水分子运动速率
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
快; _________;
b.温度降低,分子运动的速率 水冷凝成冰,水分子运动________
减慢,但不可能停止运动
分子之间有 a.物质膨胀,分子间的间隔增大; 水蒸发成水蒸气,水分子间的间隔
_________ b.物质压缩或冷凝,分子间的间隔减 _________;
小,但不可能没有间隔 水冷凝成冰,水分子间的间隔
________
分子的种类决 a.分子相同的物质是同种物质,且化学性 水与冰的化学式都是HO,属于同种
2
定其化学性质 质_________; 物质,化学性质_________;
b.分子不同的物质是不同物质,且性质 水与双氧水化学式分别为HO和
2
_________ HO,不是同种物质,化学性质
2 2
【特别提醒】通过化学变化生成的物质是与反应物性质不同的新物质,分子不同,化学性质不同;通过物
理变化形成的物质是与反应物的大小、状态等不同的同种物质,分子相同、化学性质相同。
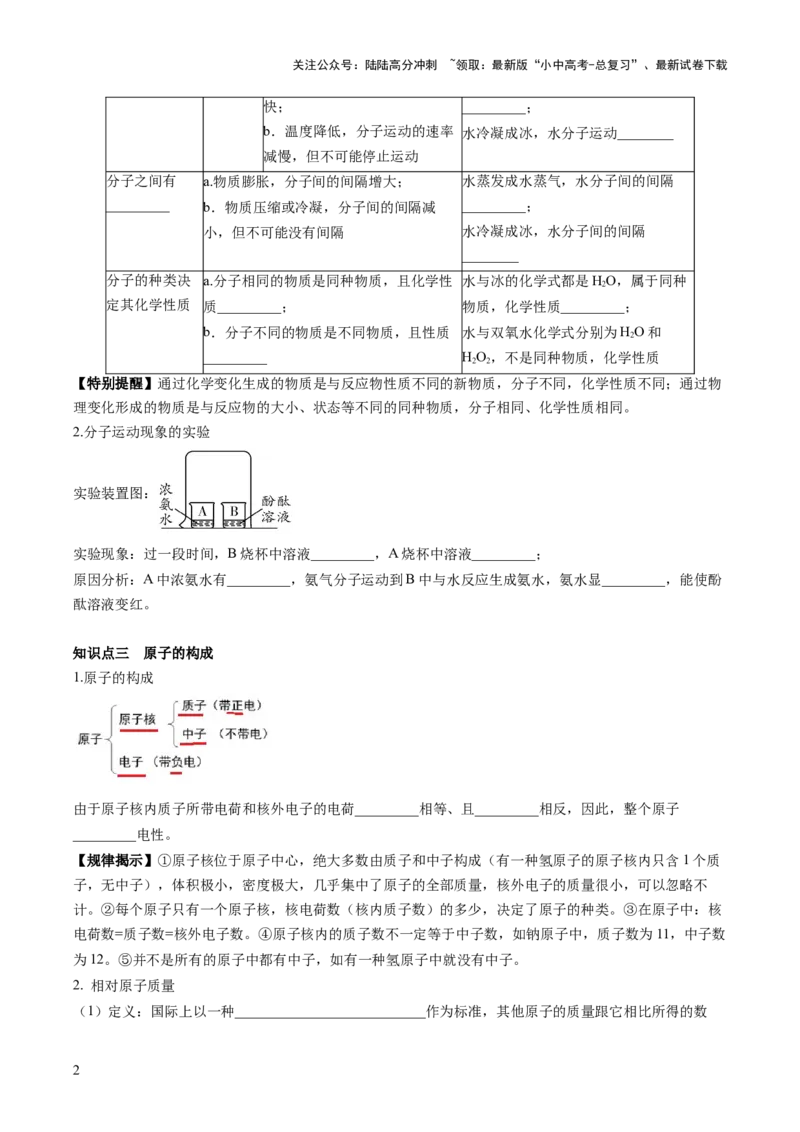
2.分子运动现象的实验
实验装置图:
实验现象:过一段时间,B烧杯中溶液_________,A烧杯中溶液_________;
原因分析:A中浓氨水有_________,氨气分子运动到B中与水反应生成氨水,氨水显_________,能使酚
酞溶液变红。
知识点三 原子的构成
1.原子的构成
由于原子核内质子所带电荷和核外电子的电荷_________相等、且_________相反,因此,整个原子
_________电性。
【规律揭示】①原子核位于原子中心,绝大多数由质子和中子构成(有一种氢原子的原子核内只含1个质
子,无中子),体积极小,密度极大,几乎集中了原子的全部质量,核外电子的质量很小,可以忽略不
计。②每个原子只有一个原子核,核电荷数(核内质子数)的多少,决定了原子的种类。③在原子中:核
电荷数=质子数=核外电子数。④原子核内的质子数不一定等于中子数,如钠原子中,质子数为11,中子数
为12。⑤并不是所有的原子中都有中子,如有一种氢原子中就没有中子。
2. 相对原子质量
(1)定义:国际上以一种___________________________作为标准,其他原子的质量跟它相比所得的数
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
值,就是这种原子的相对原子质量。
(2)计算公式:某原子的相对原子质量=该原子的实际质量/ (碳-12原子质量的1/12)
(3)相对原子质量≈_________+_________
3.核外电子的排布
(1)核外电子排布的初步知识
①通常用_________表明运动着的电子离核远近的不同。
②元素原子核外电子最少的有1层,最多的有7层,最外层电子最多不超过_________个(只有第1层的不
超过_________个)。
(2)原子结构示意图
①原子结构示意图的含义
说明:圆圈表示原子核,里面的数字表示_________;弧线表示_________,上面的数字表示每
一个电子层上的_________
②原子结构与元素性质的关系
元素种类 最外层电子数 元素的性质 结论
金属元素 _________个 原子易_________电子
_________决定了
非金属元素 _________个 原子易_________电子
元素的化学性质
稀有气体元素 _________个(氦2个) 不易得、失电子,稳定
知识点四 离子
1.概念:离子是带电的_________或_________,带正电的离子叫_________,带负电的离子叫_________。
2. 表示方法:在元素符号右上角标明_________和_________,数字在_________,符号在_________。若数
字为1时,可省略不写。
3.分类及形成:阳离子(由于原子_________电子而形成)带_________电。
阴离子(由于原子_________电子而形成)带_________电。
【特别提醒】原子变为离子时,质子数、元素种类没有改变;电子数、最外层电子数发生了改变。
4.离子符号表示的意义:表示一个某种离子;表示带n个单位某种电荷的离子。
5.离子中质子数与电子数的关系:
阳离子:质子数_________电子数 阴离子:质子数_________电子数
6.原子与离子的区别与联系
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【名师点拨】①判断是否为稳定结构:最外层电子数为8(一个电子层时为2)个电子的是相对稳定结构;
②判断化学性质是否相似:最外层电子数(只有一个电子层的除外)相同的粒子,化学性质相似。
知识点五 元素
1.元素
定义 具有相同_________(_________)的一类原子的总称
在地壳中排前四位的元素_____、_____、_____、_____,其中含量最多的金属元
分布
素为_____。
决定元素种类:__________(__________)
三个
决定元素化学性质:_______________
决定
决定原子的质量:__________
分类 金属元素、非金属元素和稀有气体元素
【规律揭示】物质、元素、微粒之间的关系:
2.元素和原子的区别与联系
项目 元 素 原 子
定义 具有相同核电荷数的一类原子的总称 化学变化中的最小粒子
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①微观概念,既表示种类又表示个数
①宏观概念,只表示种类不表示个数
②表示物质的________构成
②表示物质的________组成
区别 ③可以构成分子,也可以直接构成物
③可以组成单质或化合物
质。
④根据质子数和中子数分类
④根据质子数(核电荷数)分类
①元素是具有相同核电荷数(即质子数)的一类原子的总称
②原子核内的________决定元素的种类,即同种元素的原子核电荷数(即质子
联系
数)一定相同
③若原子的最外层电子数相同,则它们的化学性质________ (H、He除外)
【易错警示】①元素属于宏观概念,只讲种类,不讲个数。 ②同种元素的原子,核电核(荷)数一定相
同;而核电核(荷)数相同的粒子不一定属于同种元素,如Na+和NH +; ③同种元素的离子因所带的电荷
4
数不同,性质也不同,如Fe2+、Fe3+。 ④同种原子和其所形成的离子一定是同种元素,如Na和Na+。
3.元素符号
(1)元素符号书写原则:国际上统一采用元素的________名称的第一个大写字母来表示元素,若第一个
字母相同,就再加一个小写字母来区别。
(2)元素符号表示的意义:
宏观:表示一种________,如O表示氧元素。
微观:表示该元素的一个________,如O表示一个氧原子。
【名师点拨】①由原子直接构成的物质(金属、某些固态非金属和稀有气体),它们的元素符号还可以表示
该物质。如Fe表示:铁元素,一个铁原子,铁(这种单质)。②元素符号前面的数字不是1时,只表示原子
的个数。如:2H只表示2个氢原子。
知识点六 元素周期表
1.原子序数:按元素原子 递增的顺序给元素编号。原子序数与原子核电荷数(或质子数)在数值上
。
2.元素周期表的结构
(1)周期:具有相同的电子层数且又按原子序数递增的顺序从左到右排列的一系列元素。每一个横行叫
一个周期,共有7个周期。
(2)族:具有相同的最外层电子数且按电子层数递增顺序由上到下排列的一系列元素。
3.元素周期表与原子结构的关系
原子序数= =
周期序数=
主族序数=
4.由元素周期表一格获取的信息(以锌元素为例)
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【特别提醒】元素周期表是由许多元素单元格组成的,因此通过元素周期表我们可以查找元素所在的周
期、族、元素名称、元素符号、相对原子质量、原子序数等信息,但不能查到元素原子核内中子的数目。
热点题型剖析
题型一 分子、原子、离子、元素的概念判断
本题型主要考查方向有两个:(1)分子、原子、离子、元素的概念及它们之间的关系;(2)构成物质的
微粒的判断.主要以选择题、填空题的形式呈现。解题关键是理解和熟记分子、原子、离子的概念及它们之
间的关系,会灵活运用和辨析。
例1 物质是由微观粒子构成的,下列物质由原子直接构成的是
A.金刚石 B.水蒸气 C.氯化钠 D.碳酸钠
变式训练1 下列说法正确的是( )
A.热胀冷缩说明温度能改变分子大小
B.原子是不可再分的最小的粒子
C.分子、原子、离子都是构成物质的粒子
D.不同元素的本质区别是中子数不同
变式训练2 下列物质由分子构成的是( )
A.铜 B.汞 C.氢气 D.硫酸镁
题型二 用微粒的性质解释现象
用微粒的观点解释常见现象是贵阳中考每年必考内容之一,以选择题或填空题的形式呈现,考查用微观粒
子的性质解释生活或实验中常见的现象。解答此类题目的关键是根据分子的基本特征:分子质量和体积都很
小;分子之间有间隔;分子总是在不断地运动;同种物质的分子性质相同,不同物质的分子性质不同。结合事
实分析判断即可。
例2 我国在文昌航天发射场使用长征五号遥七运载火箭,成功将通信技术试验卫星十一号发射升空,卫星顺
利进入预定轨道,发射任务获得圆满成功。 火箭第三级的推进剂可以为液氢和液氧组合,下列说法正确的
是
A.氢气液化过程中,氢分子之间的间隔保持不变
B.分离液态空气得到液氧的过程中,氧分子静止不动
C.液氧变成气态氧时,放出热量
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.氢气与氧气反应的本质是氢、氧原子的重新组合
变式训练3 下列事实的微观解释中,不正确的是( )
A.墙内开花墙外可闻到花香——分子在不断地运动
B.蔗糖放入水中溶解——蔗糖分子分解了
C.氧气和液氧都能支持燃烧——物质的分子相同,其化学性质相同
D.水壶中的水烧开沸腾后,壶盖被顶起——水分子间的间隔增大
变式训练4 下列对宏观事实的微观解释不正确的是( )
A.水通电生成氢气和氧气——化学反应中分子发生了改变
B.压瘪的乒乓球在热水中能鼓起来——温度升高,分子变大
C.端午时节粽飘香——分子不断运动
D.一氧化碳和二氧化碳的化学性质不同——不同种分子的性质不同
题型三 原子的构成与微粒结构示意图的相关判断
对原子的结构知识的考查,主要以选择题、填空及简答题的形式呈现,对原子结构示意图、离子结构示意
图所表示的信息进行综合考查。掌握粒子结构示意图中各部分数字表示的含义是解题的基础。需牢记:在原
子中,原子序数=核电荷数=质子数=核外电子数。相对原子质量≈质子数十中子数。决定元素种类的是质
子数或核电荷数。如果核内质子数=核外电子数,则该粒子为原子;如果核内质子数>核外电子数,则该粒子
为阳离子;如果核内质子数<核外电子数,则该粒子为阴离子。微粒结构示意图中,元素的化学性质与原子
最外层电子数关系密切,质子数决定元素的种类。
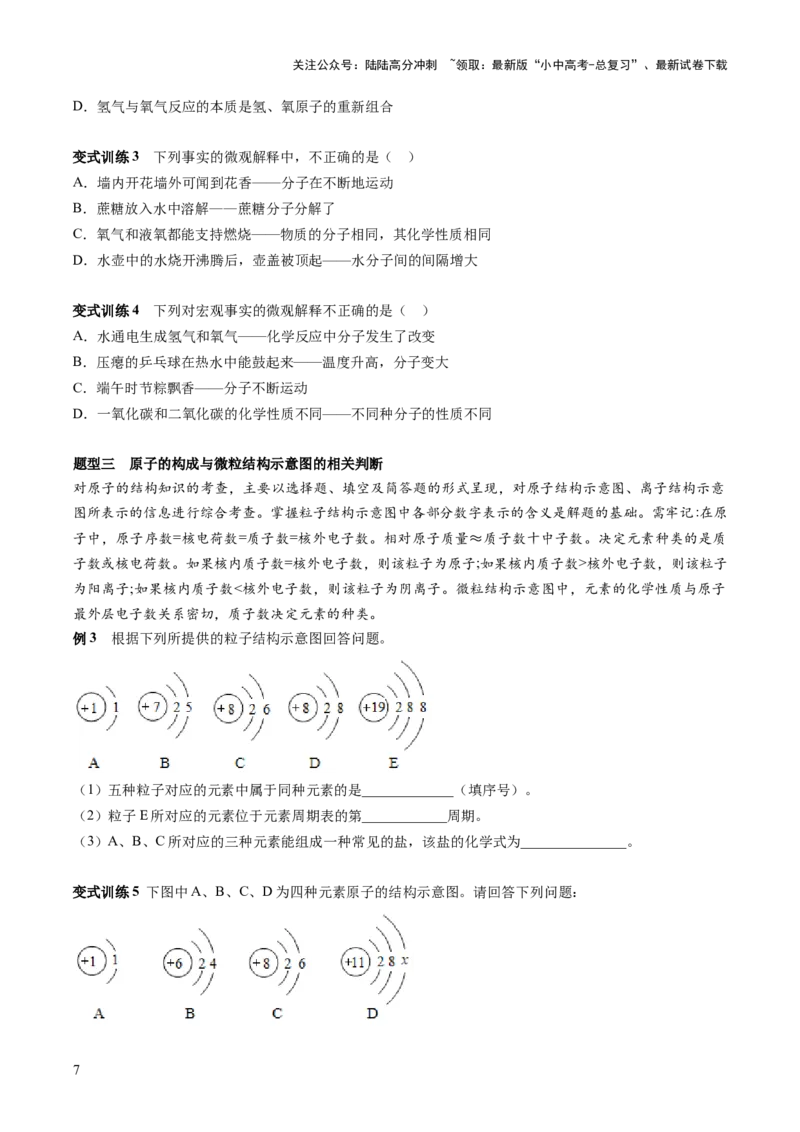
例3 根据下列所提供的粒子结构示意图回答问题。
(1)五种粒子对应的元素中属于同种元素的是_____________(填序号)。
(2)粒子E所对应的元素位于元素周期表的第____________周期。
(3)A、B、C所对应的三种元素能组成一种常见的盐,该盐的化学式为_______________。
变式训练5 下图中A、B、C、D为四种元素原子的结构示意图。请回答下列问题:
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)A、C两种原子相互结合形成的化合物的化学式为________________(任写一种)
(2)D中x= __________ 。
(3)写出B、C两种原子形成的化合物BC 的名称_________________。
2
变式训练6 中国科学院院士张青莲教授曾主持测定了铟、铱、锑等九种元素相对原子质量的新值,被国际
原子量委员会采用为国际新标准。其中锑元素原子结构示意图如下所示。
(1)锑属于___________(填“金属”或“非金属”)元素;
(2)锑原子的核电荷数是__________;
(3)锑原子最外层有______________个电子。
题型四 化学符号周围数字的意义
例4 请你用合适的化学用语或语言文字填空。
(1)两个氮原子______________;
(2)保持氦气化学性质的最小微粒_________________;
(3)氧化铝____________________;
(4)在符号“ ”中H正上方的“+1”表示___________,H右下角的“2”表示__________。
变式训练7 化学用语是国际通用语言,是学习化学的重要工具。
(1)请用化学用语填空:
①汞元素__________。
②2个甲烷分子_______。
③铵根离子______。
④标出水中氢元素的化合价_______。
(2)写出符号“3SO ”中数字的含义
2
①“3”表示_____________。
②“2”表示___________。
题型五 根据元素周期表中元素小格信息进行判断
元素及元素周期表在贵阳中考中的考查主要以填空题的形式呈现,通常会把元素的概念、元素的化学性
质、元素周期表的运用、微粒结构示意图和物质微粒构成等知识点结合在一起进行综合考查。解答此类题
目的关键是灵活运用元素周期表中元素的信息、原子结构示意图的意义进行分析解答。看到某一元素符
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
号, 就能联想到它所代表的元素、并能在元素周期表中找到对应元素,读懂周期表中所呈现的该元素的
相关信息。
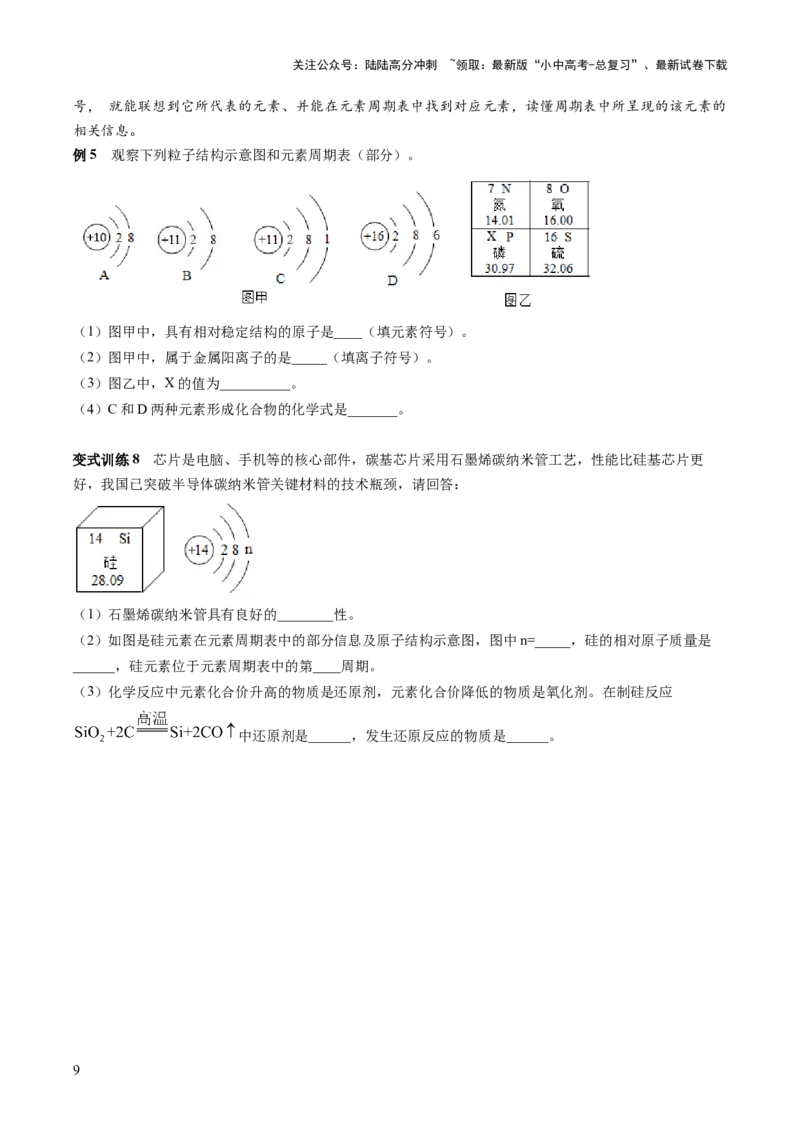
例5 观察下列粒子结构示意图和元素周期表(部分)。
(1)图甲中,具有相对稳定结构的原子是____(填元素符号)。
(2)图甲中,属于金属阳离子的是_____(填离子符号)。
(3)图乙中,X的值为__________。
(4)C和D两种元素形成化合物的化学式是_______。
变式训练8 芯片是电脑、手机等的核心部件,碳基芯片采用石墨烯碳纳米管工艺,性能比硅基芯片更
好,我国已突破半导体碳纳米管关键材料的技术瓶颈,请回答:
(1)石墨烯碳纳米管具有良好的________性。
(2)如图是硅元素在元素周期表中的部分信息及原子结构示意图,图中n=_____,硅的相对原子质量是
______,硅元素位于元素周期表中的第____周期。
(3)化学反应中元素化合价升高的物质是还原剂,元素化合价降低的物质是氧化剂。在制硅反应
中还原剂是______,发生还原反应的物质是______。
9