文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
精练 11 化学实验探究
知识点回顾(时间:5分钟)
知识点一、实验方案的评价
1.主要考查方式
主要是对所设计的实验方案、实验装置、操作步骤等,从某个角度否定、排除不合理或不可行
或可行不最优等方面进行评价,从而选择创新出更好的方法。
2.明确评价的内容
(1)科学性:反应能否发生,即方案在理论上是否科学、合理、严密。
(2)简约性:操作是否简便易行、优化,反应条件是否易达到。
(3)可行性:所有原料是否常见、易得、廉价。
(4)安全性:操作是否安全可靠。
(5)注意环保:反应过程是否节能与环保。
(6)要有创意:操作更简单,实验误差更小。
3.熟悉解题的一般步骤
明确目的→确定实验原理→评价实验方案的优劣(或可行性)→提出改进建议(依题意解答)。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
知识点二、解题方法技巧点拨
1.明确目的原理——明确实验的目的要求,弄清题给信息。
2.选择仪器药品——选择合理的化学仪器和药品。
3.设计装置步骤——设计出合理的实验装置和实验操作步骤。
4.记录现象和数据——全面、及时而准确地记录实验过程中的现象和数据。
5.分析得出结论——根据实验观察的现象和记录的数据,通过分析、计算、图表、推理等处
理,得出正确的结论。
【题型一】物质组成和性质类的探究
[例题1] (2023•双台子区校级二模)我国第四套人民币硬币中使用到镍(Ni)、铜、铁等
金属。某兴趣小组决定探究Ni、Fe、Cu的金属活动性顺序。
(1)查阅资料:镍与盐酸或稀硫酸反应,生成溶于水的正二价镍的化合物,并放出氢气。
①写出镍与盐酸反应的化学方程式 。
②据所查阅的资料内容, (填“能”或“不能”)直接比较出Ni、Fe的金属活动性强
弱。
(2)探究实验:(所用金属片均已用砂纸打磨。)
实验步骤 实验现象 实现结论
铁片表面有固体析出,铜片 三种金属活动性由强到弱的
表面 顺序为
(3)迁移应用:用镍片、硫酸亚铁溶液和 (填化学式)溶液
通过实验也能判断Fe、Ni、Cu的金属活动性顺序。
(4)将10gCu−Zn合金粉末放到盛有50g稀盐酸的烧杯中,恰好完全反应后,称量反应后烧杯中
物质的总质量59.8g。计算稀盐酸溶液的溶质的质量分数是 。
[例题2] (2023•洪泽区校级模拟)请回答下列问题。
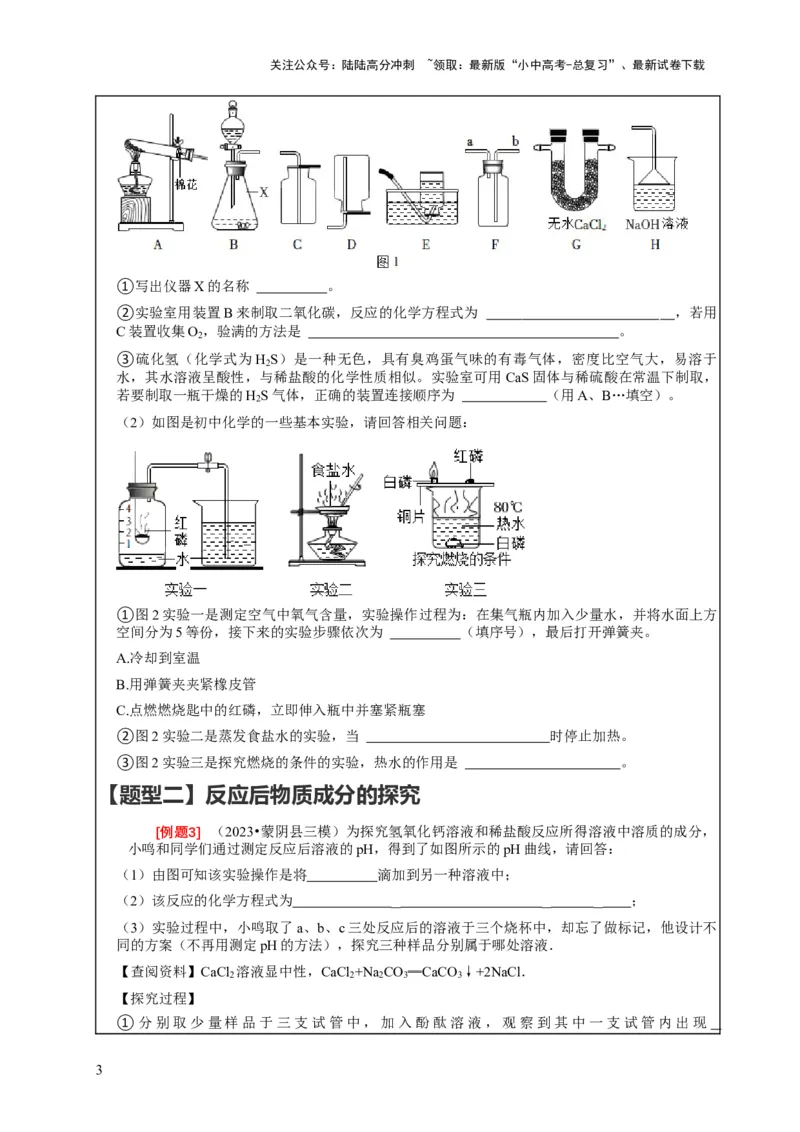
(1)根据图1实验装置回答有关问题(温馨提示:无水CaCl 具有吸水性)。
2
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①写出仪器X的名称 。
②实验室用装置B来制取二氧化碳,反应的化学方程式为 ,若用
C装置收集O ,验满的方法是 。
2
③硫化氢(化学式为H S)是一种无色,具有臭鸡蛋气味的有毒气体,密度比空气大,易溶于
2
水,其水溶液呈酸性,与稀盐酸的化学性质相似。实验室可用CaS固体与稀硫酸在常温下制取,
若要制取一瓶干燥的H S气体,正确的装置连接顺序为 (用A、B…填空)。
2
(2)如图是初中化学的一些基本实验,请回答相关问题:
①图2实验一是测定空气中氧气含量,实验操作过程为:在集气瓶内加入少量水,并将水面上方
空间分为5等份,接下来的实验步骤依次为 (填序号),最后打开弹簧夹。
A.冷却到室温
B.用弹簧夹夹紧橡皮管
C.点燃燃烧匙中的红磷,立即伸入瓶中并塞紧瓶塞
②图2实验二是蒸发食盐水的实验,当 时停止加热。
③图2实验三是探究燃烧的条件的实验,热水的作用是 。
【题型二】反应后物质成分的探究
[例题3] (2023•蒙阴县三模)为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,
小鸣和同学们通过测定反应后溶液的pH,得到了如图所示的pH曲线,请回答:
(1)由图可知该实验操作是将 滴加到另一种溶液中;
(2)该反应的化学方程式为 ;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了做标记,他设计不
同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl 溶液显中性,CaCl +Na CO ═CaCO ↓+2NaCl.
2 2 2 3 3
【探究过程】
①分别取少量样品于三支试管中,加入酚酞溶液,观察到其中一支试管内出现
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了以下方案:
实验步骤 实验现象 实验结论
另取余下样品少量于两支试管 该样品为b处溶液.
中,分别滴加足量的Na CO 溶
2 3
液.
该样品为c处溶液,并推知溶
液中的阳离子有
.
【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑
.
[例题4] (2023•明山区校级模拟)甲乙两个小组同学想探究氢氧化钙的化学性质,取 4支
试管分别用A~D编号后,如图进行实验。请回答下列问题:
(1)产生白色沉淀的现象的试管是 。(填试管编号)
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式
。若想证明其确实发生了反应,可向反应前的溶液中加入酚酞溶液,若观察到
现象,可说明其发生了反应。
(3)上述实验体现了碱具有相似的性质的试管编号是 (填字母)。
(4)实验结束后,甲、乙两组同学分别将本组4支试管中所有物质各倒入一个洁净烧杯中,充分
反应后静置,发现:
①甲组烧杯底部有白色沉淀,上层清液为红色,则下列说法错误的是 。
A.沉淀是碳酸钙
B.清液中一定含有氢氧化钠
C.清液中一定没有氯化氢
②乙组烧杯中只得到无色澄清溶液,则烧杯中废液的溶质(指示剂除外)一定有
(写出化学式),为了确定可能有的物质是否存在,还需要补充的实验方案是
。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【题型三】物质变质的探究
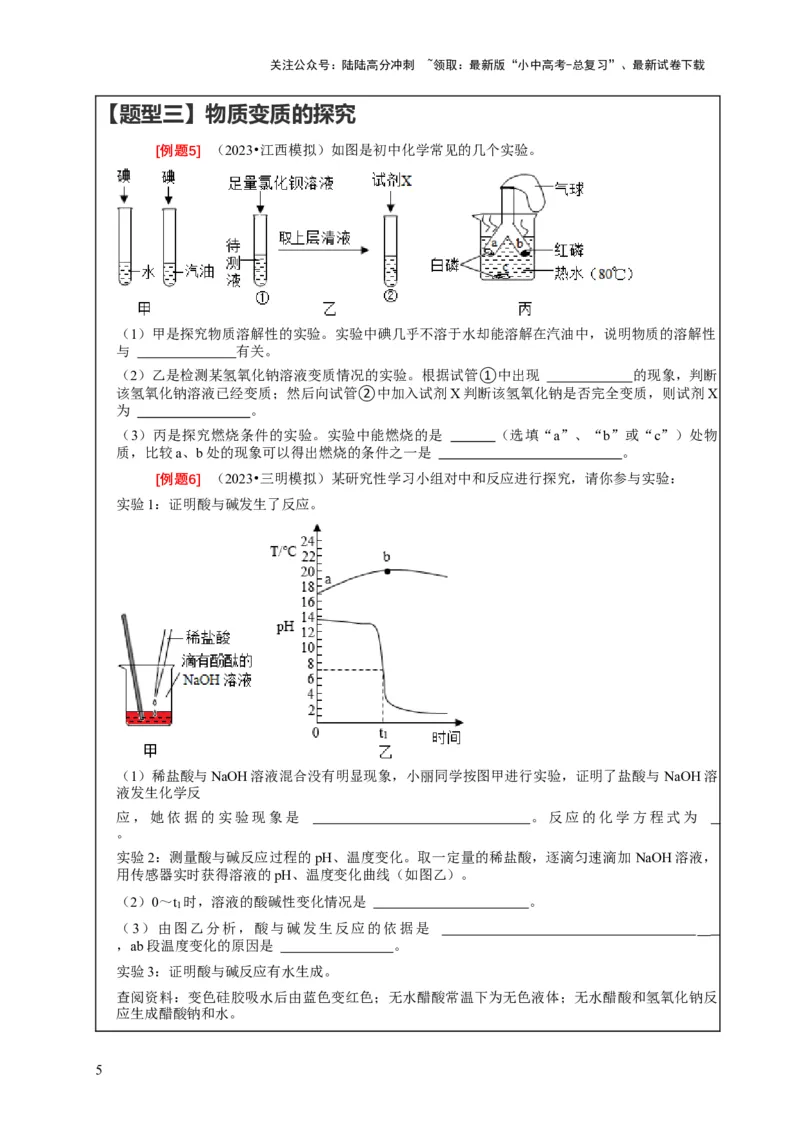
[例题5] (2023•江西模拟)如图是初中化学常见的几个实验。
(1)甲是探究物质溶解性的实验。实验中碘几乎不溶于水却能溶解在汽油中,说明物质的溶解性
与 有关。
(2)乙是检测某氢氧化钠溶液变质情况的实验。根据试管①中出现 的现象,判断
该氢氧化钠溶液已经变质;然后向试管②中加入试剂X判断该氢氧化钠是否完全变质,则试剂X
为 。
(3)丙是探究燃烧条件的实验。实验中能燃烧的是 (选填“a”、“b”或“c”)处物
质,比较a、b处的现象可以得出燃烧的条件之一是 。
[例题6] (2023•三明模拟)某研究性学习小组对中和反应进行探究,请你参与实验:
实验1:证明酸与碱发生了反应。
(1)稀盐酸与NaOH溶液混合没有明显现象,小丽同学按图甲进行实验,证明了盐酸与 NaOH溶
液发生化学反
应,她依据的实验现象是 。反应的化学方程式为
。
实验2:测量酸与碱反应过程的pH、温度变化。取一定量的稀盐酸,逐滴匀速滴加NaOH溶液,
用传感器实时获得溶液的pH、温度变化曲线(如图乙)。
(2)0~t 时,溶液的酸碱性变化情况是 。
1
(3)由图乙分析,酸与碱发生反应的依据是
,ab段温度变化的原因是 。
实验3:证明酸与碱反应有水生成。
查阅资料:变色硅胶吸水后由蓝色变红色;无水醋酸常温下为无色液体;无水醋酸和氢氧化钠反
应生成醋酸钠和水。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
小明同学在老师指导下进行图丙所示的三个实验。
(4)加入试剂后,要迅速塞紧橡胶塞的原因 。
(5)证明无水醋酸与氢氧化钠反应有水生成的现象是
。
(6)小芳认为实验丙不严密,还应补充的实验是 。
【题型四】影响因素类的探究
[例题7] (2023•云南模拟)金属材料广泛应用于各个领域,其应用推动了社会的发展。
(1)建筑领域:钢铁是基本的结构材料,称为“工业的骨骼”。铁制品易生锈,铁生锈的过程实
际上是铁
与空气中的 发生化学反应的过程。铁锈可用盐酸除去,其反应原理为
(用化学反应方程式表示)。
(2)航空航天领域:
①镍基高温合金应用于“神舟”号火箭发动机等处。镍基高温合金具有的性质有 (填字
母)。
A.熔点低 B.耐腐蚀 C.硬度大
②铝合金是航空航天领域常用的轻量化材料,强度高,耐腐蚀性好。铝具有很好的抗腐蚀性能的
原 因 是
。
③某铝合金中主要含铝、铜、镁三种金属,为验证三种金属的活动性顺序,某同学进行了如图实
验,充分反应后,观察到三支试管底部均有固体。等质量的铝粉和镁粉分别与等体积、溶质质量
分数相等的稀硫酸反应,反应的剧烈程度铝 (填“大于”“小于”或“等于”)镁。将
三支试管中的物质全部倒入洁净的烧杯中,充分反应后过滤,得到滤渣和滤液。下列说法错误的
是 (填字母)。
A.向滤渣中加入稀盐酸,一定有气泡冒出
B.滤液中最多含有四种溶质
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.充分混合后烧杯中溶液的质量一定不变
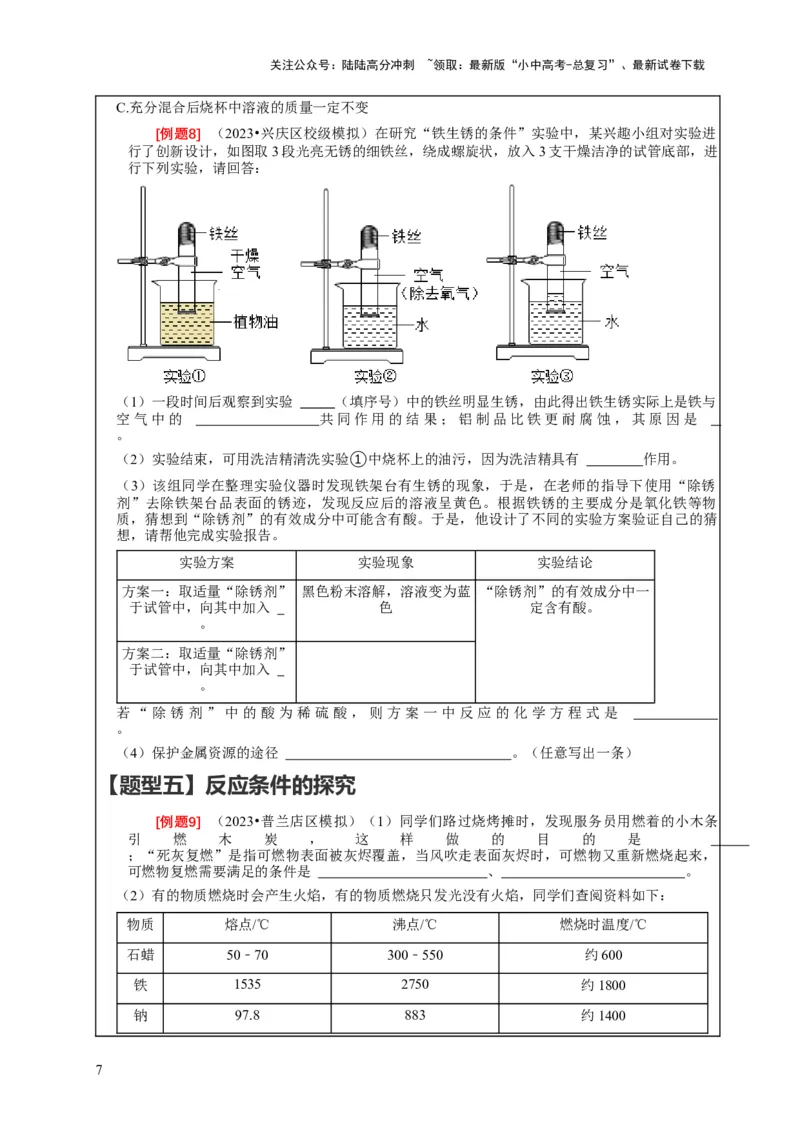
[例题8] (2023•兴庆区校级模拟)在研究“铁生锈的条件”实验中,某兴趣小组对实验进
行了创新设计,如图取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进
行下列实验,请回答:
(1)一段时间后观察到实验 (填序号)中的铁丝明显生锈,由此得出铁生锈实际上是铁与
空气中的 共同作用的结果;铝制品比铁更耐腐蚀,其原因是
。
(2)实验结束,可用洗洁精清洗实验①中烧杯上的油污,因为洗洁精具有 作用。
(3)该组同学在整理实验仪器时发现铁架台有生锈的现象,于是,在老师的指导下使用“除锈
剂”去除铁架台品表面的锈迹,发现反应后的溶液呈黄色。根据铁锈的主要成分是氧化铁等物
质,猜想到“除锈剂”的有效成分中可能含有酸。于是,他设计了不同的实验方案验证自己的猜
想,请帮他完成实验报告。
实验方案 实验现象 实验结论
方案一:取适量“除锈剂” 黑色粉末溶解,溶液变为蓝 “除锈剂”的有效成分中一
于试管中,向其中加入 色 定含有酸。
。
方案二:取适量“除锈剂”
于试管中,向其中加入
。
若“除锈剂”中的酸为稀硫酸, 则方案一中反应的化学方程式是
。
(4)保护金属资源的途径 。(任意写出一条)
【题型五】反应条件的探究
[例题9] (2023•普兰店区模拟)(1)同学们路过烧烤摊时,发现服务员用燃着的小木条
引 燃 木 炭 , 这 样 做 的 目 的 是
;“死灰复燃”是指可燃物表面被灰烬覆盖,当风吹走表面灰烬时,可燃物又重新燃烧起来,
可燃物复燃需要满足的条件是 、 。
(2)有的物质燃烧时会产生火焰,有的物质燃烧只发光没有火焰,同学们查阅资料如下:
物质 熔点/℃ 沸点/℃ 燃烧时温度/℃
石蜡 50﹣70 300﹣550 约600
铁 1535 2750 约1800
钠 97.8 883 约1400
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
由表可知,物质燃烧能否产生火焰与 (填“熔点”或“沸点”)和 有
关;可推测钠燃烧时 (填“有”或“没有”)火焰产生。
[例题10](2023•安次区一模)某化学兴趣小组利用如图装置进行燃烧条件的探究,装置的
气密性良好,实验前弹簧夹K 、K 都处于关闭状态。
1 2
①打开弹簧夹K ,关闭K 注入足量过氧化氢溶液,A中发生反应的化学方程式为
1 2
, 一 段 时 间 后 , 打 开 K 观 察 到 B 中 气 球 变 大 , 其 原 因 是
2
。
② 若 要 得 出 燃 烧 的 条 件 之 一 是 与 氧 气 接 触 , 需 要 进 行 的 操 作 是
。
难度:★★★ 建议时间:25分钟
1. (2023•寻乌县模拟)蔗糖是一种常见的生活用品,化学兴趣小组的同学们为探究蔗
糖的组成元素进行了一系列实验。
【进行实验】小明同学将蔗糖在氧气中燃烧,为检验其燃烧产物,首先用一个内壁涂有澄清石
灰水的烧杯罩在蔗糖燃烧火焰的上方。
【收集证据】
(1)一段时间后观察到的现象是 ,由此说明蔗糖燃烧生成了二氧化碳。
(2)若欲证明蔗糖燃烧有水生成,小明还需要进行的操作以及对应的现象是
。
【得出结论】蔗糖是由碳、氢、氧元素组成。
【 讨 论 交 流 】 有 同 学 认 为 上 述 结 论 不 一 定 正 确 , 理 由 是 ( 3 )
。
【反思改进】在老师的帮助下,同学们用如下定量分析的方法最终确定了蔗糖的组成元素。
【查阅资料】:①无水硫酸铜吸收水分变蓝;②碱石灰(含有氢氧化钠和氧化钙)可以吸收二
氧化碳和水;③装置B、C、D中试剂均足量。
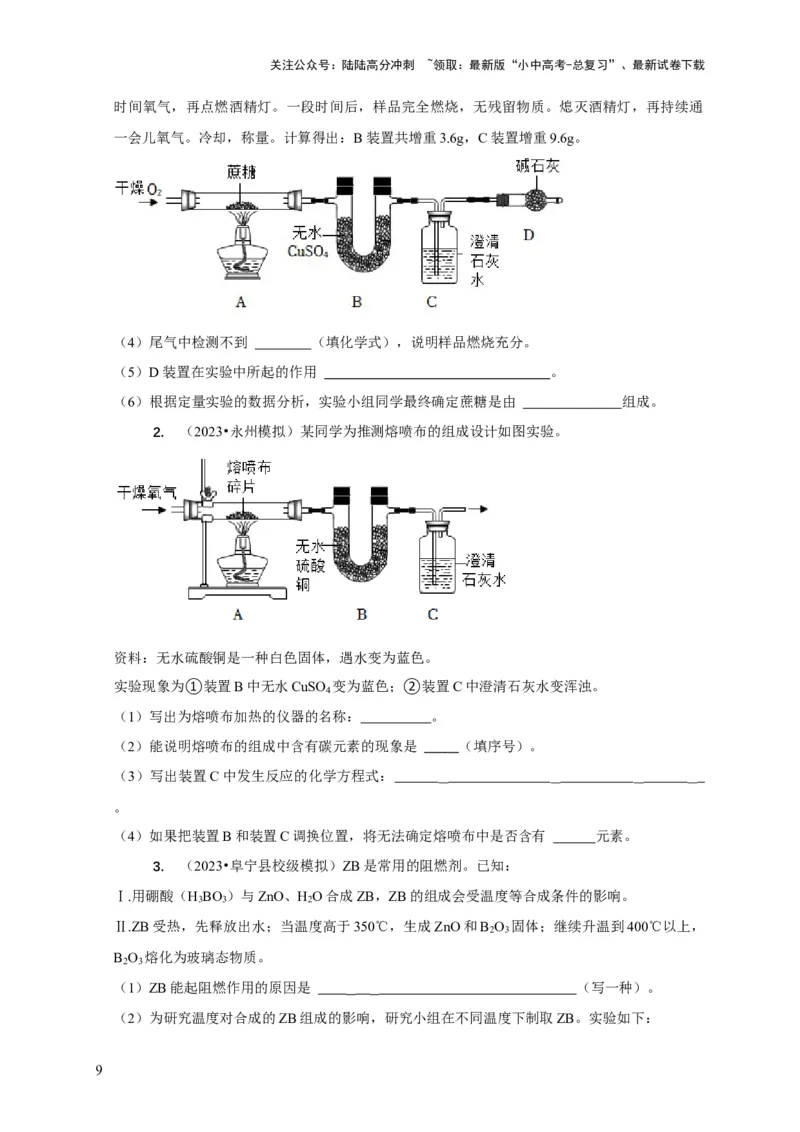
【定量实验】连接如图所示装置,检查装置的气密性,将6.2g蔗糖装入玻璃管中,先通入一段
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
时间氧气,再点燃酒精灯。一段时间后,样品完全燃烧,无残留物质。熄灭酒精灯,再持续通
一会儿氧气。冷却,称量。计算得出:B装置共增重3.6g,C装置增重9.6g。
(4)尾气中检测不到 (填化学式),说明样品燃烧充分。
(5)D装置在实验中所起的作用 。
(6)根据定量实验的数据分析,实验小组同学最终确定蔗糖是由 组成。
2. (2023•永州模拟)某同学为推测熔喷布的组成设计如图实验。
资料:无水硫酸铜是一种白色固体,遇水变为蓝色。
实验现象为①装置B中无水CuSO 变为蓝色;②装置C中澄清石灰水变浑浊。
4
(1)写出为熔喷布加热的仪器的名称: 。
(2)能说明熔喷布的组成中含有碳元素的现象是 (填序号)。
(3)写出装置C中发生反应的化学方程式:
。
(4)如果把装置B和装置C调换位置,将无法确定熔喷布中是否含有 元素。
3. (2023•阜宁县校级模拟)ZB是常用的阻燃剂。已知:
Ⅰ.用硼酸(H BO )与ZnO、H O合成ZB,ZB的组成会受温度等合成条件的影响。
3 3 2
Ⅱ.ZB受热,先释放出水;当温度高于350℃,生成ZnO和B O 固体;继续升温到400℃以上,
2 3
B O 熔化为玻璃态物质。
2 3
(1)ZB能起阻燃作用的原因是 (写一种)。
(2)为研究温度对合成的ZB组成的影响,研究小组在不同温度下制取ZB。实验如下:
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
m(H BO )/g m(ZnO)/g V(H O)/mL t/℃
3 3 2
实验1 28 10 100 94
实验2 x 10 100 98
实验3 28 y 100 102
x、y分别为 和 。
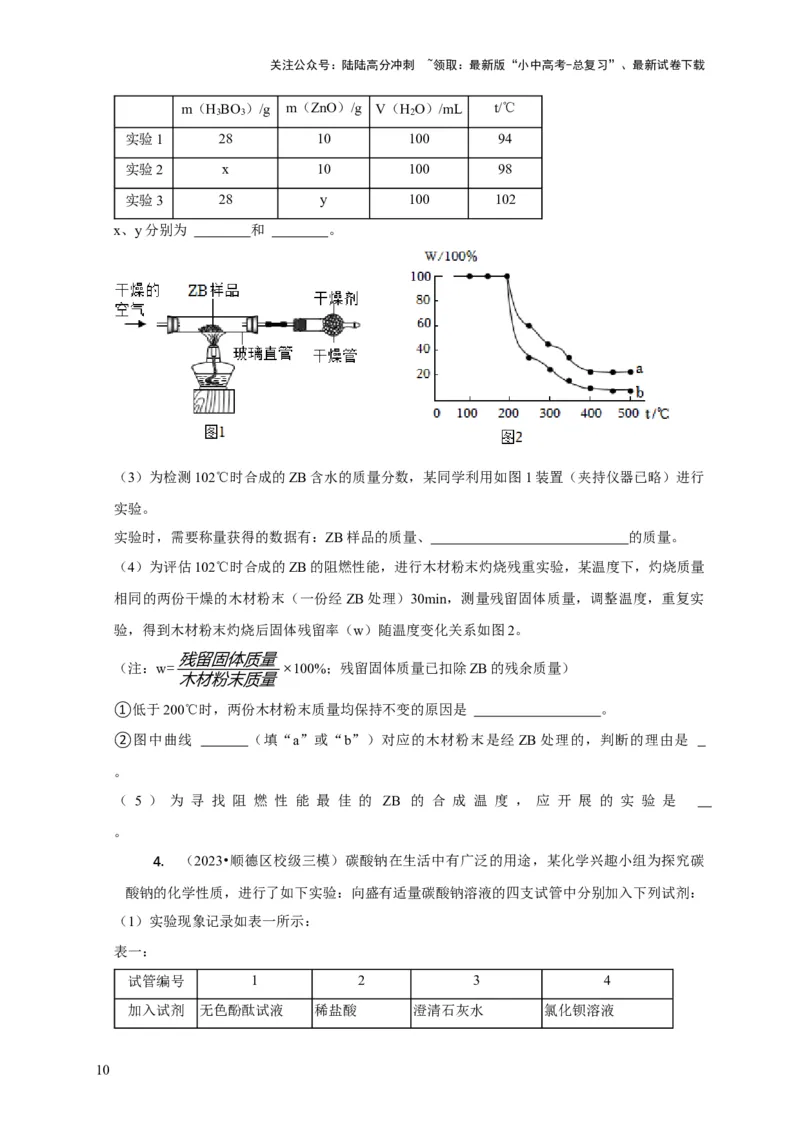
(3)为检测102℃时合成的ZB含水的质量分数,某同学利用如图1装置(夹持仪器已略)进行
实验。
实验时,需要称量获得的数据有:ZB样品的质量、 的质量。
(4)为评估102℃时合成的ZB的阻燃性能,进行木材粉末灼烧残重实验,某温度下,灼烧质量
相同的两份干燥的木材粉末(一份经ZB处理)30min,测量残留固体质量,调整温度,重复实
验,得到木材粉末灼烧后固体残留率(w)随温度变化关系如图2。
残留固体质量
(注:w= ×100%;残留固体质量已扣除ZB的残余质量)
木材粉末质量
①低于200℃时,两份木材粉末质量均保持不变的原因是 。
②图中曲线 (填“a”或“b”)对应的木材粉末是经ZB处理的,判断的理由是
。
( 5 ) 为 寻 找 阻 燃 性 能 最 佳 的 ZB 的 合 成 温 度 , 应 开 展 的 实 验 是
。
4. (2023•顺德区校级三模)碳酸钠在生活中有广泛的用途,某化学兴趣小组为探究碳
酸钠的化学性质,进行了如下实验:向盛有适量碳酸钠溶液的四支试管中分别加入下列试剂:
(1)实验现象记录如表一所示:
表一:
试管编号 1 2 3 4
加入试剂 无色酚酞试液 稀盐酸 澄清石灰水 氯化钡溶液
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
实验现象 有气泡产生 有白色沉淀产生 有白色沉淀产生
试管1的实验现象是 ,试管3中发生反应的化学方程式为:
。
化学兴趣小组的同学对反应后溶液中溶质的成分进一步探究:小组同学将试管3中的物质过滤,
得到滤液A。
【提出问题】
滤液A中溶质的成分是什么?
(2)【猜想假设】
猜想一:NaOH
猜想二:NaOH和Na CO
2 3
猜想三:NaOH和
猜想四:NaOH、Na CO 和Ca(OH)
2 3 2
(3)【活动探究】
小 组 讨 论 : 有 同 学 认 为 猜 想 四 不 成 立 , 原 因 是
。
(4)【进行实验】
如表二所示:
表二:
实验操作 实验现象 实验结论
方案甲:取少量滤液A于试管中,加入过 有 生成;写出该现象相应的化 猜想二成
量的稀盐酸 学方程式 立
方案乙:取少量滤液A于试管中,加入适 有 产生
量的Ba(NO ) 溶液
3 2
(5)【反思与评价】
a.碳酸钠溶液呈碱性,可以和盐酸、氢氧化钙、氯化钡等物质发生反应。
b.要验证反应后物质的成分,既要考虑生成物,还应考虑 。
5. (2023•岳阳一模)金属材料的使用作为一个时代的标志,见证了人类文明发展的过
程。人类经历了新石器时代、青铜器时代、铁器时代,后来陆续使用了锌、铝、钠、镁等金属。
金属材料在生产生活中有不同的用途,发挥着重大的作用。某化学兴趣小组对金属的活动性强
弱产生了浓厚的兴趣,在老师的指导下,他们开启了铝、铁、铜三种金属的活动性强弱的探究
之旅。请你和他们一起完善下表的探究方案并回答有关问题。
(1)任务一:小明同学设计了用铜丝、铁丝、铝丝和稀硫酸,只用一支试管,取一次硫酸的探
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
究方案。
实验步骤 实验现象 实验结论
步骤①:在试管中取少量稀 三种金属活动性由强到弱的
硫酸,插入铁丝,充分反应 顺序是:
步骤②:在①所得的溶液 无现象
中,插入铜丝,充分反应
步骤③:在②所得的溶液 溶液由浅绿色变为无色
中插入铝丝,充分反应
(2)步骤①将铁丝插入前,应用砂纸将表面打磨干净,目的是 。
(3)任务二:小强同学认为要得到Al>Fe>H>Cu的结论,不必做补充实验,只需将小明同学
的方案中插入金属的顺序调整即可,你认为调整后插入金属丝的顺序是 。
6. (2023•方城县模拟)某实验小组的同学将一定量的稀盐酸加入到盛有 NaOH溶液的
小烧杯中,进行“酸碱中和反应”的探究活动。
(1)反应后溶液中溶质是什么呢?有同学猜想如下:①NaCl,②NaCl、NaOH,③NaCl、
HCl,④NaCl、HCl和NaOH。以上猜想你认为不合理的是 (填编号)。
(2)为了验证上述合理的猜想,某同学取烧杯中的溶液少量于试管中,滴加几滴 CuSO 溶液,
4
无明显变化,说明猜想 不正确(填编号)。另有同学利用烧杯中的溶液,并选用pH试纸、
铜片、AgNO 溶液、Na CO 溶液,进行如下三个方案的探究。
3 2 3
实验方案 ①测溶液pH ②滴加Na CO 溶液 ③滴加AgNO 溶液
2 3 3
实验操作
实验现象 试纸变色,对比比色 试管中有气泡 产生白色沉淀
卡,pH<7
实验结论 溶液中有HCl 溶液中有HCl 溶液中有HCl
经过上述实验可确定猜想 是正确的(填编号);实验方案中错误的是 (填实验方案
标号);操作有错误的实验是 。(填实验操作标号)
(3)若在烧杯中加入20g40%的氢氧化钠溶液,再逐滴加入稀盐酸,当滴入的稀盐酸质量为 25g
时恰好完全反应。
①所用氢氧化钠溶液中溶质的物质的量为 mol。
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
②加入盐酸的质量分数。(根据化学方程式计算,精确到0.1%)
7. (2023•黄州区校级模拟)某化学小组的同学在完成了木炭和氧化铜实验后,对试管
内的已部分变红固体粉末产生了兴趣,大家对固体成分进行了猜想:
猜想I.铜和炭粉;猜想Ⅱ.铜和氧化铜;猜想Ⅲ.铜、氧化铜、炭粉。
探究一:固体粉末的成分。
取少量固体粉末于试管,加入足量稀硫酸充分反应。
(1)固体粉末部分溶解,溶液变蓝,证明固体中存在 ,反应的化学方程式为
。
(2)试管内混合物过滤,将滤渣洗涤、干燥后充分灼烧,产生使澄清石灰水变浑浊气体,说明
猜想 成立。
探究二:固体粉末中铜元素的质量。
如图装置,检查装置气密性,在A中装入锌粒和稀硫酸,取固体粉末40.0g放入如图所示的硬质
玻璃管中,打开分液漏斗滴入稀硫酸,在球形干燥管出口处检验氢气纯净后,点燃酒精灯,待
充分反应后,熄灭酒精灯,冷却至室温,其它装置中试剂均足量,请回答下列问题:
(1)装置中B的作用是 。
( 2 ) 实 验 前 先 打 开 分 液 漏 斗 滴 入 稀 硫 酸 , 再 点 燃 酒 精 灯 的 目 的 是
。
(3)某同学用以上气体和装置进行实验,实验过程中无污染性气体生成,且实验结束,硬质玻
璃管中剩余固体仅为金属,并测得以下几组数据:
反应前 完全反应后
D装置的质量为180.2g D装置的质量为183.8g
E装置的质量为160.0g E装置的质量为164.4g
则固体粉末中铜元素的质量是 。
8. (2023•历城区校级模拟)如图所示为实验室常见气体制备、净化、干燥、收集和性
质实验的部分仪器(组装实验装置时,可重复选择仪器)。某学校两个化学实验探究小组的同
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
学欲用它们完成各自的探究实验。
(1)第一组同学以石灰石和稀盐酸为原料制取的二氧化碳气体中,常混有少量水蒸气和 HCl气
体。为制得一瓶不含水蒸气和HCl气体的二氧化碳,按照需要选择实验装置、连接仪器。(提
示:少量HCl气体可用饱和碳酸氢钠溶液吸收)
①请帮助一组同学选择并按正确顺序连接仪器装置:A→ → →F(从左到右填写仪
器序号)。
②若将二氧化碳通入澄清的石灰水中,石灰水的pH将 (填“变大”“变小”“不变”
之一)。
(2)第二组同学以过氧化氢溶液为原料(MnO 为催化剂)制备氧气,并对某种塑料的组成元
2
素 进 行 分 析 探 究 ( 资 料 显 示 该 塑 料 只 含 C 、 H 、 O 三 种 元 素 ) , 所 选 仪 器 按
“A→B →E→B →D”的顺序连接,(B 、B 均为浓硫酸洗气瓶),实验前检验装置气密性,
1 2 1 2
使该塑料试样碎屑在纯氧气中充分燃烧,观察现象,收集有关实验数据(假设发生的化学反应
都充分反应),试回答下列问题:
①仪器A中所发生反应的化学方程式为 。
②仪器E的玻璃管中放入的塑料试样碎屑质量为m克,塑料试样充分燃烧后,测得仪器B 质量
2
增加3.6克,则m克塑料试样中含氢元素的质量为 克。
③若装置中没有连接仪器 B ,这样测算出的该塑料试样中氢元素的质量与实际值比较将
1
(填“偏小”“偏大”“基本一致”之一)。
9. (2023•武进区校级模拟)用下列实验探究Al与CuCl 溶液的反应。
2
实验一:将打磨后的铝片插入CuCl 溶液,铝片表面出现红色固体且产生气泡,最终溶液呈无色。
2
(1)生成红色固体的化学方程式为 。
(2)收集气体,点燃,产生淡蓝色火焰。该气体为 。
实验二:将实验一所得无色溶液倒入水中,出现白色固体。过滤、洗涤、低温烘干。对所得白
色固体作如下探究。
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【资料】①AlCl 能与H O作用生成Al(OH) 。Al(OH) 白色固体,不溶于水,受热易分
3 2 3 3
解生成Al O 和H O。
2 3 2
②Al与CuCl 溶液反应会生成CuCl。CuCl白色固体,不溶于水,能溶于含氯离子浓度较大的
2
溶液,受热不分解。
【猜测】白色固体可能是:
a.Al(OH) ;
3
b.CuCl;
c.Al(OH) 和CuCl。
3
【实验】取适量白色固体,利用如图装置充分加热,U形管中 ,则猜测b成立。
【反思】无色溶液倒入水中后出现白色固体的原因是 。
实验三:CuCl在空气中被氧化成碱式氯化铜[Cu (OH) Cl ]蓝绿色固体,其受热会分解生成
x y z
CuO、H O和HCl。取一定量蓝绿色固体,充分加热,将生成的气体依次用足量的吸水剂氯化钙
2
和烧碱溶液充分吸收。
(1)实验测得氯化钙增重0.36g,烧碱溶液增重0.73g。则碱式氯化铜的化学式为
。
(2)若烧碱溶液吸收了空气中的CO ,则测得的Cu (OH) Cl 中x的值 (填“偏
2 x y z
大”“偏小”或“不变”)。
10. (2023•肇东市校级模拟)实验室有一包久置的生铁粉末(成分为铁、碳和氧化铁)。
为测定各组分的质量分数,将20g生铁粉末均分成两份,进行如下实验。(装置气密性良好)
实验一:测定碳的质量分数
(1)将10g样品于足量的稀硫酸反应,待反应结束,过滤,得滤渣0.36g,则碳的质量分数为
。
实验二:测定氧化铁的质量分数
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
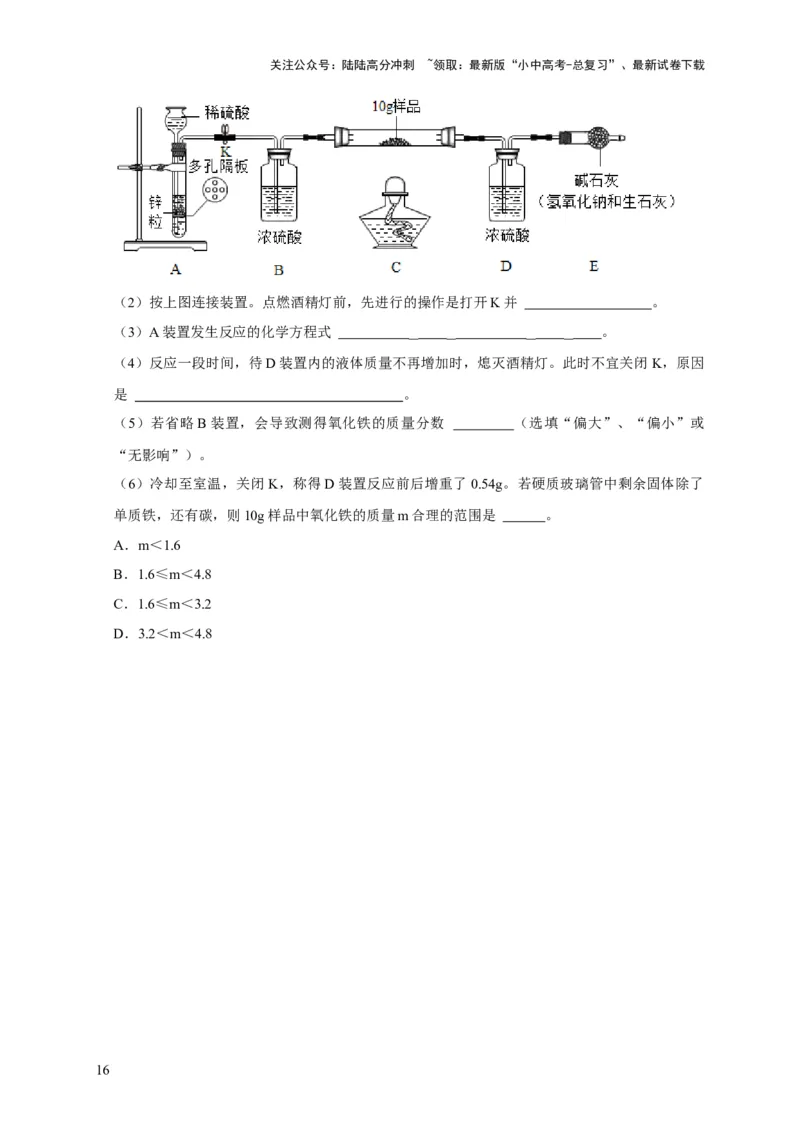
(2)按上图连接装置。点燃酒精灯前,先进行的操作是打开K并 。
(3)A装置发生反应的化学方程式 。
(4)反应一段时间,待D装置内的液体质量不再增加时,熄灭酒精灯。此时不宜关闭 K,原因
是 。
(5)若省略B装置,会导致测得氧化铁的质量分数 (选填“偏大”、“偏小”或
“无影响”)。
(6)冷却至室温,关闭K,称得D装置反应前后增重了0.54g。若硬质玻璃管中剩余固体除了
单质铁,还有碳,则10g样品中氧化铁的质量m合理的范围是 。
A.m<1.6
B.1.6≤m<4.8
C.1.6≤m<3.2
D.3.2<m<4.8
16