文档内容
(二)化工工艺流程
1.锂辉石矿(主要含有LiAlSi O ,还含有少量Fe2+、Mg2+)是主要锂源,现利用锂辉石矿制
2 6
取LiBr,用于高级电池的电解质、医用镇静剂等。工艺流程如下:
(1)锂辉石中主要成分LiAlSi O 改写为氧化物形式为__________________。
2 6
(2)工业选择石灰石进行“中和”而不选择纯碱主要考虑的是__________;在“除镁除铁(调
节pH≈11)”步骤中得到的滤渣中含铁成分是__________;写出“除铝”所发生反应的离子
方 程 式 :
__________________________________________________________________________。
(3)碳酸锂在水中的溶解度较小,其-lg K 与温度t关系如下表:
sp
t/℃ 0 10 20 30 40 50 60 70 80
-lg K 1.44 1.53 1.63 1.71 1.80 1.90 2.00 2.21 2.43
sp
由此可知碳酸锂在水中的溶解热效应ΔH____(填“>”或“<”)0;加入纯碱试剂进行“沉
锂”后,依次进行保温静置、________(填序号)。
①洗涤 ②趁热过滤 ③离心分离
(4)在“合成”中,碳酸锂粉末分次少量加入冰水中溶解,再加入尿素搅拌得到“料液”,
料液中徐徐加入溴,控制pH=5.0,反应生成LiBr和两种无色无味气体,写出化学方程式:
______________________________________________________________________________。
2.五氧化二钒(V O)广泛用于冶金、化工等行业,用作合金添加剂、生产硫酸或石油精炼
2 5
用的催化剂等。从废钒催化剂(含有KSO 、VO 、VO 、SiO 、Fe O 、NiO等)中回收钒,
2 4 2 5 2 4 2 2 3
既能避免对环境的污染,又能节约宝贵的资源,回收工艺流程如下:
已知:①“酸浸”时VO 和VO 与稀硫酸反应分别生成VO和VO2+。
2 5 2 4②溶液中VO与VO可相互转化:VO+HOVO+2H+,且NH VO 为沉淀。
2 4 3
(1)“酸浸”前,需对废钒催化剂进行粉碎预处理,其目的是_________________________。
(2)“还原转化”中加入FeSO 的目的是将VO转化为VO2+,写出反应的离子方程式:
4
____________________________________________________________________________。
(3)加入HO 的目的是将过量的Fe2+转化为Fe3+。“氧化1”后,溶液中含有的金属阳离子
2 2
主要有Fe3+、Ni2+、VO2+,调节pH使离子沉淀,若溶液中c(Ni2+)=0.2 mol·L-1,则调节溶
液的pH最小值为________可使Fe3+沉淀完全(离子浓度≤1.0×10-5 mol·L-1时沉淀完全),
此时__________(填“有”或“无”)Ni(OH) 沉淀生成{假设溶液体积不变,lg 6≈0.8,
2
K [Fe(OH) ]=2.16×10-39,K [Ni(OH) ]=2×10-15}。
sp 3 sp 2
(4)“氧化2”过程中发生反应的离子方程式为____________________________________。
(5)“沉钒”时,通入氨气的作用是_______________________________________________。
(6)若该废钒催化剂中VO 的含量为10%(原料中所有的钒已换算成VO)。取100 g待处理
2 5 2 5
样品,按照上述流程进行实验。当加入 150 mL 0.1 mol·L-1 KClO 溶液时,溶液中的钒元素
3
恰好完全反应,则该工艺中钒的回收率是______%。(假设与KClO 反应后的操作步骤中钒
3
元素无损失)
3.高铁酸钾(K FeO)是一种暗紫色固体,在低温碱性条件下比较稳定,微溶于KOH浓溶液。
2 4
工业上湿法制备KFeO 的流程如图:
2 4
(1)强碱性介质中,NaClO 可氧化 Fe(NO ) 生成高铁酸钠,写出该反应的离子方程式:
3 3
_______________________________________________________________________________。
(2)请比较工业上湿法制备 KFeO 的条件下 NaFeO 和 KFeO 的溶解度大小:
2 4 2 4 2 4
NaFeO_____
2 4
(填“>” “<”或 “=”)K FeO
2 4
(3)将NaFeO 粗品[含有Fe(OH) 、NaCl等杂质]转化为KFeO 的实验方案为
2 4 3 2 4
a.在不断搅拌下,将NaFeO 粗品溶于冷的3 mol·L-1 KOH溶液中,快速过滤除去Fe(OH)
2 4 3
等难溶的物质。
b.将滤液置于__________中,向滤液中加入________________,过滤。
c.对产品进行洗涤时使用乙醇,其目的是____________________________________(答两
点)。
(4)高铁酸盐具有强氧化性,溶液pH越小氧化性越强,可用于除去废水中的氨、重金属等。
KFeO 的浓度与pH关系如图1所示;用KFeO 除去某氨氮(NH -N)废水,氨氮去除率与pH
2 4 2 4 3
关系如图2所示;用KFeO 处理Zn2+浓度为0.12 mg·L-1的含锌废水{K [Zn(OH) ]=1.2×
2 4 sp 2
10-17},锌残留量与pH关系如图3所示[已知: KFeO 与HO反应生成Fe(OH) 的过程中,
2 4 2 3
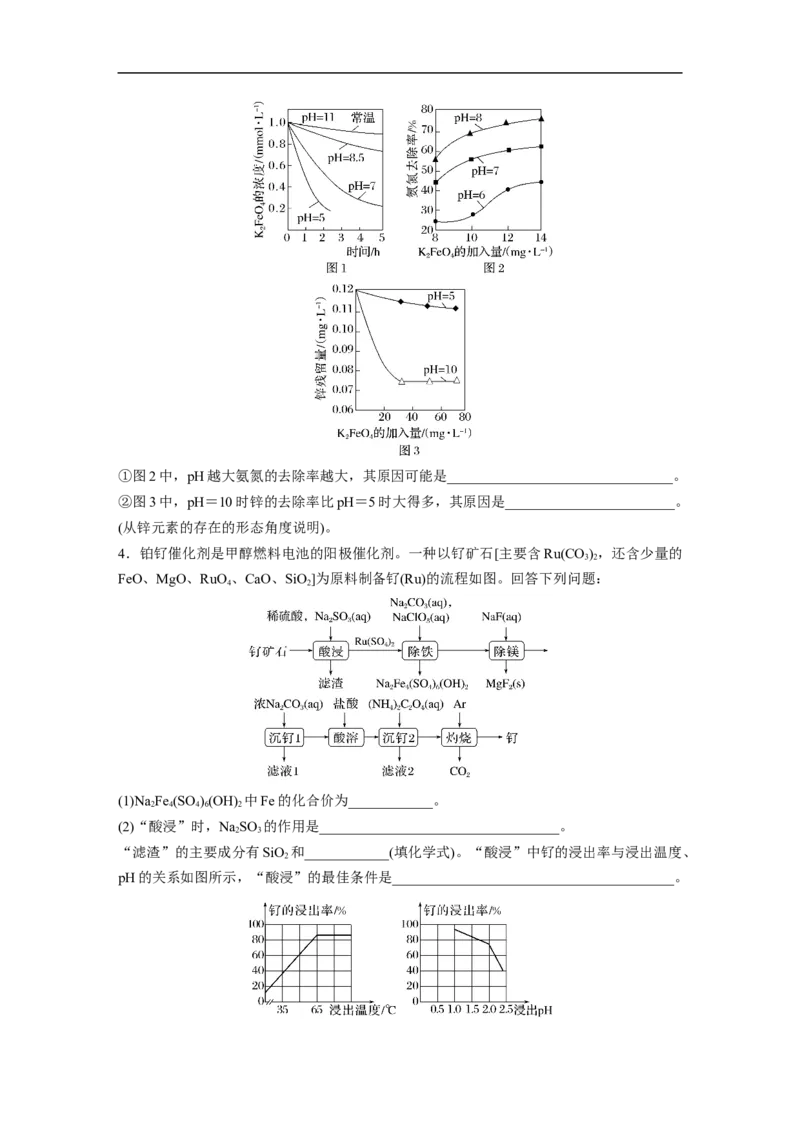
可以捕集某些难溶金属的氢氧化物形成共沉淀]。①图2中,pH越大氨氮的去除率越大,其原因可能是________________________________。
②图3中,pH=10时锌的去除率比pH=5时大得多,其原因是________________________。
(从锌元素的存在的形态角度说明)。
4.铂钌催化剂是甲醇燃料电池的阳极催化剂。一种以钌矿石[主要含Ru(CO) ,还含少量的
3 2
FeO、MgO、RuO、CaO、SiO]为原料制备钌(Ru)的流程如图。回答下列问题:
4 2
(1)Na Fe (SO )(OH) 中Fe的化合价为____________。
2 4 4 6 2
(2)“酸浸”时,NaSO 的作用是__________________________________。
2 3
“滤渣”的主要成分有SiO 和____________(填化学式)。“酸浸”中钌的浸出率与浸出温度、
2
pH的关系如图所示,“酸浸”的最佳条件是________________________________________。(3)“除铁”的离子方程式为_______________________________________(提示:1 mol
NaClO 参与反应,转移6 mol电子)。
3
(4)从“滤液2”中可提取一种化肥,其电子式为________________________________。
(5)“灼烧”时Ar的作用是___________________________________________________。
(6)某工厂用10 t钌矿石[含8.84 t Ru(CO ) 、165 kg RuO ],最终制得3 636 kg Ru,则Ru的
3 2 4
产率为____________(结果保留三位有效数字)。
5.镁菱锌矿(主要成分为ZnCO 、MgCO 等,含有少量FeCO 、CaCO 等杂质)可用于生产
3 3 3 3
媒染剂、防腐剂ZnSO·7H O以及耐火材料MgO。制备工艺流程如下:
4 2
已知:65 ℃时 K [Mg(OH) ]= 1.8×10-11;K [Zn(OH) ]=2.0×10-17,K =10-13;lg
sp 2 sp 2 w
2≈0.3。
回答下列有关问题:
(1)浓盐酸浸取矿石时,保持较大液固体积比(如3∶1),目的是___________________,还可
采用________________________________(写出一种)等方式达到此目的。
(2)“氧化除铁”在 90 ℃,控制溶液 pH 在 4.0~5.0,得到针铁矿渣的离子方程式为
__________
________________________________________________________________________。
(3)“沉锌”前,滤液(65 ℃)中含有0.50 mol·L-1 Zn2+和1.8 mol·L-1Mg2+,保持该温度,则
应加入氨水调节pH在________________范围(c≤1.0×10-5 mol·L-1,沉淀完全)。利用平衡
移动原理说明“沉锌”时加入氨水的作用是______________________________________。
(4)“酸解”后获得ZnSO·7H O的操作依次经过蒸发浓缩、________、过滤、洗涤、干燥。
4 2
制得的ZnSO·7H O在烘干时需减压烘干的原因是___________________________________。
4 2
(5)“滤液”中加入HC O 饱和溶液产生MgC O 沉淀。写出“灼烧”步骤的化学方程式:
2 2 4 2 4
______________________________________________________________________________。