文档内容
2022〜 2023年度河南省高三年级入学摸底考试(一)
化 学
考生注意:
1. 本试卷分第 卷(选择题)和第 卷(非选择题)两部分,共1〇〇分。考试时间9〇分钟。
I n
2. 请将各题答案填写在答题卡上。
3. 本试卷主要考试内容:高考全部内容。
4. 可能用到的相对原子质量 1 7 12 14 0 16 1 27 32 40
:H Li C N A S Ca
56 59 64
Fe Ni Cu
第 I 卷 (选 择 题 共 42分)
_ 、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1. 生活、生产等与化学联系紧密,下列叙述正确的是
. 陶瓷砚台的主要化学成分与水晶相同
A
. “薪柴之灰”的主要成分有碳酸钾
B
. 烟火中的红色来源于钠盐的灼烧
C
. 温室气体是形成酸雨的主要物质 .
D
2. 乙硫醇( 3 2 )是一种易挥发且具有强烈刺激性气味的液体,可用作天然气及石油气
C H C H S H
给定冬件
的警告剂。以乙醇为原料可制得乙硫醇,反应原理为 3 +
C H C H 2O H H 2S
3 2 + 2()。下列说法正确的是
C H C H S H H
. 中子数为10的氧原子可表示为 〇
A ws
. 乙醇和乙硫醇互为同系物
B
. 羟基的电子式为
C : H
. 硫化氢的结构式为 —
D H S - H
3.下列有关物质的性质与用途具有对应关系的是
选项 物质的性质 用途
A N2无色无味 可用作食品防腐剂
B Al2()3具有两性 可用作耐火材料
C 石墨具有优良的导电性 可用作电极材料
D Fe2(S()4)3具有氧化性 可用作净水剂
4.设 为阿伏加德罗常数的值。下列说法错误的是
JVA
. 5. 6 完全反应可能失去0. 2 A 个电子
A g F e JV
. 1 1 • —1的 1 13溶液中含有 严的数目等于 ,
B L mol L A C A N
常温常压下,11. 2 氢气所含的氢原子数小于
C L N a
. 16 肼( 2 中含有的极性键的总数为2
D g N H J iVA
【高 三 化 学 第 1 页(共 8 页)】 23-03C ■5.仅用下表提供的玻璃仪器(非玻璃仪器任选)不能实现相应实验目的的是
选项 实验目的 玻璃仪器
A 用 Na2sa 固体配制 240 mL 0• 1 mol • L—―1 Na2SC),溶液 容量瓶、烧杯、玻璃棒
B 用已知浓度的盐酸测定未知浓度的NaOH溶液 酸(碱)式滴定管、锥形瓶
C 除去NaCl(l)中少g 的Mn()2 烧杯、玻璃棒、普通漏斗
D 分离乙酸乙酯和水的混合物 分液漏斗、烧杯
6. 合成某种具有解毒消肿、袪风活络的功能药物的中间体( )的结构简式如
M
图所示。下列有关 的说法错误的是
M
. 1 最多与4: 2发生加成反应
A mol M mol H
. 该分子中含有3种官能团
B
. 该分子中所有碳原子一定共面
C
. 环上的一氯代物有3种
D
7. 乙醇在醋酸菌作用下被空气氧化是制造醋酸的有效方法,然而这一传统过程远远不能满足工
业的需求。目前工业上多采用甲醇和一氧化碳反应制备醋酸: + —-
C H 3O H C O
C H
3
C O O H
。以
[Rh
(
C O
) 212 ]-为催化剂、碘甲烷为助催化剂合成醋酸(
Monsanto
法)的反应
过程如图所示,其中①②③④均为阴离子。下列有关说法中错误的是
CH,
CO
H20 /| \ CHj
T 1 CCO
,CH,1 I
②
CO
CH,OH /|\
HI ① r ' rCO
CH3COOH CO ch3 ③
CO
⑤
h2o
\
i /I ' cr o④ 」
.甲醇生成碘甲烷的反应为取代反应 .⑤可表示为
A B C H 3COI
.在反应过程中 的成键数目发生改变 .该反应过程中不存在非极性键的形成
C R h D
8. 、、、 为原子序数依次增大的短周期丰族元素,、 的最外层电子数分别是其电子层数
X Y Z W X Y
的2倍、3倍,的原子半径在短周期主族元素中是最大的, 的原子序数是 与 的原子序
Z W X Z
数之和。下列说法正确的是
. 仅由 、、 形成的化合物的水溶液可能呈中性
A Y Z W
. 氢化物的沸点:
B Y > X
. 简单离子半径:
C Z > W
. 、 与 均只能形成两种化合物
D X W Y
9. 我国自主开发应用的铁一铬液流储能电池的放电工作原理如图所示。图中贮液器可储存电
解质溶液,提高电池的容量;电极 、均为惰性电极。下列说法正确的是
a b
【高三化学第2 页(共8页)】 • 23—03C .贮 ^<
液 液
器 溶液 器
gV ^
— ^
t 子 t
交 擁
. 放电时,极为电池的负极
A a
. 放电时,极区的 +可通过质子交换膜向 极区迁移
B a H b
. 充电时,极连接外电源的正极
C a
放由
. 电池反应式为 3++ @ 3++ 2+
D Cr FeH Fe Cr
无电
10.某兴趣小组利用铁矿石(主要成分为
FeO
、
Fe
2
Q
)制取硫酸铁铵晶体[
N H
4
Fe
(
S
〇4)2 •
x H
2〇]
的流程如图 ; 4 ( 04)2 • : 20 受热分解时,固体剩余质量与温度关系如图2(已知
l N H Fe S tH :a
点时仅失去了一半的结晶水)。
100
77.6
55.2
, 41.5
蘇 可 网 调 州 > 过 量 % — v 輝 e(s〇4)2_ .
T/X
图1 图2
下列叙述正确的是
A. 溶液A 中所含的阳离子只有Fe2+、Fe3+
B. a点时,剩余固体可表示为NH4Fe(S04)2 • 6H20
. 加人 202的目的是将 2+全部还原为 3+
C H Fe Fe
D. d — e的过程中无气体放出,e点剩余的固体为FeS04
11.下列依据有关实验操作和实验现象(或数据)能得出相应的实验结论且实验结论符合客观事
实的是
选项 实验操作 实验现象(或数据) 实验结论
将盐酸与CaC03反应得到的气体直接通
A 产生白色胶状的沉淀 酸性:H2C03> H2Si(〕3
人硅酸钠溶液中
向 10 mL 0. 1 mol . L——1 Na2S溶液中滴加
先产生白色沉淀,后产生
B 2 mL 0. 1 mol • L—1 ZnS04 溶液,再加人 Ksp(ZnS)>Ksp(CuS)
黑色沉淀
几滴同浓度的CuS04溶液
常温下,将等体积的饱和nh4hco3溶液 常温下,NaHCft的溶解度
C 试管中有白色沉淀产生
与饱和NaCl溶液混合 小于NH4 HC03和 NaCl的
同 温 下 ,不 同 浓 度 的
常温下,用 pH计分别测定0. 2 mol • L-1
D pH均等于7 CH3COONH4 溶液中水的
和 2 mol. LHCHsCOONA 溶液的 pH
电离程度相同
【高三化学第3 页(共8页)】 • 23—03C •12.某化合物W 是由四种位于前四周期且均不同周期的常见元素组成的,探究其组成的实验过
程如图(略去部分产物)。
已知:气体 燃烧时,火焰呈淡蓝色且有水生成;白色沉淀 可溶于强酸或强碱的溶液;沉
F E
淀 为红色固体氧化物 和白色沉淀 的混合物。
A M E
下列说法中错误的是
•白色沉淀 为 1(() )3
A E A H
. 化合物 中一定含有氢元素
B W
. 生成无色气体 的反应中 ( ) : 〇3)=3 : 2
C B n M tK H N
D. 化合物W 中质量分数最大的元素是铜元素
13.CuS04 • 5H 20 和少量水蒸气置于容积可变的真空密闭容器中,受热逐渐失去H 2◦ 的三个
反应式为 I.CuS04 .5H 20(s) # CuS04 • 3H 2〇(s)十 2H 20(g); n _ CuS04 .3H 20(s)
^=^CuS04 . H 20(s)+2H 20(g);in.CuS04 . H 20(s)^=^CuS04(s) + H 20(g);25 °C和
50 °C下,上述三个反应中水蒸气的平衡压强数据如表所示;不同温度下上述三个反应中水
蒸气的平衡压强随温度的变化情况如图所示。
/»(H2〇)/kPa
反应 “p(H20)
25 °C 50 °C a ,
I 1.04 6. 05
n 0. 75 4. 12
0 j
IK 0. 11 0. 60
下列说法错误的是
. 表示反应 的是曲线
A I a
. 图中表示 04 • 3 20 稳定存在的区域是区域
B CuS H B
. 上述三个反应处于 点时,正逆反应速率的关系均为吨>1;逆
C M
D. 25 °C下,反应I 达到平衡后,再通人H 2 0( g),重新平衡后,〆H 2 O )增大
14.室温下,将0. 1 mol • L-1的盐酸不断滴加到10. 00 m L 相 同 浓 度 的 ‘
溶液中,溶 液 中 水 电 离 出 的 —) 的 负 对 数 11
B O H O H
[一 ^( )]与加人盐酸的体积[ (盐酸)/ ]的关系如图所7
lgc O P T V m L
示。下列说法错误的是
. 室温下, 的电离平衡常数约为 5 〇
A B O H K T
. 点溶液中存在: ( +) + ( — 2 ) + ( —)十 )
B b c H c Cl X K B O H c O H K I T
. 、、三点溶液中,点溶液的离子总浓度最大
C a b c c
. 溶液中 ( + ) = 1—)对应的点为 点
D c B K C a
【高三化学第4 页(共8页)】 • 23-03C •第 n 卷 (非 选 择 题 共 58分)
二、非选择题:包括必考题和选考题两部分。第 15〜 17题为必考题,每个试题考生都必须作答。
第18〜 19题为选考题,考生根据要求作答。
(一)必考题:此题共3小题,共43分。
15. (14分)三氯化氮(
N C
13,其中
C
1为+ 1价)是一种用于柠檬等水果的熏蒸处理的黄色油状液
体。某兴趣小组利用氯化铵溶液和氯气制备
N C
13,实验装置如图所示。
查阅资料:I . N C 13的熔点为一40 °C,沸点为70 °C。
. 13在 95 以上易爆炸,有刺激性气味,不溶于冷水,可与热水反应(即水解)。
U N C °C
实验步骤:先检查装置气密性,按上述装置装人试剂,然后打开仪器 的活塞和& ,使 2
X Cl
与 4 1溶液在低温下反应,观察现象,一段时间后,关闭仪器 的活塞和& ,停止向装置
N H C X
中通人 2,并控制装置 中水浴温度,使 13蒸气逸出。
B Cl B N C
(1) 装置 中的仪器 为恒压漏斗,与使用分液漏斗滴加浓盐酸相比,在该实验中使用恒压
A X
漏斗的优点为________。
(2)① 装置接口连接顺序为 —_ —_ _ —_ _ —_ - _ _ (填小写字
a
母,装置可重复使用)。
② 装置 的作用是___________________________________________________________。
C
③ 在实验过程中,装置 中可观察到的现象是___________________________________。
E
(3) 反应一段时间后,用干燥、洁净的玻璃棒蘸取装置E 中U 形管内的液体滴到干燥的红色
石蕊试纸上,试纸不褪色;若取该液体滴人热水中,片刻后取该水溶液再滴到干燥的红色
石蕊试纸上,则试纸先变蓝后褪色。结合化学方程式解释该现象:__________________。
(4) 在pH = 4 的条件下,电解NH4C1溶液也可以制得NC13,然后利用空气流将产物带出电
解槽。电解池中产生NC13 的电极连接电源的________ (填“正极”或“负极”),电解
~ :^0溶 液 制 得 13总反应的离子方程式为_______ 。
N C
(5) 13可与 102溶液反应制取 102气体,同时产生一种无污染的气体,则参与反应
N C N aC C
的《( 13) : 7 ()2)=________。
N C KNaCl
16. (14分)镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯[主要成分为
( )2、〇(〇 )2及少量铁、铝的氧化物等]生产硫酸镍、碳酸钴的工艺流程如图。
Ni O H C H
H2S〇4,H202 NaHC〇3
丄④ 丄⑤
NiS04-7H20
【高 三 化 学 第 5 页(共 8页)] • 23—03C •已知:
部分金属阳离子以氢氧化物的形式沉淀时溶液的 见表:
p H
金属阳离子 Fe2+ Fe3+ Al3+ Ni2+ Co2-
开始沉淀时pH 6. 3 1.5 3.4 6.2 7. 15
完全沉淀时pH
9.0 3.2 4. 7 9.2 9. 15
(金属阳离子浓度<1〇_5 mol • L一4
回答下列问题:
(1) 步骤①用稀硫酸浸取金属电极芯前,需先粉碎金属电极芯,粉碎的目的是________。
(2) 步骤②调 的范围为______。
p H
(3)将 “母液1”的
p H
调至3〜 4,再加人
N aC
10,
N aC
10的作用是____________。
(4) 步骤④中若用盐酸代替 2 04和 202的混合液也能达到目的,从环保角度分析不采
H S H
用盐酸的原因:_________ 。
(5) 步骤⑤中“母液3”与 〇3溶液反应的离子方程式为___________ 。
N a H C
⑹已知:常温下,Ksp (CaC03) = 2. 8 X 10-9、Ksp (CoC()3 ) = 1.6X10-13,若向浓度相同的
CaCl2和C〇Cl2的混合溶液中加入足量Na2C03固体,则所得溶液中c(Ca2+) : c(Co2T)
(7) 04可形成多种结晶水合物,采用热重分析法测定某 04 • « 20 样品所含的结晶
NiS NiS H
水数。将样品在900 °下进行锻烧,失重率随时间变化如图, 点时失去全部结晶水
C B ,n
的值为________; 点固体的化学式为________。
D
(8)碱性镍氢电池的工作原理为 ( ) ^ ( )2 + ( 为储氢合金),该电
NiO O H + M H Ni O H M M
允电
池充电时阳极的电极反应式为_______。
17. (15分)我国力争在2030年前实现碳达峰、2060年前实现碳中和的目标,因此
C
02的捕集、
利用与封存成为科学家研究的重要课题。
I
.以
C
02、
H
2为原料合成
C H
3
O H
涉及的主要反应如下:
① C 02( g ) + 3 H 2( g )^= C H 30 H ( g ) + H 20( g ) A H ! = —49. 5 kj • mol —1
② C02(g) + H2(g)F^C0(g) + H20(g) A H 2 = +40. 9 kj • mol —1
③ CO(g)+2H2(g )^ C H 3OH(g) AH3
(1) 3= _______ • -1。
A H kj mol
(2) 反应①和②的 ( 代表化学平衡常数)随+ ( 温度的倒数)的变化如图所示。据图判
lnX K
断,反应②对应的直线为_______ (填“”或“”),并在图中绘制反应③的 随+变化
a b l n K
的图像。
【高三化学第6 页(共8页)】 • 23-03C •(3) 在恒温条件下,上述三个反应在某体系中建立平衡后,将反应体系体积扩大到原来的2
倍,反应②的平衡将_______(填“正向”、“逆向”或“不”)移动,反应①和②重新达到平衡
时所需时间咖________( 填 或 “= ”)化。
(4) 一定条件下,向体积为 的恒容密闭容器中通人1 ( )和3 2( )发生上述
V L m d C M g mol H g
三个反应,达到平衡时,容器中 3() ( « ,()( )为6 ,此时 2 ( )的浓度为
C H H g)S mol C g mol H g
_______ (用含 、6、 的代数式表示,下同 • / 1,反应①的平衡常数为________。
a V )mol I
. 4( ) — 02( )催化重整对温室气体的减排具有重要意义,研究表明 〇2( )与
II C H g C g C g
4( )在催化剂存在下可发生反应制得合成气。
C H g
(5) 将原料按初始组成; z ( C H 4) : «( C 02) = 1 : 1充人某恒压密闭容 ■C〇2的体积分数/%
器中,发生反应 C H 4 ( g ) + C 02 ( g ) # 2 C ()( g )+2 H 2 ( g ) AH4> A
〇,体系起始总压强为 〇〇 ,达到平衡时 02( )的体积分数与
l kPa C g
温度的关系如图所示。若 、、 三点表示在不同温度和压强下, 、
A B C
反应达到平衡时 〇2 ( )的体积分数,则图中气体总压强最大的点
C g
为_______ (填标号)点,理由是_______________。
.电解法转化 02( )可实现 02( )的资源化利用,电解 ()2( )制甲酸盐的原理示意图
DI C g C g C g
如图。
0.1 mo卜 C KHCCV溶液
(6)电解一段时间后,若两侧电解液中 +的物质的量相差0. 04 ,则阳极产生的气体在
K mol
标准状况下的总体积为_______ (假设产生的气体全部逸出)。
L
(二)选考题:共15分。请考生从2道题中任选一题作答,如果多做,则按所做的第一题计分。
18. (15分)(物质结构与性质)氮及其化合物在工业、农业、生活中有着重要的应用。如二元氮
化物( 3 、 等)、三元锂过渡金属氮化物( 2等)等在储氢领域、化学电源领域都
Li N C r N LiMnN
有着重要的应用。
( ) 原子的核外电子排布式为_______ ;第一电离能 ________ (±真“> ”或“< ”)0。
1 C r :N
(2) 3可用于制备许多其他的含氮化合物{如 〇3、[ ( 3)4]-'[ ( 3)2: 、
N H H N C u N H A g N H r
[?6(%)(^氏 )5]304等丨以满足我们生产、生活的需要。 03 的杂化类型为
H N
________,[ ( 3)( 3)5] 04 中 的配位数为________。
Fe N N H S Fe
(3) 3 是很好的储氢材料,与 2发生反应生成 2和 ,写出该反应的化学方程
Li N H LiNH LiH
式:_______ ,该反应中氧化剂与还原剂的物质的量之比为 。
【高三化学第7 页(共8页)】 • 23 — 03C .⑷ 2晶体中, 为面心立方堆积, +填充了其中一半的四面体空隙,晶胞如图1
LiNH N H F U
所示,则一个 2晶胞中共含有_______ 个共价键;设该晶胞的边长为 〇11,用
LiNH a N a
表示阿伏加德罗常数的值,则该晶体的密度为________(用含 和 的代数式表示)
a iVA
g • cm—0
(5) 3-、 2+和形成立方晶体,其结构可以看作 型结构,其中 3_和 分 别 占 据
N M g NaCl N
体心和棱心,Mg〃 占据面心,立方晶胞如图2所示,该晶体的化学式为_______ 。
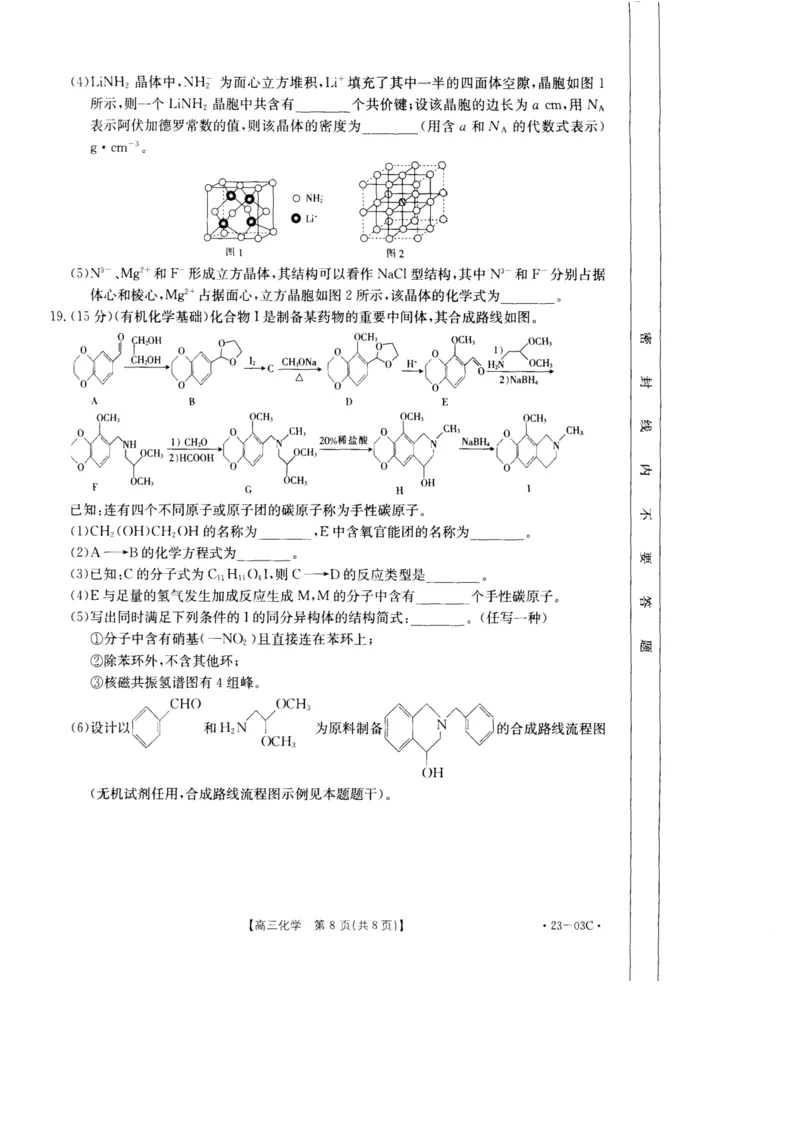
19. (15分)(有机化学基础)化合物 是制备某药物的重要中间体,其合成路线如图。
I
已知:连有四个不同原子或原子团的碳原子称为手性碳原子。
( ) 2(() ) 2 的名称为________, 中含氧官能团的名称为________。
1 C H H C H O H E
(2) —— 的化学方程式为_______ 。
A B
(3) 已知: 的分子式为 „ 04 ,则 + 的反应类型是_______。
C C H u I C D
(4) 与足量的氢气发生加成反应生成 , 的分子中含有_______ 个手性碳原子。
E M M
(5) 写出同时满足下列条件的 的同分异构体的结构简式:________。(任写一种)
I
① 分子中含有硝基(一 02 )且直接连在苯环上;
N
② 除苯环外,不含其他环;
③ 核磁共振氢谱图有4组峰。
C H O O C H 3 '
(6)设计以 和 H 2 i/ Y 为原料制备 (f Y N 的合成路线流程图
〇ch3
OH
(无机试剂任用,合成路线流程图示例见本题题干),
【高三化学第8 页(共8页)】 • 23—030