文档内容
第1讲 碳、硅及其化合物
[考纲要求]
1.掌握碳元素、硅元素的单质的主要性质及应用。2.掌握碳元素、硅元素的重要化合
物的主要性质及应用。3.了解碳元素、硅元素的单质及其重要化合物对环境质量的影响。
4.了解碳、硅的单质及其重要化合物的制备方法。
考点一 碳及其化合物
1知识梳理
1.碳
(1)存在形式既有________又有________。碳单质主要有金刚石、石墨、C 、C ,互
60 70
为____________。
(2)碳单质的结构与物理性质
(3)碳的化学性质2.碳的氧化物(CO、CO)的比较
2
CO CO
2
无色无味气体 无色无味气体
物理性质 密度比空气小 密度比空气大
难溶于水 可溶于水(溶解度小)
毒性 有毒(易结合血红蛋白) 无毒(温室效应)
可燃性
还原性 无(灭火)
还原氧化铁
①与炽热炭反应
化 氧化性
②Mg在CO 中燃烧
学 2
性 与水反应 无 CO+HO HCO
2 2 ⇌ 2 3
质
与碱反应 Ca(OH)+CO===CaCO↓+HO(检验
无 2 2 3 2
(石灰水) CO 2 )
相互转化 COCO
2
燃料
用途 灭火 制汽水 植物肥料 化工原料等
冶炼金属
3.CO 在自然界中的循环
2
CO 的主要来源:大量含碳燃料的燃烧。
2
自然界消耗CO 的主要反应:
2(1)溶于江水、海水中:CO+HO HCO;
2 2 ⇌ 2 3
(2)光合作用:6CO+6HO――→ ;
2 2
(3)岩石的风化:______________________________________________。
4.碳酸(HCO)
2 3
弱酸、不稳定。碳酸(HCO )只能在水中存在。HCO 在水中与CO 共存,因此常把CO
2 3 2 3 2 2
+HO当碳酸用。
2
5.碳酸的正盐和酸式盐的比较
正盐(CO2−
)
酸式盐(HCO−
)
3 3
溶解性 只有钾、钠、铵盐可溶 一般都可溶
热稳定性 正盐>酸式盐>碳酸
溶液pH 同浓度的:正盐>酸式盐
相互转化
CO2− HCO−
3 3
[判断] (正确的打“√”,错误的打“×”)
(1)碳有多种同素异形体,而氧不存在同素异形体( )
(2)金刚石和石墨由相同的元素组成,因此它们具有相同的性质( )
(3)石墨转变为金刚石的反应属于氧化还原反应( )
(4)向空气中排放二氧化碳会形成酸雨( )
(5)向CaCl 溶液中通入CO 气体,溶液变浑浊,继续通入CO 至过量,浑浊消失(
2 2 2
)
[提醒]
CO 与碱反应产物的判断
2
(1)CO 与单一组分反应(如CO 通入NaOH溶液)具体分析过程用数轴表示如下:
2 2
(2)CO 与多组分反应[如CO 通入NaOH、Ca(OH) 的混合溶液],反应的顺序是
2 2 2
①Ca(OH)+CO===CaCO↓+HO
2 2 3 2
②2NaOH+CO===NaCO+HO
2 2 3 2
③NaCO+CO+HO===2NaHCO
2 3 2 2 3
④CaCO+HO+CO===Ca(HCO)
3 2 2 3 2
2对点速练
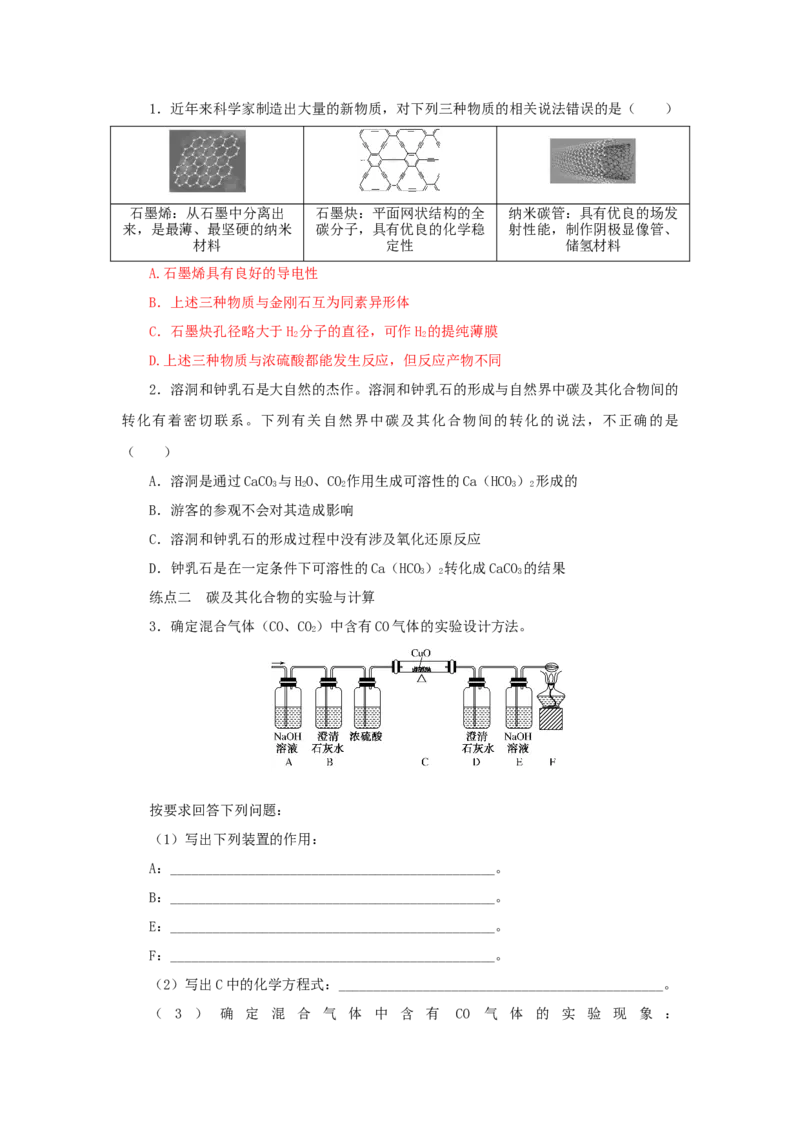
练点一 碳及其化合物的性质判断1.近年来科学家制造出大量的新物质,对下列三种物质的相关说法错误的是( )
石墨烯:从石墨中分离出 石墨炔:平面网状结构的全 纳米碳管:具有优良的场发
来,是最薄、最坚硬的纳米 碳分子,具有优良的化学稳 射性能,制作阴极显像管、
材料 定性 储氢材料
A.石墨烯具有良好的导电性
B.上述三种物质与金刚石互为同素异形体
C.石墨炔孔径略大于H 分子的直径,可作H 的提纯薄膜
2 2
D.上述三种物质与浓硫酸都能发生反应,但反应产物不同
2.溶洞和钟乳石是大自然的杰作。溶洞和钟乳石的形成与自然界中碳及其化合物间的
转化有着密切联系。下列有关自然界中碳及其化合物间的转化的说法,不正确的是
( )
A.溶洞是通过CaCO 与HO、CO 作用生成可溶性的Ca(HCO) 形成的
3 2 2 3 2
B.游客的参观不会对其造成影响
C.溶洞和钟乳石的形成过程中没有涉及氧化还原反应
D.钟乳石是在一定条件下可溶性的Ca(HCO) 转化成CaCO 的结果
3 2 3
练点二 碳及其化合物的实验与计算
3.确定混合气体(CO、CO)中含有CO气体的实验设计方法。
2
按要求回答下列问题:
(1)写出下列装置的作用:
A:______________________________________________。
B:______________________________________________。
E:______________________________________________。
F:______________________________________________。
(2)写出C中的化学方程式:______________________________________________。
( 3 ) 确 定 混 合 气 体 中 含 有 CO 气 体 的 实 验 现 象 :______________________________________________
______________________________________________。
4.标准状况下,将3.36 L CO 气体通入200 mL 1.00 mol·L-1NaOH溶液中,充分反
2
应后溶液中 c( )与 c( )的比值为(不考虑 、 的水解)
CO2− HCO− CO2− HCO−
3 3 3 3
( )
A.1∶1 B.1∶2
C.2∶1 D.1∶3
考点二 硅及其化合物、无机非金属材料
1知识梳理
1.硅
(1)硅的结构与物理性质
(2)硅的化学性质
①与氢氟酸反应:______________________________________________。
②与NaOH溶液反应:
Si+2NaOH+HO===______________________________________________。
2
③与O 反应:______________________________________________。
2
(3)硅的工业制法用 焦 炭 和 二 氧 化 硅 在 电 炉 中 反 应 得 到 粗 硅 , 反 应 的 化 学 方 程 式 为
______________________________________________。
2.二氧化硅
(1)存在
石英、水晶、玛瑙、沙子(含杂质)等。
(2)物理性质
熔、沸点高,硬而脆,不溶于水。
(3)化学性质
(4)用途:光导纤维、光学仪器。
3.硅酸的性质与用途4.硅酸盐的性质与表示方法
(1)NaSiO 水溶液俗称 ,常用于制作黏合剂、防腐剂和耐火材料。
2 3
( 2 ) 硅 酸 钠 溶 液 在 空 气 中 易 变 质 , 反 应 的 化 学 方 程 式 为
。
(3)硅酸盐组成的表示:如硅酸钠(NaSiO )可表示为 ,石棉
2 3
(CaMgSiO )可表示为______________________________________________。
3 4 12
5.常见无机非金属材料
(1)传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。
①常见硅酸盐材料比较
水泥 玻璃 陶瓷
生产原料
主要设备
生产条件 高温
②玻璃生产中的两个重要反应:
______________________________________________;
______________________________________________。
(2)新型无机非金属材料
①高温结构陶瓷 ②生物陶瓷 ③压电陶瓷
[判断] (正确的打“√”,错误的打“×”)
(1)硅在自然界中只以化合态的形式存在( )
(2)硅的化学性质不活泼,常温下不与任何物质反应( )
(3)单质硅常用作半导体材料和光导纤维( )
(4)SiO 不与任何酸反应,可用石英制造耐酸容器( )
2
(5)Si→SiO→HSiO 均能进行一步转化( )
2 2 3
(6)石英砂可用于生产单晶硅( )
(7)向一定浓度的NaSiO 溶液中通入适量CO 出现白色沉淀,证明HCO 的酸性比
2 3 2 2 3
HSiO 的酸性强( )
2 3
(8)传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料( )
(9)水泥、玻璃、青花瓷、水晶、玛瑙都属于硅酸盐产品( )
(10)水玻璃是混合物,可用于生产黏合剂和防火剂( )
(11)硅胶是硅酸钠的水溶液失去水后形成的凝胶( )
[提醒](1)SiO 虽能与HF反应,但不是两性氧化物,是酸性氧化物。
2
(2)SiO 虽是酸酐,但难溶于水,不能直接与水作用制备HSiO。
2 2 3
(3)HCO 酸性强于HSiO,但高温下可发生NaCO+SiO=====NaSiO+CO↑。
2 3 2 3 2 3 2 2 3 2
(4)Si还原性强于C,但高温下可发生2C+SiO=====Si+2CO↑。
2
2对点速练
1.下列有关硅的说法中,不正确的是( )
A.高纯度的硅广泛用于制作计算机
B.硅可由二氧化硅还原制得
C.低温时,硅与水、空气和酸不反应,但能与氢氟酸反应
D.自然界中硅的储量丰富,自然界中存在大量的单质硅
2.下列关于二氧化硅的说法正确的是( )
A.二氧化硅是酸性氧化物,因此能与水反应生成硅酸
B.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
C.二氧化硅不能与碳酸钠溶液反应,但能与碳酸钠固体在高温时发生反应
D.用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅
3.水玻璃(NaSiO 溶液)广泛应用于耐火材料、洗涤剂生产等领域,是一种重要的
2 3
工业原料。
如图是用稻壳灰(SiO:65%~70%、C:30%~35%)制取水玻璃的工艺流程:
2
下列说法正确的是( )
A.原材料稻壳灰价格低廉,且副产品活性碳有较高的经济价值
B.操作A与操作B完全相同
C.该流程中硅元素的化合价发生改变
D.反应器中发生的复分解反应为SiO+2NaOH===NaSiO+HO
2 2 3 2
练点二 硅的工业制取
4.高纯度晶体硅是典型的无机非金属材料,又称“半导体”材料,它可以按下列方法
制备:SiO――→Si(粗)――→SiHCl――→Si(纯)
2 3
下列说法正确的是( )
A.步骤①的化学方程式为SiO+C=====Si+CO↑
2 2
B.步骤①②③中每生成或反应1 mol Si,转移4 mol电子
C.二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D.SiHCl (沸点为33.0 ℃)中含有少量的SiCl (沸点为67.6 ℃),通过蒸馏(或
3 4
分馏)可提纯SiHCl
3
练后归纳
在设计制备纯硅的过程中,常遇到的知识点
(1)高温下用碳还原二氧化硅制得粗硅:
SiO+2C=====Si(粗)+2CO↑
2
(2)粗硅与干燥HCl气体反应制得SiHCl:
3
Si+3HCl=====SiHCl+H
3 2
(3)粗硅与干燥Cl 反应制得SiCl:
2 4
Si(粗)+2Cl=====SiCl
2 4
(4)SiHCl 与过量H 在高温下反应制得纯硅:
3 2
SiHCl+H=====Si(纯)+3HCl
3 2
(5)SiCl 与过量H 在高温下反应制得纯硅:
4 2
SiCl+2H=====Si(纯)+4HCl
4 2
练点三 无机非金属材料
5.“九秋风露越窑开,夺得千峰翠色来”是赞誉越窑秘色青瓷的诗句,描绘我国古代
精美的青瓷工艺品。玻璃、水泥和陶瓷均为硅酸盐制品,下列有关说法中正确的是
( )
A.玻璃是人类最早使用的硅酸盐制品
B.制水泥的原料为纯碱、石灰石和石英
C.硅酸盐制品的性质稳定、熔点较高
D.沙子和黏土的主要成分均为硅酸盐
6.氮化硅可用作高温陶瓷复合材料,在航空航天、汽车发动机、机械等领域有着广泛
的应用。由石英砂合成氮化硅粉末的路线如下图所示:其中—NH 中各元素的化合价与NH 相同。
2 3
请回答下列问题:
(1)石英砂不能与碱性物质共同存放,以NaOH为例,用化学反应方程式表示其原因:
______________________________________________
______________________________________________。
(2)图示①~⑤的变化中,属于氧化还原反应的是 。
(3)SiCl 在潮湿的空气中剧烈水解,产生白雾,军事工业中用于制造烟雾剂。SiCl
4 4
水解的化学反应方程式为 。
(4)在反应⑤中,3 mol Si(NH ) 在高温下加热可得1 mol氮化硅粉末和8 mol A
2 4
气体,则氮化硅的化学式为 。
(5)在高温下将SiCl 在B和C两种气体的气氛中,也能反应生成氮化硅,B和C两种
4
气体在一定条件下化合生成A。
写 出 SiCl 与 B 和 C 两 种 气 体 反 应 的 化 学 方 程 式
4
______________________________________________
______________________________________________。
本讲真题研练
1.[2020·天津卷,4]下列离子方程式书写正确的是( )
A.CaCO 与稀硝酸反应: + ===HO+CO↑
3 CO2− 2H+ 2 2
3
B.FeSO 溶液与溴水反应:2Fe2++Br===2Fe3++2Br−
4 2
C.NaOH溶液与过量HCO 溶液反应:HCO+ === +2HO
2 2 4 2 2 4 2OH− C O2− 2
2 4
D.CHONa溶液中通入少量CO: +CO+HO===2CHOH+
6 5 2 2C H O− 2 2 6 5 CO2−
6 5 3
2.[2020·浙江7月,24]CaSiO 是硅酸盐水泥的重要成分之一,其相关性质的说法
3 5
不正确的是( )A.可发生反应:CaSiO+4NHCl=====CaSiO+2CaCl+4NH↑+2HO
3 5 4 3 2 3 2
B.具有吸水性,需要密封保存
C.能与SO 反应生成新盐
2
D.与足量盐酸作用,所得固体产物主要为SiO
2
3.[2018·江苏卷,1]CO 是自然界碳循环中的重要物质。下列过程会引起大气中CO
2 2
含量上升的是( )
A.光合作用 B.自然降雨
C.化石燃料的燃烧 D.碳酸盐的沉积
4.[2017·全国卷Ⅱ,26]水泥是重要的建筑材料。水泥熟料的主要成分为 CaO、
SiO ,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程
2
如图所示:
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。
加入硝酸的目的是 ,还可使用 代替硝酸。
(2)沉淀A的主要成分是 ,其不溶于强酸但可与一种弱酸反应,该反应的化
学 方 程 式 为
________________________________________________________________________
________________________________________________________________________。
(3)加氨水过程中加热的目的是 。沉淀B的主要成分为 、
(填化学式)。
(4)草酸钙沉淀经稀HSO 处理后,用KMnO 标准溶液滴定,通过测定草酸的量可间接
2 4 4
获知钙的含量,滴定反应为: + +HCO―→ +CO+HO。实验中称取0.400
MnO− H+ 2 2 4 Mn2+ 2 2
4
g水泥样品,滴定时消耗了0.050 0 mol·L-1的KMnO 溶液36.00 mL,则该水泥样品中钙
4
的质量分数为 。
5.[2019·天津理综,10节选]多晶硅是制作光伏电池的关键材料。以下是由粗硅制
备多晶硅的简易过程。回答下列问题:
(1)硅粉与HCl在300 ℃时反应生成1 mol SiHCl 气体和H ,放出225 kJ热量,该
3 2
反应的热化学方程式为 。SiHCl 的电子式为
3
。
(2)由粗硅制备多晶硅过程中循环使用的物质除 SiCl 、SiHCl 和Si外,还有
4 3
(填分子式)。
第1讲 碳、硅及其化合物
考点一
1知识梳理
1.(1)游离态 化合态 同素异形体 (2)正四面体 高 大 正六边形 高 小
能 正五 正六 (3)C+O=====CO 2C+O=====2CO 3C+FeO=====3CO↑+2Fe 2C
2 2 2 2 3
+SiO=====Si+2CO↑ C+HO(g)=====CO+H C+2HSO (浓) CO↑+2SO↑+2HO
2 2 2 2 4 ≜ 2 2 2
C+4HNO(浓) CO↑+4NO↑+2HO
3 ≜ 2 2 2
3.(2)CH O+6O (3)CaCO+HO+CO===Ca(HCO)
6 12 6 2 3 2 2 3 2
判断 答案:(1)× (2)× (3)× (4)× (5)×
2对点速练
1.解析:A项,石墨烯是一种新发现的材料,它的物理性质是拉力好、导电性和导热
性好、硬度大、熔点高等;B项,同种元素的不同单质互称同素异形体;C项,碳原子半径
大于氢原子,则石墨炔孔径大于H 分子的直径,可以容纳H 分子;D项,碳与浓硫酸反应
2 2
产物均为二氧化碳和二氧化硫。
答案:D
2.答案:B
3.答案:(1)除去混合气体中的CO 气体 检验混合气体中的CO 是否除尽 除去尾
2 2
气中的CO 气体 除去尾气中的CO气体、防止污染环境
2
(2)CO+CuO Cu+CO
≜ 2(3)B中无明显现象,C中的物质由黑色变成红色,D中的澄清石灰水变浑浊
3.36 L
4.解析:n(CO )= =0.150 mol,n(NaOH)=0.200 L×1.00
2
22.4 L·mol-1
mol·L-1=0.200 mol,
n(NaOH) 0.200 mol 4 n(NaOH)
= = ,即 1< <2,反应产物为 NaCO 、
n(CO2) 0.15 mol 3 n(CO2)
2 3
{2x+y=0.2 mol {x=0.05 mol
NaHCO ,设其物质的量分别为x、y,则 ,解得 ,所
3 x+y=0.15 mol y=0.10 mol
以 n(CO 3 2− ) =1。
n(HCO− ) 2
3
答案:B
考点二
1知识梳理
1.(2)Si+4HF===SiF↑+2H↑ NaSiO +2H↑ Si+O SiO (3)SiO +
4 2 2 3 2 2≜ 2 2
2C=====Si+2CO↑
2.(3)2NaOH+SiO===NaSiO +HO CaO+SiO=====CaSiO SiO +2C=====Si+
2 2 3 2 2 3 2
2CO↑ 2Mg + SiO=====2MgO + Si NaCO + SiO=====NaSiO + CO↑ CaCO +
2 2 3 2 2 3 2 3
SiO=====CaSiO+CO↑
2 3 2
3.难 碳酸 NaCO +HSiO↓ HSiO SiO +HO NaSiO +2HCl===HSiO↓+
2 3 2 3 2 3≜ 2 2 2 3 2 3
2NaCl
4.(1)水玻璃 (2)NaSiO +HO+CO===NaCO +HSiO↓ (3)NaO·SiO
2 3 2 2 2 3 2 3 2 2
CaO·3MgO·4SiO
2
5.(1)石灰石、黏土 纯碱、石灰石和石英 黏土 水泥回转窑 玻璃窑 陶瓷窑
NaCO+SiO=====NaSiO+CO↑ CaCO+SiO=====CaSiO+CO↑
2 3 2 2 3 2 3 2 3 2
判断 答案:(1)√ (2)× (3)× (4)× (5)× (6)√ (7)√
(8)√ (9)× (10)√ (11)×
2对点速练
1.解析:硅是重要的半导体材料,可用于生产制造计算机中的芯片,A正确;2C+
SiO=====Si+2CO↑,B正确;常温下,Si的性质稳定,但可以与F 、HF、强碱溶液反应,
2 2C正确;自然界中不存在单质硅,D错误。
答案:D
2.解析:二氧化硅是酸性氧化物,但是二氧化硅不溶于水,与水不反应,故 A错误;
二氧化硅制成的光导纤维,由于其良好的光学特性而被用于制造光缆,故B错误;碳酸的
酸性强于硅酸,二氧化硅不能与碳酸钠溶液反应,但在高温时,二氧化硅能够与碳酸钠固
体反应生成硅酸钠和二氧化碳,故C正确;由方程式SiO +2C=====Si+2CO↑,可知当生
2
成2.24 L(标准状况)即0.1 mol气体时,得到0.05 mol即1.4 g硅,故D错误。
答案:C
3.解析:A项,稻壳灰来源广泛,价格低廉,活性炭具有吸附性,有较高的经济价值,
正确;B项,操作A为过滤,操作B为蒸发浓缩,是两种不同的操作,错误;C项,二氧化
硅中,硅元素的化合价是+4价,硅酸钠中,硅元素的化合价是+4价,所以该流程中硅元
素的化合价没有发生改变,错误;D项,由复分解反应的概念可知,SiO+2NaOH===NaSiO
2 2 3
+HO,不属于复分解反应,错误。
2
答案:A
4.解析:A项,步骤①的化学方程式为SiO +2C=====Si+2CO↑;B项,步骤②③中
2
每生成或反应1 mol Si,转移2 mol电子;C项,硅能与氢氟酸反应生成SiF 和氢气;D
4
项,SiHCl 和SiCl 的沸点相差较大,可通过蒸馏(或分馏)提纯SiHCl。
3 4 3
答案:D
5.解析:陶瓷是人类最早使用的硅酸盐制品,A项错误;纯碱、石灰石和石英是制玻
璃的原料,而制水泥的原料是黏土和石灰石,B项错误;硅酸盐制品性质稳定、熔点高,C
项正确;沙子的主要成分是SiO,黏土的主要成分是硅酸盐,D项错误。
2
答案:C
6.解析:石英砂不能与碱性物质共同存放的实质是 SiO 与碱性物质可以发生反应。
2
反应①是石英砂与焦炭发生氧化还原反应,反应②是硅单质与 Cl 反应,也是氧化还原反
2
应。SiCl 水解可以看做Si结合四个OH-生成HSiO ,HSiO 不稳定失水生成HSiO ,Cl-结
4 4 4 4 4 2 3
合H+生成HCl。氮化硅的化学式可通过题目信息运用质量守恒求得。结合题给信息,SiCl
4
与N、H 反应可得到SiN 和HCl。
2 2 3 4
答案:(1)SiO+2NaOH===NaSiO+HO
2 2 3 2
(2)①②
(3)SiCl+3HO===4HCl↑+HSiO↓
4 2 2 3
(4)SiN
3 4(5)3SiCl+2N+6H=====SiN+12HCl
4 2 2 3 4
本讲真题研练
1.解析:本题考查离子方程式的正误判断,考查的化学学科核心素养是宏观辨识与微
观探析。碳酸钙难溶于水,在离子方程式中应写成化学式,A项错误;Br 能够氧化Fe2+,
2
B项正确;NaOH与过量HCO 反应生成NaHCO ,C项错误;苯酚的酸性比 强,在苯
2 2 4 2 4 HCO−
3
酚钠溶液中通入少量CO 或过量CO,均只生成 ,D项错误。
2 2 HCO−
3
答案:B
2.解析:本题考查元素化合物知识,考查的化学学科核心素养是证据推理与模型认知。
加热时氯化铵分解生成HCl和氨气,HCl与CaSiO 反应得到硅酸钙、氯化钙和水,A项正
3 5
确;水泥吸水会变硬,需密封保存,B项正确;Ca SiO 能与二氧化硫反应得到亚硫酸钙,
3 5
C项正确;由上述分析可知,CaSiO 与足量盐酸反应得不到二氧化硅,D项错误。
3 5
答案:D
3.解析:光合作用过程中植物吸收CO ,使CO 含量下降,A项不符合题意;自然降雨
2 2
的过程会消耗CO ,使CO 含量下降,B项不符合题意;化石燃料燃烧时会产生CO ,使CO
2 2 2 2
含量上升,C项符合题意;碳酸盐能够与CO 反应生成可溶性的碳酸氢盐,消耗CO ,使CO
2 2 2
含量下降,D项不符合题意。
答案:C
4.解析:(1)Fe3+容易在pH较小时转化为沉淀,所以需要将Fe2+氧化为Fe3+。双氧
水可以将Fe2+氧化为Fe3+且不会引入杂质。
(2)二氧化硅不与强酸反应,但与 HF 反应,所以沉淀 A 是二氧化硅。SiO +
2
4HF===SiF↑+2HO。
4 2
(3)加热可以促进Fe3+、Al3+水解生成Fe(OH)、Al(OH) 沉淀。pH为4~5时Ca2
3 3
+、Mg2+不沉淀,Fe3+、Al3+沉淀,所以沉淀B为Fe(OH)、Al(OH)。
3 3
(4)5Ca2+~5HCO ~2KMnO ,n(KMnO )=0.050 0 mol/L×36.00 mL×10-3L·mL-1
2 2 4 4 4
=1.80×10-3mol,n(Ca2+)=4.50×10-3mol,水泥中钙的质量分数为×100%=45.0%。
答案:(1)将Fe2+氧化为Fe3+ 双氧水
(2)SiO SiO+4HF===SiF↑+2HO
2 2 4 2
(3)防止胶体生成,易沉淀分离 Fe(OH) Al(OH)
3 3(4)45.0%
5.答案:(1)Si(s)+3HCl(g)=====SiHCl (g)+H (g) ΔH=-225
3 2
kJ·mol-1
(2)HCl、H
2