文档内容
第 12 讲 氧化还原反应方程式的配平
复习目标 1.掌握氧化还原反应的配平方法。2.整合有效信息书写氧化还原反应方程式。
考点一 氧化还原反应方程式的配平
1.氧化还原方程式配平的基本原则
2.氧化还原方程式配平的一般步骤
配平化学方程式:
HS+HNO―→S↓+NO↑+HO
2 3 2
分析 配平步骤如下
第一步:标变价,HS+HNO3 ―→S↓+NO↑+HO
2 2
第二步:列得失,HS + HNO
2 3
失去2e-↓ ↓得到(5-2)e-
S NO
第三步:求总数,从而确定氧化剂(或还原产物)和还原剂(或氧化产物)的化学计量数。
HS + HNO
2 3
失去2e-×3↓ ↓得到3e-×2
S NO
故HS的化学计量数为3,HNO 的化学计量数为2。
2 3
第四步:配系数,先配平变价元素,再利用原子守恒配平其他元素。3HS+2HNO===3S↓+2NO↑+4HO
2 3 2
第五步:查守恒,其他原子在配平时相等,最后利用O原子守恒来进行验证。
题组一 正向配平类
1.(1)______HCl(浓)+______MnO =====______Cl↑+______MnCl +______HO
2 2 2 2
(2)______Cu+______HNO(稀)===______Cu(NO )+______NO↑+______HO
3 3 2 2
(3)______KI+______KIO +______HSO ===______I+______KSO +______HO
3 2 4 2 2 4 2
(4)______MnO+______H++______Cl-===______Mn2++______Cl↑+______HO
2 2
答案 (1)4 1 1 1 2 (2)3 8 3 2 4
(3)5 1 3 3 3 3 (4)2 16 10 2 5 8
题组二 逆向配平类
2.(1)______S+______KOH===______KS+______KSO +______HO
2 2 3 2
(2)______P +______KOH+______HO===______KPO +______PH
4 2 3 4 3
答案 (1)3 6 2 1 3 (2)2 9 3 3 5
题组三 缺项配平类
3.(1)______ClO-+______Fe(OH) +________===______Cl-+______FeO+______HO
3 2
(2)______MnO+______HO+________===______Mn2++______O↑+______HO
2 2 2 2
(3)某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有:Al O、C、N、CO。
2 3 2
请将AlN之外的反应物与生成物分别填入以下空格内,并配平。
++===AlN+
答案 (1)3 2 4OH- 3 2 5
(2)2 5 6H+ 2 5 8
(3)AlO 3C N 2 3CO
2 3 2
解析 (3)根据氮元素、碳元素的化合价变化,N 是氧化剂,C是还原剂,AlN为还原产物,
2
CO为氧化产物。
题组四 含有未知数的配平
4.(1)______FeS+______HCl===______S+______FeCl +______HS
x 2 2
(2)______Na S+______NaClO+______NaOH===______NaSO +______NaCl+______HO
2 x 2 4 2
答案 (1) 2 (-1) 1 1
(2)1 3x+1 2x-2 x 3x+1 x-1
题组五 有机物参与的氧化还原反应方程式的配平
5 . (1)______KClO + ______HC O + ______HSO ===______ClO ↑ + ______CO↑ +
3 2 2 4 2 4 2 2
______KHSO+______HO
4 2
(2)______C HO + ______KMnO + ______HSO ===______KSO + ______MnSO +
2 6 4 2 4 2 4 4
______CO↑+______HO
2 2答案 (1)2 1 2 2 2 2 2
(2)5 12 18 6 12 10 33
配平的基本技能
(1)全变从左边配:氧化剂、还原剂中某元素化合价是全变的,一般从左边反应物着手配平。
(2)自变从右边配:自身氧化还原反应(包括分解、歧化)一般从右边着手配平。
(3)缺项配平法:先将得失电子数配平,再观察两边电荷。若反应物这边缺正电荷,一般加 H
+,生成物一边加水;若反应物这边缺负电荷,一般加OH-,生成物一边加水,然后进行两
边电荷数配平。
(4)当方程式中有多个缺项时,应根据化合价的变化找准氧化剂、还原剂、氧化产物、还原
产物。
(5)在有机物参与的氧化还原反应方程式的配平中,一般有机物中H显+1价,O显-2价,
根据物质中元素化合价代数和为零的原则,确定碳元素的平均价态,然后进行配平。
考点二 信息条件下氧化还原反应方程式的书写
“四步法”突破新情景下氧化还原反应方程式的书写
[示例]
1.KMnO 能与热的经硫酸酸化的NaC O 溶液反应,生成Mn2+和CO ,该反应的离子方程
4 2 2 4 2
式是__________________________________________________________________________。
分析 第一步:依题意,锰元素的化合价降低,故 KMnO 是氧化剂,Mn2+是还原产物;碳
4
元素的化合价升高,故NaC O(碳元素化合价为+3价)是还原剂,CO 是氧化产物。
2 2 4 2
第二步:按“氧化剂+还原剂―→还原产物+氧化产物”把离子方程式初步写成:MnO+
C O―→Mn2++CO↑。
2 2
由MnO→Mn2+,锰元素降了5价;由C O→CO ,碳元素升了1价,1 mol C O共失去2 mol
2 2 2
e-,故在C O前配5,在氧化产物CO 前配10;在MnO前配2,在还原产物Mn2+前配2,
2 2即2MnO+5C O―→2Mn2++10CO↑。
2 2
第三步:反应在硫酸中进行,故在左边补充H+,右边补充HO,2MnO+5C O+H+
2 2
―→2Mn2++10CO↑+HO。
2 2
第四步:依据电荷守恒及H、O原子守恒配平如下:
2MnO+5C O+16H+=====2Mn2++10CO↑+8HO。
2 2 2
2.以低品位铜矿砂(主要成分为CuS)为原料制备氯化亚铜的路线如下:
写出酸溶1发生反应的化学方程式:__________________________________________。
分析 书写步骤:
(1)“瞻前”确定反应物
根据进料→确定反应物:CuS+MnO +HSO
2 2 4
(2)“顾后”确定生成物
根据出料中含有S,后续除锰生成MnCO ,说明酸溶1生成的是S和MnSO
3 4
(3)根据得失电子守恒配平发生氧化还原反应的物质
CuS+MnO +HSO ―→MnSO +S
2 2 4 4
(4)根据质量守恒补充并配平未发生氧化还原反应的物质
CuS+MnO +2HSO ===MnSO +S+2HO+CuSO
2 2 4 4 2 4
(5)检查质量、得失电子是否守恒
题组一 根据题干信息书写方程式
1.按要求完成下列方程式。
(1)已知在酸性介质中FeSO 能将+6价铬还原成+3价铬。写出Cr O与FeSO 溶液在酸性条
4 2 4
件下反应的离子方程式:______________________________________________________。
(2)KMnO 氧化废水中Mn2+生成MnO 的离子方程式为_______________________________。
4 2
(3)利用石灰乳和硝酸工业的尾气(含NO、NO )反应,既能净化尾气,又能获得应用广泛的
2
Ca(NO ) 。生产中溶液需保持弱碱性,在酸性溶液中 Ca(NO ) 会发生分解,产物之一是
2 2 2 2
NO , 反 应 的 离 子 方 程 式 :
____________________________________________________________。
(4)生产硫化钠大多采用无水芒硝(Na SO )—碳粉还原法,若煅烧所得气体为等物质的量的
2 4
CO 和 CO , 写 出 煅 烧 时 发 生 反 应 的 化 学 方 程 式 :
2
________________________________________。
(5)向含碘废液中加入稍过量的 NaSO 溶液,将废液中的 I 还原为I-,其离子方程式:
2 3 2________________________________________________________________________。
(6)H PO 的工业制法:将白磷(P )与Ba(OH) 溶液反应生成PH 气体和Ba(HPO ) ,后者再与
3 2 4 2 3 2 2 2
HSO 反应。写出白磷与Ba(OH) 溶液反应的化学方程式:__________________________。
2 4 2
答案 (1)Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
(2)3Mn2++2MnO+2HO===5MnO ↓+4H+
2 2
(3)3NO+2H+===NO+2NO↑+HO
2
(4)3Na SO +8C=====3NaS+4CO↑+4CO↑
2 4 2 2
(5)SO+I+HO===2I-+SO+2H+
2 2
(6)2P +3Ba(OH) +6HO===3Ba(HPO )+2PH ↑
4 2 2 2 2 2 3
题组二 根据图示信息书写方程式
2.(1)利用钴渣[含Co(OH) 、Fe(OH) 等]制备钴氧化物的工艺流程如下:
3 3
Co(OH) 溶解还原反应的离子方程式为___________________________________________。
3
(2)二氧化氯(ClO )是一种高效、广谱、安全的杀菌、消毒剂。氯化钠电解法是一种可靠的工
2
业生产ClO 方法。
2
该法工艺原理示意图如下。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO)与盐
3
酸反应生成ClO 。发生器中生成ClO 的化学方程式为_______________________________。
2 2
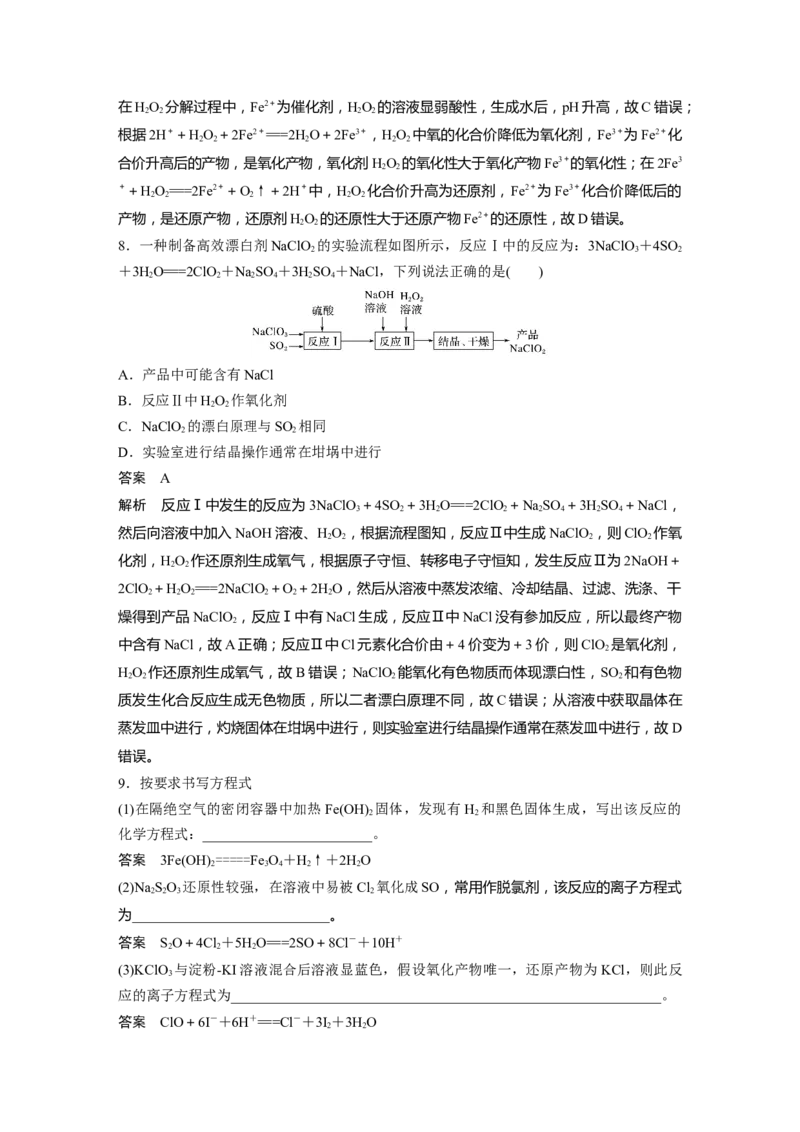
(3)地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题。文献报道某课题组模拟地
下水脱氮过程,利用Fe粉和KNO 溶液反应,探究脱氮原理及相关因素对脱氮速率的影响。
3
上图表示足量Fe粉还原上述KNO 溶液过程中,测出的溶液中相关离子浓度、pH随时间的
3
变化关系(部分副反应产物曲线略去)。请根据图中信息写出t 时刻前该反应的离子方程式:
1
________________________________________________________________________。
(4)以氧缺位铁酸铜(CuFe O )作催化剂,可利用太阳能热化学循环法分解HO制H ,其物
2 4-x 2 2
质转化如图所示。氧缺位铁酸铜(CuFe O )与水反应的化学方程式为_________________________________。
2 4-x
答案 (1)2Co(OH) +SO+4H+===2Co2++SO+5HO
3 2
(2)2NaClO+4HCl===2ClO ↑+Cl↑+2NaCl+2HO
3 2 2 2
(3)4Fe+NO+10H+===4Fe2++NH+3HO
2
(4)CuFe O +xHO===CuFe O+xH↑
2 4-x 2 2 4 2
1.[2020·全国卷Ⅱ,26(3)(4)(5)](3)Cl O为淡棕黄色气体,是次氯酸的酸酐,可由新制的
2
HgO和Cl 反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制
2
备 ClO 的 化 学 方 程 式 为
2
________________________________________________________________。
(4)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为
2
NaClO 、NaHSO 、NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到
2 4 3
ClO 溶液。上述过程中,生成ClO 的反应属于歧化反应,每生成1 mol ClO 消耗NaClO 的
2 2 2 2
量 为 ________mol ; 产 生 “ 气 泡 ” 的 化 学 方 程 式 为
________________________________________。
(5)“84 消 毒 液 ” 的 有 效 成 分 为 NaClO , 不 可 与 酸 性 清 洁 剂 混 用 的 原 因 是
________________(用离子方程式表示)。工业上是将氯气通入30%的NaOH溶液中来制备
NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1 000 kg该溶液需消耗氯气
的质量为________ kg(保留整数)。
答案 (3)2Cl +HgO===HgCl +ClO
2 2 2
(4)1.25 NaHCO +NaHSO===CO↑+NaSO +HO
3 4 2 2 4 2
(5)ClO-+Cl-+2H+===Cl↑+HO 203
2 2
解析 (3)由新制的HgO和Cl 反应制备ClO,由于该反应为歧化反应,所以只有氯元素的
2 2
化合价发生变化,由 0 价变为+1 价和-1 价,所以反应的化学方程式为 2Cl +
2
HgO===HgCl +ClO。(4)由题意知,在NaClO 生成ClO 的过程中,发生歧化反应,NaClO
2 2 2 2 2
既是氧化剂,又是还原剂,4NaClO―――→4ClO ,NaClO――→NaCl,每生成4 mol ClO ,需
2 2 2 2
消耗5 mol NaClO ,所以每生成1 mol ClO ,需消耗 mol(即1.25 mol) NaClO 。产生的气泡
2 2 2
的成分为CO ,反应的化学方程式为NaHCO +NaHSO===CO↑+NaSO +HO。(5)“84
2 3 4 2 2 4 2
消毒液”遇到酸性清洁剂能发生氧化还原反应:ClO-+Cl-+2H+===Cl↑+HO,消毒液
2 2失效且产生有毒Cl ,故“84消毒液”不能和酸性清洁剂混用。1 000 kg溶液中NaOH的质
2
量为m(NaOH)=1 000 kg×1%=10 kg,设反应中消耗Cl 的质量为x kg,则:
2
2NaOH+Cl===NaCl+NaClO+HO
2 2
80 71
x kg x kg
需要NaOH溶液的质量为(10 kg+x kg)÷30%=(10+x)kg。溶液的质量=NaOH溶液的质量
+Cl 的质量,1 000 kg=(10+x)kg+x kg,解得x≈203。
2
2.(1)[2019·全国卷Ⅱ,26(2)①]重晶石在回转炉中900~1 200 ℃条件下,被过量焦炭还原
为可溶性硫化钡,该过程的化学方程式为______________________________。回转炉尾气中
含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO 和一种清洁能源气体,该反应
2
的化学方程式为_________________________________________________________________。
(2)[2019·全国卷Ⅲ,26(1)]工业上可由天然二氧化锰粉和硫化锰矿用硫酸溶浸得硫单质和硫
酸锰,写出该反应的化学方程式:__________________________________________________。
答案 (1)BaSO +4C=========BaS+4CO↑ CO+HO===CO+H
4 2 2 2
(2)MnO +MnS+2HSO ===2MnSO +S+2HO
2 2 4 4 2
3.[2017·全国卷Ⅲ,27(1)]FeO·Cr O+NaCO+NaNO ――→NaCrO+Fe O+CO+NaNO
2 3 2 3 3 2 4 2 3 2 2
上述反应配平后FeO·Cr O 与NaNO 的系数比为________。该步骤不能使用陶瓷容器,原因
2 3 3
是________________________________________________________________________。
答案 2∶7 陶瓷在高温下会与NaCO 反应
2 3
解析 首先标出变价元素的化合价,分析价态变化可知:1 mol FeO·Cr O 失去7 mol电子,
2 3
1 mol NaNO 得到2 mol电子,则由得失电子守恒可知二者系数比应为2∶7;该步骤中主要
3
反应的反应物中有NaCO ,而陶瓷中含有二氧化硅,二者在熔融时反应,故不能使用陶瓷
2 3
容器。
4.[2017·全国卷Ⅰ,27(6)]已知FePO 沉淀―――――――→LiFePO ,写出该反应的化学方程式
4 4
________________________________________________________________________。
答案 2FePO +LiCO+HC O=====2LiFePO +HO↑+3CO↑
4 2 3 2 2 4 4 2 2
解析 反应物为FePO 、LiCO 、HC O ,生成物有LiFePO ,铁元素的化合价降低,则
4 2 3 2 2 4 4
HC O 中碳元素的化合价升高,产物为CO,配平。
2 2 4 2
5.[2016·全国卷Ⅱ,26(2)]实验室中可用次氯酸钠溶液与氨反应制备联氨(N H),反应的化
2 4
学方程式为______________________________________________________________________。
答案 NaClO+2NH ===NH+NaCl+HO
3 2 4 2
解析 次氯酸钠溶液与氨反应制备联氨的反应中,氮元素的化合价由氨分子中的-3价升高
到联氨分子中-2价,氯元素的化合价由次氯酸钠中的+1价降低到-1价,根据化合价升
高与降低总数相等和原子守恒配平化学方程式为NaClO+2NH ===NH+NaCl+HO。
3 2 4 21.高铁酸钾(K FeO)是一种既能杀菌消毒又能絮凝净水的水处理剂。工业制备高铁酸钾反
2 4
应的离子方程式为Fe(OH) +ClO-+OH-―→FeO+Cl-+HO(未配平)。下列有关说法不正
3 2
确的是( )
A.上述反应中氧化剂和还原剂的物质的量之比为3∶2
B.高铁酸钾中铁显+6价
C.由上述反应可知,Fe(OH) 的氧化性强于FeO
3
D.KFeO 处理水时,不仅能杀菌消毒,而且生成的Fe3+水解形成Fe(OH) 胶体能吸附水中
2 4 3
的悬浮杂质
答案 C
解析 根据质量守恒、电荷守恒和得失电子守恒配平方程式为 2Fe(OH) +3ClO-+4OH-
3
===2FeO+3Cl-+5HO。上述反应中ClO-为氧化剂,Fe(OH) 为还原剂,氧化剂和还原剂
2 3
的物质的量之比为3∶2,故A正确;高铁酸钾中铁显+6价,故B正确;由上述反应可知,
Fe(OH) 为还原剂,FeO为氧化产物,故不能比较Fe(OH) 和FeO的氧化性,故C错误;因
3 3
为铁离子水解生成氢氧化铁胶体,具有吸附性,所以 KFeO 处理水时,不仅能杀菌消毒,
2 4
而且能净水,故D正确。
2.根据下表信息,下列叙述中正确的是( )
序号 氧化剂 还原剂 氧化产物 还原产物
① Cl FeBr FeCl
2 2 3
② KMnO HO O MnO
4 2 2 2 2
③ KClO 浓盐酸 Cl
3 2
④ KMnO 浓盐酸 Cl MnCl
4 2 2
A.表中①反应的氧化产物只能有FeCl
3
B.表中②生成1 mol的O 将有4 mol的电子转移
2
C.表中④的离子方程式配平后,H+的化学计量数为16
D.表中③还原产物是KCl
答案 C
解析 若氧化剂足量,其氧化产物有氯化铁和溴单质两种,故A错误;该反应中HO 作还
2 2
原剂,氧元素化合价由-1价升高到0价,则生成1 mol的O 将有2 mol的电子转移,故B
2
错误;该反应中,锰元素价态从+7价降到+2价,氯元素价态从-1价升到0价,反应的方
程式为:2MnO+16H++10Cl-===2Mn2++5Cl↑+8HO,H+的化学计量数为16,故C正
2 2
确;该反应的方程式为:KClO+6HCl===3Cl↑+KCl+3HO,KClO 中氯元素价态从+5价
3 2 2 3
降到0价,HCl中部分氯元素价态从-1价升到0价,生成的Cl 中有是氧化产物,是还原产
2物,氯化钾不是还原产物,故D错误。
3.工业上常利用反应Cr O+CHOH+H+―→Cr3++CO↑+HO(未配平)来测定工业甲醇
2 3 2 2
中甲醇的含量,下列说法中正确的是( )
A溶液的颜色从灰绿色变为橙色
B.Cr O发生氧化反应
2
C.若配平后Cr3+和CO 的化学计量数比为2∶1,则Cr O中的n=2
2 2
D.若有3.2 g CH OH参加反应,则转移的电子数为6.02×1022
3
答案 C
解析 根据反应方程式可知,Cr3+为灰绿色,是生成物,溶液的颜色应该变成灰绿色,故A
错误;反应中CHOH中C元素的化合价由-2价升高到+4价,被氧化,则Cr O发生还原
3 2
反应,故B错误;若配平后Cr3+和CO 的化学计量数比为2∶1,假设生成的二氧化碳为1
2
mol,则转移6 mol电子,根据得失电子守恒,Cr O中Cr元素的化合价为+6价,因此n=
2
2,故C正确;3.2 g CH OH的物质的量为=0.1 mol,则转移的电子为 0.6 mol,数目为
3
0.6×6.02×1023,故D错误。
4.某离子反应涉及HO、ClO-、NH、H+、N 、Cl-等微粒,其中N 、ClO-的物质的量随
2 2 2
时间变化的曲线如图所示,下列说法正确的是( )
A.该反应中Cl-为氧化产物
B.消耗1 mol还原剂,转移6 mol电子
C.反应后溶液的酸性减弱
D.NH被ClO-氧化成N
2
答案 D
解析 反应的方程式应为3ClO-+2NH===N↑+2H++3HO+3Cl-。由方程式可知,N元
2 2
素的化合价升高,则N 为氧化产物,Cl-为还原产物,故A错误;N元素化合价由-3价升
2
高到0价,则消耗1 mol还原剂,转移3 mol电子,故B错误;根据方程式可知,反应生成
了氢离子,反应后溶液的酸性增强,故C错误;由方程式可知,NH被ClO-氧化成N ,故
2
D正确。
5.(2020·滨州调研)工业上用发烟HClO 将潮湿的CrCl 氧化为棕色的烟[CrO (ClO )],来除
4 3 2 4 2
去Cr(Ⅲ),HClO 中部分氯元素转化为最低价态。下列说法错误的是( )
4
A.CrO(ClO ) 中Cr元素显+6价
2 4 2
B.HClO 属于强酸,该反应还生成了另一种强酸
4
C.该反应中,参加反应的氧化剂与氧化产物的物质的量之比为3∶8
D.该反应的离子方程式为19ClO+8Cr3++8OH-===8CrO(ClO )+3Cl-+4HO
2 4 2 2答案 D
解析 CrO(ClO ) 中O为-2价、Cl为+7价,则根据化合物中元素化合价代数和等于 0,
2 4 2
可知Cr元素化合价为+6价,A正确;Cl元素非金属性较强,HClO 属于强酸,HClO 氧化
4 4
CrCl 为棕色的CrO(ClO ) ,部分HClO 被还原生成HCl,HCl也属于强酸,B正确;根据
3 2 4 2 4
得失电子守恒、电荷守恒及原子守恒,可得该反应的离子方程式为 19ClO+8Cr3++
4HO===8CrO(ClO ) +3Cl-+8H+,化合价降低的为氧化剂,即ClO,其中有3 mol Cl元素
2 2 4 2
发生变化,化合价升高的为还原剂,对应的产物为氧化产物,故 CrO(ClO ) 为氧化产物,
2 4 2
其中有8 mol Cr元素发生变化,故氧化剂与氧化产物的物质的量之比为3∶8,C正确、D错
误。
6.(2020·山东东营调研)NaNO 是一种食品添加剂。但食用过量可能致癌。酸性KMnO 溶液
2 4
与NaNO 反应的化学方程式为MnO+NO+―→Mn2++NO+HO(未配平)。下列叙述中正确
2 2
的是( )
A.该反应中NO被还原
B.反应过程中溶液的pH减小
C.生成1 mol NaNO 需消耗0.4 mol KMnO
3 4
D.中的粒子是OH-
答案 C
解析 NO中N元素的化合价升高,NO被氧化,A项错误;根据得失电子守恒和原子守恒
可知反应的离子方程式为2MnO+5NO+6H+===2Mn2++5NO+3HO,据此可知B、D项错
2
误,C项正确。
7.常温下,向HO 溶液中滴加少量Fe (SO ) 溶液,反应原理如图所示,下列说法正确的是
2 2 2 4 3
( )
A.该反应过程中,M是Fe3+,M′是Fe2+
B.当有1 mol O 生成时,转移2 mol电子
2
C.在HO 分解过程中,溶液的pH逐渐降低
2 2
D.HO 的氧化性比Fe3+强,还原性比Fe2+弱
2 2
答案 B
解析 根据箭头方向,找出反应物和生成物,两步反应分别为:2H++HO +2M===2HO
2 2 2
+2M′;2M′+HO===2M+O↑+2H+;根据HO 的化合价变化,M为Fe2+,M′为
2 2 2 2 2
Fe3+,故A错误;总反应为:2HO===2HO+O↑,每有1 mol O 生成时,2 mol H O 中2
2 2 2 2 2 2 2
mol
-1价氧元素生成2 mol 0价氧元素,转移2 mol电子,故B正确;2HO===2HO+O↑,
2 2 2 2在HO 分解过程中,Fe2+为催化剂,HO 的溶液显弱酸性,生成水后,pH升高,故C错误;
2 2 2 2
根据2H++HO +2Fe2+===2HO+2Fe3+,HO 中氧的化合价降低为氧化剂,Fe3+为Fe2+化
2 2 2 2 2
合价升高后的产物,是氧化产物,氧化剂HO 的氧化性大于氧化产物Fe3+的氧化性;在2Fe3
2 2
++HO===2Fe2++O↑+2H+中,HO 化合价升高为还原剂,Fe2+为Fe3+化合价降低后的
2 2 2 2 2
产物,是还原产物,还原剂HO 的还原性大于还原产物Fe2+的还原性,故D错误。
2 2
8.一种制备高效漂白剂NaClO 的实验流程如图所示,反应Ⅰ中的反应为:3NaClO +4SO
2 3 2
+3HO===2ClO +NaSO +3HSO +NaCl,下列说法正确的是( )
2 2 2 4 2 4
A.产品中可能含有NaCl
B.反应Ⅱ中HO 作氧化剂
2 2
C.NaClO 的漂白原理与SO 相同
2 2
D.实验室进行结晶操作通常在坩埚中进行
答案 A
解析 反应Ⅰ中发生的反应为3NaClO +4SO +3HO===2ClO +NaSO +3HSO +NaCl,
3 2 2 2 2 4 2 4
然后向溶液中加入NaOH溶液、HO ,根据流程图知,反应Ⅱ中生成NaClO ,则ClO 作氧
2 2 2 2
化剂,HO 作还原剂生成氧气,根据原子守恒、转移电子守恒知,发生反应Ⅱ为2NaOH+
2 2
2ClO +HO===2NaClO+O+2HO,然后从溶液中蒸发浓缩、冷却结晶、过滤、洗涤、干
2 2 2 2 2 2
燥得到产品NaClO ,反应Ⅰ中有NaCl生成,反应Ⅱ中NaCl没有参加反应,所以最终产物
2
中含有NaCl,故A正确;反应Ⅱ中Cl元素化合价由+4价变为+3价,则ClO 是氧化剂,
2
HO 作还原剂生成氧气,故B错误;NaClO 能氧化有色物质而体现漂白性,SO 和有色物
2 2 2 2
质发生化合反应生成无色物质,所以二者漂白原理不同,故C错误;从溶液中获取晶体在
蒸发皿中进行,灼烧固体在坩埚中进行,则实验室进行结晶操作通常在蒸发皿中进行,故D
错误。
9.按要求书写方程式
(1)在隔绝空气的密闭容器中加热Fe(OH) 固体,发现有H 和黑色固体生成,写出该反应的
2 2
化学方程式:________________________。
答案 3Fe(OH) =====Fe O+H↑+2HO
2 3 4 2 2
(2)Na SO 还原性较强,在溶液中易被Cl 氧化成SO,常用作脱氯剂,该反应的离子方程式
2 2 3 2
为____________________________。
答案 SO+4Cl+5HO===2SO+8Cl-+10H+
2 2 2
(3)KClO 与淀粉-KI溶液混合后溶液显蓝色,假设氧化产物唯一,还原产物为 KCl,则此反
3
应的离子方程式为_____________________________________________________________。
答案 ClO+6I-+6H+===Cl-+3I+3HO
2 2(4)MnO 与 KClO 、KOH 溶液共热,可得到 KMnO ,此反应的化学方程式是
2 3 2 4
________________________________________________________________________。
答案 3MnO +6KOH+KClO=====3KMnO +KCl+3HO
2 3 2 4 2
(5)氨基甲酸铵(NH COONH)极易水解,产物是碳酸氢铵和一种弱碱,请写出其水解反应方
2 4
程式:_______________________________________________________________________。
答案 NH COONH+2HONH HCO +NH ·H O
2 4 2 4 3 3 2
(6)在催化剂作用下,尿素[CO(NH)]也可以与NO 反应生成N 和HO。写出CO(NH) 与
2 2 x 2 2 2 2
NO 反应的化学方程式:__________________________________________________________。
2
答案 4CO(NH)+6NO =====7N+4CO+8HO
2 2 2 2 2 2
10.已知还原性:HSO>I-,氧化性:IO>I 。
2
(1)在NaIO 溶液中滴加少量NaHSO 溶液,发生下列反应。配平反应方程式,并标出电子转
3 3
移的方向和数目。
NaIO +NaHSO===I+NaSO +HSO +HO
3 3 2 2 4 2 4 2
(2)在NaIO 溶液中滴加过量 NaHSO 溶液,反应完全,推测反应后溶液中的还原产物为
3 3
__________(填化学式)。
(3)在含5 mol NaHSO 的溶液中逐滴加入NaIO 溶液,加入NaIO 的物质的量和析出I 的物
3 3 3 2
质的量的关系曲线如图所示。写出反应过程中与 AB 段曲线对应的离子方程式:
________________________________________________________________________;
当溶液中I-与I 的物质的量之比为5∶3时,加入的NaIO 为__________mol。
2 3
答案 (1) ===2I+7NaSO +3HSO +2HO
2 2 4 2 4 2
(2)NaI (3)IO+5I-+6H+===3I+3HO
2 2
解析 (1)碘元素的化合价由+5降低到0,硫元素的化合价由+4升高到+6。根据化合价升
降总数相等,配平反应方程式,标出电子转移的方向和数目。(2)由还原性:HSO>I-可知,
当NaHSO 溶液过量时,IO先被还原成I ,再被还原成I-。(3)OA段,随着IO的量增加,
3 2
NaHSO 的量减少,IO被还原成I-,至A点恰好完全反应,此时继续加入NaIO ,又发生
3 3
NaIO 氧化I-的反应:IO+6H++5I-===3I +3HO。当I-与I 的物质的量之比为5∶3时,
3 2 2 2
设加入的NaIO 为x mol,根据转移电子数守恒,得5×2=x×6+x×5,解得x=。
3