文档内容
专项提能特训 4 含氯化合物的制备
1.(2020·新乡模拟)ClO 和NaClO 均具有漂白性,工业上用ClO 气体制NaClO 的工艺流程
2 2 2 2
如图所示。
下列说法不正确的是( )
A.步骤a的操作包括过滤、洗涤和干燥
B.吸收器中生成NaClO 的离子方程式:2ClO +HO===2ClO+O↑+2H+
2 2 2 2 2
C.工业上可将ClO 制成NaClO 固体,便于贮存和运输
2 2
D.通入空气的目的是驱赶出ClO ,使其被吸收器充分吸收
2
答案 B
解析 冷却结晶得到的固体需过滤、洗涤固体表面吸附的离子、干燥,A项正确;反应在碱
性条件下发生,正确的离子方程式为2ClO +HO +2OH-===2ClO+O +2HO,B项错误;
2 2 2 2 2
通入空气可以使ClO 与溶液充分接触,D项正确。
2
2.(2020·浙江模拟)某同学通过以下流程制取 NaClO 晶体:
2
已知:ClO 浓度过高时易发生分解,NaClO 在温度高于60 ℃时易分解, NaClO 饱和溶
2 2 2
液在低于38 ℃时析出NaClO·3H O,高于38 ℃时析出 NaClO。
2 2 2
下列说法不正确的是( )
A.步骤①中工业上常用HC O 代替NaSO
2 2 4 2 3
B.步骤②发生反应的离子方程式为2ClO +2OH-+HO===2ClO+O+2HO
2 2 2 2 2
C.步骤③的结晶方法为蒸发浓缩,冷却结晶
D.步骤④中制得的NaClO 晶体可用略高于38 ℃的热水洗涤2~3遍
2
答案 C
解析 步骤①中NaSO 作为还原剂,HC O 也是常见的还原剂,工业上常用HC O 代替
2 3 2 2 4 2 2 4
NaSO ,故A正确;步骤②发生的反应为碱性条件下ClO 与双氧水发生氧化还原反应生成
2 3 2
ClO、O 和HO,反应的离子方程式为 2ClO +2OH-+HO===2ClO+O +2HO,故B正
2 2 2 2 2 2 2
确;由于NaClO 在温度高于60 ℃时易分解,因此结晶方法不可以用蒸发浓缩和冷却结晶
2
的方法,应该用减压蒸发的办法,故C错误;由于NaClO 饱和溶液在低于38 ℃时析出
2NaClO·3H O,高于38 ℃时析出 NaClO ,步骤④中制得的NaClO 晶体中可用略高于38
2 2 2 2
℃的热水洗涤2~3遍,故D正确。
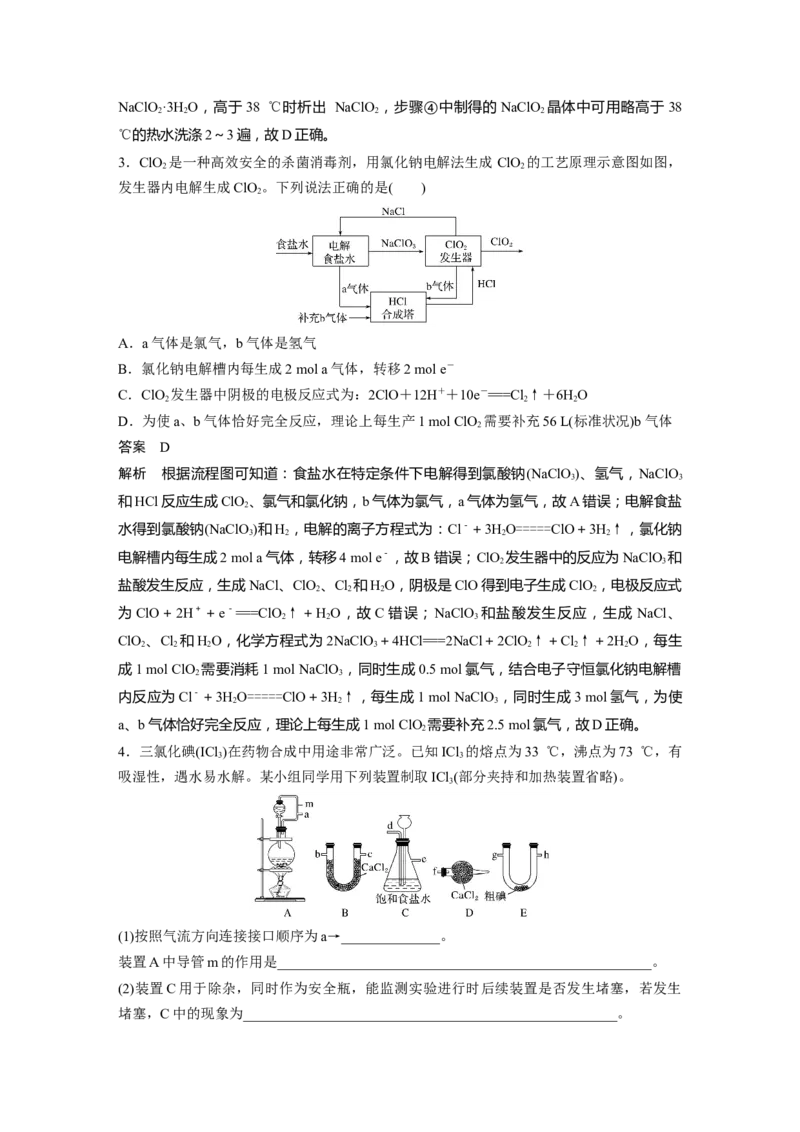
3.ClO 是一种高效安全的杀菌消毒剂,用氯化钠电解法生成 ClO 的工艺原理示意图如图,
2 2
发生器内电解生成ClO 。下列说法正确的是( )
2
A.a气体是氯气,b气体是氢气
B.氯化钠电解槽内每生成2 mol a气体,转移2 mol e-
C.ClO 发生器中阴极的电极反应式为:2ClO+12H++10e-===Cl↑+6HO
2 2 2
D.为使a、b气体恰好完全反应,理论上每生产1 mol ClO 需要补充56 L(标准状况)b气体
2
答案 D
解析 根据流程图可知道:食盐水在特定条件下电解得到氯酸钠(NaClO)、氢气,NaClO
3 3
和HCl反应生成ClO 、氯气和氯化钠,b气体为氯气,a气体为氢气,故A错误;电解食盐
2
水得到氯酸钠(NaClO)和H ,电解的离子方程式为:Cl-+3HO=====ClO+3H↑,氯化钠
3 2 2 2
电解槽内每生成2 mol a气体,转移4 mol e-,故B错误;ClO 发生器中的反应为NaClO 和
2 3
盐酸发生反应,生成NaCl、ClO 、Cl 和HO,阴极是ClO得到电子生成ClO ,电极反应式
2 2 2 2
为ClO+2H++e-===ClO ↑+HO,故 C错误;NaClO 和盐酸发生反应,生成 NaCl、
2 2 3
ClO 、Cl 和HO,化学方程式为2NaClO +4HCl===2NaCl+2ClO ↑+Cl↑+2HO,每生
2 2 2 3 2 2 2
成1 mol ClO 需要消耗1 mol NaClO ,同时生成0.5 mol氯气,结合电子守恒氯化钠电解槽
2 3
内反应为Cl-+3HO=====ClO+3H↑,每生成1 mol NaClO ,同时生成3 mol氢气,为使
2 2 3
a、b气体恰好完全反应,理论上每生成1 mol ClO 需要补充2.5 mol氯气,故D正确。
2
4.三氯化碘(ICl )在药物合成中用途非常广泛。已知ICl 的熔点为33 ℃,沸点为73 ℃,有
3 3
吸湿性,遇水易水解。某小组同学用下列装置制取ICl (部分夹持和加热装置省略)。
3
(1)按照气流方向连接接口顺序为a→______________。
装置A中导管m的作用是_____________________________________________________。
(2)装置C用于除杂,同时作为安全瓶,能监测实验进行时后续装置是否发生堵塞,若发生
堵塞,C中的现象为_____________________________________________________。(3)氯气与单质碘需在温度稍低于70 ℃下反应,则装置E适宜的加热方式为______________。
装置E中发生反应的化学方程式:________________________________________________。
(4)该装置存在的明显缺陷是______________________________________________________。
答案 (1)d→e→b→c→g→h→f(接口b与c、g与h可互换) 使浓盐酸顺利滴下 (2)锥形瓶
中液面下降,长颈漏斗中液面上升 (3)水浴加热 3Cl +I=====2ICl (4)缺少尾气处理装
2 2 3
置
解析 (1)在装置A中用浓盐酸与MnO 混合加热制取Cl ,浓盐酸易挥发,制取的氯气中会
2 2
含有氯化氢、水蒸气等杂质,通过装置C除去HCl杂质,再通过装置B干燥,得到干燥、
纯净的氯气,然后在装置E中氯气与碘单质反应制得ICl ;为防止ICl 水解,在E后面连接
3 3
盛有干燥剂的装置D,防止空气中的水蒸气进入E装置。故按照气流方向连接装置接口顺序
为:a→d→e→b→c→g→h→f,(接口b与c、g与h可互换);在装置A中导管m使分液漏斗
中的液体上下压强一致,这样分液漏斗中的浓盐酸可以顺利滴下。
(2)装置C也是安全瓶,监测实验E中是否发生堵塞,若装置E发生堵塞,则C中气体压强
增大,液体会进入长颈漏斗中,使锥形瓶中液面下降,长颈漏斗中液面上升。
(3)因水浴加热能简便控制加热的温度,且能使反应装置受热均匀,又因为氯气与单质碘需
在温度稍低于70 ℃下反应,故应采取水浴加热的方式;在装置E中Cl 与I 在低于70 ℃下
2 2
发生反应:3Cl+I=====2ICl 。
2 2 3
(4)Cl 是有毒气体,通过盛有无水氯化钙的干燥管只能吸收水分,不能吸收氯气,这样就会
2
造成大气污染,故该装置的缺陷是缺少尾气处理装置。