文档内容
专项提能特训 9 化学反应过程与能量变化
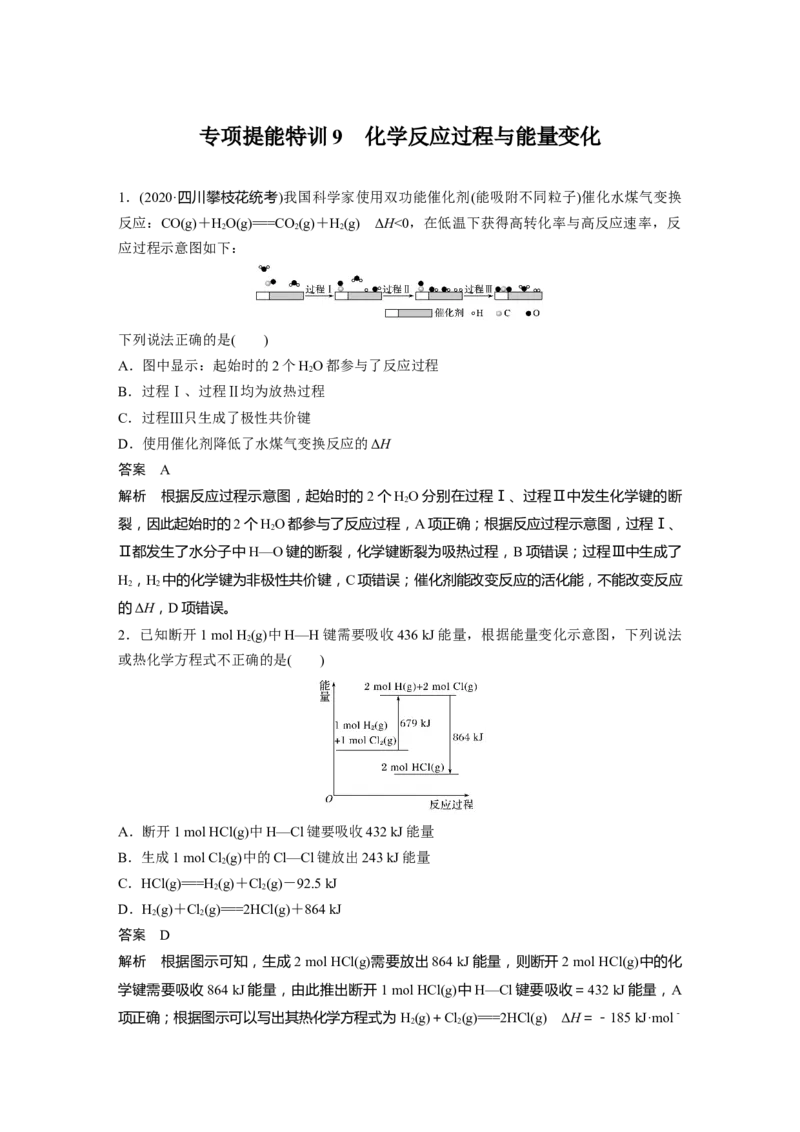
1.(2020·四川攀枝花统考)我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换
反应:CO(g)+HO(g)===CO(g)+H(g) ΔH<0,在低温下获得高转化率与高反应速率,反
2 2 2
应过程示意图如下:
下列说法正确的是( )
A.图中显示:起始时的2个HO都参与了反应过程
2
B.过程Ⅰ、过程Ⅱ均为放热过程
C.过程Ⅲ只生成了极性共价键
D.使用催化剂降低了水煤气变换反应的ΔH
答案 A
解析 根据反应过程示意图,起始时的2个HO分别在过程Ⅰ、过程Ⅱ中发生化学键的断
2
裂,因此起始时的2个HO都参与了反应过程,A项正确;根据反应过程示意图,过程Ⅰ、
2
Ⅱ都发生了水分子中H—O键的断裂,化学键断裂为吸热过程,B项错误;过程Ⅲ中生成了
H,H 中的化学键为非极性共价键,C项错误;催化剂能改变反应的活化能,不能改变反应
2 2
的ΔH,D项错误。
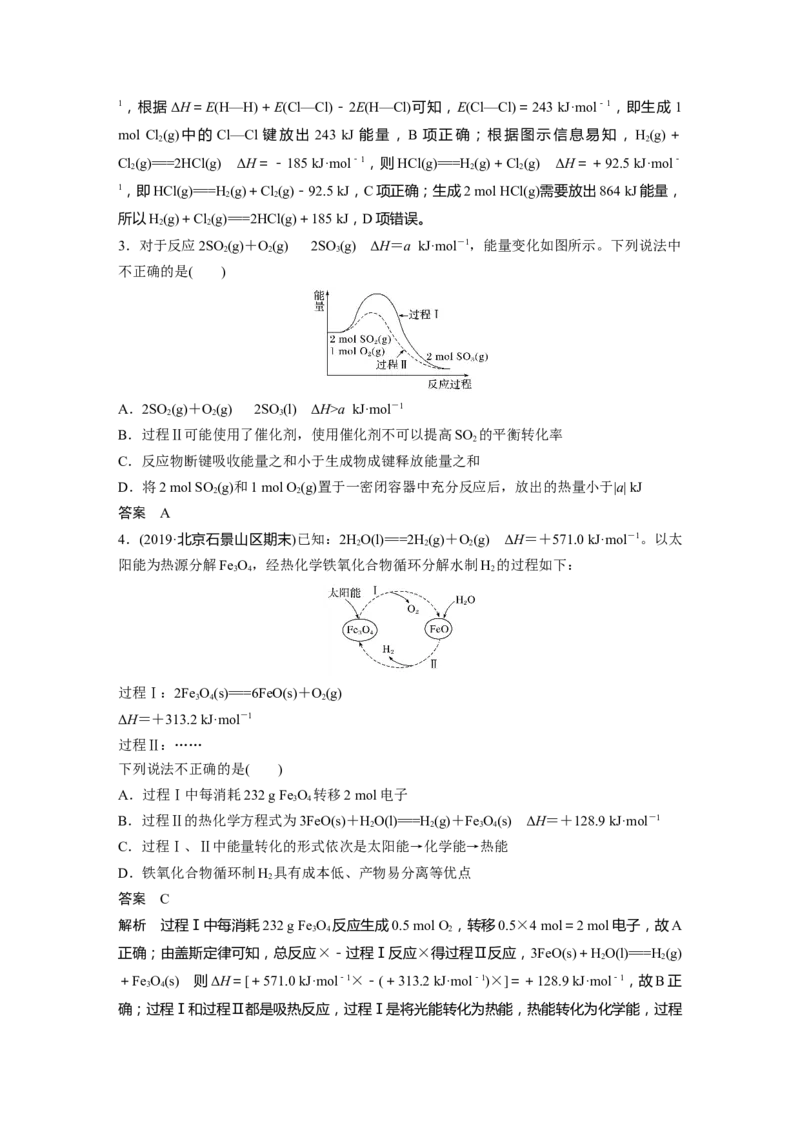
2.已知断开1 mol H (g)中H—H键需要吸收436 kJ能量,根据能量变化示意图,下列说法
2
或热化学方程式不正确的是( )
A.断开1 mol HCl(g)中H—Cl键要吸收432 kJ能量
B.生成1 mol Cl (g)中的Cl—Cl键放出243 kJ能量
2
C.HCl(g)===H(g)+Cl(g)-92.5 kJ
2 2
D.H(g)+Cl(g)===2HCl(g)+864 kJ
2 2
答案 D
解析 根据图示可知,生成2 mol HCl(g)需要放出864 kJ能量,则断开2 mol HCl(g)中的化
学键需要吸收864 kJ能量,由此推出断开1 mol HCl(g)中H—Cl键要吸收=432 kJ能量,A
项正确;根据图示可以写出其热化学方程式为 H(g)+Cl(g)===2HCl(g) ΔH=-185 kJ·mol-
2 21,根据ΔH=E(H—H)+E(Cl—Cl)-2E(H—Cl)可知,E(Cl—Cl)=243 kJ·mol-1,即生成1
mol Cl (g)中的 Cl—Cl 键放出 243 kJ 能量,B 项正确;根据图示信息易知,H(g)+
2 2
Cl(g)===2HCl(g) ΔH=-185 kJ·mol-1,则HCl(g)===H(g)+Cl(g) ΔH=+92.5 kJ·mol-
2 2 2
1,即HCl(g)===H(g)+Cl(g)-92.5 kJ,C项正确;生成2 mol HCl(g)需要放出864 kJ能量,
2 2
所以H(g)+Cl(g)===2HCl(g)+185 kJ,D项错误。
2 2
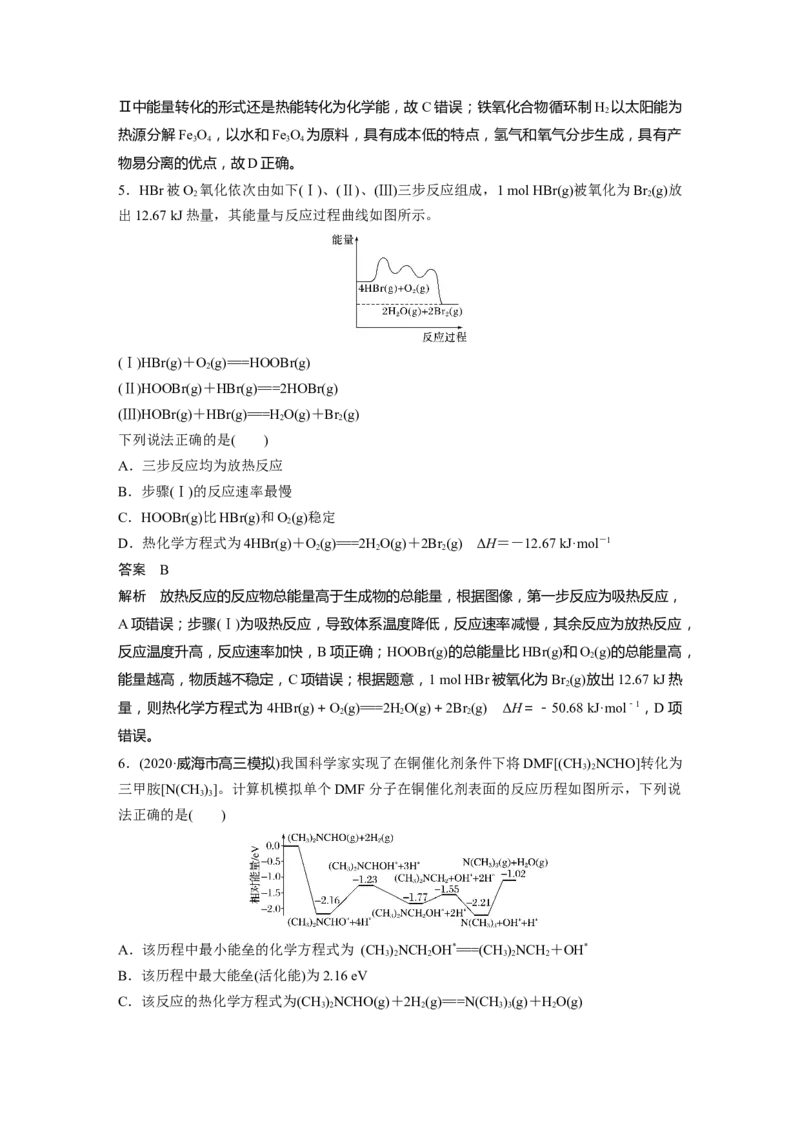
3.对于反应2SO (g)+O(g)2SO (g) ΔH=a kJ·mol-1,能量变化如图所示。下列说法中
2 2 3
不正确的是( )
A.2SO (g)+O(g)2SO (l) ΔH>a kJ·mol-1
2 2 3
B.过程Ⅱ可能使用了催化剂,使用催化剂不可以提高SO 的平衡转化率
2
C.反应物断键吸收能量之和小于生成物成键释放能量之和
D.将2 mol SO (g)和1 mol O (g)置于一密闭容器中充分反应后,放出的热量小于|a| kJ
2 2
答案 A
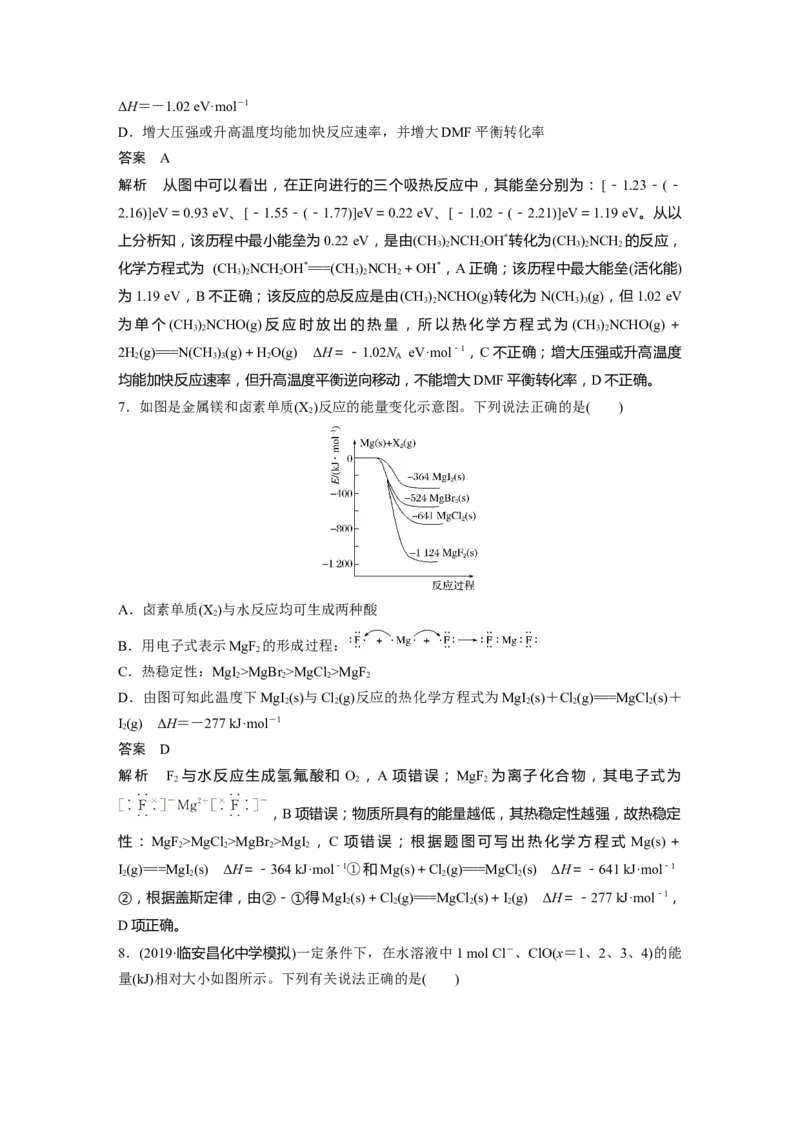
4.(2019·北京石景山区期末)已知:2HO(l)===2H(g)+O(g) ΔH=+571.0 kJ·mol-1。以太
2 2 2
阳能为热源分解Fe O,经热化学铁氧化合物循环分解水制H 的过程如下:
3 4 2
过程Ⅰ:2Fe O(s)===6FeO(s)+O(g)
3 4 2
ΔH=+313.2 kJ·mol-1
过程Ⅱ:……
下列说法不正确的是( )
A.过程Ⅰ中每消耗232 g Fe O 转移2 mol电子
3 4
B.过程Ⅱ的热化学方程式为3FeO(s)+HO(l)===H(g)+Fe O(s) ΔH=+128.9 kJ·mol-1
2 2 3 4
C.过程Ⅰ、Ⅱ中能量转化的形式依次是太阳能→化学能→热能
D.铁氧化合物循环制H 具有成本低、产物易分离等优点
2
答案 C
解析 过程Ⅰ中每消耗232 g Fe O 反应生成0.5 mol O ,转移0.5×4 mol=2 mol电子,故A
3 4 2
正确;由盖斯定律可知,总反应×-过程Ⅰ反应×得过程Ⅱ反应,3FeO(s)+HO(l)===H(g)
2 2
+Fe O(s) 则ΔH=[+571.0 kJ·mol-1×-(+313.2 kJ·mol-1)×]=+128.9 kJ·mol-1,故B正
3 4
确;过程Ⅰ和过程Ⅱ都是吸热反应,过程Ⅰ是将光能转化为热能,热能转化为化学能,过程Ⅱ中能量转化的形式还是热能转化为化学能,故C错误;铁氧化合物循环制H 以太阳能为
2
热源分解Fe O ,以水和Fe O 为原料,具有成本低的特点,氢气和氧气分步生成,具有产
3 4 3 4
物易分离的优点,故D正确。
5.HBr被O 氧化依次由如下(Ⅰ)、(Ⅱ)、(Ⅲ)三步反应组成,1 mol HBr(g)被氧化为Br (g)放
2 2
出12.67 kJ热量,其能量与反应过程曲线如图所示。
(Ⅰ)HBr(g)+O(g)===HOOBr(g)
2
(Ⅱ)HOOBr(g)+HBr(g)===2HOBr(g)
(Ⅲ)HOBr(g)+HBr(g)===HO(g)+Br (g)
2 2
下列说法正确的是( )
A.三步反应均为放热反应
B.步骤(Ⅰ)的反应速率最慢
C.HOOBr(g)比HBr(g)和O(g)稳定
2
D.热化学方程式为4HBr(g)+O(g)===2HO(g)+2Br (g) ΔH=-12.67 kJ·mol-1
2 2 2
答案 B
解析 放热反应的反应物总能量高于生成物的总能量,根据图像,第一步反应为吸热反应,
A项错误;步骤(Ⅰ)为吸热反应,导致体系温度降低,反应速率减慢,其余反应为放热反应,
反应温度升高,反应速率加快,B项正确;HOOBr(g)的总能量比HBr(g)和O(g)的总能量高,
2
能量越高,物质越不稳定,C项错误;根据题意,1 mol HBr被氧化为Br (g)放出12.67 kJ热
2
量,则热化学方程式为4HBr(g)+O(g)===2HO(g)+2Br (g) ΔH=-50.68 kJ·mol-1,D项
2 2 2
错误。
6.(2020·威海市高三模拟)我国科学家实现了在铜催化剂条件下将DMF[(CH )NCHO]转化为
3 2
三甲胺[N(CH )]。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示,下列说
3 3
法正确的是( )
A.该历程中最小能垒的化学方程式为 (CH)NCH OH*===(CH)NCH +OH*
3 2 2 3 2 2
B.该历程中最大能垒(活化能)为2.16 eV
C.该反应的热化学方程式为(CH)NCHO(g)+2H(g)===N(CH )(g)+HO(g)
3 2 2 3 3 2ΔH=-1.02 eV·mol-1
D.增大压强或升高温度均能加快反应速率,并增大DMF平衡转化率
答案 A
解析 从图中可以看出,在正向进行的三个吸热反应中,其能垒分别为:[-1.23-(-
2.16)]eV=0.93 eV、[-1.55-(-1.77)]eV=0.22 eV、[-1.02-(-2.21)]eV=1.19 eV。从以
上分析知,该历程中最小能垒为0.22 eV,是由(CH)NCH OH*转化为(CH)NCH 的反应,
3 2 2 3 2 2
化学方程式为 (CH)NCH OH*===(CH)NCH +OH*,A正确;该历程中最大能垒(活化能)
3 2 2 3 2 2
为1.19 eV,B不正确;该反应的总反应是由(CH)NCHO(g)转化为N(CH )(g),但1.02 eV
3 2 3 3
为单个(CH)NCHO(g)反应时放出的热量,所以热化学方程式为(CH)NCHO(g)+
3 2 3 2
2H(g)===N(CH )(g)+HO(g) ΔH=-1.02N eV·mol-1,C不正确;增大压强或升高温度
2 3 3 2 A
均能加快反应速率,但升高温度平衡逆向移动,不能增大DMF平衡转化率,D不正确。
7.如图是金属镁和卤素单质(X )反应的能量变化示意图。下列说法正确的是( )
2
A.卤素单质(X )与水反应均可生成两种酸
2
B.用电子式表示MgF 的形成过程:
2
C.热稳定性:MgI >MgBr >MgCl >MgF
2 2 2 2
D.由图可知此温度下MgI (s)与Cl(g)反应的热化学方程式为MgI (s)+Cl(g)===MgCl (s)+
2 2 2 2 2
I(g) ΔH=-277 kJ·mol-1
2
答案 D
解析 F 与水反应生成氢氟酸和 O ,A 项错误;MgF 为离子化合物,其电子式为
2 2 2
,B项错误;物质所具有的能量越低,其热稳定性越强,故热稳定
性:MgF >MgCl >MgBr >MgI ,C 项错误;根据题图可写出热化学方程式 Mg(s)+
2 2 2 2
I(g)===MgI (s) ΔH=-364 kJ·mol-1①和Mg(s)+Cl(g)===MgCl (s) ΔH=-641 kJ·mol-1
2 2 2 2
②,根据盖斯定律,由②-①得MgI (s)+Cl(g)===MgCl (s)+I(g) ΔH=-277 kJ·mol-1,
2 2 2 2
D项正确。
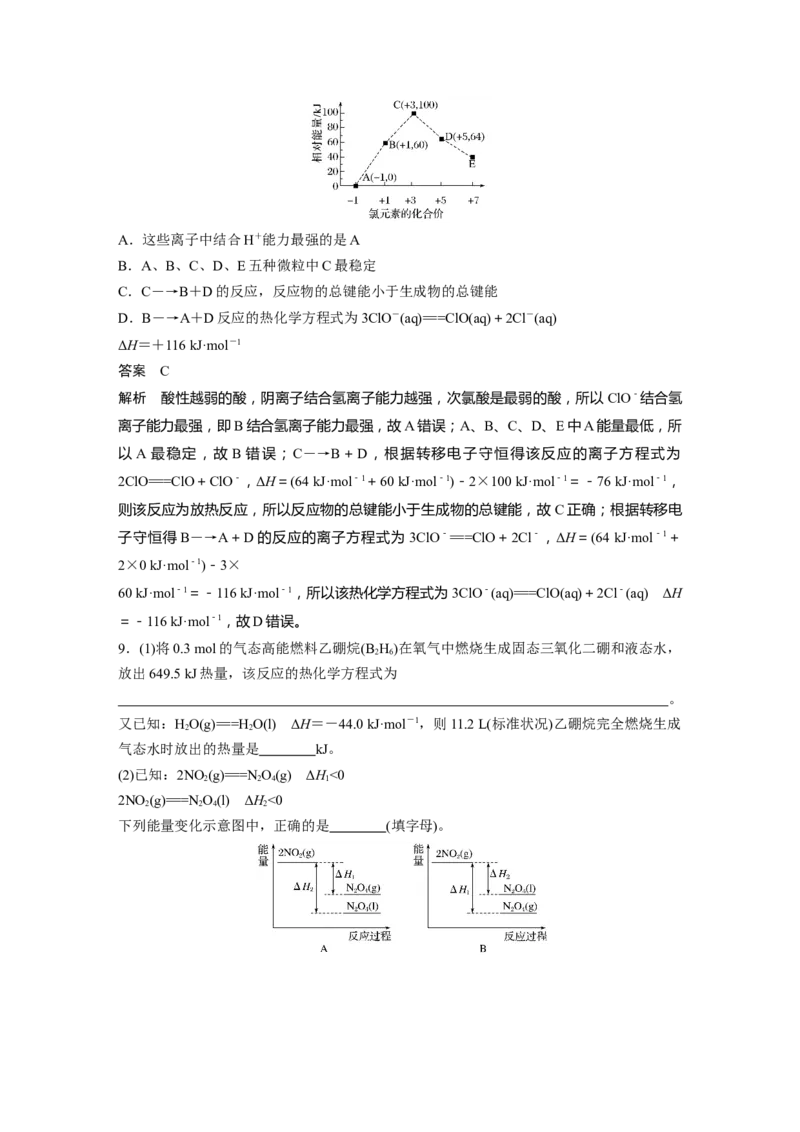
8.(2019·临安昌化中学模拟)一定条件下,在水溶液中1 mol Cl-、ClO(x=1、2、3、4)的能
量(kJ)相对大小如图所示。下列有关说法正确的是( )A.这些离子中结合H+能力最强的是A
B.A、B、C、D、E五种微粒中C最稳定
C.C―→B+D的反应,反应物的总键能小于生成物的总键能
D.B―→A+D反应的热化学方程式为3ClO-(aq)===ClO(aq)+2Cl-(aq)
ΔH=+116 kJ·mol-1
答案 C
解析 酸性越弱的酸,阴离子结合氢离子能力越强,次氯酸是最弱的酸,所以ClO-结合氢
离子能力最强,即B结合氢离子能力最强,故A错误;A、B、C、D、E中A能量最低,所
以 A 最稳定,故 B 错误;C―→B+D,根据转移电子守恒得该反应的离子方程式为
2ClO===ClO+ClO-,ΔH=(64 kJ·mol-1+60 kJ·mol-1)-2×100 kJ·mol-1=-76 kJ·mol-1,
则该反应为放热反应,所以反应物的总键能小于生成物的总键能,故C正确;根据转移电
子守恒得B―→A+D的反应的离子方程式为 3ClO-===ClO+2Cl-,ΔH=(64 kJ·mol-1+
2×0 kJ·mol-1)-3×
60 kJ·mol-1=-116 kJ·mol-1,所以该热化学方程式为3ClO-(aq)===ClO(aq)+2Cl-(aq) ΔH
=-116 kJ·mol-1,故D错误。
9.(1)将0.3 mol的气态高能燃料乙硼烷(B H)在氧气中燃烧生成固态三氧化二硼和液态水,
2 6
放出649.5 kJ热量,该反应的热化学方程式为
。
又已知:HO(g)===HO(l) ΔH=-44.0 kJ·mol-1,则11.2 L(标准状况)乙硼烷完全燃烧生成
2 2
气态水时放出的热量是 kJ。
(2)已知:2NO (g)===NO(g) ΔH<0
2 2 4 1
2NO (g)===NO(l) ΔH<0
2 2 4 2
下列能量变化示意图中,正确的是 (填字母)。(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(石墨,s)+O(g)===CO(g)
2 2
ΔH=-393.5 kJ·mol-1
1
2H(g)+O(g)===2HO(l)
2 2 2
ΔH=-571.6 kJ·mol-1
2
2C H(g)+5O(g)===4CO(g)+2HO(l)
2 2 2 2 2
ΔH=-2 599 kJ·mol-1
3
根据盖斯定律,计算298 K时由C(石墨,s)和H(g)生成1 mol C H(g)反应的焓变(列出简单
2 2 2
的计算式):
。
(4)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H 化合来制备甲醇气体(结构简式
2
为CHOH)。
3
部分化学键的键能数据如下表:
化学键 C—C C—H H—H C—O C≡O H—O
键能/kJ·mol-1 348 413 436 358 1 072 463
已知CO中的C与O之间为三键连接,则工业制备甲醇的热化学方程式为
。
答案 (1)B H(g)+3O(g)===B O(s)+3HO(l) ΔH=-2 165 kJ·mol-1 1 016.5 (2)A
2 6 2 2 3 2
(3)[(-393.5)×4+(-571.6)-(-2 599)]×kJ·mol-1=+226.7 kJ·mol-1
(4)CO(g)+2H(g)===CHOH(g) ΔH=-116 kJ·mol-1
2 3
解析 (1)0.3 mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出
649.5 kJ的热量,则1 mol气态高能燃料乙硼烷在氧气中燃烧生成固态三氧化二硼和液态水,
放出2 165 kJ的热量,反应的热化学方程式为B H(g)+3O(g)===B O(s)+3HO(l)
2 6 2 2 3 2
ΔH=-2 165 kJ·mol-1。
①B H(g)+3O(g)===B O(s)+3HO(l)
2 6 2 2 3 2
ΔH=-2 165 kJ·mol-1
②HO(l)===HO(g) ΔH=+44.0 kJ·mol-1
2 2
根据盖斯定律,由①+②×3得B H(g)+3O(g)===B O(s)+3HO(g) ΔH=-2 033 kJ·mol-
2 6 2 2 3 2
1,11.2 L(标准状况)即0.5 mol乙硼烷完全燃烧生成气态水时放出的热量是 2 033 kJ×0.5
=1 016.5 kJ。
(2)由题给信息可知,ΔH<0,ΔH<0,两个反应均为放热反应,所以反应物的总能量比生成
1 2
物的总能量高;同种物质气态变成液态会放出热量,即液态时能量比气态时能量低,则
NO(l)具有的能量比NO(g)具有的能量低,A符合。
2 4 2 4
(3)已知:①C(石墨,s)+O(g)===CO(g)
2 2
ΔH=-393.5 kJ·mol-1
1
②2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ·mol-1
2 2 2 2
③2C H(g)+5O(g)===4CO(g)+2HO(l) ΔH=-2 599 kJ·mol-1
2 2 2 2 2 3
根据盖斯定律,由(①×4+②-③)×得到反应的热化学方程式为 2C(石墨,s)+
H(g)===C H(g) ΔH=(4ΔH+ΔH-ΔH)×=[(-393.5)×4+(-571.6)-(-2 599)]×
2 2 2 1 2 3
kJ·mol-1=+226.7 kJ·mol-1。
(4)CO(g)+2H(g)===CHOH(g),焓变=反应物总键能-生成物总键能,依据题表中提供的
2 3
化学键的键能计算得ΔH=1 072 kJ·mol-1+2×436 kJ·mol-1-(3×413 kJ·mol-1+358 kJ·mol-
1+463 kJ·mol-1)=-116 kJ·mol-1,则热化学方程式为CO(g)+2H(g)===CHOH(g) ΔH=
2 3
-116 kJ·mol-1。