文档内容
专项提能特训 14 弱电解质电离常数计算与图像分析
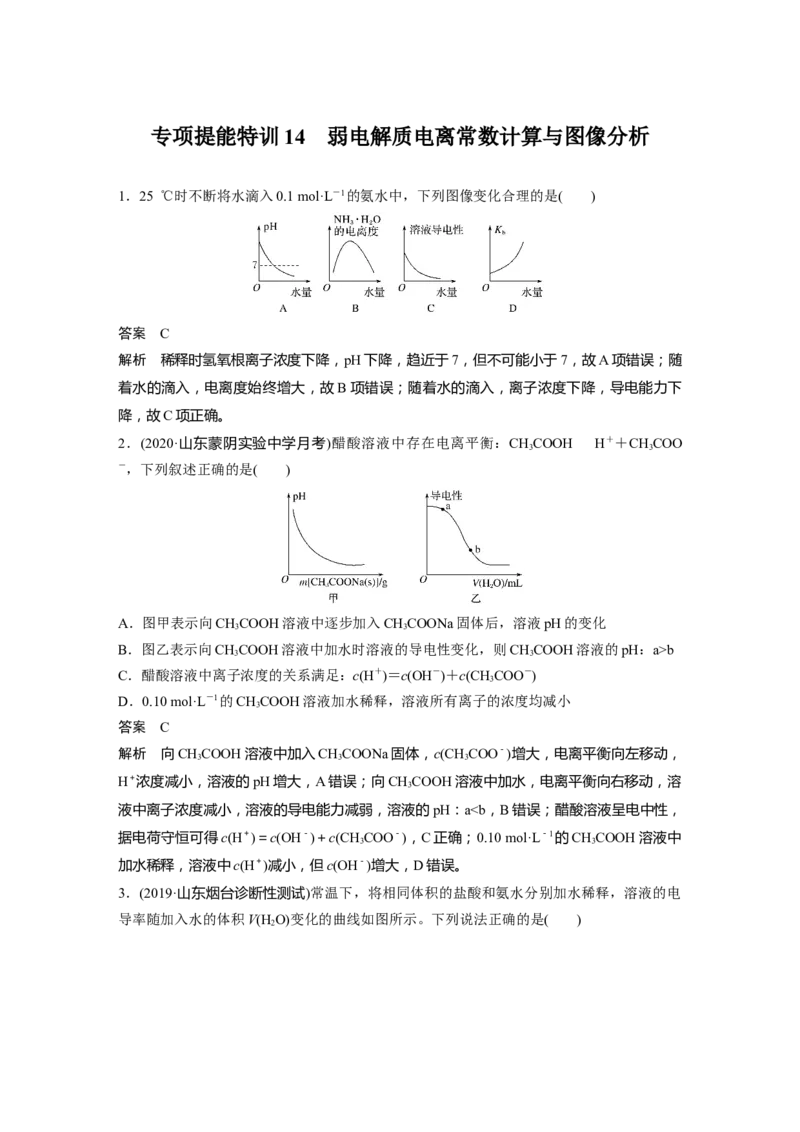
1.25 ℃时不断将水滴入0.1 mol·L-1的氨水中,下列图像变化合理的是( )
答案 C
解析 稀释时氢氧根离子浓度下降,pH下降,趋近于7,但不可能小于7,故A项错误;随
着水的滴入,电离度始终增大,故B项错误;随着水的滴入,离子浓度下降,导电能力下
降,故C项正确。
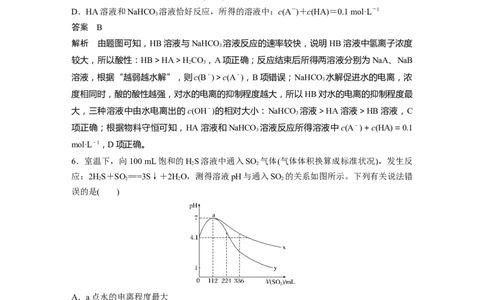
2.(2020·山东蒙阴实验中学月考)醋酸溶液中存在电离平衡:CHCOOHH++CHCOO
3 3
-,下列叙述正确的是( )
A.图甲表示向CHCOOH溶液中逐步加入CHCOONa固体后,溶液pH的变化
3 3
B.图乙表示向CHCOOH溶液中加水时溶液的导电性变化,则CHCOOH溶液的pH:a>b
3 3
C.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CHCOO-)
3
D.0.10 mol·L-1的CHCOOH溶液加水稀释,溶液所有离子的浓度均减小
3
答案 C
解析 向CHCOOH溶液中加入CHCOONa固体,c(CHCOO-)增大,电离平衡向左移动,
3 3 3
H+浓度减小,溶液的pH增大,A错误;向CHCOOH溶液中加水,电离平衡向右移动,溶
3
液中离子浓度减小,溶液的导电能力减弱,溶液的pH:ab>c,B项正确;
a、b两点溶液混合后的溶质为NH Cl和过量的NH ·H O,C项错误;稀释过程中,NH ·H O
4 3 2 3 2
电离平衡向右移动,增大,D项错误。
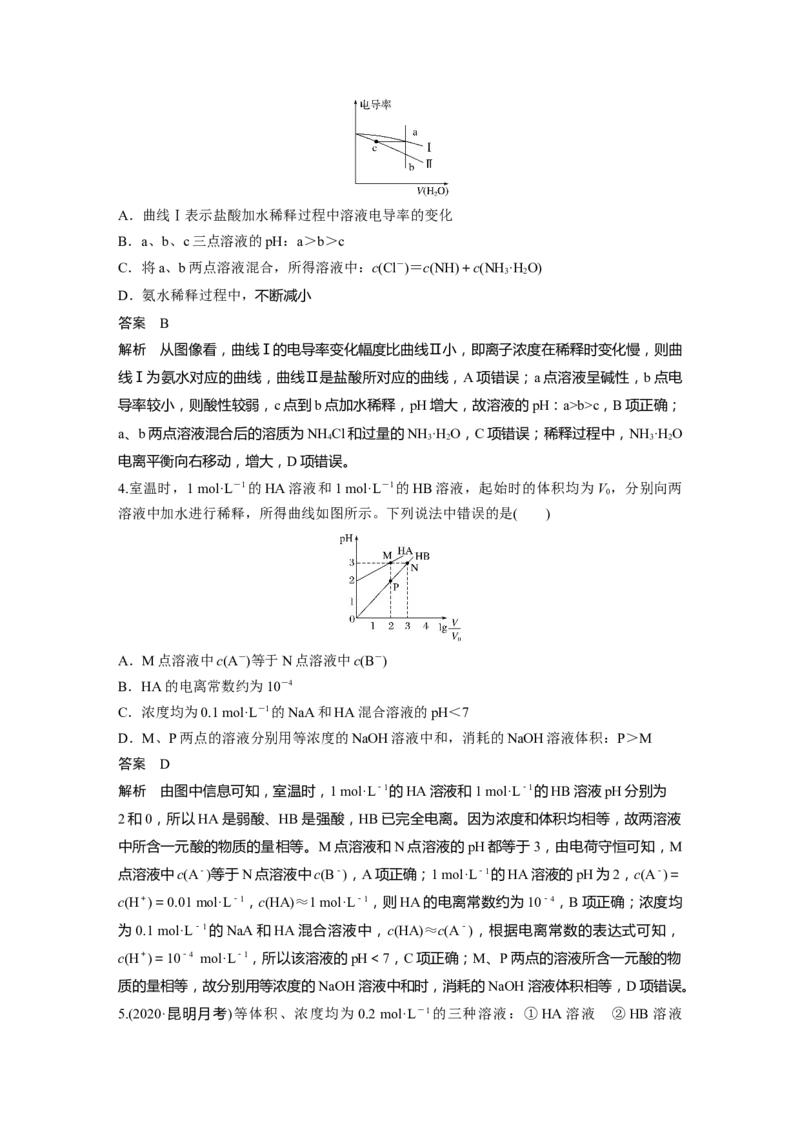
4.室温时,1 mol·L-1的HA溶液和1 mol·L-1的HB溶液,起始时的体积均为V ,分别向两
0
溶液中加水进行稀释,所得曲线如图所示。下列说法中错误的是( )
A.M点溶液中c(A-)等于N点溶液中c(B-)
B.HA的电离常数约为10-4
C.浓度均为0.1 mol·L-1的NaA和HA混合溶液的pH<7
D.M、P两点的溶液分别用等浓度的NaOH溶液中和,消耗的NaOH溶液体积:P>M
答案 D
解析 由图中信息可知,室温时,1 mol·L-1的HA溶液和1 mol·L-1的HB溶液pH分别为
2和0,所以HA是弱酸、HB是强酸,HB已完全电离。因为浓度和体积均相等,故两溶液
中所含一元酸的物质的量相等。M点溶液和N点溶液的pH都等于3,由电荷守恒可知,M
点溶液中c(A-)等于N点溶液中c(B-),A项正确;1 mol·L-1的HA溶液的pH为2,c(A-)=
c(H+)=0.01 mol·L-1,c(HA)≈1 mol·L-1,则HA的电离常数约为10-4,B项正确;浓度均
为0.1 mol·L-1的NaA和HA混合溶液中,c(HA)≈c(A-),根据电离常数的表达式可知,
c(H+)=10-4 mol·L-1,所以该溶液的pH<7,C项正确;M、P两点的溶液所含一元酸的物
质的量相等,故分别用等浓度的NaOH溶液中和时,消耗的NaOH溶液体积相等,D项错误。
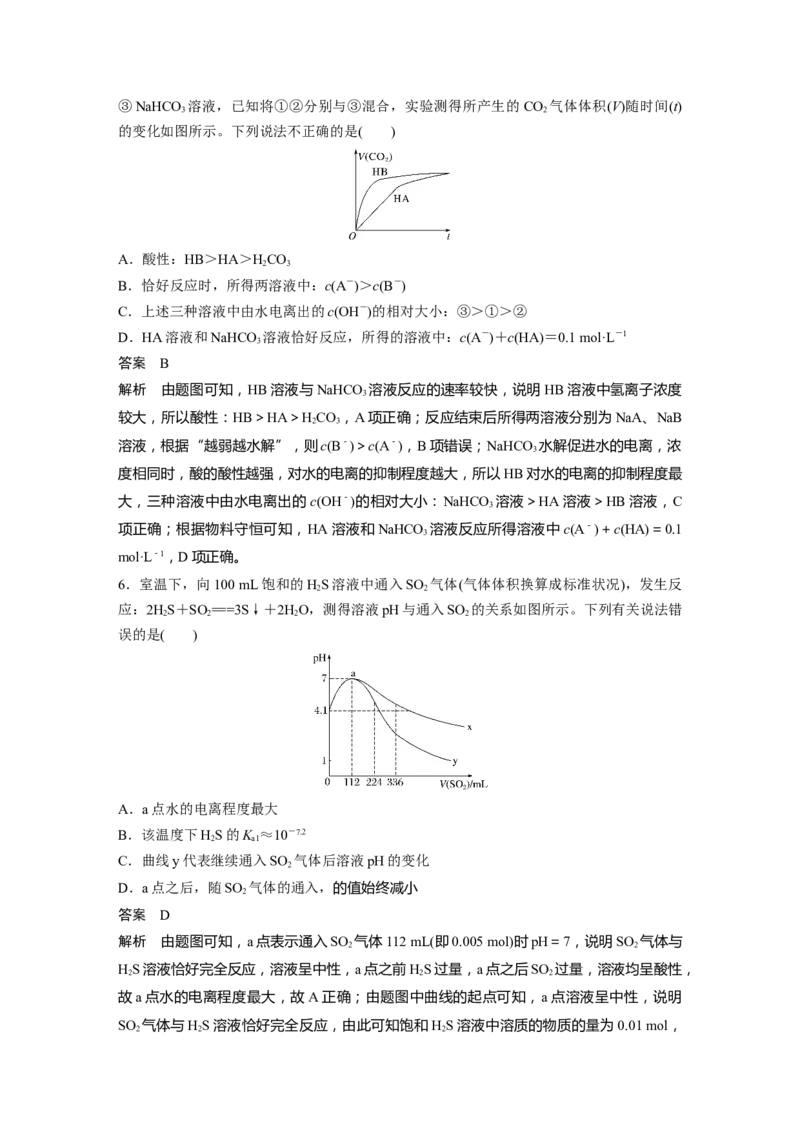
5.(2020·昆明月考)等体积、浓度均为 0.2 mol·L-1的三种溶液:①HA溶液 ②HB溶液③NaHCO 溶液,已知将①②分别与③混合,实验测得所产生的CO 气体体积(V)随时间(t)
3 2
的变化如图所示。下列说法不正确的是( )
A.酸性:HB>HA>HCO
2 3
B.恰好反应时,所得两溶液中:c(A-)>c(B-)
C.上述三种溶液中由水电离出的c(OH-)的相对大小:③>①>②
D.HA溶液和NaHCO 溶液恰好反应,所得的溶液中:c(A-)+c(HA)=0.1 mol·L-1
3
答案 B
解析 由题图可知,HB溶液与NaHCO 溶液反应的速率较快,说明HB溶液中氢离子浓度
3
较大,所以酸性:HB>HA>HCO ,A项正确;反应结束后所得两溶液分别为NaA、NaB
2 3
溶液,根据“越弱越水解”,则c(B-)>c(A-),B项错误;NaHCO 水解促进水的电离,浓
3
度相同时,酸的酸性越强,对水的电离的抑制程度越大,所以HB对水的电离的抑制程度最
大,三种溶液中由水电离出的 c(OH-)的相对大小:NaHCO 溶液>HA溶液>HB溶液,C
3
项正确;根据物料守恒可知,HA溶液和NaHCO 溶液反应所得溶液中c(A-)+c(HA)=0.1
3
mol·L-1,D项正确。
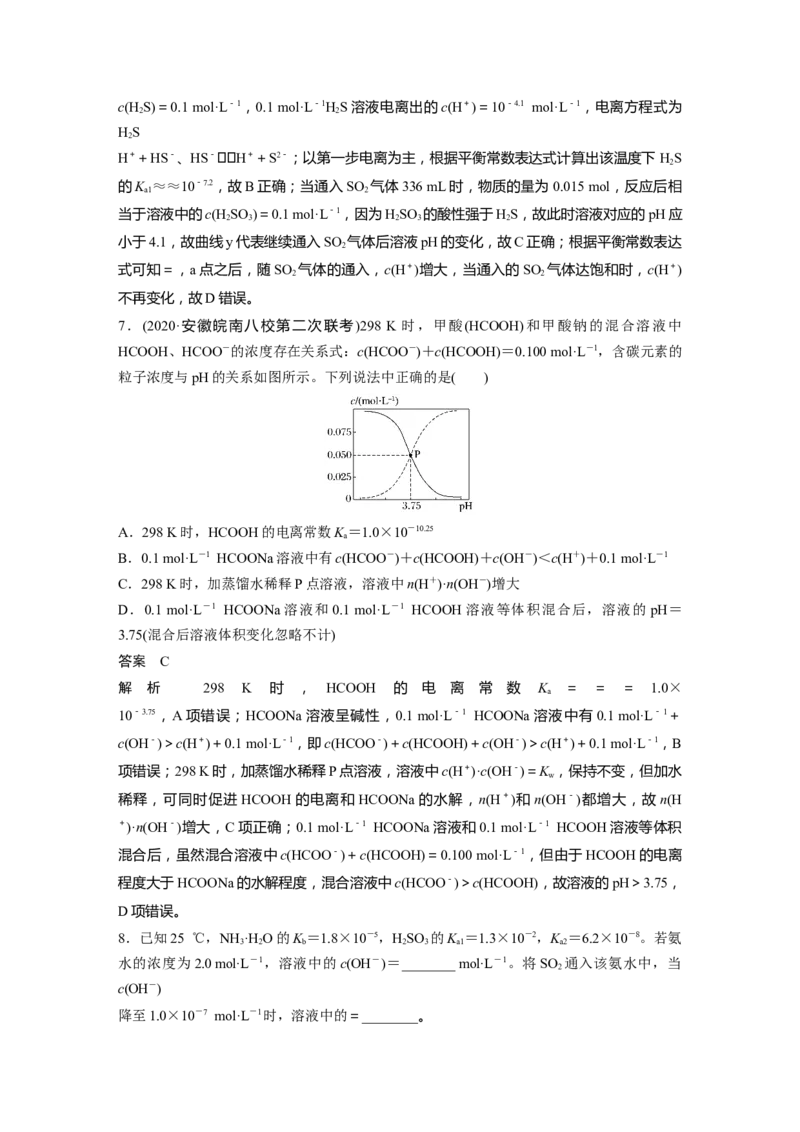
6.室温下,向100 mL饱和的HS溶液中通入SO 气体(气体体积换算成标准状况),发生反
2 2
应:2HS+SO ===3S↓+2HO,测得溶液pH与通入SO 的关系如图所示。下列有关说法错
2 2 2 2
误的是( )
A.a点水的电离程度最大
B.该温度下HS的K ≈10-7.2
2 a1
C.曲线y代表继续通入SO 气体后溶液pH的变化
2
D.a点之后,随SO 气体的通入,的值始终减小
2
答案 D
解析 由题图可知,a点表示通入SO 气体112 mL(即0.005 mol)时pH=7,说明SO 气体与
2 2
HS溶液恰好完全反应,溶液呈中性,a点之前HS过量,a点之后SO 过量,溶液均呈酸性,
2 2 2
故a点水的电离程度最大,故A正确;由题图中曲线的起点可知,a点溶液呈中性,说明
SO 气体与HS溶液恰好完全反应,由此可知饱和HS溶液中溶质的物质的量为0.01 mol,
2 2 2c(H S)=0.1 mol·L-1,0.1 mol·L-1HS溶液电离出的c(H+)=10-4.1 mol·L-1,电离方程式为
2 2
HS
2
H++HS-、HS-H++S2-;以第一步电离为主,根据平衡常数表达式计算出该温度下 HS
2
的K ≈≈10-7.2,故B正确;当通入SO 气体336 mL时,物质的量为0.015 mol,反应后相
a1 2
当于溶液中的c(H SO )=0.1 mol·L-1,因为HSO 的酸性强于HS,故此时溶液对应的pH应
2 3 2 3 2
小于4.1,故曲线y代表继续通入SO 气体后溶液pH的变化,故C正确;根据平衡常数表达
2
式可知=,a点之后,随SO 气体的通入,c(H+)增大,当通入的SO 气体达饱和时,c(H+)
2 2
不再变化,故D错误。
7.(2020·安徽皖南八校第二次联考)298 K 时,甲酸(HCOOH)和甲酸钠的混合溶液中
HCOOH、HCOO-的浓度存在关系式:c(HCOO-)+c(HCOOH)=0.100 mol·L-1,含碳元素的
粒子浓度与pH的关系如图所示。下列说法中正确的是( )
A.298 K时,HCOOH的电离常数K=1.0×10-10.25
a
B.0.1 mol·L-1 HCOONa溶液中有c(HCOO-)+c(HCOOH)+c(OH-)<c(H+)+0.1 mol·L-1
C.298 K时,加蒸馏水稀释P点溶液,溶液中n(H+)·n(OH-)增大
D.0.1 mol·L-1 HCOONa溶液和0.1 mol·L-1 HCOOH溶液等体积混合后,溶液的 pH=
3.75(混合后溶液体积变化忽略不计)
答案 C
解 析 298 K 时 , HCOOH 的 电 离 常 数 K = = = 1.0×
a
10-3.75,A项错误;HCOONa溶液呈碱性,0.1 mol·L-1 HCOONa溶液中有0.1 mol·L-1+
c(OH-)>c(H+)+0.1 mol·L-1,即c(HCOO-)+c(HCOOH)+c(OH-)>c(H+)+0.1 mol·L-1,B
项错误;298 K时,加蒸馏水稀释P点溶液,溶液中c(H+)·c(OH-)=K ,保持不变,但加水
w
稀释,可同时促进HCOOH的电离和HCOONa的水解,n(H+)和n(OH-)都增大,故n(H
+)·n(OH-)增大,C项正确;0.1 mol·L-1 HCOONa溶液和0.1 mol·L-1 HCOOH溶液等体积
混合后,虽然混合溶液中c(HCOO-)+c(HCOOH)=0.100 mol·L-1,但由于HCOOH的电离
程度大于HCOONa的水解程度,混合溶液中c(HCOO-)>c(HCOOH),故溶液的pH>3.75,
D项错误。
8.已知25 ℃,NH ·H O的K =1.8×10-5,HSO 的K =1.3×10-2,K =6.2×10-8。若氨
3 2 b 2 3 a1 a2
水的浓度为2.0 mol·L-1,溶液中的c(OH-)=________ mol·L-1。将SO 通入该氨水中,当
2
c(OH-)
降至1.0×10-7 mol·L-1时,溶液中的=________。答案 6.0×10-3 0.62
解析 由NH ·H O的电离方程式及其电离平衡常数K =1.8×10-5可知,K ==1.8×10-5,
3 2 b b
当氨水的浓度为2.0 mol·L-1时,溶液中的c(NH)=c(OH-)=6.0×10-3 mol·L-1。由HSO 的
2 3
第二步电离方程式HSOSO+ H+及其电离平衡常数K =6.2×10-8可知,K ==6.2×10
a2 a2
-8,将SO 通入该氨水中,当c(OH-)降至1.0×10-7 mol·L-1时,溶液的c(H+)=1.0×10-7
2
mol·L-1,则==0.62。
9.联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的平衡常数值为
__________(已知:NH +H+NH的K=8.7×107;K =1.0×10-14)。联氨与硫酸形成的
2 4 2 w
酸式盐的化学式为________________________________。
答案 8.7×10-7 NH(HSO )
2 6 4 2
解析 联氨为二元弱碱,在水中的电离方式与氨相似,则联氨第一步电离的方程式为 NH
2 4
+HONH+OH-,再根据已知:NH +H+NH的K=8.7×107及K =1.0×10-14,故
2 2 2 4 2 w
联氨第一步电离平衡常数为K====K·K =8.7×107×1.0×10-14=8.7×10-7;联氨为二元
w
弱碱,酸碱发生中和反应生成盐,则联氨与硫酸形成酸式盐的化学式为NH(HSO )。
2 6 4 2