文档内容
离子反应 达标检测
一、单项选择题:共12小题,每小题2分,共24分。每小题只有一个选项符合题意。
1.钠元素在自然界中分布很广,储量极为丰富。金属钠的性质活泼,可与 等物质反
应,钠的化合物 等在生产、生活中应用广泛。
下列物质不属于电解质的是 ( )
A.Na B. C. D.NaOH
2.下列物质溶于水不能导电的是( )
A. B. C. D.
3.下列物质在水溶液中的电离方程式错误的是( )
A. B.
C. D.
4.下列离子方程式中,书写正确的是 ( )
A. 稀硫酸和铁的反应:2Fe+6H+=2Fe3++3H ↑
2
B. 盐酸和碳酸氢钠溶液反应:2H++ =H O+CO↑
2 2
C. 硫酸铜和氢氧化钡溶液反应: +Ba2+=BaSO ↓
4
D. 铁片插入硫酸铜溶液:Fe+Cu2+=Fe2++Cu
5.下列反应属于离子反应的是( )
A.高锰酸钾加热分解制取 B. 和 反应生成
C.Zn片投入稀硫酸溶液中 D. 遇HCl气体生成白烟( )
6.下列离子组能大量共存的是( )
A. B.
C. D.
7.粗盐水过滤后仍含有可溶性的 、 、 等杂质,通过以下几个实验步
骤可以除去这些杂质:
①加入稍过量的 溶液;
②加入稍过量的 溶液;
③加入稍过量的 溶液;
④滴入稀盐酸至无气泡产生;
⑤过滤。
正确的操作顺序是( )A.③②①⑤④ B.②③①④⑤ C.①③②⑤④ D.③⑤②①④
8.用食用白醋(醋酸浓度约为1 mol/L)进行下列实验,能证明醋酸为弱电解质的是( )
A.白醋中滴入石蕊试液呈红色 B.白醋加入豆浆中有沉淀产生
C.蛋壳浸泡在白醋中有气体放出 D.pH试纸显示醋酸的pH为2~3
9.下列关于电解质的说法正确的是( )
A. 在水溶液中难导电,但熔融状态下能导电,所以 是电解质
B. 溶于水形成的溶液能导电,所以 是电解质
C. 溶于水能导电,所以 是电解质
D.纯硫酸不导电,所以硫酸不是电解质
10.室温时,下列有关电解质的说法正确的是( )
pH相等的 和HCN两种酸溶液中,
A.
B. NaHB溶液呈酸性,可推知 在水中不能完全电离
C. 往 溶液中加入镁粉,可生成两种气体
D. 溶液中通入 所得的中性溶液中:
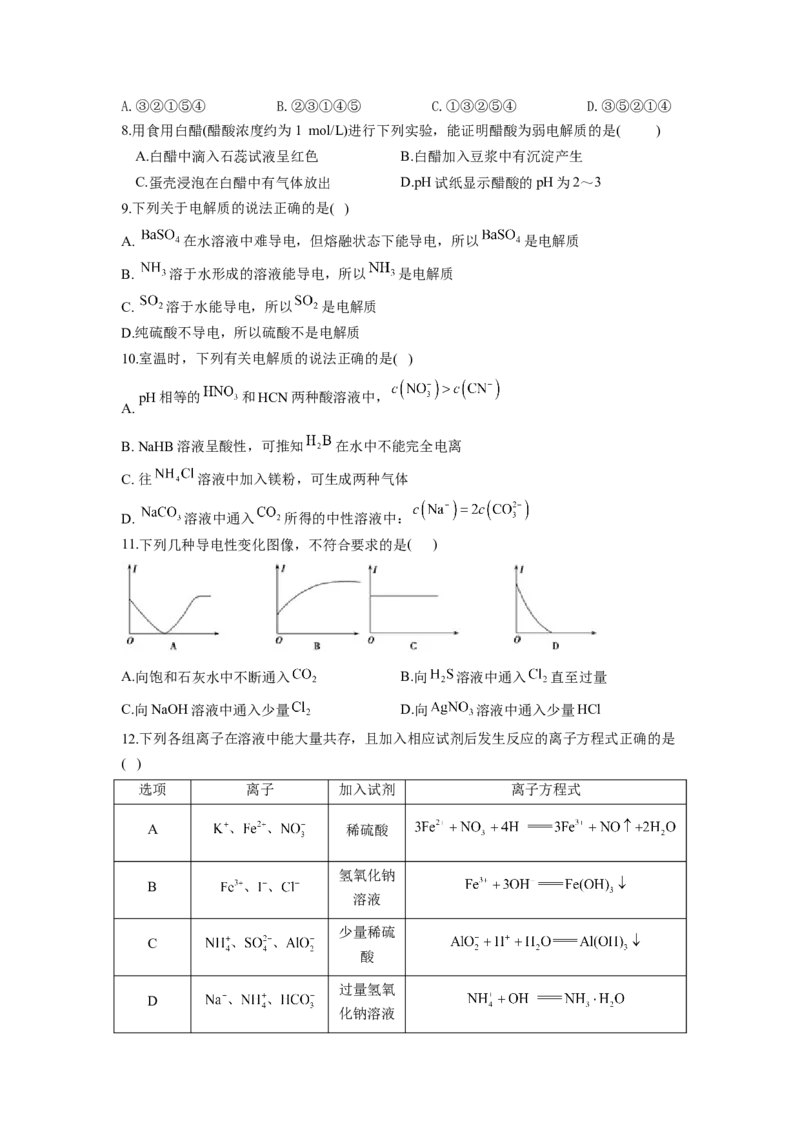
11.下列几种导电性变化图像,不符合要求的是( )
A.向饱和石灰水中不断通入 B.向 溶液中通入 直至过量
C.向NaOH溶液中通入少量 D.向 溶液中通入少量HCl
12.下列各组离子在溶液中能大量共存,且加入相应试剂后发生反应的离子方程式正确的是
( )
选项 离子 加入试剂 离子方程式
A 稀硫酸
氢氧化钠
B
溶液
少量稀硫
C
酸
过量氢氧
D
化钠溶液A.A B.B C.C D.D
二、多项选择题:共5小题,每小题4分,共20分。每小题有多个选项符合题意,全部选
对得4分,选对但不全的得2分,有选错的得0分。
13.下列说法中不正确的是( )
A.在标准状况下22.4L H 中含有的氢分子的个数为N
2 A
-
B.1L1mol/L的KClO 溶液中含有的Cl 个数为N
3 A
C.凡是溶于水能导电的化合物就是电解质
D.某溶液中滴加烧碱溶液,加热产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定
+
存在NH
4
14.下列离子方程式正确的是( )
A. 通入冷的NaOH溶液:
B.用醋酸和淀粉-KI溶液检验加碘盐中的 :
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合:
15.下列有关离子共存或离子方程式的叙述正确的是( )
A. 不能大量共存
B. 能大量共存
C. 溶于氢碘酸:
D.将过量的铁溶入稀硝酸中:
16.除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作方法均正确的一组是(
)
选项 待提纯的物质 选用试剂 操作方法
A 无 加热分解
溶解、过滤、洗
B 稀盐酸
涤、干燥
C 氢氧化钠溶液 过滤
D 氧气 点燃
A.A B.B C.C D.D
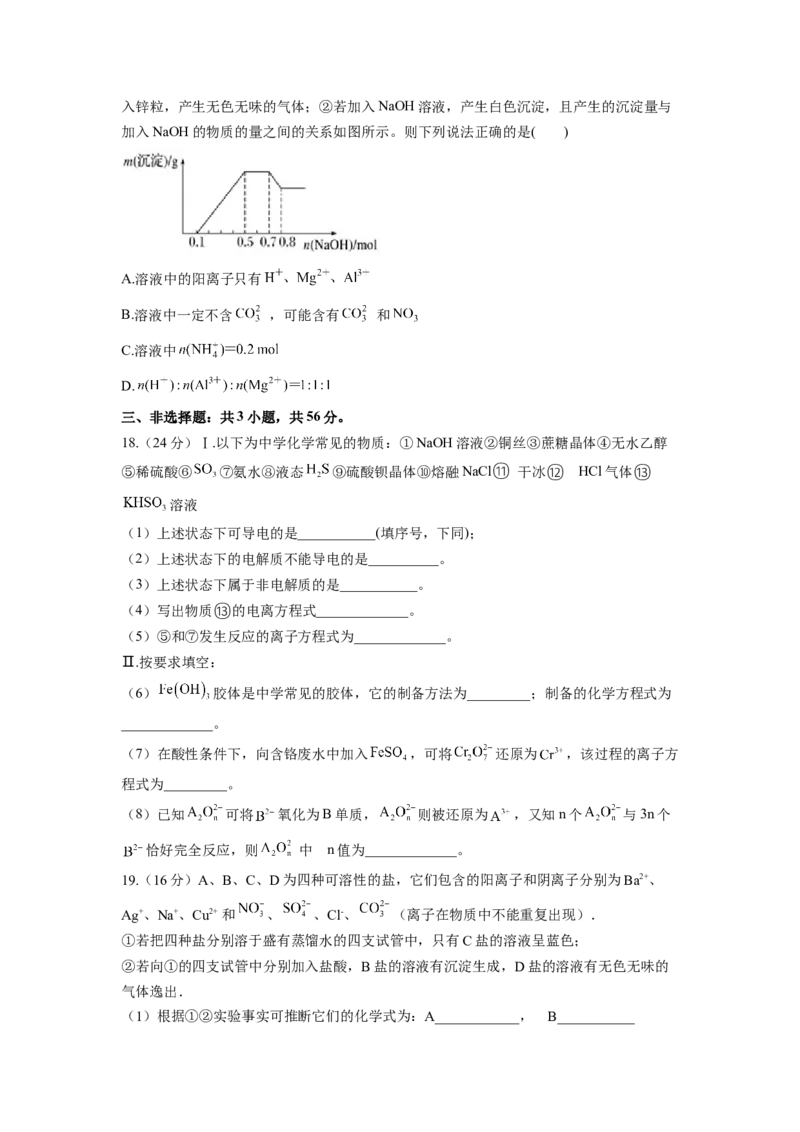
17.某溶液中可能含有 中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与
加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
A.溶液中的阳离子只有
B.溶液中一定不含 ,可能含有 和
C.溶液中
D.
三、非选择题:共3小题,共56分。
18.(24分)Ⅰ.以下为中学化学常见的物质:①NaOH溶液②铜丝③蔗糖晶体④无水乙醇
⑤稀硫酸⑥ ⑦氨水⑧液态 ⑨硫酸钡晶体⑩熔融NaCl⑪ 干冰⑫ HCl气体⑬
溶液
(1)上述状态下可导电的是___________(填序号,下同);
(2)上述状态下的电解质不能导电的是__________。
(3)上述状态下属于非电解质的是___________。
(4)写出物质⑬的电离方程式_____________。
(5)⑤和⑦发生反应的离子方程式为_____________。
Ⅱ.按要求填空:
(6) 胶体是中学常见的胶体,它的制备方法为_________;制备的化学方程式为
_____________。
(7)在酸性条件下,向含铬废水中加入 ,可将 还原为 ,该过程的离子方
程式为_________。
(8)已知 可将 氧化为B单质, 则被还原为 ,又知n个 与3n个
恰好完全反应,则 中 的n值为_____________。
19.(16分)A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、
Ag+、Na+、Cu2+ 和 、 、Cl-、 (离子在物质中不能重复出现).
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的
气体逸出.
(1)根据①②实验事实可推断它们的化学式为:A____________, B___________(2)写出醋酸与D反应的离子方程式:________________
(3)将含相同物质的量A、B、C的溶液混合后,写出溶液中存在的离子的物质的量之比
____________;在此溶液中加入锌粒,写出发生反应的离子方程式:
________________________
(4)C溶液中阴离子的检验方法:_________________________
20.(16分)常温下, 的某溶液中可能有
中的某几种,现取100mL该溶液进行如图实验。
已知:单质碘是紫黑色固体,且氧化性 。
根据上述实验,回答下列问题:
(1)步骤①的实验操作名称是_________,步骤①中生成紫黑色固体单质的离子方程式是
_________。
(2)此溶液中_________(填“是”或“否”)存在 。若存在,则其物质的量浓度为
_________(若不存在,此问不作答)
(3)该溶液中一定不存在的离子有_________。
(4)根据整个实验过程推断 是否存在并说明理由。_________。若存在,计算其物质
的量浓度_________。(若不存在,此问不作答)
答案以及解析
1.答案:A
解析:A.钠是单质,既不是电解质也不是非电解质,故A正确;
B氧化钠在熔融状态下能导电,属于电解质,故B错误;
C. 在水溶液中能导电,属于电解质,故C错误;
D. NaOH在水溶液中能导电,属于电解质,故D错误;
故选: A.
2.答案:A
解析:A.乙醇属于非电解质,溶于水不导电,故A正确;
B.硝酸钾溶于水电离生成离子,可以导电,故B错误;
C.氢氧化钡属于电解质,溶于水可导电,故C错误;
D.氯气既不是电解质,也不是非电解质,但是氯气溶于水会生成氯化氢和次氯酸,属于电解质,能导电,故D错误;
故选: A。
3.答案:D
解析:A.氯化钙为强电解质,电离方程式为: ,故A正确; B.硫酸
氢钠为强电解质,在水中完全电离,电离方程式: ,故B正确;
C.硝酸为强电解质,电离方程式为: ,故C正确; D.氯酸钾为强电
解质,电离方程式: ,故D错误;故选:D.
4.答案:D
解析:A.稀硫酸和铁的反应的离子反应为 ,故A错误; B.盐酸和
碳酸氢钠溶液反应的离子反应为 ,故B错误;C.硫酸铜和氢
氧化钡溶液反应的离子反应为 ,故C
错误; D.铁片插入硫酸铜溶液的离子反应为 ,故D正确;故选:D
5.答案:C
解析:凡是有离子参加的反应都是离子反应。常见的有电解质在水溶液中进行的反应。A
项中 加热分解也不属于离子反应;B、D项是分子间的反应。
6.答案:C
解析: 和 不能大量共存,A项错误; 可氧化 ,B项错误; 和 不
能大量共存,D项错误。
7.答案:A
解析: 加入稍过量的 溶液除去 →加入稍过量的 溶液除去 →加入
稍过量的 溶液除去 和过量的 ,然后过滤除去沉淀,得到 、
、 的混合溶液,最后加入适量盐酸除去 、 即可,故选项A符
合。
8.答案:D
解析:
9.答案:A解析:
10.答案:C
解析:本题考查弱电解质的电离平衡、水解平衡。pH相等的 和HCN两种酸溶液中,
相等,根据电荷守恒可知 ,A项错误;NaHB溶液呈酸性,可能
是 ,对应的 在水中能完全电离,B项错误; 溶液中 水解生成
和 ,加入镁粉,镁粉与 反应生成 ,会促进 水解,生成的
较多时会转化为 ,C项正确; 溶液中通入 ,溶液中存在电荷守
恒关系: ,溶液呈中性时,
,则 ,D项错误。
11.答案:D
解析:A.向饱和石灰水中不断通入 ,先生成 沉淀,使溶液的导电性降低,
再和 反应生成可溶于水的 ,使溶淩的导电性增大,A项正确; B.
向 溶液中通入 直至过量,先是反应得到盐酸和硫单质,盐酸是强酸,所以导电性
增强,继续通入氯气得到氯水,溶液的导电性变化不大,B项正确; C.
,向NaOH溶液中通入少里a,反应前后离子浓度不
变,溶液的导电性不变,C项正确;向 溶液通入少里HCl,发生反应生成氯化银沉
淀和硝酸,减少的银离子由氢离子补充,濬液中度基本不变,导电性基本不变,D项错误;
D
12.答案:A
解析:反应符合事实,遵循物质拆分原则,A符合题意; 会发生氧化还原反应,
产生 ,不能大量共存,B不符合题意; 会发生盐的相互促进的水解反
应,不能大量共存,C不符合题意;过量NaOH电离产生的 与 反应产生
;与 反应产生 ,反应不符合事实,D不符合题意。
13.答案:BC
解析:A、在标准状况下22.4LH 的物质的量=22.4L÷22.4L/mol=1mol,因此分子中含有的
2
+ -
氢分子的个数为N ,A正确;B、氯酸钾溶于水不能电离出氯离子,而是K 与ClO ,所以选
A 3
项B不正确;C、溶于水或在熔融状态下能够自身电离出离子的化合物是电解质,因此溶于水
能导电的化合物不一定是电解质,例如SO 等是非电解质,C不正确;D、某溶液中滴加烧碱溶
2
液,加热产生能使湿润的红色石蕊试纸变蓝的气体,该气体一定是氨气,则原溶液中一定存在
+
NH ,D正确,答案选BC。
4
14.答案:AC
解析:15.答案:AD
解析:A. 具有强氧化性,可氧化具有还原性的 ,两者不能大量共存,A正确B.
与 会发生反应,不能大量共存,B错误; C.氢碘酸除了具有酸性,其中碘离子
还具有还原性, 溶于氢碘酸生成的铁离子会继续与碘离子发生氧化还原反应,C
错误; D.将过量的铁溶入稀硝酸中会生成硝酸亚铁NO和水,反应的离子方程式为:
,D正确;故选AD。
16.答案:AB
解析: 受热分解得到CaO,故A项正确;在混合物中加入盐酸,氧化铜会与盐酸反
应而溶解,铜不与盐酸反应,过滤后再进行洗涤、干燥即可得到铜,故B项正确;混合物
中加入氢氧化钠,氢氧化钠既会与硫酸反应,也会与硫酸铜反应,杂质除去了, 也
除去了,故C项错误;一氧化碳可以在氧气中燃烧,故D项错误。
17.答案:AB
解析:根据①可知,溶液显酸性,则溶液中一定不存在 和 ;根据②可知,产生
的是白色沉淀,说明不存在 ;根据产生的沉淀量与加入NaOH的物质的量之间的关系
图可知,溶液中一定含有 ;又因为当沉淀达到最大值时,继续加入氢氧化钠,
沉淀不变,这说明溶液中还存在 ,根据溶液电中性可知,溶液中一定存在阴离子
;根据图象可知,第一阶段为氢离子与氢氧化钠反应,消耗氢氧化钠为0.1mol,则
;第三阶段为铵根离子与氢氧化钠反应,消耗氢氧化钠为
0.7mol-0.5mol=0.2mol,则 ;最后阶段为氢氧化钠溶解氢氧化铝,消耗氢
氧化钠0.8mol-0.7mol=0.1mol,则 ,根据铝元素守恒可知
;第二阶段为氢氧化钠沉淀镁离子、铝离子,共消耗氢氧化钠为
0.5mol-0.1mol=0.4mol,则 ,A.由上述分析可
知,溶液中的阳离子只有 ,故A正确。B.第三阶段为铵根离子与氢
氧化钠反应,消耗氢氧化钠为0.7mol-0.5mol=0.2mol,则 ,故B正确;
C.由上述分析可知,溶液中一定不含 ,溶液中一定存在阴离子 ,故C错
误; D.由上述分析可知,溶液中
,故D错误;故选AB.18.答案:(1)①②⑤⑦⑩⑬
(2)⑧⑨⑫
(3)③④⑥⑪
(4)
(5)
(6)向沸水中逐滴加入5-6滴饱和 溶液,继续煮沸至液体呈红褐色,停止加热,可得到
胶体;
(7)
(8)7
解析:①NaOH溶液,可导电,是混合物,既不是电解质,也不是非电解质;
②铜丝,能导电,既不是电解质,也不是非电解质;
③蔗糖晶体,不导电,非电解质;
④无水乙醇,不导电,非电解质;
⑤稀硫酸,可导电,是混合物,既不是电解质,也不是非电解质;
⑥ 不导电,非电解质;
⑦氨水,可导电,既不是电解质,也不是非电解质;
⑧液态 不导电,电解质;
⑨硫酸钡晶体,不导电,电解质;
⑩熔融NaC1,可导电,电解质;
⑪ 干冰,不导电,非电解质:
⑫ HCl气体,不导电,电解质;
⑬ 溶液,导电,是混合物,既不是电解质,也不是非电解质。
(1)上述状态下可导电的是①②⑤⑦⑩⑬。
(2)上述状态下的电解质不能导电的是⑧⑨⑫。
(3)上述状态下属于非电解质的是③④⑥⑪。
(4) 为强电解质,故电离方程式为 。
(5)稀硫酸和氨水生成硫酸铵,离子方程式为 。(6) 胶体是中学常见的胶体,它的制备方法为向沸水中逐滴加入5-6滴饱和 溶
液,继续煮沸至液体呈红褐色,停止加热,可得到 胶体.制备的化学方程式为
。
(7)在酸性条件下,向含铬废水中加入 ,可将 还原为 ,该过程的离子方程
式为 。
(8)已知 可将 氧化为B单质, 则被还原为 ,又知n个 与3个
恰好完全反应,则B共升高了2×3=6价,根据得失电子守恒,每个A降低6价,则
中A为+6价,则n值为7。
19.答案:(1)BaCl ; AgNO
2 3
(2) +2CHCOOH=2CHCOO-+CO↑+H O
3 3 2 2
(3)n(Cl-):n( ):n(Cu2+)=1:1:1; Zn+Cu2+═Zn2++Cu
(4)取少量C溶液于试管中,先加盐酸,无现象,再加氯化钡溶液,有白色沉淀生成,
则证明C中阴离子为
解析:(1)由于是可溶性盐,所以溶液中存在的盐离子和阴离子对应物质一定是可溶性,根据
盐类物质溶解性情况可知:Ba2+不能和 、 结合,而只能和 、Cl−;Ag+不能和
、Cl−、 三种离子结合,而只能和 结合,则一定是BaCl 、AgNO.Cu2+不能和
2 3
结合,所以为CuSO ,Na+对应 为NaCO.即四种物质为BaCl 、AgNO、CuSO 、
4 2 3 2 3 4
NaCO.
2 3
①中由于C盐是蓝色的,所以C为CuSO ;
4
②四支试管加入盐酸,B有沉淀,则B溶液为AgNO;而D生成无色气体,则为二氧化碳,即D
3
为NaCO.
2 3
综上所述:A为BaCl ;B为AgNO;C为CuSO ;D为NaCO;
2 3 4 2 3
由上述分析可知A为BaCl ;B为AgNO;故答案为:BaCl ;AgNO;
2 3 2 3
(2)盐酸与D(NaCO)反应的离子反应方程式为: +2H+=CO↑+HO,故答案为:
2 3 2 2
+2H+=CO↑+HO;
2 2
(3)A为BaCl ;B为AgNO;C为CuSO ,将含相同物质的量A. B. C的溶液混合后,溶液中存在
2 3 4
的离子及物质的量之比为:n(Cl−):n( ):n(Cu2+)=1:1:1,在此溶液中加入锌粒,可以将其中的
铜置换出来,发生反应的离子方程式Zn+Cu2+═Fe2++Cu,故答案为:n(Cl−):n(
):n(Cu2+)=1:1:1;Zn+Cu2+═Zn2++Cu;(4)C为CuSO ,检验物质C中阴离子的方法是取少量C溶液于试管中,先加盐酸,无现象,再加
4
氯化钡溶液,有白色沉淀生成,则证明C中阴离子为 ,故答案为:取少量C溶液于试管中,
先加盐酸,无现象,再加氯化钡溶液,有白色沉淀生成,则证明C中阴离子为 .
20.答案:(1)萃取;
(2)是;0.2mol/L
(3)
(4)存在,原溶液中含有 ,根据电荷守恒可知,原溶液
中一定含有 ;
解析: 的溶液显酸性,故溶液中不存在 ;向溶液中通入氯气分液后
得到紫色的 溶液,再分离得到紫黑色固体,说明有 生成,则原溶液中含有 ,
能够氧化 ,则一定不存在 ,2.54g碘单质的物质的量为0.01mol,所以原溶液中
;水层中加入NaOH溶液得到固体,说明原溶液中一定有 ,该固体为
,灼烧得到 ,根据铁原子守恒可知原溶液中 ;
带有的正电荷为0.04mol, 带有的正电荷为0.1mol/L×0.1L=0.01mol,
带有的负电荷为0.02mol,根据电荷守恒,原溶液中一定含有 ,不能确定是否
存在 。
(1)步骤①中加入 ,从水溶液中提取 的实验操作是萃取氯气氧化碘离子生成 ,
离子方程式为 。
(2)由分析可知,原溶液中 。
(4)由分析可知,原溶液中可能含有 ,一定含有 ,根据电荷守恒可知,
,所以 。