文档内容
专项 01 工业流程
该专题分为两个板块
【1】知识清单
一、 原料的预处理
1. 粉碎/研磨/雾化
2. 浸出与浸出率
3. 灼烧/焙烧/煅烧
4. 重点:控温环节
二、 原料杂质、分离
1. 调节pH
2. 拓宽思维:常见沉淀剂选择
三、 制备与提纯
1. 沉淀与结晶
2. 过洗干的那些事
3. 结晶过程
4. 广义水解
四、氧化还原滴定计算
1. 直接滴定
2. 间接滴定
3. 返滴定
【2】专项练习
【1】知识清单
一、原料的预处理
1、粉碎/研磨/雾化
将块状或颗粒状的物质磨成粉末或将液体分散成微小液滴。
模板一:粉碎/研磨/雾化的作用是?
。
例1.(2022·河南·高三·节选)二氧化锰常用作电池的正极材料,一种以软锰矿粉(主要成分是 ,含
少量 、 ,CuO、 等)为原料制备化学纯二氧化锰的流程如下:
(1)“酸浸”时将软锰矿粉碎的目的是_____ .练习1. (2022·山东·青岛市即墨区第一中学·节选)铍是原子能、火箭、导弹、航空以及冶金工业中不可
缺少的宝贵材料。以绿柱石 ( )为原料制备两性金属铍的工艺如图:
“水浸”时“产物压碎磨细”的目的是 .
2、浸出的目的:向固体中加入适当溶剂或溶液,使其中可溶性的物质溶解,不溶性物质通过过滤除去的
过程。
浸出的类别有: 、 、 。
①酸浸作用:与酸反应或溶解,金属氧化物、难溶性弱酸盐转变为金属离子进入溶液,不溶物通过过滤除
去。
非氧化性酸: 、 。
强氧化性酸: 、 、 。
变式: 、 、 。
②碱浸的作用:除去油污;溶解铝(氧化铝等两性物质)、二氧化硅;调节pH促进水解,实现金属离子的沉
淀(Al3+、Fe3+)
例2. 以铝土矿(主要成分为Al O、Fe O、SiO 等)为原料。画出冶炼Al的工业生成流程图,要求第一步
2 3 2 3 2
用酸浸的方式。
练习2. 以铝土矿(主要成分为Al O、Fe O、SiO 等)为原料。画出冶炼Al的工业生成流程图,要求第
2 3 2 3 2
一步用碱浸的方式。
练习3. 铝是应用广泛的金属。以铝土矿(主要成分为Al O、Fe O、SiO 等杂质)为原料制备铝的一种工艺
2 3 2 3 2
流程如下:
注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
2
(1)“碱溶”时生成偏铝酸钠的离子方程式为________________ _____。(2)“碱溶”后滤渣的成分: .
③浸出率:固体溶解后,离子在溶液中的含量的多少。
浸出速率:物质溶解于溶液的快慢。
模板二:如何提高浸出率?
。
模板三:如何提高浸出速率?
。
例3. 硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为MgB O·H O和Fe O,还有少量Fe O、
2 2 5 2 3 4 2 3
FeO、CaO、Al O 和SiO 等)为原料制备硼酸(H BO)的工艺流程如图所示:
2 3 2 3 3
已知:硼酸为粉末状晶体,易溶于水,加热到一定温度可分解为无水物。
回答下列问题:
(1)写出MgB O·H O与硫酸反应的化学方程式 。
2 2 5 2
(2)为提高浸出速率,除适当增加硫酸浓度浓度外,还可采取的措施有(写两条):
。
3. 灼烧/焙烧/煅烧
固体加热,高温发生化学反应,改变物质结构,生成易溶解物质,并使一些杂质高温下氧化,分解。煅烧
后一般跟随溶解操作。
作用:除去可燃性杂质(碳、有机物);氢氧化物、碳酸盐类分解为氧化物;
。
例4. (2022·黑龙江·铁人中学·改编)硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主要成分为含锰
化合物及FeS)与氧化锰矿(主要成分为 等锰的氧化物)为原料制备硫酸锰的工艺流程如下:
已知:
①“混合焙烧”后烧渣含MnSO 、Fe O 及少量FeO、Al O、MgO
4 2 3 2 3
将高硫锰矿与氧化锰矿混合焙烧的作用: 。4. 控制温度目的?在T < T < T 之间
1 2
模板四:温度高于T 时
1
①加快反应速率或溶解速率;
②促进平衡向吸热方向移动;
③除杂,除去热不稳定的杂质,如NaHCO 、Ca(HCO )、KMnO 、NH Cl等物质;
3 3 2 4 4
④使沸点相对较低或易升华的原料汽化。
模板五:温度低于T 时
2
①防止某物质在高温时会溶解(或分解);
②使化学平衡向着题目要求的方向(放热方向)移动;
③使某个沸点较高的产物液化,使其与其他物质分离;
④降低晶体的溶解度,减少损失。
⑤降温或减压可以减少能源成本
例5. (2022·河南·高三·节选)过碳酸钠( )是一种强氧化剂,易溶于水形成碳酸钠和过氧化
氢的混合液,难溶于乙醇,主要用作漂白剂和氧化剂,通常用作洗衣粉的助剂。某实验小组模拟工业在实
验室用饱和食盐水制备过碳酸钠,其流程如下:
(1)“反应Ⅰ”中应先向饱和食盐水中通入 (填化学式),其反应Ⅰ的离子方程式为
。
(2)操作Ⅰ为 。
(3)“反应Ⅱ”需控制温度在20℃左右的原因是 ,
乙醇的作用是 。
练习4. (2021山东济南历城第一中学·节选)氯化亚铜( )广泛应用于化工、印染、电镀等行业。
难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是
和少量 )为原料,采用硝酸铵(受热到一定温度时,易分解)氧化分解技术生产 的工艺过程如图:(1) 步骤①中主要反应的离子方程式 。
(2) 步骤③中主要反应的离子方程式 。
(3) 溶解温度应控制在60-70℃,原因是 。
练习5. 硫酸锌可作为食品锌强化剂的原料.工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是
ZnCO ,并含少量的Fe O、FeCO 、MgO、CaO等,生产工艺流程示意如下:
3 2 3 3
[相关资料]不溶性碱受热分解后生成对应的氧化物。
(1)将菱锌矿研磨成粉的目的是 ______ _。
(2)“浸取”过程中,加入过量浓盐酸的作用是 。
(3)“浸取”过程中需要控制温度在50-70℃的作用: 。
二、原料杂质、分离
1. 调节pH
pH控制在X-X 之间的原因?
1 2
答:①控制一定的pH,以提供反应所需环境。反应环境的不同会导致反应产物的差异。
②控制一定的pH,以改变元素的存在形式。
③控制一定的pH,使金属阳离子形成氢氧化物沉淀。
。
2. 拓宽思维:常见沉淀剂选择
①背诵溶解度表教材附录II.
②S2-:Zn2+、Fe2+、Cu2+、Ni2+等都是沉淀③F-:Ca2+、Mg2+等
④金属阳离子M2+与浓度较大的碳酸氢盐反应制备碳酸盐通式:M2++2HCO- =MCO ↓+CO ↑+H O
3 3 2 2
例6. 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、
Al、Mg、Zn、Ni、Si等元素)制备,工艺如图所示。
已知:①“滤渣1”含有S和SiO;
2
②相关金属离子 形成氢氧化物沉淀的pH范围如下:
金属离子
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
回答下列问题:
(1)“氧化”中添加适量的MnO 的作用是 。
2
(2)“调pH”的目的是除铁和铝,则溶液的pH范围应调节为_______~6之间。
(3)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是 。
(4)“除杂2”的目的是生成MgF 时沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
2
_____________________________________________________________________。
(5)写出“沉锰”的离子方程式: 。
三、制备与提纯
1. 沉淀与结晶区别
(1)沉淀:难溶物,Ksp较小的物质
(2)结晶:从溶液中获取可溶物的晶体
①带结晶水
例 :从硫酸铜溶液中获取CuSO ·5H O的操作: 。使用这种操作方法的原因:
4 2
。
② 不带结晶水
模板七:从氯化铝溶液中获取AlCl 晶体的操作: 。该操
3作过程中HCl的作用: 。
从NaCl溶液中获取NaCl晶体的操作: 。(NaCl的溶解度随温度的变化比较缓
慢)
从KNO 溶液中获取KNO 晶体的操作: 。(KNO 的溶解度随
3 3 3
温度的变化比较快。)使用这种操作方法的原因: 。
注意:
I.对于可水解且产生挥发性酸的盐,在结晶的过程中需要不断的加入相应的酸,以防止其水解生成氢
氧化物。
II. 对于溶解度随温度变化缓慢的盐,使用蒸发结晶;对于溶解度随温度变化比较快的盐,使用蒸发浓
缩,降温结晶。
(3)过滤后滤液仍然浑浊的可能操作原因?
模板八:①倾倒液体过快,使液体没过滤纸;
②玻璃棒没有靠在三层滤纸处,使滤纸破损。
(4)沉淀如何洗涤?
模板九: 。
(5)如何证明沉淀洗涤干净?
模板十:取最后一次洗涤液于试管中,加入··· ···(后面答相应离子的检验方法。)
注意:检验的离子,一定是沉淀以外的离子。
例7. 氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、
Ni(Ⅱ)等杂质]的流程如下:
提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO 。
2
回答下列问题:
(1)反应②中除掉的杂质离子是________,发生反应的离子方程式为________;在加高锰酸钾溶液前,
若pH较低,对除杂的影响是________。
(2)反应③的反应类型为________,过滤得到的滤渣中,除了过量的锌外还有________。
(3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是______________。
(4)反应④中产物的成分可能是ZnCO ·xZn(OH)。取干燥后的滤饼11.2 g,煅烧后可得到产品8.1 g,
3 2
则x等于________。
2、洗涤总结
(1)洗涤的目的: 。(2)热水洗: 。
(3)冷水洗: 。
(4)有机溶剂洗: 。
3、干燥方法
(1)加热烘干: 。
(2)常温干燥/低温烘干: 。
练习、得绿矾晶体用少量冰水洗涤其目的是?
模板十一: 。
4、广义水解
SOCl 是一种无色或淡黄色液体,遇水剧烈反应,是常用的脱水剂,将SOCl 与FeCl ·6H O混合并加热,
2 2 3 2
可得到无水FeCl ,得到无水FeCl 的化学方程式:
3 3
例8. 以硅孔雀石[主要成分为 CuCO·Cu(OH) 、CuSiO·2H O, 含SiO、FeCO、Fe O 等杂质]为原料制备
3 2 3 2 2 3 2 3
CuCl 的工艺流程如下:
2
已知: SOCl +HO SO ↑+2HCl↑
2 2 2
(1) “酸浸”时盐酸与 CuCO·Cu(OH) 反应的化学方程式为 ________________。 为提高“酸浸”时
3 2
铜元素的浸出率,可以采取的措施有:①适当提高盐酸浓度;②适当提高反应温度;③______________。
(2) “氧化”时发生反应的离子方程式为__________________。
(3) “滤渣 2”的主要成分为_______(填化学式);“调pH”时,pH 不能过高,其原因是___________。
(4) “加热脱水”时, 加入 SOCl 的目的是_____________________________________。
2
练习:亚硝酰氯NOCl 遇水后有强烈腐蚀性
碳酰氯COCl 与水反应
2
三溴氧磷POBr 与水反应
3
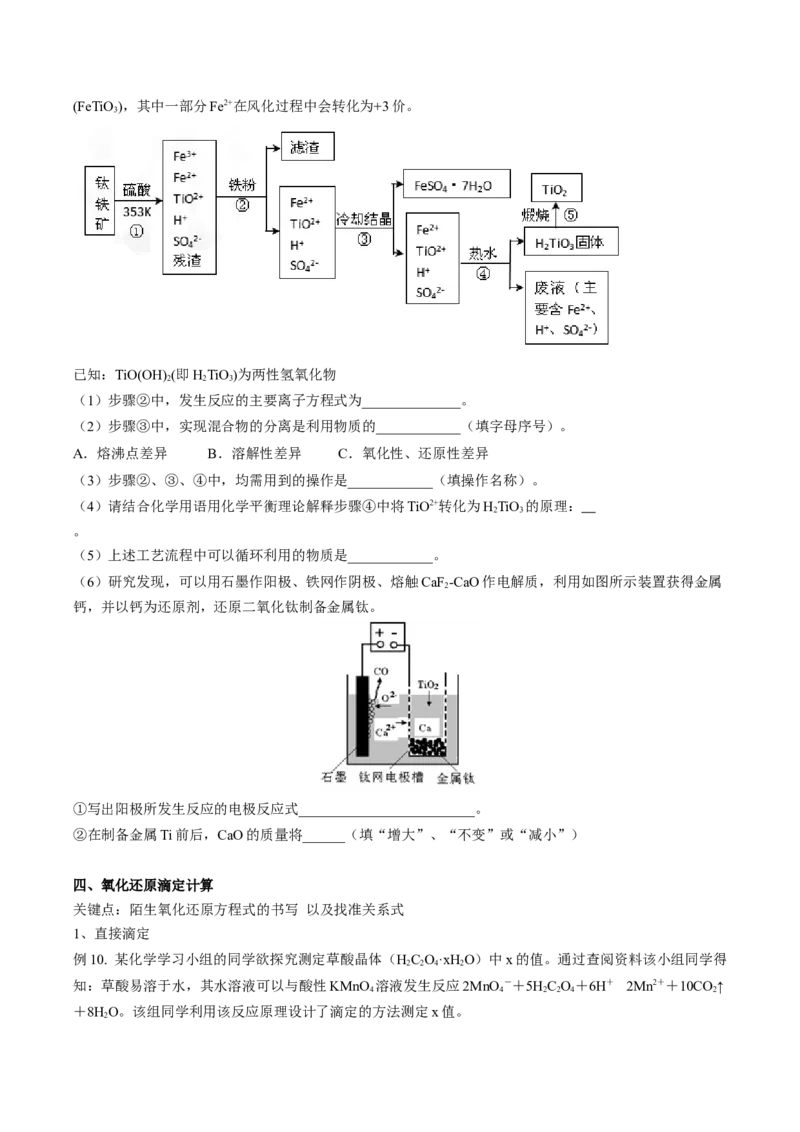
例9. 工业上,以钛铁矿为原料制备二氧化钛的工艺流程如下图所示。钛铁矿主要成分为钛酸亚铁(FeTiO),其中一部分Fe2+在风化过程中会转化为+3价。
3
已知:TiO(OH) (即HTiO)为两性氢氧化物
2 2 3
(1)步骤②中,发生反应的主要离子方程式为______________。
(2)步骤③中,实现混合物的分离是利用物质的____________(填字母序号)。
A.熔沸点差异 B.溶解性差异 C.氧化性、还原性差异
(3)步骤②、③、④中,均需用到的操作是____________(填操作名称)。
(4)请结合化学用语用化学平衡理论解释步骤④中将TiO2+转化为HTiO 的原理:
2 3
。
(5)上述工艺流程中可以循环利用的物质是____________。
(6)研究发现,可以用石墨作阳极、铁网作阴极、熔触CaF -CaO作电解质,利用如图所示装置获得金属
2
钙,并以钙为还原剂,还原二氧化钛制备金属钛。
①写出阳极所发生反应的电极反应式_________________________。
②在制备金属Ti前后,CaO的质量将______(填“增大”、“不变”或“减小”)
四、氧化还原滴定计算
关键点:陌生氧化还原方程式的书写 以及找准关系式
1、直接滴定
例10. 某化学学习小组的同学欲探究测定草酸晶体(HC O·xH O)中x的值。通过查阅资料该小组同学得
2 2 4 2
知:草酸易溶于水,其水溶液可以与酸性KMnO 溶液发生反应2MnO -+5HC O+6H+ 2Mn2++10CO↑
4 4 2 2 4 2
+8HO。该组同学利用该反应原理设计了滴定的方法测定x值。
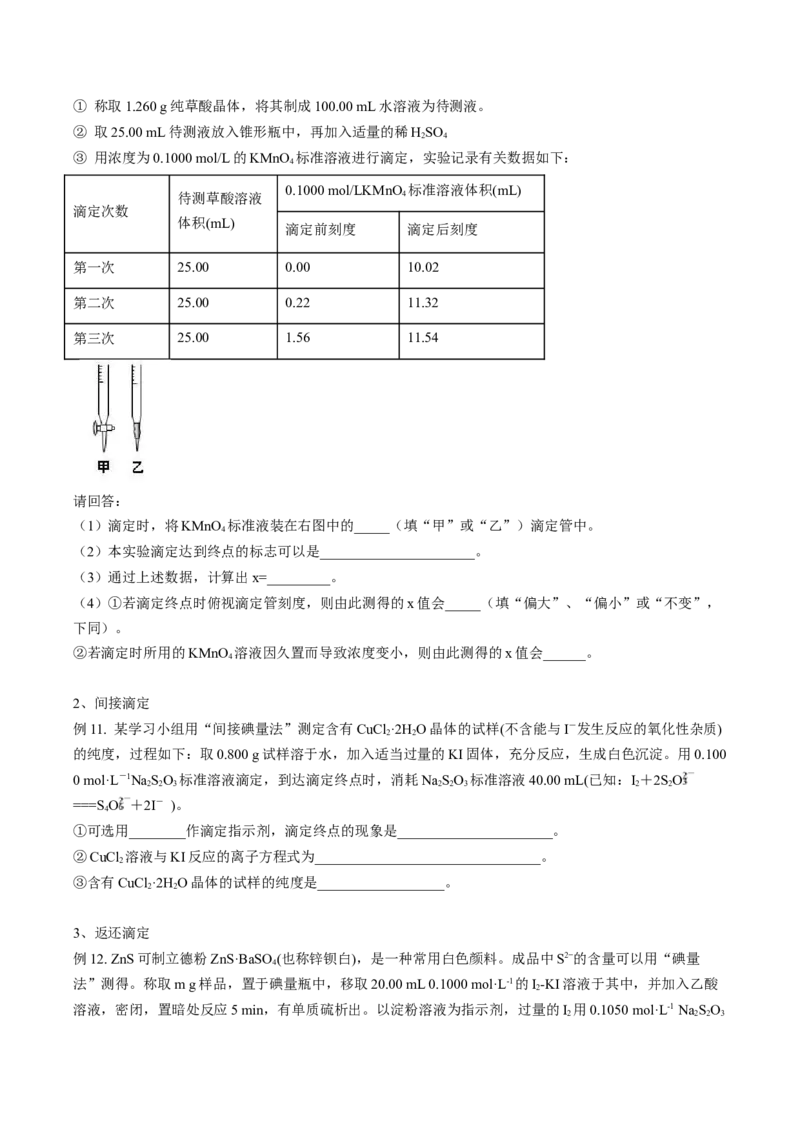
2① 称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀HSO
2 4
③ 用浓度为0.1000 mol/L的KMnO 标准溶液进行滴定,实验记录有关数据如下:
4
0.1000 mol/LKMnO 标准溶液体积(mL)
待测草酸溶液 4
滴定次数
体积(mL)
滴定前刻度 滴定后刻度
第一次 25.00 0.00 10.02
第二次 25.00 0.22 11.32
第三次 25.00 1.56 11.54
请回答:
(1)滴定时,将KMnO 标准液装在右图中的_____(填“甲”或“乙”)滴定管中。
4
(2)本实验滴定达到终点的标志可以是______________________。
(3)通过上述数据,计算出x=_________。
(4)①若滴定终点时俯视滴定管刻度,则由此测得的x值会_____(填“偏大”、“偏小”或“不变”,
下同)。
②若滴定时所用的KMnO 溶液因久置而导致浓度变小,则由此测得的x值会______。
4
2、间接滴定
例11. 某学习小组用“间接碘量法”测定含有CuCl ·2H O晶体的试样(不含能与I-发生反应的氧化性杂质)
2 2
的纯度,过程如下:取0.800 g试样溶于水,加入适当过量的KI固体,充分反应,生成白色沉淀。用0.100
0 mol·L-1NaSO 标准溶液滴定,到达滴定终点时,消耗NaSO 标准溶液40.00 mL(已知:I+2SO
2 2 3 2 2 3 2 2
===S O +2I- )。
4
①可选用________作滴定指示剂,滴定终点的现象是______________________。
②CuCl 溶液与KI反应的离子方程式为________________________________。
2
③含有CuCl ·2H O晶体的试样的纯度是__________________。
2 2
3、返还滴定
例12. ZnS可制立德粉ZnS·BaSO(也称锌钡白),是一种常用白色颜料。成品中S2−的含量可以用“碘量
4
法”测得。称取m g样品,置于碘量瓶中,移取20.00 mL 0.1000 mol·L-1的I-KI溶液于其中,并加入乙酸
2
溶液,密闭,置暗处反应5 min,有单质硫析出。以淀粉溶液为指示剂,过量的I 用0.1050 mol·L-1 NaSO
2 2 2 3溶液滴定,反应式为I+2S O2-=2I−+S O2-。测定时消耗NaSO 溶液体积V mL。测定时消耗Na2S2O3溶液
2 2 3 4 6 2 2 3
体积V mL。终点颜色变化为_________________,该样品中S2-的百分含量为_______(写出表达式)。若
NaSO 溶液标定后,放置过久使用,则测定结果_______(填“偏高”、“偏低”或“无影响”)。
2 2 3
【2】专项练习
1.(2022·河北沧州·高三阶段练习)我国科学家开发催化剂 来提高 燃料电池的性能。某小
组以含镍废料(主要含 ,以及少量 和 等)为原料提取
镍的流程如下:
请回答下列问题:
(1)“酸浸”中产生了一种还原性气体,它是_______(填化学式)。“除铁铝”中双氧水的作用是_______。
(2)“固体2”中除 、 外,还可能含硫单质等物质,生成硫单质的离子方程式为_______。
(3)为提高原料利用率,“电沉积”得到的“废液”可以循环用于_______(填名称)工序。
(4)在“除铁铝”中, 最终转化为_______(填化学式)。
(5)可以通过电解法提纯镍,粗镍作_______(填“阳”或“阴”)极,阴极的电极反应式为_______。
(6)氢氧化氧镍 是镍电池的正极活性材料。在 溶液加入 和 混合液可以制备
,其离子方程式为_______。
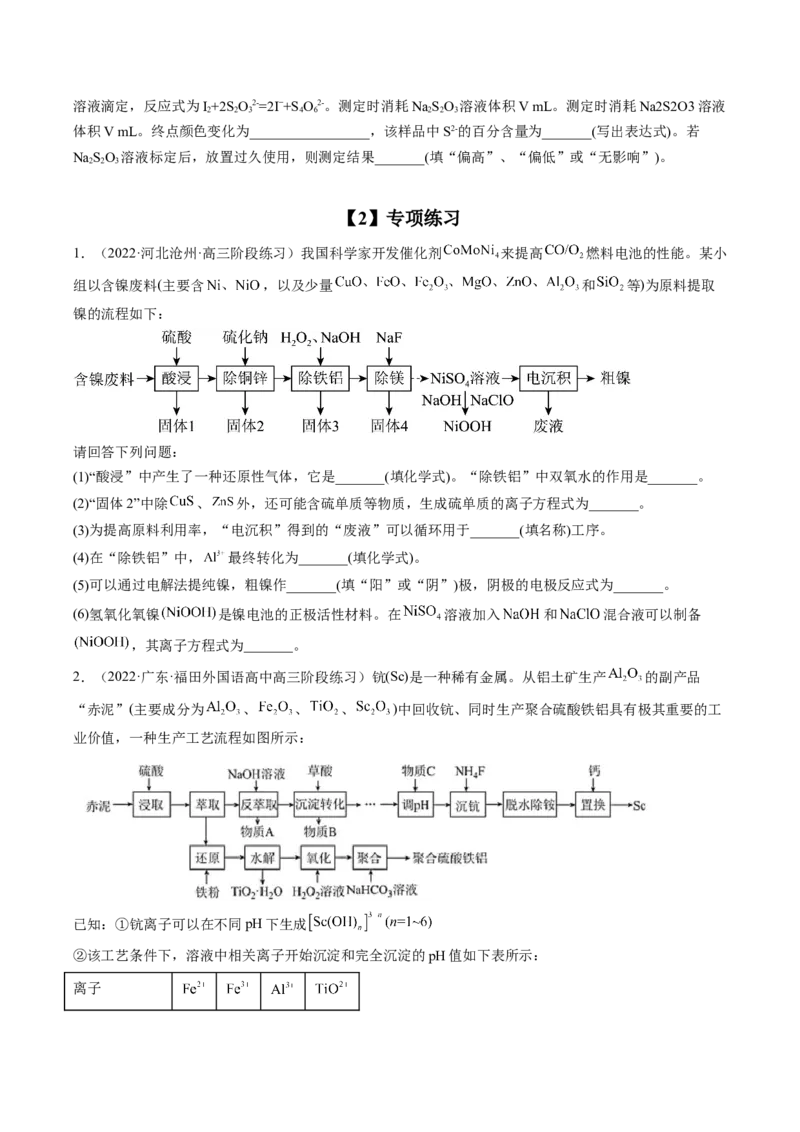
2.(2022·广东·福田外国语高中高三阶段练习)钪(Sc)是一种稀有金属。从铝土矿生产 的副产品
“赤泥”(主要成分为 、 、 、 )中回收钪、同时生产聚合硫酸铁铝具有极其重要的工
业价值,一种生产工艺流程如图所示:
已知:①钪离子可以在不同pH下生成
②该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如下表所示:
离子开始沉淀的pH 7.0 1.9 3.0 0.3
完全沉淀的pH 9.0 3.2 4.7 2.0
回答下列问题:
(1)写出基态Sc原子的核外电子排布式:_______。
(2)流程中经处理后可循环利用的物质是_______(填“物质A”或“物质B”);物质C最好选用_______(填
“NaOH溶液”或“氨水”)。
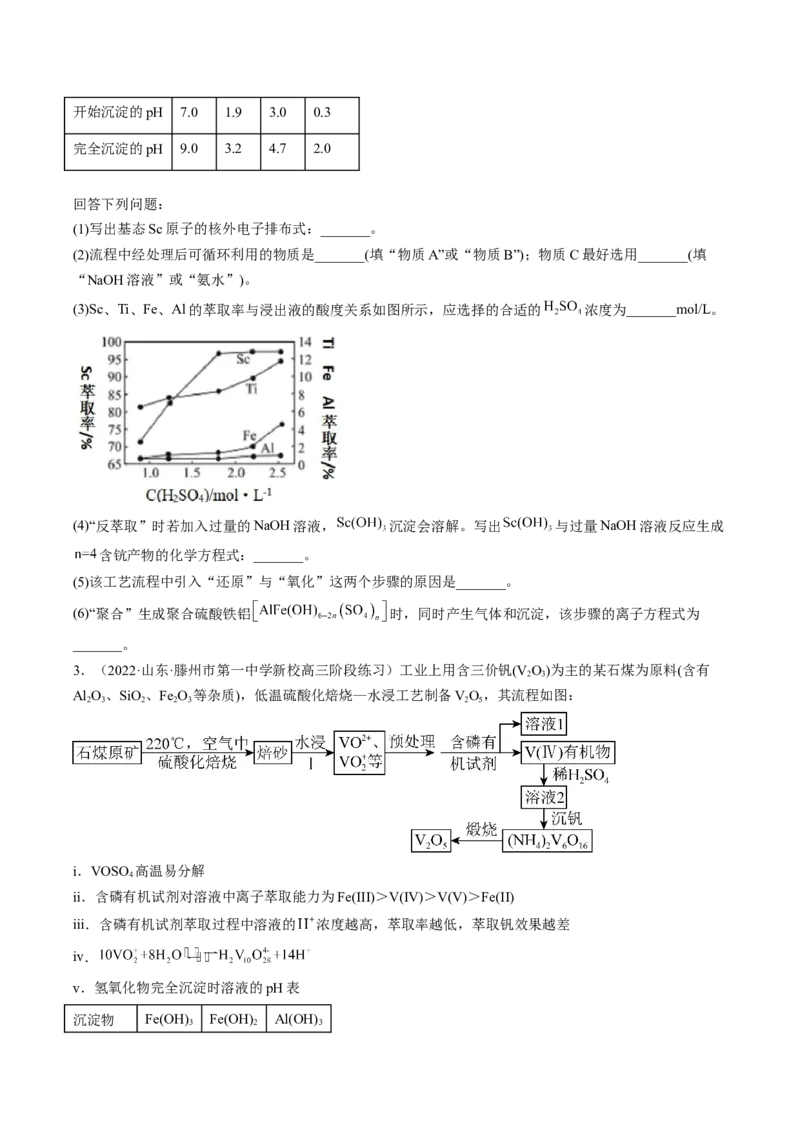
(3)Sc、Ti、Fe、Al的萃取率与浸出液的酸度关系如图所示,应选择的合适的 浓度为_______mol/L。
(4)“反萃取”时若加入过量的NaOH溶液, 沉淀会溶解。写出 与过量NaOH溶液反应生成
含钪产物的化学方程式:_______。
(5)该工艺流程中引入“还原”与“氧化”这两个步骤的原因是_______。
(6)“聚合”生成聚合硫酸铁铝 时,同时产生气体和沉淀,该步骤的离子方程式为
_______。
3.(2022·山东·滕州市第一中学新校高三阶段练习)工业上用含三价钒(V O)为主的某石煤为原料(含有
2 3
Al O、SiO、Fe O 等杂质),低温硫酸化焙烧—水浸工艺制备VO,其流程如图:
2 3 2 2 3 2 5
i.VOSO 高温易分解
4
ii.含磷有机试剂对溶液中离子萃取能力为Fe(III)>V(IV)>V(V)>Fe(II)
iii.含磷有机试剂萃取过程中溶液的 浓度越高,萃取率越低,萃取钒效果越差
iv.
v.氢氧化物完全沉淀时溶液的pH表
沉淀物 Fe(OH) Fe(OH) Al(OH)
3 2 3完全沉
3.2 9.0 4.7
淀
(1)焙烧过程中向石煤中加硫酸焙烧,将VO 转化为VOSO 的化学方程式是___________。
2 3 4
(2)预处理过程中先加入NaSO 溶液进行还原预处理,加入NaSO 溶液的第一个作用是将V(V)还原为
2 3 2 3
V(IV)减少钒的损失,再用氨水混合并调节溶液pH。
①请结合相关离子方程式,说明加入NaSO 的第二个作用___________。
2 3
②解释加氨水调节pH≈5的原因是___________。
(3)上述I的具体操作为___________。
(4)测定产品中VO 的纯度:
2 5
称取a g产品,先用硫酸溶解,得到(VO )SO 溶液。再加入b mLc mol/L(NH )Fe(SO ) 溶液(
2 2 4 1 1 4 2 4 2
)最后用c mol/L KMnO 溶液滴定过量的(NH )Fe(SO ) 至终点,消耗
2 4 4 2 4 2
KMnO 溶液的体积为b mL。已知 ,被还原为Mn2+,假设杂质不参与反应。则产品中VO 的质量分
4 2 2 5
数是___________。(V O 的摩尔质量:182 g/mol)
2 5
4.(2022·湖南· 邵东市第一中学高三阶段练习)一种含铝、锂、钴的新型电子材料,生产中产生的废料
数量可观,废料中的铝以金属铝箔的形式存在;钴以 的形式存在,吸附在铝箔的单面或双面;
锂混杂于其中。从废料中制取高纯碳酸钴 的工艺流程如图:
(1)写出一条加快碱溶速率的措施_______。
(2)过程II中加入稀 酸化后,再加入 溶液浸出钴。则浸出钴的离子反应方程式为_______(产
物中只有一种酸根)。该过程不能用盐酸代替硫酸进行酸化,原因是_______。
(3)过程III中碳酸钠溶液的作用是沉淀 和 ,写出沉淀 的离子方程式_______。已知 微溶于
水,过程Ⅲ控制 不宜过低,否则会影响沉淀 ,原因是_______。
(4)过程IV沉钴的离子方程式是_______。
(5) 可用于制备锂离子电池的正极材料 ,其生产工艺是将 的 和
的固体混合物在空气中加热至700℃~900℃。试写出该反应的化学方程式____。
5.(2022·辽宁·高三阶段练习)KIO 是一种重要的无机化合物,可作为食盐中的补碘剂。利用“KClO 氧
3 3化法”制备KIO 工艺流程如下图所示,回答下列问题:
3
(1)KIO 中I元素的化合价为_______。
3
(2)“酸化反应”所需I 从海带中提取。经历灼烧海带,浸泡海带灰等步骤,向获得的I-溶液加入MnO ,在
2 2
酸性条件下生成I,其离子反应方程式为_______。
2
(3)“酸化反应”化学方程式为:6I+11KClO +3H O=6KH(IO)+5KCl+3Cl ,每生成3mol KH(IO ),反应中
2 3 2 3 2 2 3 2
转移的电子数为_______。(用N 代表阿伏加德罗常数的值)
A
(4)“逐Cl”采用的方法是_______,排出的Cl 可用KOH碱液吸收,该反应的离子方程式为_______。
2 2
(5)“滤液”中的溶质主要是_______。
(6)“调pH”中发生反应的化学方程式为_______。
(7)已知KIO 在水中溶解度随温度升高而增大,则浓缩结晶的具体步骤是_______、_______、过滤、洗涤。
3
6.(2022·辽宁·高三阶段练习)I.氢化铝锂(LiAlH )、硼氢化钠(NaBH )在有机合成中应用广泛。回答下列
4 4
问题:
(1)NaBH 与水反应生成NaBO ,该反应的离子方程式为_______。
4 2
(2)还原能力(单位质量转移电子数):NaBH _______LiAlH (填“>”“=”或“<") 。
4 4
(3)工业上湿法合成NaBH 路线如下:
4
①"合成”步骤中常将NaH分散到矿物油中,再与硼酸三甲酯[化学式:B(OCH ),易溶于矿物油中]反应,
3 3
其目的是_______。
②“合成”反应的化学方程式为_______。
II.氨氮废水的处理是当前科学研究的热点问题之一、氨氮废水中的氮元素多以 、NH •H O的形式存在。
3 2
某工厂处理氨氮废水的流程如图:
(4)过程①的目的是将 转化为NH ,并鼓入大量热空气将氨气吹出,写出 转化为NH 的离子方程
3 3
式_______。
(5)过程②中加入NaClO溶液可将含氮化合物( 、NH •H O)转化为无毒无害的物质,反应后含氯元素、
3 2
氮元素的物质的化学式分别为_______、_______。(6)图中含余氯废水中含有NaClO,可选用X试剂_______(填序号)达到去除余氯的目的。
a.NaOH溶液 b.KMnO 溶液 c.KCl溶液 d.NaSO 溶液
4 2 3
7.(2022·天津一中高三阶段练习)一种以辉铜矿(主要成分为Cu S,含少量SiO)为原料制备硝酸铜的工
2 2
艺流程如图所示:
(1)写出“浸取”过程中Cu S溶解时发生反应的离子方程式:____。
2
(2)恒温“浸取”的过程中发现铜元素的浸取速率先增大后减少,有研究指出CuCl 是该反应的催化剂,该
2
过程的反应原理可用化学方程式表示为
①Cu S+2CuCl =4CuCl+S;
2 2
②____。
(3)向滤液M中加入(或通入)____(填字母),可得到一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾 d.氯化氢
(4)“保温除铁”过程中,加入CuO的目的是____;“蒸发浓缩、冷却结晶”过程中,要用HNO 溶液调节
3
溶液的pH,其理由是____。
(5)辉铜矿可由黄铜矿(主要成分为CuFeS)通过电化学反应转变而成,有关转化见图,转化时转移0.2mol电
2
子,生成Cu S___mol。
2
8.(2022·天津·南开中学高三阶段练习)高锰酸钾生产过程中产生的废锰渣(主要成分为 、 、
和 )可用于制备 晶体,工艺流程如下:该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子
开始沉淀pH 2.10 7.45 9.27 9.60
完全沉淀pH 3.20 8.95 10.87 11.13
回答以下问题:
(1) 中阴离子的中心原子杂化类型为_______。
(2)提高“反应I”速率可采取的措施是_______(除“加热”外,任写一种),滤渣A的主要成分为_______(填
化学式)。
(3)“反应II”中硫铁矿( )的作用为_______。
(4)“反应III”的离子方程式为_______。
(5)“调pH”步骤中,应调节pH不低于_______。
(6)取 产品,溶于适量水中,加硫酸酸化,用过量 (难溶于水)将其完全氧化为 ,
过滤,洗涤,洗涤液并入滤液后,加入 固体,充分反应后,用_______(填“酸”或“碱”)
式滴定管盛装 溶液滴定,最终用去20.00mL,计算样品中 的质量分数是
_______(保留三位有效数字)。
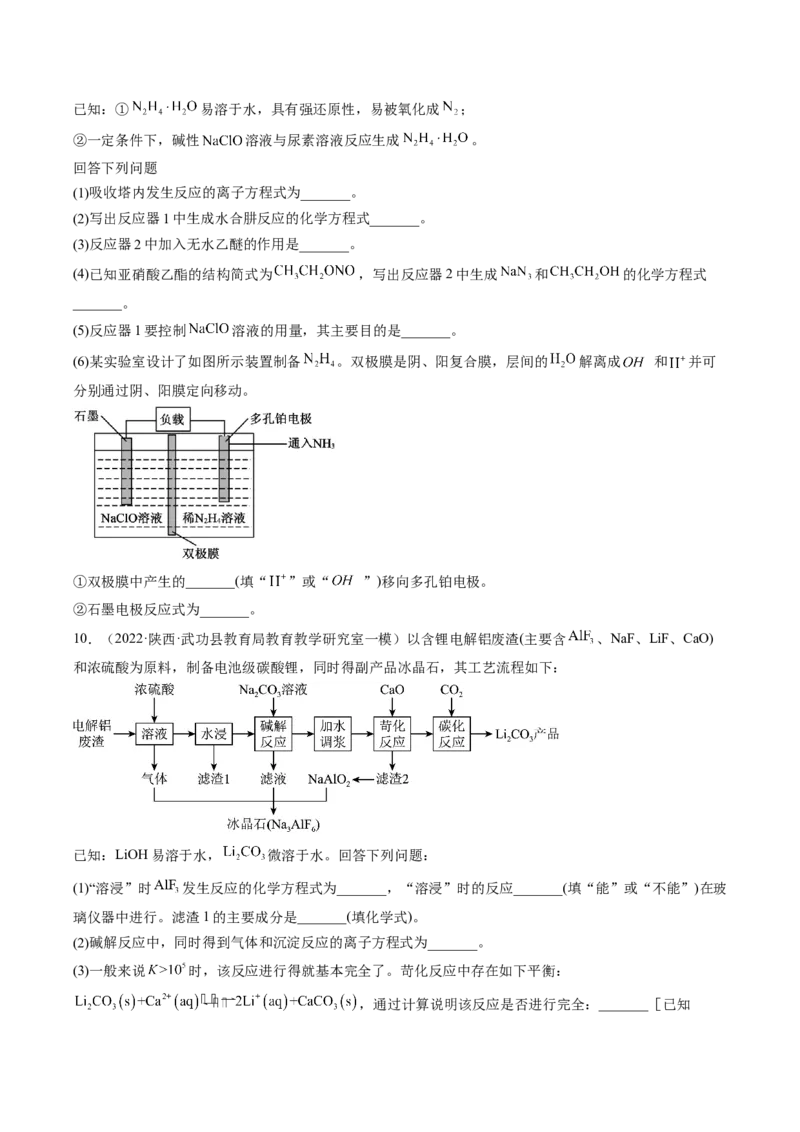
9.(2022·黑龙江·牡丹江市第二高级中学高三阶段练习)叠氮化钠( )不溶于乙醚,微溶于乙醇,易溶
于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合
肼( )并利用其进一步反应制取 的流程如下:已知:① 易溶于水,具有强还原性,易被氧化成 ;
②一定条件下,碱性 溶液与尿素溶液反应生成 。
回答下列问题
(1)吸收塔内发生反应的离子方程式为_______。
(2)写出反应器1中生成水合肼反应的化学方程式_______。
(3)反应器2中加入无水乙醚的作用是_______。
(4)已知亚硝酸乙酯的结构简式为 ,写出反应器2中生成 和 的化学方程式
_______。
(5)反应器1要控制 溶液的用量,其主要目的是_______。
(6)某实验室设计了如图所示装置制备 。双极膜是阴、阳复合膜,层间的 解离成 和 并可
分别通过阴、阳膜定向移动。
①双极膜中产生的_______(填“ ”或“ ”)移向多孔铂电极。
②石墨电极反应式为_______。
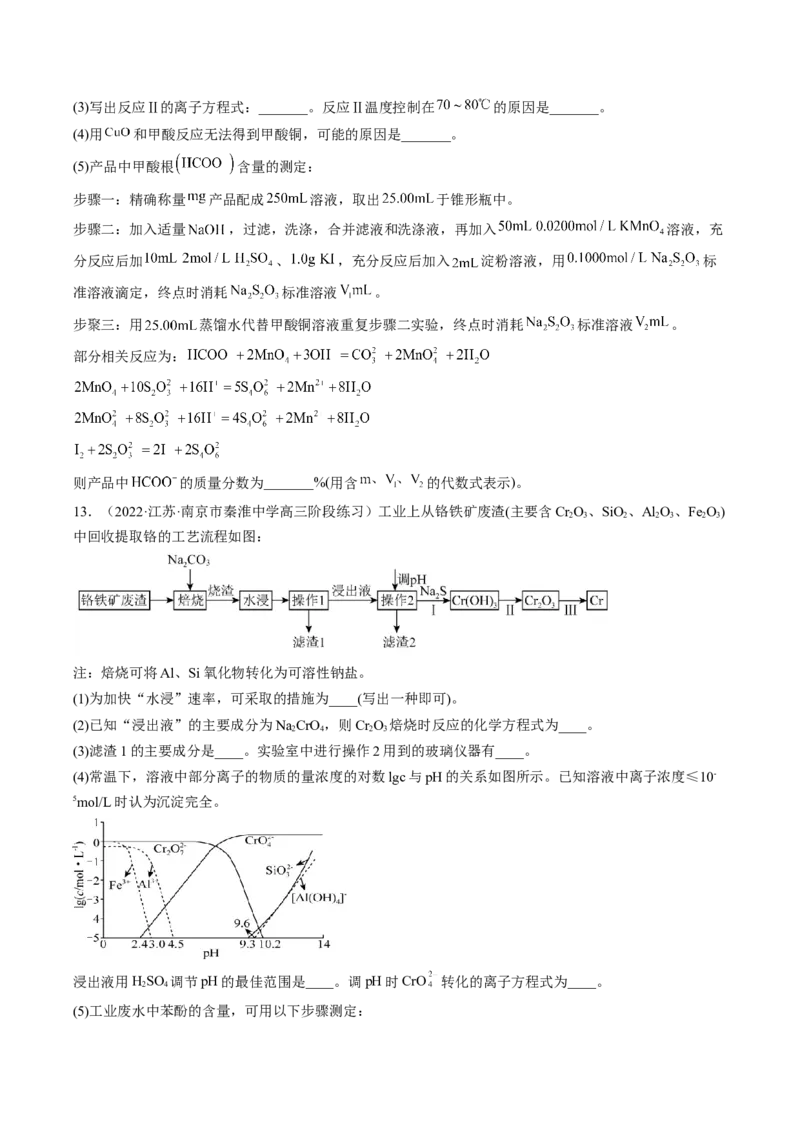
10.(2022·陕西·武功县教育局教育教学研究室一模)以含锂电解铝废渣(主要含 、NaF、LiF、CaO)
和浓硫酸为原料,制备电池级碳酸锂,同时得副产品冰晶石,其工艺流程如下:
已知:LiOH易溶于水, 微溶于水。回答下列问题:
(1)“溶浸”时 发生反应的化学方程式为_______,“溶浸”时的反应_______(填“能”或“不能”)在玻
璃仪器中进行。滤渣1的主要成分是_______(填化学式)。
(2)碱解反应中,同时得到气体和沉淀反应的离子方程式为_______。
(3)一般来说 时,该反应进行得就基本完全了。苛化反应中存在如下平衡:
,通过计算说明该反应是否进行完全:_______[已知、 ]。
(4)从碳化反应后的溶液得到 固体的具体实验操作中,第一步应在_______(填一种主要仪器的名称)
中进行,该流程中可以循环使用的物质是_______。
(5)上述流程得到副产品冰晶石的化学方程式为_______。
11.(2022·广东·清远市华侨中学高三阶段练习)铍是火箭、导弹、航空以及冶金工业中不可缺少的宝贵
材料。以绿柱石[Be Al (SiO)]为原料制备两性金属铍的工艺流程如图所示。
3 2 3 6
回答下列问题:
(1)绿柱石中Be的化合价为_______ 。
(2)750℃烧结时,NaFeF 仅与绿柱若中BeO作用生成易溶于水的NaBeF ,则滤渣的主要成分是Fe O 和
3 6 2 4 2 3
_______ 。
(3)“水浸”时“粉碎”的目的是_______ 。
(4)加适量氢氧化钠溶液使铍元素完全转化为氢氧化铍沉淀,已知25℃时K [Be(OH) ]=4×10-22,计算25℃
sp 2
时,饱和氢氧化铍溶液的pH=_______(可用对数表示),“沉氟”的化学方程式为_______。
(5)镍作阴极、石墨作阳极,350~400℃电解NaCl—BeCl 熔融混合物得到金属铍,阳极反应式为_______;
2
不能用该电解槽电解熔融氯化铍制金属铍的原因可能是_______。
12.(2022·浙江·高三阶段练习)用废铜(主要是Cu、CuO,含少量Fe、Fe O)制取甲酸铜晶体的流程如下:
2 3
请回答:
(1)反应Ⅰ最佳方案应选择_______。
A.废铜煅烧成氧化铜后与稀硫酸反应 B.废铜与稀硫酸、稀硝酸反应
C.废铜与浓硫酸反应 D.废铜与稀硫酸、双氧水反应
(2)从下列选项中选择“系列操作Ⅰ”的正确步骤并排序(操作可重复使用):_______。
_______→c→_______→_______→_______。
a.加热蒸发至溶液表面出现晶膜 b.加热蒸发至出现大量晶体 c.过滤 d.趁热过滤 e.用 调节 f.用
调节 g.冷却 h.用余热蒸干(3)写出反应Ⅱ的离子方程式:_______。反应Ⅱ温度控制在 的原因是_______。
(4)用 和甲酸反应无法得到甲酸铜,可能的原因是_______。
(5)产品中甲酸根 含量的测定:
步骤一:精确称量 产品配成 溶液,取出 于锥形瓶中。
步骤二:加入适量 ,过滤,洗涤,合并滤液和洗涤液,再加入 溶液,充
分反应后加 、 ,充分反应后加入 淀粉溶液,用 标
准溶液滴定,终点时消耗 标准溶液 。
步聚三:用 蒸馏水代替甲酸铜溶液重复步骤二实验,终点时消耗 标准溶液 。
部分相关反应为:
则产品中 的质量分数为_______%(用含 的代数式表示)。
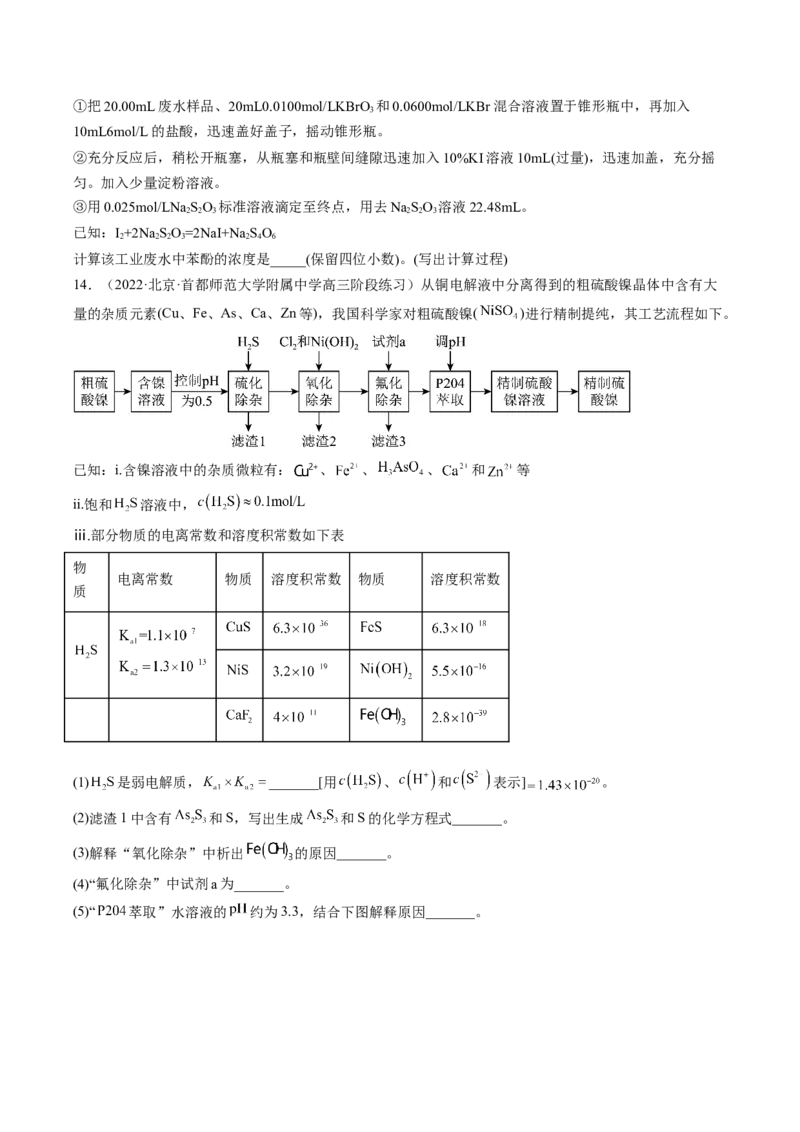
13.(2022·江苏·南京市秦淮中学高三阶段练习)工业上从铬铁矿废渣(主要含Cr O、SiO、Al O、Fe O)
2 3 2 2 3 2 3
中回收提取铬的工艺流程如图:
注:焙烧可将Al、Si氧化物转化为可溶性钠盐。
(1)为加快“水浸”速率,可采取的措施为____(写出一种即可)。
(2)已知“浸出液”的主要成分为NaCrO,则Cr O 焙烧时反应的化学方程式为____。
2 4 2 3
(3)滤渣1的主要成分是____。实验室中进行操作2用到的玻璃仪器有____。
(4)常温下,溶液中部分离子的物质的量浓度的对数lgc与pH的关系如图所示。已知溶液中离子浓度≤10-
5mol/L时认为沉淀完全。
浸出液用HSO 调节pH的最佳范围是____。调pH时CrO 转化的离子方程式为____。
2 4
(5)工业废水中苯酚的含量,可用以下步骤测定:①把20.00mL废水样品、20mL0.0100mol/LKBrO 和0.0600mol/LKBr混合溶液置于锥形瓶中,再加入
3
10mL6mol/L的盐酸,迅速盖好盖子,摇动锥形瓶。
②充分反应后,稍松开瓶塞,从瓶塞和瓶壁间缝隙迅速加入10%KI溶液10mL(过量),迅速加盖,充分摇
匀。加入少量淀粉溶液。
③用0.025mol/LNa SO 标准溶液滴定至终点,用去NaSO 溶液22.48mL。
2 2 3 2 2 3
已知:I+2Na SO=2NaI+Na SO
2 2 2 3 2 4 6
计算该工业废水中苯酚的浓度是_____(保留四位小数)。(写出计算过程)
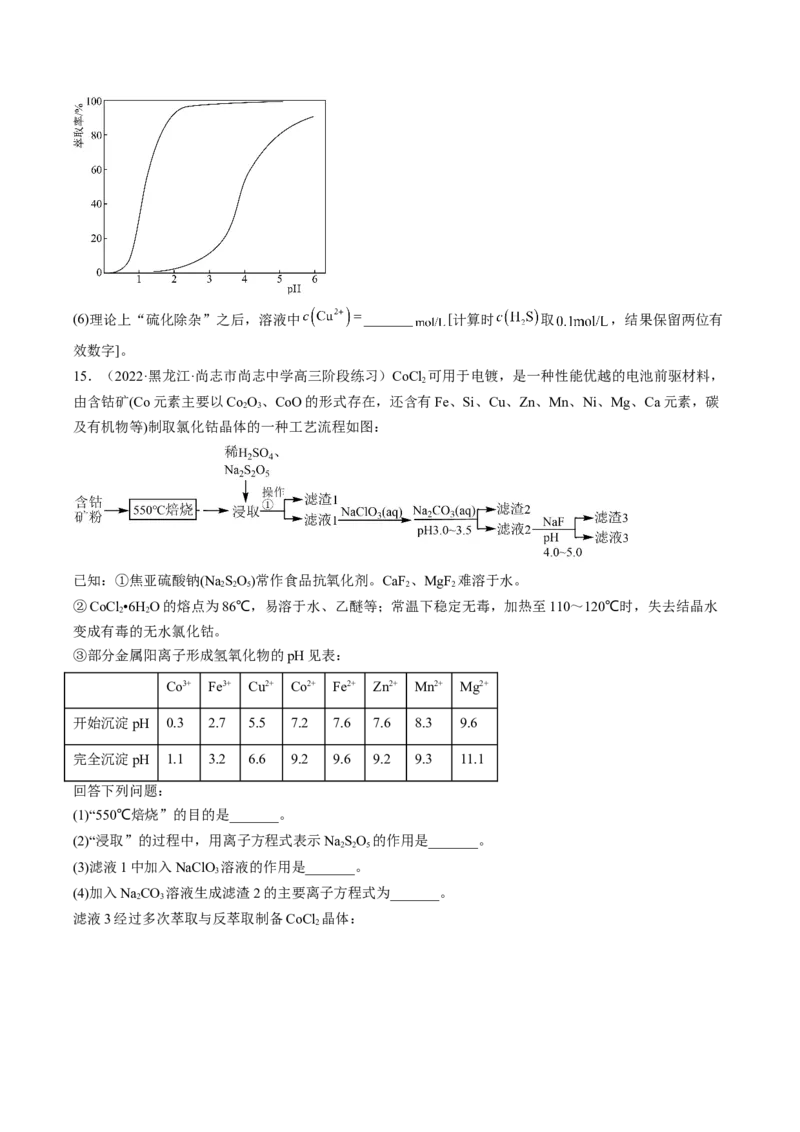
14.(2022·北京·首都师范大学附属中学高三阶段练习)从铜电解液中分离得到的粗硫酸镍晶体中含有大
量的杂质元素(Cu、Fe、As、Ca、Zn等),我国科学家对粗硫酸镍( )进行精制提纯,其工艺流程如下。
已知:i.含镍溶液中的杂质微粒有: 、 、 、 和 等
ii.饱和 溶液中,
ⅲ.部分物质的电离常数和溶度积常数如下表
物
电离常数 物质 溶度积常数 物质 溶度积常数
质
(1) 是弱电解质, _______[用 、 和 表示] 。
(2)滤渣1中含有 和S,写出生成 和S的化学方程式_______。
(3)解释“氧化除杂”中析出 的原因_______。
(4)“氟化除杂”中试剂a为_______。
(5)“ 萃取”水溶液的 约为3.3,结合下图解释原因_______。(6)理论上“硫化除杂”之后,溶液中 _______ [计算时 取 ,结果保留两位有
效数字]。
15.(2022·黑龙江·尚志市尚志中学高三阶段练习)CoCl 可用于电镀,是一种性能优越的电池前驱材料,
2
由含钴矿(Co元素主要以Co O、CoO的形式存在,还含有Fe、Si、Cu、Zn、Mn、Ni、Mg、Ca元素,碳
2 3
及有机物等)制取氯化钴晶体的一种工艺流程如图:
已知:①焦亚硫酸钠(Na SO)常作食品抗氧化剂。CaF 、MgF 难溶于水。
2 2 5 2 2
②CoCl •6H O的熔点为86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水
2 2
变成有毒的无水氯化钴。
③部分金属阳离子形成氢氧化物的pH见表:
Co3+ Fe3+ Cu2+ Co2+ Fe2+ Zn2+ Mn2+ Mg2+
开始沉淀pH 0.3 2.7 5.5 7.2 7.6 7.6 8.3 9.6
完全沉淀pH 1.1 3.2 6.6 9.2 9.6 9.2 9.3 11.1
回答下列问题:
(1)“550℃焙烧”的目的是_______。
(2)“浸取”的过程中,用离子方程式表示NaSO 的作用是_______。
2 2 5
(3)滤液1中加入NaClO 溶液的作用是_______。
3
(4)加入NaCO 溶液生成滤渣2的主要离子方程式为_______。
2 3
滤液3经过多次萃取与反萃取制备CoCl 晶体:
2(5)滤液3中加入萃取剂I,然后用稀盐酸反萃取的目的是_______。
(6)氯化钴溶液,经过_______、过滤、洗涤、干燥得到晶体。
(7)制备晶体CoCl •6H O,需在减压环境下烘干的原因是_______。
2 2
16.(2022·广东·高三阶段练习)钪(Sc)是一种重要的稀土金属,常用来制特种玻璃、轻质耐高温合金。从
“赤泥”矿(主要成分为 、 、 、 )中回收钪,同时生产聚合氯化铁铝[
]具有极其重要的工业价值,一种工艺流程如图所示:
已知:钪离子可以在不同pH下生成 (n=1~6)。请回答以下问题:
(1)基态钪原子的价电子排布式为_______,过氧化氢的电子式为_______。
(2)“还原”步骤中发生的主要离子反应方程式为_______。
(3)“反萃取”时若加入的氢氧化钠大量过量,则生成的含Sc元素的粒子主要为_______。
(4)为了使水解步骤反应更加彻底,可以采取的措施为_______(不能添加化学式剂,任答一条即可)。
(5)步骤X中生成聚合氯化铁铝[ ]的化学反应方程式为_______。
(6)如图是 晶胞的示意图,晶胞中含有的氧原子数目为_______个,已知Ti原子的配位数为6,则O原子
的配位数为_______,该晶体的密度约为_______ 。(N 取 ,结果用含a、b、c的最简分数表
A
达式表示)。
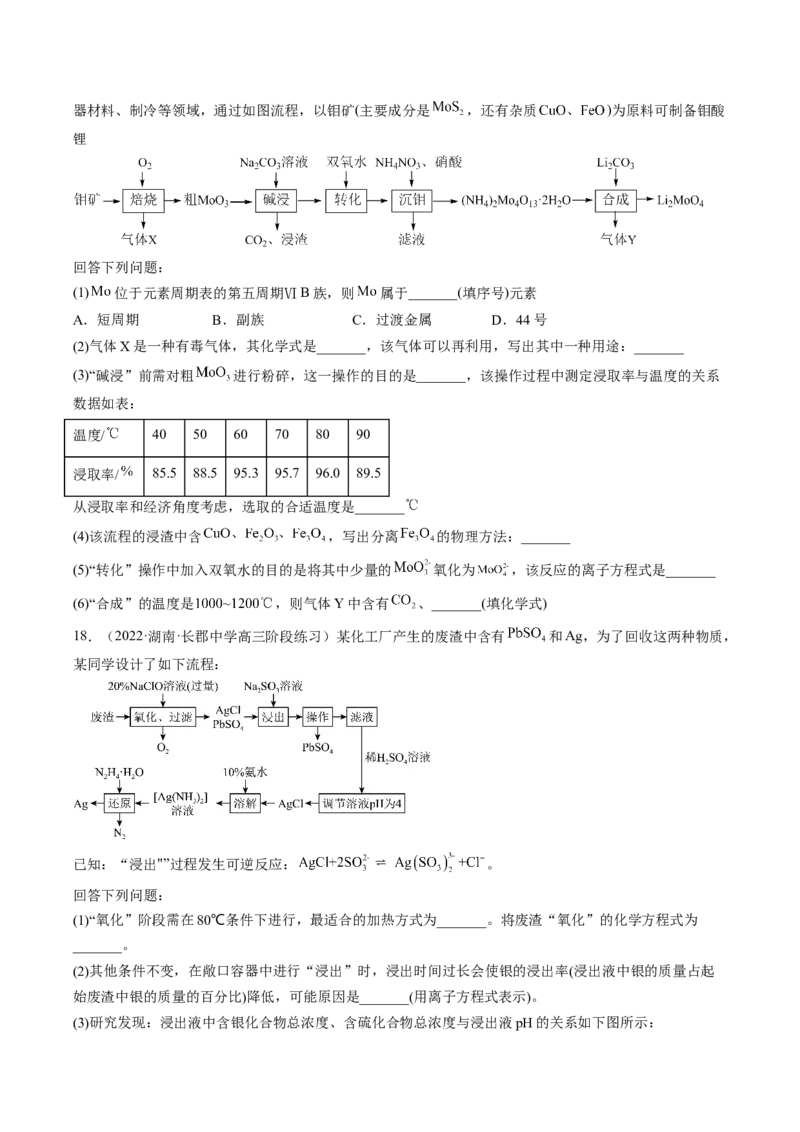
17.(2022·河南·高三阶段练习)钼酸锂 主要用于化工、缓蚀剂、电极材料、金属陶瓷、电阻器材料、制冷等领域,通过如图流程,以钼矿(主要成分是 ,还有杂质 )为原料可制备钼酸
锂
回答下列问题:
(1) 位于元素周期表的第五周期ⅥB族,则 属于_______(填序号)元素
A.短周期 B.副族 C.过渡金属 D.44号
(2)气体X是一种有毒气体,其化学式是_______,该气体可以再利用,写出其中一种用途:_______
(3)“碱浸”前需对粗 进行粉碎,这一操作的目的是_______,该操作过程中测定浸取率与温度的关系
数据如表:
温度/ 40 50 60 70 80 90
浸取率/ 85.5 88.5 95.3 95.7 96.0 89.5
从浸取率和经济角度考虑,选取的合适温度是_______
(4)该流程的浸渣中含 ,写出分离 的物理方法:_______
(5)“转化”操作中加入双氧水的目的是将其中少量的 氧化为 ,该反应的离子方程式是_______
(6)“合成”的温度是 ,则气体Y中含有 、_______(填化学式)
18.(2022·湖南·长郡中学高三阶段练习)某化工厂产生的废渣中含有 和Ag,为了回收这两种物质,
某同学设计了如下流程:
已知:“浸出"”过程发生可逆反应: 。
回答下列问题:
(1)“氧化”阶段需在80℃条件下进行,最适合的加热方式为_______。将废渣“氧化”的化学方程式为
_______。
(2)其他条件不变,在敞口容器中进行“浸出”时,浸出时间过长会使银的浸出率(浸出液中银的质量占起
始废渣中银的质量的百分比)降低,可能原因是_______(用离子方程式表示)。
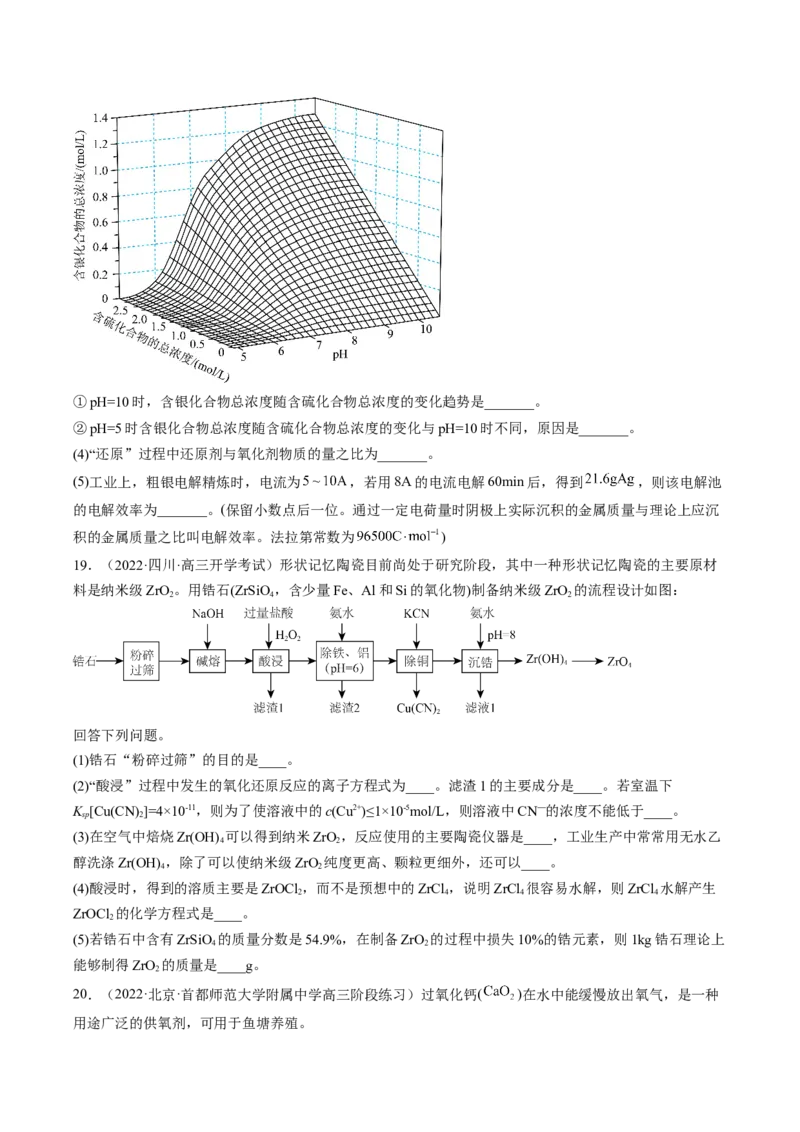
(3)研究发现:浸出液中含银化合物总浓度、含硫化合物总浓度与浸出液pH的关系如下图所示:①pH=10时,含银化合物总浓度随含硫化合物总浓度的变化趋势是_______。
②pH=5时含银化合物总浓度随含硫化合物总浓度的变化与pH=10时不同,原因是_______。
(4)“还原”过程中还原剂与氧化剂物质的量之比为_______。
(5)工业上,粗银电解精炼时,电流为 ,若用8A的电流电解60min后,得到 ,则该电解池
的电解效率为_______。(保留小数点后一位。通过一定电荷量时阴极上实际沉积的金属质量与理论上应沉
积的金属质量之比叫电解效率。法拉第常数为 )
19.(2022·四川·高三开学考试)形状记忆陶瓷目前尚处于研究阶段,其中一种形状记忆陶瓷的主要原材
料是纳米级ZrO。用锆石(ZrSiO,含少量Fe、Al和Si的氧化物)制备纳米级ZrO 的流程设计如图:
2 4 2
回答下列问题。
(1)锆石“粉碎过筛”的目的是____。
(2)“酸浸”过程中发生的氧化还原反应的离子方程式为____。滤渣1的主要成分是____。若室温下
K [Cu(CN) ]=4×10-11,则为了使溶液中的c(Cu2+)≤1×10-5mol/L,则溶液中CN—的浓度不能低于____。
sp 2
(3)在空气中焙烧Zr(OH) 可以得到纳米ZrO,反应使用的主要陶瓷仪器是____,工业生产中常常用无水乙
4 2
醇洗涤Zr(OH) ,除了可以使纳米级ZrO 纯度更高、颗粒更细外,还可以____。
4 2
(4)酸浸时,得到的溶质主要是ZrOCl ,而不是预想中的ZrCl,说明ZrCl 很容易水解,则ZrCl 水解产生
2 4 4 4
ZrOCl 的化学方程式是____。
2
(5)若锆石中含有ZrSiO 的质量分数是54.9%,在制备ZrO 的过程中损失10%的锆元素,则1kg锆石理论上
4 2
能够制得ZrO 的质量是____g。
2
20.(2022·北京·首都师范大学附属中学高三阶段练习)过氧化钙( )在水中能缓慢放出氧气,是一种
用途广泛的供氧剂,可用于鱼塘养殖。(1) 的电子式为_______。
(2) 与水反应的化学方程式是_______。
(3)由电石渣(主要成分为氢氧化钙)制备过氧化钙可实现工业废渣的资源化,其制备流程如下:
①滤液Y可循环使用,其主要溶质的质量与反应前的加入量几乎没有变化,该溶质是_______。解释其质
量不变的原因_______。(用化学方程式表示)。
②I和Ⅱ的反应装置均需置于冰水浴中,解释Ⅱ中冰水浴的作用:_______(答出一点即可)。
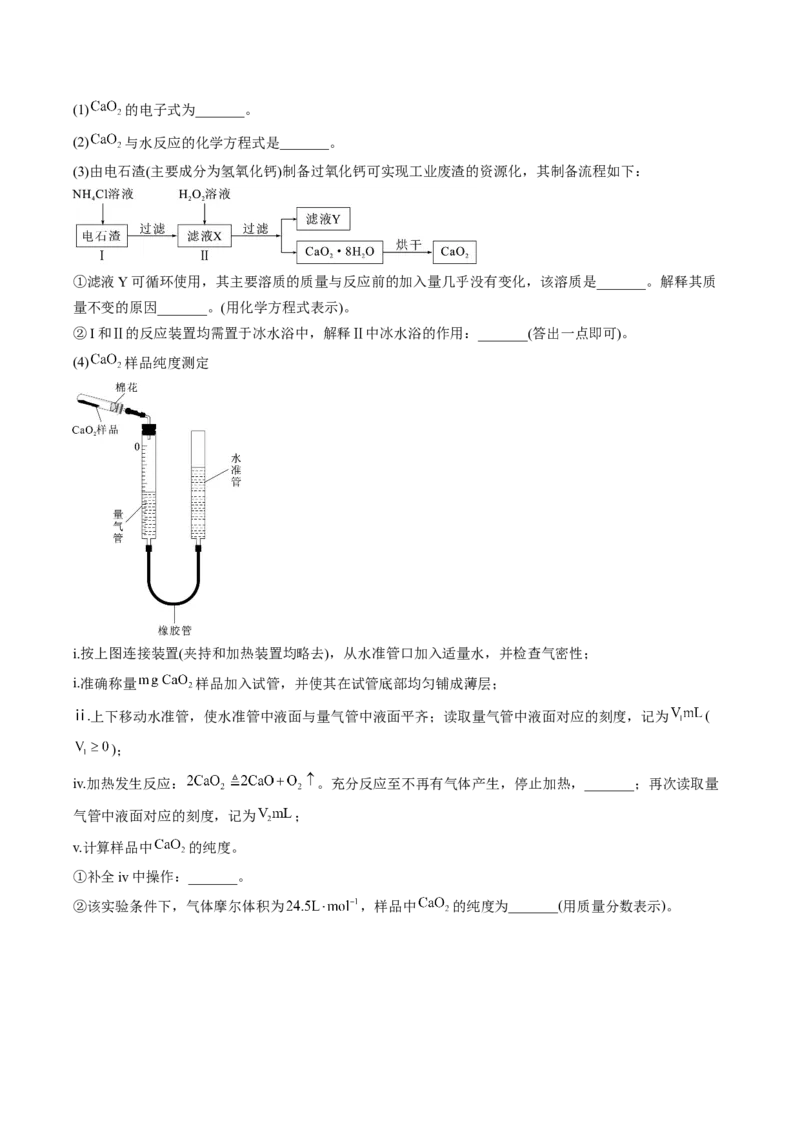
(4) 样品纯度测定
i.按上图连接装置(夹持和加热装置均略去),从水准管口加入适量水,并检查气密性;
i.准确称量 样品加入试管,并使其在试管底部均匀铺成薄层;
ⅱ.上下移动水准管,使水准管中液面与量气管中液面平齐;读取量气管中液面对应的刻度,记为 (
);
iv.加热发生反应: 。充分反应至不再有气体产生,停止加热,_______;再次读取量
气管中液面对应的刻度,记为 ;
v.计算样品中 的纯度。
①补全iv中操作:_______。
②该实验条件下,气体摩尔体积为 ,样品中 的纯度为_______(用质量分数表示)。