文档内容
第二篇 元素及其化合物
专项 16 新型化合物分析
近年来高考化学科命题出现以新型化合物为载体来测量自主学习的能力。以新型化合物为载体,可全
面检测学生的化学科学素养。新型化合物的正确解读便成了解题的关键,试题中介绍陌生无机物的任何内
容都可看做是信息,从信息呈现的方式看,可分为直接信息和潜在信息。高考试题中以新型化合物为载体
的考查,需从获取信息的角度来解读新型化合物。
1.(2022•湖北省选择性考试)硫代碳酸钠能用于处理废水中的重金属离子,可通过如下反应制备:
NaHS(s)+CS(l)=NaCS(s)+ H S(g),下列说法正确的是( )
2 2 3 2
A.NaCS 不能被氧化 B.NaCS 溶液显碱性
2 3 2 3
C.该制备反应是熵减过程 D.CS 的热稳定性比CO 的高
2 2
【答案】B
【解析】A项,NaCS 中硫元素为-2价,还原性比较强,能被氧化,故A错误;B项, 类比NaCO
2 3 2 3
溶液,O与S同主族,可知NaCS 溶液显碱性,故B正确;C项,由反应方程式可知,固体与液体反应制
2 3
备了硫化氢气体,故该制备反应是熵增过程,故C错误;D项,S的原子半径比O小,故C=S键长比C=O
键长长,键能小,故CS 的热稳定性比CO 的低,故D错误;故选B。
2 2
2.(2022•浙江6月选考)关于化合物:FeO(OCH)的性质,下列推测不合理的是( )
3
A.与稀盐酸反应生成FeCl 、CHOH、HO
3 3 2
B.隔绝空气加热分解生成FeO、CO、HO
2 2
C.溶于氢碘酸(HI),再加CCl 萃取,有机层呈紫红色
4
D.在空气中,与SiO 高温反应能生成Fe (SiO)
2 2 3 3
【答案】B
【解析】已知化合物:FeO(OCH)中Fe的化合价为+3价,CHO-带一个单位负电荷。A项,化合物:
3 3
1
原创精品资源学科网独家享有版权,侵权必究!
1
学科网(北京)股份有限公司FeO(OCH)中Fe的化合价为+3价,故其与稀盐酸反应生成FeCl 、CHOH、HO,反应原理为:
3 3 3 2
FeO(OCH)+3HCl=FeCl +H O+CHOH,A不合题意;B项,化合物:FeO(OCH)中Fe的化合价为+3价,C
3 3 2 3 3
为-2,若隔绝空气加热分解生成FeO、CO、HO则得失电子总数不相等,不符合氧化还原反应规律,即不
2 2
可能生成FFeO、CO、HO,B符合题意;C项,化合物:FeO(OCH)中Fe的化合价为+3价,故其溶于氢
2 2 3
碘酸(HI)生成的Fe3+能将I-氧化为I,反应原理为:2FeO(OCH)+6HI=2FeI +I +2H O+2CHOH,再加CCl
2 3 2 2 2 3 4
萃取,有机层呈紫红色,C不合题意;D项,化合物:FeO(OCH)在空气中高温将生成Fe O、CO 和
3 2 3 2
HO,然后Fe O 为碱性氧化物,SiO 为酸性氧化物,故化合物:FeO(OCH)与SiO 高温反应能生成
2 2 3 2 3 2
Fe (SiO),D不合题意;故选B。
2 3 3
3.(2021•浙江6月选考)关于化合物ClONO 的性质,下列推测不合理的是( )
2
A.具有强氧化性 B.与NaOH溶液反应可生成两种钠盐
C.与盐酸作用能产生氯气 D.水解生成盐酸和硝酸
【答案】D
【解析】A项,ClONO 里面含有正一价的氯元素和正五价的氮元素,具有强氧化性,A正确;B项,
2
ClONO 与NaOH溶液反应可生成次氯酸盐和硝酸盐,B正确;C项,ClONO 与盐酸发生归中反应生成氯
2 2
气,C正确;D项,ClONO 发生水解反应生成次氯酸和硝酸,D错误;故选D。
2
4.(2021•浙江1月选考)铝硅酸盐型分子筛中有许多笼状空穴和通道(如图),其骨架的基本结构单元是
硅氧四面体和铝氧四面体,化学组成可表示为M[(AlO )·(SiO)]·zHO(M代表金属离子)。
a 2 x 2 y 2
下列推测不正确的是( )
A.常采用水玻璃、偏铝酸钠在强酸溶液中反应后结晶制得分子筛
B.若a=x/2,则M为二价阳离子
C.调节y/x(硅铝比)的值,可以改变分子筛骨架的热稳定性
D.分子筛中的笼状空穴和通道,可用于筛分分子
【答案】A
【解析】A项,偏铝酸钠在强酸性溶液中不能稳定存在容易形成Al3+,不可以利用偏铝酸钠在强酸性
2
原创精品资源学科网独家享有版权,侵权必究!
2
学科网(北京)股份有限公司溶液中制备分子筛,A错误;B项,设M的化合价为m,则根据正负化合价代数和为0计算,m×
+x×(-1)=0,解得m=+2,B正确;C项,调节硅铝比可以改变分子筛的空间结构,从而改变分子筛的稳定
性,C正确;D项,调节硅铝比可以调节分子筛的孔径,根据分子筛孔径的大小可以筛分不同大小的分子,
D正确;故选A。
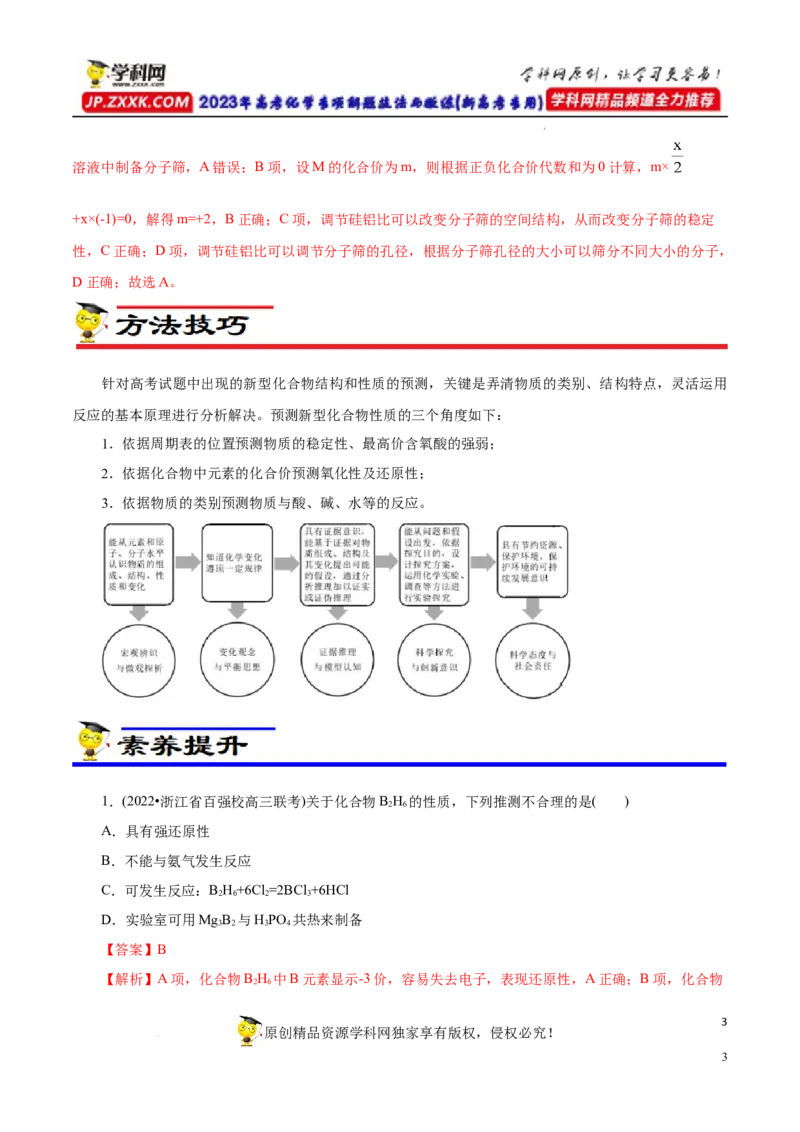
针对高考试题中出现的新型化合物结构和性质的预测,关键是弄清物质的类别、结构特点,灵活运用
反应的基本原理进行分析解决。预测新型化合物性质的三个角度如下:
1.依据周期表的位置预测物质的稳定性、最高价含氧酸的强弱;
2.依据化合物中元素的化合价预测氧化性及还原性;
3.依据物质的类别预测物质与酸、碱、水等的反应。
1.(2022•浙江省百强校高三联考)关于化合物B H 的性质,下列推测不合理的是( )
2 6
A.具有强还原性
B.不能与氨气发生反应
C.可发生反应:B H+6Cl=2BCl +6HCl
2 6 2 3
D.实验室可用MgB 与HPO 共热来制备
3 2 3 4
【答案】B
【解析】A项,化合物B H 中B元素显示-3价,容易失去电子,表现还原性,A正确;B项,化合物
2 6
3
原创精品资源学科网独家享有版权,侵权必究!
3
学科网(北京)股份有限公司B H 中B有空轨道,可以和氨气形成配位键,可以发生反应,B错误;C项,化合物B H 有还原性,氯气
2 6 2 6
有氧化性,可以发生氧化还原反应,B H+6Cl=2BCl +6HCl,C正确;D项,实验室可用MgB 与HPO
2 6 2 3 3 2 3 4
发生复分解反应来制备B H,方程式为:MgB +2H PO Mg(PO )+ B H↑,D正确;故选B。
2 6 3 2 3 4 3 4 2 2 6
2.(2022•浙江省新高考Z20联盟高三联考)SiS 的无限长链状结构截取部分如图所示。下列说法不正确
2
的是( )
A.92gSiS 中含有4mol共价键 B.SiS 为原子晶体
2 2
C.SiS 的熔沸点比CS 高 D.SiS 水解产生HS
2 2 2 2
【答案】B
【解析】A项,由无限长链状结构截图可知,SiS 中每个硅原子与4个硫原子形成4个硅硫键,则
2
92gSiS 中含有共价键的物质的量为 ×4=4mol,A正确;B项,SiS 的空间结构不是空间网状结构,
2 2
则SiS 不是原子晶体,是分子晶体,B错误;C项,SiS 与CS 为结构相似的分子晶体,SiS 的 相对分子
2 2 2 2
质量大于CS,分子间作用力大于CS,熔沸点比CS 高,C正确;D项,SiS 能与水发生水解反应生成
2 2 2 2
HSiO 和HS,D正确;故选B。
2 3 2
3.(2022•浙江省山水联盟高三联考)已知三氟化氯(ClF )是一种很强氧化剂和氟化剂,它能大多数有机
3
和无机材料甚至塑料反应,可以使许多材料不接触火源就燃烧,可应用于航天工业。下列推测不合理的是(
)
A.ClF 与水按照1:2反应只生成一种弱酸和一种强酸
3
B.能与一些金属反应生成氯化物和氟化物
C.三氟化氯可用于清洁化学气相沉积的反应舱附着的半导体物质
D.可以代替HO 充当火箭推进剂中的氧化物
2 2
【答案】A
【解析】A项,ClF 与水按照1:2发生反应ClF +2H O=3HF+HClO ,生成了两种弱酸,A错误;B项,
3 3 2 2
4
原创精品资源学科网独家享有版权,侵权必究!
4
学科网(北京)股份有限公司ClF 中Cl为+3价,有氧化性,故能与一些金属反应生成氯化物和氟化物,B正确;C项,三氟化氯与水反
3
应生成了HF,HF可与硅反应,故可用于清洁化学气相沉积的反应舱附着的半导体物质,C正确;D项,
因ClF 有氧化性,可以使许多材料不接触火源就燃烧,故可以代替HO 充当火箭推进剂中的氧化物,D正
3 2 2
确;故选A。
4.(2022•浙南名校联盟高三第一次联考)通过电氧化合成法可制得特殊高价金属化合物高铜酸钠(化学
式为NaCuO )。关于该物质的推测,下列有关说法不正确的是( )
2
A.NaCuO 具有强氧化性
2
B.NaCuO 与浓盐酸作用会产生无色无味气体
2
C.强碱性条件下,通过次氯酸钠氧化氢氧化铜可制得
D.NaCuO 与氢气反应可能有紫红色固体生成
2
【答案】B
【解析】A项,在高铜酸钠(化学式为NaCuO )中Cu元素化合价为+3价,不稳定,容易获得电子,表
2
现强氧化性,A正确;B项,NaCuO 具有强氧化性,浓盐酸具有强还原性,NaCuO 与浓盐酸混合会发生
2 2
氧化还原反应产生黄绿色有刺激性气味的气体Cl,B错误;C项,次氯酸钠具有强氧化性,在强碱性条件
2
下可以将氢氧化铜氧化产生NaCuO ,C正确;D项,H 具有强的还原性,NaCuO 具有强氧化性,二者在
2 2 2
一定条件下会发生氧化还原反应,H 将NaCuO 还原产生单质Cu,因此会看到可能有紫红色固体生成,D
2 2
正确;故选B。
5.(2022•浙江省十校联盟高三10月联考)关于化合物氨基磺酸(H N-SO H)的性质,下列推测不正确的
2 3
是( )
A.水溶液呈酸性 B.受热分解产物中可能含有N 和SO
2 2
C.常温下可能为固体 D.与足量 溶液混合后加热没有气体逸出
【答案】D
【解析】A项,氨基磺酸是一种硫酸的一个羟基被氨基取代而形成的无机固体酸,还可以继续电离出
一个氢离子,故具有酸性,故A正确;B项,氨基磺酸受热分解的化学方程式为HN-SO H
2 3
SO +N +SO+2H +H O,故B正确;C项,氨基磺酸(H N-SO H)能形成分子间氢键,熔沸点较高, 常温可
2 2 3 2 2 2 3
能为固体,故C正确;D项,HN-SO H+NaOH= H N-SO Na+ H O,氨基磺酸钠在碱性条件下不稳定,受
2 3 2 3 2
热易分解产生氨气,故加热后气体产生,故D错误;故选D。
6.(2022•浙江省云峰联盟高三10月联考)新型洗涤剂过氧碳酸钠(NaCO)固体,能瞬间清除衣服上的
2 4
5
原创精品资源学科网独家享有版权,侵权必究!
5
学科网(北京)股份有限公司汗渍、果汁等顽固污渍。它与水反应生成碳酸钠和其他化合物,关于过氧碳酸钠(NaCO)的性质,下列推
2 4
测不合理的是( )
A.过氧碳酸钠也可作为水体供氧剂
B.过碳酸钠中的氧元素有-1、-2两种价态
C.过氧碳酸钠能使酸性高锰酸钾溶液褪色,体现了过氧碳酸钠的强氧化性
D.过碳酸钠的水溶液既有碱性也有强氧化性
【答案】C
【解析】A项,过氧碳酸钠中含有过氧键,类比过氧化钠可知过氧碳酸钠可以和水反应生成氧气,故
过氧碳酸钠也可作为水体供氧剂,A正确;B项,根据正负化合价为零和氧元素的结构特征,可知过碳酸
钠中的氧元素有-1、-2两种价态,B正确;C项,过氧碳酸钠能使酸性高锰酸钾溶液褪色,此时过氧碳酸
钠中氧的化合价升高变成氧气,C错误;D项,与水反应生成碳酸钠可知过碳酸钠的水溶液既有碱性,过
氧碳酸钠中含有过氧键,就有强氧化性,D正确;故选C。
7.(2022•浙江省9 +1高中联盟高三联考)H O、HO 和HO (超氧化氢)等都属于氢氧化合物,其中HO
2 2 2 2 2
又叫超氧酸,与HO 化学性质相似,又有某些性质与HX(X=Cl、Br、I)相似。下列说法不正确的是( )
2 2
A.HO 在碱性条件下比酸性条件更易分解产生O
2 2
B.向品红溶液中加入足量HO ,红色褪去,加热后又恢复红色
2
C.HO 可与硝酸银溶液发生如下反应:HO +AgNO =AgO↓+HNO
2 2 3 2 3
D.KO 与冰水反应理论上可得到HO
2 2
【答案】B
【解析】A项,HO 又叫超氧酸,能和碱反应,故在碱性条件下更不能稳定存在,A正确;B项,HO
2 2
具有强氧化性,能使品红褪色,加热不能恢复,B错误;C项,HO 性质与卤化氢相似,故能和硝酸银反
2
应,方程式为:HO +AgNO =AgO↓+HNO ,C正确;D项,KO 与冰水反应理论上发生水解反应生成氢
2 3 2 3 2
氧化钾和HO ,D正确;故选B。
2
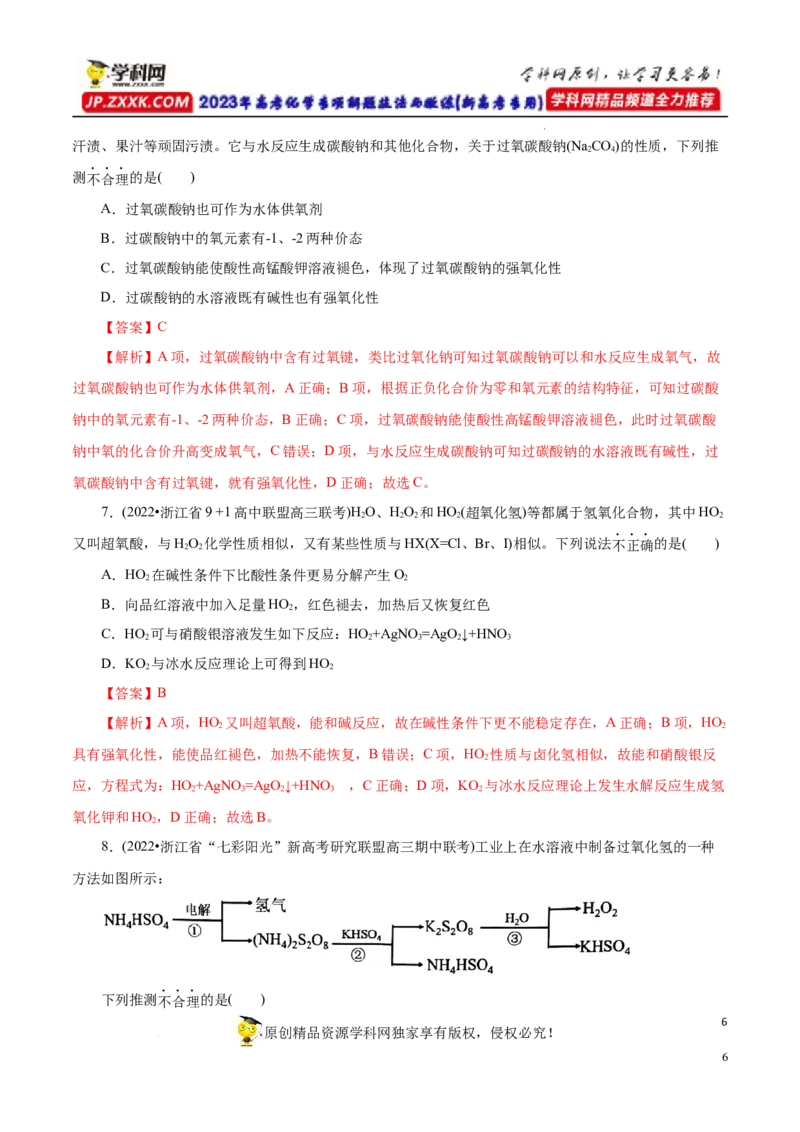
8.(2022•浙江省“七彩阳光”新高考研究联盟高三期中联考)工业上在水溶液中制备过氧化氢的一种
方法如图所示:
下列推测不合理的是( )
6
原创精品资源学科网独家享有版权,侵权必究!
6
学科网(北京)股份有限公司A.(NH )SO 具有强氧化性,硫化合价为+6
4 2 2 8
B.反应②可以发生的原因可能是KSO 水溶性较小
2 2 8
C.以上有两步反应为氧化还原反应
D.以上有两种物质可循环使用,体现了绿色化学理念
【答案】C
【解析】A项,(NH )SO 中含有过氧键,具有强氧化性,根据正负化合价的代数和为0,铵根显+1
4 2 2 8
价,SO2-的6个O显-2价、2个O显-1价,则硫显+6价,故A合理;B项,根据复分解反应的条件,反
2 8
应②可以发生的原因可能是KSO 水溶性较小,形成了沉淀,故B合理;C项,反应①是电解,为氧化还
2 2 8
原反应,反应②为复分解反应,不是氧化还原反应,反应③中没有元素化合价的变化,不是氧化还原反应,
只有一步反应为氧化还原反应,故C不合理;D项,根据流程图,硫酸氢钾和硫酸氢铵可以循环使用,体
现了绿色化学理念,故D合理;故选C。
9.(2022•浙江省杭州地区及周边重点中学高三联考)叠氮化钠(NaN )用作汽车司机安全防护袋(内有
3
)的气源:可用次氯酸钠溶液对含有NaN 的溶液进行销毁,产生无毒无害物质,下列说法不正确的是
3
( )
A.叠氮钠(NaN )水溶液呈碱性
3
B.当汽车受撞击时产生的 与 反应产物为NaO 和
2 2
C.安全防护袋内 可用 或KNO 代替
3
D.销毁时的反应:
【答案】B
【解析】根据题目信息叠氮化钠的化学式判断,钠的化合价为+1价,氮元素的化合价- ,根据氮的
化合价判断该物质的性质,根据产生无毒害物质判断,生成的是氮气。A项,叠氮钠会与水发生反应生成
氢氧化钠,故溶液显碱性,故A正确;B项,氧化铁的氧化性比较弱,不能生成过氧化钠,故B不正确;
C项,安全防护袋内的氧化物或硝酸钾含有氧都能与钠反应,处理生成钠,故C正确;D项,根据次氯酸
钠的氧化性判断,可以与叠氮化钠发生氧化还原反应,根据化合价升降守恒配平;故选B。
10.(2022•浙江省湖州、衢州、丽水三地市高三教学质量检测)化合物HOSOCl的性质,下列推测不合
2
7
原创精品资源学科网独家享有版权,侵权必究!
7
学科网(北京)股份有限公司理的是( )
A.具有酸性 B.与足量NaOH溶液反应可生成两种钠盐
C.与盐酸作用能产生SO D.水解生成盐酸和硫酸
2
【答案】C
【解析】A项,化合物HOSOCl结构类似硫酸,有羟基能电离出氢离子,具有酸性,故A正确; B
2
项,HOSOCl中S显+6价,Cl显示-1价,与足量NaOH溶液反应可生成硫酸钠和氯化钠,两种钠盐,故B
2
正确;C项,HOSOCl中S显+6价,Cl显示-1价,与盐酸作用不能发生氧化还原,故C错误;D项,
2
HOSOCl中Cl显示-1价,与水作用生成盐酸和硫酸,故D正确;故选C。
2
11.(2022•浙江省稽阳联谊学校高三联考)NaBO ·4H O的阴离子结构如图所示。硼砂(Na B O·10H O)
3 2 2 4 7 2
与氢氧化钠的混合溶液中加入双氧水可以制备NaBO ·4H O。下列说法不正确的是
3 2
A.硼砂与氢氧化钠、双氧水的反应为氧化还原反应
B.NaBO ·4H O具有杀菌消毒功能与漂白性
3 2
C.用酸性高锰酸钾处理NaBO ·4H O可以得到O
3 2 2
D.分别向同体积的硼砂溶液和蒸馏水中加入相同的少量盐酸,pH变化前者小
【答案】A
【解析】A项,硼砂中B元素为+3价,双氧水中O为-1价,据图可知NaBO ·4H O中含有过氧键,
3 2
有-1价的O元素,B元素为+3价,该反应的化学方程式应为
NaB O·10H O+2NaOH+4H O=4NaBO ·4H O,没有元素化合价发生变化,不是氧化还原反应,A错误;B
2 4 7 2 2 2 3 2
项,根据NaBO ·4H O中阴离子的结构可知,其含有过氧键,具有强氧化性,具有杀菌消毒功能与漂白性,
3 2
B正确;C项,根据双氧水可以被酸性高锰酸钾氧化生成氧气,可知用酸性高锰酸钾处理NaBO ·4H O可
3 2
以得到O,C正确;D项,硼砂为强碱弱酸盐,加入盐酸时其溶液中存在的水解平衡会起到缓冲作用,而
2
蒸馏水显中性,加入少量盐酸,pH都会发生突变,D正确;故选A。
12.(2022•浙江省金华十校高三选考模拟考试)关于化合物 HSO Cl的性质,下列推测不合理的是
3
8
原创精品资源学科网独家享有版权,侵权必究!
8
学科网(北京)股份有限公司( )
A.具有强氧化性
B.与足量NaOH溶液反应可生成两种钠盐
C.与盐酸作用能产生氯气
D.水解生成盐酸和硫酸
【答案】C
【解析】A项,化合物 HSO Cl中的硫化合价为+6价,具有强氧化性,故A正确;B项,化合物
3
HSO Cl与足量NaOH溶液反应可生成NaCl和NaSO 、HO,故B正确;C项,化合物 HSO Cl不能氧化
3 3 4 2 3
盐酸产生氯气,故C错误;D项,化合物 HSO Cl发生水解反应为,C HSOCl+ H O HSO4+ HCl,
3 3 2 2
故D正确;故选C。
13.(2022•浙江省绍兴市高三选考诊断性考试)关于化合物NH SCN (与NH CNO性质相似)的性质,下
4 4
列推测不合理的是( )
A.与NaNO 溶液共热产生N B.与铁盐反应生成血红色沉淀
2 2
C.与NaOH溶液共热产生氨气 D.加热后生成硫脲( )
【答案】B
【解析】A项,NH SCN中的N为-3价,NaNO 中N为+3价,两者可以发生氧化还原反应生成N,
4 2 2
故A正确;B项,NH SCN中的SCN-能和Fe3+反应生成血红色的Fe(SCN) ,Fe(SCN) 溶于水,不沉淀,故
4 3 3
B错误;C项,NH SCN中的NH +能和OH-共热生成氨气,故C正确;D项,NH CNO加热能生成尿素(
4 4 4
),NH SCN 与NH CNO性质相似,所以NH SCN 加热能生成硫脲( ),故D正确;
4 4 4
故选B。
14.(2022•浙江省温州市高三适应性测试)氨硼烷(H N-BH )是种有效、安全的储氢材料,可由硼烷
3 3
B H 和氨气合成,其结构与乙烷相似。下列关于氨硼烷的性质推测不合理的是( )
2 6
A.氨硼烷为分子晶体 B.其沸点比乙烷高得多
C.氨硼烷难溶于水 D.加热时可缓慢释放出H
2
【答案】C
9
原创精品资源学科网独家享有版权,侵权必究!
9
学科网(北京)股份有限公司【解析】A项,氨硼烷的结构与乙烷相似,为分子晶体,故A正确;B项,氨硼烷能形成分子间氢键,
其沸点比乙烷高,故B正确;C项,氨硼烷和水分子间形成氢键,氨硼烷能溶于水,故C错误;D项,氨
硼烷是有效、安全的储氢材料,加热硼烷氨时,它首先会聚合成(NH BH),如果继续加热,再继续聚合成
2 2 n
(NHBH) ,所以加热时可缓慢释放出H,故D正确;故选C。
n 2
15.(2022•浙江省五校高三联考)铝可用于制取高温金属陶瓷,将铝粉、石墨和二氧化钛等高熔点金属
氧化物按一定比例混合均匀,涂在金属表面,在高温下煅烧,在金属表面发生反应:
4Al+3TiO +3C=2Al O+3TiC,下列有关说法不正确的是( )
2 2 3
A.最终留在金属表面的涂层是耐高温的物质
B.该反应中氧化剂是C
C.Al O 是一种白色难溶于水的固体,有多种变体
2 3
D.TiC具有导电性,其导电能力随温度升高而增强,故表现出金属性
【答案】D
【解析】A项,在金属表面发生的此反应的目的是制取高温金属陶瓷,所以最终留在金属表面的涂层
是耐高温的物质,故A正确;B项,该反应中C的化合价从0价降低到-4价,做氧化剂,故B正确;C项,
Al O 是一种白色难溶于水的固体,有多种变体,故C正确;D项,金属的导电能力随温度升高而降低,故
2 3
D错误;故选D。
16.(2022•浙江省嘉兴市高三选考模拟测试)SOCl ( )极易水解,主要用于制备酰基氯化物。
2
下列关于SOCl 说法不正确的是( )
2
A.既有氧化性又有还原性
B.遇水反应生成SO 和HCl
3
C.可用作由MgCl ·6H O制取无水MgCl 的脱水剂
2 2 2
D.CHCOOH+ SOCl →CHCOCl+SO +HCl
3 2 3 2
【答案】B
【解析】A项,由SOCl 结构式知,S元素为+4价,Cl元素为-1价,O元素为-2价,+4硫元素化合价
2
可以升高到+6价,表现还原性,也可以降低到0价,表现氧化性,A正确;B项,由于SOCl 中S元素为
2
+4价,故遇水水解应生成SO 和HCl,B错误;C项,由于SOCl 极易水解,且产物HCl可抑制Mg2+水解,
2 2
故SOCl 可用作MgCl ·6H O的脱水剂,C正确;D项,根据SOCl 水解生成HSO (不稳定分解生成SO )和
2 2 2 2 2 3 2
10
原创精品资源学科网独家享有版权,侵权必究!
10
学科网(北京)股份有限公司HCl,知羟基可以取代SOCl 上氯原子生成HSO ,同理,乙酸羧基上羟基也可以取代SOCl 上氯原子,即
2 2 3 2
2个CHCOOH与1个SOCl 反应生成2个CHCOCl、1个SO 、1个HO,由于CHCOCl遇水水解,故产
3 2 3 2 2 3
物中1个CHCOCl与生成1个HO反应生成CHCOOH和HCl,故总反应为:CHCOOH+
3 2 3 3
SOCl →CHCOCl+SO +HCl,D正确;故选B。
2 3 2
17.(2022•浙江省普通高中强基联盟高三统一测试)关于化合物SiHCl,下列说法不正确的是( )
2 2
A.该化合物为四面体结构 B.与水反应产生H
2
C.与足量NaOH溶液反应生成两种盐 D.与盐酸混合无沉淀生成
【答案】D
【解析】A项,SiHCl 类似于甲烷的分子结构CH,C被Si取代,2个H被Cl取代故其结构为四面体
2 2 4
结构,A正确;B项,SiHCl 水解生成氢气,B正确;C项,SiHCl 与足量NaOH溶液反应生成硅酸钠和
2 2 2 2
盐酸两种盐,C正确;D项,与盐酸混合生成二氧化硅沉淀,D错误;故选D。
18.(2022•浙江省台州市高三选考科目教学质量评估)一定条件下,F 与水反应,生成物除了O 外,还
2 2
会生成次氟酸(HFO)、OF 等。下列推测不合理的是( )
2
A.F 与水反应还可能生成HO
2 2 2
B.HFO的分子结构中O原子位于H与F之间,O元素的化合价为-2价
C.HFO不稳定,分解生成HF与O
2
D.OF 是一种强氧化剂,与盐酸反应会生成HF、Cl、O 等
2 2 2
【答案】B
【解析】A项,根据氧化还原反应的规律,有化合价的降低就有化合价的升高,HO中O元素为-2价,
2
HO 中O元素为-1价,因为F为最强的非金属,反应时化合价不可能升高,所以F 与水反应还可能生成
2 2 2
HO,推断合理,故A正确;B项,HFO中若O元素为-2价,则F元素为+1价,与事实不符,故B错误;
2 2
C项,HFO不稳定,分解生成HF和氧气,故C正确;D项,OF 中O元素为+2价,与盐酸反应时被还原,
2
生成HF、氯气、氧气等,故D正确;故选B。
19.(2022•浙江省学军中学高三选考模拟测试)高能燃料乙硼烷是一种强还原性物质,结构与乙烷不同,
性质很活泼,在空气中自燃且易水解,下列有关说法正确的是( )
A.B H 的结构简式为HB-BH
2 6 3 3
B.可用NaBH 和稀硫酸反应制备B H:2NaBH +H SO =B H+Na SO +2H
4 2 6 4 2 4 2 6 2 4 2
C.B H 可以与Cl 发生反应:B H+Cl=B HCl+HCl
2 6 2 2 6 2 2 5
D.B H 可与甲醇反应:B H+6CH OH=2B(OCH )+6H
2 6 2 6 3 3 3 2
11
原创精品资源学科网独家享有版权,侵权必究!
11
学科网(北京)股份有限公司【答案】D
【解析】A项,乙烷的结构简式为HC-CH,因为乙硼烷的结构与乙烷不同,所以B H 的构简式错
3 3 2 6
误,其结构中两个H形成的是氢桥键( ),A错误;B项,因为B H 易水解,稀硫酸中B H
2 6 2 6
会发生水解,B错误;C项,B H 还原性强,Cl 氧化性强,B H 和Cl 反应生成BCl 和HCl,C错误;D
2 6 2 2 6 2 3
项,B H 还原性强,甲醇中羟基的氢活泼,可以被还原成H,D正确。故选D。
2 6 2
20.(2022•浙江省丽水市缙云中学等三校高三联考模拟)CaOCl 是一种常见的混盐(混盐:一种金属阳
2
离子与两种或两种以上的酸根离子形成的盐),下列说法不正确的是( )
A.CaOCl 有较强的氧化性
2
B.CaOCl 遇水呈碱性,需要密封保存
2
C.能与SO 反应生成新盐,每消耗1mol CaOCl ,转移的电子为2mol
2 2
D.含0.1molCaOCl 的饱和溶液中加入足量的浓硫酸,可析出0.1molCaSO 固体和2.24L Cl
2 4 2
【答案】D
【解析】由混盐定义可知,CaOCl 混盐中的酸根为Cl-和ClO-,次氯酸根具有强的氧化性,所以混盐
2
也具有较强的氧化性。A项,CaOCl 混盐中的酸根为Cl-和ClO-,ClO-有较强的氧化性,故A不符合题意;
2
B项,CaOCl 混盐中的酸根为Cl-和ClO-,ClO-易水解呈碱性,需要密封保存,故B不符合题意;C项,
2
ClO-能与SO 反应生成硫酸根生成新盐硫酸钙,每1molCaOCl 中含ClO-1mol,反应时变为Cl-转移的电子
2 2
为2mol,故C不符合题意;D项,CaOCl 与浓硫酸的反应为CaOCl +H SO (浓)=CaSO ↓+Cl↑+H O,只含
2 2 2 4 4 2 2
0.1molCaOCl 析出0.1molCaSO 固体,产生了0.1molCl ,但Cl 的体积与温度、压强有关,无法确定
2 4 2 2
0.1molCl 的体积,故D符合题意;故选D。
2
21.(2022•浙江省余姚市慈溪市高三适应性测试)关于化合物HOO-SO H的性质,下列推测不合理的是
3
( )
A.具有强氧化性 B.水解可生成HO 和HSO
2 2 2 4
C.具有强酸性 D.与足量NaOH溶液反应最终产物为NaSO 和HO
2 4 2 2
【答案】D
【解析】化合物HOO-SO H,根据结构和电负性分析,H元素显+1价,S元素显+6价,O元素显-1
3
和-2价。A项,HOO-SO H中S元素显+6价,具有强氧化性,故A正确;B项,HOO-SO H溶于水中发生
3 3
水解反应:HOO-SO H+HO= H O+H SO ,故B正确;C项,HOO-SO H水解可生成HSO ,具有强酸性,
3 2 2 2 2 4 3 2 4
12
原创精品资源学科网独家享有版权,侵权必究!
12
学科网(北京)股份有限公司故C正确;D项,NaSO 和HO 会结合成一种加和物x Na SO •yH O•zH O,故D错误;选D。
2 4 2 2 2 4 2 2 2
22.(2022•浙江省诸暨市高三选考诊断性考试)关于化合物(CN) 的性质,已知其性质与卤素单质相似。
2
下列推测不合理的是( )
A.(CN) +H O HCN+HOCN B.能与某些金属化合形成盐
2 2
C.AgCN难溶于水 D.(CN) 具有强还原性
2
【答案】D
【解析】A项,(CN) 的性质与卤素单质相似,则类似于氯气与水发生可逆反应,CN) +H O
2 2 2
HCN+HOCN,故A正确;B项,(CN) 性质活泼,能与活泼金属直接发生化合反应生成盐,故B正确;C
2
项,卤族离子和银离子结合都是难溶物,则AgCN难溶于水,故C正确;D项,氯气易得到电子,为常见
的氧化剂,则(CN) 具有强氧化性,故D错误;故选D。
2
23.(2022•浙江省精诚联盟高三份适应性联考)如图是石膏的部分层状结构,中间的虚线代表层与层的
分界线。已知: 。下列说法不正确的是( )
A.层与层之间通过氢键连在一起
B.每个HO连接在Ca2+和相邻两层各1个SO 2-的O上
2 4
C.无水CaSO 可用作吸水剂
4
13
原创精品资源学科网独家享有版权,侵权必究!
13
学科网(北京)股份有限公司D.加热图示所示石膏,只破坏层与层之间的作用力
【答案】D
【解析】A项,由图可知,层与层之间由水分子通过氢键连在一起,A正确;B项,由图可知,每个
HO连接在Ca2+和相邻两层各1个SO 2-的O上,B正确;C项,CaSO+2H O=CaSO·2H O,故无水CaSO
2 4 4 2 4 2 4
可用作吸水剂,C正确;D项,加热图示所示石膏,将失去结晶水而发生化学变化,故有化学键的断裂和
形成,而不仅仅破坏层与层之间的作用力,D错误;故选D。
24.(2022•浙江省金丽衢十二校高三第一次联考)已知Pb O 与HNO 溶液发生反应Ⅰ:
3 4 3
Pb O+4H+=PbO+2Pb2++2H O;PbO与酸化的MnSO 溶液发生反应Ⅱ:5PbO +2Mn2++4H++5 SO 2-=2 MnO -
3 4 2 2 4 2 4 4
+5PbSO+2H O。下列推断不正确的是( )
4 2
A.由反应Ⅰ可知,Pb O 中Pb(Ⅱ)和Pb(Ⅳ)含量之比为2∶1
3 4
B.由反应Ⅱ可知,氧化性:PbO >MnO -
2 4
C.Pb可与稀硝酸发生反应:3Pb+16HNO =3Pb(NO )+4NO↑+8HO
3 3 4 2
D.Pb O 可与盐酸发生反应:Pb O+8HCl=3PbCl +4H O+Cl ↑
3 4 3 4 2 2 2
【答案】C
【解析】A项,由反应Ⅰ可知,n(Pb2+):n(PbO )=2:1,则Pb O 中Pb(Ⅱ)和Pb(Ⅳ)含量之比为2∶1,
2 3 4
A正确;B项,由反应Ⅱ可知,氧化剂为PbO ,氧化产物为MnO -,则氧化性:PbO >MnO -,B正确;C
2 4 2 4
项,根据反应I,Pb(Ⅱ)可存在于硝酸溶液中,则Pb可与稀硝酸发生反应:
3Pb+8HNO =3Pb(NO )+2NO↑+4HO,C错误;D项,根据反应I,与酸反应后有PbO 存在,PbO 具有强
3 3 2 2 2 2
氧化性,可使氯离子变为氯气,则Pb O 可与盐酸发生反应:Pb O+8HCl=3PbCl +4H O+Cl ↑,D正确;故
3 4 3 4 2 2 2
选C。
25.白色固体NaSO 常用于织物的漂白,也能将污水中的某些重金属离子还原为单质除去。下列关于
2 2 4
NaSO 说法不正确的是( )
2 2 4
A.可以使品红溶液褪色
B.其溶液可用作分析化学中的吸氧剂
C.其溶液可以和Cl 反应,但不能和AgNO 溶液反应
2 3
D.已知隔绝空气加热NaSO 分解可生成SO ,则其残余固体产物中可能有NaSO
2 2 4 2 2 2 3
【答案】C
【解析】A项,NaSO 溶于水,会与溶解在水中的氧气反应产生SO ,SO 能使品红溶液褪色,所以
2 2 4 2 2
NaSO 的水溶液具有漂白性,A正确;B项,NaSO 溶液与少量氧气反应产生亚硫酸氢钠和硫酸氢钠两
2 2 4 2 2 4
14
原创精品资源学科网独家享有版权,侵权必究!
14
学科网(北京)股份有限公司种盐,反应方程式为:NaSO+O +H O=NaHSO +NaHSO ,所以NaSO 溶液可用作分析化学中的吸氧剂,
2 2 4 2 2 3 4 2 2 4
B正确;C项,NaSO 中S元素平均化合价为+3价,具有还原性,Cl 具有氧化性,AgNO 具有酸性和氧
2 2 4 2 3
化性,所以NaSO 与Cl 和AgNO 溶液都可以发生反应,C错误;D项,隔绝空气加热NaSO 分解可生
2 2 4 2 3 2 2 4
成SO 和两种盐NaSO、NaSO ,D正确;故选C。
2 2 2 3 2 3
26.五氧化二钒为两性氧化物,氧化性类似于二氧化锰。下列说法不正确的是( )
A.VO + 6NaOH = 2Na VO + 3H O
2 5 3 4 2
B.VO + 10HCl(浓) 2VCl + 5H O
2 5 5 2
C.VO 常作工业生产SO 的催化剂,以降低反应活化能
2 5 3
D.根据铝比钒活泼的性质,可以用铝热法冶炼钒
【答案】B
【解析】A项,五氧化二钒为两性氧化物,可与氢氧化钠反应生成盐和水,反应为:VO + 6NaOH =
2 5
2NaVO + 3H O,故A正确;B项,五氧化二钒的氧化性类似于二氧化锰,则五氧化二钒与浓盐酸发生氧
3 4 2
化还原反应生成氯气,反应为:VO + 6HCl(浓) 2VOCl + Cl (g) + 3HO,故B错误;C项,VO 常作
2 5 2 2 2 2 5
工业生产SO 的催化剂,催化剂可以降低反应活化能,加快反应速率,故C正确;D项,金属性强的金属
3
可以将金属性弱的金属从其氧化物中置换出金属单质,铝的金属性大于钒,可用铝与五氧化二钒反应制取
金属钒,即可以用铝热法冶炼钒,故D正确; 故选B。
27.由一种阳离子与两种或两种以上酸根阴离子组成的盐称为混盐。如混盐CaOCl 组成可看作:
2
CaCl •Ca(ClO) 。下列有关混盐的说法不正确的是( )
2 2
A.混盐CaOCl 水溶液具有漂白、杀菌消毒作用
2
B.混盐CaOCl 在酸性条件下可以产生氯气
2
C.混盐NaSO 的水溶液显碱性
4 2 3
D.混盐NaSO 与足量稀硫酸反应的离子方程式为:2S2-+SO2-+6H+=3S↓+3H O
4 2 3 3 2
【答案】D
【解析】A项,混盐CaOCl 组成可看作CaCl •Ca(ClO) ,CaOCl 水溶液中含有次氯酸根水解产物次氯
2 2 2 2
酸,具有漂白、杀菌消毒作用,A正确;B项,混盐CaOCl 在酸性条件下,氯离子和次氯酸根离子发生归
2
中反应,可以产生氯气,B正确;C项,混盐NaSO 等价于 NaS·Na SO ,两者均为强碱弱酸盐,水溶液
4 2 3 2 2 3
显碱性,C正确;D项,混盐NaSO 与足量稀硫酸反应的离子方程式为2S2-+2SO2+
4 2 3 3
+8H+=3S↓+4H O+SO ↑,D错误。故选D。
2 2
28.二水合甲醛次硫酸氢钠(NaHSO·HCHO·2H O)俗称“吊白块”,具有强还原性和漂白性,常温下
2 2
15
原创精品资源学科网独家享有版权,侵权必究!
15
学科网(北京)股份有限公司较为稳定,120 ℃以上产生甲醛、二氧化硫和硫化氢。下列关于 NaHSO·HCHO·2H O 的说法正确的是(
2 2
)
A.因其具有强还原性,可用作食品抗氧化剂
B.久置甲醛次硫酸氢钠溶液会有浑浊产生
C.据所学知识预测,NaHSO 中存在—O—O—结构
2
D.“吊白块”能使溴水褪色,体现了其漂白性
【答案】B
【解析】A项,甲醛次硫酸氢钠有毒,不可用作食品抗氧化剂,A错误;B项,久置甲醛次硫酸氢钠溶
液缓慢分解出二氧化硫和硫化氢会产生硫沉淀,B正确;C项,NaHSO· HCHO·2H O具有强还原性,不
2 · 2
存在强氧化性—O—O—结构,C错误;D项,甲醛能与溴水溶液反应,D 错误;故选B。
29.白磷的性质不太稳定,与过量氢氧化钠溶液反应,会歧化生成磷化氢与次磷酸钠,
P+3NaOH+3HO 3NaH PO +PH↑。已知:PH 是一种强还原性的无色剧毒气体,结构与NH 相似,在水
4 2 2 2 3 3 3
中溶解度却小得多,PH 在水中的碱性极弱。下列说法不正确的是( )
3
A.PH 还可以通过磷化钙(Ca P)与水反应制备
3 3 2
B.PH 与卤化氢反应的产物PH X极易水解
3 4
C.NaH PO 的水溶液呈碱性,是因为其酸根离子的水解程度大于其电离程度
2 2
D.气体中混有↑,可用重铬酸钾、漂白粉的悬浮液消除其毒性
【答案】C
【解析】A项,磷化钙(Ca P)与水反应可生成氢氧化钙和PH ,故A正确;B项,PH 在水中的碱性极
3 2 3 3
弱,说明PH 与卤化氢反应的产物PH X易水解,故B正确;C项,根据题给信息,碱过量,NaH PO 是正
3 4 2 2
盐,其酸根离子不会电离,故C错误;D项,重铬酸钾、漂白粉具有强氧化性,PH 具有强还原性,所以
3
气体中混有PH ,可用重铬酸钾、漂白粉的悬浮液消除其毒性,故D正确;故选C。
3
30.NCl 为黄色油状液体,可用于漂白,也用于柠檬等水果的熏蒸处理,其相关性质的说法不正确的
3
是( )
A.缓慢与水发生反应:NCl +2H O=HNO +3HCl
3 2 2
B.具有强氧化性,能与HCl气体反应生成Cl
2
C.很不稳定,受热或受震动时发生猛烈爆炸而分解,2NCl N↑+3Cl↑
3 2 2
D.遇碱迅速分解得到一种碱性气体和能杀灭新冠病毒的消毒液
【答案】A
16
原创精品资源学科网独家享有版权,侵权必究!
16
学科网(北京)股份有限公司【解析】A项,在NCl 中,N显-3价,Cl显+1价,缓慢与水发生反应:NCl +3H O=NH +3HClO,
3 3 2 3
HClO还可将NH 氧化为N,A不正确;B项,NCl 中Cl显+1价,HCl中Cl显-1价,NCl 与HCl中Cl元
3 2 3 3
素发生归中反应,生成Cl 和NH ,若HCl过量,则生成NH Cl,B正确;C项,NCl 很不稳定,对光、热、
2 3 4 3
有机化合物都十分敏感,甚至震动时都会发生猛烈爆炸,从而生成N 和Cl,C正确;D项,NCl 遇碱会
2 2 3
发生迅速分解,生成NH 和NaClO,NaClO可作杀灭新冠病毒的消毒液,D正确;故选A。
3
31.已知:100%硫酸吸收SO 可生成焦硫酸(分子式为HSO 或HSO ·SO );焦硫酸水溶液发生如下电
3 2 2 7 2 4 3
离:HSO(aq)=H+(aq)+ HS O- (aq),HS O-(aq) H+(aq)+ SO2-(aq) K =2.7×10-2。下列说法不正确的
2 2 7 2 7 2 7 2 7 2
是( )
A.焦硫酸具有强氧化性
B.NaSO 水溶液显中性
2 2 7
C.98%的HSO 可以表示为SO • HO
2 4 3 2
D.焦硫酸与水反应的化学方程式:HSO+H O=2HSO
2 2 7 2 2 4
【答案】B
【解析】A项,由浓硫酸中+6价硫具有强氧化性可知,焦硫酸中+6价硫也具有强氧化性,A正确;B
项,NaSO 可写成NaSO ·SO ,溶于水后SO 和水反应生成硫酸,溶液显酸性,B错误;C项,假设浓硫
2 2 7 2 4 3 3
酸的质量为100 g,则HSO 的质量为100 g×98%=98 g,HO的质量为100 g-98 g=2 g,则HSO 的物质的
2 4 2 2 4
量为 =1 mol,HO的物质的量为 = mol,故98%的HSO 可表示为HSO • HO,如
2 2 4 2 4 2
果把HSO 表示为SO ·H O,则98%的浓硫酸也可表示为SO • HO,C正确;D项,焦硫酸与水反应可
2 4 3 2 3 2
表示为HSO ·SO +H O=2HSO ,D正确。
2 4 3 2 2 4
32.根据资料显示:将Cu(OH) 溶于浓的NaOH溶液可得到蓝色透明溶液,蓝色透明溶液中的铜是以
2
四羟基合铜酸钠[Na Cu(OH) ]存在,关于该蓝色溶液下列说法不正确的是( )
2 4
A.该溶液不稳定,久置或加热易产生黑色沉淀
B.该溶液中逐滴滴加盐酸的反应现象为先产生白色沉淀后沉淀溶解
C.该溶液可以检验还原性糖
D.该溶液中加铝粉,可以产生气体同时产生红色黑色掺杂的固体,溶液最终变为无色
17
原创精品资源学科网独家享有版权,侵权必究!
17
学科网(北京)股份有限公司【答案】B
【解析】四羟基合铜酸钠[Na Cu(OH) ]中存在铜离子作为中心原子,羟基作为配体的四羟基合铜配离子,
2 4
由此分析。A项,该溶液不稳定,久置或加热易产生黑色的氧化铜沉淀,故A不符合题意;B项,向该溶
液中滴加盐酸,达一定量时可得到蓝色絮状不溶物(氢氧化铜)或者黑色不溶物(氧化铜),继续滴加,不溶物
可溶解,同时得到蓝色铜盐溶液,故B符合题意;C项,由于四羟基合铜酸钠[Na Cu(OH) ]中存在二价铜
2 4
离子,具有弱氧化性,能氧化还原性糖,直接加热或用沸水浴持续加热,其本身还原产物为砖红色的氧化
亚铜,该溶液可以检验还原性糖,故C不符合题意;D项,向该溶液中加入铝粉,产生氢气,同时出现红
色黑色掺杂的不溶细颗粒(主要为铜单质、氧化铜,伴随有氧化亚铜),溶液最终变无色,铝则以
[Na Cu(OH) ]形式存在,故D不符合题意;故选B。
2 4
33.硫化钠的溶液能溶解单质硫生成多硫化钠:NaS+(x-1)S=Na S。多硫化钠易燃,在酸性条件下不
2 2 x
稳定,并且能强烈吸潮性结晶。下列关于 NaS 的说法错误的是( )
2 x
A.NaS溶液久置在空气中,可能生成 NaS
2 2 x
B.酸性条件下NaS 发生分解,可能生成一种淡黄色沉淀与一种能使品红褪色的气体
2 x
C.NaS 应在远离火种、热源的阴凉、干燥处密封保存
2 x
D.NaS 具有一定氧化性,可以将葡萄糖中的醛基转化为羧基
2 x
【答案】B
【解析】A项,NaS溶液久置在空气中,部分S2-被空气中氧气氧化为S,结合题干信息可知,可能生
2
成 NaS,故A正确;B项, 酸性条件下NaS 发生分解,如果生成一种淡黄色沉淀(S单质)与一种能使品
2 x 2 x
红褪色的气体(SO ),根据得失电子守恒可知,在酸性条件下还应当有HS生成,而HS与SO 会发生反应,
2 2 2 2
不能在同一溶液中同时生成,故B错误;C项,多硫化钠易燃且能强烈吸潮性结晶,所以NaS 应在远离
2 x
火种、热源的阴凉、干燥处密封保存,故C正确;D项,醛基的还原性强,可以被Cu(OH) 等弱氧化剂优
2
化,NaS 中的S为- 价,能够降低到-2价,所以NaS 具有一定氧化性,可以将葡萄糖中的醛基转化为
2 x 2 x
羧基,故D正确;故选B。
34.(2022·江西省赣州市十六县市十七校高三期中)Fe(OH) 胶体的胶团结构如图所示,下列说法错误
3
的是( )
18
原创精品资源学科网独家享有版权,侵权必究!
18
学科网(北京)股份有限公司A.胶体粒子的直径介于1~100nm之间
B.Fe(OH) 胶体带正电
3
C.胶体能够稳定存在是因为吸附层微粒(即胶粒)存在静电斥力
D.电泳现象出现的原因是:扩散层与吸附层分离,带正电的胶粒向阴极移动
【答案】B
【解析】A项,按定义知,胶体粒子的直径介于1~100 nm之间,故A正确;B项,Fe(OH) 胶体不带
3
电,胶粒带正电,故B错误;C项,胶体整体上不带电,氢氧化铁胶体稳定存在的主要原因是氢氧化铁胶
粒带正电荷,相互排斥,不能聚沉,故C正确;D项,Fe(OH) 胶粒带正电,通电发生电泳,带正电的胶
3
粒向阴极移动,故D正确;故选B。
35.(2022·重庆市名校联盟高三联考)饱和FeCl 溶液与HO反应制得胶体的胶团结构如图所示。下列
3 2
说法正确的是( )
A.反应的离子方程式为:Fe3++3H O Fe(OH) ↓+3H+
2 3
B.FeCl 溶液能使血液凝聚,是因为FeCl 溶液是电解质,血液是胶体
3 3
C.由图可知,Fe(OH) 胶体带正电,在盛有Fe(OH) 胶体的U型管中插入石墨电极通电,阴极周围颜
3 3
色加深
D.Fe(OH) 受热分解可得一种碱性氧化物——Fe O
3 2 3
【答案】D
19
原创精品资源学科网独家享有版权,侵权必究!
19
学科网(北京)股份有限公司【解析】A项,该反应生成氢氧化铁胶体,不是沉淀,离子方程式为:Fe3++3H O Fe(OH) (胶体)
2 3
+3H+,故A错误;B项,FeCl 溶液是混合物,不属于电解质,FeCl 是电解质,故B错误;C项,Fe(OH)
3 3 3
胶体不带电,其中所含的胶粒因吸附离子带电,故C错误;D项,Fe(OH) 不稳定,受热分解成氧化铁,
3
氧化铁属于碱性氧化物,故D正确;故选D。
20
原创精品资源学科网独家享有版权,侵权必究!
20
学科网(北京)股份有限公司21
原创精品资源学科网独家享有版权,侵权必究!
21
学科网(北京)股份有限公司