文档内容
第六篇 物质结构与性质
专项 37 物质结构式的元素推断
利用元素及其化合物特殊组成与结构推断题,是近几年高考的热点题型,题目一般通过结构式,解题
时抓住这些关键特性,首先确定其为何种元素,然后以此为突破口,推知其他未知元素。
1.(2022•湖南选择性考试)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序
数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是( )
A.原子半径:X>Y>Z B.非金属性:Y>X>W
C.Z的单质具有较强的还原性 D.原子序数为82的元素与W位于同一主族
【答案】C
【解析】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1个共价键,
X、Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和,则X为C
元素、Y为O元素、Z为F元素、W为Si元素。A项,同周期元素,从左到右原子半径依次减小,则C、
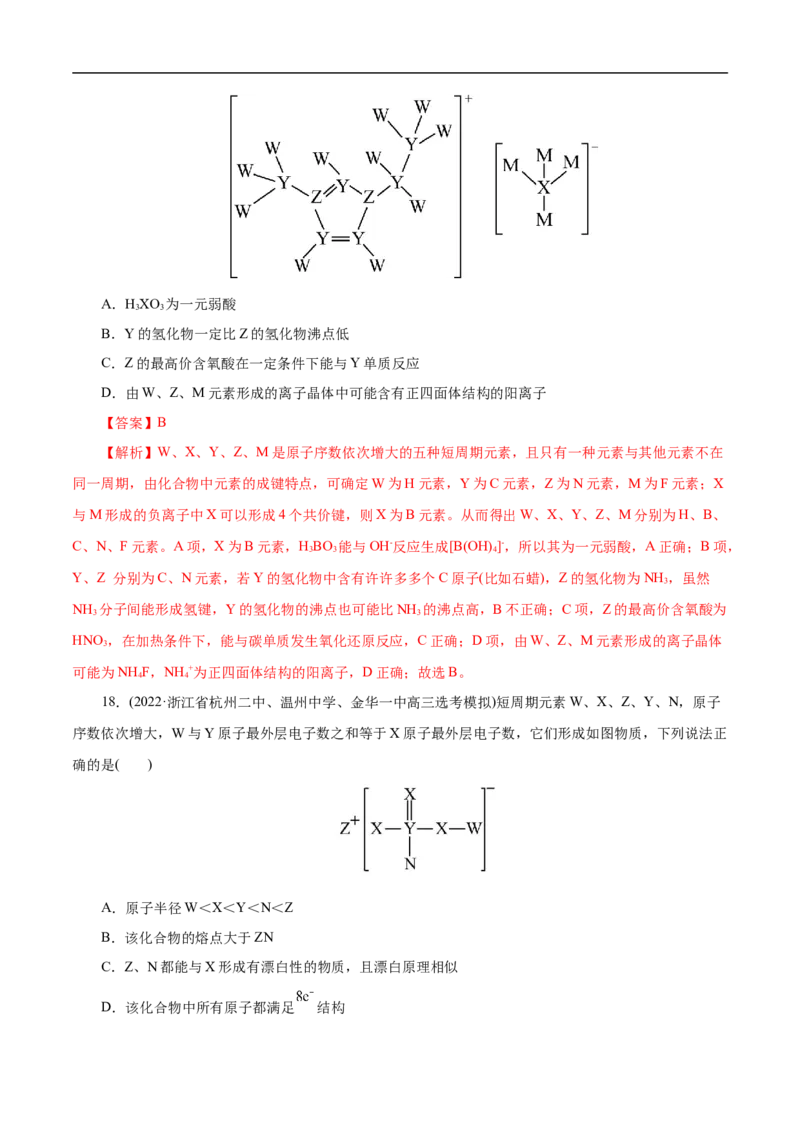
O、F的原子半径大小顺序为C>O>F,故A正确;B项,同周期元素,从左到右元素的非金属性依次增
强,同主族元素,从上到下元素的非金属性依次减弱,则C、O、Si的非金属性强弱顺序为O>C>Si,故
B正确;C项,位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;D
项,原子序数为82的元素为铅元素,与硅元素都位于元素周期表ⅣA族,故D正确;故选C。
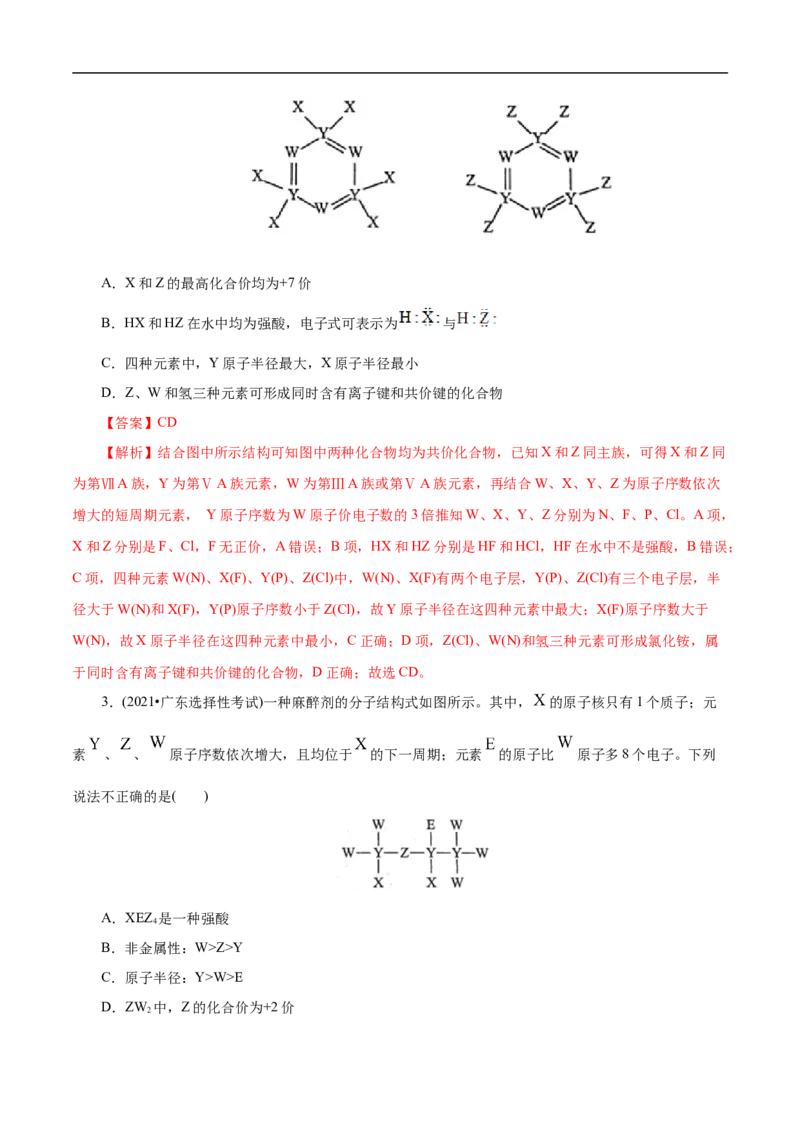
2.(2021•河北选择性考试)如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、X、
Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。下列说
法正确的是( )A.X和Z的最高化合价均为+7价
B.HX和HZ在水中均为强酸,电子式可表示为 与
C.四种元素中,Y原子半径最大,X原子半径最小
D.Z、W和氢三种元素可形成同时含有离子键和共价键的化合物
【答案】CD
【解析】结合图中所示结构可知图中两种化合物均为共价化合物,已知X和Z同主族,可得X和Z同
为第ⅦA族,Y为第ⅤA族元素,W为第ⅢA族或第ⅤA族元素,再结合W、X、Y、Z为原子序数依次
增大的短周期元素, Y原子序数为W原子价电子数的3倍推知W、X、Y、Z分别为N、F、P、Cl。A项,
X和Z分别是F、Cl,F无正价,A错误;B项,HX和HZ分别是HF和HCl,HF在水中不是强酸,B错误;
C项,四种元素W(N)、X(F)、Y(P)、Z(Cl)中,W(N)、X(F)有两个电子层,Y(P)、Z(Cl)有三个电子层,半
径大于W(N)和X(F),Y(P)原子序数小于Z(Cl),故Y原子半径在这四种元素中最大;X(F)原子序数大于
W(N),故X原子半径在这四种元素中最小,C正确;D项,Z(Cl)、W(N)和氢三种元素可形成氯化铵,属
于同时含有离子键和共价键的化合物,D正确;故选CD。
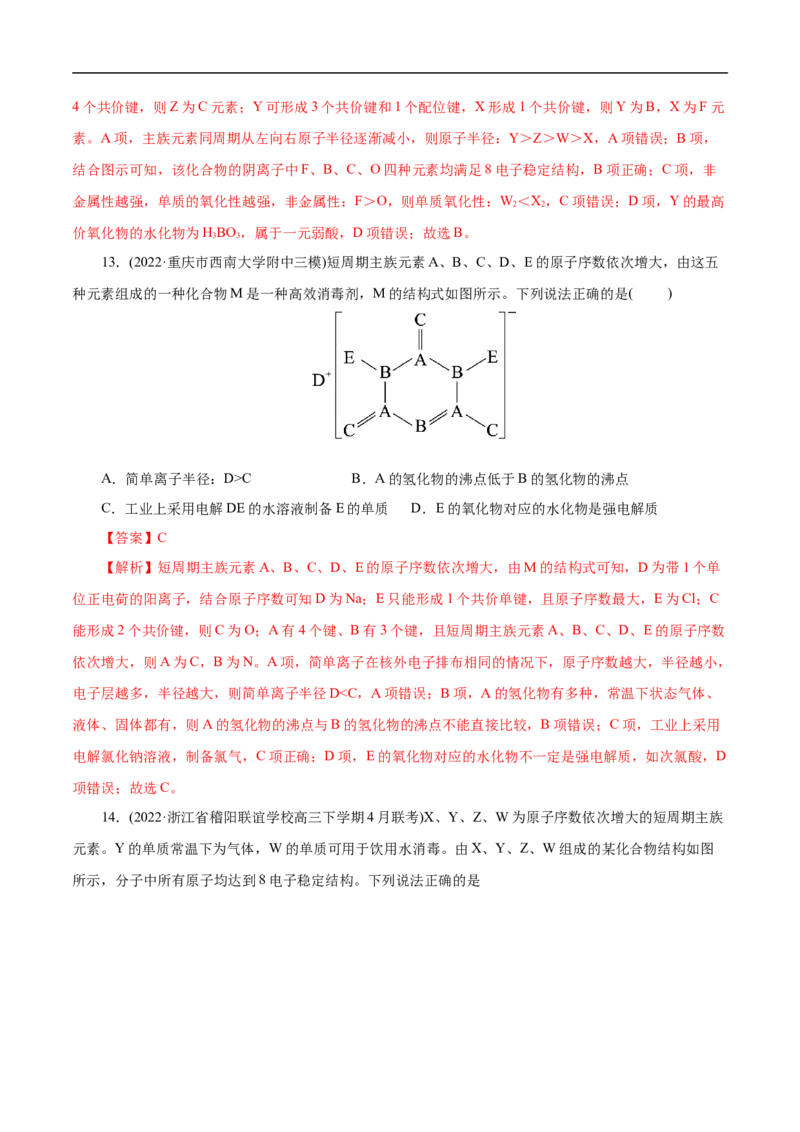
3.(2021•广东选择性考试)一种麻醉剂的分子结构式如图所示。其中, 的原子核只有1个质子;元
素 、 、 原子序数依次增大,且均位于 的下一周期;元素 的原子比 原子多8个电子。下列
说法不正确的是( )
A.XEZ 是一种强酸
4
B.非金属性:W>Z>Y
C.原子半径:Y>W>E
D.ZW 中,Z的化合价为+2价
2【答案】C
【解析】题给化合物结构中X、W、E均形成1个共价键、Y形成4个共价键、Z形成2个共价键。X
的原子核只有1个质子,则X为H元素;元素Y、Z、W原子序数依次增大,且均位于X的下一周期,即
第二周期元素,则Y为C元素,Z为O元素,W为F元素;元素E的原子比W原子多8个电子,则E为
Cl元素,综合以上分析可知,X、Y、Z、W、E分别为H、C、O、F、Cl元素。A项,氯元素非金属性较
强,其最高价氧化物的水化物HClO 是一种强酸,故A正确;B项,同一周期元素从左到右非金属性逐渐
4
增强,所以非金属性:F>O>C,故B正确;C项,同一周期从左到右原子半径逐渐减小,同一主族从上到
下原子半径逐渐增大,电子层越多半径越大,所以原子半径:Cl>C>F,故C错误; D项,OF 中,F为-1
2
价,则O的化合价为+2价,故D正确;故选C。
4.(2021•辽宁选择性考试)某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依
次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法正确的是( )
A.氢化物沸点: B.原子半径:
C.第一电离能: D.阴、阳离子中均有配位键
【答案】D
【解析】由题干信息可知,基态Z原子的电子填充了3个能级,其中有2个未成对电子,故Z为C或
者O,根据多孔储氢材料前驱体结构图可知Y周围形成了4个单键,再结合信息M、W、X、Y、Z五种元
素原子序数依次增大,故Y为N,故Z为O,M只形成一个单键,M为H,X为C,则W为B。A项,由
分析可知,X、Y的氢化物分别为:CH 和NH ,由于NH 存在分子间氢键,故氢化物沸点:X<Y,A错
4 3 3
误;B项,根据同一周期从左往右主族元素的原子半径依次减小,同一主族从上往下依次增大,故原子半
径:M<Z<Y<X,B错误;C项,根据同一周期从左往右元素的第一电离能呈增大趋势,IIA与IIIA,
VA与VIA反常,故第一电离能:W<X<Z<Y,C错误;D项,由于阳离子中的Y原子是N原子,形成
了类似于铵根离子的阳离子,故存在配位键,阴离子中的W为B,最外层上只有3个电子,能形成3个共
价键,现在形成了4个共价键,故还有一个配位键,D正确;故选D。
5.(2021•湖北选择性考试)某离子液体的阴离子的结构如图所示,其中W、X、Y、Z、M为原子序数
依次增大的短周期非金属元素,W是有机分子的骨架元素。下列说法正确的是( )A.Z元素的最高价态为+7 B.基态原子未成对电子数:W>Y
C.该阴离子中X不满足8电子稳定结构 D.最简单氢化物水溶液的pH:X>M
【答案】D
【解析】推断元素:W为有机物骨架元素,故W为碳元素;由图可知,Y形成1个双键,则其最外层
有6个电子,结合原子序数关系知,Y为氧元素,则X为氮元素;Z形成1个单键,则Z为氟元素;M的
成键总数为6,则M为硫元素。氟元素没有正化合价,A项错误;碳原子的电子排布式为1s22s22p2,未成
对电子数也为2,B项错误;-1价阴离子得到1个电子,故该阴离子中N形成2个单键,有2对孤对电子,
满足8电子稳定结构,C项错误;NH 的水溶液呈碱性,HS的水溶液呈酸性,故水溶液的 pH:NH >
3 2 3
HS,D项正确。
2
1.陌生物质中的信息突破
(1)化学键信息:如能形成1个共价键的元素为H、F、Cl,能形成4个共价键的元素为C、Si,能形成
2个共价键的元素为O、S。、
(2)根据形成的简单阴、阳离子可确定原子的最外层电子数,如 X2+和Y2-,即X、Y原子最外层电子数
分别为2和6。
(3)化合价信息:化合物中各元素化合价代数和为0,结合某些常见元素的化合价或化学键,可确定未
知元素的化合价,间接确定最外层电子数目。
2.“两步”快速突破元素推断题1.(2023届·河北省唐山市高三摸底考试)下图所示离子对应的钾盐易溶于水,常被用来鉴别Z元素某
种离子。其中X、Y、Z为前四周期原子序数依次增大的三种元素,X、Y为相邻元素,Z原子核外电子数
是X、Y原子质子数之和的2倍。下列说法错误的是( )
A.与Y同周期的主族元素中,只有一种元素的第一电离能大于Y的第一电离能
B.简单氢化物沸点:
C.基态Z原子的电子排布式: 1s22s22p63s23p63d5
D.该离子中σ键与π键的个数比为1∶1
【答案】C
【解析】X、Y、Z为前四周期原子序数依次增大的三种元素,X、Y为相邻元素,根据图示,Y能形
成3个共价键、X能形成4个共价键,则X是ⅣA族元素、Y是ⅤA族元素,Z原子核外电子数是X、Y
原子质子数之和的2倍,则X是C元素、Y是N元素,Z是Fe元素。K[Fe(CN) ]用来检验Fe2+。A项,与
3 6
N同周期的主族元素中,只有F元素的第一电离能大于N的第一电离能,故A正确;B项,NH 分子间能
3
形成氢键,所以简单氢化物沸点:CH<NH ,故B正确;C项,Fe是26号元素,基态Fe原子的电子排布
4 3
式:1s22s22p63s23p63d64s2,故C错误;D项,该离子中Fe3+与CN-通过配位键结合,配位键属于σ键,CN-
中存在碳氮叁键,叁键中有1个σ键和2个π键,所以该离子中有12个σ键,12个π键,σ键、π键的个
数比为1∶1,故D正确;故选C。
2.(2023届·湖南省益阳市高三质量检测)短周期元素W、R、X、Y、Z原子序数依次增大,可形成甲、
乙两种具有强还原性的物质(结构如下图),基态X原子的2p能级上只有1个电子,Z原子的最外层电子数
与电子层数相同。下列说法中错误的是( )
甲: 乙:
A.W、R、Y在元素周期表中位于同一主族
B.甲、乙两物质中W都显-1价
C.电负性:Y<ZD.Z元素最高价氧化物对应的水化物只能与酸反应,不能与碱反应
【答案】D
【解析】基态X原子的2p能级上只有1个电子,则X为B;Z原子的最外层电子数与电子层数相同,
且其原子序数比X大,则Z为Al;R、Y分别能形成R+、Y+,且R的原子序数小于B,Y的原子序数在B
和Al之间,故R为Li,Y为Na;W和B、Al分别构成两种阴离子[BW ]-和[AlW ]-,且W的原子序数比B
4 4
小,则W为H;综上所述,W为H,R为Li,X为B,Y为Na,Z为Al,甲为NaBH ,乙为LiAlH 。A项,
4 4
W为H,R为Li,Y为Na,三者均位于元素周期表中IA族,A正确;B项,W为H,甲为NaBH ,乙为
4
LiAlH ,两种物质中,H都显-1价,B正确;C项,Y为Na,Z为Al,Al的非金属性比Na强,所以Al的
4
电负性大于Na,C正确;D项,Z为Al,其最高价氧化物对应的水化物Al(OH) ,是两性氢氧化物,既可
3
以和酸反应,也能与碱反应,D错误;故选D。
3.(2023届·江西省五市九校高三第一次联考)物质M可用作调味剂、乳化剂、抗氧化增效剂、吸湿剂、
pH调节剂、增香剂、缓冲剂,其结构式如图所示。M的组成元素X、Y、Z、Q为原子序数依次增大的短
周期主族元素,且Y的一种核素常用于检测文物的年代。下列说法错误的是( )
A.物质M与稀硫酸反应生成的一种化合物中含有两种官能团
B.Y与Z分别形成的简单氢化物的沸点:Z>Y
C.Z、Q两种元素的简单离子半径:Q>Z
D.Y、Z两种元素形成化合物时,Z总显负价,说明非金属性:Z>Y
【答案】C
【解析】M的组成元素X、Y、Z、Q为原子序数依次增大的短周期主族元素,且Y的一种核素常用于
检测文物的年代,可知Y为C元素;结合M中X形成1个共价单键,且X的原子序数最小,可知X为H
元素;Z形成2个共价键,Z为O元素;Q可形成带1个单位正电荷的阳离子,结合原子序数可知Q为Na
元素,根据上述分析可知:X为H、Y为C、Z为O、Q为Na元素。A项,物质M与稀硫酸反应生成的有
机物为CHCHOHCOOH,分子物质中含羟基、羧基两种官能团,A正确;B项,Y为C、Z为O,元素的
3
非金属性:O>C,元素的非金属性越强,其简单氢化物的稳定性就越强,所以Y与Z分别形成的简单氢
化物的沸点:Z>Y,B正确;C项,Z为O、Q为Na,二者形成的简单离子O2-、Na+核外电子排布都是
2、8,离子的核外电子层结构相同,离子的核电荷数越大,离子半径就越小,所以离子半径:Q<Z,C错误;D项,Y为C、Z为O,二者都是非金属元素,原子之间通过共价键结合形成化合物。元素非金属性越
强,在形成化合物时,共用电子对就偏向吸引电子能力强的O元素,该元素化合价就显负价,吸引电子能
力弱的形成化合物时元素显正价,因此可根据Y、Z两种元素形成化合物时,Z总显负价,判断元素的非
金属性:Z>Y,D正确;故选C。
4.(2022·四川省成都市高三检测)麻黄素是中枢神经兴奋剂,结构式如图。其组成元素Y、X、W、Z
为原子序数依次增大的前两周期主族元素。下列说法正确的是( )
A.Y、W、Z三元素形成的化合物一定能抑制水的电离
B.氢化物沸点:Z>W>X
C.X、W、Z分别与Y 均可形成既含极性键又含非极性键的化合物
D.X与钙形成的化合物的电子式:
【答案】C
【解析】由麻黄素的结构式可知,Y周围只形成了1个共价键,X周围形成了4个共价键,W周围形
成了3个发共价键,Z周围形成了2个共价键,且组成元素Y、X、W、Z为原子序数依次增大的前两周期
主族元素,则可知Y为H、X为C、W为N、Z为O。A项,Y、W、Z三元素分别为H、N、O,则三种元
素形成的化合物不一定能抑制水的电离,如NH NO ,NH NO 由于NH +发生水解而促进水的电离,
4 3 4 2 4
NH ·H O由于电离出的OH-而抑制水的电离,A错误;B项,Z、W、X为O、N、C,由于C的氢化物种
3 2
类很多,沸点相差较大,则氢化物沸点大小无法比较,B错误;C项,X、W、Z分别为C、N、O与Y即
H均可形成既含极性键又含非极性键的化合物如CHCH、CH=CH 、NH、HO 等,C正确;D项,X即
3 3 2 2 2 4 2 2
C与钙形成的化合物即CaC ,则其电子式为: ,D错误;故选C。
2
5.(2022·东北三省三校高三第二次联合模拟考试)一种由短周期主族元素组成的化合物,其阴离子结构如图所示。W、X、Y、Z原子序数之和为20。下列有关叙述正确的是( )
A.还原性:ZW>WY B.原子半径:WC,单质氧化性O>C,氢化
2
物还原性HOZ>W
【答案】A
【解析】短周期主族元素X、Y、Z、W、R的原子序数依次增加,X、Y、W位于不同周期,常温下
X与Y可组成两种液态二元化合物,则X为H元素、Y为O元素;由缓冲溶液的主要成分结构中W为正
一价阳离子、R形成5个共价键可知,W为Na元素、R为P元素;由原子序数:3Y=Z+R可知,Z为F元
素。A项,磷元素的最高价氧化物对应的水化物磷酸为中强酸,故A错误;B项,元素的非金属性越强,
简单氢化物的稳定性越强,氧元素的非金属性弱于氟元素,所以水的稳定性弱于氟化氢,故B正确;C项,
过氧化氢和过氧化钠都具有强氧化性,都是具有漂白性的化合物,故C正确;D项,电子层结构相同的离
子,核电荷数越大,离子半径越小,所以简单离子的离子半径为O2—>F—>Na+,故D正确;故选A。
8.(2022·浙江省舟山市高三第三次模拟)Z、Y、X、W、Q为五种原子序数依次增大的短周期主族元素。
其中Z、Y、W分别位于三个不同周期,Y、Q位于同一主族,Y原子的最外层电子数是W原子的最外层
电子数的2倍,Y、X、W三种简单离子的核外电子排布相同。由Z、Y、X、W形成的某种化合物的结构
如图所示。下列说法不正确的是( )A.简单氢化物的稳定性:
B.该物质中所有原子均满足最外层 的稳定结构
C.X与Y、Y与Z均可形成含非极性共价键的化合物
D.W与X两者的最高价氧化物对应的水化物之间可发生反应
【答案】B
【解析】由结构图和题意可知,X为Na。而Z、Y、X、W、Q为五种原子序数依次增大的短周期主族
元素,其中Z、Y、W分别位于三个不同周期,则Z位于第一周期为H,Y位于第二周期,W位于第三周
期。Y、Q位于同一主族,Y原子的最外层电子数是W原子的最外层电子数的2倍,Y、X、W三种简单离
子的核外电子排布相同,且结构图中Y只能形成两个共价键,因此Y为O,Q为S,且W得一个电子后形
成四个共价键,W为Al。因此Z、Y、X、W、Q分别为H、O、Na、Al、S。A项,非金属性越强,其简
单氢化物越稳定,非金属性O>S,A正确;B项,该物质中H不满足8电子稳定结构,B错误;C项,H
与O形成的过氧化氢为含有非极性共价键的化合物,O与Na形成的过氧化钠为含有非极性共价键的化合
物,C正确;D项,氢氧化铝为两性氢氧化物,能与氢氧化钠溶液反应,D正确;故选B。
9.(2022·北京市中关村中学三模)2021年,英国剑桥大学Dominic S.Wright课题组设计了一种新型电
池中电解质(结构如图所示)的合成路线。已知X、Y、Z为原子序数依次增大的短周期主族元素,X的电负
性为4,三者的核外电子数之和等于35,Y与Z位于同一周期,则下列说法正确的是( )
A.简单离子的半径:X>Y
B.Z的最高价氧化物对应水化物是强酸
C.工业上常采用电解Y的氧化物冶炼单质Y
D.该化合物阴离子中各原子均满足8电子稳定结构
【答案】A
【解析】根据所给的结构为离子化合物,则Y+为Li+或Na+,X为负价元素,应为H或F(X、Y、Z序
数依次增大,X不是Cl),根据三者核外电子数之和为35,且X、Y、Z为原子序数依次增大,若X为H,
Y为Li,则Z的原子序数为31,不符合题意,若X为H,Y为Na,则Z的原子序数为23,不符合题意,
故X不为H,应为F,则Y为Na,Z为P。A项,X、Y分别为F、Na,F-和Na+电子结构相同,原子序数
越小半径越大,故F->Na+,A项正确;B项,Z为P,P最高价氧化物对应水化物为HPO ,不是强酸,B
3 4项错误;C项,工业上用电解熔融状态下的NaCl来冶炼Na,C项错误;D项,该化合物阴离子中P最外
层5个电子,得到1个电子、形成6个共价键,多于把电子结构,不满足8电子稳定结构,D项错误;故
选A。
10.(2022·江苏省南京师大附中高三模拟)M、W、X、Y、Z是同周期主族元素,X原子的最外层电子
数是W原子次外层电子数的3倍。它们形成的化合物可用作新型电池的电极材料,结构如图所示,化合物
中除 外其他原子均满足8电子稳定结构。下列说法正确的是( )
A.M的单质通常保存在煤油中
B.原子半径:
C.W的最高价氧化物对应的水化物是一元弱酸
D.WY 分子为含极性键的极性分子
3
【答案】C
【解析】M、W、X、Y、Z是同周期主族元素, X的最外层电子数是W次外层电子数的3倍, W有
两个电子层,次外层为2个电子, X为O元素,由盐的结构可知,Z可以形成四个共价键,且能与氧形成
双键,因此Z的最外层电子数为4 ,Z为C元素;四种元素位于同周期,且Y能形成一个共价键,Y为F
元素; W能形成4个共价键,W为B元素;新型电池材料,除M外均满足8电子稳定结构,M形成+1价
离子,M为Li元素;故M为Li元素, X为O元素, Y为F元素,Z为C元素,W为B元素。A项,M
为Li元素,Li单质密度比煤油小,不可以保存在煤油中,一般保存在石蜡油中,A错误;B项,W为B、
X为O、Y为F、Z为C,同周期从左到右,半径逐渐减小,半径关系为r(B)>r(C)>r(N)>r(O),B错误;C
项,W为B元素,W的最高价氧化物对应的水化物为HBO 为一元弱酸,C正确;D项,W为B、Y为
3 3
F,BF 分子中含有极性,中心原子B采取sp2杂化,没有孤对电子,空间构型为平面三角形,结构对称,
3
正负电荷的中心重合,属于非极性分子,D错误;故选C。
11.(2022·湖南省桃源县第一中学三模)有一种净水剂,结构如图所示,短周期元素X、Y、Z、W原子
序数依次增大,X、Y、Z分布在不同周期,X、Y原子的最外层电子数之和等于W原子的最外层电子数,
W与Z的原子序数相差4,下列叙述正确的是( )A.Y、Z的简单离子的半径Z>Y
B. 的水溶液中可能存在
C.X与Z不可形成离子晶体
D.Z、W的最高价氧化物对应的水化物之间不能发生反应
【答案】B
【解析】短周期元素X、Y、Z、W原子序数依次增大,X、Y、Z分布在不同周期,由结构可知,X
可形成1个共价键,Y能形成2个共价键,故可知X为H、Y为O,X、Y原子的最外层电子数之和等于W
原子的最外层电子数,则W最外层上有7个电子,即W为Cl,W与Z的原子序数相差4,则Z为Al。A
项,具有相同电子排布的离子,原子序数大的离子半径小,则Y、Z的简单离子的半径Y> Z,即O2->
Al3+,A错误;B项,铝离子有空轨道、氯离子有孤电子对,参照图中结构,二者可形成配位键,则ZW
3
即氯化铝水溶液中可能存在ZW-,B正确;C项, X与Z形成的AlH 属于离子晶体,C错误;D项,Z、
4 3
W的最高价氧化物对应的水化物分别为氢氧化铝和高氯酸,能发生中和反应,D错误;故选B。
12.(2022·河北省衡水中学高三模拟)短周期元素X、Y、Z、W是同周期主族元素,W元素形成的某
种单质具有强氧化性,可用于杀菌消毒。四种元素与锂组成的盐是一种新型的锂离子电池的电解质,结构
如图所示(→表示配位键),下列说法正确的是( )
A.原子半径:X>Y> Z> W
B.图中阴离子部分中四种元素均满足8电子稳定结构
C.单质氧化性:W> X
2 2
D.Y的最高价氧化物的水化物为强酸
【答案】B
【解析】短周期元素X、Y、Z、W是同周期主族元素,W元素形成的某种单质具有强氧化性,可用
于杀菌消毒,结合图示可知,W形成2个共价键,则W为O元素,说明四种元素均位于第二周期;Z形成4个共价键,则Z为C元素;Y可形成3个共价键和1个配位键,X形成1个共价键,则Y为B,X为F元
素。A项,主族元素同周期从左向右原子半径逐渐减小,则原子半径:Y>Z>W>X,A项错误;B项,
结合图示可知,该化合物的阴离子中F、B、C、O四种元素均满足8电子稳定结构,B项正确;C项,非
金属性越强,单质的氧化性越强,非金属性:F>O,则单质氧化性:W<X,C项错误;D项,Y的最高
2 2
价氧化物的水化物为HBO,属于一元弱酸,D项错误;故选B。
3 3
13.(2022·重庆市西南大学附中三模)短周期主族元素A、B、C、D、E的原子序数依次增大,由这五
种元素组成的一种化合物M是一种高效消毒剂,M的结构式如图所示。下列说法正确的是( )
A.简单离子半径:D>C B.A的氢化物的沸点低于B的氢化物的沸点
C.工业上采用电解DE的水溶液制备E的单质 D.E的氧化物对应的水化物是强电解质
【答案】C
【解析】短周期主族元素A、B、C、D、E的原子序数依次增大,由M的结构式可知,D为带1个单
位正电荷的阳离子,结合原子序数可知D为Na;E只能形成1个共价单键,且原子序数最大,E为Cl;C
能形成2个共价键,则C为O;A有4个键、B有3个键,且短周期主族元素A、B、C、D、E的原子序数
依次增大,则A为C,B为N。A项,简单离子在核外电子排布相同的情况下,原子序数越大,半径越小,
电子层越多,半径越大,则简单离子半径DY>Z
B.氧化物对应的水化物的酸性:W>Y>X
C.氢元素与X、Y、Z均能形成两种或两种以上的二元化合物
D.Y的单质与镁反应的产物既含离子键、又含共价键
【答案】C
【解析】根据题意,W的单质可用于饮用水消毒,且形成1个共价键,则应是Cl元素;该分子中所有
原子均达到8电子稳定结构,Y可以形成3个共价键,则Y原子最外层应有5个电子,其单质常温下为气
体,则Y为N元素;X可以形成4个共价键,且原子序数小于N元素,则X为C元素,Z可以形成2个共
价键,原子序数大于N小于Cl,则为O或S元素。A项,若Z为S元素,则原子半径:S>C>N,A错误;
B项,最高价氧化物对应的水化物的酸性:W>Y>X,然题中没有注明“最高价”,无法比较酸性强弱,B
错误;C项,H元素可以和C元素形成CH、C H 等多种烃类化合物,H元素可以和N元素形成NH 、
4 2 6 3
NH 等化合物,H元素可以和O元素形成HO、HO 两种化合物,可以和S元素形成HS、HS 两种化合
2 4 2 2 2 2 2 2
物,C正确;D项,Y的单质为N,与Mg反应生成MgN,只含离子键,不含共价键,D错误;故选C。
2 3 2
15.(2022·浙江省杭州教学质量检测二模)有一种化合物是很多表面涂层的重要成分,其结构如图所示.
其中W、X、Y、Z为原子序数依次增大的短周期元素,只有X、Y在同一周期,Z的单质是黄绿色气体;
下列有关说法不正确的是( )
A.非金属性强弱比较:Y>X
B.XW 的沸点高于WY的沸点
4 2
C.X的含氧酸有一元弱酸、二元弱酸等
D.ZY中所有原子最外层都满足8电子结构
2【答案】B
【解析】根据题意,W、X、Y、Z为原子序数依次增大的短周期元素,Z的单质是黄绿色气体,Z为
氯;只有X、Y在同一周期, 则W为氢,位于第一周期,XY位于第二周期;由结构可知,XY形成共价
键数分别为4、2,则XY分别为碳、氧。A项,同周期从左到右,金属性减弱,非金属性变强,非金属性
强弱比较:Y>X,A正确;B项,氧电负性较强,水分子中可以形成氢键,故CH 的沸点低于HO的沸点,
4 2
B错误;C项,碳的含氧酸有一元弱酸醋酸、二元弱酸碳酸等,C正确;D项,ClO 中氯、氧原子的最外
2
层都满足8电子结构,D正确;故选B。
16.(2022·浙江省名校协作体高三下学期化学模拟联考)如图所示化合物是合成纳米管原料之一,W、
X、Z、Y是原子半径逐渐减小的短周期元素,且原子序数均为奇数,Z元素无正化合价,W与Z同周期。
则下列叙述正确的是( )
A.液态XY 气化过程中需要破坏X和Y之间的共价键
3
B.气态氢化物的稳定性:X>Z
C.离子半径:Y-Li+,C错误;D项,与W同主族短周期
元素形成的单质即铝,铝可以与氢氧化钠溶液反应产生氢气,D正确;故选D。
17.(2022·浙江省五校高三联考)W、X、Y、Z、M是构成如图所示离子液体的五种短周期元素,原子
序数依次增大且只有一种元素与其他元素不在同一周期。下列有关说法不正确的是( )A.HXO 为一元弱酸
3 3
B.Y的氢化物一定比Z的氢化物沸点低
C.Z的最高价含氧酸在一定条件下能与Y单质反应
D.由W、Z、M元素形成的离子晶体中可能含有正四面体结构的阳离子
【答案】B
【解析】W、X、Y、Z、M是原子序数依次增大的五种短周期元素,且只有一种元素与其他元素不在
同一周期,由化合物中元素的成键特点,可确定W为H元素,Y为C元素,Z为N元素,M为F元素;X
与M形成的负离子中X可以形成4个共价键,则X为B元素。从而得出W、X、Y、Z、M分别为H、B、
C、N、F元素。A项,X为B元素,HBO 能与OH-反应生成[B(OH) ]-,所以其为一元弱酸,A正确;B项,
3 3 4
Y、Z 分别为C、N元素,若Y的氢化物中含有许许多多个C原子(比如石蜡),Z的氢化物为NH ,虽然
3
NH 分子间能形成氢键,Y的氢化物的沸点也可能比NH 的沸点高,B不正确;C项,Z的最高价含氧酸为
3 3
HNO,在加热条件下,能与碳单质发生氧化还原反应,C正确;D项,由W、Z、M元素形成的离子晶体
3
可能为NH F,NH +为正四面体结构的阳离子,D正确;故选B。
4 4
18.(2022·浙江省杭州二中、温州中学、金华一中高三选考模拟)短周期元素W、X、Z、Y、N,原子
序数依次增大,W与Y原子最外层电子数之和等于X原子最外层电子数,它们形成如图物质,下列说法正
确的是( )
A.原子半径W<X<Y<N<Z
B.该化合物的熔点大于ZN
C.Z、N都能与X形成有漂白性的物质,且漂白原理相似
D.该化合物中所有原子都满足 结构【答案】C
【解析】短周期元素W、X、Z、Y、N,原子序数依次增大,W与Y原子最外层电子数之和等于X原
子最外层电子数,它们形成如图物质,根据结构式可知Z位于第ⅠA族,X位于第ⅥA族,因此X是O,
W是H,Z是Na,Y的最外层电子数是6-1=5,Y是P,N形成一个单键,原子序数最大,所以N是
Cl。可知W、X、Z、Y、N分别是H、O、Na、P、Cl。A项,同周期自左向右原子半径逐渐减小,同主族
从上到下原子半径逐渐增大,则原子半径W<X<N<Y<Z,A错误;B项,该化合物中离子键强度小于
氯化钠中离子键强度,所以其熔点小于NaCl,B错误;C项,Z、N都能与X形成有漂白性的物质,即
NaO 和ClO ,都具有强氧化性,因此漂白原理相似,C正确;D项,该化合物中H、P原子不满足8 e-结
2 2 2
构,D错误;故选C。