文档内容
专项训练 热重曲线的计算(解析版)
一、单选题
1.W、X、Y是三种短周期主族元素且分别位于三个周期,X和Y位于同一主族且原
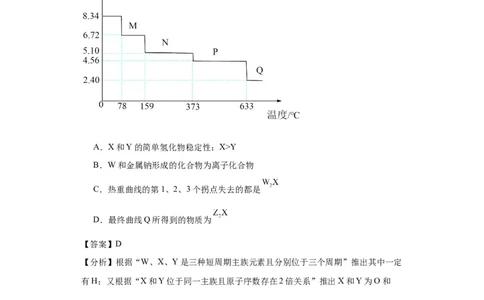
子序数存在2倍关系。 (M=278g/mol)的热重曲线(空气中加热)如图所示。
下列说法不正确的是
A.X和Y的简单氢化物稳定性:X>Y
B.W和金属钠形成的化合物为离子化合物
C.热重曲线的第1、2、3个拐点失去的都是
D.最终曲线Q所得到的物质为
【答案】D
【分析】根据“W、X、Y是三种短周期主族元素且分别位于三个周期”推出其中一定
有H;又根据“X和Y位于同一主族且原子序数存在2倍关系”推出X和Y为O和
S,则W为H,结合化合物的化学式,知X为O,Y为S。根据 的
,推出乙的摩尔质量为 ,故Z为Fe,该物质为 。
【详解】A.同一主族元素自上而下简单氢化物的热稳定性逐渐减弱,故稳定性:
,A正确;
B.NaH是由 和 构成的离子化合物,B正确;
资料收集整理【淘宝店铺:向阳百分百】C.8.34g的 的物质的量为0.03mol,结合M、N、P的质量计算,第一个
拐点失去0.09mol ,第二个拐点失去0.09mol ,第三个拐点失去0.03mol
,C正确;
D.最终剩余的是Fe的氧化物,其中Fe的物质的量为0.03mol,质量为1.68g,则O的
质量为0.72g,物质的量0.045mol, ,故最终曲线Q所
得物质为 ,D错误;
故选D。
2.化合物 是分析化学中重要的基准物质,其中X、Y、Z、T
分别位于三个短周期,原子序数依次增加;T与Z同主族;常温下 为气体,其分
子的总电子数为奇数;W为常见的金属元素,在该化合物中W离子的价层电子排布式
为 。在惰性气体氛围中该物质的热重曲线如图所示。下列说法错误的是
A.简单离子半径:T>Y>Z
B.W元素位于元素周期表的d区
C.简单气态氢化物的稳定性:Z>Y
D.580℃热分解后得到的固体化合物是WZ
【答案】D
【分析】X、Y、Z、T分别位于三个短周期,原子序数依次增加,W为常见的金属元
素,在该化合物中W离子的价层电子排布式为 ,则W为Fe元素,Fe2+的价层电子
排布式为 ,常温下 为气体,其分子的总电子数为奇数, 为NO ,总电子数
2
资料收集整理【淘宝店铺:向阳百分百】为23,Y为N,Z为O,T与Z同主族,T为S元素,该化合物为
可以推知X为H元素,以此解答。
【详解】A.根据题意可知元素X、Y、Z、T、W分别为H、N、O、S、Fe。一般电子
层数越多,离子半径越大;离子核外电子层结构相同时,原子序数越小,离子半径越
大,则简单离子半径: ,A正确;
B.铁元素位于元素周期表的d区,B正确;
C.简单气态氢化物的稳定性: ,C正确;
D.该化合物为 ,相对分子质量为392,取1 mol该物质进行热
重分析,根据热重分析曲线可知,580℃热分解后得到的固体的质量
g,故为0.5 mol
,D错误;
故选D。
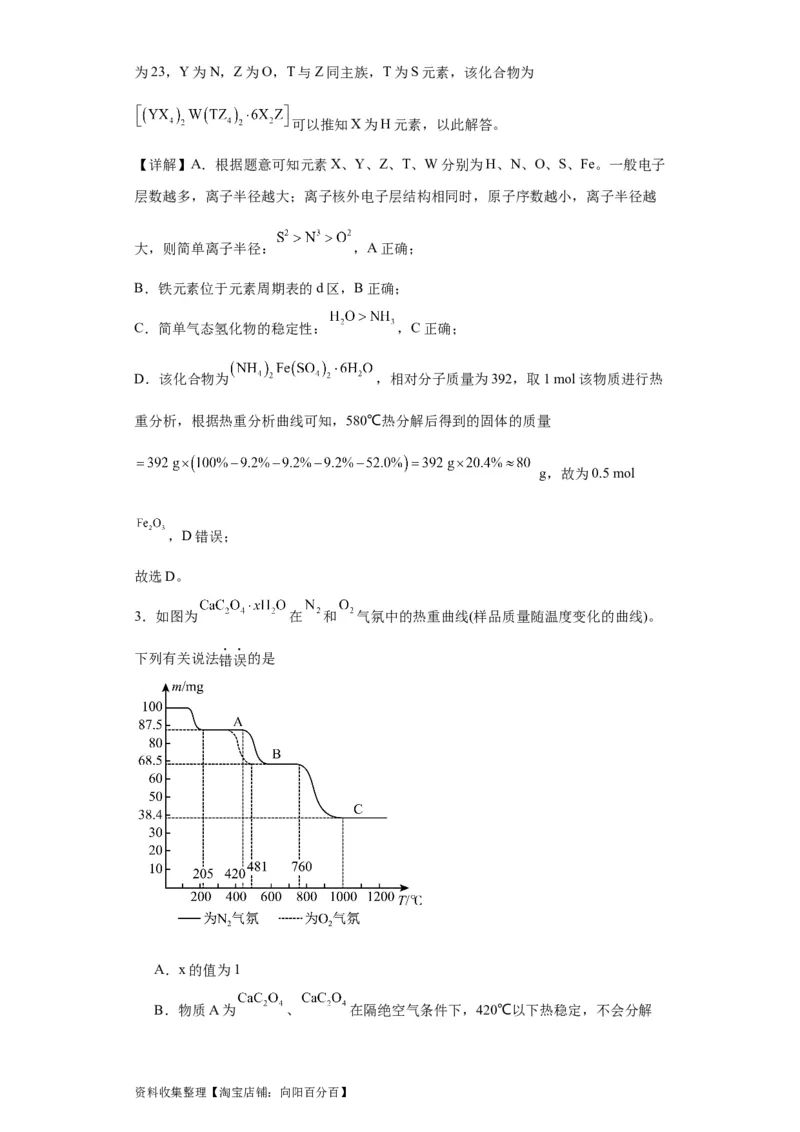
3.如图为 在 和 气氛中的热重曲线(样品质量随温度变化的曲线)。
下列有关说法错误的是
A.x的值为1
B.物质A为 、 在隔绝空气条件下,420℃以下热稳定,不会分解
资料收集整理【淘宝店铺:向阳百分百】C.800℃-1000℃氮气气氛中的反应为
D.无论是 气氛还是 气氛,当1个 最终转变为C时,转移电子
的个数不同
【答案】C
【分析】第1步质量由100mg减小到87.5mg,该反应为 CaC O·H O失去结晶水生成
2 4 2
CaC O;第2步质量由87.5mg减小到68.5mg,减少了21.7%,故反应为CaC O 分解
2 4 2 4
生成CaCO 与碳的氧化物;第3步质量由68.5mg减小到38.4mg,减少了44%,故继续
3
加热固体,碳酸钙分解生成氧化钙和二氧化碳,所以A为CaC O,B为CaCO ,C的
2 4 3
固体是CaO,据此分析作答。
【详解】A.第1步质量由100mg减小到87.5mg,该反应为 CaC O·H O失去结晶水
2 4 2
生成CaC O,根据质量守恒定律有 ,解得x=1,A正确;
2 4
B.420℃以下氮气气氛中,A的质量随温度升高保持不变,说明420℃以下CaC O 在
2 4
隔绝空气条件下,较稳定,不会分解,B正确;
C.由分析可知,800℃-1000℃氮气气氛中的反应为CaCO CaO+CO ↑,C错误;
3 2
D.C为CaO,O 气氛中1个 CaC O·H O最终转变为1个 HO、1个CaO和2个
2 2 4 2 2
CO,电子转移2个,在N 气氛中,1个 CaC O·H O最终转变为1个HO、1个
2 2 2 4 2 2
CaO、1个 CO 和1个CO,电子转移1个,转移电子的个数不同,D正确;
2
故选C。
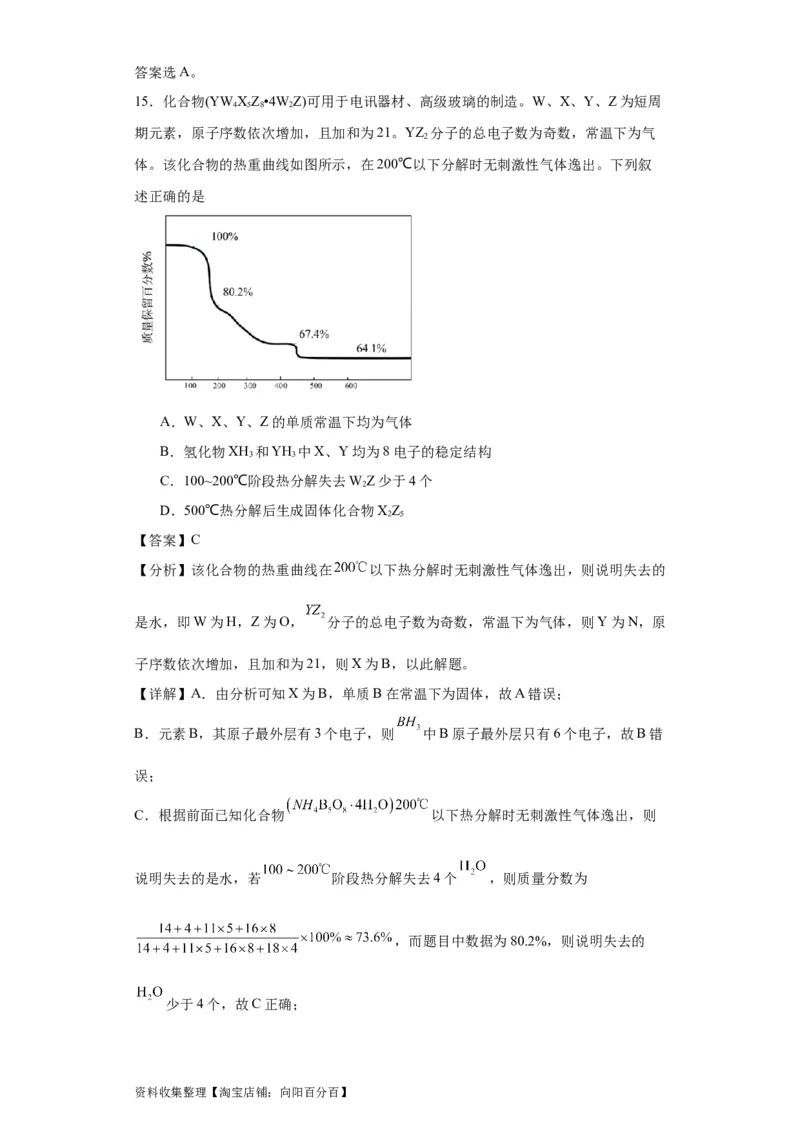
4.化合物( )可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周
期元素,原子序数依次增加,且加和为21, 分子的总电子数为奇数,常温下为气
体。该化合物的热重曲线如图所示,在200℃以下分解时无刺激性气体逸出。下列叙
述错误的是
资料收集整理【淘宝店铺:向阳百分百】A.W与Y可形成既含极性键也含非极性键的化合物
B.最高价氧化物的水化物的酸性:
C.最简单气态氢化物的稳定性顺序为:
D.100~200℃阶段热分解的化学方程式为:
【答案】D
【分析】YZ 分子的总电子数为奇数,常温下为气体,该气体应为NO ;Y为N元素,
2 2
Z为O元素;在化合物(YW XZ·4W Z )中WZ应为结晶水,则W为H元素;W、
4 5 8 2 2
X、Y、Z为短周期元素,原子序数依次增加,且加和为21,则X的核电外电子总数为
21-1-7-8=5,则X为B元素,以此分析解答。
【详解】根据上述分析可知:W为H元素,X为B元素,Y为N元素,Z为O元素。
A.W是H,Y是N元素,H与N元素形成的肼分子中含有N-H极性键和N-N非极性
键,A正确;
B.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强。元素的非金属
性:N>B,则最高价氧化物的水化物酸性:HNO>HBO,B正确;
3 3 3
C.X为B元素,Y为N元素,Z为O元素,同周期元素从左向右非金属性逐渐增强,
氢化物稳定性逐渐增强,最简单气态氢化物的稳定性顺序为: ,C正确;
D.化合物(YW XZ·4W Z )为NH B O·4H O,已知该200℃以下热分解时无刺激性气
4 5 8 2 4 5 8 2
体逸出,说明失去的是结晶水,若100 ~ 200℃阶段热分解失去4个HO,该化合物的
2
化学式变为NH B O,此时的质量保留百分数为
4 5 8
,与图示曲线数据( 80.2% )不一致,说明
100~200℃阶段不是失去4个HO,D错误;
2
资料收集整理【淘宝店铺:向阳百分百】故选D。
5.8.34g FeSO •7H O(相对分子质量:278)样品受热脱水过程的热重曲线(样品质量随温
4 2
度变化的曲线)如图所示,下列说法正确的是
A.温度为78℃时固体物质M的化学式为FeSO •5H O
4 2
B.温度为159℃时固体物质N的化学式为FeSO •2H O
4 2
C.在隔绝空气条件下,N得到P的化学方程式为FeSO •2H O FeSO +2H O
4 2 4 2
D.取适量380℃时所得的样品P,隔绝空气加热至650℃得到一种固体物质Q,同
时有两种无色气体生成,Q的化学式为Fe O
2 3
【答案】D
【分析】8.34 g FeSO·7H O样品物质的量为0.03 mol,其中m(HO)=0.03 mol×7×18
4 2 2
g·mol -1=3.78 g,如晶体全部失去结晶水,固体的质量应为8.34 g-3.78 g=4.56 g,可知
在加热到373 ℃之前,晶体失去部分结晶水,加热至635 ℃时,固体的质量为2.40 g,
应为铁的氧化物,其中n(Fe)=n(FeSO ·7H O)=0.03 mol ,m(Fe)=0.03 mol ×56 g·mol
4 2
-1=1.68 g,则固体中m(O)=2.40 g-1.68 g=0.72 g,n(O)=0.045 mol ,则n(Fe)∶n(O)=0.03
mol∶0.045 mol =2∶3,则固体物质Q的化学式为Fe O。
2 3
【详解】A.温度为78 ℃时,固体质量为6.72 g,其中m(FeSO)=0.03 mol ×152 g·mol
4
-1=4.56 g,m(HO)=6.72 g-4.56 g=2.16 g,n(H O)=0.12 mol ,则n(H O)∶n(FeSO )=0.12
2 2 2 4
mol ∶0.03 mol =4∶1,则化学式为FeSO ·4H O,故78 ℃时,M的化学式为
4 2
FeSO ·4H O,故A错误;
4 2
B.温度为159 ℃时,固体质量为5.10 g,其中m(FeSO)=0.03 mol ×152 g·mol -1=4.56
4
g,m(HO)=5.10 g-4.56 g=0.54 g,n(H O)=0.03 mol ,则n(H O)∶n(FeSO )=0.03 mol∶0.03
2 2 2 4
mol=1∶1,则化学式为FeSO ·H O,故B错误;
4 2
C.由B知N的化学式为FeSO ·H O,且P化学式为FeSO ,在隔绝空气条件下由N得
4 2 4
资料收集整理【淘宝店铺:向阳百分百】到P的化学方程式为FeSO ·H O FeSO +H O,故C错误;
4 2 4 2
D.由上述分析可知,P化学式为FeSO ,Q的化学式为Fe O,铁的化合价升高,必有
4 2 3
硫的化合价降低,即有二氧化硫生成,设SO 、SO 的物质的量分别为x mol、y mol,
2 3
则 ,解得x=y=0.015,所以方程式为2FeSO
4
Fe O+SO↑+SO↑,Q的化学式为Fe O,故D正确。
2 3 2 3 2 3
故选D。
6. 在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,
取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用
盐酸将其恰好完全溶解,得到 溶液和4.48L(标准状况)黄绿色
气体。下列说法错误的是
A.290℃时,若固体中只含有两种元素,则为
B.400℃时,
C.500℃时,固体中氧元素质量分数约为26.6%
D.生成的黄绿色气体可用于工业上生产“84”消毒液
【答案】B
【详解】A.290℃时,所得固体的摩尔质量为 ,可知固体为
,即 ,A项正确;
B.400℃时,由盐酸反应的离子方程式可得: ,当标准状况
资料收集整理【淘宝店铺:向阳百分百】下,4.48L即0.2mol黄绿色气体产生时,此时 转化为 ,此时溶
液中溶质为 ,根据溶液电荷守恒可得 ,因此溶
液中含有的 , ,400℃
产物中 ,即 ,B
项错误;
C.500℃时, 的摩尔质量为93g/mol,总的钴原子的物质的量为
,质量为 ,氧原子的质量为
,氧的质量分数为 ,C项正确;
D.根据元素守恒可知黄绿色气体为氯气,与NaOH溶液反应可生成NaClO,可以工
业生产“84”消毒液,D项正确;
答案选B。
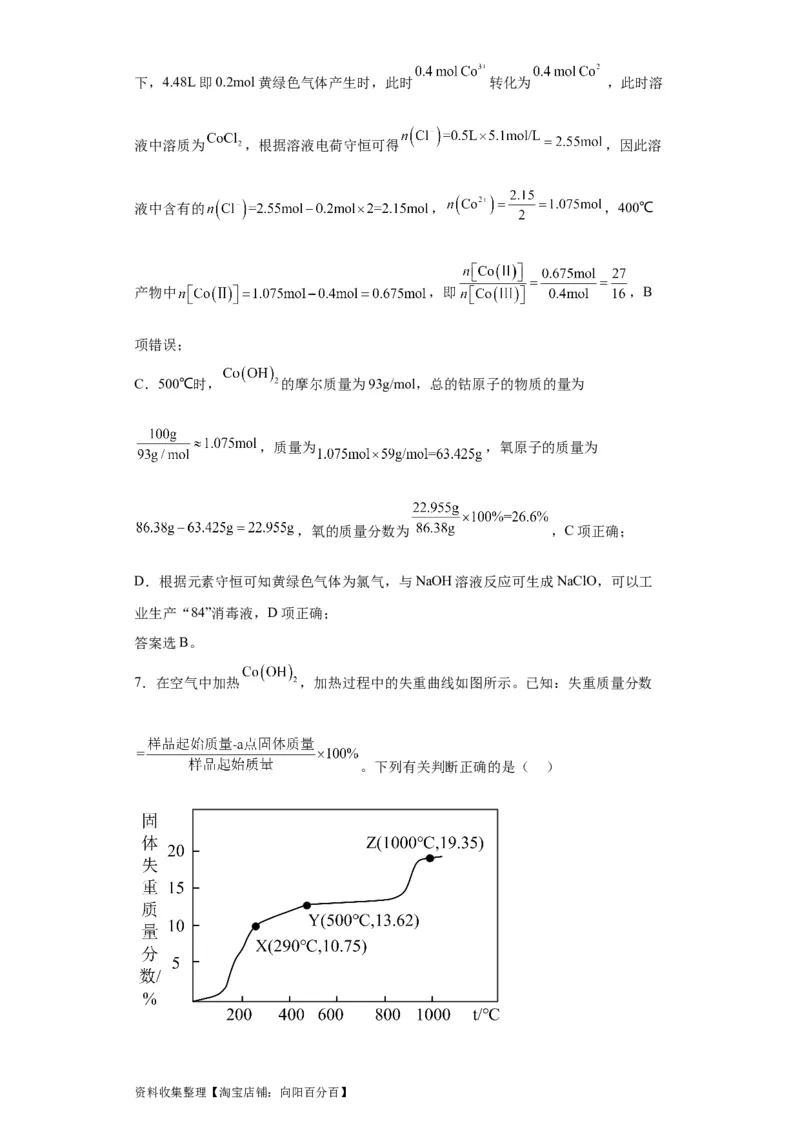
7.在空气中加热 ,加热过程中的失重曲线如图所示。已知:失重质量分数
。下列有关判断正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A. 的加热失重过程均为分解反应 B.X点是 和 的混合
物
C.Y点是 的纯净物 D.Z点是 的纯净物
【答案】D
【分析】Co(OH) 受热分解,生成CoO和HO,CoO易被空气中O 氧化,生成Co的
2 2 2
氧化物。从图中可以看出,随着温度的不断升高,固体失重质量分数不断增大,所以
从反应开始至X点,Co(OH) 不仅发生分解反应,还发生氧化反应;从X点到Y点、
2
从Y点到Z点,都为钴的氧化物的分解反应。
【详解】A.由选项内容可知, 的加热失重先生成 , 元素化合价逐
渐从 价,升高至 价,因此空气中的 参与了该反应,则 的加热失重过
程不是分解反应。A错误;
B.由图象可知,X点失重质量分数为10.75%,则加热后的残留率为89.25%,若取
的初始质量为 ,则残留的质量为 ,因 元素质量不
变, ,则残留物质中O质量 ,则残留物为 ,即为
,B错误;
C.若取 的初始质量为 ,则残留的质量为 ,因
元素质量不变, ,则残留物质中O质量 ,则残留物为 ,
即Y点为 ,C错误;
D.Z点,残留的质量为 ,因 ,则残留物质中O质
量 ,故残留物为 ,D正确;
故选D。
8.X、Y、Z、W为原子序数依次增大的前四周期元素,X为周期表中原子半径最小的
资料收集整理【淘宝店铺:向阳百分百】元素,Y、Z位于同一主族,且原子序数之和为24,基态W原子的价电子数为11,化
合物WZY •5X Y的热重曲线如图。下列说法错误的是
4 2
A.同周期中第一电离能大于Y的元素有3种 B.Z的最高价含氧酸酸性是同主族
中最强的
C.WZY •5X Y中有三种不同结合力的XY D.220℃时,固体物质的化学式为
4 2 2
WZY
4
【答案】D
【分析】X、Y、Z、W为原子序数依次增大的前四周期元素,X为周期表中原子半径
最小的元素,X为氢;Y、Z位于同一主族,且原子序数之和为24,则Y为氧、Z为硫;
基态W原子的价电子数为11,W为铜;故该化合物为CuSO ∙5H O;
4 2
【详解】A.同一周期随着原子序数变大,第一电离能变大,N的2p轨道为半充满稳
定状态,第一电离能大于同周期相邻元素,故同周期中第一电离能大于Y的元素有氮、
氟、氖3种,A正确;
B.非金属性越强,最高价氧化物对应水化物的酸性越强,O只有负价没有正价,故Z
的最高价含氧酸酸性是同主族中最强的,B正确;
C.CuSO ∙5H O完全失去结晶水时保留质量 ,结合图像可知,晶体分
4 2
三个阶段失去结晶水,故有三种不同结合力的HO,C正确;
2
D.由C分析可知,220℃时,晶体没有完全失去结晶水,故固体物质的化学式不是
CuSO ,D错误;
4
故选D。
9.将26.3g 样品在900℃下煅烧,样品受热过程的热重曲线(样品质量随
温度变化的曲线)如图所示。已知:L→N时失掉全部的结晶水。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.
B.固体M的化学式为
C.生成固体P时,样品的失重率约为71.5%
D.固体Q的化学式为NiO
【答案】D
【详解】A.L→N时失掉全部的结晶水,则分解反应为 = + ,
根据图像可知,L→N剩余固体 质量是15.5,失去结晶水的质量是26.3-
15.5=10.8,则根据 ~ 建立等式, ,解得n=6,A项正确;
B.L→M时失掉结晶水的质量是3.6g,则失去2个结晶水,则固体M的化学式为
,B项正确;
C.失重率等于固体失去的质量与原固体质量的比值,则生成固体P时,样品的失重率
= ×100%≈71.5%,C项正确;
D.N→P失重后,根据质量比例,可知发生的反应是 =NiO+SO↑, 的摩
3
尔质量是155,NiO 的摩尔质量是75,所以P→Q固体质量上升,应该是NiO 被氧化
得到NiO,D项错误。
2
故答案选D。
10. 是一种白色晶体粉末,不溶于水,用于陶瓷上釉等。W、X、Y、Z
为元素周期表前20号元素,已知W、X形成的化合物种类最多,Y原子最外层电子数
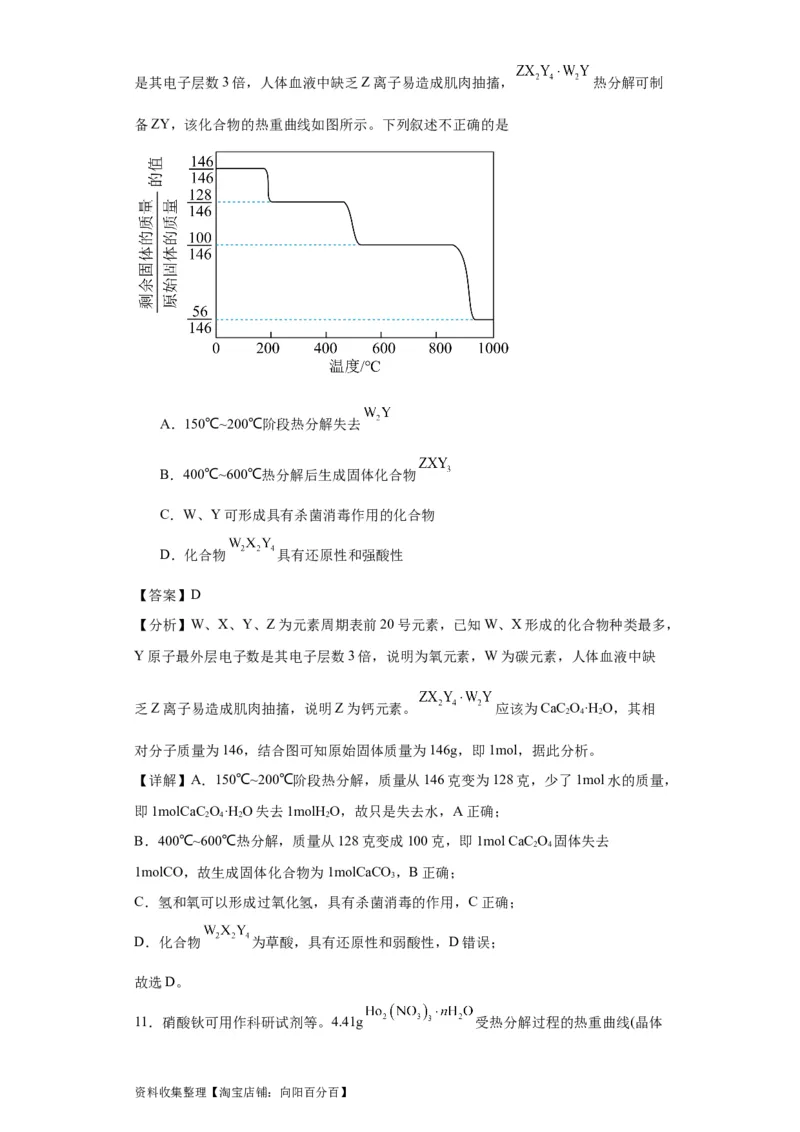
资料收集整理【淘宝店铺:向阳百分百】是其电子层数3倍,人体血液中缺乏Z离子易造成肌肉抽搐, 热分解可制
备ZY,该化合物的热重曲线如图所示。下列叙述不正确的是
A.150℃~200℃阶段热分解失去
B.400℃~600℃热分解后生成固体化合物
C.W、Y可形成具有杀菌消毒作用的化合物
D.化合物 具有还原性和强酸性
【答案】D
【分析】W、X、Y、Z为元素周期表前20号元素,已知W、X形成的化合物种类最多,
Y原子最外层电子数是其电子层数3倍,说明为氧元素,W为碳元素,人体血液中缺
乏Z离子易造成肌肉抽搐,说明Z为钙元素。 应该为CaC O·H O,其相
2 4 2
对分子质量为146,结合图可知原始固体质量为146g,即1mol,据此分析。
【详解】A.150℃~200℃阶段热分解,质量从146克变为128克,少了1mol水的质量,
即1molCaC O·H O失去1molH O,故只是失去水,A正确;
2 4 2 2
B.400℃~600℃热分解,质量从128克变成100克,即1mol CaC O 固体失去
2 4
1molCO,故生成固体化合物为1molCaCO,B正确;
3
C.氢和氧可以形成过氧化氢,具有杀菌消毒的作用,C正确;
D.化合物 为草酸,具有还原性和弱酸性,D错误;
故选D。
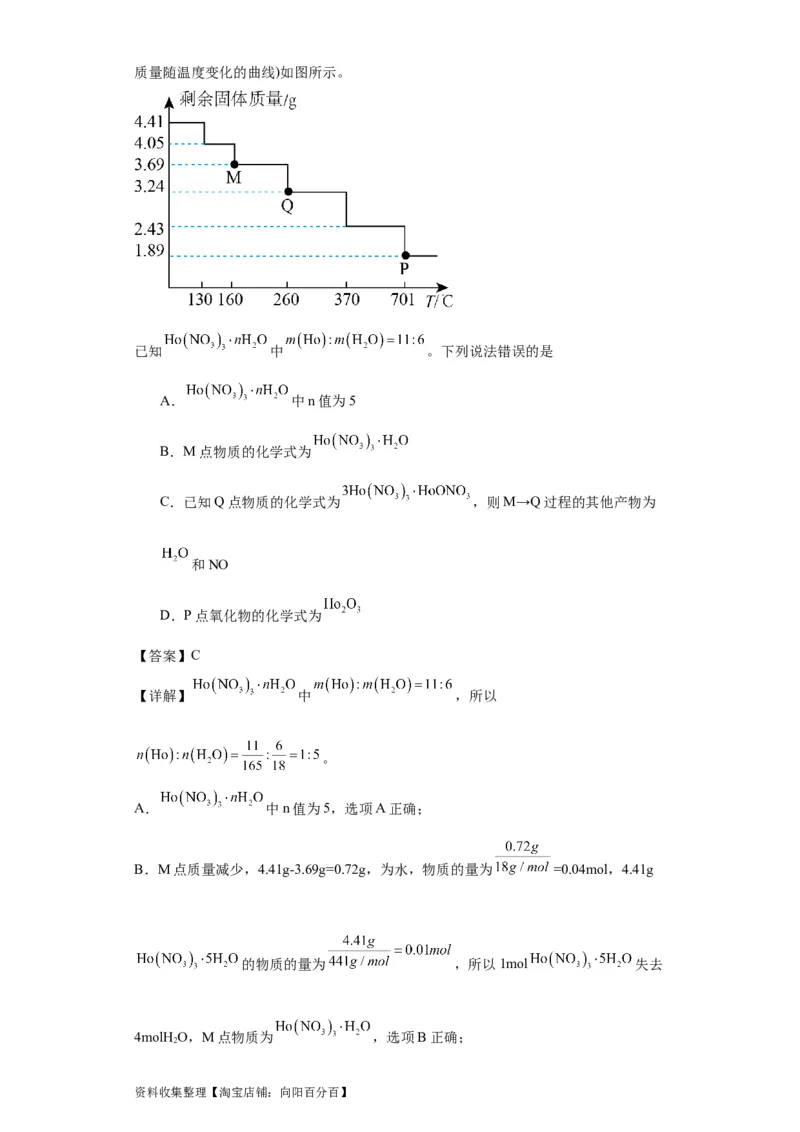
11.硝酸钬可用作科研试剂等。4.41g 受热分解过程的热重曲线(晶体
资料收集整理【淘宝店铺:向阳百分百】质量随温度变化的曲线)如图所示。
已知 中 。下列说法错误的是
A. 中n值为5
B.M点物质的化学式为
C.已知Q点物质的化学式为 ,则M→Q过程的其他产物为
和NO
D.P点氧化物的化学式为
【答案】C
【详解】 中 ,所以
。
A. 中n值为5,选项A正确;
B.M点质量减少,4.41g-3.69g=0.72g,为水,物质的量为 =0.04mol,4.41g
的物质的量为 ,所以1mol 失去
4molH O,M点物质为 ,选项B正确;
2
资料收集整理【淘宝店铺:向阳百分百】C.Q点产物 ,由Ho元素守恒n(Ho)=0.01mol,则
为0.0025mol,质量为0.0025mol 594g/mol=1.485g,另外产物质
量3.24g-1.485g=1.755g,但若是HO和NO,只涉及N的化合价降低,没有化合价升
2
高,不可能,选项C错误;
D.由Ho元素守恒m(Ho)=0.01mol 165g/mol=1.65g,则m(O)=1.89g-1.65g=0.24g,
n(O)= =0.015mol,所以n(Ho):n(O)=0.01mol:0.015mol=2:3,则P点氧化物化学
式为Ho O,选项D正确;
2 3
答案选C。
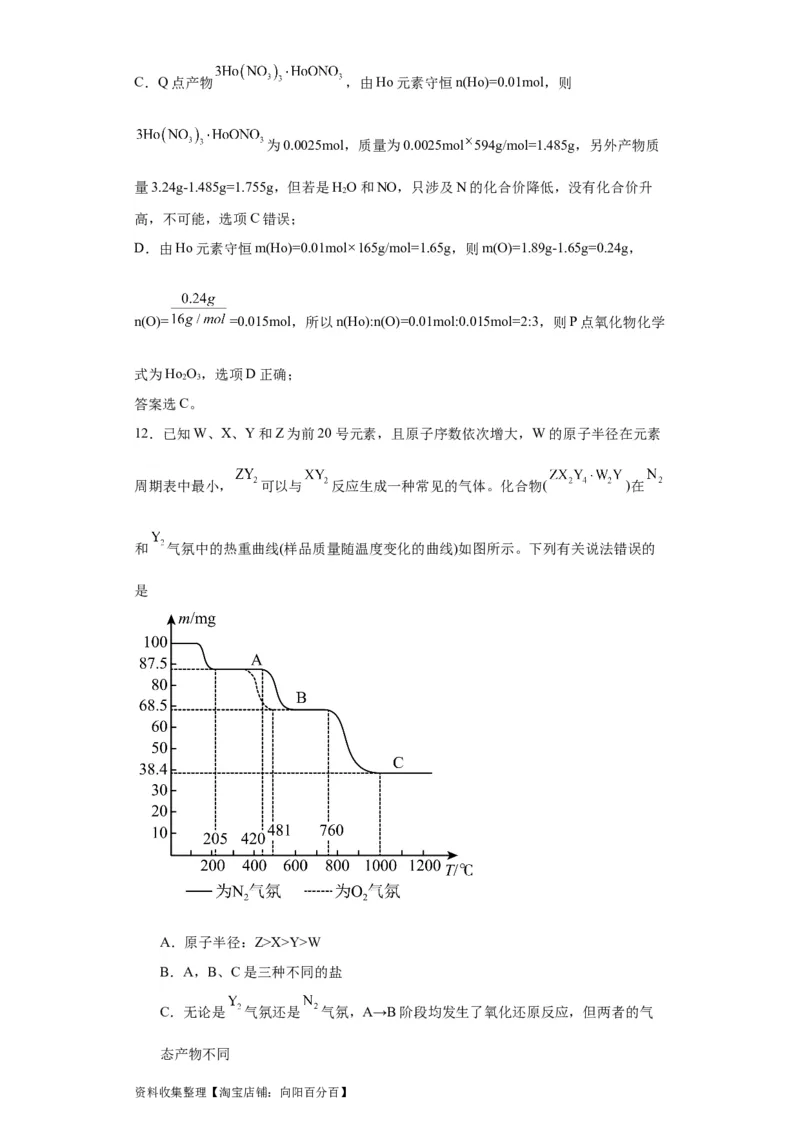
12.已知W、X、Y和Z为前20号元素,且原子序数依次增大,W的原子半径在元素
周期表中最小, 可以与 反应生成一种常见的气体。化合物( )在
和 气氛中的热重曲线(样品质量随温度变化的曲线)如图所示。下列有关说法错误的
是
A.原子半径:Z>X>Y>W
B.A,B、C是三种不同的盐
C.无论是 气氛还是 气氛,A→B阶段均发生了氧化还原反应,但两者的气
态产物不同
资料收集整理【淘宝店铺:向阳百分百】D.在酸性 溶液中加入少量A固体样品时,溶液褪色且有少量气泡产生
【答案】B
【分析】W、X、Y和Z为前20号元素,且原子序数依次增大,W的原子半径在元素
周期表中最小,W是H元素; 可以与 反应生成一种常见的气体,CaO 和CO
2 2
反应生成碳酸钙和氧气,所以X是C元素、Y是O元素、Z是Ca元素。
【详解】A.原子半径:Ca>C>O>H,故A正确;
B. 中 的质量分数为87.7%,所以A是 ; 中
CaCO 的质量分数为68.5%,所以B是CaCO ; 中CaO的质量分数为
3 3
38.4%,所以C是CaO,故B错误;
C.无论是 气氛还是 气氛,A→B阶段均发生反应 ,C元素化
合价改变,都发生氧化还原反应,在 气氛中生成的气体产物是CO,在O 氛围中气
2
态产物是CO,故C正确;
2
D.在酸性 溶液中加入少量 固体样品时, 被氧化为二氧化碳,
溶液褪色且有少量气泡产生,故D正确;
选B。
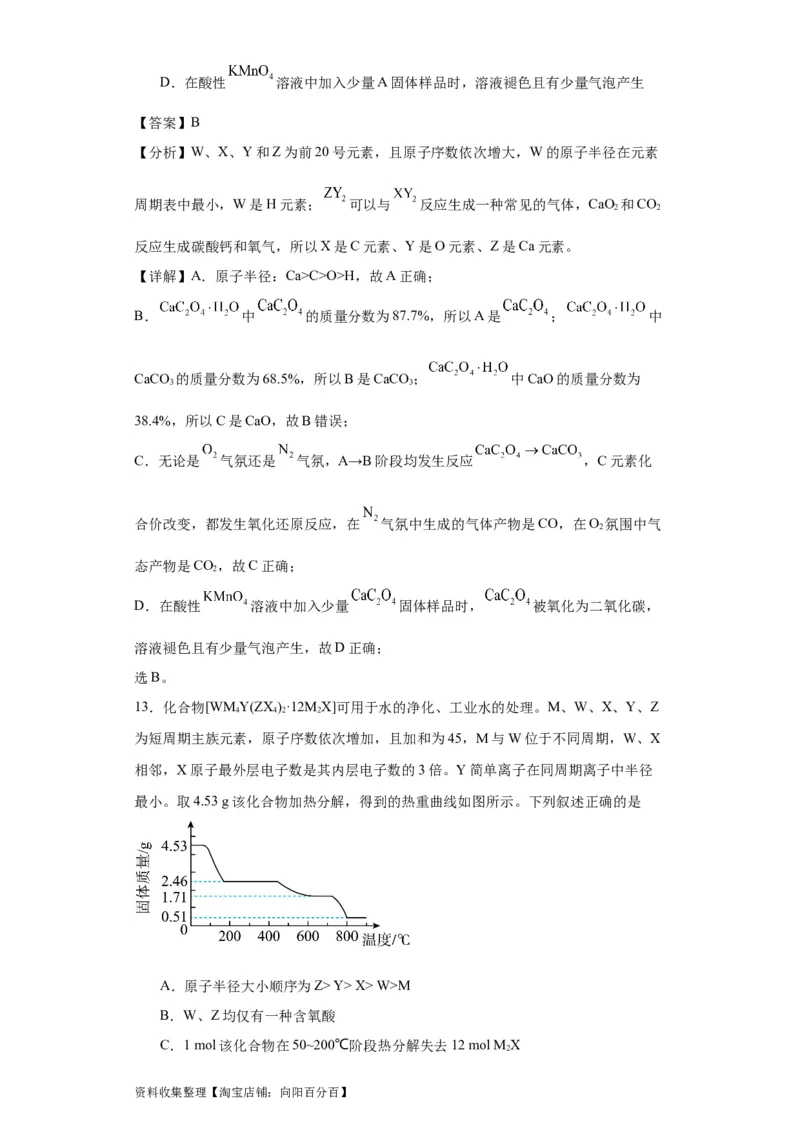
13.化合物[WMY(ZX )·12M X]可用于水的净化、工业水的处理。M、W、X、Y、Z
4 4 2 2
为短周期主族元素,原子序数依次增加,且加和为45,M与W位于不同周期,W、X
相邻,X原子最外层电子数是其内层电子数的3倍。Y简单离子在同周期离子中半径
最小。取4.53 g该化合物加热分解,得到的热重曲线如图所示。下列叙述正确的是
A.原子半径大小顺序为Z> Y> X> W>M
B.W、Z均仅有一种含氧酸
C.1 mol该化合物在50~200℃阶段热分解失去12 mol M X
2
资料收集整理【淘宝店铺:向阳百分百】D.650℃、850℃热分解所得固体化合物分别为Y(ZX)、YX
2 4 3 2 3
【答案】D
【分析】X原子最外层电子数是其内层电子数的3倍,根据核外电子排布规律,X位
于第二周期,即X为O元素,W、X相邻,且原子序数依次增大,则W为N,M与W
位于不同周期,且原子序数依次增大,则M为H,Y简单离子在同周期离子中半径最
小,一般电子层数越多,微粒半径越大,因此Y不位于第二周期,应位于第三周期,
一般电子层数相同,微粒半径随着原子序数的递增而减小,则Y为Al,根据原子序数
之和为45,推出Z为S元素,据此分析;
【详解】根据上述分析,M为H,W为N,X为O,Y为Al,Z为S;
A.一般电子层数越多,微粒半径越大,电子层数相同,微粒半径随着原子序数的递
增而减小,因此原子半径大小顺序是r(Al)>r(S)>r(N)>r(O)>r(H),故A错误;
B.N的化合价多种,含氧酸有HNO、HNO 等,Z为S,含氧酸为HSO 、HSO 等,
3 2 2 3 2 4
故B错误;
C.根据上述分析,该化合物为NH Al(SO )·12H O,加热时,先失去结晶水,4.53g该
4 4 2 2
化合物的物质的量为0.01mol,假设全部失去结晶水,失去0.12mol水,即固体质量减
少2.16g,此时固体的质量为2.37g,根据图象可知,50~200℃固体减少的质量为2.07g
<2.16g,因此1mol该化合物在该阶段分解失去水的物质的量小于12mol,故C错误;
D.失去全部结晶水后,得到NH Al(SO ),可以看作由(NH )SO 、Al (SO ) 组成,继
4 4 2 4 2 4 2 4 3
续对固体加强热,硫酸铵分解为氨气、二氧化硫、氮气和水,此时剩余固体为
Al (SO ),NH Al(SO )·12H O~ Al (SO ),0.1molNH Al(SO )·12H O完全转化成硫
2 4 3 4 4 2 2 2 4 3 4 4 2 2
酸铝,得到铝的质量为0.005mol×342g/mol=1.71g,因此650℃得到固体化合物是
Al (SO ),硫酸铝继续加强热,硫酸铝分解为氧化铝和三氧化硫,完全转化成氧化铝
2 4 3
时有NH Al(SO )·12H O~ Al O,得到氧化铝的质量为0.005mol×102g/mol=0.51g,
4 4 2 2 2 3
因此850℃得到固体化合物是Al O,故D正确;
2 3
故答案为D。
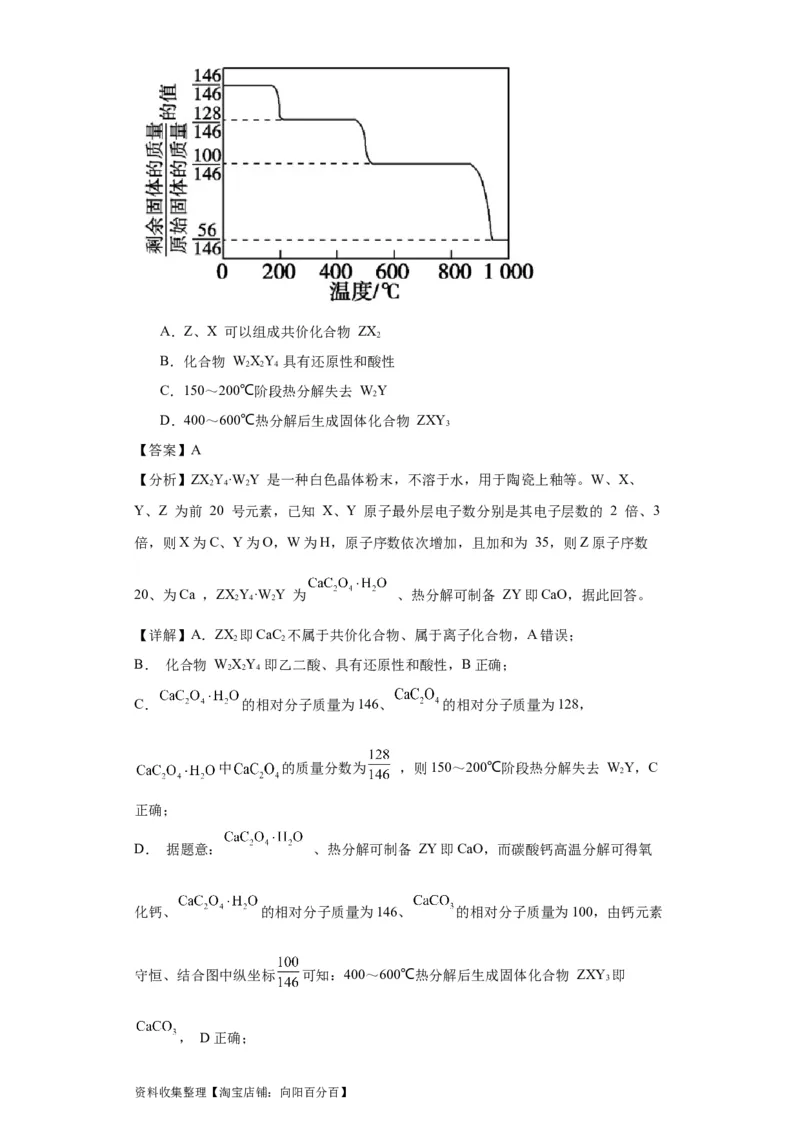
14.ZXY·W Y 是一种白色晶体粉末,不溶于水,用于陶瓷上釉等。W、X、Y、Z
2 4 2
为前 20 号元素,原子序数依次增加,且加和为 35,已知 X、Y 原子最外层电子数
分别是其电子层数的 2 倍、3 倍,ZXY·W Y 热分解可制备 ZY,该化合物的热重
2 4 2
曲线如图所示。下列叙述不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.Z、X 可以组成共价化合物 ZX
2
B.化合物 WXY 具有还原性和酸性
2 2 4
C.150~200℃阶段热分解失去 WY
2
D.400~600℃热分解后生成固体化合物 ZXY
3
【答案】A
【分析】ZXY·W Y 是一种白色晶体粉末,不溶于水,用于陶瓷上釉等。W、X、
2 4 2
Y、Z 为前 20 号元素,已知 X、Y 原子最外层电子数分别是其电子层数的 2 倍、3
倍,则X为C、Y为O,W为H,原子序数依次增加,且加和为 35,则Z原子序数
20、为Ca ,ZXY·W Y 为 、热分解可制备 ZY即CaO,据此回答。
2 4 2
【详解】A.ZX 即CaC 不属于共价化合物、属于离子化合物,A错误;
2 2
B. 化合物 WXY 即乙二酸、具有还原性和酸性,B正确;
2 2 4
C. 的相对分子质量为146、 的相对分子质量为128,
中 的质量分数为 ,则150~200℃阶段热分解失去 WY,C
2
正确;
D. 据题意: 、热分解可制备 ZY即CaO,而碳酸钙高温分解可得氧
化钙、 的相对分子质量为146、 的相对分子质量为100,由钙元素
守恒、结合图中纵坐标 可知:400~600℃热分解后生成固体化合物 ZXY 即
3
, D正确;
资料收集整理【淘宝店铺:向阳百分百】答案选A。
15.化合物(YW XZ•4WZ)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周
4 5 8 2
期元素,原子序数依次增加,且加和为21。YZ 分子的总电子数为奇数,常温下为气
2
体。该化合物的热重曲线如图所示,在200℃以下分解时无刺激性气体逸出。下列叙
述正确的是
A.W、X、Y、Z的单质常温下均为气体
B.氢化物XH 和YH 中X、Y均为8电子的稳定结构
3 3
C.100~200℃阶段热分解失去WZ少于4个
2
D.500℃热分解后生成固体化合物XZ
2 5
【答案】C
【分析】该化合物的热重曲线在 以下热分解时无刺激性气体逸出,则说明失去的
是水,即W为H,Z为O, 分子的总电子数为奇数,常温下为气体,则Y为N,原
子序数依次增加,且加和为21,则X为B,以此解题。
【详解】A.由分析可知X为B,单质B在常温下为固体,故A错误;
B.元素B,其原子最外层有3个电子,则 中B原子最外层只有6个电子,故B错
误;
C.根据前面已知化合物 以下热分解时无刺激性气体逸出,则
说明失去的是水,若 阶段热分解失去4个 ,则质量分数为
,而题目中数据为80.2%,则说明失去的
少于4个,故C正确;
资料收集整理【淘宝店铺:向阳百分百】D.元素B为第ⅢA族元素,最高化合价为 价,不可能生成 ;另外,假设化合
物 在 热分解后生成固体化合物 ,根据硼元素守恒,
则得到关系式 ,则固体化合物 质量分数为
,与题目不符,说明假设错误,故D
错误;
故选C。
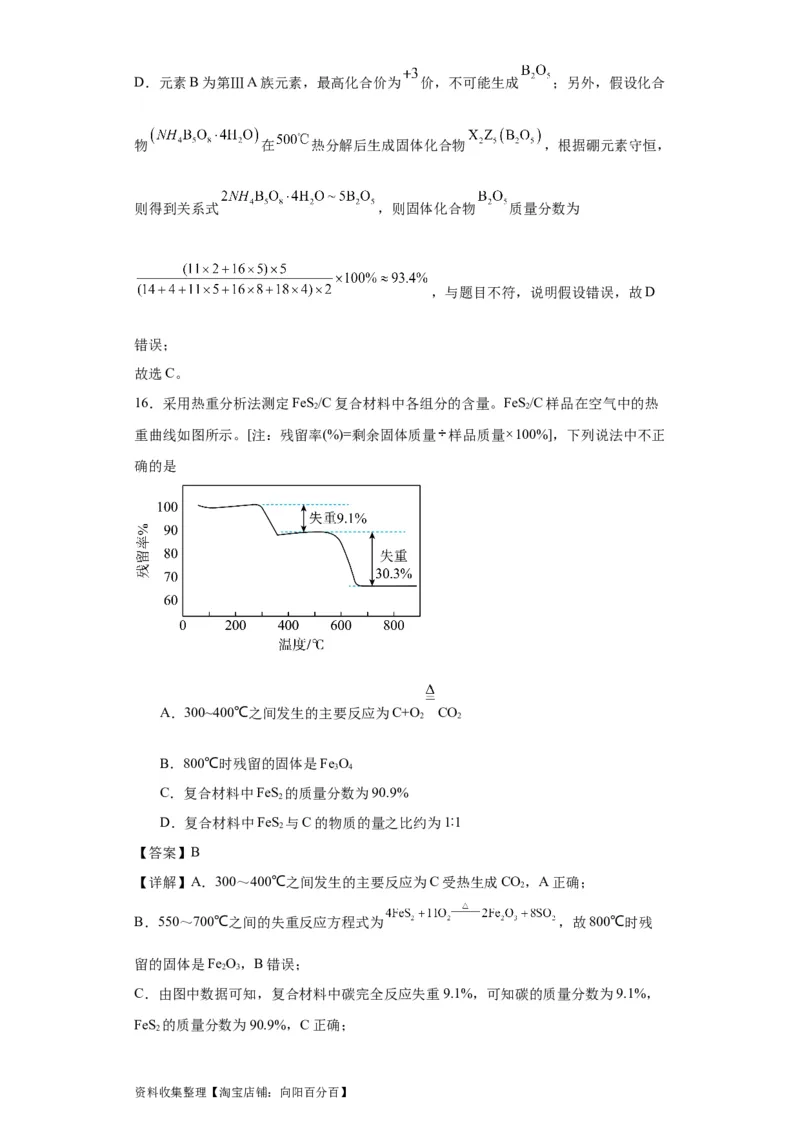
16.采用热重分析法测定FeS/C复合材料中各组分的含量。FeS/C样品在空气中的热
2 2
重曲线如图所示。[注:残留率(%)=剩余固体质量 样品质量 100%],下列说法中不正
确的是
A.300~400℃之间发生的主要反应为C+O CO
2 2
B.800℃时残留的固体是Fe O
3 4
C.复合材料中FeS 的质量分数为90.9%
2
D.复合材料中FeS 与C的物质的量之比约为1∶1
2
【答案】B
【详解】A.300~400℃之间发生的主要反应为C受热生成CO,A正确;
2
B.550~700℃之间的失重反应方程式为 ,故800℃时残
留的固体是Fe O,B错误;
2 3
C.由图中数据可知,复合材料中碳完全反应失重9.1%,可知碳的质量分数为9.1%,
FeS 的质量分数为90.9%,C正确;
2
资料收集整理【淘宝店铺:向阳百分百】D.FeS 与C的物质的量之比为 ,D正确;
2
故选B。
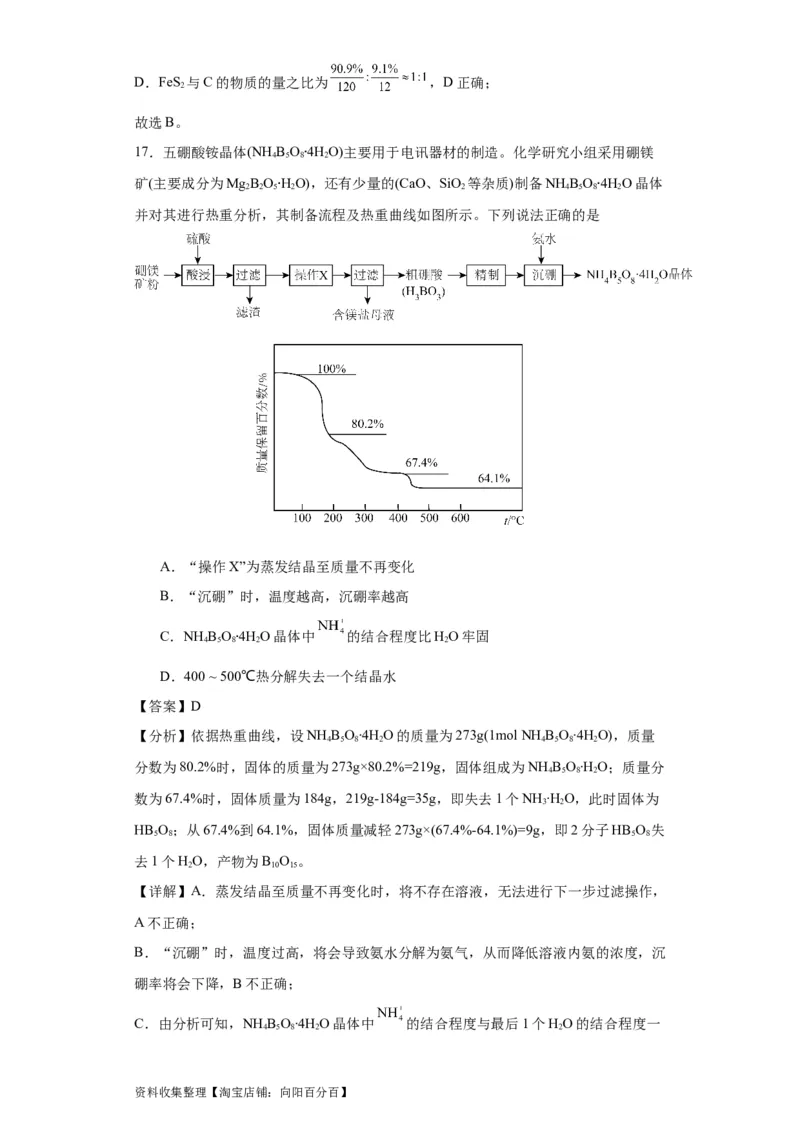
17.五硼酸铵晶体(NH B O 4HO)主要用于电讯器材的制造。化学研究小组采用硼镁
4 5 8 2
矿(主要成分为MgB O HO∙),还有少量的(CaO、SiO 等杂质)制备NH B O 4HO晶体
2 2 5 2 2 4 5 8 2
并对其进行热重分析,其∙ 制备流程及热重曲线如图所示。下列说法正确的是∙
A.“操作X”为蒸发结晶至质量不再变化
B.“沉硼”时,温度越高,沉硼率越高
C.NH B O 4HO晶体中 的结合程度比HO牢固
4 5 8 2 2
∙
D.400 ~ 500℃热分解失去一个结晶水
【答案】D
【分析】依据热重曲线,设NH B O∙4H O的质量为273g(1mol NH B O∙4H O),质量
4 5 8 2 4 5 8 2
分数为80.2%时,固体的质量为273g×80.2%=219g,固体组成为NH B O∙H O;质量分
4 5 8 2
数为67.4%时,固体质量为184g,219g-184g=35g,即失去1个NH ∙H O,此时固体为
3 2
HB O;从67.4%到64.1%,固体质量减轻273g×(67.4%-64.1%)=9g,即2分子HB O 失
5 8 5 8
去1个HO,产物为B O 。
2 10 15
【详解】A.蒸发结晶至质量不再变化时,将不存在溶液,无法进行下一步过滤操作,
A不正确;
B.“沉硼”时,温度过高,将会导致氨水分解为氨气,从而降低溶液内氨的浓度,沉
硼率将会下降,B不正确;
C.由分析可知,NH B O∙4H O晶体中 的结合程度与最后1个HO的结合程度一
4 5 8 2 2
资料收集整理【淘宝店铺:向阳百分百】样牢固,C不正确;
D.由分析可知,400 ~ 500℃时,2分子HB O 失去1个HO,产物为B O ,相当于
5 8 2 10 15
热分解失去一个结晶水,D正确;
故选D。
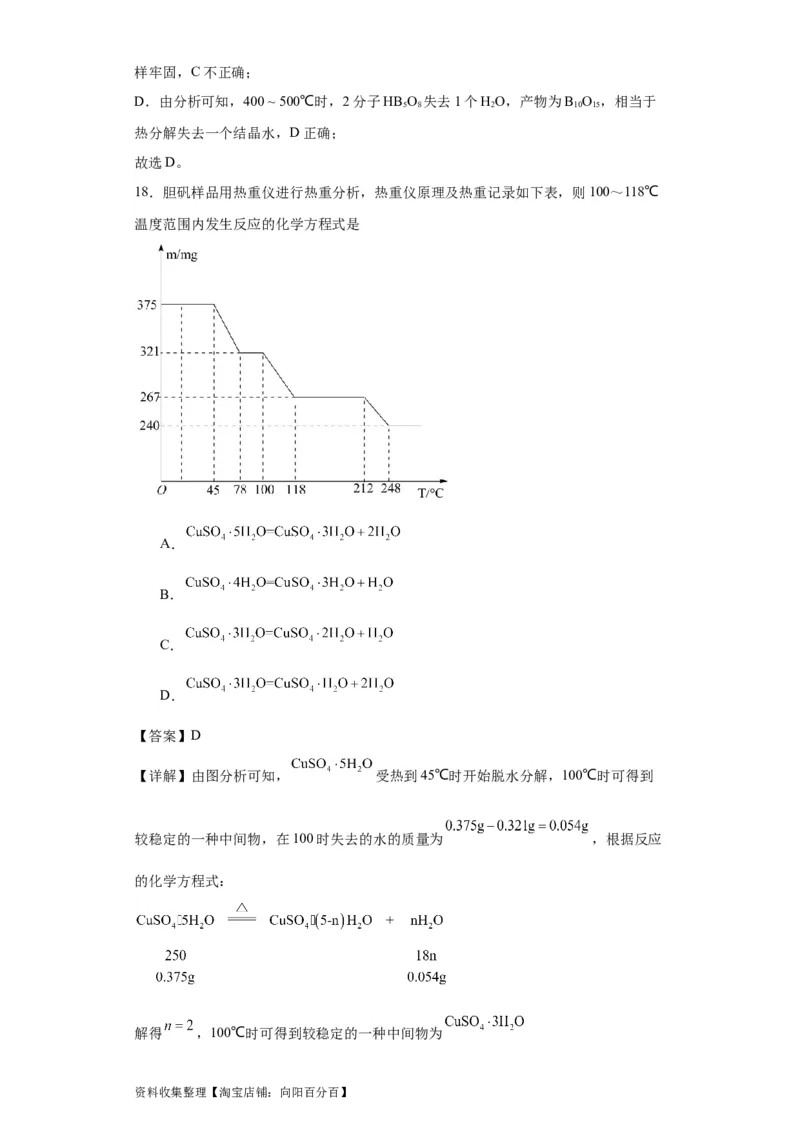
18.胆矾样品用热重仪进行热重分析,热重仪原理及热重记录如下表,则100~118℃
温度范围内发生反应的化学方程式是
A.
B.
C.
D.
【答案】D
【详解】由图分析可知, 受热到45℃时开始脱水分解,100℃时可得到
较稳定的一种中间物,在100时失去的水的质量为 ,根据反应
的化学方程式:
解得 ,100℃时可得到较稳定的一种中间物为
资料收集整理【淘宝店铺:向阳百分百】118℃时可得到较稳定的一种中间物,根据反应的化学方程式:
解得 ,118℃时可得到较稳定的一种中间物为 ,100-118℃温度范围内
发生反应的化学方程式为 。
选D。
资料收集整理【淘宝店铺:向阳百分百】