文档内容
专题 02 化学计量及其应用
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
题型一 阿伏伽德罗常数的应用.......................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.气体摩尔体积适用条件及物质的聚集状态................................................................................................
2.物质的组成和结构.........................................................................................................................................
3.氧化还原反应中转移电子数目....................................................................................................................
4.电解质溶液中粒子的数目............................................................................................................................
5.隐含的可逆反应.............................................................................................................................................
【命题预测】...........................................................................................................................................................
考向1 不含有题干描述......................................................................................................................................
考向2 含有题干描述..........................................................................................................................................
题型二一定物质的量浓度溶液的配制...............................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.配制一定物质的量浓度的溶液的操作........................................................................................................
2.配制一定物质的量浓度的溶液的误差分析................................................................................................
【命题预测】...........................................................................................................................................................
考向1配制一定物质的量浓度的溶液的操作...................................................................................................
考向2配制一定物质的量浓度的溶液的误差分析...........................................................................................考点要求 考题统计 考情分析
2024·广东卷,10,2分;2024· 海
南卷,6,2分;2024· 贵州卷,
从近三年高考试题来看,有关
6,3分;2024·江西卷,7,3分;
物质的量浓度的概念主要体现在
2024·河北卷,4,3分;2024·辽吉
N 、水溶液中的离子平衡及化学
黑卷,4,3分;2024·安徽卷, A
计算中;一定物质的量浓度溶液
6,3分;2023辽宁卷5题,3
的配制是重要的化学定量实验之
阿伏加德罗常数的 分;2023全国甲卷10题,6分; 一,融合于选择题的化学实验基
应用 2023浙江6月7题,3分;2022福 本操作,填空题主要以穿插在生
建卷5题,4分;2022重庆卷5 活、生产中的化学分析计算(如食
题,32分;2022全国甲卷11题, 品污染物空气污染物的测定、食
6分;2022浙江6月12题,2分; 品中的营养物质的测定、化工生
2022浙江1月12题,2分;2022 产中的产品是否合格等等)为主,
海南卷7题,3分;2022辽宁卷3 中需关注滴定实验中有关物质的
题,3分; 量浓度的计算。
2024·甘肃卷,6,3分;2024·北京 预计在2025年高考中,仍会
卷,6,3分;2024·江苏卷,3,3 利用阿伏加德罗常数这个载体综
分;2024·湖北卷,18(1),2分; 合考查相关知识,涉及一定量的
物质所含粒子数目、氧化还原反
一定物质的量浓度 2023•全国甲卷9题,6分;2022
应中转移电子的数目、以及由于
溶液的配制 山东卷6题,2分;2022•全国乙
反应、浓度等的变化导致微粒数
卷27(1)题,2分;2022•广东卷7
目变化等。
题(1)(2),4分;2021广东卷7
题,2分;题型一 阿伏伽德罗常数的应用
1.(2024·广东卷,10,2分)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.26gH-C≡C-H中含有σ键的数目为3N
A
B.1L1mol⋅L-1NH NO 溶液中含NH +的数目为N
4 3 4 A
C.1molCO和H 的混合气体含有的分子数目为3N
2 A
D.Na与HO反应生成11.2LH ,转移电子数目为N
2 2 A【答案】A
【解析】A项,26gC H 的物质的量为1mol,一个C H 分子中含有3个σ键,故26gC H 中含有σ键
2 2 2 2 2 2
的数目为3N ,A正确;B项,NH +在水溶液中发生水解,1L1mol⋅L-1NH NO 溶液中含NH +的数目小于
A 4 4 3 4
N ,B错误;C项,CO和H 均由分子构成,1molCO和H 的混合气体含有的分子数目为N ,C错误;D
A 2 2 A
项,Na与HO反应生成11.2LH ,由于未给出气体所处的状态,无法求出生成气体的物质的量,也无法得
2 2
出转移电子数目,D错误;故选A。
2.(2024· 海南卷,6,2分)N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.2.2 g超重水(3HO)所含的电子数目为N
2 A
B.1L0.1mol·L-1NaClO溶液中ClO-的数目为0.1N
A
C.过量C与1molSiO 充分反应转移电子数目为3N
2 A
D.1molCl 与足量CH 发生取代反应生成HCl分子的数目为2N
2 4 A
【答案】A
【解析】A项,2.2 g超重水((3HO为 )所含的电子为0.1mol×10=1mol,电子数目为
2
N ,A正确; B项,次氯酸根离子为弱酸根离子,水溶液中部分水解生成次氯酸和氢氧根离子,故
A
1L0.1mol·L-1NaClO的数目小于0.1N ,B错误;C项,过量C与1molSiO 充分生成硅单质和CO,硅化合
A 2
价由+4变为0,则反应转移电子数目为4N ,C错误; D项,甲烷与氯气发生取代反应为连锁反应,同
A
时得到四种氯代产物和HCl,结合氯守恒,1molCl 与足量CH 发生取代反应生成HCl分子的数目为N ,D
2 4 A
错误;故选A。
3.(2024· 贵州卷,6,3分)二氧化氯(ClO )可用于自来水消毒。实验室用草酸(H C O)和KClO 制取
2 2 2 4 3
ClO 的反应为HC O+2KClO +H SO =2ClO ↑+CO ↑+K SO +2H O。设N 为阿伏加德罗常数的值。下列说
2 2 2 4 3 2 4 2 2 2 4 2 A
法正确的是( )
A.0.1molH18O中含有的中子数为1.2N
2 A
B.每生成67.5g ClO ,转移电子数为2.0N
2 A
C.0.1mol·L-1 HC O 溶液中含有的H+数目为0.2N
2 2 4 A
D.标准状况下,22.4LCO 中含σ键数目为2.0N
2 A
【答案】D
【解析】A项,H18O分子中H原子无中子,18O原子的中子数为10,则0.1molH18O中含有的中子数
2 2
为N ,故A错误;B项,由反应方程式HC O+2KClO +H SO =2ClO ↑+CO ↑+K SO +2H O可知,每生成
A 2 2 4 3 2 4 2 2 2 4 2
2mol ClO 转移电子数为2mol,则每生成67.5g ClO ,即1mol ClO 转移电子数为N ,故B错误;C项,
2 2 2 A
未给出草酸溶液的体积,无法计算氢离子的物质的量,故C错误;D项,1个二氧化碳分子中含有2个σ
键和2个π键,则标准状况下22.4LCO ,即1molCO 中含σ键数目为2.0N ,故D正确;故选D。
2 2 A的
4.(2024·江西卷,7,3分)我国学者把游离态氮固定在碳上(示踪反应如下),制得 [N=C=N]2﹣离子可
用于合成核酸的结构单元。阿伏加德罗常数的值为N ,下列说法正确的是( )
A
15N+C(石墨)+2LiH Li[15NC15N]+H
2 2 2
A.22.4L15N 含有的中子数为16N
2 A
B.12gC(石墨)中sp2杂化轨道含有的电子数为6N
A
C.1mol[N=C=N]2﹣中含有的π键数为4N
A
D.生成1mol H 时,总反应转移的电子数为6N
2 A
【答案】D
【解析】A项,22.4L15N 的温度压强不知,不能计算物质的量,故A错误;B项,12gC 物质的量n
2 (石墨)
1mol,C原子的杂化轨道上3个电子,有一个电子未参与杂化,sp2杂化轨道含有的电子数
为3N ,故B错误;C项,双键中一个σ键,一个π键,则1mol[N=C=N]2﹣中含有的π键数为2N ,故C错
A A
误;D项,该反应中氮元素化合价0价降低到﹣3价,碳元素化合价0价升高到+4价,氢元素化合价﹣1价
升高到0价,电子转移总数6e﹣,生成1mol H 时,总反应转移的电子数为6N ,故D正确;故选D。
2 A
5.(2024·河北卷,4,3分)超氧化钾(KO )可用作潜水或宇航装置的CO 吸收剂和供氧剂,反应为
2 2
4KO +2CO =2K CO+O ,N 为阿伏加德罗常数的值。下列说法正确的是( )
2 2 2 3 2 A
A.44gCO 中 键的数目为2N
2 A
B.1mol KO 晶体中离子的数目为3N
2 A
C.1 L1mol·L-1 KCO 溶液中CO2-的数目为N
2 3 3 A
D.该反应中每转移1mol电子生成O 的数目为1.5N
2 A
【答案】A
【解析】A项,44g (即1mol ) CO 中 键的数目为2N ,A正确;B项,KO 由K+和O-构成,1mol
2 A 2 2
KO 晶体中离子的数目为2N ,B错误;C项,CO2-在水溶液中会发生水解:CO2-+H O HCO -
2 A 3 3 2 3
+OH-,故1 L1mol·L-1溶液中CO2-的数目小于N ,C错误;D项,该反应中部分氧元素化合价由-0.5价升
3 A
至0价,部分氧元素化合价由-0.5价降至-2价,则每4mol KO 参加反应转移3mol 电子,每转移1mol 电
2
子生成O 的数目为N ,D错误;故选A。
2 A
6.(2024·辽吉黑卷,4,3分)硫及其化合物部分转化关系如图。设N 为阿伏加德罗常数的值,下列说
A
法正确的是( )A.标准状况下,11.2L SO 中原子总数为0.5N
2 A
B.100mL0.1mol·L-1NaSO 溶液中,SO 2-数目为0.01N
2 3 3 A
C.反应①每消耗3.4g HS,生成物中硫原子数目为0.1N
2 A
D.反应②每生成 还原产物,转移电子数目为2N
A
【答案】D
【解析】A项,标况下SO 为气体,11.2L SO 为0.5mol,其含有1.5mol原子,原子数为1.5N ,A错
2 2 A
误;B项,SO 2-为弱酸阴离子,其在水中易发生水解,因此,100mL 0.1mol L-1 Na SO 溶液中SO 2-数目小
3 2 3 3
于0.01N ,B错误;C项,反应①的方程式为SO +2H S=3S↓+2H O,反应中每生成3mol S消耗2mol HS,
A 2 2 2 2
3.4g HS为0.1mol,故可以生成0.15mol S,生成的原子数目为0.15N ,C错误;D项,反应②的离子方程
2 A
式为3S+6OH-=SO2-+2S2-+3H O,反应的还原产物为S2-,每生成2mol S2-共转移4mol电子,因此,每生成
3 2
1mol S2-,转移2mol电子,数目为2N ,D正确;故选D 。
A
7.(2024·安徽卷,6,3分)地球上的生物氮循环涉及多种含氮物质,转化关系之一如下图所示(X、Y
均为氮氧化物),羟胺(NH OH)以中间产物的形式参与循环。常温常压下,羟胺易潮解,水溶液呈碱性,与
2
盐酸反应的产物盐酸羟胺([NH OH]Cl)广泛用子药品、香料等的合成。
3
已知25℃时,K(HNO)=7.2×10-4,K(NH ·H O)=1.8×10-5 ,K(NH OH)=8.7×10-9。
a 2 b 3 2 b 2
N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,2.24LX和Y混合气体中氧原子数为0.1N
A
B.1L0.1mol·L-1NaNO 溶液中Na+和NO -数均为0.1N
2 2 A
C.3.3gNH OH完全转化为NO -时,转移的电子数为0.6N
2 2 A
D.2.8gN 中含有的价电子总数为0.6N
2 A
【答案】A
【解析】NO -在亚硝酸盐还原酶的作用下转化为 X,X在X还原酶的作用下转化为Y,X、Y均为氮
2
氧化物,即X为NO,Y为NO。A项,标准状况下,2.24LNO和NO混合气体物质的量为0.1mol,氧原
2 2
子数为0.1N ,故A正确;B项,HNO 为弱酸,因此NO -能够水解为HNO ,1L0.1mol·L-1NaNO 溶液中
A 2 2 2 2NO -数目小于 0.1N ,故 B 错误;C 项,NH OH 完全转化为 NO -时,N 的化合价由-1 上升到+3,
2 A 2 2
3.3gNH OH物质的量为0.1mol,转移的电子数为0.4N ,故C错误;D项,2.8gN 物质的量为0.1mol,N
2 A 2
的价电子数等于最外层电子数为5,2.8gN 含有的价电子总数为N ,故D错误;故选A。
2 A
解答有关阿伏加德罗常数类题目的“三个步骤”
对于N 的正误判断必须排除各种陷阱,要认真审题,明确题中的陷阱所在。解题时要注意物质的量的
A
核心和桥梁作用。解题的一般思路为:已知数据――→物质的量――→N ,具体为:
A
1 . 气体摩尔体积适用条件及物质的聚集状态
考查角度 命题分析 注意事项
熟记在标准状况下为非气态的常考物质。如
在标准状况(0 ℃、101 kPa)下,1 mol任
标准 单质溴、HO、苯、CCl 、CHCl 、CHCl 、
何气体的体积约为22.4 L,分子数为N , 2 4 2 2 3
状况下 即V =22.4 L·mol-1。非气体不适用 A CH 3 OH、CH 3 CH 2 OH、SO 3 、碳原子数大于4
m 的烃等均不是气体
①非标准状况(一般考查常温常压)下,气 ①常温常压下,气体体积不能通过 22.4
体摩尔体积未必为22.4 L·mol-1 L·mol-1转化计算;
非标准
②非标准状况下气体的物质的量或质 ②常温常压下,1 mol CO 质量为44 g,分
状况下 2
量、物质所含的粒子数与温度、压强等外 子数是N (气体质量和所含的粒子数与所处外
A
界条件无关 界条件无关)
2 . 物质的组成和结构
考查角度 命题分析 注意事项
分析物质是否由分子构 如:HCl溶于水,完全电离,不存在分子;NaCl是离
分子数 成,或是否有相应分子存 子化合物,物质中无分子;SiO 是原子晶体,物质中也
2
在 无分子
①惰性气体是单原子分子,Cl 、O 、N 等是双原子分
原子数 ①要分析分子中的原子组 2 2 2
成,注意单原子分子、多 子,O 3 、P 4 等是多原子分子;原子分子;
②对实验式相同的混合物,按最简式来计算
②分子中原子及原子数比
如NO 和NO 、乙烯与丙烯、同分异构体、乙炔与苯、
值相同的混合物,总质量 2 2 4
乙酸与葡萄糖等,只要总质量一定,则其中所含原子数
一定,分子数不确定,但
与二者比例无关
原子数确定
确定核外电子数,要分析
电子数 基团与离子的差异:—OH与OH-的电子数不同
微粒的结构
①苯环中的碳碳键是介于单键和双键之间的一种独特的
明确结构情况,不能只看 键,不含有碳碳双键;
化学式来确定化学键数,
化学键数
要分析分子结构和晶体结
②1 mol白磷(P
4
)中含有P—P的数目为6N
A
;1 mol S
8
含8
构来确定 mol S—S;1 mol金刚石(晶体硅)中含有2 mol C—C(Si—
Si);1 mol SiO 含有4 mol Si—O
2
【易错提醒】
(1)记住特殊物质中所含微粒的数目,如Ne、DO、18O、—OH、OH-等;
2 2
(2)记住最简式相同的物质,如NO 和NO、乙烯(C H)和丙烯(C H)等;
2 2 4 2 4 3 6
(3)记住摩尔质量相同的物质,如N、CO、C H 等
2 2 4
3 . 氧化还原反应中转移电子数目
解题步骤 过程分析 注意事项
知晓常见反应的反应产物,
第一步:判断反应是 注 意 常 考 易 错 反 应 , 如 : 2Fe+3Cl
特别是涉及一些可变价元素 2
否正确 2FeCl ,Fe+2HCl=FeCl +H ↑
的反应 3 2 2
根据化学方程式,计算物质 如FeBr 和Cl 的反应中,当有部分Br-发生
第二步:相关物质过 2 2
是否过量,按不过量物质计 反应时,Fe2+已完全反应,计算转移电子数
量判断
算 时,要把两步的转移电子数合并计算
要注意特殊物质,如
①由NaO 、HO 制取1 mol O 转移2 mol电
根据化合价的升降来计算确 2 2 2 2 2
第三步:判断化合价 子;
定氧化、还原产物及转移的
变化
电子数 ②Fe与S、I 、非氧化性酸反应,1 mol Fe转
2
移 2 mol 电子;1 mol Fe 与足量的 Cl 、稀
2
HNO 反应,转移3 mol电子
3
【归纳总结】
熟记特殊反应中电子转移总数
反应 物质变化量 转移电子的物质的量或数目
1 mol Na O 1 mol或N
2 2 A
NaO+CO (或HO)
2 2 2 2
1 mol O 2 mol或2N
2 A
Cl+NaOH 1 mol Cl 1 mol或N
2 2 A
1 mol Cl 2 mol或2N
2 A
Cl+Fe
2
1 mol Fe 3 mol或3N
A
4 . 电解质溶液中粒子的数目
考查角度 命题分析 注意事项HSO 等强电解质在水中完全电离,稀溶
2 4
强电解质在水溶液中完全电离,弱 液中不存在硫酸分子;醋酸溶液中,
电离 电解质部分电离,计算分子数及离子 CHCOOH部分发生电离,CHCOOH分子
3 3
数时要考虑是否完全电离 数减少;CHCHOH是非电解质,水溶液
3 2
中分子数不变
有些盐中弱离子要发生水解,离子 如在 NaCO 溶液中,由于水解因素,
水解 2 3
数会增加或减少 CO-会减少,但阴离子数增加
3
常见陷阱是溶液的体积未知,则溶质的
计算溶液中微粒数目时要确认题干
体积因素 物质的量无法计算,所含微粒数也无法计
中是否已明确溶液体积
算
【易错提醒】
审准题目“要求”,是突破该类题目的关键
(1)溶液中是否有“弱粒子”,即是否存在弱电解质或能水解的“弱离子”,如1 L 1 mol·L-1的乙酸或1 L
1 mol·L-1乙酸钠溶液中CHCOO-的数目均小于N 。
3 A
(2)题目中是否指明了溶液的体积,如在pH=1的HCl溶液中,因溶液体积未知而无法求算H+的数目。
(3)所给条件是否与电解质的组成有关,如pH=1的HSO 溶液中c(H+)=0.1 mol·L-1,与电解质的组成无关;
2 4
0.05 mol·L-1的Ba(OH) 溶液,c(OH-)=0.1 mol·L-1,与电解质的组成有关。
2
5 .隐含的可逆反应
考查角度 命题分析 注意事项
经常考查的反应有:2SO +O 2SO 、2NO
2 2 3 2
在可逆反应中,由于反应不完全,计 NO 、N+3H 2NH 、Cl+H O
可逆反应 2 4 2 2 3 2 2
算微粒数时不能按完全反应计算 HCl+HClO 、 NH +H O NH ·H O NH +
3 2 3 2 4
+OH-
某些反应在反应过程中由于溶液浓度
发生变化会造成反应发生改变或停止, 如MnO 与浓盐酸反应,Cu与浓HSO 反应,Zn与
浓度影响 2 2 4
此类反应在判断转移电子数目、物质的 浓HSO 反应,Cu与浓硝酸反应
2 4
量的变化时均要考虑反应的改变
【归纳总结】
中学重要的可逆反应
(1)工业合成氨;(2)工业催化氧化二氧化硫;(3)制备水煤气;(4)氯气溶于水;(5)二氧化氮聚合;(6)铬酸
钾转化成重铬酸钾;
(7)所有的酯化反应;(8)在酸性条件下酯的水解反应等。
考向 1 不含有题干描述考查 N
A
1.(2025·四川省名校联盟高三大联考)设N 为阿伏加德罗常数的值,下列叙述错误的是( )
AA.28gC H 分子中含有的σ键数目为5N
2 4 A
B.密闭容器中0.2molNO与0.1molO 充分反应,产物的分子数为0.2N
2 A
C.在25℃时,1LpH为12的Ba(OH) 溶液中含有的OH-数目为0.01N
2 A
D.NaCl和NH Cl的混合物中含1molCl-,则混合物中质子数为28N
4 A
【答案】B
【解析】A项,1个C H 分子中5个σ键,28gC H 的物质的量为1mol,其中含有的 键数目为5N ,
2 4 2 4 A
故A正确;B项,密闭容器中0.2molNO与0.1molO 充分反应,生成0.2molNO ,NO 再发生2NO
2 2 2 2
NO,则产物的分子数小于0.2N ,故B错误;C项,在25℃时,1LpH为12的Ba(OH) 溶液中含有的OH-
2 4 A 2
的物质的量为1L×10-2mol/L=0.01mol,其数目为0.01N ,故C正确;D项,NaCl和NH Cl的混合物中含
A 4
1molCl-,即NaCl和NH Cl的物质的量和为1mol,1molNaCl质子数为28N 、1molNH Cl的质子数也为
4 A 4
28N ,则含1molCl-的混合物中质子数为28N ,故D正确;故选B。
A A
2.(2025·浙江部分高中高三开学考试)N 为阿伏加德罗常数的值。下列说法不正确的是( )
A
A.16gO(其分子结构为 )中共价键的数目为1.5N
8 A
B.1LHO中的OH-的数目为10-7N
2 A
C.2molNO与1molO 在密闭容器中充分反应后的分子数小于2N
2 A
D.1molCa(CN) 中存在 键
2
【答案】B
【解析】A项,1个O 分子中含有12个共价键,16gO 中共价键的数目为 ,A正
8 8
确;B项,不确定水的物质的量,且水为弱电解质,只能部分电离,故不能确定氢氧根离子数目,B错误;
C项,NO和氧气生成二氧化氮,部分二氧化氮转化为四氧化二氮,则2molNO与1molO 在密闭容器中充
2
分反应后的分子小于2mol,数目小于2N ,C正确;D项,Ca(CN) 为离子化合物,在CN-中存在1个碳氮
A 2
σ共价键,则1molCa(CN) 中存在 键,D正确;故选B。
2
3.(2025·浙江省名校协作体高三联考)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.标准状况下,22.4L HCl气体中,H+的数目为N
A
B.2.4g石墨晶体中含有C—C键的数目为0.6N
A
C.4.6gNa与 稀硫酸充分反应,转移的电子数为0.2N
A
D.已知N 为正盐,则1mol HPO 含羟基数为2N
A 3 2 A
【答案】C
【解析】A项,HCl气体是由分子构成,未发生电离,无H+,A错误;B项,2.4g石墨物质的量为0.2mol,根据石墨的结构,1molC含共价键1.5mol,故0.2mol石墨含C-C键数目为0.3N ,B错误;C项,
A
4.6g Na物质的量为0.2mol,与稀硫酸充分反应,即使稀硫酸量不足,水也会和钠反应,故Na完全反应生
成H 0.1mol,转移的电子数为0.2N ,C正确;D项,含氧酸中羟基氢原子有酸性,NaH PO 为正盐,
2 A 2 2
HPO 为一元酸,故1mol HPO 含羟基数为N ,D错误;故选C。
3 2 3 2 A
4.(2025·浙江省金华第一中学高三选考模拟)设N 为阿伏伽德罗常数的值,下列说法正确的是( )
A
A.10g的2H18O中含有的质子数与中子数均为5 N
2 A
B.32g硫在足量的氧气中充分燃烧,转移电子数为6 N
A
C.N(g)+3H(g) 2NH (g) ΔH=−92.4kJ/mol,1mol N 被还原,放出92.4kJ能量
2 2 3 2
D.pH=4的盐酸和pH=4的醋酸溶液等体积混合后,溶液中 的数目仍为10-4 N
A
【答案】C
【解析】A项,2H18O中有10个质子,12个中子,相对分子量为22,10g2H18O物质的量为 mol,
2 2
质子数为 N ,中子数为 N ,A错误;B项,32g硫物质的量为1mol,在足量氧气中充分燃烧,生成
A A
1molSO ,转移电子数为4N ,B错误;C项,N(g)+3H(g) 2NH (g) ΔH=−92.4kJ/mol,根据热化学方
2 A 2 2 3
程式的含义,1mol N 参与反应被还原,放出92.4kJ能量,C正确;D项,没有说明体积具体是多少,无法
2
计算氢离子数目,D错误;故选C。
考向 2 含有题干描述考查 N
A
5.[新题型](2025·河北省邢台市邢襄联盟高三期中)ClO 能把废水中的CN-氧化成无毒气体,发生的反
2
应为2ClO +2NaCN=2CO+N +2NaCl,设N 为阿伏加德罗常数的值。下列说法正确的是( )
2 2 2 A
A.ClO 与CO 的VSEPR模型相同
2 2
B.1molCN-中含有的π键数目为2N
A
C.22.4LN 中含有的原子数为N
2 A
D.1mol·L-1NaCl溶液中含有的 的数目为N
A
【答案】B
【解析】A项,ClO 中心原子Cl原子价层电子对=2+ ,其中Cl提供一个单电子,2个O
2
原子的2p轨道各提供两个电子,形成π 5大π键,中心原子Cl的价电子数为3,VSEPR为平面三角形,
3CO 中心原子C原子价层电子对=2+ =2,VSEPR构型为直线形结构,二者的VSEPR模型不同,A
2
错误;B项,CN-中有一个σ键和2个π键,1molCN-中含有的π键数目为2N ,B正确;C项,没有注明标
A
准状况,不能确定N 的物质的量,C错误;D项,没有给出溶液的体积,无法计算NaCl的物质的量,D
2
错误;故选B。
6.(2025·河南省许平名校高三期中)已知反应NaClO+H O+H SO →ClO ↑+Na SO +H O+O↑ (未配平)。
3 2 2 2 4 2 2 4 2 2
设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A. 的NaClO 溶液中含 数为0.1N
3 A
B.3.4gH O 中含质子数为1.8N
2 2 A
C.0.1 molH O中含极性共价键的数目为0.1N
2 A
D.每生成2.24L(标准状况下)O 转移电子数为0.1N
2 A
【答案】B
【解析】A项,只给出了溶液的浓度,无体积,无法计算,A项错误;B项,每个HO 分子含18个质
2 2
子,3.4gH O 为0.1mol,含质子数为1.8N ,B项正确;C项,0.1 molH O中含极性共价键的数目为
2 2 A 2
0.2N ,C项错误;D项,该反应是HO 两个-1价的氧原子被氧化,每生成标准状况下2.24LO 转移电子数
A 2 2 2
为0.2N ,D项错误;故选B。
A
7.(2025·山西省三晋名校高三联考)设N 为阿伏加德罗常数的值。关于反应4BF+2
A 3
NaCO+2H O=3NaBF+Na[B(OH) ]+2CO↑,下列叙述正确的是( )
2 3 2 4 4 2
A.0.1molBF 中B原子最外层电子数为0.8N
3 A
B.10.6gNaCO 固体含CO2-数为0.1N
2 3 3 A
C.标准状况下,4.48LCO 含 键数为0.8N
2 A
D.1mol Na[B(OH) ]含配位键数为4N
4 A
【答案】B
【解析】A项,三氟化硼分子中硼原子的最外层电子数为6,则0.1mol三氟化硼分子中硼原子最外层
电子数为0.1mol×6×N mol—1=0.6N ,故A错误;B项,10.6g碳酸钠固体中含有的碳酸根离子数目为
A A
×1×N mol—1=0.1N ,故B正确;C项,二氧化碳的结构式为O=C=O,分子中碳氧双键含有1个σ
A A
键,标准状况下,4.48L二氧化碳中含有σ键的数目为 ×2×N mol—1=0.4N ,故C错误;D项,四
A A
羟基合硼酸钠中含有1个配位键,则1mol四羟基合硼酸钠中含有的配位键数目为1mol×1×N mol—1=N ,故
A AD错误;故选B。
8.[新考法](2025·广西邕衡教育名校联盟高三适应性检测)某工厂利用烟气处理含NaCr O 的废水,在
2 2 7
脱硫的同时制备Cr O,具体流程如下图所示。N 表示阿伏加德罗常数的值,下列说法正确的是( )
2 3 A
A.1L含0.2mol·L-1NaCr O 的废水中,Cr O2-的数目为0.2N
2 2 7 2 7 A
B.每处理0.1molCr O2-,消耗SO 的体积为6.72L
2 7 2
C.1molSO 中σ键的数目为2N
2 A
D.每生成Cr O,转移电子数为3N
2 3 A
【答案】C
【解析】A项,1L含0.2mol·L-1NaCr O 的废水中,Cr O2-会部分变成CrO2-,无法计算Cr O2-的个数,
2 2 7 2 7 4 2 7
故A错误;B项,由于题中未交代是否为标准状况,无法计算每处理0.1molCr O2-时消耗的SO 体积,故
2 7 2
B错误;C项,一个二氧化硫分子含有两个σ键,N=nN ,1molSO 中含有σ键的数目为2N ,故C正确;
A 2 A
项,每生成1mol Cr O,铬元素由+6价降为+3价,一个Cr O2-转化为Cr O 得到6个电子,每生成Cr O,
2 3 2 7 2 3 2 3
转移6mol电子、转移电子数为N=nN =6N ,故D错误;故选C。
A A
9.[新考法](2025·江西省上进联考高三)设N 为阿伏加德罗常数的值,部分含氮的物质有如图转化关
A
系。下列叙述正确的是( )
A.常温常压下,2.24LN 含原子数为0.2N
2 A
B.3.7gNHF固体含离子总数为0.1N
4 A
C.反应①中,生成0.1mol还原产物,则需要HNO 分子数为0.3N
2 A
D.3.2gN H 中含极性键总数为0.5N
2 4 A
【答案】C
【解析】A项,常温常压下,气体摩尔体积 ,2.24LN 的物质的量不是0.1mol,A错
2
误;B项,3.7gNHF固体的物质的量为0.1mol,NH F是离子化合物,含阴、阳两种离子,B错误;C项,
4 4
反应①为3NH+3HNO =HN(还原产物)+2HN(氧化产物)+6H O,生成0.1mol还原产物,需要0.3mol
2 4 2 3 3 2HNO,C正确;D项,1个NH 分子中有4个N—H键和1个N—N键,3.2gN H(0.1mol)含极性共价键数
2 2 4 2 4
目为0.4N ,D错误;故选C。
A
10.[新考法](2025·山西省三晋卓越联盟高三质量检测)硫及其化合物部分转化关系如图。设N 为阿伏
A
加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2LSO 中质子总数为16 N
2 A
B.1mol·L-1的NaS溶液中,含S微粒总数目为N
2 A
C.反应①每生成9.6gS,转移电子数目为0.6 N
A
D.反应②每生成 还原产物,则溶液中阴离子的数目减少1.5 N
A
【答案】A
【解析】A项,SO 中含有32个质子,标准状况下,11.2LSO 的物质的量为0.5mol,所含质子数为
2 2
,A正确;B项,无溶液体积,无法计算含S微粒总数目,B错误;C项,反应
①中SO 的S元素由+4价下降到0价,HS的S元素由-2价上升到0价,化学方程式为
2 2
SO +2H S=3S+2H O,9.6gS的物质的量为 ,每生成0.3mol S,消耗0.1mol SO ,转移电子
2 2 2 2
数目为 ,C错误;D项,反应②中S由0价下降到-2价被还原生成S2-,又由0价上升到
+4价被氧化为SO 2-,离子方程式为 ,每生成1molS2-消耗3mol OH-,同时生
3
成0.5mol SO 2-,但由于S2-和SO 2-会水解,则溶液中阴离子减少的数目小于1.5N ,D错误;故选A。
3 3 A
题型二 一定物质的量浓度溶液的配制
1.(2024·甘肃卷,6,3分)下列实验操作对应的装置不正确的是( )A B C D
灼烧海带制海带 准确量取15.00mL稀 配制一定浓度的 使用电石和饱和食
灰 盐酸 NaCl溶液 盐水制备C H
2 2
【答案】A
【解析】A项,灼烧海带制海带灰应在坩埚中进行,并用玻璃棒搅拌,给坩埚加热时不需要使用石棉
网或陶土网,A项错误;B项,稀盐酸呈酸性,可用酸式滴定管量取15.00mL稀盐酸,B项正确;C项,
配制一定浓度的NaCl溶液时,需要将在烧杯中溶解得到的NaCl溶液通过玻璃棒引流转移到选定规格的容
量瓶中,C项正确;D项,电石的主要成分CaC 与水发生反应CaC +2H O→Ca(OH) +CH≡CH↑制取C H,
2 2 2 2 2 2
该制气反应属于固体与液体常温制气反应,分液漏斗中盛放饱和食盐水,具支锥形瓶中盛放电石,D项正
确;故选A。
2.(2024·北京卷,6,3分)下列实验的对应操作中,不合理的是( )
眼睛注视锥形瓶中溶液
A.用 标准溶液滴定 溶液 B.稀释浓硫酸
C.从提纯后的 溶液获得 晶体 D.配制一定物质的量浓度的 溶液
【答案】D
【解析】A项,用HCl标准溶液滴定NaOH溶液时,眼睛应注视锥形瓶中溶液,以便观察溶液颜色的
变化从而判断滴定终点,A项合理;B项,浓硫酸的密度比水的密度大,浓硫酸溶于水放热,故稀释浓硫酸时应将浓硫酸沿烧杯内壁缓慢倒入盛水的烧杯中,并用玻璃棒不断搅拌,B项合理;C项,NaCl的溶解
度随温度升高变化不明显,从NaCl溶液中获得NaCl晶体采用蒸发结晶的方法,C项合理;D项,配制一
定物质的量浓度的溶液时,玻璃棒引流低端应该在容量瓶刻度线以下;定容阶段,当液面在刻度线以下约
1cm时,应改用胶头滴管滴加蒸馏水,D项不合理;故选D。
3.(2024·江苏卷,3,3分)实验室进行铁钉镀锌实验。下列相关原理、装置及操作不正确的是( )
A B C D
配制NaOH溶液 铁钉除油污 铁钉除锈 铁钉镀锌
【答案】A
【解析】A项,配制一定物质的量浓度的溶液时,溶质要放在烧杯中溶解,不能直接放在容量瓶中溶
解,A不正确;B项,油污的主要成分是油脂,油脂在碱性条件下可以发生水解反应生成可溶于水的甘油
和高级脂肪酸盐,因此,铁钉放在NaOH溶液中加热后可以除去其表面的油污,B正确;C项,铁锈的主
要成分是Fe O·nH O,其可溶于盐酸,因此,将铁钉放在盐酸中可以除去其表面的铁锈,C正确;D项,
2 3 2
该装置为电解池,铁钉与电源负极相连作阴极,锌片与电源的正极相连作阳极,电解质溶液为 ZnCl 溶液,
2
因此,该装置为电镀装置,可以实现铁钉上镀锌,D正确;故选A。
4.(2023•全国甲卷,9)实验室将粗盐提纯并配制 的NaCl溶液。下列仪器中,本实验必
须用到的有( )
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥ B.①④⑤⑥ C.②③⑦⑧ D.①⑤⑥⑧
【答案】D
【解析】实验室将粗盐提纯时,需要将其溶于一定量的水中,然后将其中的硫酸根离子、钙离子、镁
离子依次用稍过量的氯化钡溶液、碳酸钠溶液和氢氧化钠溶液除去,该过程中有过滤操作,需要用到烧杯、
漏斗和玻璃棒;将所得滤液加适量盐酸酸化后蒸发结晶得到较纯的食盐,该过程要用到蒸发皿和酒精灯;
用提纯后得到的精盐配制溶液的基本步骤有称量、溶解、转移、洗涤、定容、摇匀等操作,需要用到天平、
容量瓶、烧杯、玻璃棒、胶头滴管等。综上所述,本实验必须用到的有①天平、⑤容量瓶、⑥烧杯、⑧酒
精灯,故选D。
5.(2024·湖北卷,18节选)(1)配制1.00mol·L-1的CoSO 溶液,需要用到下列仪器中的 (填标号)。
4a. b. c. d.
【答案】(1)bc
【解析】(1)配制1.00 mol·L-1的CoSO 溶液,需要用到容量瓶、胶头滴管等等,因此选bc。
4
6.(2024·全国甲卷,9节选)下图为“溶液配制”的部分过程,操作a应重复3次,目的是 ,定容
后还需要的操作为 。
【答案】(4)避免溶质损失 盖好瓶塞,反复上下颠倒、摇匀
【解析】(4)操作a为洗涤烧杯和玻璃棒,并将洗涤液转移到容量瓶中,目的是避免溶质损失;定容后
应盖好瓶塞,反复上下颠倒、摇匀。
溶液配制过程中的“四个数据”
数据 要求或解释
药吕的质量 实验室中一般用托盘天平称量药品,而托盘天平只能精确到0.1 g,所以记录数
据时只能保留小数点后一位数字。如所需 NaCl的质量为 14.6 g,不能写为
14.60 g
容量瓶的规格 (1)选择容量瓶的规格时应该与所配溶液体积相等或稍大,如需配制 480 mL某
溶液,则应该选择500 mL容量瓶; (2)回答补充仪器的问题时应该注明容量瓶
的规格,如回答“500 mL容量瓶”时,不能只回答“容量瓶”
洗涤烧杯和玻璃棒 移液时洗涤烧杯和玻璃棒2~3次是为了确保溶质全部转入容量瓶中,否则会导
2~3次 致溶液浓度偏低
液面距容量瓶刻度线 定容时,当液面距容量瓶刻度线1~2 cm时,应该改用胶头滴管滴加,否则容易
1~2 cm 导致液体体积超过刻度线,使溶液浓度偏低
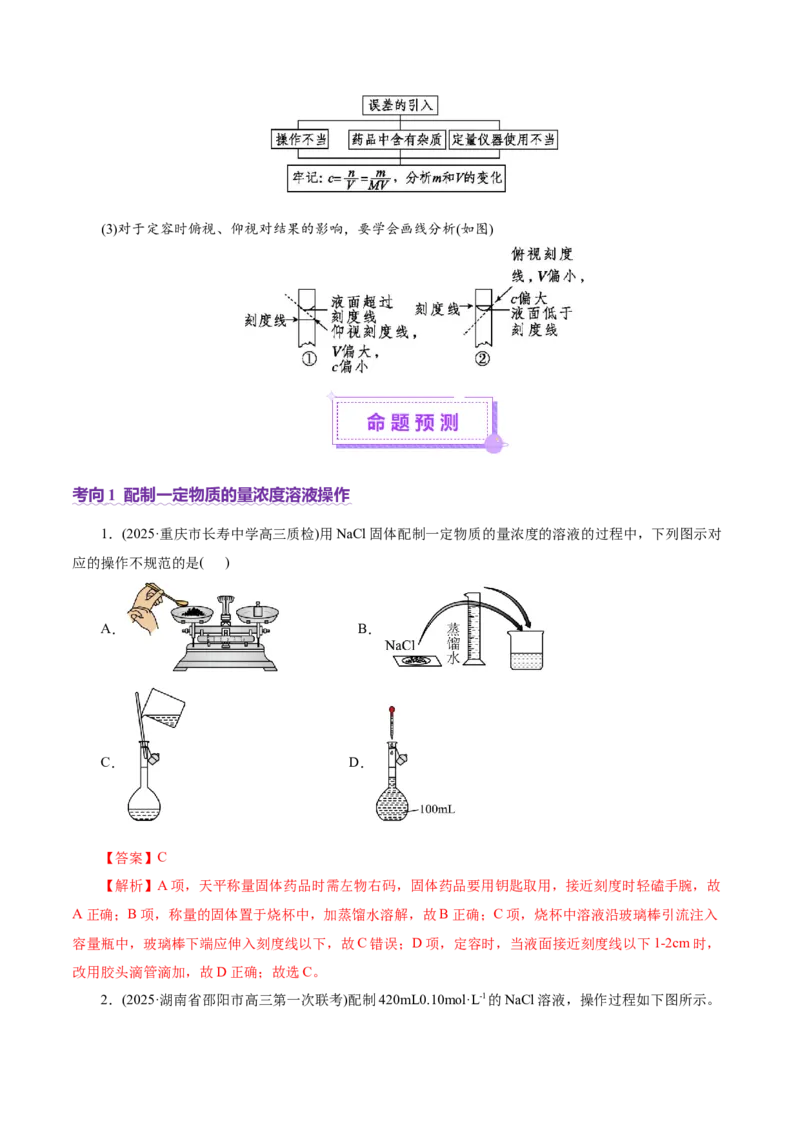
1. 配制一定物质的量浓度溶液操作
以配制500 mL 1.0 mol·L-1 NaCl溶液为例:【易错提醒】
1.做需要补充仪器的实验题时,要学会“有序思考”——按照实验的先后顺序、步骤,思考每一步
所需仪器,然后与已知仪器对比,就一定不会漏写某种仪器。
2.容量瓶的规格,常见的有100 mL、250 mL、500 mL、1 000 mL。
3.所用定量仪器量筒、托盘天平的精确度。
2 .配制一定物质的量浓度的溶液的误差分析
(1)判断配制实验误差模板
(2)误差分析的思维流程(3)对于定容时俯视、仰视对结果的影响,要学会画线分析(如图)
考向 1 配制一定物质的量浓度溶液操作
1.(2025·重庆市长寿中学高三质检)用NaCl固体配制一定物质的量浓度的溶液的过程中,下列图示对
应的操作不规范的是( )
A. B.
C. D.
【答案】C
【解析】A项,天平称量固体药品时需左物右码,固体药品要用钥匙取用,接近刻度时轻磕手腕,故
A正确;B项,称量的固体置于烧杯中,加蒸馏水溶解,故B正确;C项,烧杯中溶液沿玻璃棒引流注入
容量瓶中,玻璃棒下端应伸入刻度线以下,故C错误;D项,定容时,当液面接近刻度线以下1-2cm时,
改用胶头滴管滴加,故D正确;故选C。
2.(2025·湖南省邵阳市高三第一次联考)配制420mL0.10mol·L-1的NaCl溶液,操作过程如下图所示。下列说法中正确的是( )
A.“操作1”前需用托盘天平称取2.5gNaCl固体
B.“操作3”中烧杯、玻璃棒需用自来水洗涤2 3次
C.“操作4”中若仰视容量瓶刻度线,会使NaC∼l溶液浓度偏低
D.“操作5”中摇匀后发现液面低于刻度线,使用胶头滴管定容
【答案】C
【解析】A项,420mL0.10mol·L-1的NaCl溶液,需要NaCl的质量为
,A错误;B项,“操作3”中烧杯、玻璃棒需用蒸馏水洗涤
2 3次,B错误;C项,“操作4”中若仰视容量瓶刻度线,导致加水偏多,V偏大,所以NaCl溶液浓度偏
低∼,C正确;D项,摇匀后发现液面低于刻度线,属于正常情况,不应该再补加蒸馏水,D错误;故选
C。
3.用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸,下列操作正确的是(
)
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.必需的定量仪器有50 mL量筒、250 mL容量瓶和托盘天平
C.量取浓硫酸的体积为25.0 mL
D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
【答案】C
【解析】稀释浓硫酸时,应将浓硫酸缓慢注入水中并不断搅拌,A项错误;该实验不需要托盘天平,
B项错误;根据稀释前后溶质质量不变知,配制该稀硫酸需要浓硫酸的体积为V==25.0 mL,C项正确;
不能在容量瓶里稀释浓硫酸,在烧杯里稀释并冷却后,再转移到容量瓶中,最后加水定容,D项错误。
4.用密度为1.84 g·mL-1、质量分数为98%的浓硫酸配制100 mL 3 mol·L-1稀硫酸。下列各步骤中操作
正确的是( )
A.计算、量取:用10 mL量筒量取16.3 mL浓硫酸
B.溶解、稀释:先将浓硫酸倒入烧杯,再直接倒入30 mL左右的蒸馏水,搅拌,静置
C.转移、洗涤:待溶液冷却后,将溶液转移到容量瓶中,用蒸馏水洗涤烧杯和玻璃棒,洗涤液转入
容量瓶,重复2~3次
D.定容、摇匀:加水至凹液面最低处与刻度线相切,摇匀,在容量瓶上贴上标签,写上溶液成分及
浓度【答案】C
【解析】A 项,密度为 1.84 g·mL-1、质量分数为 98%的浓硫酸的物质的量浓度为 c=
1 000×1.84×98%
mol·L-1=18.4 mol·L-1,配 100 mL 3 mol·L-1稀硫酸时所需浓硫酸的体积为 V =
浓
98
0.1×3
L≈0.016 3 L=16.3 mL,应用25 mL的量筒量取16.3 mL浓硫酸,A错误;B项,浓硫酸稀释时,
18.4
将浓硫酸倒入蒸馏水中,并且不断搅拌,B错误;D项,容量瓶不可贮存溶液,定容、摇匀后,应将溶液
倒入试剂瓶并贴上标签,注明溶液成分及浓度,D错误。
考向 2 配制一定物质的量浓度溶液误差分析
5.(2025·黑龙江省实验中学高三月考)实验室用氢氧化钠固体配制0.1mol/L、500mL的氢氧化钠溶液,
下列说法错误的是( )
A.称量氢氧化钠固体要用小烧杯,不能直接放到滤纸上称量
B.如果把氢氧化钠和砝码放反了,会导致所配溶液浓度偏低
C.如果没有冷却至室温就进行定容,会导致所配溶液浓度偏高
D.某同学仰视定容,会导致所配溶液浓度偏低
【答案】B
【解析】A项,氢氧化钠会吸收空气中的二氧化碳和水蒸气,为防止氢氧化钠变质,称量氢氧化钠固
体时,要用小烧杯称量,不能直接放到滤纸上称量,故A正确;B项,配制0.1mol/L、500mL的氢氧化钠
溶液需要氢氧化钠的质量为0.1mol/L×0.5L×40g/mol=2.0g,则称量氢氧化钠固体时,不需要用到游码,所
以砝码和物品的位置放反,对结果没有影响,故B错误;C项,如果没有冷却至室温就进行定容会使溶液
的体积偏小,导致所配溶液浓度偏高,故C正确;D项,仰视定容会使溶液的体积偏大,导致所配溶液浓
度偏低,故D正确;故选B。
6.(2025·山西省部分学校高三联考)配制一定物质的量浓度的硫酸溶液,下列情况会使所配制的硫酸
溶液浓度偏高的是( )
A.用量筒量取一定体积的浓硫酸时俯视刻度线
B.硫酸溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
C.俯视容量瓶颈部的刻度线定容
D.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
【答案】C
【解析】A项,配制硫酸溶液,用量筒量取浓硫酸时俯视刻度线,量取的浓硫酸的体积偏少,会使所
配制的硫酸溶液浓度偏低,故A项错误;B项,硫酸溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤,
会使所配制的硫酸溶液浓度偏低,故B项错误;C项,俯视容量瓶颈部的刻度线定容,则所加水的量偏少,会使所配制的硫酸溶液浓度偏高,故C项正确;D项,定容后摇匀,发现液面降低,又补加少量水,重新
达到刻度线,则所加水的量偏多,会使所配制的硫酸溶液浓度偏低,故D项错误;故选C。
7.(2025·江苏省盐城市高三第一阶段检测)配制一定物质的量浓度的NaCO 溶液时,下列操作使配制
2 3
溶液浓度偏高的是( )
A.溶液转移到容量瓶后,烧杯内壁及玻璃棒未用蒸馏水洗涤
B.溶解后未经冷却就移液
C.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分
D.容量瓶用蒸馏水洗净后,没烘干就直接使用
【答案】B
【解析】A项,溶液转移到容量瓶后,烧杯内壁及玻璃棒未用蒸馏水洗涤,则有一部分溶质滞留在烧
杯内,容量瓶内溶质的物质的量减小,所配溶液的浓度偏低,A不符合题意;B项,溶解后未经冷却就移
液,定容后冷却,溶液的体积偏小,所配溶液的浓度偏高,B符合题意;C项,定容时如果加水超过了刻
度线,用胶头滴管直接吸出多余部分,将造成溶质的物质的量减小,所配溶液的浓度偏低,C不符合题意;
D项,容量瓶用蒸馏水洗净后,没烘干就直接使用,对溶质的物质的量、溶液的体积都不产生影响,所配
溶液的浓度不受影响,D不符合题意;故选B。
8.(2024•宁夏石嘴山市期末)用溶质质量分数为 的浓硫酸(ρ=1.84g· cm-3)配制 稀
硫酸,下列操作正确的是( )
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.必须用到的定量仪器有200mL容量瓶和托盘天平
C.量取浓硫酸的体积为20.0mL
D.量取浓硫酸时仰视,定容时俯视,都会使所配硫酸溶液浓度偏大
【答案】D
【解析】A项,稀释浓硫酸时,应将浓硫酸缓慢注入盛有一定量蒸馏水的烧杯中,并不断搅拌至冷却,
A错误;B项,实验室没有200mL容量瓶,则配制200ml1.84mol/L稀硫酸时,必须用到的定量仪器为
250mL容量瓶和量筒,B错误;C项,由c= 可知,浓硫酸的浓度为 mol/
L=18.4mol/L,由稀释定律可知,量取浓硫酸的体积为 ×103mL/L=25.0mL,C错误;D项,
量取浓硫酸时仰视会使硫酸的物质的量增大,导致所配硫酸溶液浓度偏大,定容时俯视会使溶液的体积偏
小,导致所配硫酸溶液浓度偏大,D正确;故选D。