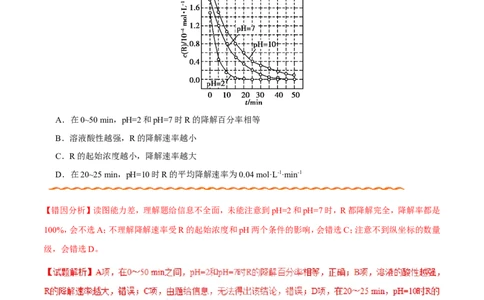
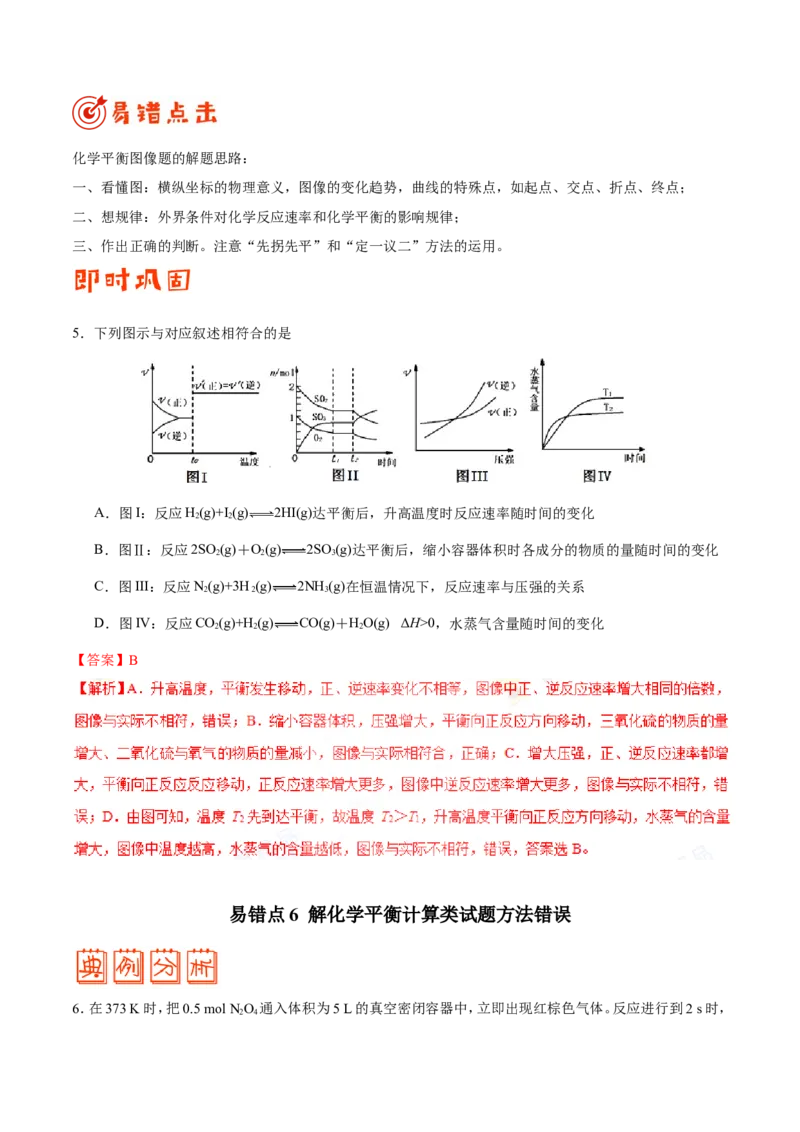
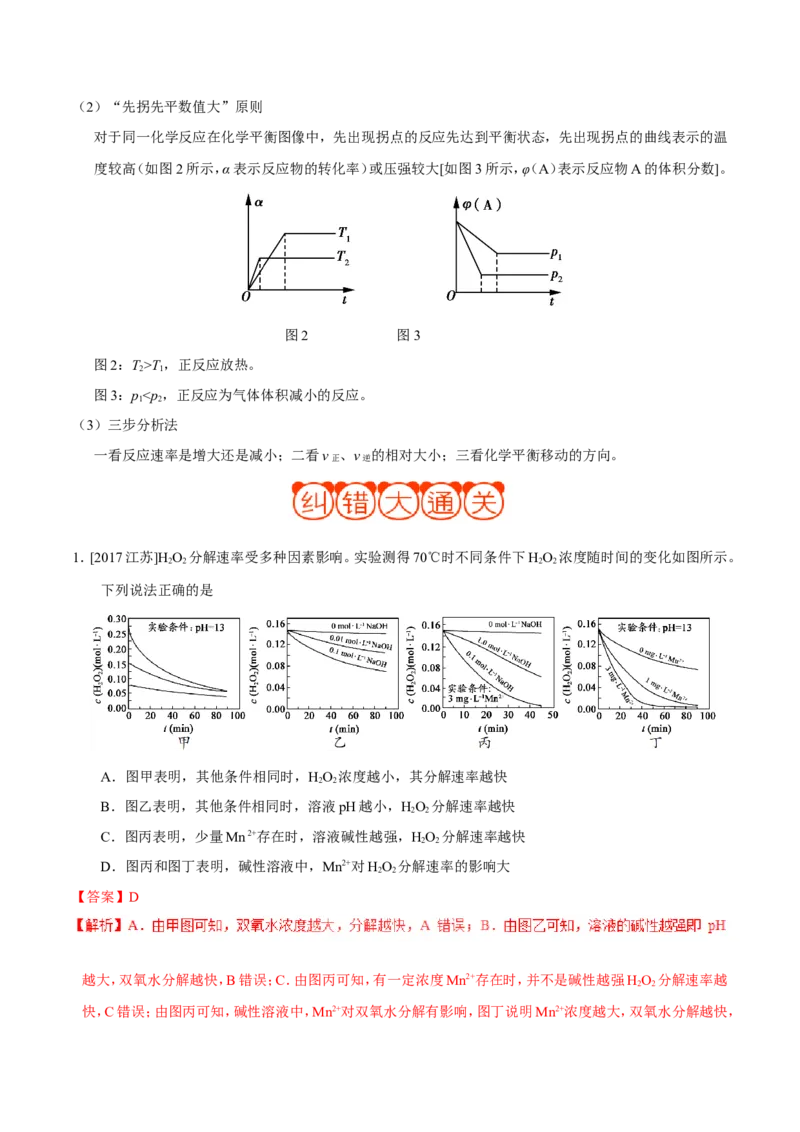
1.一定条件下,溶液的酸碱性对TiO 光催化染料R降解反应的影响如图所示。下列判断正确的是
2
A.在0~50 min,pH=2和pH=7时R的降解百分率相等
B.溶液酸性越强,R的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在20~25 min,pH=10时R的平均降解速率为0.04 mol·L-1·min-1
【错因分析】读图能力差,理解题给信息不全面,未能注意到pH=2和pH=7时,R都降解完全,降解率都是
100%,会不选A;不理解降解速率受R的起始浓度和pH两个条件的影响,会错选C;注意不到纵坐标的数量
级,会错选D。
【参考答案】A1.根据定义求化学反应速率:v= 。
2.根据反应速率与化学方程式中各物质的化学计量数的关系计算。同一个化学反应,同一段时间内,用不同
物质的浓度变化表示的反应速率,数值可能不同,但意义相同,其数值之比等于化学方程式中各物质的化
学计量数之比。对于化学反应 mA(g)+nB(g) pC(g),即 v(A)∶v(B)∶v(C)=m∶n∶p,或
。
3.由于同一反应的化学反应速率用不同的物质表示时数值可能不同,所以比较反应的快慢不能只看数值的
大小,而要进行一定的转化。
(1)单位是否统一,若不统一,换算成相同的单位。
(2)换算成同一物质表示的反应速率,再比较数值的大小。
(3)比较反应速率与化学计量数的比值,即对于一般的化学反应aA(g)+bB(g) cC(g)+dD(g),比较
与 ,若 > ,则用A表示的反应速率比B的大。
注意:理解化学反应速率概念应注意的“三点”
(1)平均速率和瞬时速率:中学化学中,通常所说的化学反应速率一般是指平均速率,即某段时间内的平均
反应速率,而不是某时刻的瞬时速率。
(2)化学反应速率越快不等于化学反应现象越明显,如某些中和反应。
(3)同一反应中,同一时间段内用不同物质的物质的量浓度变化表示的反应速率,数值可能不同,但意义相同,
其数值之比等于化学方程式中对应物质的化学计量数之比。
1.在容积固定的容器中发生反应:CO(g)+2H(g) CHOH(g) ΔH<0,各物质的浓度如表所示:
2 3
c(CO)mol/L c(H )mol/L c(CHOH)mol/L
2 3
0 0.8 1.6 0
2 min 0.6 x 0.2
4 min 0.3 0.6 0.5
6 min 0.3 0.6 0.5
下列说法错误的是
A.2~4 min内用H 表示的平均反应速率为0.3 mol/(L·min)
2B.达到平衡时,CO的转化率为62.5%
C.反应在第2 min时改变了条件,可能是加入了催化剂
D.反应在第2 min时改变了条件,可能是增加了H 的浓度
2
【答案】D
易错点2 不理解外界条件对反应速率的影响实质
2.下列说法错误的是
A.已知在T ℃时,反应2A(g)+B(g) 3C(g) ΔH>0的正反应速率表示为v,若降低温度,逆反应速率
减小
B.在恒容容器中发生反应N(g)+3H(g) 2NH (g),若往容器中充入He,正逆反应的速率均不变
2 2 3
C.当一定量的锌粉和4 mol·L-1的过量盐酸反应时,为了减慢反应速率,又不影响产生H 的总量,可向容
2
器中加入一些水或硝酸钠溶液
D.对任何一个化学反应,温度发生变化,化学反应速率一定发生变化
【错因分析】如果不明白外界因素对化学反应速率的影响,不能抓住影响反应速率的实质(是浓度变化引起的,
还是加入催化剂引起的),将会错解。如:本题选项B,若分不清恒压条件和恒容条件下向容器中充入不反应
的气体,导致反应物和生成物浓度的变化情况,则会陷入解题误区。学&科网
【试题解析】选项A,温度降低,正、逆反应速率均减小,A正确;在恒容容器中充入不反应的气体,反应物和生
成物的浓度均不发生变化,正、逆反应速率均不变,B正确;选项C,若能使溶液中氢离子的浓度减小,反应速
率将减小,因此可以加入一些水,但是不能加入硝酸钠溶液,因为在酸性条件下,硝酸根离子将与锌粉发生氧
化还原反应,生成氮的氧化物,从而使生成氢气的量减少,C项错。
【参考答案】C外界条件对化学反应速率的影响
中学化学反应速率的实质是某段时间内的平均反应速率,在外界条件不变时,对于可逆反应,化学反应
速率一般是由小变大,再变小,最终达到平衡状态。外界条件对化学反应速率及化学平衡的影响:
(1)增大反应物浓度,瞬时,正反应速率增大,逆反应速率不变,正反应速率大于逆反应速率,平衡向正
反应方向移动,达到新平衡;减小生成物浓度,瞬时,逆反应速率减小,正反应速率不变,正反应速率大于逆
反应速率,平衡向正反应方向移动,达到新平衡。
(2)增大压强,正、逆反应速率都增大,气体分子数多的一边的速率增大的程度较大;减压时,气体分子
数多的一边的速率减小的程度较大。
(3)升温,吸热和放热反应的速率都增大,吸热反应速率增大的程度较大;降温,吸热反应速率减小的程
度较大。
(4)使用催化剂时,同倍数、同时增大正、逆反应速率,正、逆反应速率始终相等。
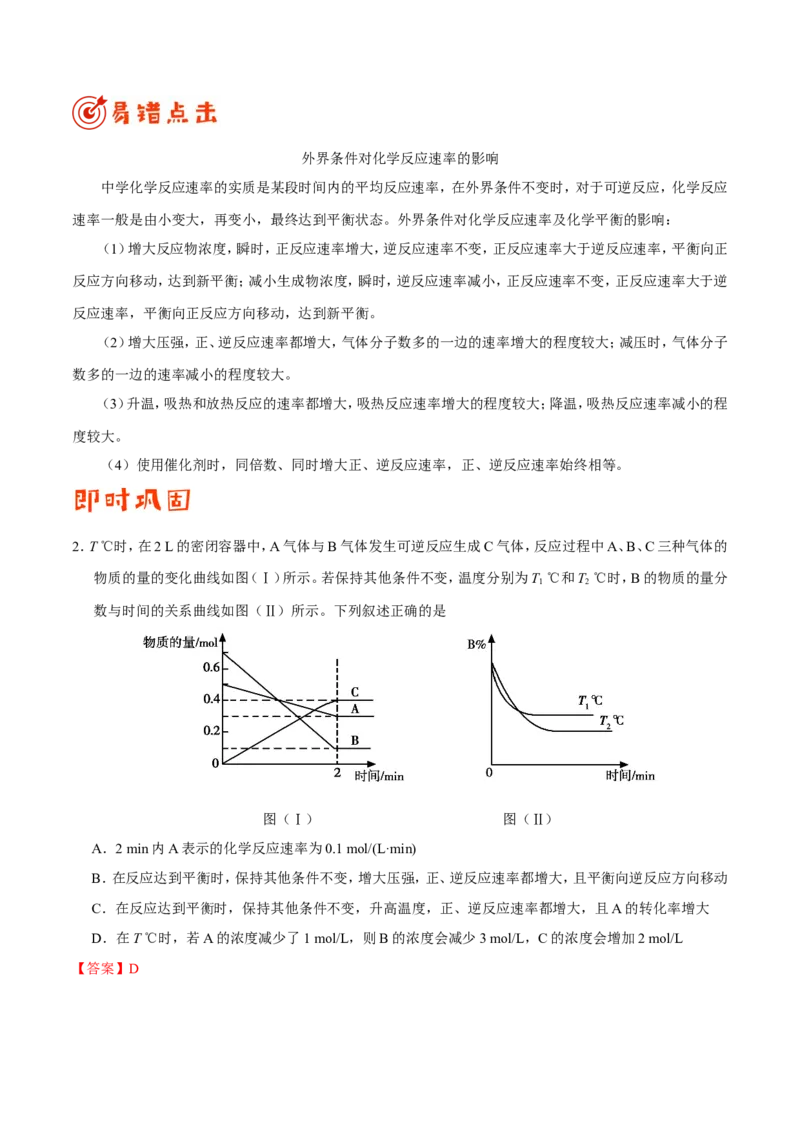
2.T ℃时,在2 L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B、C三种气体的
物质的量的变化曲线如图(Ⅰ)所示。若保持其他条件不变,温度分别为T ℃和T ℃时,B的物质的量分
1 2
数与时间的关系曲线如图(Ⅱ)所示。下列叙述正确的是
图(Ⅰ) 图(Ⅱ)
A.2 min内A表示的化学反应速率为0.1 mol/(L·min)
B.在反应达到平衡时,保持其他条件不变,增大压强,正、逆反应速率都增大,且平衡向逆反应方向移动
C.在反应达到平衡时,保持其他条件不变,升高温度,正、逆反应速率都增大,且A的转化率增大
D.在T ℃时,若A的浓度减少了1 mol/L,则B的浓度会减少3 mol/L,C的浓度会增加2 mol/L
【答案】D增大压强,正、逆反应速率均增大,但平衡向气体体积减小的方向移动,B错误;从图(Ⅱ)知T>T,因为T
1 2 1
℃达到平衡所需的时间短,温度高反应速率大,而T ℃时B的物质的量分数高,说明温度升高,平衡向逆反
1
应方向移动,则A的转化率减小,C错误;从所得的反应方程式可知D正确。学&科网
易错点3 对化学平衡状态的理解不透彻
3.在一个不传热的固定容积的密闭容器中,可逆反应mA(g)+nB(g) pC(g)+qD(g),当m、n、p、q为任意整
数时,下列说法一定能说明反应已达到平衡的是
①体系的压强不再改变 ②体系的温度不再改变 ③各组分的浓度不再改变
④各组分的质量分数不再改变 ⑤反应速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q
⑥单位时间内m mol A发生断键反应,同时p mol C也发生断键反应
A.③④⑤⑥ B.②③④⑥ C.①③④⑤ D.①③④⑥
【错因分析】反应达到平衡状态时,正、逆反应速率相等,各物质的浓度、百分含量不变,由此衍生出来的各种
量不变。需要注意的是,选择判断的物理量,随着反应的进行发生变化,当该物理量由变量变为定值时,说明
可逆反应达到平衡状态。若不清楚有可能存在m+n=p+q,体系压强始终不变,则易错选①,若不清楚反应速率
之比始终存在v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q,与是否达到平衡状态无关,易错选⑤。【参考答案】B
化学平衡状态的判断
达到化学平衡状态的标志:v =v ,平衡混合物中各组成成分的含量保持不变。“v =v ”是化学平衡
正 逆 正 逆
的本质特征,即反应体系中同一物质的消耗速率和生成速率相等。各组分的含量不变,是指各组分的浓度、质
量分数、体积分数(有气体参加的可逆反应)、反应物的转化率等均保持不变。
判断某一可逆反应是否达到平衡状态的“等价标志”:
(1)对于反应前后气体体积不等的反应,当恒温、恒容时,压强不变、气体的平均相对分子质量不变,或
恒温、恒压时,体积不变、混合气体的密度不变,说明反应处于平衡状态。
(2)对于有颜色的物质参加的反应,体系颜色不变,说明反应处于平衡状态。
(3)对于吸热或放热反应,绝热体系的温度不变,说明反应处于平衡状态。
注意化学反应速率与化学平衡的区别和联系:
化学反应速率v是表示在一定条件下,某一化学反应进行的快慢程度的物理量,它不仅涉及化学反应的
实际进行步骤,同时也与物质的微观状况有密切的联系。而化学平衡是指可逆反应进行的方向和限度的问题,
只考虑物质的宏观状况就可以解决问题,与反应的实际步骤无关,只与反应的初始状态和最终状态有关。两
者虽属于不同的范畴,但它们之间有联系:对于一个可逆反应,当v =v 时,即达到化学平衡;而当v ≠v
正 逆 正 逆
时,就表示该可逆反应未达到平衡或原平衡被破坏。
3.如图所示,隔板M和活塞N均可无摩擦地左右移动。向甲中充入1 mol N 和3 mol H ,向乙中充入4 mol
2 2
NH ,此时M、N的位置如图所示。在一定条件下发生可逆反应:N(g)+3H(g) 2NH (g),反应达到平衡
3 2 2 3后,恢复到反应发生前时的温度。下列有关说法不正确的是
A.当M、N不再移动时,甲、乙中的反应均达到平衡状态
B.平衡时,若M停在3处则N停在9处
C.平衡时,乙容器中NH 的物质的量是甲容器中NH 的物质的量的2倍
3 3
D.达到平衡后,再向甲中充入1 mol He,重新达到平衡时两容器中NH 的体积分数相等
3
【答案】D
易错点4 混淆平衡移动和转化率的关系
4.在一定条件下,体积不变的密闭容器中,发生可逆反应2SO (g)+O(g) 2SO (g) ΔH<0,达到平衡后,
2 2 3
当单独改变下列条件后,有关叙述正确的是
A.使用催化剂,此反应的ΔH仍保持不变
B.增大O 浓度,SO 的平衡转化率减小
2 2
C.降低温度,化学平衡常数减小
D.升高温度,SO 的转化率一定增大
2
【错因分析】改变温度时,反应物的转化率可根据平衡移动方向来判断,若正反应是吸热反应,升高温度,平
衡正向移动,则转化率是增大的,若正反应是放热反应,升高温度,平衡逆向移动,则转化率是减小的,本题中若不能根据反应的热效应判断温度升高时,化学平衡的移动方向,则易误选D项。
【试题解析】A项,使用催化剂不能改变反应的ΔH,A项正确;B项,增大O浓度,平衡正向移动,SO 的平衡转
2 2
化率增大,B错误;C项,降低温度,平衡正向移动,化学平衡常数增大,C错误;升高温度,平衡逆向移动,SO
2
的转化率一定减小,D错误。学&科网
【参考答案】A
若把化学平衡向正反应方向移动与原料转化率的提高等同起来,则会造成错误。化学平衡向正反应方向移动
时,反应物的转化率可能增大,也可能不变或减小。具体有以下两种情况:
(1)当可逆反应达平衡后,不增大反应物的浓度,而是通过改变温度、压强或减小生成物的浓度使平衡正向移
动,这时反应物的转化率一定增大。
(2)若不改变其他条件,只增大反应物的浓度,使平衡正向移动,则反应物的转化率不一定增大,必须根据具
体反应具体分析,如对于反应物是两种或两种以上的气体反应,当增大某一种气体反应物的浓度,平衡正向
移动,可使其他反应物的转化率增大,而自身的转化率是减小的。
4.PCl (g) PCl (g)+Cl (g) ①,2HI(g) H(g)+I (g) ②,2NO (g) NO(g) ③
5 3 2 2 2 2 2 4
在一定条件下,达到化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加
入一定量的各自的反应物,则转化率
A.均不变
B.均增大
C.①增大,②不变,③减小
D.①减小,②不变,③增大
【答案】D
易错点5 不会正确运用图像解化学平衡问题5.[2016四川]一定条件下,CH 与HO(g)发生反应:CH(g)+HO(g) CO(g)+3H(g),设起始 =Z,在
4 2 4 2 2
恒压下,平衡时CH 的体积分数 (CH)与Z和T(温度)的关系如图所示。下列说法正确的是
4 4
A.该反应的焓变ΔH>0
B.图中Z的大小为a>3>b
C.图中X点对应的平衡混合物中 =3
D.温度不变时,图中X点对应的平衡在加压后 (CH)减小
4
【错因分析】注意图中三条线分别是指不同的 时CH 的体积分数与温度的关系,本图除了表示温
4
度对平衡的影响外,还表示浓度对平衡的影响,解答本题需要先确定一个变量,讨论另一个变量与CH 的体
4
积分数的关系,否则将无从下手。
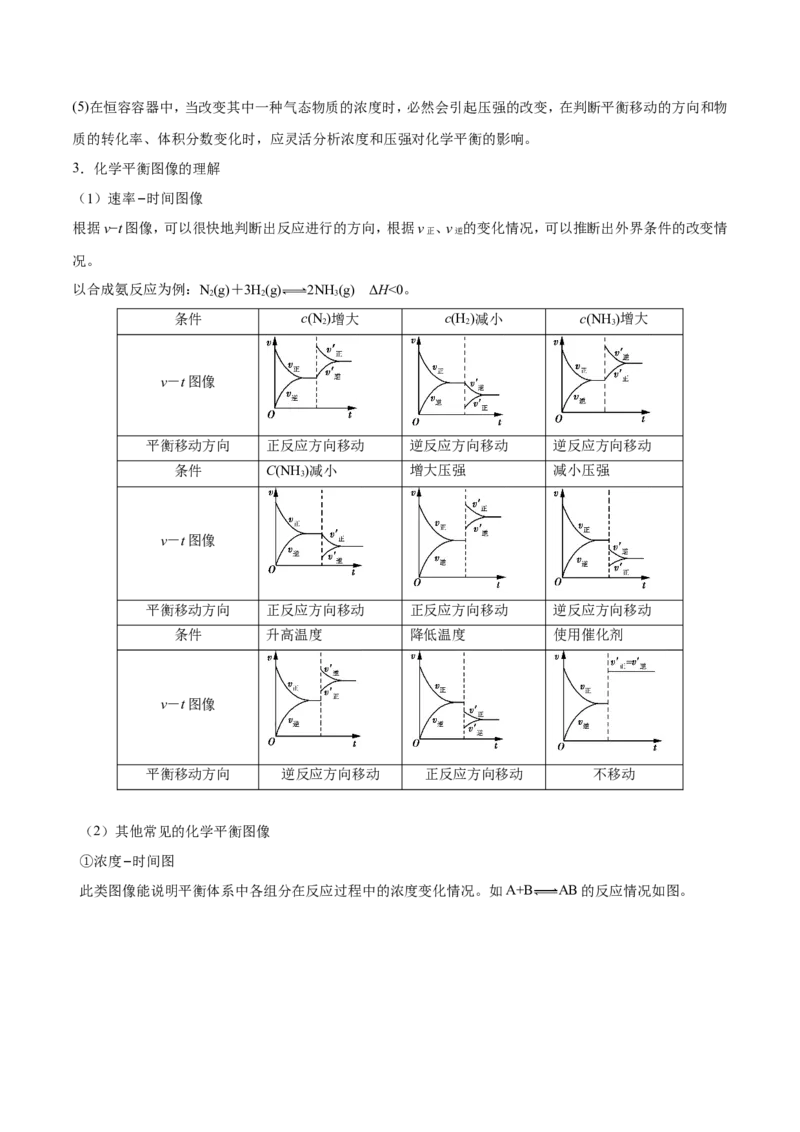
【参考答案】A化学平衡图像题的解题思路:
一、看懂图:横纵坐标的物理意义,图像的变化趋势,曲线的特殊点,如起点、交点、折点、终点;
二、想规律:外界条件对化学反应速率和化学平衡的影响规律;
三、作出正确的判断。注意“先拐先平”和“定一议二”方法的运用。
5.下列图示与对应叙述相符合的是
A.图I:反应H(g)+I (g) 2HI(g)达平衡后,升高温度时反应速率随时间的变化
2 2
B.图Ⅱ:反应2SO (g)+O(g) 2SO (g)达平衡后,缩小容器体积时各成分的物质的量随时间的变化
2 2 3
C.图III:反应N(g)+3H (g) 2NH (g)在恒温情况下,反应速率与压强的关系
2 2 3
D.图IV:反应CO(g)+H(g) CO(g)+HO(g) ΔH>0,水蒸气含量随时间的变化
2 2 2
【答案】B
易错点6 解化学平衡计算类试题方法错误
6.在373 K时,把0.5 mol NO 通入体积为5 L的真空密闭容器中,立即出现红棕色气体。反应进行到2 s时,
2 4NO 的浓度为0.02 mol·L-1。在60 s时,体系达到平衡状态,此时容器内的压强为开始时的1.6倍。下列说
2
法正确的是
A.前2 s以NO 的浓度变化表示的平均反应速率为0.01 mol·L-1·s-1
2 4
B.在2 s时体系内的压强为开始时的1.1倍
C.平衡时体系内含NO 0.25 mol
2 4
D.平衡时,NO 的转化率为40%
2 4
【错因分析】在运用三段式解答本题时一定要注意各量的单位要一致,若理不清平衡时与起始时量的关系,不
会运用题设条件“此时容器内的压强为开始时的1.6倍”,导致无法准确计算。学&科网
【试题解析】NO 和NO 之间存在如下转化关系:
2 4 2
NO(g) 2NO(g)
2 4 2
前2 s时
【参考答案】B化学平衡相关计算问题
化学平衡问题中常涉及到化学平衡常数、转化率的计算,通常利用“三段式”求解。所谓“三
段式”就是在化学方程式下面,表示出“起始状态”、“转化部分”、“平衡状态”各组分的浓度
或物质的量,进行列式求解。如下所示(a、b可指物质的量、浓度等):
mA(g)+nB(g) pC(g)+qD(g)
起始:a b 0 0
转化: mx nx px qx
平衡: a−mxb−nx px qx
6.某恒定温度下,在一个2 L的密闭容器中充入A气体,B气体,测得其浓度为2 mol/L和1 mol/L;且发生如
下反应:
3A(g)+2B(g) 4C(?)+2D(?)
已知“?”代表C、D状态未确定;反应一段时间后达到平衡,测得生成1.6 mol C,且反应前后压强比为
5∶4,则下列说法中正确的是
①该反应的化学平衡常数表达式为:K=
②此时B的转化率为35%
③增大该体系压强,平衡向右移动,但化学平衡常数不变
④增加C的量,A、B转化率不变
A.①② B.②③ C.①④ D.③④
【答案】D易错点7 不会灵活运用化学平衡常数
7.利用醋酸二氨合铜[Cu(NH )Ac]溶液吸收CO,能达到保护环境和能源再利用的目的,反应方程式为
3 2
Cu(NH )Ac+CO+NH [Cu(NH )]Ac·CO。已知该反应的化学平衡常数与温度的关系如表所示:
3 2 3 3 3
温度/℃ 15 50 100
化学平衡常数 5×104 2 1.9×10‒5
下列说法正确的是
A.上述正反应为吸热反应
B.15 ℃时,反应[Cu(NH )]Ac·CO Cu(NH )Ac+CO+NH 的平衡常数为0.5
3 3 3 2 3
C.保持其他条件不变,减小压强,CO的转化率减小
D.醋酸二氨合铜溶液的浓度大小对CO的吸收没有影响
【错因分析】若不能利用化学平衡常数与温度的关系分析反应的热效应,易错选A;若不明白逆反应的化学平
衡常数与正反应的化学平衡常数互为倒数,易错选B。【参考答案】C
有关化学平衡常数类试题解题技巧
1.考生要能正确书写出化学平衡常数。以可逆反应mA(g)+nB(g) pC(g)+qD(g)为例,K= 。要
注意三点:
(1)各物质的浓度必须是平衡浓度,固体、纯液体或水溶液中水的浓度不列入平衡常数的表达式。
(2)反应方向的改变或化学计量系数的增大或减小,平衡常数均发生改变。
(3)K不随反应物或生成物浓度的改变而改变,仅随温度的改变而改变,可通过温度变化后,K值的变化情况,
判断出反应放热或吸热,如反应N(g)+3H(g) 2NH (g),温度升高,平衡常数K减小,说明平衡向逆反
2 2 3
应方向移动,表明正反应放热。
2.考生要能正确应用化学平衡常数。
(1)推断反应进行的程度:一定温度下,K越大,反应进行的程度越大,反应物的转化率越大;反之,K越小,
表示反应进行的程度和反应物的转化率越小。
(2)判断反应是否达到化学平衡状态:一定温度下,若Q=K,说明化学反应达到平衡状态;若Q<K,说明反
c c
应向正反应方向进行;反之,则说明反应向逆反应方向进行。
7.在一定温度下,向2 L体积固定的密封容器中加入1 mol HI,发生反应:2HI(g) H(g)+I (g) ΔH>0,测
2 2
得H 的物质的量随时间变化如表,下列说法正确的是
2
t/min 1 2 3
n(H )/mol 0.06 0.1 0.1
2
A.2 min内的HI的分解速度为0.05 mol·L−1·min−1B.该温度下,反应的平衡常数K= ,平衡时HI的转化率为20%
C.该温度下的平衡常数为K ,温度升高10℃后平衡常数为K ,则K >K
1 2 1 2
D.达平衡后其他条件不变,压缩容器体积,平衡不移动,c(HI)不变
【答案】A
易错点8 不能区分“等效平衡”和“等同平衡”
8.在体积恒定的密闭容器Ⅰ中,充入3 mol A和1 mol B发生反应3A(g)+B(g) xC(g),维持温度不变,向与
容器Ⅰ体积相同的密闭容器Ⅱ中充入1.2 mol A、0.4 mol B、0.6 mol C,达到平衡后两容器中压强、C的
体积分数均相同,则x值是
A.1 B.2 C.3 D.4
【错因分析】若不能区分“等效平衡”和“等同平衡”易误选D,解题时宜抓住3个变量,即体积分数、物质
的量、浓度,若是“等同平衡”三者皆相同,若是“等效平衡”,则体积分数一定相同,物质的量、浓度可能会
同比例发生变化。【参考答案】A
等效平衡与等同平衡的异同
条件 等效条件 结果
恒温恒容:反应前后气体体积不相
投料换算成相同物质表示的物质 两次平衡时各组分百分含量、n、c
等的可逆反应,aA(g)+bB(g)
的量相同→回归定值 均相同→完全相同→等同平衡
cC(g)[Δn(g)≠0]
恒温恒容:反应前后气体体积相等
投料换算成相同物质表示的物质 两次平衡时各组分百分含量相同,
的可逆反应,aA(g)+bB(g)
的量等比例→回归定比 n、c同比例变化→等效平衡
cC(g)[Δn(g)=0]
恒温恒压:所有有气体参加的可逆 投料换算成相同物质表示的物质 两次平衡时各组分百分含量相同、
反应 的量等比例→回归定比 c相同,n同比例变化→等效平衡
8.在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得达到平衡时的有关数
据如下[已知X(g)+3Y(g) 2Z(g) ΔH=−Q kJ·mol−1]:
容器 甲 乙 丙
反应物投入量 1 mol X、3 mol Y 2 mol Z 4 mol Z
Z的浓度(mol·L−1) c c c
1 2 3
反应的能量变化 放出a kJ 吸收b kJ 吸收c kJ
体系压强(Pa) p p p
1 2 3
反应物转化率 α α α
1 2 3
下列说法正确的是
A.2c>c B.a+b=Q C.2p
v
正 逆 动
浓度
减小反应物的浓度 减小 不变 v 正 <v 逆 向逆反应方向移动
向逆反应方向移
增大生成物的浓度 不变 增大 v <v
正 逆 动
v >v 向正反应方向移
减小生成物的浓度 不变 减小 正 逆
动
增大压 向正反应方向移
增大 增大 v >v
强 正 逆 动
m+n>p+q
减小压 向逆反应方向移
减小 减小 v <v
强 正 逆 动
增大压 向逆反应方向移
压强(通过 增大 增大 v <v
强 正 逆 动
改变体积
m+nv 逆 动
增大压
增大 增大 v =v 平衡不移动
强 正 逆
m+n=p+q
减小
减小 减小 v =v 平衡不移动
压强 正 逆
容积不变充入He 不变 不变 v =v 平衡不移动
正 逆
向逆反应方向移
m+n>p+q 减小 减小 v <v
正 逆 动
压强不变
m+n=p+q 减小 减小 v =v 平衡不移动
充入He 正 逆
向正 反应方向
m+n<p+q 减小 减小 v >v
正 逆 移动
升高温 向逆反应方向移
增大 增大 v <v
度 正 逆 动
ΔH<0
降低温 向正反应方向移
减小 减小 v >v
度 正 逆 动
温度
升高温 向正反应方向移
增大 增大 v >v
ΔH>0 度 正 逆 动
降低 向逆反应方向移
减小 减小 v <v
温度 正 逆 动
使用正催化剂 增大 增大 v =v 平衡不移动
正 逆
催化剂
使用负催化剂 减小 减小 v =v 平衡不移动
正 逆
浓度、压强和温度对平衡移动影响的几种特殊情况:
(1)改变固体或纯液体的量,对平衡无影响。
(2)当反应混合物中不存在气态物质时,压强的改变对平衡无影响。
(3)对于反应前后气体体积无变化的反应,如H(g)+I(g) 2H(I g),压强的改变对平衡无影响。但增大(或
2 2
减小)压强会使各物质的浓度增大(或减小),混合气体的颜色变深(或浅)。
(4)恒容时,同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响,增大(减小)浓度相当于增大
(减小)压强。(5)在恒容容器中,当改变其中一种气态物质的浓度时,必然会引起压强的改变,在判断平衡移动的方向和物
质的转化率、体积分数变化时,应灵活分析浓度和压强对化学平衡的影响。
3.化学平衡图像的理解
(1)速率−时间图像
根据v−t图像,可以很快地判断出反应进行的方向,根据v 、v 的变化情况,可以推断出外界条件的改变情
正 逆
况。
以合成氨反应为例:N(g)+3H(g) 2NH (g) ΔH<0。
2 2 3
条件 c(N )增大 c(H )减小 c(NH )增大
2 2 3
v-t图像
平衡移动方向 正反应方向移动 逆反应方向移动 逆反应方向移动
条件 C(NH )减小 增大压强 减小压强
3
v-t图像
平衡移动方向 正反应方向移动 正反应方向移动 逆反应方向移动
条件 升高温度 降低温度 使用催化剂
v-t图像
平衡移动方向 逆反应方向移动 正反应方向移动 不移动
(2)其他常见的化学平衡图像
①浓度−时间图
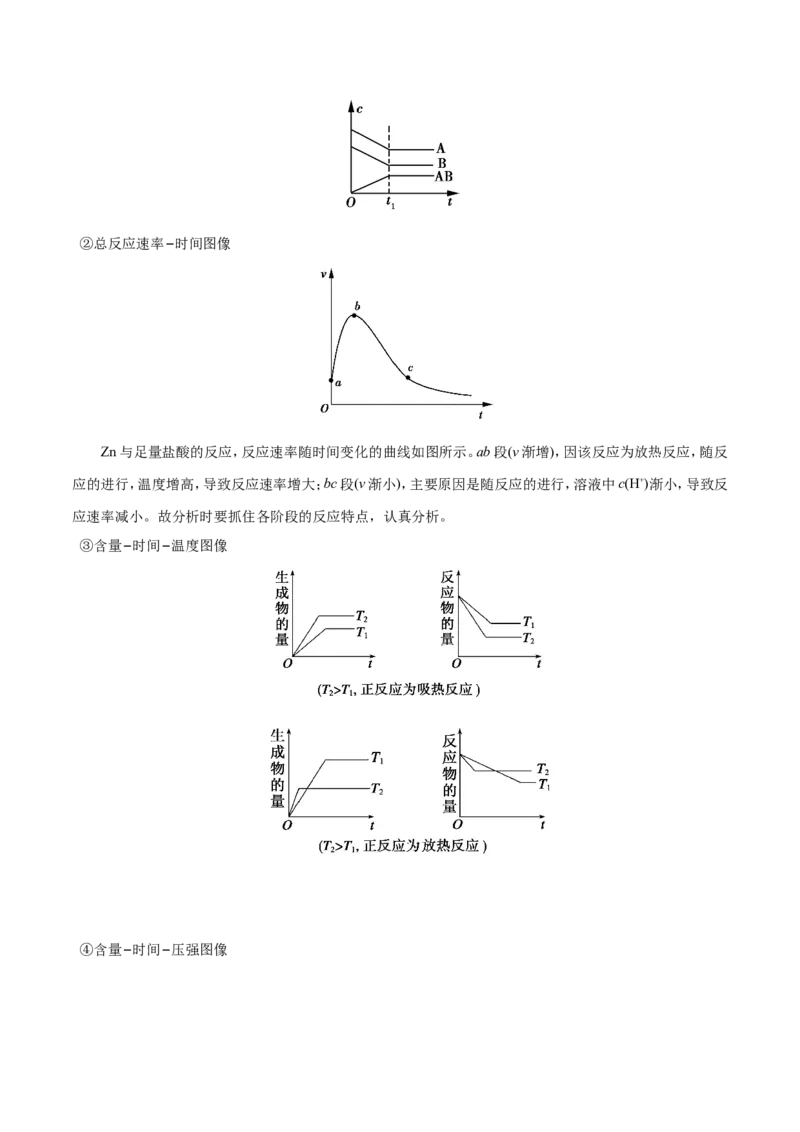
此类图像能说明平衡体系中各组分在反应过程中的浓度变化情况。如A+B AB的反应情况如图。②总反应速率−时间图像
Zn与足量盐酸的反应,反应速率随时间变化的曲线如图所示。ab段(v渐增),因该反应为放热反应,随反
应的进行,温度增高,导致反应速率增大;bc段(v渐小),主要原因是随反应的进行,溶液中c(H+)渐小,导致反
应速率减小。故分析时要抓住各阶段的反应特点,认真分析。
③含量−时间−温度图像
④含量−时间−压强图像⑤含量−时间−有无催化剂
4.化学平衡图像题解题技巧
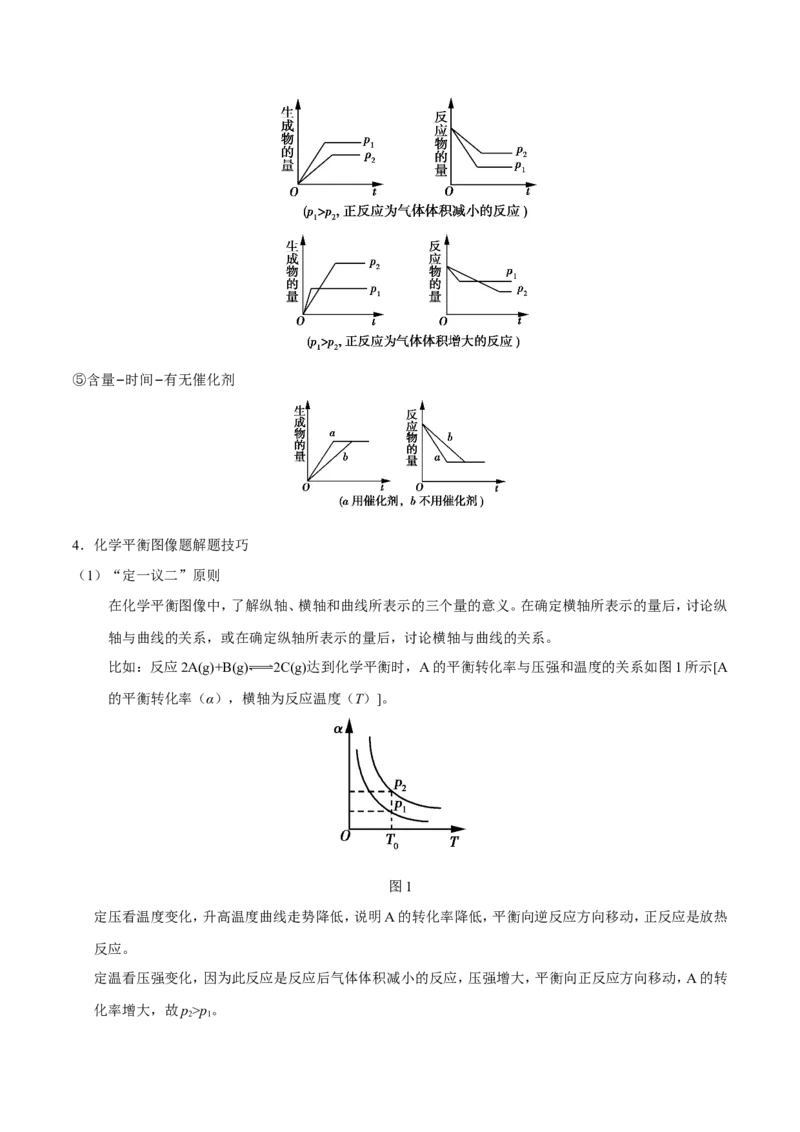
(1)“定一议二”原则
在化学平衡图像中,了解纵轴、横轴和曲线所表示的三个量的意义。在确定横轴所表示的量后,讨论纵
轴与曲线的关系,或在确定纵轴所表示的量后,讨论横轴与曲线的关系。
比如:反应2A(g)+B(g) 2C(g)达到化学平衡时,A的平衡转化率与压强和温度的关系如图1所示[A
的平衡转化率(α),横轴为反应温度(T)]。
图1
定压看温度变化,升高温度曲线走势降低,说明A的转化率降低,平衡向逆反应方向移动,正反应是放热
反应。
定温看压强变化,因为此反应是反应后气体体积减小的反应,压强增大,平衡向正反应方向移动,A的转
化率增大,故p>p。
2 1(2)“先拐先平数值大”原则
对于同一化学反应在化学平衡图像中,先出现拐点的反应先达到平衡状态,先出现拐点的曲线表示的温
度较高(如图2所示,α表示反应物的转化率)或压强较大[如图3所示,φ(A)表示反应物A的体积分数]。
图2 图3
图2:T>T,正反应放热。
2 1
图3:p T
2 正 逆 2 1
【答案】CD
A.根据容器II的起始投料,浓度商Q= = <K,平衡将向正反应方向移动,所以容器II在平衡时气
体的总物质的量一定大于1 mol,故达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比一定小于4∶5,A错误;B.若
cO
容器II在某时刻, 2 1,
cNO
2
由反应2NO 2NO + O
2 2
起始量(mol/L) 0.3 0.5 0.2
变化量(mol/L) 2x 2x x
平衡量(mol/L) 0.3−2x 0.5+2x 0.2+x【名师点睛】试题主要从浓度、温度对化学反应速率、化学平衡的影响以及平衡常数的计算等方面,考查学生
对化学反应速率、化学平衡等化学基本原理的理解和应用,关注信息获取、加工和处理能力的提高。解题时首
先要分析反应的特征,如是恒温恒容还是恒温恒压反应,是气体分子数目增加的还是气体分子数目减小的反
应,其次分析所建立的平衡状态的条件和平衡状态的特征,最后逐一分析试题中所设计的选项,判断是否正
确。本题只给了一个平衡量,通过化学平衡计算的三步分析法,分析容器I中平衡态的各种与4个选项相关的
数据,其他容器与I进行对比,通过浓度商分析反应的方向,即可判断。本题难度较大,如能用特殊值验证的
反证法,则可降低难度。学&科网
4.[2016江苏]一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H(g)+CO(g) CHOH(g) 达到
2 3
平衡。下列说法正确的是
A.该反应的正反应放热
B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C.达到平衡时,容器Ⅱ中c(H )大于容器Ⅲ中c(H )的两倍
2 2D.达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
【答案】AD
5.对于铁与盐酸生成氢气的反应,下列条件下反应速率最快的是
选项 铁的状态 盐酸的浓度 反应的温度
A 片状 1 mol·L-1 20 ℃
B 片状 3 mol·L-1 40 ℃
C 粉末 1 mol·L-1 20 ℃
D 粉末 3 mol·L-1 40 ℃
【答案】D
【解析】该反应中,温度越高、反应物接触面积越大、稀盐酸浓度越大,其反应速率越大,且温度对反应速率影
响大于浓度对反应速率影响,根据表中数据知,B、D温度高于A、C,所以B、D反应速率大于A、C,B中反应
物接触面积小于D,所以反应速率D>B;A中反应物接触面积小于C,所以反应速率C>A,通过以上分析知,
反应速率大小顺序是D>B>C>A,所以反应速率最快的是D。学&科网
6.某探究小组利用丙酮的溴代反应(CHCOCH +Br ――→CHCOCH Br+HBr)来研究反应物浓度与反应速
3 3 2 3 2
率的关系。反应速率v(Br)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下表实验数
2
据:
初始浓度(c)/mol·L-1 溴颜色消失
实验序号
CHCOCH HCl Br 所需时间(t)/s
3 3 2
① 0.80 0.20 0.001 0 290
② 1.60 0.20 0.001 0 145
③ 0.80 0.40 0.001 0 145
④ 0.80 0.20 0.002 0 580
分析表中实验数据得出的结论不正确的是A.增大c(CH
3
COCH
3
), v(Br
2
)增大
B.实验②和③的 v(Br
2
)相等
C.增大c(HCl), v(Br
2
)增大
D.增大c(Br
2
), v(Br
2
)增大
【答案】D
【解析】由①②两组数据可知,CHCOCH 的浓度增大,反应速率加快,溴颜色消失所用的时间缩短;由②③两
3 3
组数据可知,Br
2
的颜色消失时间相等,则 v(Br
2
)相等;而由①④两组数据可知,Br
2
的浓度与Br
2
的颜色消失时
间成倍数关系,所以 v(Br
2
)不变。学&科网
7.羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫的危害。在恒容密闭容器中,CO和HS混合加热生
2
成羰基硫的反应为 CO(g)+HS(g)===COS(g)+H(g)。下列说法能充分说明该反应已经达到化学平衡状
2 2
态的是
A.正、逆反应速率都等于零
B.CO、HS、COS、H 的浓度相等
2 2
C.CO、HS、COS、H 在容器中共存
2 2
D.CO、HS、COS、H 的浓度均不再变化
2 2
【答案】D
8.在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:
3A(g)+B(g) xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-
1,下列判断正确的是
A.平衡常数约为0.3
B.B的转化率为60%C.从反应开始至平衡,A的平均反应速率为0.3 mol·L-1·min-1
D.若混合气体的密度不变,则表明该反应达到平衡状态
【答案】C
【解析】平衡时D的浓度是0.8 mol÷2 L=0.4 mol·L-1,则x∶2=0.2 mol·L-1∶0.4 mol·L-1,故x=1。
3A(g)+B(g) C(g)+2D(g)
起始浓度(mol·L-1) 1.5 0.5 0 0
平衡浓度(mol·L-1) 0.9 0.3 0.2 0.4
将平衡时各物质的浓度代入平衡常数表达式,计算得K约为0.15,选项A错误;B的转化率是0.2 mol·L−1÷0.5
mol·L-1×100%=40%,选项B错误;从反应开始至平衡,A的平均反应速率是0.6 mol·L-1÷2 min=0.3 mol·L
-1·min-1,选项C正确;各物质均是气体,总质量不变,且容器体积一定,故无论反应是否达到平衡,混合气体
的密度都是定值,选项D错误。学&科网
9.如图表示恒容密闭器中,反应X(g) 4Y(g)+Z(g) ΔH<0在某温度时X的浓度随时间的变化曲线:
下列有关该反应的描述正确的是
A.8 min时,反应停止
B.X的平衡转化率为85%
C.若升高温度,X的平衡转化率将大于85%
D.若降低温度,
v正
和
v逆
将以同样程度减少
【答案】B
10.[2017新课标Ⅰ]近期发现,HS是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信
2
号传递、舒张血管减轻高血压的功能。回答下列问题:(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是_________(填标号)。
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
B.氢硫酸的导电能力低于相同浓度的亚硫酸
C.0.10 mol·L−1的氢硫酸和亚硫酸的pH分别为4.5和2.1
D.氢硫酸的还原性强于亚硫酸
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。
通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为________________、______________,
制得等量H 所需能量较少的是_____________。
2
(3)HS与CO 在高温下发生反应:HS(g)+CO(g) COS(g) +H O(g)。在610 K时,将0.10 mol CO 与
2 2 2 2 2 2
0.40 mol HS充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
2
①HS的平衡转化率 =_______%,反应平衡常数K=________。
2
②在620 K重复试验,平衡后水的物质的量分数为 0.03,HS的转化率 _____ ,该反应的
2
H_____0。(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使HS转化率增大的是________(填标号)
2
A.HS B.CO C.COS D.N
2 2 2
【答案】(1)D
(2)HO(l)=H(g)+ O(g) ΔH=+286 kJ/mol HS(g)=H(g)+S(s) ΔH=+20 kJ/mol 系统(II)
2 2 2 2 2
(3)①2.5 2.8×10–3 ②> > ③B(3)① HS(g) + CO (g) COS(g)+ H O(g)
2 2 2
开始 0.40mol 0.10mol 0 0
反应 x x x x
平衡 (0.40–x)mol (0.10–x)mol x x
解得x=0.01mol,所以HS的转化率是
2
由于该反应是反应前后气体体积相等的反应,所以在该条件下反应达到平衡时化学平衡常数;学&科网
②根据题目提供的数据可知温度由610K升高到620K时,化学反应达到平衡,水的物质的量分数由0.02变
为0.03,所以HS的转化率增大。α>α;根据题意可知:升高温度,化学平衡向正反应方向移动,根据平衡移
2 2 1
动原理:升高温度,化学平衡向吸热反应方向移动,所以该反应的正反应为吸热反应,故△H>0;③A.增大
HS的浓度,平衡正向移动,但加入量远远大于平衡移动转化消耗量,所以HS转化率降低,A错误;B.增大
2 2
CO 的浓度,平衡正向移动,使更多的HS反应,所以HS转化率增大,B正确;C.COS是生成物,增大生成
2 2 2
物的浓度,平衡逆向移动,HS转化率降低,C错误;D.N 是与反应体系无关的气体,充入N,不能使化学平
2 2 2
衡发生移动,所以对HS转化率无影响,D错误。答案选B。学&科网
2
【名师点睛】本题是化学反应原理的综合考查,易错点是压强对平衡状态的影响,尤其是惰性气体的影响,
“惰性气体”对化学平衡的影响:①恒温、恒容条件:原平衡体系 体系总压强增大→体系中各组
分的浓度不变→平衡不移动。②恒温、恒压条件:原平衡体系 容器容积增大,各反应气体的分压减
小→体系中各组分的浓度同倍数减小(等效于减压),平衡向气体体积增大的方向移动。
11.[2016海南]顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如下转化:
INCLUDEPICTURE "F:\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\
\AN97%S3A)LWTI351UKOB){X.png" \* MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\
\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\AN97%S3A)LWTI351UKOB){X.png" \*
MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\
\WinTemp\\RichOle\\AN97%S3A)LWTI351UKOB){X.png" \* MERGEFORMATINET INCLUDEPICTURE
"F:\\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\AN97%S3A)LWTI351UKOB)
{X.png" \* MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\\Roaming\\Tencent\\Users\\54151154\
\QQ\\WinTemp\\RichOle\\AN97%S3A)LWTI351UKOB){X.png" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\
\AN97%S3A)LWTI351UKOB){X.png" \* MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\
\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\AN97%S3A)LWTI351UKOB){X.png" \*
MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\
\WinTemp\\RichOle\\AN97%S3A)LWTI351UKOB){X.png" \* MERGEFORMATINET INCLUDEPICTURE
"F:\\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\AN97%S3A)LWTI351UKOB)
{X.png" \* MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\AN97%S3A)LWTI351UKOB){X.png" \* MERGEFORMATINET
该反应的速率方程可表示为:v(正)=k(正)c(顺)和v(逆)=k(逆)c(反),k(正)和k(逆)在一定温度时为常数,分
别称作正、逆反应速率常数。回答下列问题:
(1)已知:t 温度下,k(正)=0.006s-1,k(逆)=0.002s-1,该温度下反应的平衡常数值K =_____;该反应的活
1 1
化能E(正)小于E(逆),则 ________0(填“小于”“等于”或“大于”)。
a a
(2)t 温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是_______(填曲线编号),平衡常数
2
值 K =_____ ; 温 度 t___t( 填 “ 小 于 ” “ 等 于 ” 或 “ 大 于 ” ) , 判 断 理 由 是
2 2 1
_______________________。
INCLUDEPICTURE "F:\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\VC]
(L(6[85RS]WLTGLOEVJD.png" \* MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\\Roaming\
\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\VC](L(6[85RS]WLTGLOEVJD.png" \*
MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\
\WinTemp\\RichOle\\VC](L(6[85RS]WLTGLOEVJD.png" \* MERGEFORMATINET INCLUDEPICTURE "F:\
\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\VC]
(L(6[85RS]WLTGLOEVJD.png" \* MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\\Roaming\
\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\VC](L(6[85RS]WLTGLOEVJD.png" \*
MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\
\WinTemp\\RichOle\\VC](L(6[85RS]WLTGLOEVJD.png" \* MERGEFORMATINET INCLUDEPICTURE "F:\
\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\VC]
(L(6[85RS]WLTGLOEVJD.png" \* MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\\Roaming\
\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\VC](L(6[85RS]WLTGLOEVJD.png" \*
MERGEFORMATINET INCLUDEPICTURE "F:\\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\
\WinTemp\\RichOle\\VC](L(6[85RS]WLTGLOEVJD.png" \* MERGEFORMATINET INCLUDEPICTURE "F:\
\..\\AppData\\Roaming\\Tencent\\Users\\54151154\\QQ\\WinTemp\\RichOle\\VC](L(6[85RS]WLTGLOEVJD.png" \* MERGEFORMATINET
【答案】(1)3 小于
(2)B 7/3 大于 放热反应升高温度时平衡向逆反应方向移动
为0.7x,所以平衡常数值K =0.7x÷0.3x=7/3,因为K >K ,放热反应升高温度时平衡向逆反应方向移动, 所以
2 1 2
温度t 大于t。学&科网
2 1
12.[2016新课标Ⅱ]丙烯腈(CH=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要
2
副产物有丙烯醛(CH=CHCHO)和乙腈(CHCN)等,回答下列问题:
2 3
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C HN)和副产物丙烯醛(C HO)的热化学方
3 3 3 4
程式如下:
①C H(g)+NH (g)+ O(g)=C HN(g)+3H O(g) ΔH=-515 kJ/mol
3 6 3 2 3 3 2
②C H(g)+O(g)=C HO(g)+H O(g) ΔH=-353 kJ/mol
3 6 2 3 4 2
两个反应在热力学上趋势均很大,其原因是________;有利于提高丙烯腈平衡产率的反应条件是
________;提高丙烯腈反应选择性的关键因素是________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产
率________(填“是”或者“不是”)对应温度下的平衡产率,判断理由是________;高于460℃时,
丙烯腈产率降低的可能原因是________(双选,填标号)
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D.反应活化能增大INCLUDEPICTURE "http://182.92.3.219/Uploads/word/2016/0711/57833467a963b482763.files/
image020.jpg" \* MERGEFORMATINET INCLUDEPICTURE
"http://182.92.3.219/Uploads/word/2016/0711/57833467a963b482763.files/image020.jpg" \*
MERGEFORMATINET
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为
__________,理由是_______________。进料气氨、空气、丙烯的理论体积比约为________。
【答案】(1)两个反应均为放热量大的反应 降低温度、降低压强 催化剂
(2)不是 该反应为放热反应,平衡产率应随温度升高而降低 AC
(3)1 该比例下丙烯腈产率最高,而副产物丙烯醛产率最低 1:7.5:1 学&科网
【名师点睛】本题考查影响化学平衡的因素,化学图像的分析与判断,化学计算等知识。该题是对化学平衡的
集中考查,涉及的知识点不多,解题的关键点是看懂图像的含义,看图像时:①一看面:纵坐标与横坐标的意
义;②二看线:线的走向和变化趋势;③三看点:起点,拐点,终点,然后根据图象中呈现的关系、题给信息和
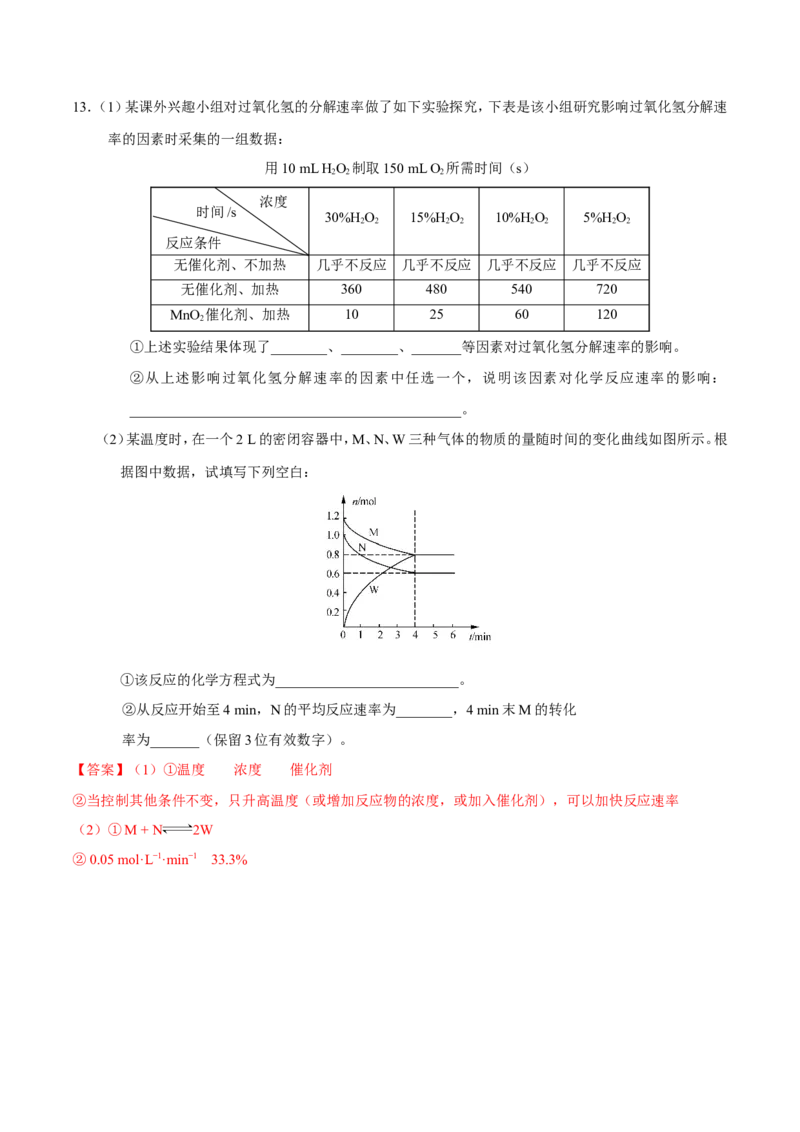
所学知识相结合,做出符合题目要求的解答。学&科网13.(1)某课外兴趣小组对过氧化氢的分解速率做了如下实验探究,下表是该小组研究影响过氧化氢分解速
率的因素时采集的一组数据:
用10 mL H O 制取150 mL O 所需时间(s)
2 2 2
浓度
时间/s
30%H O 15%H O 10%H O 5%H O
2 2 2 2 2 2 2 2
反应条件
无催化剂、不加热 几乎不反应 几乎不反应 几乎不反应 几乎不反应
无催化剂、加热 360 480 540 720
MnO 催化剂、加热 10 25 60 120
2
①上述实验结果体现了________、________、_______等因素对过氧化氢分解速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率的影响:
_______________________________________________。
(2)某温度时,在一个2 L的密闭容器中,M、N、W三种气体的物质的量随时间的变化曲线如图所示。根
据图中数据,试填写下列空白:
①该反应的化学方程式为__________________________。
②从反应开始至4 min,N的平均反应速率为________,4 min末M的转化
率为_______(保留3位有效数字)。
【答案】(1)①温度 浓度 催化剂
②当控制其他条件不变,只升高温度(或增加反应物的浓度,或加入催化剂),可以加快反应速率
(2)①M + N 2W
②0.05 mol·L−1·min−1 33.3%14.生产、生活中产生的废水、废气是环境污染的重要源头。在环境治理方面人们可利用IO和NaSO 等化
2 5 2 3
工产品实现对废水和废气的治理。
(1)利用IO的氧化性处理废气HS,得到S、I两种单质,发生反应的化学方程式为________________。
2 5 2 2
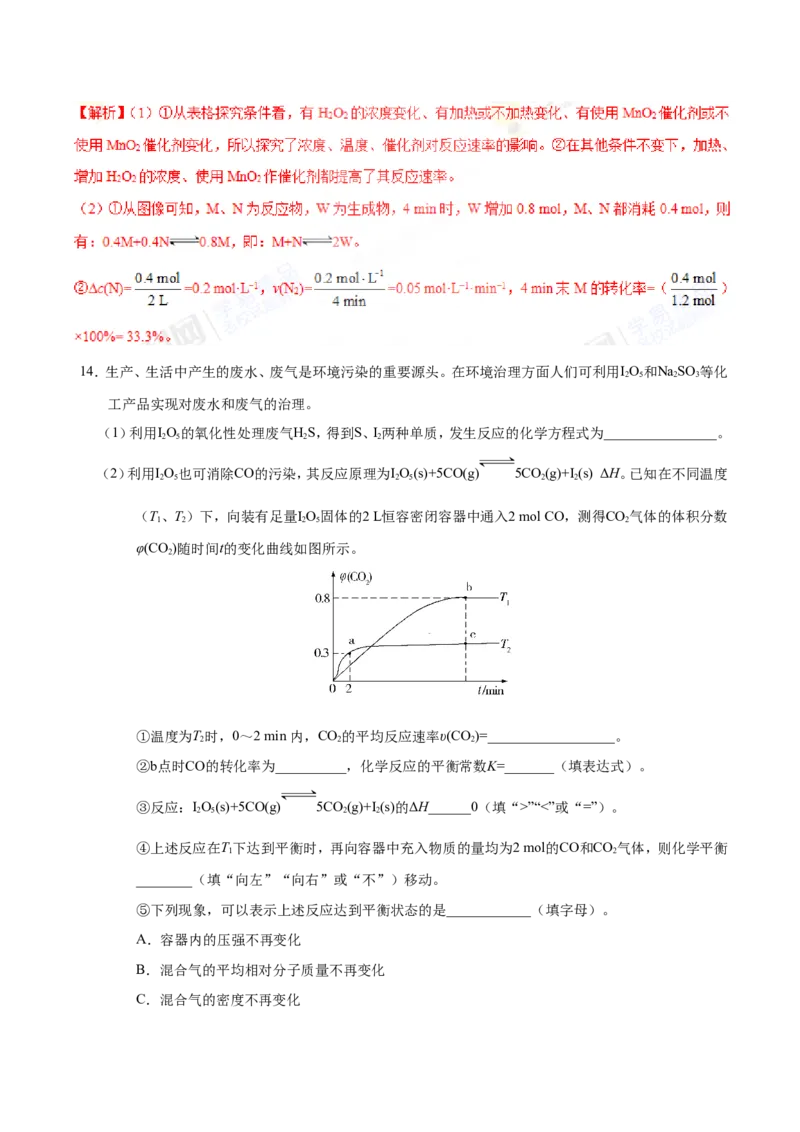
(2)利用IO也可消除CO的污染,其反应原理为IO(s)+5CO(g) 5CO(g)+I (s) ΔH。已知在不同温度
2 5 2 5 2 2
(T、T)下,向装有足量IO固体的2 L恒容密闭容器中通入2 mol CO,测得CO气体的体积分数
1 2 2 5 2
φ(CO)随时间t的变化曲线如图所示。
2
①温度为T时,0~2 min 内,CO的平均反应速率υ(CO)=__________________。
2 2 2
②b点时CO的转化率为__________,化学反应的平衡常数K=_______(填表达式)。
③反应:IO(s)+5CO(g) 5CO(g)+I (s)的ΔH______0(填“>”“<”或“=”)。
2 5 2 2
④上述反应在T下达到平衡时,再向容器中充入物质的量均为2 mol的CO和CO气体,则化学平衡
1 2
________(填“向左”“向右”或“不”)移动。
⑤下列现象,可以表示上述反应达到平衡状态的是____________(填字母)。
A.容器内的压强不再变化
B.混合气的平均相对分子质量不再变化
C.混合气的密度不再变化D.单位时间内消耗CO和生成CO的物质的量之比为1∶1
2
【答案】(1)IO+5H S I+5S+5H O
2 5 2 2 2
(2)①0.15 mol·L−1·min−1 ②80% ③<
④向右 ⑤BC
均相对分子质量 = ,在反应过程中混合气的质量发生变化,物质的量不变,所以容器内混合气的平均
相对分子质量不变,则说明达到平衡,B项正确。混合气体的密度ρ= ,在反应过程中混合气的质量发生变化,
故密度不变可作为达到平衡的标志,C项正确。根据化学方程式知,单位时间内消耗CO和生成CO的物质的
2量之比为1∶1恒成立,D项错误。学&科网
15.甲醇是基本有机化工原料。工业上可以通过反应CO(g)+2H(g) CHOH(g) ΔH<0制备甲醇。
2 3
(1)某温度下,向容积为1 L的密闭容器中充入1 mol CO和2 mol H ,加入适当的催化剂,用压力计测定
2
容器内的压强数据如下表所示:
反应时间/min 0 5 10 15 20 25
压强/MPa 25.2 21.6 19.0 17.4 16.8 16.8
①从反应开始到20 min时用CO表示的化学反应速率为_________________。
②该温度下反应的压强平衡常数K =_________________。
p
③试写出既能增大反应速率又能增大氢气转化率的措施:____________________________(回答
一条即可)。
(2)甲醇的燃烧热为a kJ·mol−1,试写出表示甲醇燃烧热的热化学方程式:_______________;3.2 g甲醇
完全燃烧后的产物通入到150 mL 1 mol·L−1的KOH溶液中,充分反应后所得溶液中离子浓度的大
小顺序为_________________。
(3)甲醇可以被氧化为甲酸,25℃时将100 mL浓度为b mol·L−1的甲酸与100 mL 1 mol·L−1的氢氧化钠
溶液混合充分反应后,所得溶液中c(Na+)=c(HCOO−),则所得溶液呈________(填“酸性”“中
性”或“碱性”),用b表示该温度下甲酸的电离常数K=_________________。
a
【答案】(1)①0.025 mol/(L·min) ②(8.4 MPa)−2 ③向容器中通入CO(或压缩容器等)
3
(2)CHOH(l)+ O(g) CO(g)+2HO(l) ΔH=−a kJ·mol−1
3 2 2 2 2
c(K+)>c(HCO )>c(CO2 )>c(OH−)>c(H+)学&科网
3 3
1107
(3)中性
b1________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
勒夏特列
法国化学家,1850年10月8日勒夏特列出生于巴黎的一个化学世家,他从小就受到化学的熏陶。1875
年,勒夏特列以优异的成绩毕业于巴黎工业大学,对热学的研究很自然的将他引导到热力学的领域中去,这
使他得以在1888年宣布了一条闻名遐迩的定律,那就是勒夏特列原理。此外,他对乙炔气也颇有研究,发明
的氧炔焰发生器,至今还用于金属的切割和焊接。