文档内容
专题 07 非金属及其化合物
1.下列能使湿润的淀粉碘化钾变蓝的是( )
A.SO B.HCl C.KBr D.Cl
2 2
2.(2022·浙江省金丽衢十二校、七彩联盟高三阶段性联考)下列说法不正确的是( )
A.氢氧化铝胶体可用于水体的净化与消毒 B.石膏可用于生产硫酸
C.二氧化硫可用于漂白纸浆或草帽 D.催化剂可降低反应温度
3.(2022·浙江省金丽衢十二校、七彩联盟高三阶段性联考)下列关于硅及其化合物的说法不正确的是
( )
A.高温下石英坩埚会被烧碱腐蚀 B.玻璃、陶瓷和水泥都是传统硅酸盐材料
C.硅元素是构成岩石的核心元素 D.光导纤维可实现光-电转换
4.(2022·浙江省宁波“十校”高三下学期联考)下列说法正确的是( )
A.氯气可用于自来水的消毒,因为氯气具有强氧化性
B.分子筛常用于分离、提纯气体或液体混合物
C.溴化银是一种重要的感光材料,可用于人工降雨
D.乙二醇的水溶液凝固点高,故可用作汽车发动机的抗冻剂
5. (2022•浙江省百强校高三联考)下列说法不正确的是( )
A.新制氯水中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
B.硫在过量的空气中燃烧生成二氧化硫
C.氨气与氯气反应可生成氯化铵和氮气
D.硅酸盐分子筛可以可逆地吸收水及其他小分子
6. (2022•浙江省新高考Z20联盟高三联考)下列说法不正确的是( )
A.工业上用氯气和澄清石灰水反应制备漂白粉
B.钠可用于从熔融锆、铌的金属氯化物中置换出金属单质
C.刚玉的主要成分是α-氧化铝,硬度仅次于金刚石
D.硅酸盐中有许多笼状空穴和通道,很容易可逆地吸收水及其他小分子
7. (2022•浙江省名校协作体高三联考)下列说法正确的是( )
A.大量SO 排放到空气中,不但能形成酸雨,还易产生光化学烟雾危害环境
2
B.纯碱是烘焙糕点的发酵粉的主要成分,医疗上是治疗胃酸过多的药剂C.“天宫二号”空间实验室的太阳能电池板主要材料是二氧化硅
D.铁的化合物应用广泛,FeCl 、FeSO 常用作净水剂
3 4
8.(2022·浙江省百校高三选考模拟检测)下列说法不正确的是( )
A.在通常情况下,碘单质是紫黑色固体、易升华
B.铝及其合金是目前产量最大,使用最广泛的金属
C.高纯硅可以制成计算机.通信设备和家用电器等的芯片,以及光伏电站、人造卫星和电动汽车等的硅太
阳能电池
D.液氨汽化时吸收大量的热而使周围温度急剧下降,因此可用作制冷剂
9.(2022·浙江省百校高三选考模拟检测)下列物质与其主要成分的化学式或者说法对应正确的是( )
A.侯氏制碱法得到的物质是碱式盐——碳酸钠
B.水玻璃很稳定,长期暴露在空气中也不变质
C.丹霞地貌的岩层因含Fe O 而呈红色
2 3
D.卤素主要单质有F、Cl、Br、I 等,都能与氢氧化钠溶液发生歧化反应
2 2 2 2
10.(2022·浙江省浙南名校高三联考)下列说法正确的是( )
A.二氧化硅有很好的导电性,可用于制造光导纤维
B.侯氏制碱法的原理是将氨通入二氧化碳的氯化钠饱和溶液中,使碳酸钠从溶液中析出
C.生铁含碳2%-4.5%,将生铁进一步炼制,就可以得到用途更广泛的钢(含碳0.03%-2%)
D.工业上以海带为原料制碘时,利用CCl 萃取碘水中的碘,分液、蒸馏获得粗碘
4
11.(2022•浙江省“七彩阳光”新高考研究联盟高三联考)下列说法正确的是( )
A.SiO 是酸性氧化物,能溶于氢氟酸
2
B.铜粉与硫粉加热反应可生成硫化铜
C.SO 和Cl 都能使品红溶液褪色,褪色原理相同
2 2
D.常温下浓硝酸和铁不发生反应,加热时可发生反应
12.(2022•浙江省9 +1高中联盟高三联考)下列说法不正确的是( )
A.浓硝酸、浓硫酸可贮存在铁制容器中,也可用铝槽车运输
B.硫单质通常用S表示,说明硫元素不存在同素异形体
C.硅酸钠的水溶液俗称水玻璃,可用作粘合剂和防火材料
D.人体中极少量的NO会促进血管扩张,防止血管栓塞
13.(2022·浙江省高三下学期高考选考科目联考)下列说法正确的是( )
A.普通硅酸盐水泥以黏土和石灰石为主要原料,还需加入适量石膏以调节水泥凝结时间
B.纯铝导电性好,强度高,硬度大,广泛用于生产门窗、飞机、电子元件等
C.硫黄、胆矾都可用于生产硫酸,石膏、重晶石则不用于生产硫酸D.工业制备硝酸时在吸收塔中使用浓硝酸吸收二氧化氮
14.过二硫酸本身用途并不大,其盐在工业上用途广泛。过二硫酸(H SO)可以看成HO 中的两个氢原子
2 2 8 2 2
被两个磺酸基(-SO H)取代的产物。下列说法不正确的是( )
3
A.HSO 中硫的化合价为+6价
2 2 8
B.过二硫酸与高锰酸钾溶液反应可产生氧气
C.将过二硫酸加入滴有紫色石蕊试液的水中,溶液显红色
D.工业电解硫酸氢钾溶液可得过二硫酸钾,阳极的电极反应式为2SO 2-−2e-=S O2-
4 2 8
15.硫酸亚铁铵隔绝空气加热到500℃发生的反应为2(NH )Fe(SO )
4 2 4 2
Fe O+2NH↑+N ↑+4X↑+5H O,则下列说法错误的是( )
2 3 3 2 2
A.X是SO
2
B.该反应的氧化产物为Fe O 和N
2 3 2
C.分别氧化铁元素、氮元素的硫酸根物质的量之比为1:6
D.每生成1 mol N 转移8 mol电子
2
16.(2022·浙江省台州市高三下学期4月教学质量评估二模)下列推测不合理的是( )
A.硫磺和SO 在一定条件下可以合成SO
2 2
B.NH Cl能与水反应生成一种弱酸
2
C.相同条件下,CHCl 比SiHCl 更容易与O 反应
2 2 2 2 2
D.FeO 投入足量稀硫酸中有气体生成
2
17.在给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
A.粗硅――→SiCl ――→Si B.Mg(OH) ――→MgCl (aq)――→Mg
4 2 2
C.Fe O――→FeCl (aq)――→无水FeCl D.S――→SO ――→HSO
2 3 3 3 3 2 4
18.下表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )
选项 X Y Z 箭头上所标数字的反应条件
A SiO NaSiO HSiO ①NaCO 熔融
2 2 3 2 3 2 3
B NaCl NaHCO NaCO ②加热
3 2 3
C N NO HNO ③加热
2 2 3
D C CO CO ④灼热炭粉
2
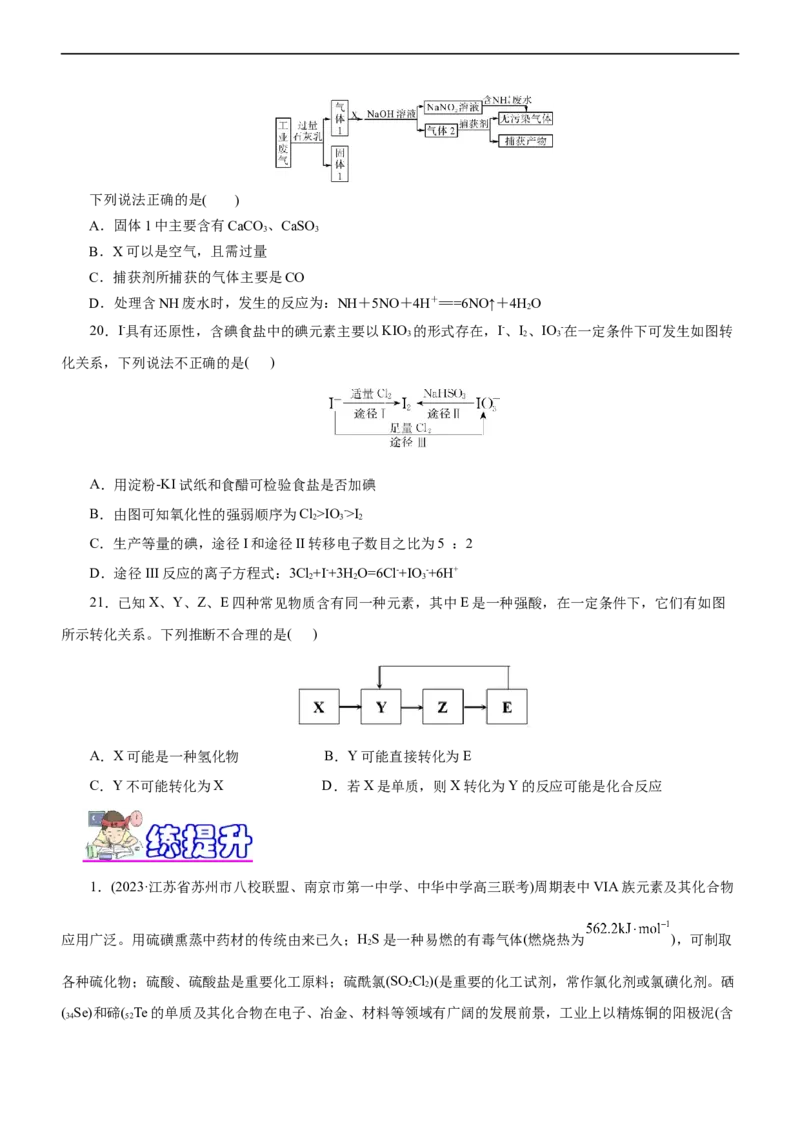
19.绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含NH废水和工业废气(主要
含N、CO、SO 、NO、CO,不考虑其他成分),设计了如下流程:
2 2 2下列说法正确的是( )
A.固体1中主要含有CaCO 、CaSO
3 3
B.X可以是空气,且需过量
C.捕获剂所捕获的气体主要是CO
D.处理含NH废水时,发生的反应为:NH+5NO+4H+===6NO↑+4HO
2
20.I-具有还原性,含碘食盐中的碘元素主要以KIO 的形式存在,I-、I、IO -在一定条件下可发生如图转
3 2 3
化关系,下列说法不正确的是( )
A.用淀粉-KI试纸和食醋可检验食盐是否加碘
B.由图可知氧化性的强弱顺序为Cl>IO ->I
2 3 2
C.生产等量的碘,途径I和途径II转移电子数目之比为5 :2
D.途径III反应的离子方程式:3Cl+I-+3H O=6Cl-+IO -+6H+
2 2 3
21.已知X、Y、Z、E四种常见物质含有同一种元素,其中E是一种强酸,在一定条件下,它们有如图
所示转化关系。下列推断不合理的是( )
A.X可能是一种氢化物 B.Y可能直接转化为E
C.Y不可能转化为X D.若X是单质,则X转化为Y的反应可能是化合反应
1.(2023·江苏省苏州市八校联盟、南京市第一中学、中华中学高三联考)周期表中VIA族元素及其化合物
应用广泛。用硫磺熏蒸中药材的传统由来已久;HS是一种易燃的有毒气体(燃烧热为 ),可制取
2
各种硫化物;硫酸、硫酸盐是重要化工原料;硫酰氯(SO Cl)(是重要的化工试剂,常作氯化剂或氯磺化剂。硒
2 2
( Se)和碲( Te的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以精炼铜的阳极泥(含
34 52CuSe)为原料回收 ,以电解强碱性NaTeO 溶液制备Te。下列化学反应表示正确的是( )
2 3
A.HS的燃烧:2HS(g)+ 3O (g)=2SO(g)+ 2H O(g) ΔH=-1124.4 kJ·mol-1
2 2 2 2 2
B.SO Cl 遇水强烈水解生成两种强酸:SO Cl+2H O=4H++SO 2-+2Cl-
2 2 2 2 2 3
C.电解强碱性NaTeO 溶液的阴极反应:TeO -+4e-+3H O=Te+6OH-
2 3 3 2
D.CuSe和浓硝酸反应:CuSe+2HNO =Cu(NO)+H Se↑
3 3 2 2
2.(2023·重庆市万州第二高级中学高三检测) 排放到空气中会引起酸雨等环境问题,严重危害人类健
康。SO 的水溶液中存在下列平衡:
2
已知:K、K、K 为各步反应的平衡常数,且 [ 表示SO 的平衡压强]。下列说
1 2 3 2
法正确的是( )
A.由图平衡可知NaSO 溶液和NaHSO 溶液都可以水解,溶液一定呈碱性
2 3 3
B.氨水也可吸收SO ,防止大气污染,同时通入O 能进一步提高SO 去除率
2 2 2
C.当 的平衡压强为p时,测得c(SO 2-) =a mol/L,则溶液
3
D.用 的 溶液吸收0.2mol的SO ,则溶液中存在关系式: c(Na+) =3c(H+) +
2
3c((HSO -) + 6c(SO ·xH O) -3c(OH-)
3 2 2
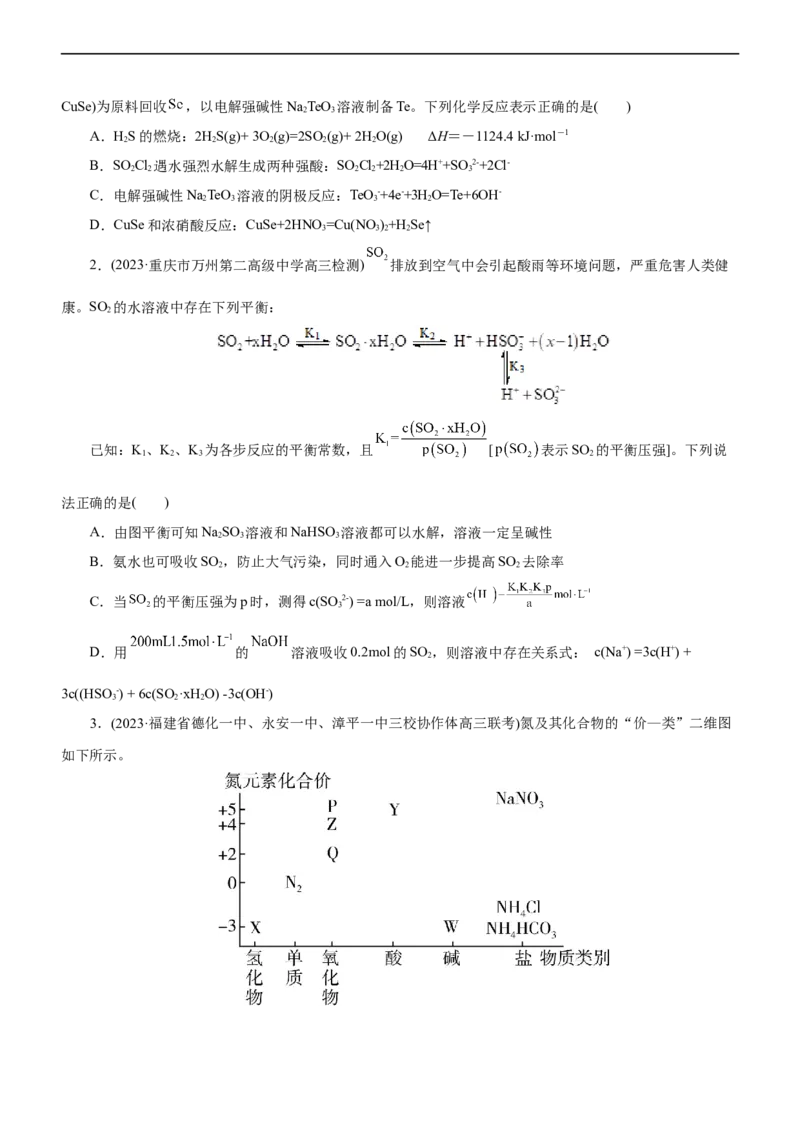
3.(2023·福建省德化一中、永安一中、漳平一中三校协作体高三联考)氮及其化合物的“价—类”二维图
如下所示。下列说法正确的是( )
A.X可通过加热氯化铵固体制取
B.从物质类别角度分析,P和Z都属于酸性氧化物
C.将X转化为Q的过程,属于氮的固定
D.浓的Y溶液保存在棕色试剂瓶中,并置于冷暗处
4.(2023·重庆市拔尖强基联合高三定时检测)某实验小组探究NiO能否催化NO和CO反应生成无毒物质。
已知:①Ni、Fe的氢氧化物化学性质相似;②2NO(g)+ 2CO(g) N (g)+2CO(g) ΔH<0 。现采用如下
2 2
两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是( )
A.从理论上推断,NO(g)与CO(g)生成N (g)和CO (g)的反应,高温有利于自发进行
2 2
B.在空气中加热Ni(OH) 可制备NiO
2
C.打开装置1中气球,通过观察气体是否变为红棕色判断是否生成N
2
D.若以上实验证明NiO能够成功催化该反应,且固体A是Ni O,则装置2中的反应方程式为:
2 3
Ni O+CO 2NiO+CO
2 3 2
5.(2022·江西省赣州市十六县市高三期中联考)中学常见的某反应的化学方程式为a+b→c+d+H O(未配平,
2
条件略去)。下列叙述不正确的是( )
A.若a是铁,b是稀硝酸(过量),且a可溶于c溶液中。则a与b反应的离子方程式为Fe+4H++NO-=Fe3+
3
+NO↑+2HO
2
B.若c、d均为气体,且都能使澄清石灰水变浑浊,则将混合气体通入溴水中,橙色褪去,其褪色过程的
离子方程式为SO +Br +2H O=4H++SO2-+2Br-
2 2 2 4
C.若a是造成温室效应的主要气体之一,c、d均为钠盐,参加反应的a、b物质的量之比为4:5,则上
述反应的离子方程式为4CO+5OH-=CO 2-+3HCO-+H O
2 3 3 2
D.若c是无色有刺激性气味的气体,其水溶液呈弱碱性。在标准状况下用排空气法收集c气体得平均摩
尔质量为20g•mol-1的混合气体进行喷泉实验。假设溶质不扩散,实验完成后所得溶液的物质的量浓度约为
0.056mol•L-1
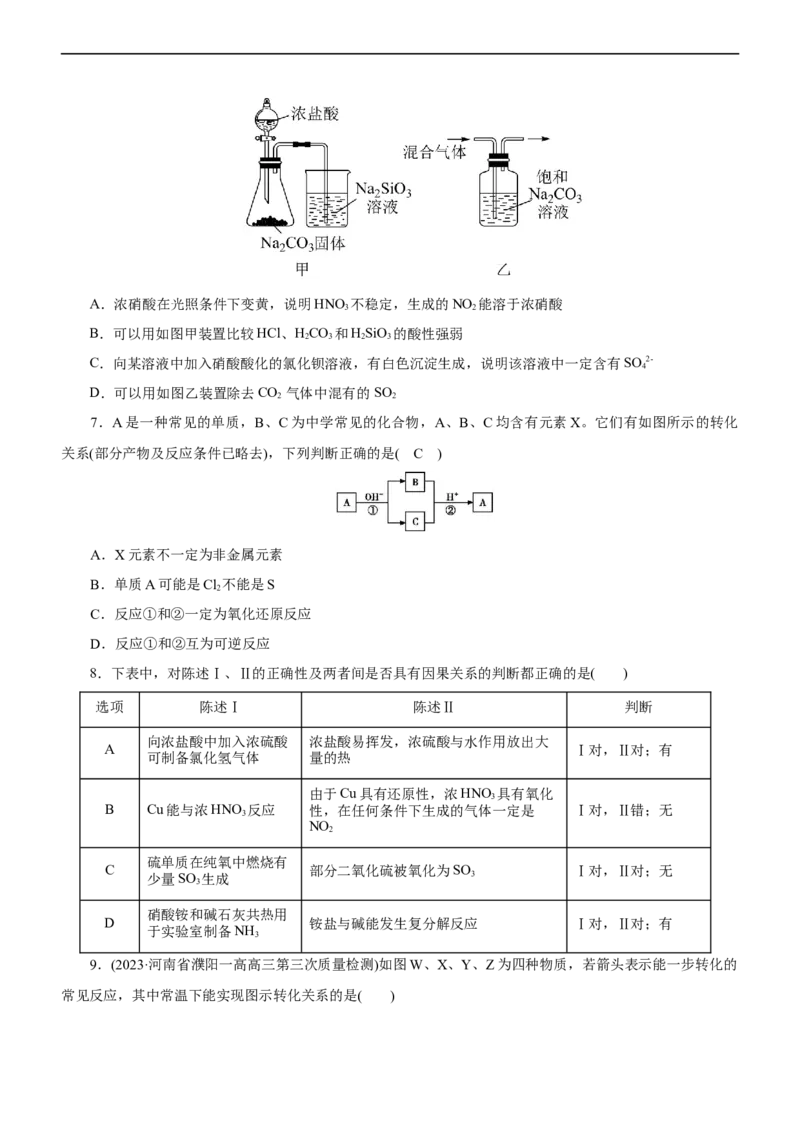
6.(2022·山西省太原市高三期中诊断性测试)下列有关实验探究的说法正确的是( )A.浓硝酸在光照条件下变黄,说明HNO 不稳定,生成的NO 能溶于浓硝酸
3 2
B.可以用如图甲装置比较HCl、HCO 和HSiO 的酸性强弱
2 3 2 3
C.向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明该溶液中一定含有SO 2-
4
D.可以用如图乙装置除去CO 气体中混有的SO
2 2
7.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X。它们有如图所示的转化
关系(部分产物及反应条件已略去),下列判断正确的是( C )
A.X元素不一定为非金属元素
B.单质A可能是Cl 不能是S
2
C.反应①和②一定为氧化还原反应
D.反应①和②互为可逆反应
8.下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断
向浓盐酸中加入浓硫酸 浓盐酸易挥发,浓硫酸与水作用放出大
A Ⅰ对,Ⅱ对;有
可制备氯化氢气体 量的热
由于Cu具有还原性,浓HNO 具有氧化
3
B Cu能与浓HNO 反应 性,在任何条件下生成的气体一定是 Ⅰ对,Ⅱ错;无
3
NO
2
硫单质在纯氧中燃烧有
C 部分二氧化硫被氧化为SO Ⅰ对,Ⅱ对;无
少量SO 生成 3
3
硝酸铵和碱石灰共热用
D 铵盐与碱能发生复分解反应 Ⅰ对,Ⅱ对;有
于实验室制备NH
3
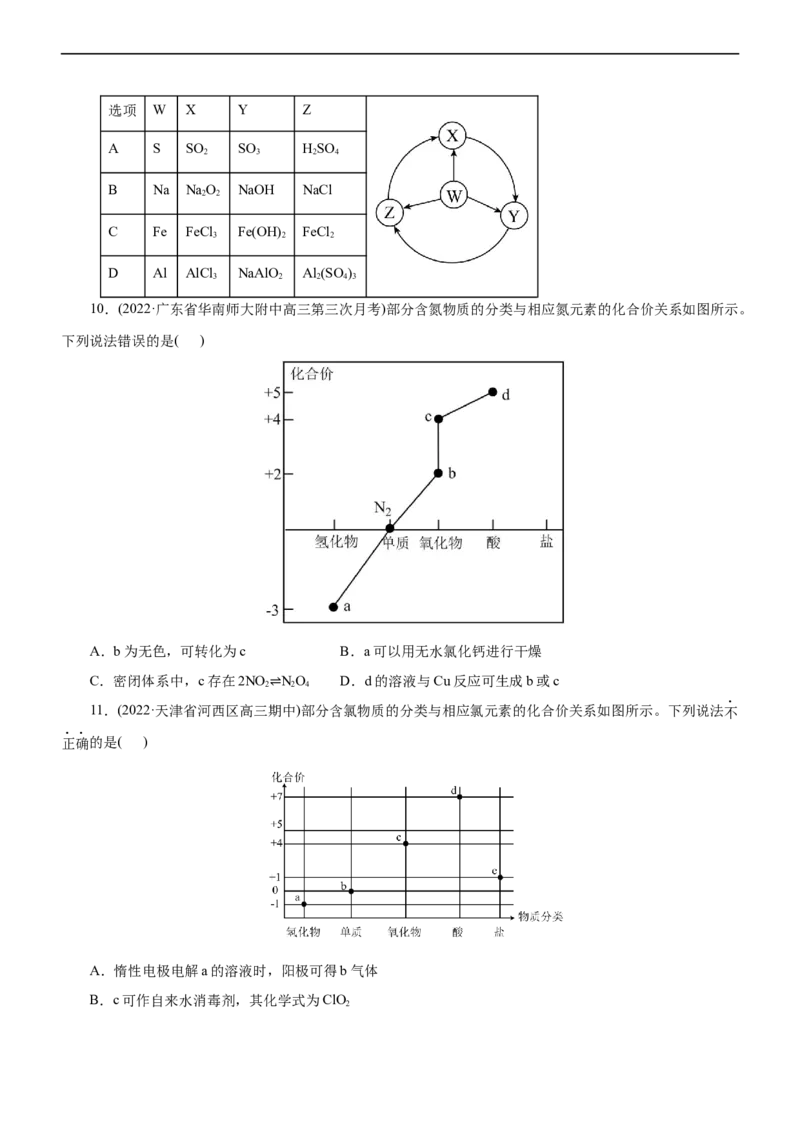
9.(2023·河南省濮阳一高高三第三次质量检测)如图W、X、Y、Z为四种物质,若箭头表示能一步转化的
常见反应,其中常温下能实现图示转化关系的是( )选项 W X Y Z
A S SO SO HSO
2 3 2 4
B Na NaO NaOH NaCl
2 2
C Fe FeCl Fe(OH) FeCl
3 2 2
D Al AlCl NaAlO Al (SO )
3 2 2 4 3
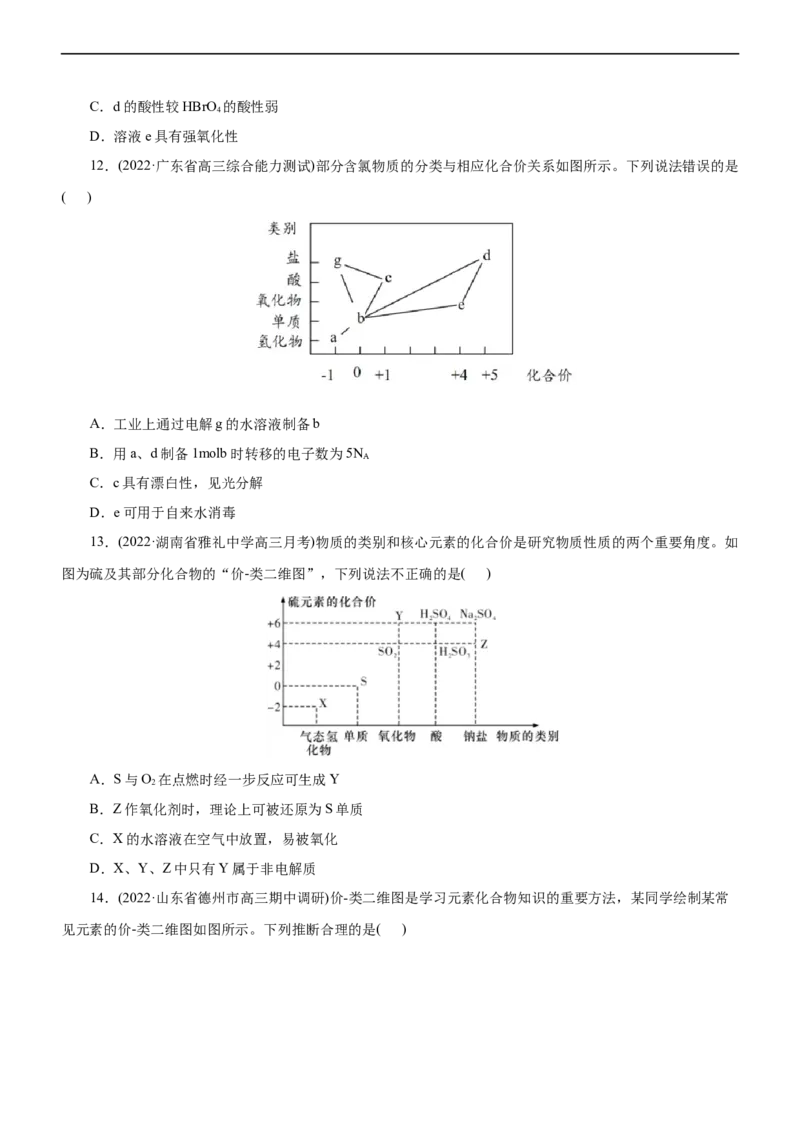
10.(2022·广东省华南师大附中高三第三次月考)部分含氮物质的分类与相应氮元素的化合价关系如图所示。
下列说法错误的是( )
A.b为无色,可转化为c B.a可以用无水氯化钙进行干燥
C.密闭体系中,c存在2NO NO D.d的溶液与Cu反应可生成b或c
2 2 4
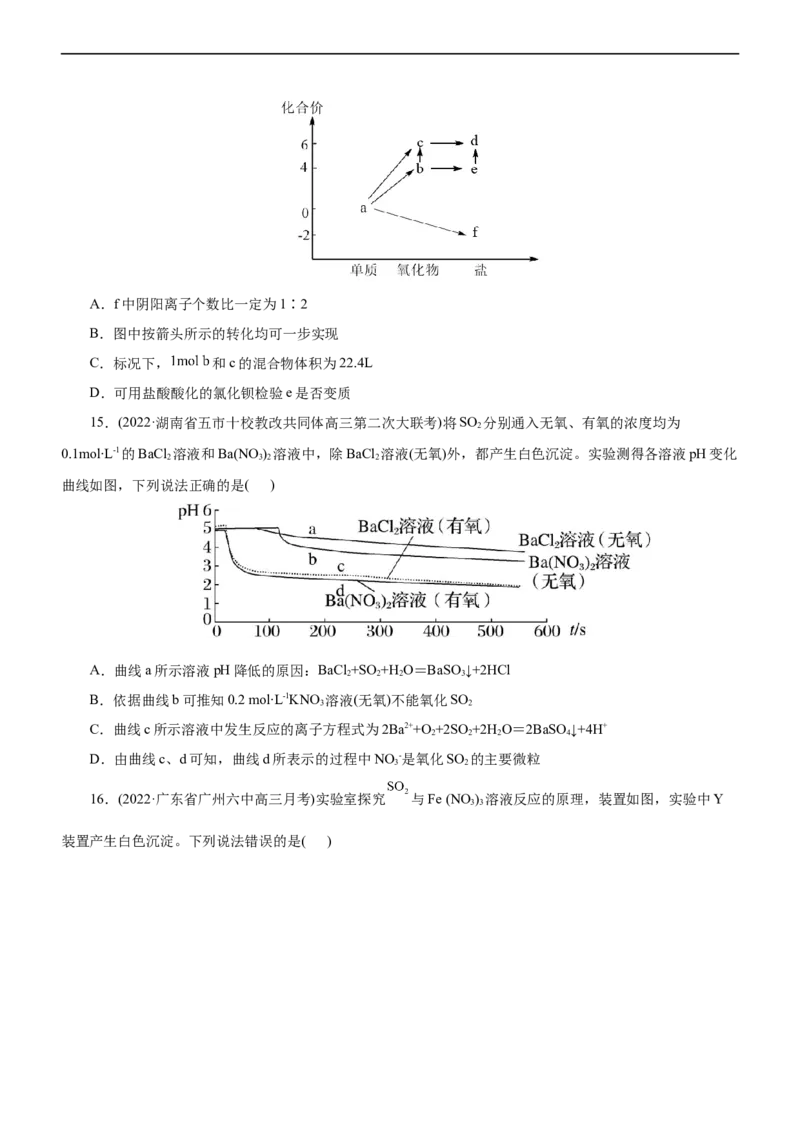
11.(2022·天津省河西区高三期⇌中)部分含氯物质的分类与相应氯元素的化合价关系如图所示。下列说法不
正确的是( )
A.惰性电极电解a的溶液时,阳极可得b气体
B.c可作自来水消毒剂,其化学式为ClO
2C.d的酸性较HBrO 的酸性弱
4
D.溶液e具有强氧化性
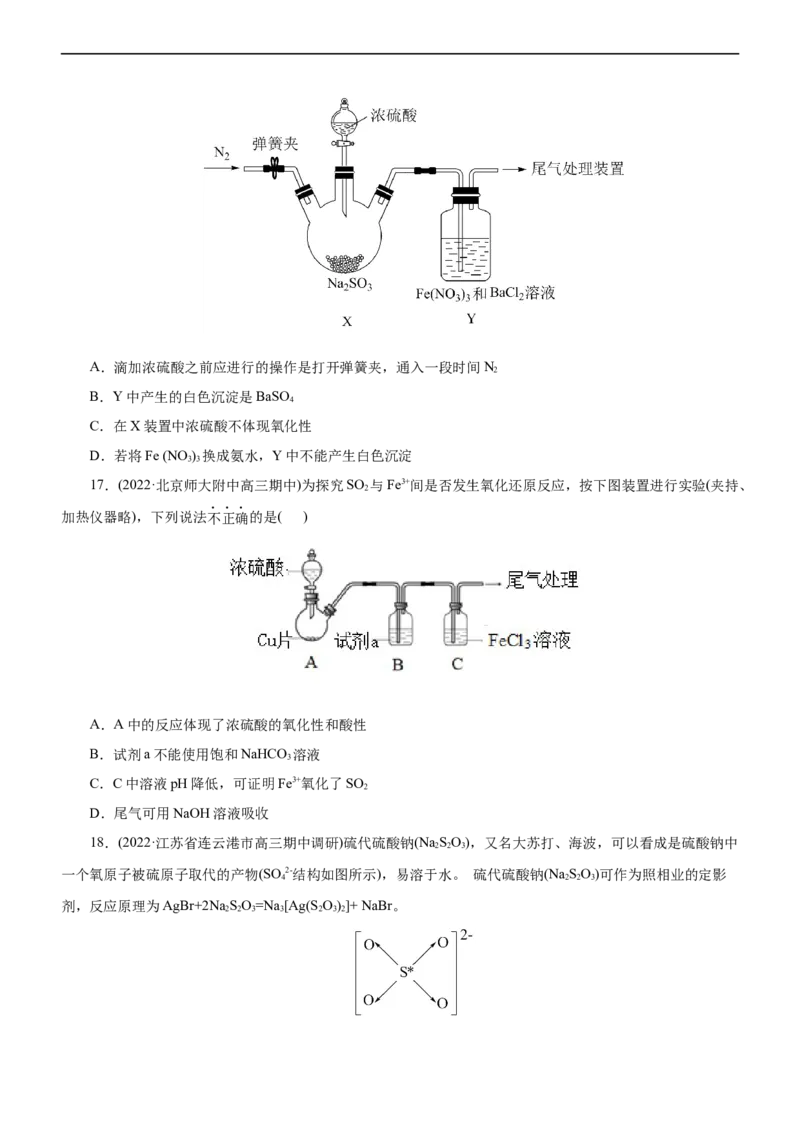
12.(2022·广东省高三综合能力测试)部分含氯物质的分类与相应化合价关系如图所示。下列说法错误的是
( )
A.工业上通过电解g的水溶液制备b
B.用a、d制备1molb时转移的电子数为5N
A
C.c具有漂白性,见光分解
D.e可用于自来水消毒
13.(2022·湖南省雅礼中学高三月考)物质的类别和核心元素的化合价是研究物质性质的两个重要角度。如
图为硫及其部分化合物的“价-类二维图”,下列说法不正确的是( )
A.S与O 在点燃时经一步反应可生成Y
2
B.Z作氧化剂时,理论上可被还原为S单质
C.X的水溶液在空气中放置,易被氧化
D.X、Y、Z中只有Y属于非电解质
14.(2022·山东省德州市高三期中调研)价-类二维图是学习元素化合物知识的重要方法,某同学绘制某常
见元素的价-类二维图如图所示。下列推断合理的是( )A.f中阴阳离子个数比一定为1∶2
B.图中按箭头所示的转化均可一步实现
C.标况下, 和c的混合物体积为22.4L
D.可用盐酸酸化的氯化钡检验e是否变质
15.(2022·湖南省五市十校教改共同体高三第二次大联考)将SO 分别通入无氧、有氧的浓度均为
2
0.1mol∙L-1的BaCl 溶液和Ba(NO ) 溶液中,除BaCl 溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化
2 3 2 2
曲线如图,下列说法正确的是( )
A.曲线a所示溶液pH降低的原因:BaCl +SO+H O=BaSO↓+2HCl
2 2 2 3
B.依据曲线b可推知0.2 mol∙L-1KNO 溶液(无氧)不能氧化SO
3 2
C.曲线c所示溶液中发生反应的离子方程式为2Ba2++O +2SO+2H O=2BaSO↓+4H+
2 2 2 4
D.由曲线c、d可知,曲线d所表示的过程中NO -是氧化SO 的主要微粒
3 2
16.(2022·广东省广州六中高三月考)实验室探究 与Fe (NO) 溶液反应的原理,装置如图,实验中Y
3 3
装置产生白色沉淀。下列说法错误的是( )A.滴加浓硫酸之前应进行的操作是打开弹簧夹,通入一段时间N
2
B.Y中产生的白色沉淀是BaSO
4
C.在X装置中浓硫酸不体现氧化性
D.若将Fe (NO) 换成氨水,Y中不能产生白色沉淀
3 3
17.(2022·北京师大附中高三期中)为探究SO 与Fe3+间是否发生氧化还原反应,按下图装置进行实验(夹持、
2
加热仪器略),下列说法不正确的是( )
A.A中的反应体现了浓硫酸的氧化性和酸性
B.试剂a不能使用饱和NaHCO 溶液
3
C.C中溶液pH降低,可证明Fe3+氧化了SO
2
D.尾气可用NaOH溶液吸收
18.(2022·江苏省连云港市高三期中调研)硫代硫酸钠(Na SO),又名大苏打、海波,可以看成是硫酸钠中
2 2 3
一个氧原子被硫原子取代的产物(SO 2-结构如图所示),易溶于水。 硫代硫酸钠(Na SO)可作为照相业的定影
4 2 2 3
剂,反应原理为AgBr+2Na SO=Na [Ag(S O)]+ NaBr。
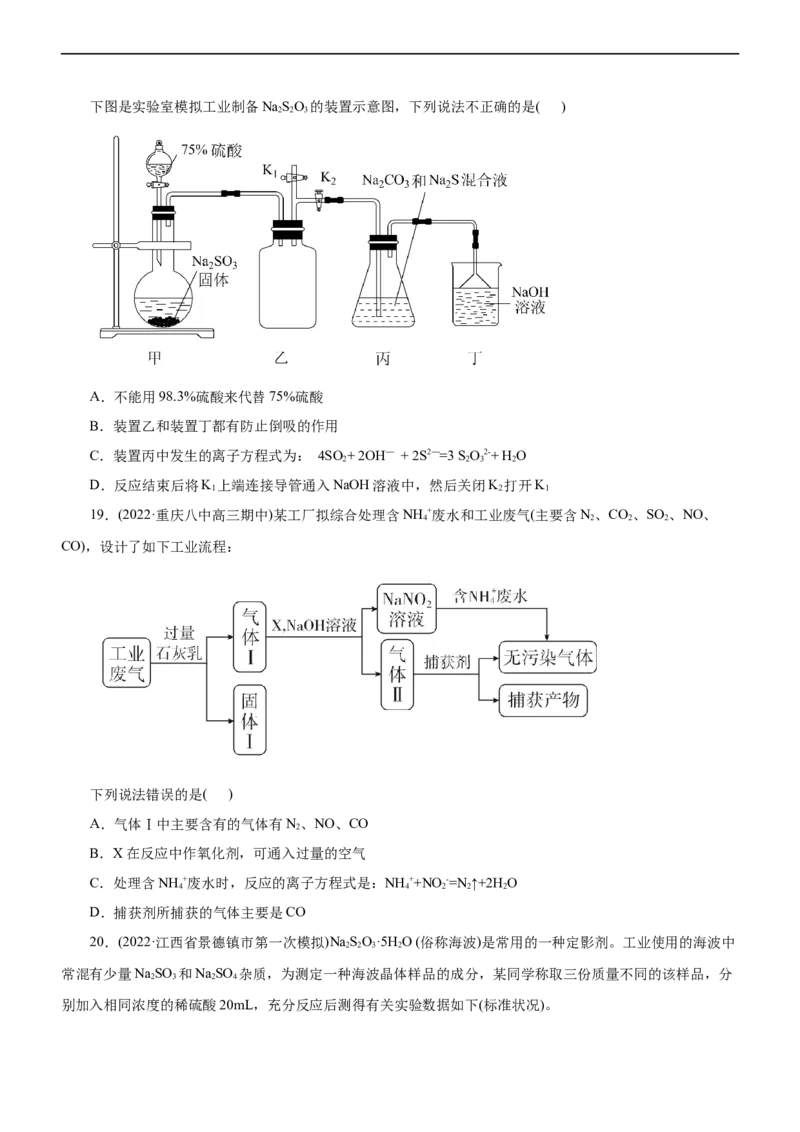
2 2 3 3 2 3 2下图是实验室模拟工业制备NaSO 的装置示意图,下列说法不正确的是( )
2 2 3
A.不能用98.3%硫酸来代替75%硫酸
B.装置乙和装置丁都有防止倒吸的作用
C.装置丙中发生的离子方程式为: 4SO + 2OH— + 2S2—=3 S O2-+ H O
2 2 3 2
D.反应结束后将K 上端连接导管通入NaOH溶液中,然后关闭K 打开K
1 2 1
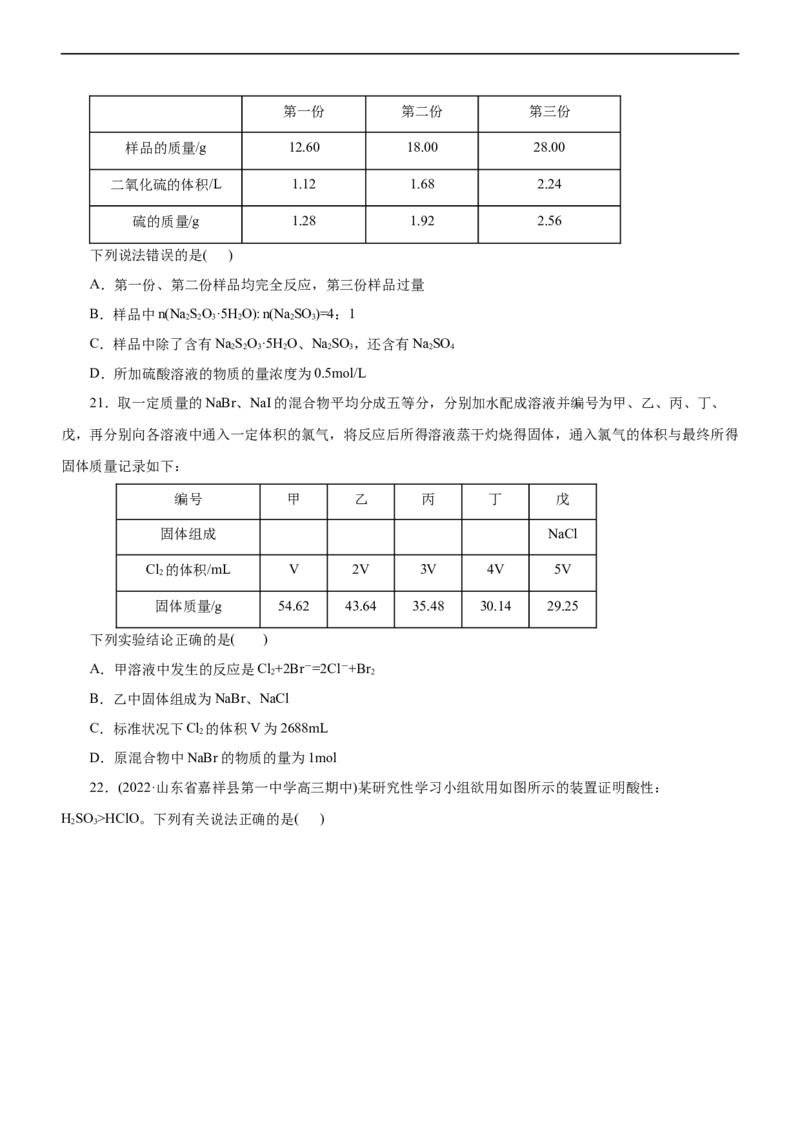
19.(2022·重庆八中高三期中)某工厂拟综合处理含NH +废水和工业废气(主要含N、CO、SO 、NO、
4 2 2 2
CO),设计了如下工业流程:
下列说法错误的是( )
A.气体Ⅰ中主要含有的气体有N、NO、CO
2
B.X在反应中作氧化剂,可通入过量的空气
C.处理含NH +废水时,反应的离子方程式是:NH ++NO-=N ↑+2H O
4 4 2 2 2
D.捕获剂所捕获的气体主要是CO
20.(2022·江西省景德镇市第一次模拟)Na SO·5H O (俗称海波)是常用的一种定影剂。工业使用的海波中
2 2 3 2
常混有少量NaSO 和NaSO 杂质,为测定一种海波晶体样品的成分,某同学称取三份质量不同的该样品,分
2 3 2 4
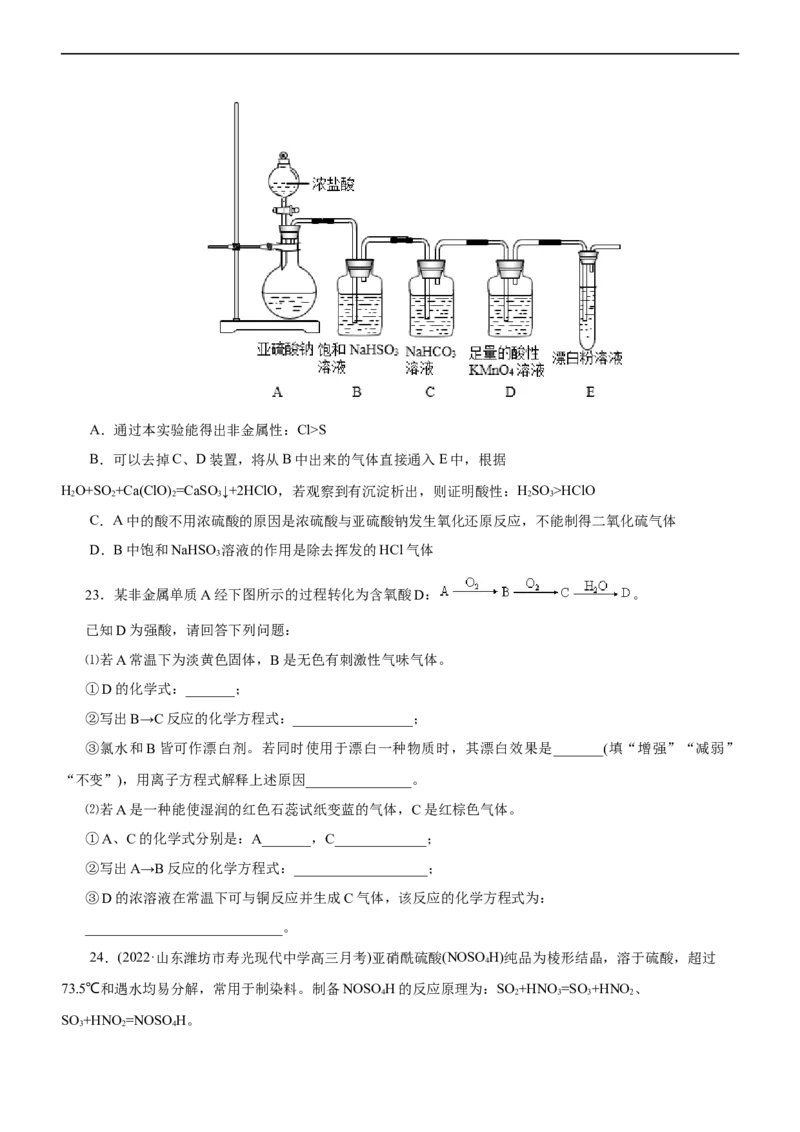
别加入相同浓度的稀硫酸20mL,充分反应后测得有关实验数据如下(标准状况)。第一份 第二份 第三份
样品的质量/g 12.60 18.00 28.00
二氧化硫的体积/L 1.12 1.68 2.24
硫的质量/g 1.28 1.92 2.56
下列说法错误的是( )
A.第一份、第二份样品均完全反应,第三份样品过量
B.样品中n(NaSO·5H O): n(NaSO )=4:1
2 2 3 2 2 3
C.样品中除了含有NaSO·5H O、NaSO ,还含有NaSO
2 2 3 2 2 3 2 4
D.所加硫酸溶液的物质的量浓度为0.5mol/L
21.取一定质量的NaBr、NaI的混合物平均分成五等分,分别加水配成溶液并编号为甲、乙、丙、丁、
戊,再分别向各溶液中通入一定体积的氯气,将反应后所得溶液蒸干灼烧得固体,通入氯气的体积与最终所得
固体质量记录如下:
编号 甲 乙 丙 丁 戊
固体组成 NaCl
Cl 的体积/mL V 2V 3V 4V 5V
2
固体质量/g 54.62 43.64 35.48 30.14 29.25
下列实验结论正确的是( )
A.甲溶液中发生的反应是Cl+2Br-=2Cl-+Br
2 2
B.乙中固体组成为NaBr、NaCl
C.标准状况下Cl 的体积V为2688mL
2
D.原混合物中NaBr的物质的量为1mol
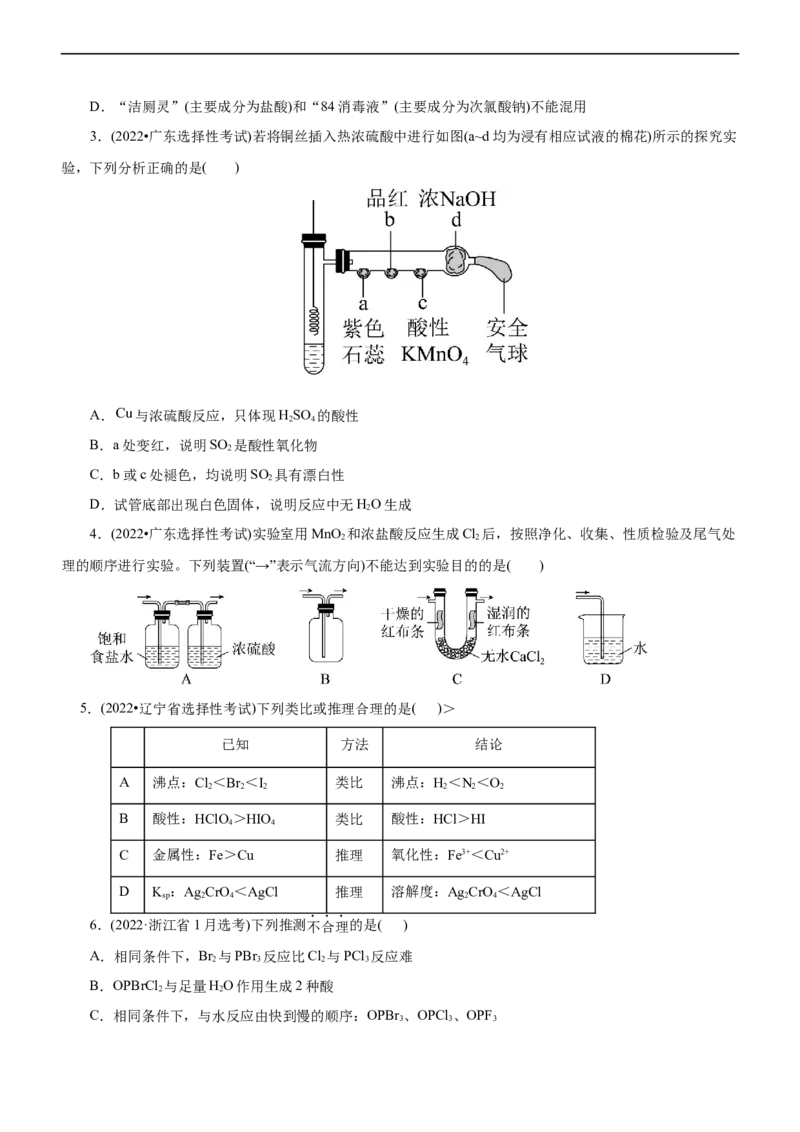
22.(2022·山东省嘉祥县第一中学高三期中)某研究性学习小组欲用如图所示的装置证明酸性:
HSO >HClO。下列有关说法正确的是( )
2 3A.通过本实验能得出非金属性:Cl>S
B.可以去掉C、D装置,将从B中出来的气体直接通入E中,根据
HO+SO +Ca(ClO) =CaSO ↓+2HClO,若观察到有沉淀析出,则证明酸性:HSO >HClO
2 2 2 3 2 3
C.A中的酸不用浓硫酸的原因是浓硫酸与亚硫酸钠发生氧化还原反应,不能制得二氧化硫气体
D.B中饱和NaHSO 溶液的作用是除去挥发的HCl气体
3
23.某非金属单质A经下图所示的过程转化为含氧酸D: 。
已知D为强酸,请回答下列问题:
⑴若A常温下为淡黄色固体,B是无色有刺激性气味气体。
①D的化学式:_______;
②写出B→C反应的化学方程式:_________________;
③氯水和B皆可作漂白剂。若同时使用于漂白一种物质时,其漂白效果是_______(填“增强”“减弱”
“不变”),用离子方程式解释上述原因_______________。
⑵若A是一种能使湿润的红色石蕊试纸变蓝的气体,C是红棕色气体。
①A、C的化学式分别是:A_______,C_____________;
②写出A→B反应的化学方程式:___________________;
③D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为:
____________________________。
24.(2022·山东潍坊市寿光现代中学高三月考)亚硝酰硫酸(NOSOH)纯品为棱形结晶,溶于硫酸,超过
4
73.5℃和遇水均易分解,常用于制染料。制备NOSOH的反应原理为:SO +HNO =SO+HNO 、
4 2 3 3 2
SO +HNO =NOSO H。
3 2 4(1)亚硝酰硫酸(NOSOH)的制备:
4
①仪器Ⅱ的名称为___________。
②按气流从左到右的顺序,上述仪器的连接顺序为___________(填仪器接口字母,部分仪器可重复使用)。
③装置B用冷水浴的目的是___________,装置D的作用是___________。
④若装置A中快速滴入硫酸,则会使NOSOH的产量___________(填“增大”“减小”或“无影响”)。
4
(2)亚硝酰硫酸(NOSOH)纯度的测定:
4
空白实验分析法是化学实验中常用的一种方法,是指在不加样品的情況下,用与测定样品相同的方法、步
骤进行定量分析,将所得结果作为空白值,从样品的分析结果中扣除,此方法可以消除试剂不纯所造成的系统
误差。现用此法测定亚硝酰硫酸(NOSOH)纯度,步骤如下:
4
步骤1:准确称取14.00g产品,在特定条件下配制成250mL溶液。
步骤2:取25.00mL产品于250mL碘量瓶中,加入60.00mL未知浓度KMnO 溶液(过量)和
4
10.00mL25%HSO 溶液,然后摇匀。
2 4
步骤3:用0.2500mol・L-1NaC O 标准溶液滴定,消耗NaC O 溶液的体积为20.00mL。把亚硝酰硫酸
2 2 4 2 2 4
(NOSOH)溶液换为蒸馏水,重复上述步骤(即进行空白实验),消耗NaC O 溶液60.00mL。
4 2 2 4
①亚硝酰硫酸(NOSOH)被KMnO 氧化成NO -和SO 2-,其离子方程式为___________。
4 4 3 4
②滴定终点的现象为___________。
③产品的纯度为___________%(保留两位有效数字)。
1.(2022•河北省选择性考试)定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的是( )
A.传统陶瓷是典型的绝缘材料 B.陶瓷主要成分为SiO 和MgO
2
C.陶瓷烧制的过程为物理变化 D.白瓷的白色是因铁含量较高
2.(2022·浙江省6月选考)下列说法正确的是( )
A.工业上通过电解六水合氯化镁制取金属镁
B.接触法制硫酸时,煅烧黄铁矿以得到三氧化硫
C.浓硝酸与铁在常温下不能反应,所以可用铁质容器贮运浓硝酸D.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用
3.(2022•广东选择性考试)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实
验,下列分析正确的是( )
A. 与浓硫酸反应,只体现HSO 的酸性
2 4
B.a处变红,说明SO 是酸性氧化物
2
C.b或c处褪色,均说明SO 具有漂白性
2
D.试管底部出现白色固体,说明反应中无HO生成
2
4.(2022•广东选择性考试)实验室用MnO 和浓盐酸反应生成Cl 后,按照净化、收集、性质检验及尾气处
2 2
理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )
5.(2022•辽宁省选择性考试)下列类比或推理合理的是( )>
已知 方法 结论
A 沸点:Cl<Br <I 类比 沸点:H<N<O
2 2 2 2 2 2
B 酸性:HClO>HIO 类比 酸性:HCl>HI
4 4
C 金属性:Fe>Cu 推理 氧化性:Fe3+<Cu2+
D K :Ag CrO<AgCl 推理 溶解度:Ag CrO<AgCl
sp 2 4 2 4
6.(2022·浙江省1月选考)下列推测不合理的是( )
A.相同条件下,Br 与PBr 反应比Cl 与PCl 反应难
2 3 2 3
B.OPBrCl 与足量HO作用生成2种酸
2 2
C.相同条件下,与水反应由快到慢的顺序:OPBr 、OPCl 、OPF
3 3 3D.PBr 与足量C HOH作用可得到P(OC H)
3 2 5 2 5 3
7.(2022•辽宁省选择性考试)HO(l)、NH (l)均可自耦电离:2HO(l) HO++OH-、2NH (l)
2 3 2 3 3
NH ++NH-。下列反应与 CHCHOH+HBr原理不同的是( )
4 2 3 2
A.MgN+6H O=3 Mg(OH) +2NH B.SiCl +8NH(l)= Si(NH )+4NHCl
3 2 2 2 3 4 3 2 4 4
C.3Cl+8NH =6NH Cl+N D.PCl +3H O=HPO +3HCl
2 3 4 2 3 2 3 3
8.(2022•北京卷)某 的多孔材料刚好可将NO “固定”,实现了NO 与NO 分离并制备HNO,如
2 4 2 2 4 3
图所示:
己知:2NO (g) NO(g) ΔH<0
2 2 4
下列说法不正确的是( )
A.气体温度升高后,不利于NO 的固定
2 4
B.NO 被固定后,平衡正移,有利于NO 的去除
2 4 2
C.制备HNO 的原理为:2NO+O +2H O=4HNO
3 2 4 2 2 3
D.每制备0.4mol硝酸,转移电子数约为6.02×1022
9.(2021•北京卷)已知1体积水可溶解40体积SO 气体,实验装置如图所示。下列说法正确的是( )
2
A.试管内液面上升能说明SO 与水发生反应
2
B.一段时间后,液面高度无明显变化,说明SO 在水中已达到饱和
2
C.向溶液中滴入石蕊试液,溶液变为红色,与下列反应有关:SO +H O HSO 、HSO H+
2 2 2 3 2 3
+HSO -、HSO - H++SO 2-
3 3 3
D.将溶液在空气中放置一段时间后,pH下降,说明SO 易挥发
2
10.(2021•天津卷)关于反应HSO +NaSO =NaSO +SO↑+H O所涉及的物质,下列说法错误的是( )
2 4 2 3 2 4 2 OA.HSO 在该反应中为氧化剂 B.NaSO 容易被空气中的O 氧化变质
2 4 2 3 2
C.NaSO 是含有共价键的离子化合物 D.SO 是导致酸雨的主要有害污染物
2 4 2
11.(2021•山东卷)下列由实验现象所得结论错误的是( )
A.向NaHSO 溶液中滴加氢硫酸,产生淡黄色沉淀,证明HSO -具有氧化性
3 3
B.向酸性KMnO 溶液中加入Fe O 粉末,紫色褪去,证明Fe O 中含Fe(Ⅱ)
4 3 4 3 4
C.向浓HNO 中插入红热的炭,产生红棕色气体,证明炭可与浓HNO 反应生成NO
3 3 2
D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应
12.(2021•浙江6月选考)下列说法不正确的是( )
A.应避免铵态氮肥与草木灰混合施用
B.工业上可用离子交换法提高海带中碘的提取率
C.电解饱和食盐水可以得到金属钠和氯气
D.将生铁进一步炼制减少含碳量,能得到耐腐蚀的钢
13.(2021•浙江1月选考)下列说法不正确的是( )
A.某些胶态金属氧化物分散于玻璃中可制造有色玻璃
B.通常以海水提取粗食盐后的母液为原料制取溴
C.生物炼铜中通常利用某些细菌把不溶性的硫化铜转化为可溶性铜盐
D.工业制备硝酸的主要设备为沸腾炉、接触室和吸收塔
14.(2021•浙江6月选考)下列“类比”结果不正确的是( )
A.HO 的热稳定性比HO的弱,则NH 的热稳定性比NH 的弱
2 2 2 2 4 3
B.HO的分子构型为V形,则二甲醚的分子骨架(C-O-C)构型为V形
2
C.Ca(HCO ) 的溶解度比CaCO 的大,则NaHCO 的溶解度比NaCO 的大
3 2 3 3 2 3
D.将丙三醇加入新制Cu(OH) 中溶液呈绛蓝色,则将葡萄糖溶液加入新制Cu(OH) 中溶液也呈绛蓝色
2 2
15.(2021•浙江6月选考)关于化合物ClONO 的性质,下列推测不合理的是( )
2
A.具有强氧化性 B.与NaOH溶液反应可生成两种钠盐
C.与盐酸作用能产生氯气 D.水解生成盐酸和硝酸
16.(2021年1月浙江选考)铝硅酸盐型分子筛中有许多笼状空穴和通道(如图),其骨架的基本结构单元是
硅氧四面体和铝氧四面体,化学组成可表示为M[(AlO )·(SiO)]·zHO(M代表金属离子)。
a 2 x 2 y 2下列推测不正确的是( )
A.常采用水玻璃、偏铝酸钠在强酸溶液中反应后结晶制得分子筛
B.若a=x/2,则M为二价阳离子
C.调节y/x(硅铝比)的值,可以改变分子筛骨架的热稳定性
D.分子筛中的笼状空穴和通道,可用于筛分分子
17.(2022•江苏卷)周期表中ⅣA族元素及其化合物应用广泛,甲烷具有较大的燃烧热(890.3 kJ·mol-l),是
常见燃料;Si、Ge是重要的半导体材料,硅晶体表面SiO 能与氢氟酸(HF,弱酸)反应生成HSiF (H SiF 在水
2 2 6 2 6
中完全电离为H+和SiF2-);1885年德国化学家将硫化锗(GeS )与H 共热制得了门捷列夫预言的类硅—锗;下
6 2 2
列化学反应表示正确的是( )
A.SiO 与HF溶液反应:SiO+6HF=2H++SiF 2-+2H O
2 2 6 2
B.高温下H 还原GeS :GeS +2H =Ge+2H S
2 2 2 2 2
C.铅蓄电池放电时的正极反应:Pb+SO2--2e-=PbSO
4 4
D.甲烷的燃烧:CH(g)+2O(g)==CO (g)+2HO(g) ΔH =890.3kJ·mol−1
4 2 2 2 2