文档内容
专题 09 反应速率、化学平衡
2020年高考真题
1.(2020年浙江卷)5mL0.1mol⋅L−1KI溶液与1mL0.1mol⋅L−1FeCl 溶液发生反应:
3
2Fe3+ (aq)+2I− (aq)⇌2Fe2+ (aq)+I (aq),达到平衡。下列说法不正确的是( )
2
A.加入苯,振荡,平衡正向移动
B.经苯2次萃取分离后,在水溶液中加入KSCN,溶液呈血红色,表明该化学反应存在限度
C.加入FeSO 固体,平衡逆向移动
4
c2(Fe2+)
D.该反应的平衡常数K=
c2(Fe3+)×c2(I−)
【答案】D
【解析】A.加入苯振荡,苯将I 萃取到苯层,水溶液中c(I)减小,平衡正向移动,A正确;
2 2
B.将5mL0.1mol/LKI溶液与1mL0.1mol/LFeCl 溶液混合,参与反应的Fe3+与I−物质的量之比为1:1,反应
3
后I−一定过量,经苯2次萃取分离后,在水溶液中加入KSCN溶液呈血红色,说明水溶液中仍含有Fe3+,
即Fe3+没有完全消耗,表明该化学反应存在限度,B正确;
C.加入FeSO 固体溶于水电离出Fe2+,c(Fe2+)增大,平衡逆向移动,C正确;
4
c2(Fe2+)⋅c(I )
D.该反应的平衡常数K= 2 ,D错误;
c2(Fe3+)⋅c2(I-)
答案选D。
2.(2020年浙江卷)一定条件下:2NO (g)⇌ N O (g) ΔH<0。在测定NO 的相对分子质量时,下列条件
2 2 4 2
中,测定结果误差最小的是( )
A.温度0℃、压强50kPa B.温度130℃、压强300kPa
C.温度25℃、压强100kPa D.温度130℃、压强50kPa
【答案】D
【解析】测定二氧化氮的相对分子质量,要使测定结果误差最小,应该使混合气体中NO 的含量越多越好,
2
为了实现该目的,应该改变条件使平衡尽可以地逆向移动。该反应是一个反应前后气体分子数减小的放热
反应,可以通过减小压强、升高温度使平衡逆向移动,则选项中,温度高的为130℃,压强低的为50kPa,结合二者选D。答案为D。
3.(2020年江苏卷)CH 与CO 重整生成H 和CO的过程中主要发生下列反应
4 2 2
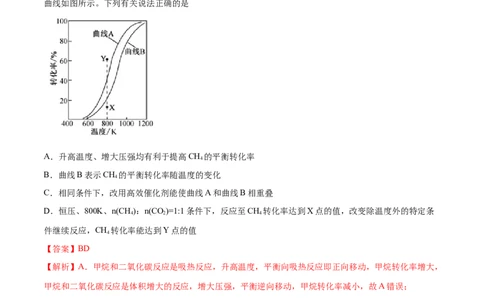
在恒压、反应物起始物质的量比 条件下,CH 和CO 的平衡转化率随温度变化的
4 2
曲线如图所示。下列有关说法正确的是
A.升高温度、增大压强均有利于提高CH 的平衡转化率
4
B.曲线B表示CH 的平衡转化率随温度的变化
4
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800K、n(CH):n(CO)=1:1条件下,反应至CH 转化率达到X点的值,改变除温度外的特定条
4 2 4
件继续反应,CH 转化率能达到Y点的值
4
【答案】BD
【解析】A.甲烷和二氧化碳反应是吸热反应,升高温度,平衡向吸热反应即正向移动,甲烷转化率增大,
甲烷和二氧化碳反应是体积增大的反应,增大压强,平衡逆向移动,甲烷转化率减小,故A错误;
B.根据两个反应得到总反应为CH(g)+2CO(g) H(g)+3CO(g) +HO (g),加入的CH 与CO 物质
4 2 2 2 4 2
的量相等,CO 消耗量大于CH,因此CO 的转化率大于CH,因此曲线B表示CH 的平衡转化率随温度
2 4 2 4 4
变化,故B正确;
C.使用高效催化剂,只能提高反应速率,但不能改变平衡转化率,故C错误;
D.800K时甲烷的转化率为X点,可以通过改变二氧化碳的量来提高甲烷的转化率达到Y点的值,故D
正确。综上所述,答案为BD。4.(2020年天津卷)已知 呈粉红色, 呈蓝色, 为无色。现将
CoCl 溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
2
,用该溶液做实验,溶液的颜色变化如下:
以下结论和解释正确的是
A.等物质的量的 和 中σ键数之比为3:2
B.由实验①可推知△H<0
C.实验②是由于c(H O)增大,导致平衡逆向移动
2
D.由实验③可知配离子的稳定性:
【答案】D
【解析】A.1个[Co(H O) ]2+中含有18个σ键,1个[CoCl ]2−中含有4个σ键,等物质的量的[Co(H O) ]2+和
2 6 4 2 6
[CoCl ]2−所含σ键数之比为18:4=9:2,A错误;
4
B.实验①将蓝色溶液置于冰水浴中,溶液变为粉红色,说明降低温度平衡逆向移动,则逆反应为放热反
应,正反应为吸热反应,∆H>0,B错误;
C.实验②加水稀释,溶液变为粉红色,加水稀释,溶液的体积增大,[Co(H O) ]2+、[CoCl ]2−、Cl−浓度都
2 6 4
减小,[Co(H O) ]2+、Cl−的化学计量数之和大于[CoCl ]2−的化学计量数,则瞬时浓度商>化学平衡常数,平
2 6 4
衡逆向移动,C错误;
D.实验③加入少量ZnCl 固体,溶液变为粉红色,说明Zn2+与Cl−结合成更稳定的[ZnCl ]2−,导致溶液中
2 4
c(Cl−)减小,平衡逆向移动,则由此说明稳定性:[ZnCl ]2−>[CoCl ]2−,D正确;
4 4
答案选D。
【点睛】本题有两个易错点:A项中[Co(H O) ]2+中不仅有Co2+与HO分子间的配位键,而且每个HO分子
2 6 2 2
中还有两个O—Hσ键;C项中HO为溶剂,视为纯液体,加水稀释,溶液体积增大,相当于利用“对气体
2
参与的反应,增大体积、减小压强,平衡向气体系数之和增大的方向移动”来理解。
5.(2020年新课标Ⅲ)二氧化碳催化加氢合成乙烯是综合利用CO 的热点研究领域。回答下列问题:
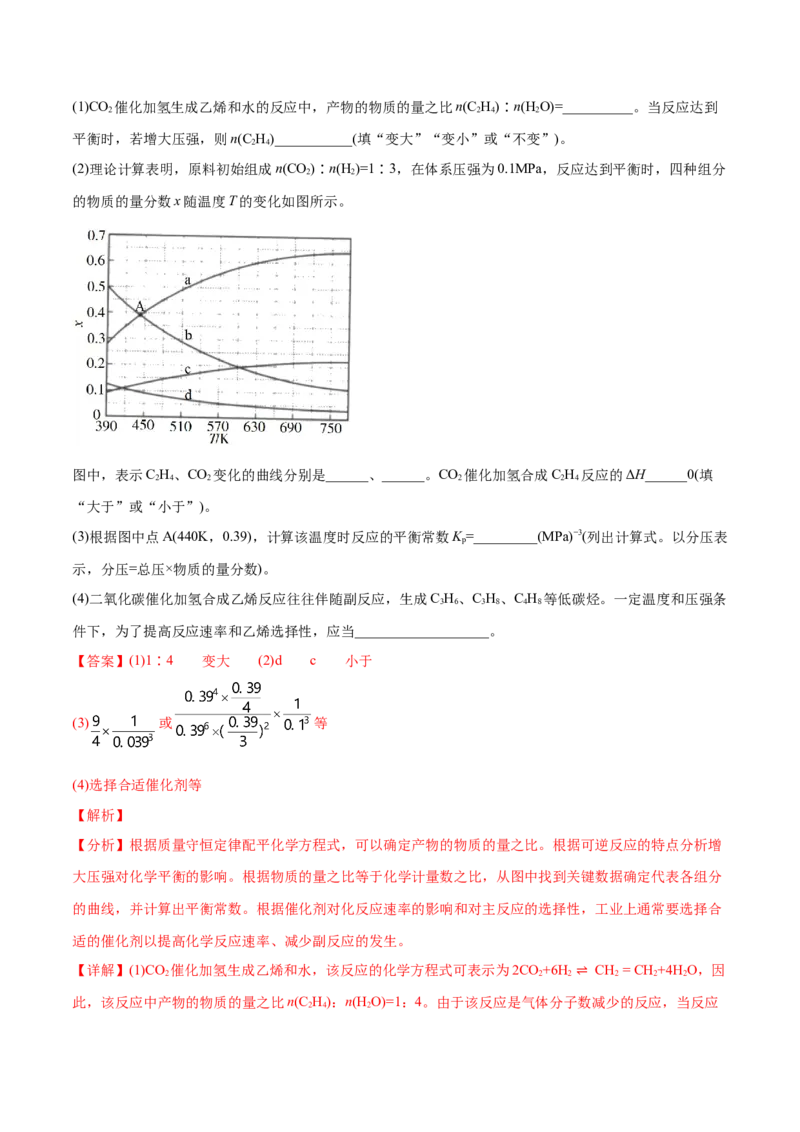
2(1)CO 催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C H)∶n(H O)=__________。当反应达到
2 2 4 2
平衡时,若增大压强,则n(C H)___________(填“变大”“变小”或“不变”)。
2 4
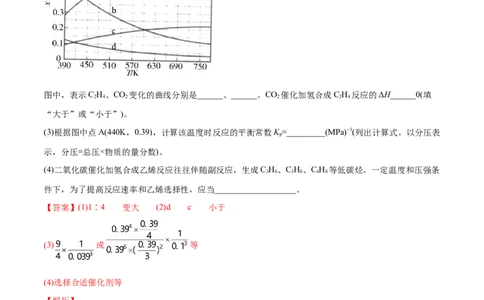
(2)理论计算表明,原料初始组成n(CO)∶n(H )=1∶3,在体系压强为0.1MPa,反应达到平衡时,四种组分
2 2
的物质的量分数x随温度T的变化如图所示。
图中,表示C H、CO 变化的曲线分别是______、______。CO 催化加氢合成C H 反应的ΔH______0(填
2 4 2 2 2 4
“大于”或“小于”)。
(3)根据图中点A(440K,0.39),计算该温度时反应的平衡常数K =_________(MPa)−3(列出计算式。以分压表
p
示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C H、C H、C H 等低碳烃。一定温度和压强条
3 6 3 8 4 8
件下,为了提高反应速率和乙烯选择性,应当___________________。
【答案】(1)1∶4 变大 (2)d c 小于
(3) 或 等
(4)选择合适催化剂等
【解析】
【分析】根据质量守恒定律配平化学方程式,可以确定产物的物质的量之比。根据可逆反应的特点分析增
大压强对化学平衡的影响。根据物质的量之比等于化学计量数之比,从图中找到关键数据确定代表各组分
的曲线,并计算出平衡常数。根据催化剂对化反应速率的影响和对主反应的选择性,工业上通常要选择合
适的催化剂以提高化学反应速率、减少副反应的发生。
【详解】(1)CO 催化加氢生成乙烯和水,该反应的化学方程式可表示为2CO+6H CH = CH+4H O,因
2 2 2 2 2 2
此,该反应中产物的物质的量之比n(C H):n(H O)=1:4。由于该反应是气体分子⇌数减少的反应,当反应
2 4 2达到平衡状态时,若增大压强,则化学平衡向正反应方向移动,n(C H)变大。
2 4
(2)由题中信息可知,两反应物的初始投料之比等于化学计量数之比;由图中曲线的起点坐标可知,c和a
所表示的物质的物质的量分数之比为1:3、d和b表示的物质的物质的量分数之比为1:4,则结合化学计量
数之比可以判断,表示乙烯变化的曲线是d,表示二氧化碳变化曲线的是c。由图中曲线的变化趋势可知,
升高温度,乙烯的物质的量分数减小,则化学平衡向逆反应方向移动,则该反应为放热反应,∆H小于0。
(3)原料初始组成n(CO)∶n(H )=1∶3,在体系压强为0.1Mpa建立平衡。由A点坐标可知,该温度下,氢
2 2
气和水的物质的量分数均为0.39,则乙烯的物质的量分数为水的四分之一,即 ,二氧化碳的物质的
量分数为氢气的三分之一,即 ,因此,该温度下反应的平衡常数 (MPa)
−3= (MPa)−3。
(4)工业上通常通过选择合适的催化剂,以加快化学反应速率,同时还可以提高目标产品的选择性,减少副
反应的发生。因此,一定温度和压强下,为了提高反应速率和乙烯的选择性,应当选择合适的催化剂。
【点睛】本题确定图中曲线所代表的化学物质是难点,其关键在于明确物质的量的分数之比等于各组分的
物质的量之比,也等于化学计量数之比(在初始投料之比等于化学计量数之比的前提下,否则不成立)。
6.(2020年山东新高考)探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产率。以CO、
3 3 2
H 为原料合成CHOH涉及的主要反应如下:
2 3
Ⅰ.
Ⅱ.
Ⅲ.
回答下列问题:(1) _________kJ∙mol−1。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO 和3 mol H 发生上述反应,达到平衡时,容
2 2
器中CHOH(g)为ɑ mol,CO为b mol,此时HO(g)的浓度为__________mol﹒L−1(用含a、b、V的代数式表
3 2
示,下同),反应Ⅲ的平衡常数为___________。
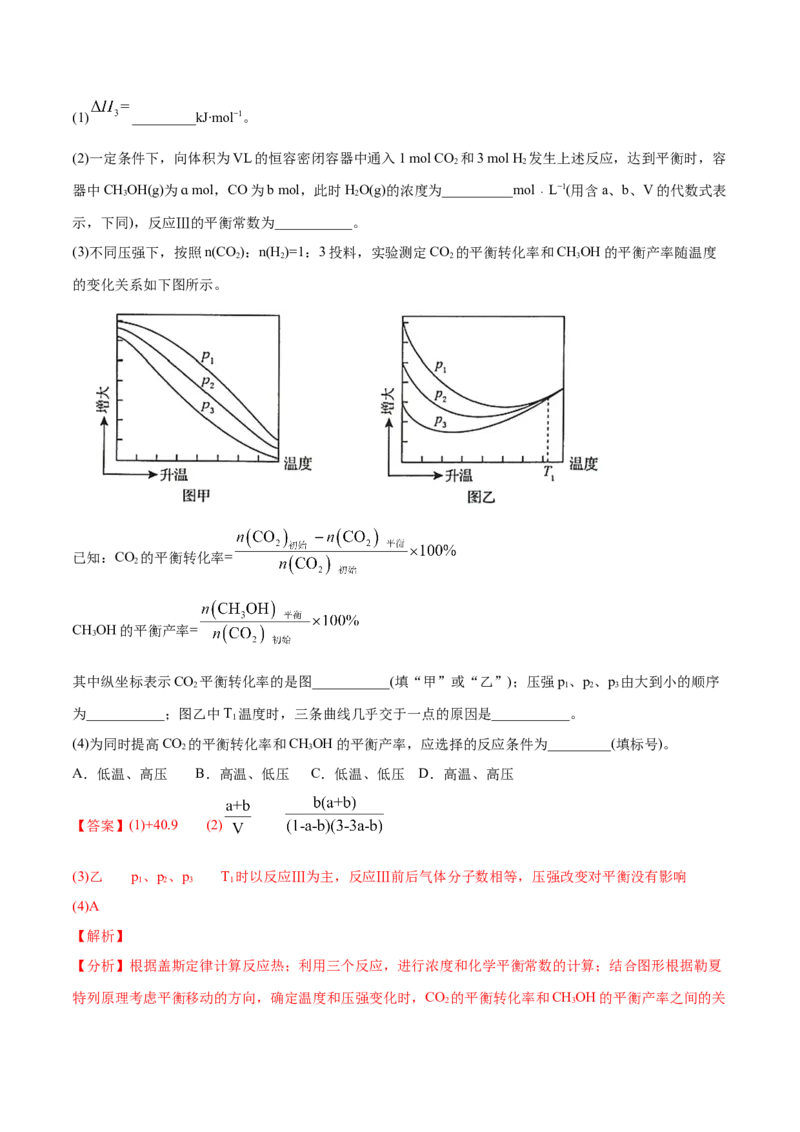
(3)不同压强下,按照n(CO):n(H )=1:3投料,实验测定CO 的平衡转化率和CHOH的平衡产率随温度
2 2 2 3
的变化关系如下图所示。
已知:CO 的平衡转化率=
2
CHOH的平衡产率=
3
其中纵坐标表示CO 平衡转化率的是图___________(填“甲”或“乙”);压强p、p、p 由大到小的顺序
2 1 2 3
为___________;图乙中T 温度时,三条曲线几乎交于一点的原因是___________。
1
(4)为同时提高CO 的平衡转化率和CHOH的平衡产率,应选择的反应条件为_________(填标号)。
2 3
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
【答案】(1)+40.9 (2)
(3)乙 p、p、p T 时以反应Ⅲ为主,反应Ⅲ前后气体分子数相等,压强改变对平衡没有影响
1 2 3 1
(4)A
【解析】
【分析】根据盖斯定律计算反应热;利用三个反应,进行浓度和化学平衡常数的计算;结合图形根据勒夏
特列原理考虑平衡移动的方向,确定温度和压强变化时,CO 的平衡转化率和CHOH的平衡产率之间的关
2 3系得到相应的答案。
【详解】(1)根据反应I+II=III,则△H= H+ H=−49.5kJ∙mol−1+(−90.4 kJ∙mol−1)=+40.9 kJ∙mol−1;
3 1 2
(2)假设反应II中,CO反应了xmol,则△II生成△的CHOH为xmol,I生成的CHOH为(a−x)mol,III生成
3 3
CO为(b+x)mol,根据反应I: ,反应II:
,反应III: ,所以平衡时水的物
质的量为(a−x)mol+(b+x)mol =(a+b)mol,浓度为: ;平衡时CO 的物质的量为
2
1mol−(a−x)mol−(b+x)mol=(1−a−b)mol,H 的物质的量为3mol−3(a−x)mol−2x−(b+x)mol=(3−3a−b)mol,CO
2
的物质的量为bmol,水的物质的量为(a+b)mol,则反应III的平衡常数为:
;
(3)反应I和II为放热反应,升高温度,平衡逆向移动,则CHOH的平衡产率减少,所以图甲表示CHOH
3 3
的平衡产率,图乙中,开始升高温度,由于反应I和II为放热反应,升高温度,平衡逆向移动,CO 的平
2
衡转化率降低,反应III为吸热反应,升高温度反应III向正反应方向移动,升高一定温度后以反应III为主,
CO 的平衡转化率又升高,所以图乙表示CO 的平衡转化率;压强增大,反应I和II是气体体积减小的反
2 2
应,反应I和II平衡正向移动,反应III气体体积不变化,平衡不移动,故压强增大CHOH的平衡产率增
3
大,根据图所以压强关系为:p>p>p;温度升高,反应I和II平衡逆向移动,反应III向正反应方向移动,
1 2 3
所以T 温度时,三条曲线交与一点的原因为:T 时以反应III为主,反应III前后分子数相等,压强改变对
1 1
平衡没有影响;
(4)根据图示可知,温度越低,CO 的平衡转化率越大,CHOH的平衡产率越大,压强越大,CO 的平衡转
2 3 2
化率越大,CHOH的平衡产率越大,所以选择低温和高压,答案选A。
3
【点睛】本题为化学反应原理综合题,考查了盖斯定律、化学平衡常数的计算、勒夏特列原理进行图像的
分析,难点为平衡常数的计算,巧用了三个反应的化学方程式,进行了数据的处理,得到反应III的各项数据,进行计算得到平衡常数。
7.(2020年浙江卷)研究 氧化 制 对资源综合利用有重要意义。相关的主要化学反应有:
Ⅰ.
Ⅱ.
Ⅲ.
Ⅳ.
已知: 时,相关物质的相对能量(如图1)。
可根据相关物质的相对能量计算反应或变化的 ( 随温度变化可忽略)。例如:
。
请回答:
(1)①根据相关物质的相对能量计算 _____ 。
②下列描述正确的是_____
A.升高温度反应Ⅰ的平衡常数增大
B.加压有利于反应Ⅰ、Ⅱ的平衡正向移动
C.反应Ⅲ有助于乙烷脱氢,有利于乙烯生成
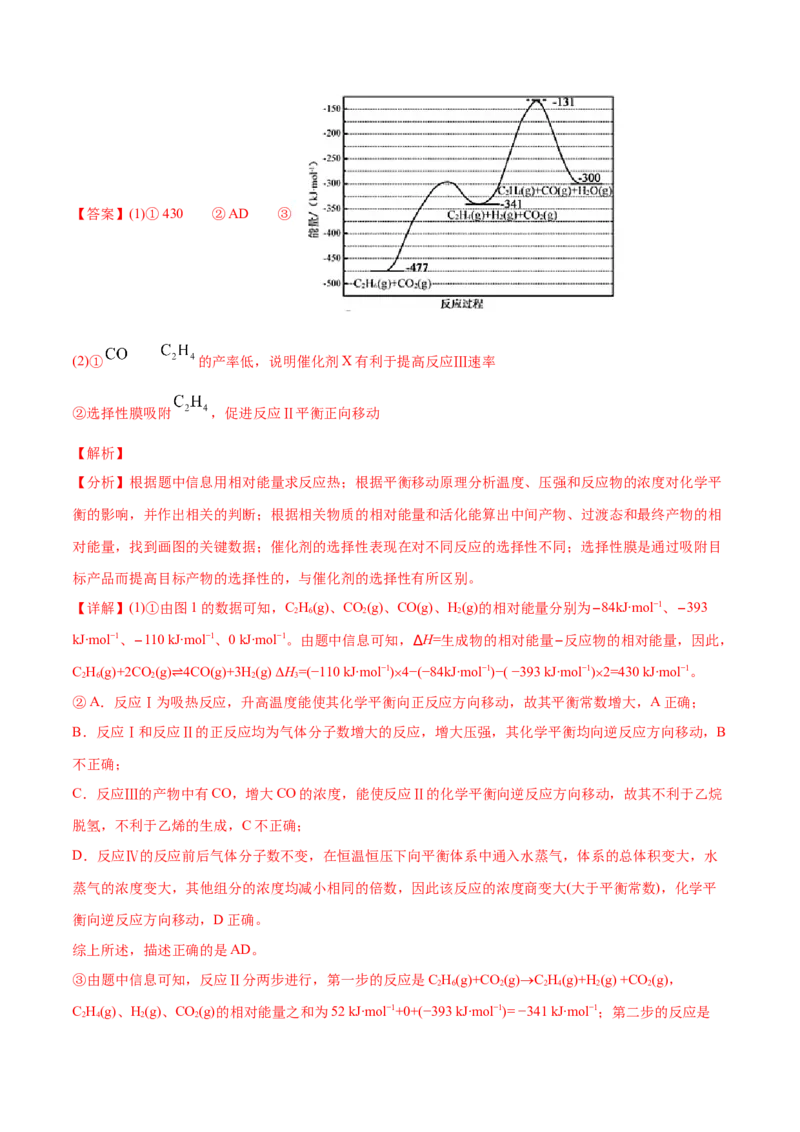
D.恒温恒压下通水蒸气,反应Ⅳ的平衡逆向移动③有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下:
,且第二步速率较慢(反应活化能为
)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从
的能量 ,开始(如图2)。
(2)① 和 按物质的量1:1投料,在 和保持总压恒定的条件下,研究催化剂X对“ 氧化
制 ”的影响,所得实验数据如下表:
催化剂 转化率 转化率 产率
催化剂X 19.0 37.6 3.3
结合具体反应分析,在催化剂X作用下, 氧化 的主要产物是______,判断依据是_______。
②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高 的选择性(生成 的物质的量
与消耗 的物质的量之比)。在 ,乙烷平衡转化率为 ,保持温度和其他实验条件不变,采
用选择性膜技术,乙烷转化率可提高到 。结合具体反应说明乙烷转化率增大的原因是_____。【答案】(1)①430 ②AD ③
(2)① 的产率低,说明催化剂X有利于提高反应Ⅲ速率
②选择性膜吸附 ,促进反应Ⅱ平衡正向移动
【解析】
【分析】根据题中信息用相对能量求反应热;根据平衡移动原理分析温度、压强和反应物的浓度对化学平
衡的影响,并作出相关的判断;根据相关物质的相对能量和活化能算出中间产物、过渡态和最终产物的相
对能量,找到画图的关键数据;催化剂的选择性表现在对不同反应的选择性不同;选择性膜是通过吸附目
标产品而提高目标产物的选择性的,与催化剂的选择性有所区别。
【详解】(1)①由图1的数据可知,C H(g)、CO(g)、CO(g)、H(g)的相对能量分别为−84kJ∙mol−1、−393
2 6 2 2
kJ∙mol−1、−110 kJ∙mol−1、0 kJ∙mol−1。由题中信息可知,∆H=生成物的相对能量−反应物的相对能量,因此,
C H(g)+2CO (g) 4CO(g)+3H(g) ∆H=(−110 kJ∙mol−1)4−(−84kJ∙mol−1)−( −393 kJ∙mol−1)2=430 kJ∙mol−1。
2 6 2 2 3
②A.反应Ⅰ为吸⇌热反应,升高温度能使其化学平衡向正反应方向移动,故其平衡常数增大,A正确;
B.反应Ⅰ和反应Ⅱ的正反应均为气体分子数增大的反应,增大压强,其化学平衡均向逆反应方向移动,B
不正确;
C.反应Ⅲ的产物中有CO,增大CO的浓度,能使反应Ⅱ的化学平衡向逆反应方向移动,故其不利于乙烷
脱氢,不利于乙烯的生成,C不正确;
D.反应Ⅳ的反应前后气体分子数不变,在恒温恒压下向平衡体系中通入水蒸气,体系的总体积变大,水
蒸气的浓度变大,其他组分的浓度均减小相同的倍数,因此该反应的浓度商变大(大于平衡常数),化学平
衡向逆反应方向移动,D正确。
综上所述,描述正确的是AD。
③由题中信息可知,反应Ⅱ分两步进行,第一步的反应是C H(g)+CO (g)C H(g)+H(g) +CO (g),
2 6 2 2 4 2 2
C H(g)、H(g)、CO(g)的相对能量之和为52 kJ∙mol−1+0+(−393 kJ∙mol−1)= −341 kJ∙mol−1;第二步的反应是
2 4 2 2C H(g)+H(g) +CO (g)C H(g)+HO(g) +CO(g),其活化能为210 kJ∙mol−1,故该反应体系的过渡态的相对
2 4 2 2 2 4 2
能量又升高了210 kJ∙mol−1,过渡态的的相对能量变为−341 kJ∙mol−1+210 kJ∙mol−1= −131 kJ∙mol−1,最终生成
物C H(g)、HO(g)、CO(g)的相对能量之和为(52 kJ∙mol−1)+(−242 kJ∙mol−1)+(−110 kJ∙mol−1)= −300 kJ∙mol−1。
2 4 2
根据题中信息,第一步的活化能较小,第二步的活化能较大,故反应Ⅱ分两步进行的“能量—反应过程
图”可以表示如下: 。
(2)①由题中信息及表中数据可知,尽管CO 和C H 按物质的量之比1:1投料,但是C H 的产率远远小于
2 2 6 2 4
C H 的转化率,但是CO 的转化率高于C H,说明在催化剂X的作用下,除了发生反应Ⅱ,还发生了反应
2 6 2 2 6
Ⅲ,而且反应物主要发生了反应Ⅲ,这也说明催化剂X有利于提高反应Ⅲ速率,因此,CO 氧化C H 的主
2 2 6
要产物是CO。故答案为:CO;C H 的产率低说明催化剂X有利于提高反应Ⅲ速率。
2 4
②由题中信息可知,选择性膜技术可提高C H 的选择性,由反应ⅡC H(g)+CO (g) C H(g)+HO(g)
2 4 2 6 2 2 4 2
+CO(g)可知,该选择性应具体表现在选择性膜可选择性地让C H 通过而离开体系,⇌即通过吸附C H 减小
2 4 2 4
其在平衡体系的浓度,从而促进化学平衡向正反应方向移动,因而可以乙烷的转化率。故答案为:选择性
膜吸附C H,促进反应Ⅱ平衡向正反应方向移动。
2 4
【点睛】本题“能量—反应过程图”是难点。一方面数据的处理较难,要把各个不同状态的相对能量算准,
不能遗漏某些物质;另一方面,还要考虑两步反应的活化能不同。这就要求考生必须有耐心和细心,准确
提取题中的关键信息和关键数据,才能做到完美。
2020届高考模拟试题
8.(2020年北京市东城区第二学期高三4月新高考适应试卷)下列事实不能用平衡移动原理解释的是A. 开启啤酒瓶后,瓶中马上泛起大量泡沫
B. 由H(g)、I(g)、HI(g)组成的平衡体系加压后颜色变深
2 2
C. 实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出
D. 石灰岩受地下水长期溶蚀形成溶洞
【答案】B
【解析】A.啤酒中存在平衡:HCO HO+CO,开启啤酒瓶,瓶内压强降低,平衡向气体体积增大
2 3 2 2
的方向移动,即向生成二氧化碳气体的方向移动,故能用平衡移动原理解释,A不选;
B.反应H+I 2HI是一个反应前后气体分子数不变的反应,压强改变并不能使平衡发生移动,混合
2 2
气体加压后颜色变深,是因为I 的浓度增大,不能用平衡移动原理解释,B选;
2
C.实验室制取乙酸乙酯时,采用加热的方式将乙酸乙酯不断蒸出,从而平衡向生成乙酸乙酯的方向移动,
能用平衡移动原理解释,C不选;
D.石灰岩形成与反应:CaCO +CO +H O Ca(HCO ),能用平衡移动原理解释,D不选;
3 2 2 3 2
答案选B。9.(天津市和平区2020届高三一模)在300mL的密闭固定容器中,一定条件下发生Ni(s)+4CO(g)
Ni(CO) (g)的反应,该反应平衡常数(K)与温度(T)的关系如下表所示:
4
T/℃ 25 80 230
K 5×104 2 1.9×10﹣5
下列说法不正确的是( )
A.上述生成Ni(CO) (g)的反应为放热反应
4
B.230℃时,该反应的正反应为不自发的反应
C.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO) 的平衡浓度为2 mol·L−1
4
D.25℃时反应Ni(CO) (g) Ni(s)+4CO(g)的平衡常数为2×10−5
4
【答案】B
【解析】A.图表数据分析,平衡常数随温度升高减小,说明平衡逆向进行,逆向是吸热反应,正向是放
热反应,故A正确;
B.230℃时,该反应的平衡常数K=1.9×10﹣5,只是说明正反应进行的程度低,但仍为自发的反应,故B错
误;
C.80℃达到平衡时,测得n(CO)=0.3mol,c(CO)= =1mol/L,依据平衡常数计算式,K=
=2,则Ni(CO) 的平衡浓度为2mol/L,故C正确;
4
D.25℃时反应Ni(CO) (g) Ni(s)+4CO(g)的平衡常数为Ni(s)+4CO(g) Ni(CO) (g),平衡常数的倒
4 4
数═ =2×10−5,故D 正确;
故答案为B。
10.(成都七中2020届高三考前热身考试)某小组探究实验条件对反应速率的影响,设计如下实验,并记录
结果如下:
编号 温度 HSO 溶液 KI溶液 1%淀粉溶液体 出现蓝色时间
2 4积
① 20℃ 0.10 mol·L−110 mL 0.40 mol·L−1 5 mL 1mL 40 s
② 20℃ 0.10 mol·L−110 mL 0.80 mol·L−1 5 mL 1mL 21 s
③ 50℃ 0.10 mol·L−110 mL 0.40 mol·L−1 5 mL 1mL 5s
④ 80℃ 0.10 mol·L−110 mL 0.40 mol·L−1 5 mL 1mL 未见蓝色
下列说法正确的是
A.由实验①②可知,反应速率v与c(I−)成正比
B.实验①−④中,应将HSO 溶液与淀粉溶液先混合
2 4
C.在I−被O 氧化过程中,H+只是降低活化能
2
D.由实验③④可知,温度越高,反应速率越慢
【答案】A
【解析】
【分析】反应速率与温度、浓度、催化剂等有关,温度越高反应速率越快,浓度越大反应速率越快,催化
剂能降低反应的活化能,加快反应速率。
【详解】A.实验①②中其它条件相同,c(I−):①<②,且反应速率:①<②,所以反应速率v与c(I−)成正
比,A正确;
B.实验①−④中,应将KI溶液与淀粉溶液先混合,再加入HSO 溶液,在酸性条件下发生氧化还原反应
2 4
生成碘单质,测定溶液变色的时间,B错误;
C.在I−被O 氧化过程中,H+除了作为催化剂降低活化能,还作为反应物参加反应,C错误;
2
D.由实验④温度越高,生成的碘单质能被氧气继续氧化,所以④不变色, D错误。
答案选A。
11.(杭州高级中学2020届高三仿真模拟)在容积为2L的刚性密闭容器中加入1molCO 和3molH ,发生反
2 2
应:CO(g)+3H(g) CHOH(g)+H O(g)。在其他条件不变的情况下,温度对反应的影响如图所示(注:
2 2 3 2
T、T 均大于300℃)。下列说法正确的是( )
1 2
A.该反应在T 时的平衡常数比在T 时的小
1 2B.处于A点的反应体系从T 变到T,达到平衡时 减小
1 2
C.T 时,反应达到平衡时生成甲醇的反应速率v(CHOH)= mol·L−1·min−1
2 3
D.T 时,若反应达到平衡后CO 的转化率为x,则容器内的压强与起始压强之比为(2−x)∶2
1 2
【答案】D
【解析】A.图象分析可知先拐先平温度高,T<T,温度越高平衡时生成甲醇物质的量越小,说明正反
1 2
应为放热反应,则温度越高,平衡常数越小,该反应在T 时的平衡常数比T 时的大,故A错误;
1 2
B.分析可知T<T,A点反应体系从T 变到T,升温平衡逆向进行,达到平衡时 增大,故B
1 2 1 2
错误;
C.T 下达到平衡状态甲醇物质的量n ,反应达到平衡时生成甲醇的平均速率为v(CHOH)= mol•L﹣
2 B 3
1•min﹣1,故C错误;
D.T 下,若反应达到平衡后CO 转化率为x,则
1 2
则容器内的压强与起始压强之比= ,故D正确;答案选D。
12.(杭州高级中学2020届高三仿真模拟)25℃,向40mL0.05mol/L的FeCl 溶液中加入10mL0.15mol/L的
3
KSCN溶液,发生反应:Fe3++3SCN− Fe(SCN) ,混合溶液中c(Fe3+)与反应时间(t)的变化如图所示。(盐
3
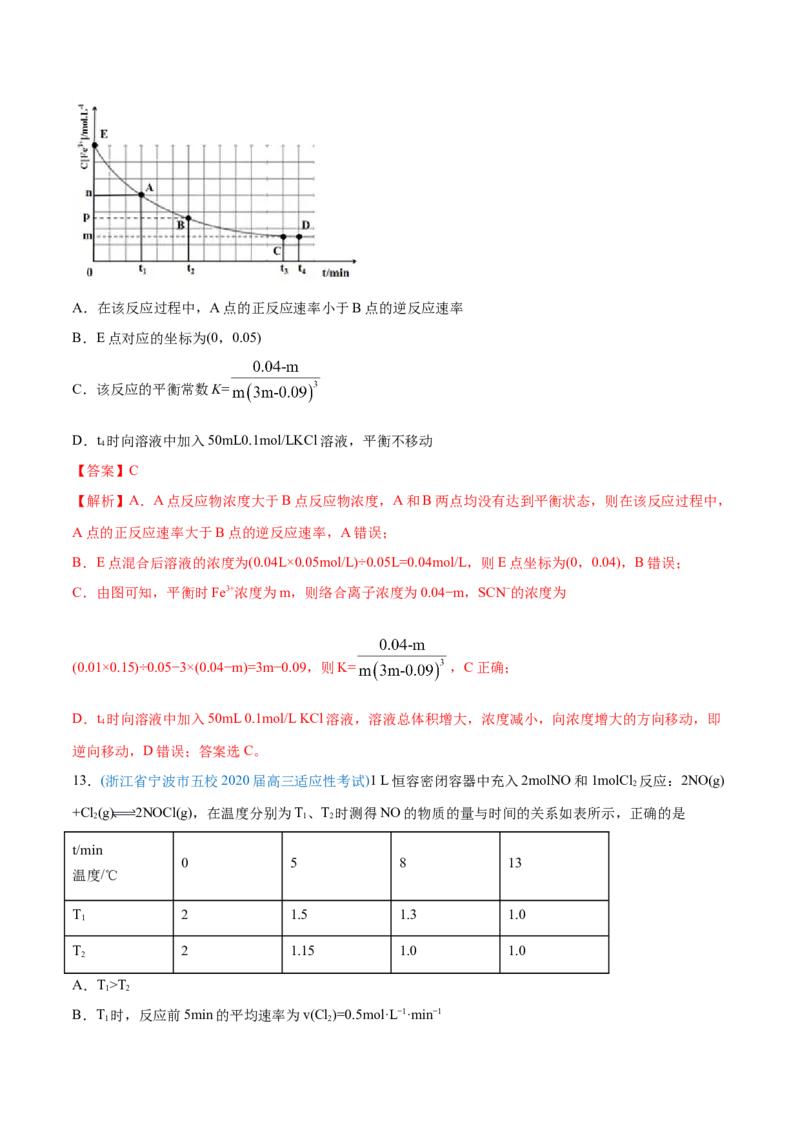
类的水解影响忽略不计)下列说法正确的是( )A.在该反应过程中,A点的正反应速率小于B点的逆反应速率
B.E点对应的坐标为(0,0.05)
C.该反应的平衡常数K=
D.t 时向溶液中加入50mL0.1mol/LKCl溶液,平衡不移动
4
【答案】C
【解析】A.A点反应物浓度大于B点反应物浓度,A和B两点均没有达到平衡状态,则在该反应过程中,
A点的正反应速率大于B点的逆反应速率,A错误;
B.E点混合后溶液的浓度为(0.04L×0.05mol/L)÷0.05L=0.04mol/L,则E点坐标为(0,0.04),B错误;
C.由图可知,平衡时Fe3+浓度为m,则络合离子浓度为0.04−m,SCN−的浓度为
(0.01×0.15)÷0.05−3×(0.04−m)=3m−0.09,则K= ,C正确;
D.t 时向溶液中加入50mL 0.1mol/L KCl溶液,溶液总体积增大,浓度减小,向浓度增大的方向移动,即
4
逆向移动,D错误;答案选C。
13.(浙江省宁波市五校2020届高三适应性考试)1 L恒容密闭容器中充入2molNO和1molCl 反应:2NO(g)
2
+Cl(g) 2NOCl(g),在温度分别为T、T 时测得NO的物质的量与时间的关系如表所示,正确的是
2 1 2
t/min
0 5 8 13
温度/℃
T 2 1.5 1.3 1.0
1
T 2 1.15 1.0 1.0
2
A.T>T
1 2
B.T 时,反应前5min的平均速率为v(Cl )=0.5mol·L−1·min−1
1 2C.反应达平衡时,升高温度促进反应向正反应方向进行
D.T 时,向反应后的容器中充入2molNOCl(g),再次平衡时,c(NOCl)>2mol·L−1
2
【答案】D
【解析】A.其他条件一定下,温度越高,化学反应速率越快。根据表格中的数据,单位时间内,T 温度
2
下,NO的反应速率快,因此T2mol·L−1,D正确;
答案选D。
14.(北京大学附中2020届高三化学阶段性测试)反应 2SiHCl (g) SiHCl(g) + SiCl (g)在催化剂作用下,
3 2 2 4
于323 K 和 343 K 时充分反应,SiHCl 的转化率随时间变化的结果如图所示:
3
下列说法不正确的是
A.343 K 时反应物的平衡转化率为 22%
B.a、b 处反应速率大小:v>v
a b
C.要提高 SiHCl 转化率,可采取的措施是降温和及时移去反应产物
3D.已知反应速率 ,k 、k 分别为正、逆反应速率常数,x为物质
正 逆
的量分数,则 343 K 时
【答案】C
【解析】
【分析】由图示,温度越高反应速率越快,达到平衡用得时间就越少,所以曲线a代表343K的反应,曲
线b代表323K的反应;要提高反应物的转化率,就需要使平衡向右移动,从此角度出发进行分析;根据
转化率列出三段式,再利用达到平衡时正反应速率等于逆反应速率,进行相关的计算。
【详解】A.由图示,温度越高反应速率越快,达到平衡用得时间就越少,所以曲线a代表343K的反应,
从图中读出343 K 时反应物的平衡转化率为 22%,A正确;
B.a、b两点的转化率相等,可以认为各物质的浓度对应相等,而a点的温度更高,所以速率更快,即v
a
>v,B正确;
b
C.由图可知,温度越高转化率越大,减少生成物,根据勒夏特列原理,平衡正向移动,则转化率增大,
所以要提高SiHCl 转化率,可采取的措施是升温和及时移去反应产物,C错误;
3
D.假设开始时SiHCl 的物质的量浓度为cmol/L,343 K 时反应物的平衡转化率为 22%,则有:
3
, ,
已知反应速率 ,平衡时v =v ,则有 ,所
正 逆以 ,D正确。
答案选C。
15.(江苏省七市2020届高三第二次调研)温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭
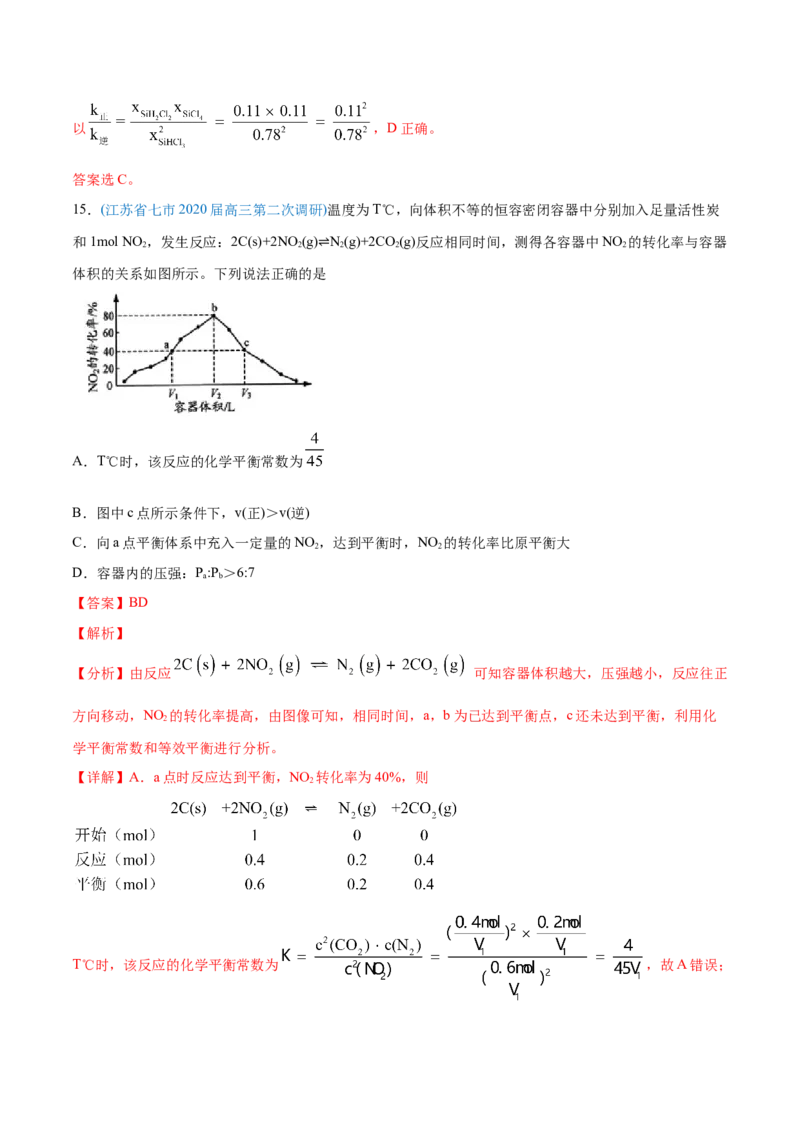
和1mol NO ,发生反应:2C(s)+2NO (g) N(g)+2CO (g)反应相同时间,测得各容器中NO 的转化率与容器
2 2 2 2 2
体积的关系如图所示。下列说法正确的是⇌
A.T℃时,该反应的化学平衡常数为
B.图中c点所示条件下,v(正)>v(逆)
C.向a点平衡体系中充入一定量的NO ,达到平衡时,NO 的转化率比原平衡大
2 2
D.容器内的压强:P:P >6:7
a b
【答案】BD
【解析】
【分析】由反应 可知容器体积越大,压强越小,反应往正
方向移动,NO 的转化率提高,由图像可知,相同时间,a,b为已达到平衡点,c还未达到平衡,利用化
2
学平衡常数和等效平衡进行分析。
【详解】A.a点时反应达到平衡,NO 转化率为40%,则
2
T℃时,该反应的化学平衡常数为 ,故A错误;B.图中c点还未达到平衡,反应往正方向进行,v(正)>v(逆),故B正确;
C.向a点平衡体系中充入一定量的NO ,等效于加压,平衡逆移,转化率降低,C错误;
2
D.由A可知a点时容器内气体物质的量为1.2mol;b点时反应三段式为
则b点容器内气体物质的量为1.4mol,由于V<V,则P:P >6:7,故D正确;
1 2 a b
故答案选:BD。
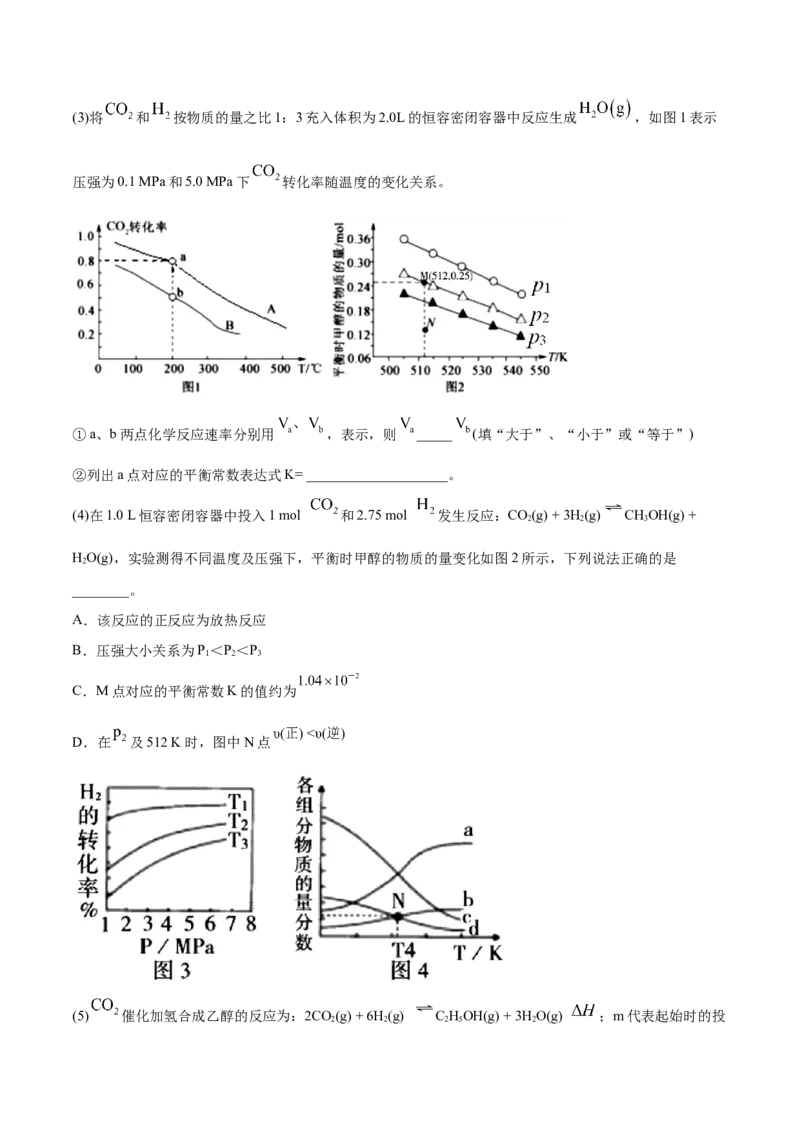
16.(泰安市肥城市2020届高三适应性训练一)利用传感技术可以探究压强对2NO (g) NO(g)化学平衡
2 2 4
移动的影响。在室温、100kPa条件下,往针筒中充入一定体积的NO 气体后密封并保持活塞位置不变。分
2
别在t、t 时刻迅速移动活塞并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列说法正确的是
1 2
( )
A.B点处NO 的转化率为3%
2
B.E点到H点的过程中,NO 的物质的量先增大后减小
2
C.E、H两点对应的正反应速率大小为v >v
H E
D.B、E两点气体的平均相对分子质量大小为M >M
B E
【答案】CD
【解析】A.由图可知B点处压强为97KPa,设起始二氧化氮为1mol,转化率为a,由题意建立如下三段
式:
由 可得 ,解得a=0.06,即二氧化氮的转化率为6%,故A错误;B.由图可知,t 时刻移动了活塞,压强迅速增大,说明迅速移动活塞使针筒体积减小,并保持活塞位置不
2
变后,体系因体积减小而压强增大,平衡向生成四氧化二氮的方向移动,则E点到H点的过程中,二氧化
氮的物质的量是一个减小过程,故B错误;
C.对于有气体参加的反应,压强越大反应速率越大,由图可知,H点压强大于E点,则反应速率v >
H
v ,故C正确;
E
D.由图可知,B到E的过程为压强减小的过程,减小压强平衡向生成二氧化氮的方向移动,气体的物质
的量增大,由质量守恒定律可知气体质量不变,则混合气体的平均相对分子质量减小,即M >M ,故D
B E
正确;故选CD。
17.(宁夏大学附属中学2020届高三第五次模拟)“绿水青山就是金山银山”,近年来,绿色发展、生态保
护成为中国展示给世界的一张新“名片”。
(I)汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
请回答下列问题:
(1)已知:
若某反应的平衡常数表达式为 ,则此反应的热化学方程式为_______。
(2) 在一定条件下可发生分解: ,一定温度下,在恒容密闭容器中充入一
定量 进行该反应,能判断反应已达到化学平衡状态的是_____(填字母)。
A. 和 的浓度比保持不变 B.容器中压强不再变化
C. D.气体的密度保持不变
(Ⅱ)甲醇、乙醇来源丰富、价格低廉、运输贮存方便,都是重要的化工原料,有着重要的用途和应用前景,
可以用多种方法合成。 CO(g) + 3H(g) CHOH(g) + H O(g)
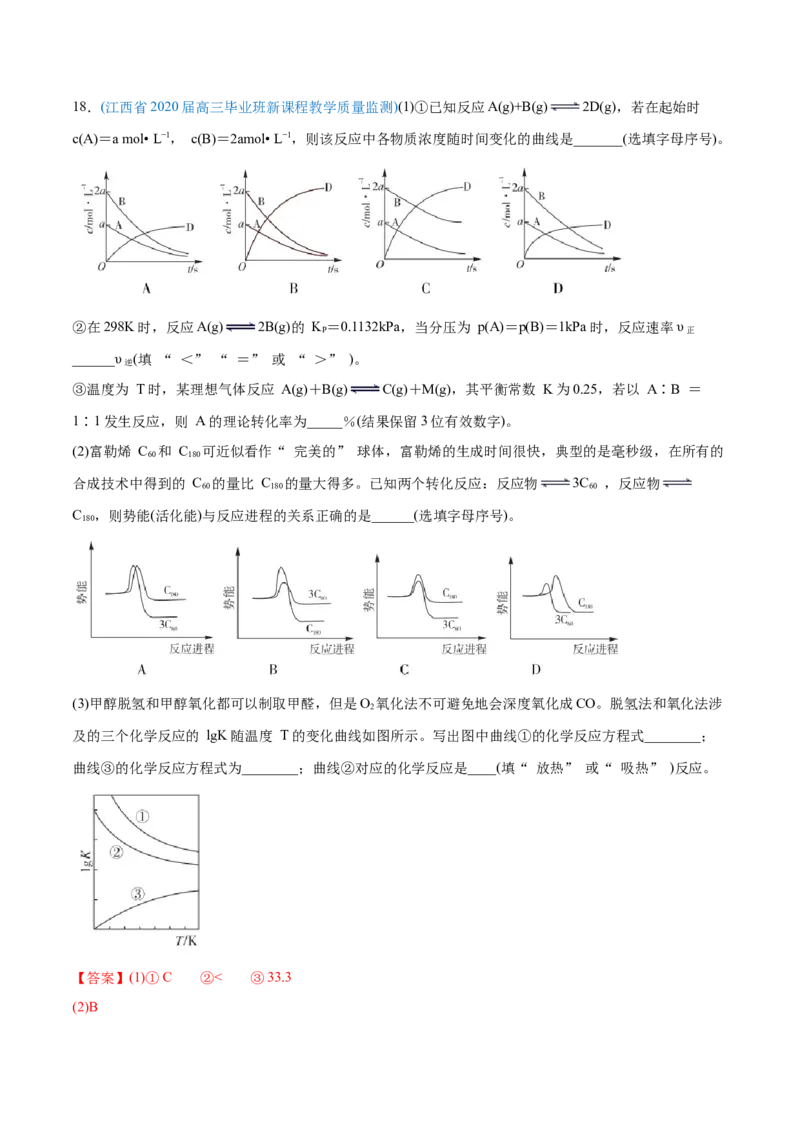
2 2 3 2(3)将 和 按物质的量之比1:3充入体积为2.0L的恒容密闭容器中反应生成 ,如图1表示
压强为0.1 MPa和5.0 MPa下 转化率随温度的变化关系。
①a、b两点化学反应速率分别用 ,表示,则 _____ (填“大于”、“小于”或“等于”)
②列出a点对应的平衡常数表达式K= ____________________。
(4)在1.0 L恒容密闭容器中投入1 mol 和2.75 mol 发生反应:CO(g) + 3H(g) CHOH(g) +
2 2 3
HO(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是
2
________。
A.该反应的正反应为放热反应
B.压强大小关系为P<P<P
1 2 3
C.M点对应的平衡常数K的值约为
D.在 及512 K时,图中N点
(5) 催化加氢合成乙醇的反应为:2CO(g) + 6H(g) C HOH(g) + 3H O(g) ;m代表起始时的投
2 2 2 5 2料比,即 。
①图3中投料比相同,温度 ,则该反应的焓变 _______0(填 )。
②m=3时,恒压条件下各物质的物质的量分数与温度的关系如图4所示,则曲线b代表的物质为
_________(填化学式)。
(6)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图5所示。离子交换膜a为 ______(填“阳
膜”、“阴膜”),阳极的电极反应式为_______________________________________
【答案】Ⅰ.(1)
(2)B
Ⅱ.(3)①大于 ② (4)AC
(5)①< ②CO
2
(6)阳膜
【解析】
【分析】根据平衡常数的计算表达式书写化学方程式,利用盖斯定律计算反应的ΔH,根据判断条件是否
为“变量”判断反应是否达到平衡,根据影响化学反应速率的因素比较化学反应速率大小,结合图像列三
段式进行平衡常数的计算,根据电解池原理进行解答。
【详解】Ⅰ.(1)某反应的平衡常数表达式为 ,发生反应为根据盖斯定律,②×2−③−①得出: ;
(2)A.NO 和O 的浓度比始终都不变,不能确定反应是否达到化学平衡状态,a错误;
2 2
B.该反应为气体体积增大的反应,压强为变量,容器中压强不再变化,说明各组分的浓度不再变化,反
应已达到化学平衡状态,b正确;
C.应为v (NO )=2v (N O)才表明达到化学平衡状态,c错误;
正 2 逆 2 5
D.该反应前后都是气体,气体总质量、气体体积为定值,则密度为定值,不能根据密度判断平衡状态,d
错误;答案选b;
Ⅱ.(3)a、b两点温度相同,正反应为气体体积减小的反应,增大压强平衡正向移动,二氧化碳转化率增大,
故压强曲线A大于曲线B,压强越大反应速率越快,故反应速率V大于V;
a b
(4)A.由图可知,随着温度升高,平衡时甲醇的物质的量在减小,所以升温平衡向逆反应方向移动,则正
反应为放热反应,故A正确;
B.由图可知,作一条等温线,因为该反应为气体体积减小的反应,压强越大,平衡时甲醇的物质的量也
越大,所以P<P<P,故B错误;
1 2 3
C.由图可知,M点对应的甲醇产量为0.25mol,则
所以K= =1.04×10−2;故C正确;
D.由图可知,在p 及512K时,N点甲醇的物质的量还小于平衡时的量,所以应该正向移动,则v >v ,
2 (正) (逆)
故D错误;
答案选AC;
(5)①由图3可知,相同压强下,温度越高氢气转化率越小,说明升高温度反应向逆向移动,正反应放热,
△H<0;
②温度升高,反应逆向进行,所以产物的物质的量是逐渐减少的,反应物的物质的量增大,由图可知,根
据反应计量系数关系,曲线a代表的物质为H,b表示CO,c为HO,d为C HOH;
2 2 2 2 5
(6)由图分析可知氧气得电子,发生还原反应,与氢离子结合生成水,该电极为阴极,则氢离子要透过交换
膜a在阴极与氧气结合,则交换膜a为阳离子交换膜;阳极上是甲醇和一氧化碳反应失电子发生氧化反应,
电极反应为:2CHOH+CO−2e−=(CH O) CO+2H+。
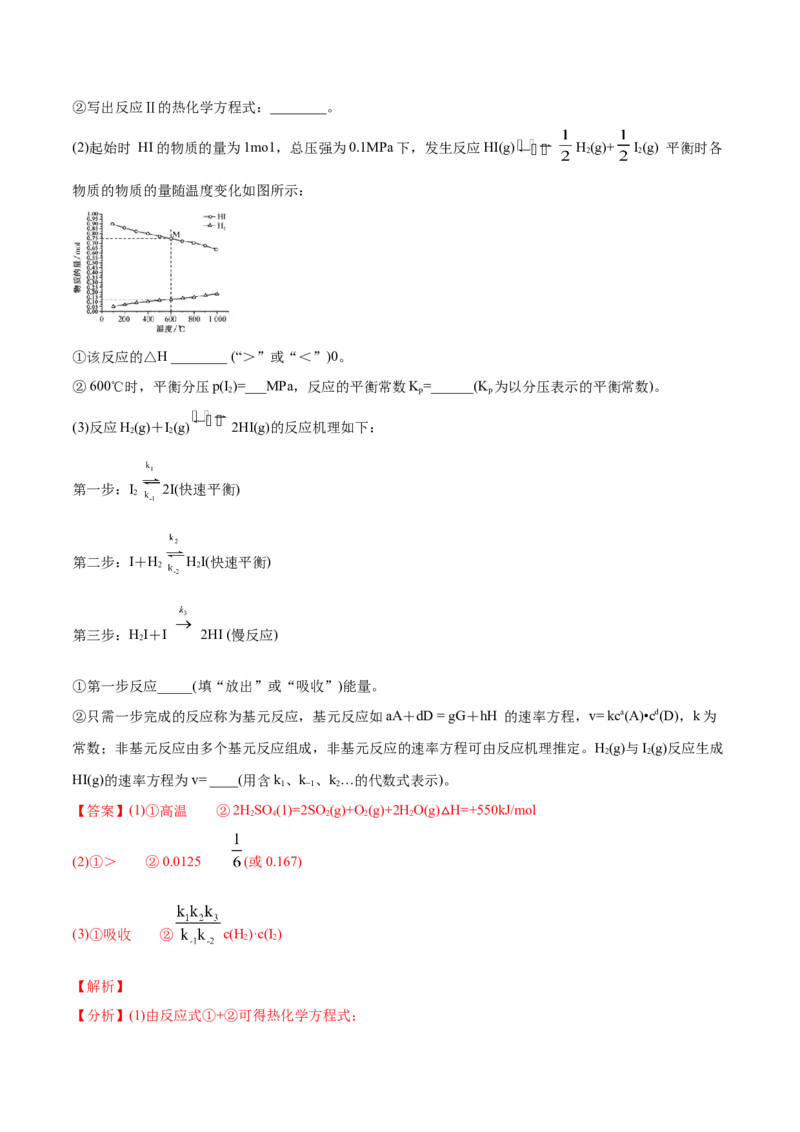
3 3 218.(江西省2020届高三毕业班新课程教学质量监测)(1)①已知反应A(g)+B(g) 2D(g),若在起始时
c(A)=a mol• L−1, c(B)=2amol• L−1,则该反应中各物质浓度随时间变化的曲线是_______(选填字母序号)。
②在298K时,反应A(g) 2B(g)的 K =0.1132kPa,当分压为 p(A)=p(B)=1kPa时,反应速率υ
P 正
______υ (填 “ <” “ =” 或 “ >” )。
逆
③温度为 T时,某理想气体反应 A(g)+B(g) C(g)+M(g),其平衡常数 K为0.25,若以 A∶B =
1∶1发生反应,则 A的理论转化率为_____%(结果保留3位有效数字)。
(2)富勒烯 C 和 C 可近似看作“ 完美的” 球体,富勒烯的生成时间很快,典型的是毫秒级,在所有的
60 180
合成技术中得到的 C 的量比 C 的量大得多。已知两个转化反应:反应物 3C ,反应物
60 180 60
C ,则势能(活化能)与反应进程的关系正确的是______(选填字母序号)。
180
(3)甲醇脱氢和甲醇氧化都可以制取甲醛,但是O 氧化法不可避免地会深度氧化成CO。脱氢法和氧化法涉
2
及的三个化学反应的 lgK随温度 T的变化曲线如图所示。写出图中曲线①的化学反应方程式________;
曲线③的化学反应方程式为________;曲线②对应的化学反应是____(填“ 放热” 或“ 吸热” )反应。
【答案】(1)①C ②< ③33.3
(2)B(3)2HCHO(g)+O(g)=2CO(g)+2HO(g) CH OH(g)=HCHO(g)+H (g) 放热
2 2 3 2
【解析】(1)①已知反应A(g)+B(g) 2D(g),根据化学反应速率跟化学计量数成正比可知,A、B减少的
量相等,同时生成2倍的D,故曲线C符号该反应中各物质浓度随时间变化,答案为:C;
②在298K时,当分压为 p(A)=p(B)=1kPa时,反应A(g) 2B(g)的Q=(1kPa)2÷1kPa=1kPa>K,则反应
p
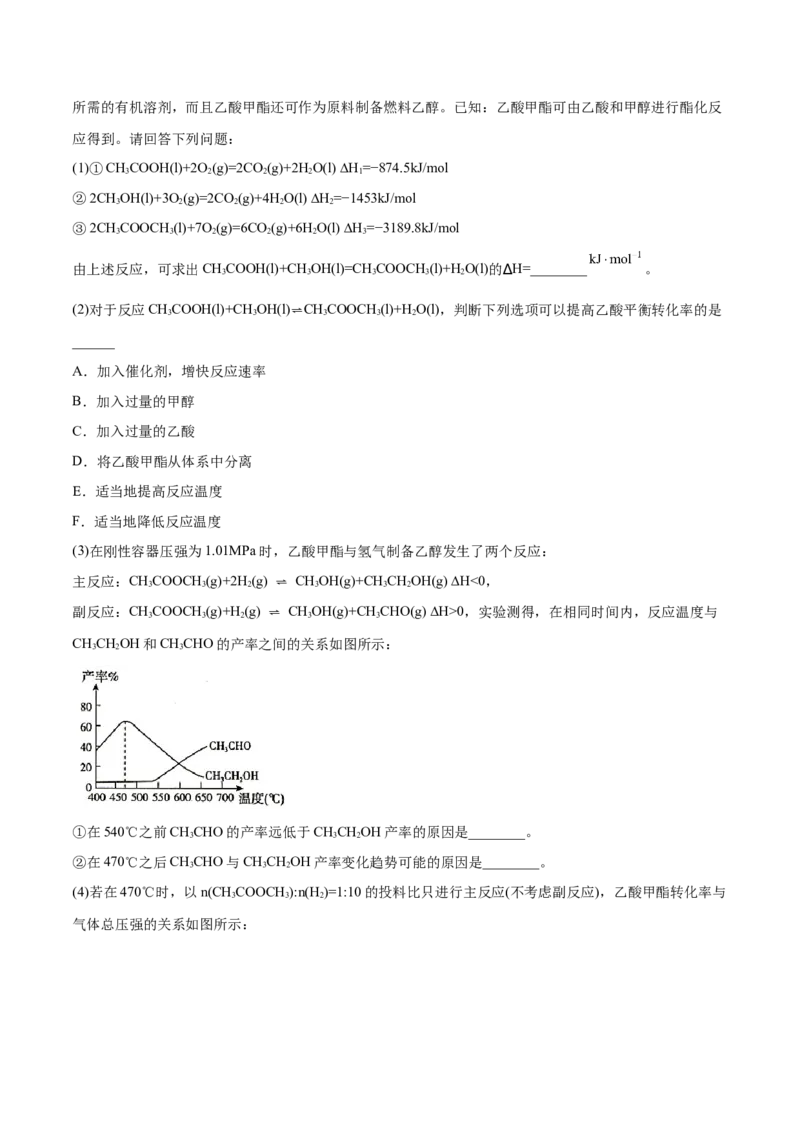
向逆反应方向进行,v 0
4 8 2 4 4 8 2 4 3 6
①某温度下,上述反应中,正反应速率为v =K c(C H)∙c(⇌C H)、逆反应速率为v =K c2(C H),其中K
正 正 4 8 2 4 逆 逆 3 6
、K 为速率常数,该反应使用WO/SiO 为催化剂,下列说法中正确的是_____________
正 逆 3 2
A.催化剂参与了歧化反应,但不改变反应历程
B.催化剂使K 和K 增大相同的倍数
正 逆
C.催化剂降低了烯烃歧化反应的活化能,增大了活化分子百分数
D.速率常数的大小与反应程度无关系
②已知tmin时达到平衡状态,测得此时容器中n(C H)=amol,n(C H)=2amol,n(C H)=bmol,且平衡时
1 4 8 2 4 3 6
C H 的体积分数为25%。再往容器内通入等物质的量的C H 和C H,在新平衡中C H 的体积分数
3 6 4 8 2 4 3 6
___________25%(填“>”、“<”、“=”)。
(3)工业上可用丙烯加成法制备1,2−二氯丙烷(CHClCHClCH ),主要副产物为3−氯丙烯(CH=CHCHCl),
2 3 2 2
反应原理为:
Ⅰ. CH=CHCH(g)+Cl (g) CHClCHClCH (g)
2 3 2 2 3
⇌II. CH =CHCH(g)+Cl (g) CH=CHCHCl(g)+HCl(g)
2 3 2 2 2
一定温度下,向恒容密闭⇌容器中充入等物质的量的CH
2
=CHCH
3
(g)和Cl
2
(g)。在催化剂作用下发生反应Ⅰ,
容器内气体的压强随时间的变化如表所示。
时间/min 0 60 120 180 240 300 360
压强/kPa 80 74.2 69.2 65.2 61.6 57.6 57.6
①用单位时间内气体分压的变化来表示反应速率,即 ,则前120min内平均反应速率
v(CHClCHClCH )=____________kPa∙min−1。
2 3
②该温度下,若平衡时HCl的体积分数为12.5%,反应Ⅰ的平衡常数K=__________kPa−1(K 为以分压表示
p p
的平衡常数,保留小数点后2位)。
【答案】(1)+124.2 ①升高温度
②丙烷直接裂解是吸热反应,通入足量O 可提供裂解所需的能量,并保持热平衡
2
(2)①BCD ②>
(3)①0.09 ②0.21
【解析】
【分析】I.(1)结合图像及盖斯定律进行计算;
①反应为吸热反应,升高温度,反应速率增大和平衡正向移动;
②通入足量O 可与裂解产生的氢气反应,提供裂解所需的能量,并保持热平衡;
2
(2)①A.催化剂参与了歧化反应,生成了中间产物,即改变反应历程;
B.催化剂导致反应速率增大,但化学平衡常数不变,则使K 和K 增大相同的倍数;
正 逆
C.催化剂导致反应速率增大,则降低了烯烃歧化反应的活化能,增大了活化分子百分数;
D.根据公式,速率常数的大小与反应的始态或终态有关,与反应程度无关系;
②Qc与K的关系判断;
II.利用三段式及反应速率的公式进行计算。
【详解】(1)根据左图,可得①C H(g) C H(g)+H(g)+CH (g) ∆H=+156.6kJ/mol,右图可得,②C H(g)
3 8 2 2 2 4 3 6
C H(g)+CH (g) ∆H=+32.4kJ/mol,根据⇌盖斯定律,①−②可得C H(g) C H(g)+H(g),则 ⇌
2 2 4 3 8 3 6 2
∆H=+124.2kJ/mol; ⇌
①该反应为吸热反应,升高温度,可同时提高反应速率和反应物的平衡转化率;
②丙烷直接裂解是吸热反应,通入足量O 可与裂解产生的氢气反应,提供裂解所需的能量,并保持热平衡;
2
(2)①A.催化剂参与了歧化反应,生成了中间产物,即改变反应历程,说法错误,A错误;B.催化剂导致反应速率增大,但化学平衡常数不变,则使K 和K 增大相同的倍数,说法正确,B正确;
正 逆
C.催化剂导致反应速率增大,且不影响反应的焓变,则降低了烯烃歧化反应的活化能,增大了活化分子
百分数,说法正确,C正确;
D.根据公式,速率常数的大小与反应的始态或终态有关,与反应程度无关系,说法正确,D正确;
答案为BCD;
②已知平衡时,n(C H)=amol,n(C H)=2amol,n(C H)=bmol,且平衡时C H 的体积分数为25%,
4 8 2 4 3 6 3 6
=25%,则b=amol,K=0.5;再往容器内通入等物质的量的C H 和C H,化学平衡常数不变,
4 8 2 4
则Qc= (x>0),(1+x)(2+x)>2,Qc0,实验测得,在相同时间内,反应温度与
CHCHOH和CHCHO的产率之间的关系如图所示:
3 2 3
①在540℃之前CHCHO的产率远低于CHCHOH产率的原因是________。
3 3 2
②在470℃之后CHCHO与CHCHOH产率变化趋势可能的原因是________。
3 3 2
(4)若在470℃时,以n(CHCOOCH ):n(H)=1:10的投料比只进行主反应(不考虑副反应),乙酸甲酯转化率与
3 3 2
气体总压强的关系如图所示:①A点时,CHCOOCH (g)的平衡分压为________MPa,CHCHOH(g)的体积分数________%(保留一位小
3 3 3 2
数)。
②470℃时,该反应的化学平衡常数K=________(MPa)−1(K 为以分压表示的平衡常数,列出计算式,不要
p p
求计算结果)。
【答案】(1)−6.1kJ∙mol−1
(2)BDF
(3)①副反应的活化能远大于主反应的活化能,副反应的化学反应速慢
②470℃之后,乙醇的产率逐渐降低是该反应是放热反应,温度升高平衡逆向移动,乙醛的产率逐渐升高
是反应速率逐渐加快,反应吸热平衡正向移动
(4)①0.01MPa 8.9 ②
【解析】(1)依据热化学方程式和盖斯定律,①+ ②− ③可得到CHCOOH(l)+CH OH(l)=CH COOCH (l)
3 3 3 3
+H O(l),则∆H=∆H + ∆H − ∆H =−6.10 kJ∙mol−1。
2 1 2 3
(2)A.加入催化剂,增快反应速率,并不会影响平衡移动,A项错误;
B.加入过量的甲醇,增大了反应物浓度,使平衡正向移动,乙酸的转化率增大,B项正确;
C.加人过量的乙酸,增大了反应物浓度,虽然使平衡正向移动,但乙酸的转化率降低,C项错误;
D.将乙酸甲酯从体系中分离,使产物减少,促进平衡正向移动,乙酸的转化率增大,D项正确;
E.根据∆H为负值,反应正向是放热反应,因此,适当降低温度,平衡正向移动,乙酸的转化率增大,E项
错误,F项正确;
综上所述,答案为BDF。
(3)①两反应快慢的核心是活化能的大小,反应快活化能小,而反应慢活化能大,根据图像可知,副反应的活
化能远大于主反应的活化能,副反应的化学反应速慢;
②470℃之后,乙醇的产率逐渐降低是该反应是放热反应,温度升高平衡逆向移动,乙醛的产率逐渐升高
是反应速率逐渐加快,反应吸热平衡正向移动。
(4)①由图可看出,转化率为90%时,总压为1.01MPa,已知n(CHCOOCH ):n(H)=1:10,列三行式求解:
3 3 2总压为1.01MPa,因此CHCOOCH (g)的平衡分压为 ;
3 3
CHCHOH(g)的体积分数即为物质的量分数,其体积分数 ;
3 2
② 。