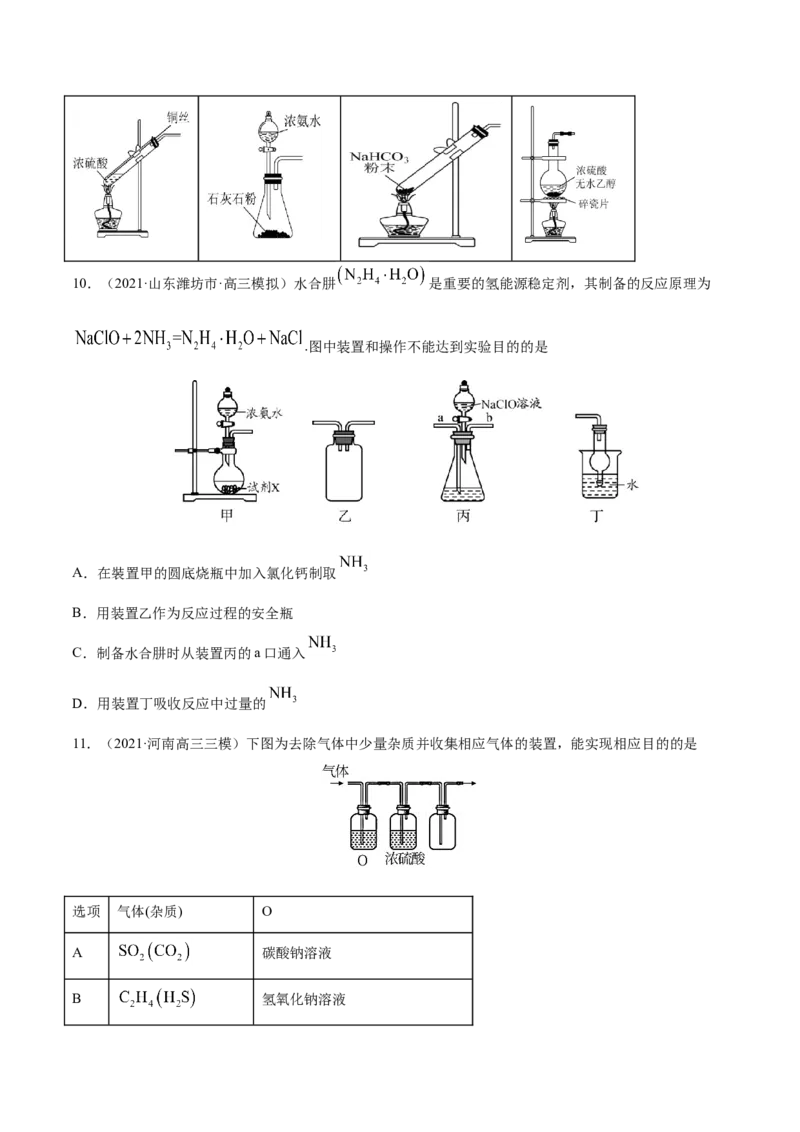
文档内容
专题 11 化学实验基础
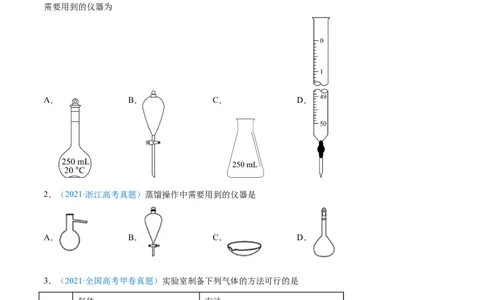
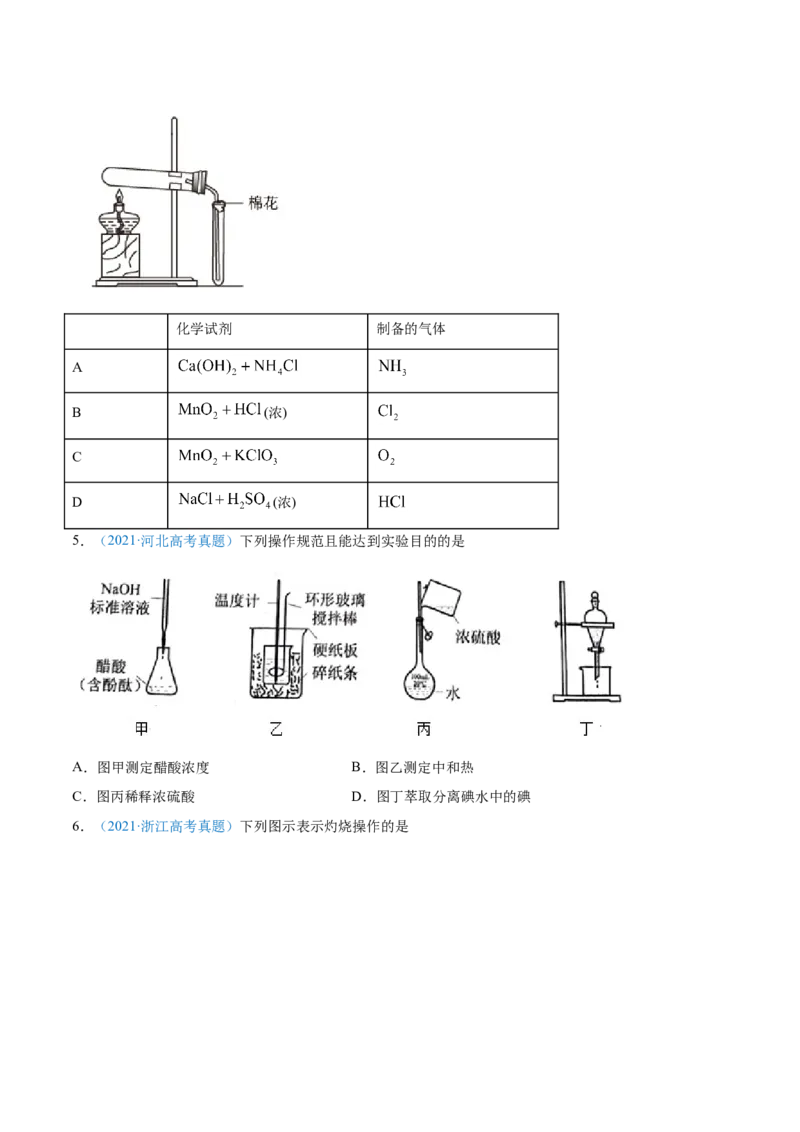
1.(2021·广东高考真题)测定浓硫酸试剂中 含量的主要操作包括:①量取一定量的浓硫酸,稀释;
②转移定容得待测液;③移取 待测液,用 的 溶液滴定。上述操作中,不
需要用到的仪器为
A. B. C. D.
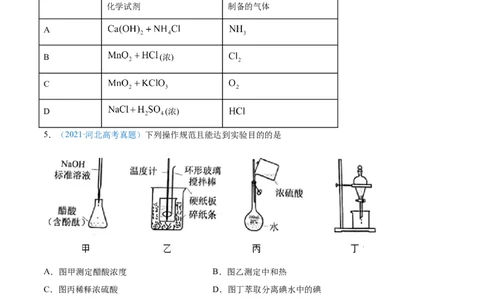
2.(2021·浙江高考真题)蒸馏操作中需要用到的仪器是
A. B. C. D.
3.(2021·全国高考甲卷真题)实验室制备下列气体的方法可行的是
气体 方法
A 氨气 加热氯化铵固体
B 二氧化氮 将铝片加到冷浓硝酸中
C 硫化氢 向硫化钠固体滴加浓硫酸
D 氧气 加热氯酸钾和二氧化锰的混合物
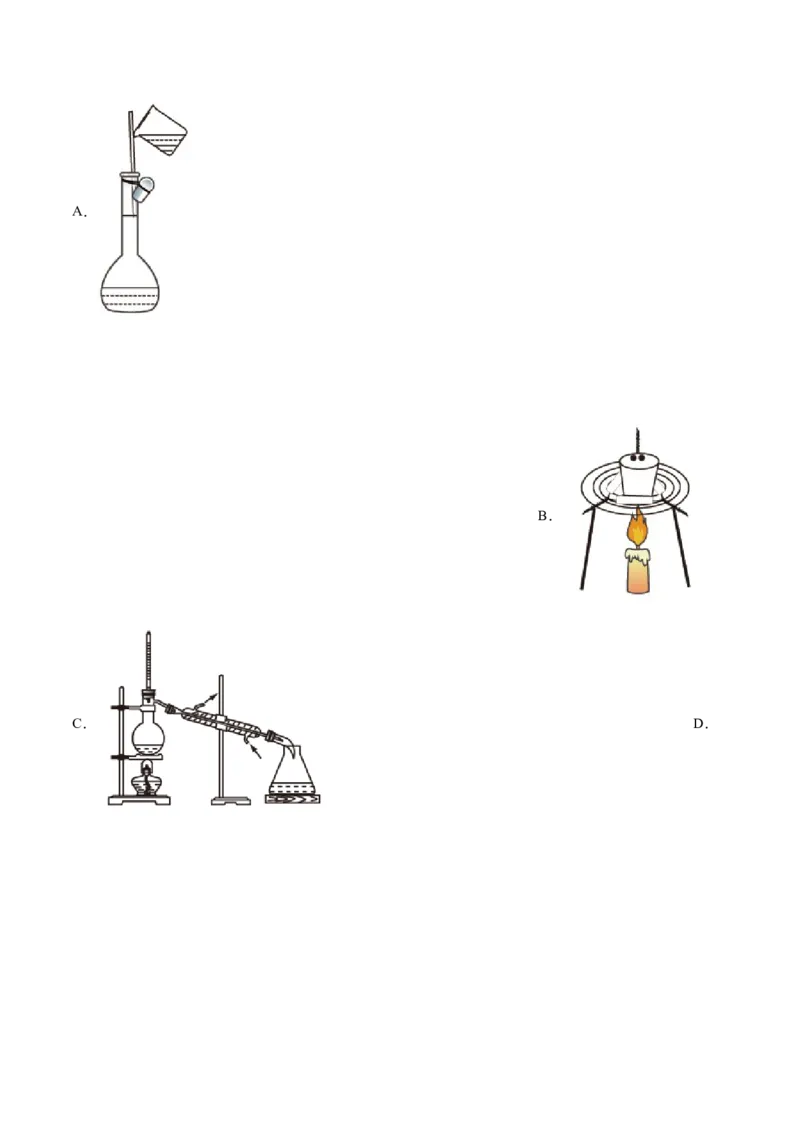
4.(2021·全国高考乙卷真题)在实验室采用如图装置制备气体,合理的是化学试剂 制备的气体
A
B (浓)
C
D (浓)
5.(2021·河北高考真题)下列操作规范且能达到实验目的的是
A.图甲测定醋酸浓度 B.图乙测定中和热
C.图丙稀释浓硫酸 D.图丁萃取分离碘水中的碘
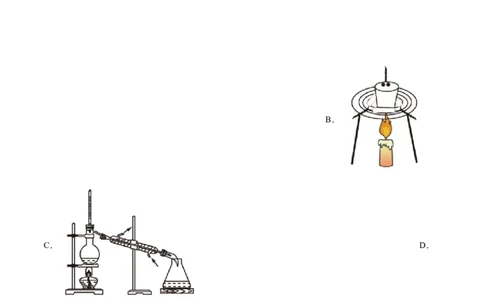
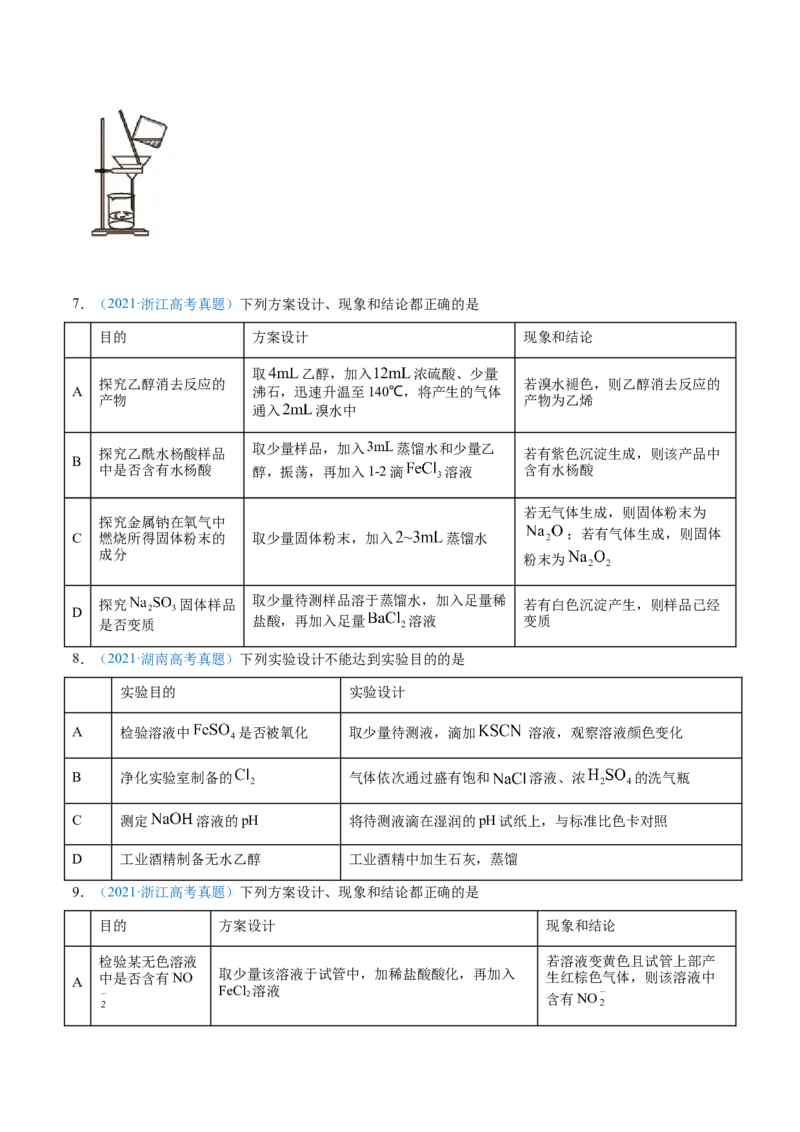
6.(2021·浙江高考真题)下列图示表示灼烧操作的是A.
B.
C. D.7.(2021·浙江高考真题)下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
取 乙醇,加入 浓硫酸、少量
探究乙醇消去反应的 若溴水褪色,则乙醇消去反应的
A 沸石,迅速升温至140℃,将产生的气体
产物 产物为乙烯
通入 溴水中
取少量样品,加入 蒸馏水和少量乙
探究乙酰水杨酸样品 若有紫色沉淀生成,则该产品中
B
中是否含有水杨酸 醇,振荡,再加入1-2滴 溶液 含有水杨酸
若无气体生成,则固体粉末为
探究金属钠在氧气中
;若有气体生成,则固体
C 燃烧所得固体粉末的 取少量固体粉末,加入 蒸馏水
成分
粉末为
取少量待测样品溶于蒸馏水,加入足量稀
探究 固体样品 若有白色沉淀产生,则样品已经
D
是否变质 盐酸,再加入足量 溶液 变质
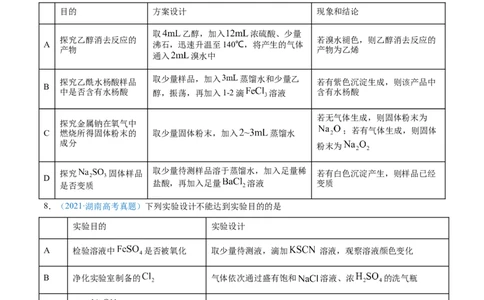
8.(2021·湖南高考真题)下列实验设计不能达到实验目的的是
实验目的 实验设计
A 检验溶液中 是否被氧化 取少量待测液,滴加 溶液,观察溶液颜色变化
B 净化实验室制备的 气体依次通过盛有饱和 溶液、浓 的洗气瓶
C 测定 溶液的pH 将待测液滴在湿润的pH试纸上,与标准比色卡对照
D 工业酒精制备无水乙醇 工业酒精中加生石灰,蒸馏
9.(2021·浙江高考真题)下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
检验某无色溶液 若溶液变黄色且试管上部产
中是否含有NO 取少量该溶液于试管中,加稀盐酸酸化,再加入 生红棕色气体,则该溶液中
A
FeCl 溶液
2 含有NO取5 mL 0.1 mol·L-1KI溶液于试管中,加入1 mL
探究KI与FeCl 若溶液变血红色,则KI与
B 3 0.1 mol·L-1 FeCl 溶液,充分反应后滴入5滴15%
反应的限度 3 FeCl 的反应有一定限度
KSCN溶液 3
判断某卤代烃中 取2 mL卤代烃样品于试管中,加入5 mL 20% 若产生的沉淀为白色,则该
C
的卤素 KOH水溶液混合后加热,再滴加AgNO 溶液 卤代烃中含有氯元素
3
探究蔗糖在酸性 取2mL20%的蔗糖溶液于试管中,加入适量稀
若没有生成砖红色沉淀 ,则
D 水溶液中的稳定 HSO 后水浴加热5 min;再加入适量新制Cu(OH)
2 4 2 蔗糖在酸性水溶液中稳定
性 悬浊液并加热
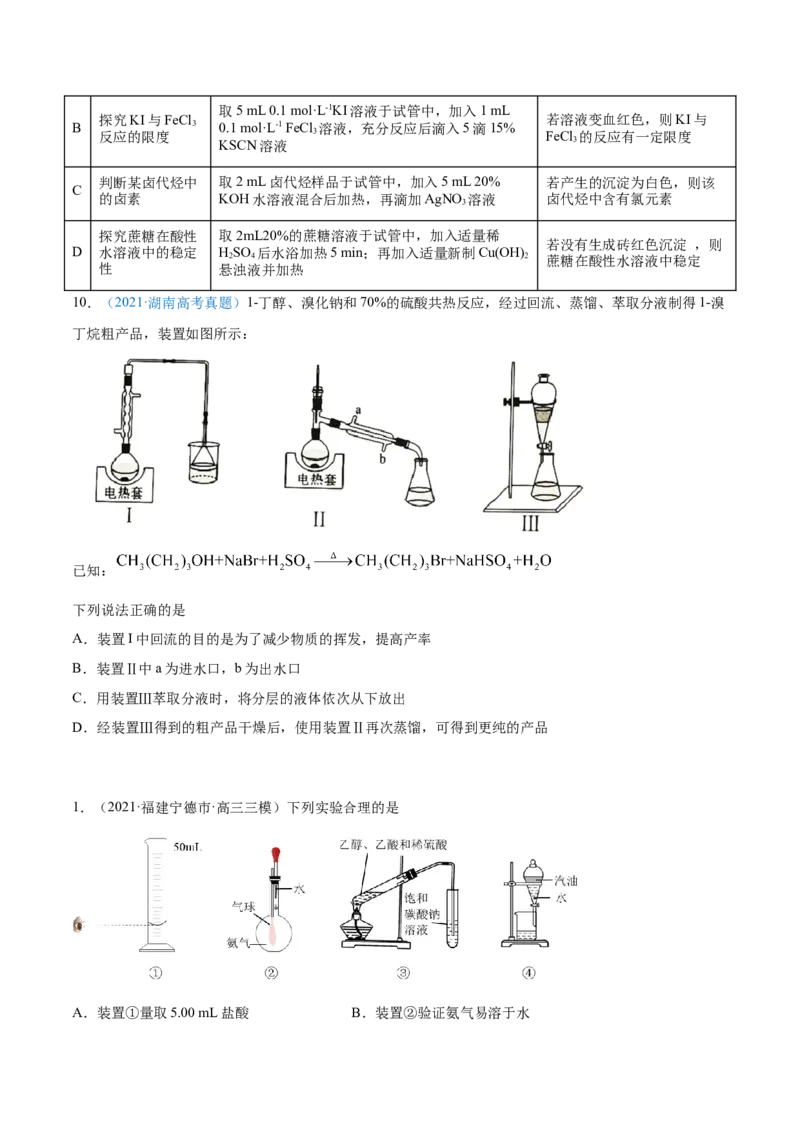
10.(2021·湖南高考真题)1-丁醇、溴化钠和70%的硫酸共热反应,经过回流、蒸馏、萃取分液制得1-溴
丁烷粗产品,装置如图所示:
已知:
下列说法正确的是
A.装置I中回流的目的是为了减少物质的挥发,提高产率
B.装置Ⅱ中a为进水口,b为出水口
C.用装置Ⅲ萃取分液时,将分层的液体依次从下放出
D.经装置Ⅲ得到的粗产品干燥后,使用装置Ⅱ再次蒸馏,可得到更纯的产品
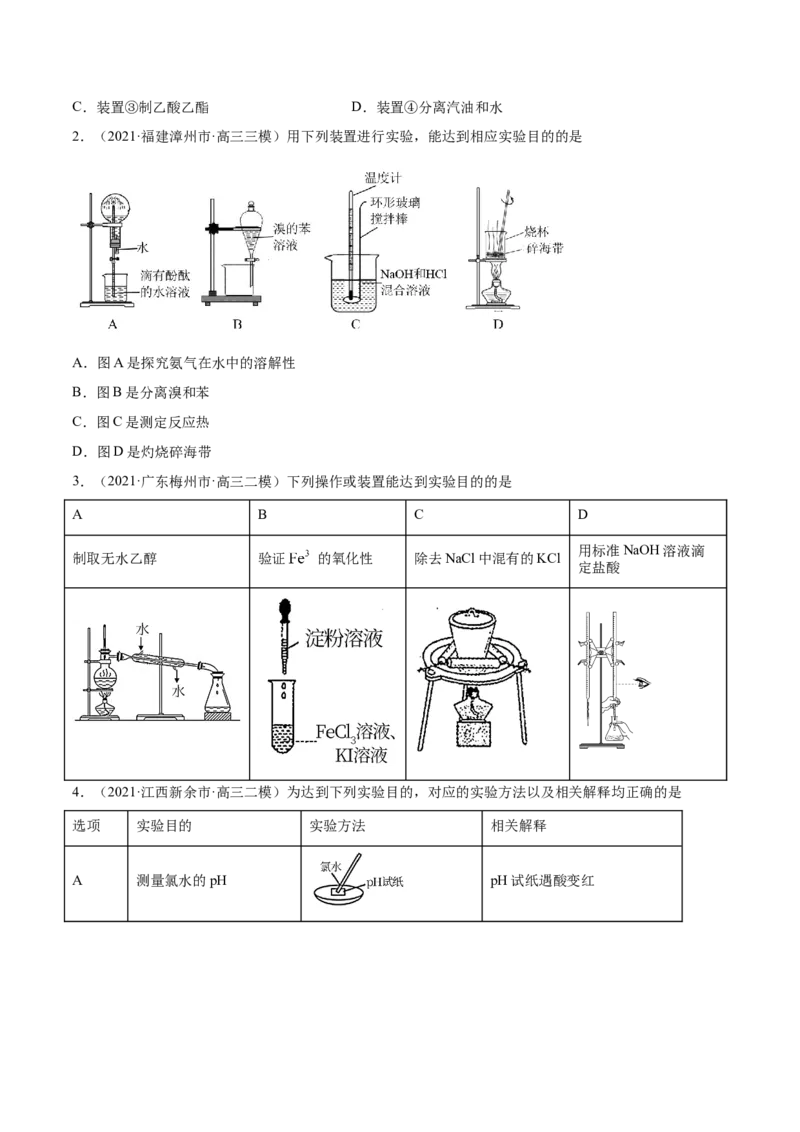
1.(2021·福建宁德市·高三三模)下列实验合理的是
A.装置①量取5.00 mL盐酸 B.装置②验证氨气易溶于水C.装置③制乙酸乙酯 D.装置④分离汽油和水
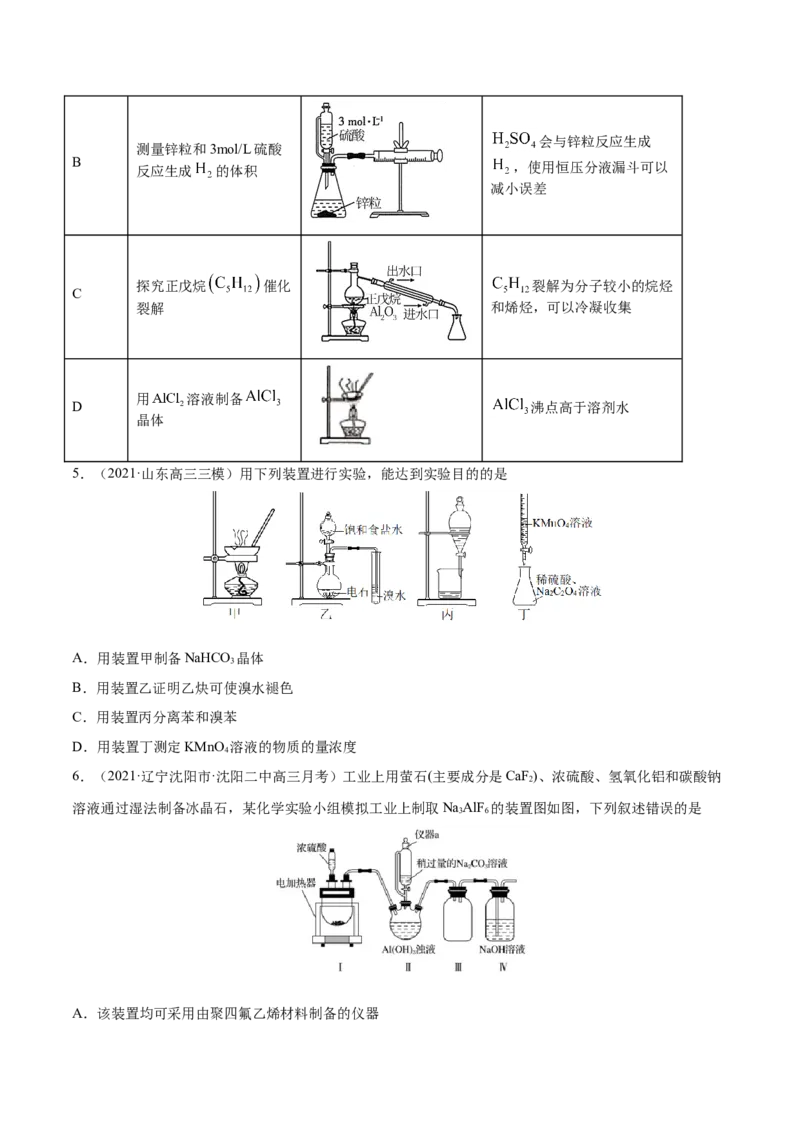
2.(2021·福建漳州市·高三三模)用下列装置进行实验,能达到相应实验目的的是
A.图A是探究氨气在水中的溶解性
B.图B是分离溴和苯
C.图C是测定反应热
D.图D是灼烧碎海带
3.(2021·广东梅州市·高三二模)下列操作或装置能达到实验目的的是
A B C D
用标准NaOH溶液滴
制取无水乙醇 验证 的氧化性 除去NaCl中混有的KCl
定盐酸
4.(2021·江西新余市·高三二模)为达到下列实验目的,对应的实验方法以及相关解释均正确的是
选项 实验目的 实验方法 相关解释
A 测量氯水的pH pH试纸遇酸变红会与锌粒反应生成
测量锌粒和3mol/L硫酸
B
反应生成 的体积 ,使用恒压分液漏斗可以
减小误差
探究正戊烷 催化 裂解为分子较小的烷烃
C
裂解 和烯烃,可以冷凝收集
用 溶液制备
D 沸点高于溶剂水
晶体
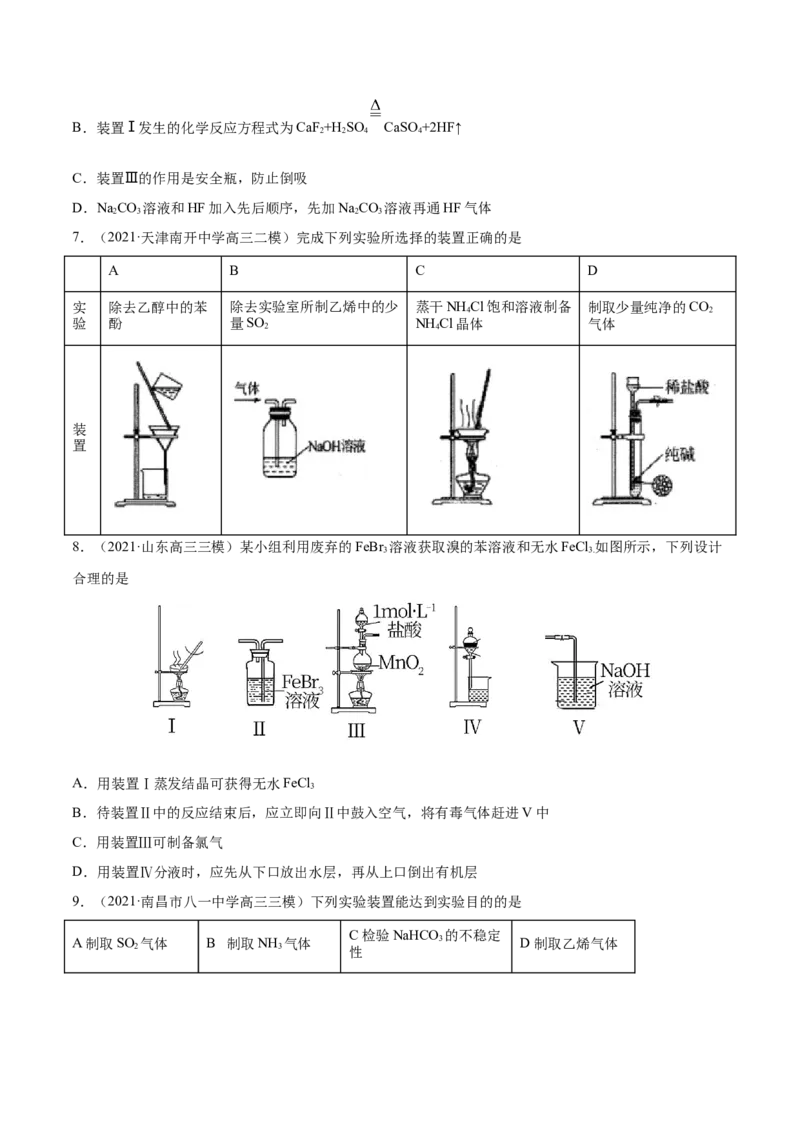
5.(2021·山东高三三模)用下列装置进行实验,能达到实验目的的是
A.用装置甲制备NaHCO 晶体
3
B.用装置乙证明乙炔可使溴水褪色
C.用装置丙分离苯和溴苯
D.用装置丁测定KMnO 溶液的物质的量浓度
4
6.(2021·辽宁沈阳市·沈阳二中高三月考)工业上用萤石(主要成分是CaF )、浓硫酸、氢氧化铝和碳酸钠
2
溶液通过湿法制备冰晶石,某化学实验小组模拟工业上制取NaAlF 的装置图如图,下列叙述错误的是
3 6
A.该装置均可采用由聚四氟乙烯材料制备的仪器B.装置Ⅰ发生的化学反应方程式为CaF +H SO CaSO+2HF↑
2 2 4 4
C.装置Ⅲ的作用是安全瓶,防止倒吸
D.NaCO 溶液和HF加入先后顺序,先加NaCO 溶液再通HF气体
2 3 2 3
7.(2021·天津南开中学高三二模)完成下列实验所选择的装置正确的是
A B C D
实 除去乙醇中的苯 除去实验室所制乙烯中的少 蒸干NH Cl饱和溶液制备 制取少量纯净的CO
4 2
验 酚 量SO NH Cl晶体 气体
2 4
装
置
8.(2021·山东高三三模)某小组利用废弃的FeBr 溶液获取溴的苯溶液和无水FeCl 如图所示,下列设计
3 3.
合理的是
A.用装置Ⅰ蒸发结晶可获得无水FeCl
3
B.待装置Ⅱ中的反应结束后,应立即向Ⅱ中鼓入空气,将有毒气体赶进V中
C.用装置Ⅲ可制备氯气
D.用装置Ⅳ分液时,应先从下口放出水层,再从上口倒出有机层
9.(2021·南昌市八一中学高三三模)下列实验装置能达到实验目的的是
C 检验NaHCO 的不稳定
A 制取SO 气体 B 制取NH 气体 3 D 制取乙烯气体
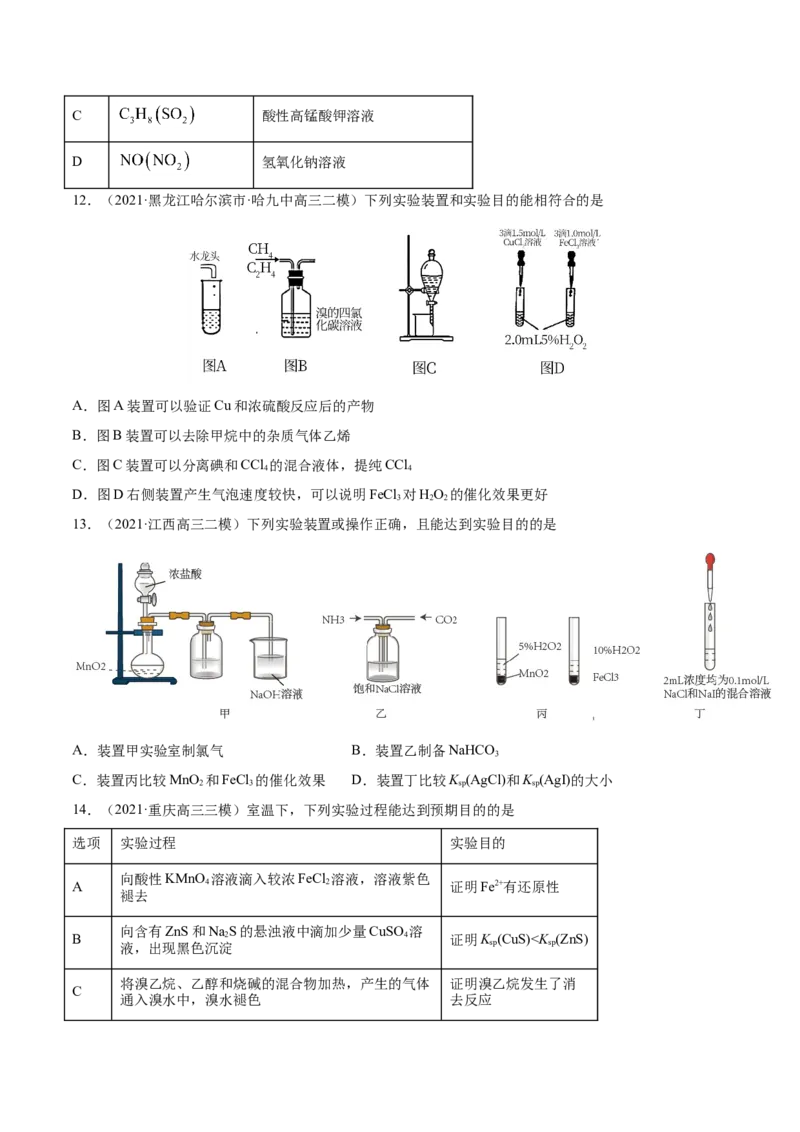
2 3 性10.(2021·山东潍坊市·高三模拟)水合肼 是重要的氢能源稳定剂,其制备的反应原理为
.图中装置和操作不能达到实验目的的是
A.在裝置甲的圆底烧瓶中加入氯化钙制取
B.用装置乙作为反应过程的安全瓶
C.制备水合肼时从装置丙的a口通入
D.用装置丁吸收反应中过量的
11.(2021·河南高三三模)下图为去除气体中少量杂质并收集相应气体的装置,能实现相应目的的是
选项 气体(杂质) O
A 碳酸钠溶液
B 氢氧化钠溶液C 酸性高锰酸钾溶液
D 氢氧化钠溶液
12.(2021·黑龙江哈尔滨市·哈九中高三二模)下列实验装置和实验目的能相符合的是
A.图A装置可以验证Cu和浓硫酸反应后的产物
B.图B装置可以去除甲烷中的杂质气体乙烯
C.图C装置可以分离碘和CCl 的混合液体,提纯CCl
4 4
D.图D右侧装置产生气泡速度较快,可以说明FeCl 对HO 的催化效果更好
3 2 2
13.(2021·江西高三二模)下列实验装置或操作正确,且能达到实验目的的是
A.装置甲实验室制氯气 B.装置乙制备NaHCO
3
C.装置丙比较MnO 和FeCl 的催化效果 D.装置丁比较K (AgCl)和K (AgI)的大小
2 3 sp sp
14.(2021·重庆高三三模)室温下,下列实验过程能达到预期目的的是
选项 实验过程 实验目的
向酸性KMnO 溶液滴入较浓FeCl 溶液,溶液紫色
A 4 2 证明Fe2+有还原性
褪去
向含有ZnS和NaS的悬浊液中滴加少量CuSO 溶
B 2 4 证明K (CuS)C>Si
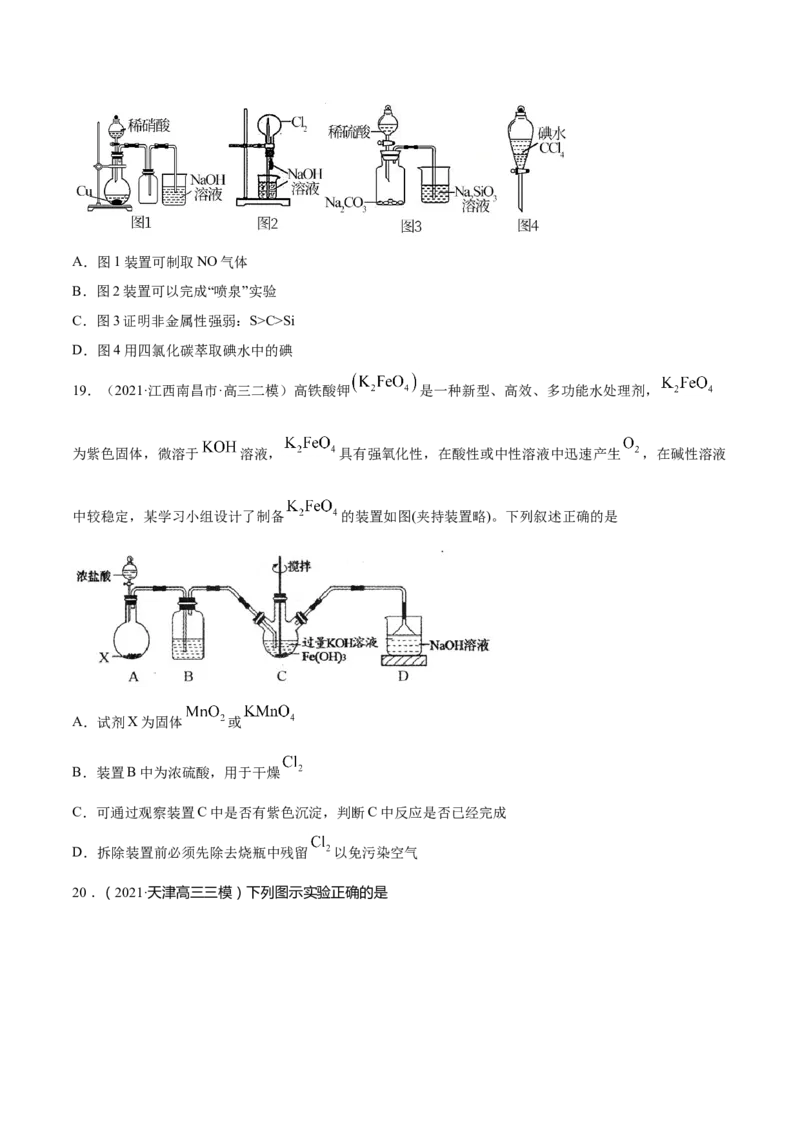
D.图4用四氯化碳萃取碘水中的碘
19.(2021·江西南昌市·高三二模)高铁酸钾 是一种新型、高效、多功能水处理剂,
为紫色固体,微溶于 溶液, 具有强氧化性,在酸性或中性溶液中迅速产生 ,在碱性溶液
中较稳定,某学习小组设计了制备 的装置如图(夹持装置略)。下列叙述正确的是
A.试剂X为固体 或
B.装置B中为浓硫酸,用于干燥
C.可通过观察装置C中是否有紫色沉淀,判断C中反应是否已经完成
D.拆除装置前必须先除去烧瓶中残留 以免污染空气
20.(2021·天津高三三模)下列图示实验正确的是A.洗涤烧杯并将洗涤液 B.制备并观察 C.实验室快速制备
D.实验室制备乙酸乙酯
转入容量瓶中 的颜色
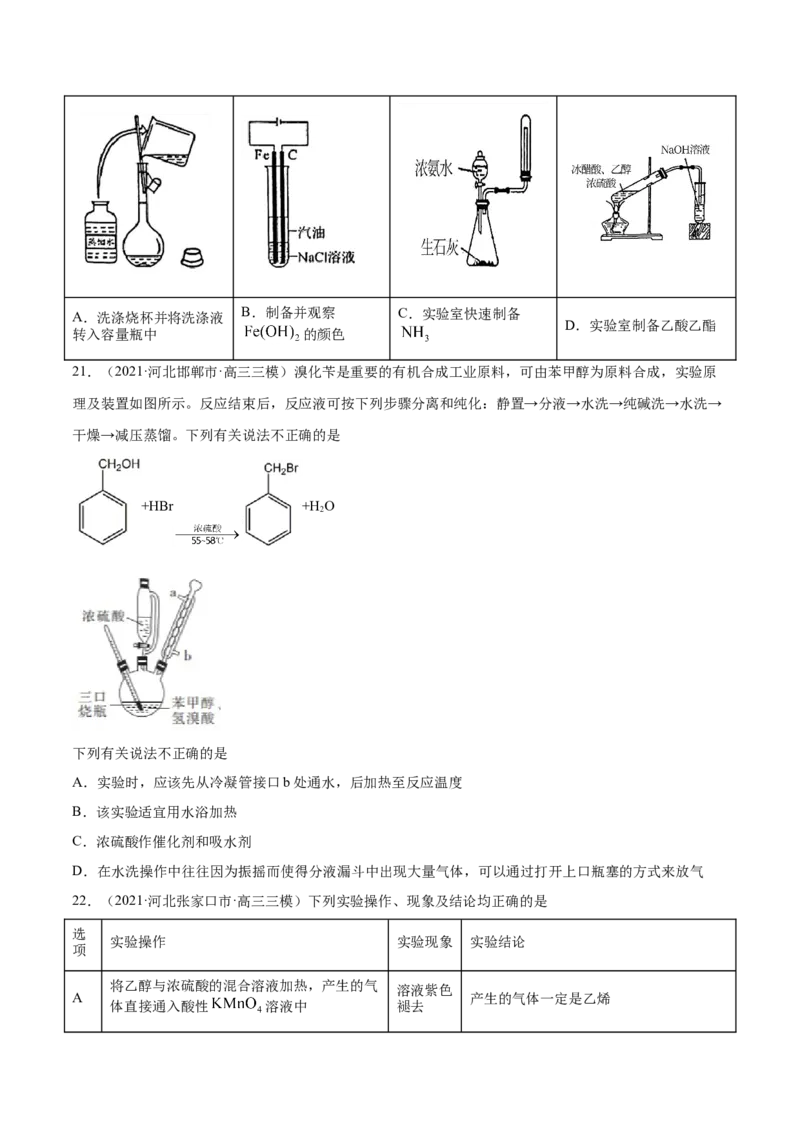
21.(2021·河北邯郸市·高三三模)溴化苄是重要的有机合成工业原料,可由苯甲醇为原料合成,实验原
理及装置如图所示。反应结束后,反应液可按下列步骤分离和纯化:静置→分液→水洗→纯碱洗→水洗→
干燥→减压蒸馏。下列有关说法不正确的是
+HBr +H O
2
下列有关说法不正确的是
A.实验时,应该先从冷凝管接口b处通水,后加热至反应温度
B.该实验适宜用水浴加热
C.浓硫酸作催化剂和吸水剂
D.在水洗操作中往往因为振摇而使得分液漏斗中出现大量气体,可以通过打开上口瓶塞的方式来放气
22.(2021·河北张家口市·高三三模)下列实验操作、现象及结论均正确的是
选
实验操作 实验现象 实验结论
项
将乙醇与浓硫酸的混合溶液加热,产生的气
溶液紫色
A 产生的气体一定是乙烯
体直接通入酸性 溶液中 褪去得到澄清
B 向 溶液中滴加过量氨水 与 能大量共存
溶液
常温下,
常温下,向含等浓度 和 的溶液中 先生成蓝
C
色沉淀
逐滴加入NaOH溶液
将用稀硫酸酸化后的 溶液滴入
D 溶液变黄 氧化性:
溶液中
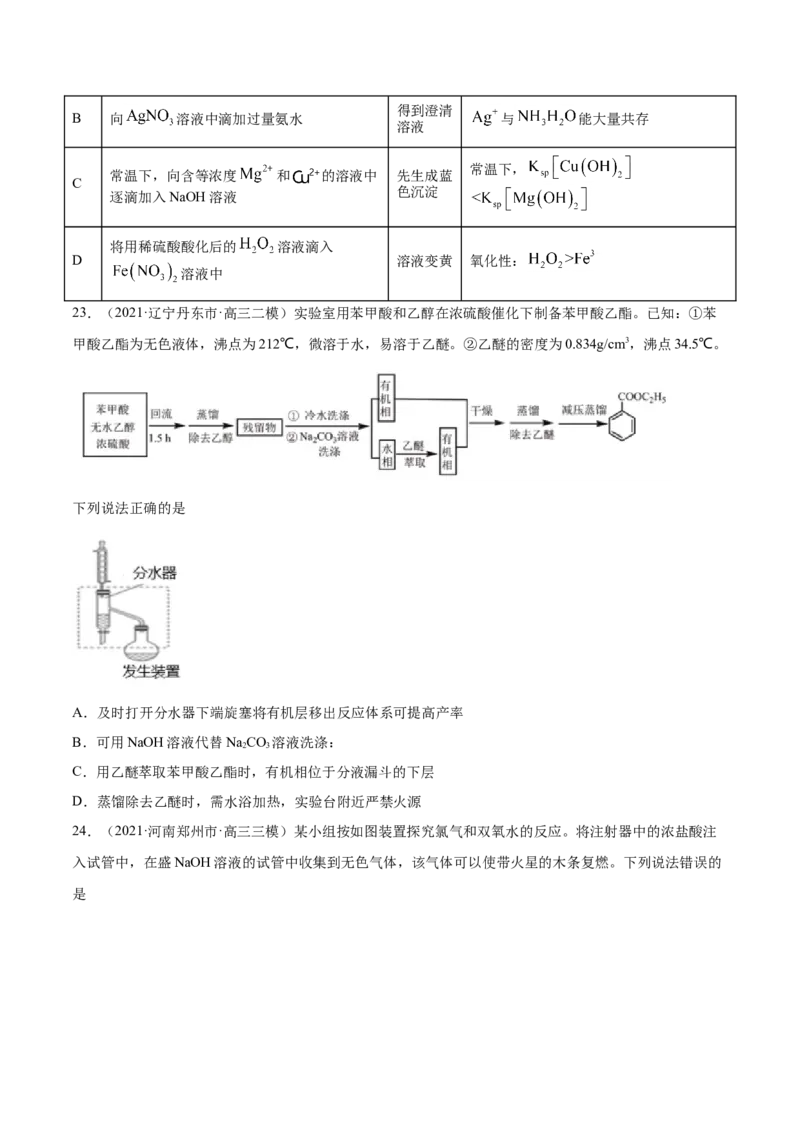
23.(2021·辽宁丹东市·高三二模)实验室用苯甲酸和乙醇在浓硫酸催化下制备苯甲酸乙酯。已知:①苯
甲酸乙酯为无色液体,沸点为212℃,微溶于水,易溶于乙醚。②乙醚的密度为0.834g/cm3,沸点34.5℃。
下列说法正确的是
A.及时打开分水器下端旋塞将有机层移出反应体系可提高产率
B.可用NaOH溶液代替NaCO 溶液洗涤:
2 3
C.用乙醚萃取苯甲酸乙酯时,有机相位于分液漏斗的下层
D.蒸馏除去乙醚时,需水浴加热,实验台附近严禁火源
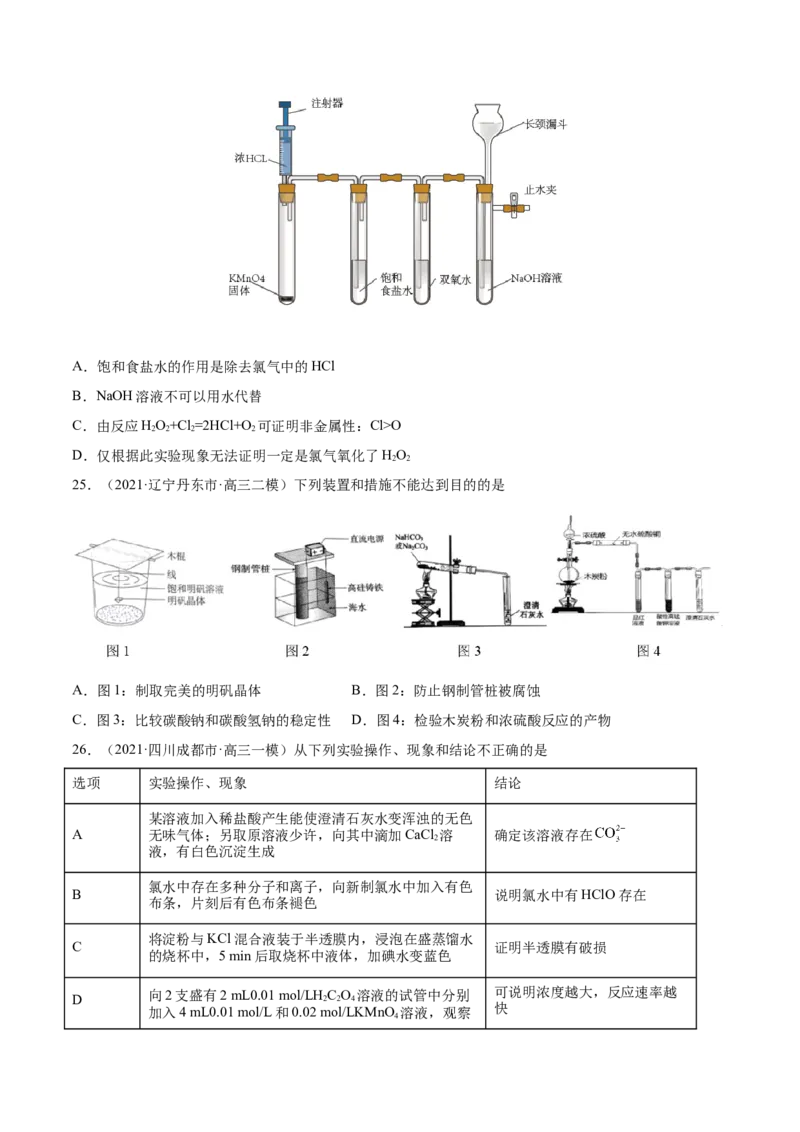
24.(2021·河南郑州市·高三三模)某小组按如图装置探究氯气和双氧水的反应。将注射器中的浓盐酸注
入试管中,在盛NaOH溶液的试管中收集到无色气体,该气体可以使带火星的木条复燃。下列说法错误的
是A.饱和食盐水的作用是除去氯气中的HCl
B.NaOH溶液不可以用水代替
C.由反应HO+Cl=2HCl+O 可证明非金属性:Cl>O
2 2 2 2
D.仅根据此实验现象无法证明一定是氯气氧化了HO
2 2
25.(2021·辽宁丹东市·高三二模)下列装置和措施不能达到目的的是
A.图1:制取完美的明矾晶体 B.图2:防止钢制管桩被腐蚀
C.图3:比较碳酸钠和碳酸氢钠的稳定性 D.图4:检验木炭粉和浓硫酸反应的产物
26.(2021·四川成都市·高三一模)从下列实验操作、现象和结论不正确的是
选项 实验操作、现象 结论
某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色
A 无味气体;另取原溶液少许,向其中滴加CaCl 溶 确定该溶液存在
2
液,有白色沉淀生成
氯水中存在多种分子和离子,向新制氯水中加入有色
B 说明氯水中有HClO存在
布条,片刻后有色布条褪色
将淀粉与KCl混合液装于半透膜内,浸泡在盛蒸馏水
C 证明半透膜有破损
的烧杯中,5 min后取烧杯中液体,加碘水变蓝色
向2支盛有2 mL0.01 mol/LH C O 溶液的试管中分别 可说明浓度越大,反应速率越
D 2 2 4
快
加入4 mL0.01 mol/L和0.02 mol/LKMnO 溶液,观察
4现象
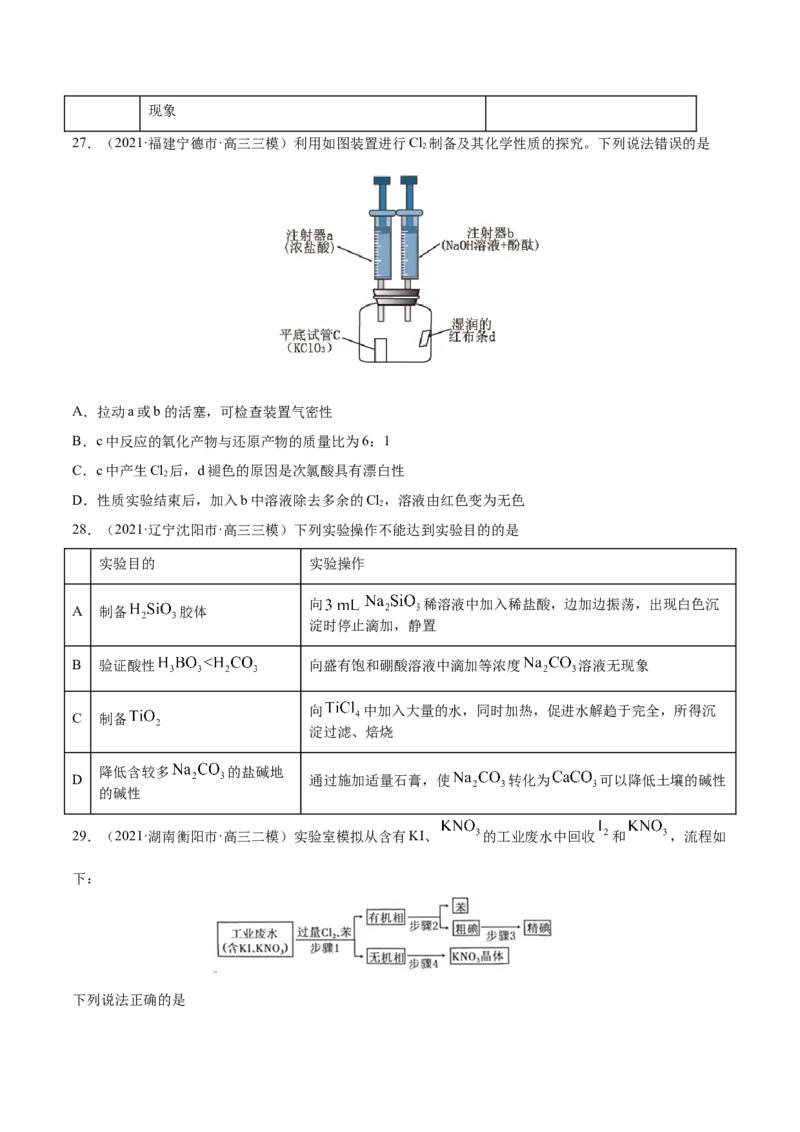
27.(2021·福建宁德市·高三三模)利用如图装置进行Cl 制备及其化学性质的探究。下列说法错误的是
2
A.拉动a或b的活塞,可检查装置气密性
B.c中反应的氧化产物与还原产物的质量比为6:1
C.c中产生Cl 后,d褪色的原因是次氯酸具有漂白性
2
D.性质实验结束后,加入b中溶液除去多余的Cl,溶液由红色变为无色
2
28.(2021·辽宁沈阳市·高三三模)下列实验操作不能达到实验目的的是
实验目的 实验操作
向 稀溶液中加入稀盐酸,边加边振荡,出现白色沉
A 制备 胶体
淀时停止滴加,静置
B 验证酸性 向盛有饱和硼酸溶液中滴加等浓度 溶液无现象
向 中加入大量的水,同时加热,促进水解趋于完全,所得沉
C 制备
淀过滤、焙烧
降低含较多 的盐碱地
D 通过施加适量石膏,使 转化为 可以降低土壤的碱性
的碱性
29.(2021·湖南衡阳市·高三二模)实验室模拟从含有KI、 的工业废水中回收 和 ,流程如
下:
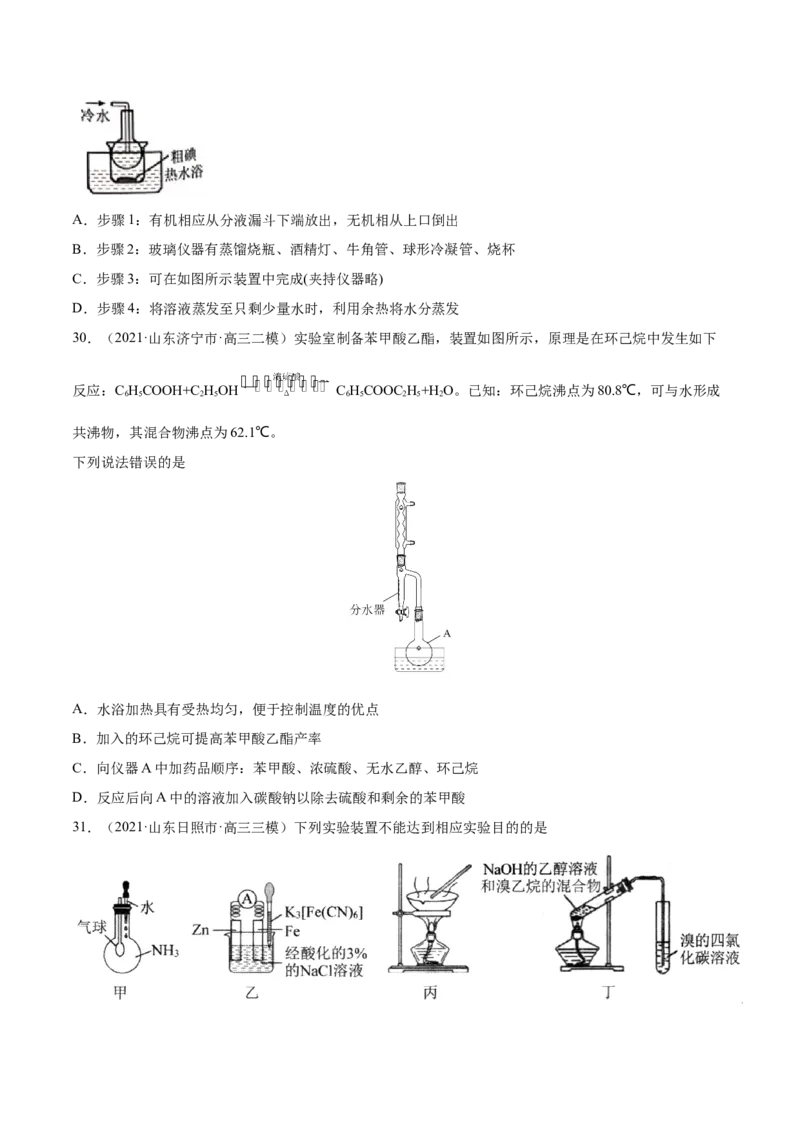
下列说法正确的是A.步骤1:有机相应从分液漏斗下端放出,无机相从上口倒出
B.步骤2:玻璃仪器有蒸馏烧瓶、酒精灯、牛角管、球形冷凝管、烧杯
C.步骤3:可在如图所示装置中完成(夹持仪器略)
D.步骤4:将溶液蒸发至只剩少量水时,利用余热将水分蒸发
30.(2021·山东济宁市·高三二模)实验室制备苯甲酸乙酯,装置如图所示,原理是在环己烷中发生如下
反应:C HCOOH+C HOH C HCOOC H+H O。已知:环己烷沸点为80.8℃,可与水形成
6 5 2 5 6 5 2 5 2
共沸物,其混合物沸点为62.1℃。
下列说法错误的是
A.水浴加热具有受热均匀,便于控制温度的优点
B.加入的环己烷可提高苯甲酸乙酯产率
C.向仪器A中加药品顺序:苯甲酸、浓硫酸、无水乙醇、环己烷
D.反应后向A中的溶液加入碳酸钠以除去硫酸和剩余的苯甲酸
31.(2021·山东日照市·高三三模)下列实验装置不能达到相应实验目的的是A.用甲装置验证NH 在水中的溶解度大
3
B.用乙装置验证牺牲阳极保护法
C.用丙装置将CuC1 溶液蒸干制备CuC1
2 2
D.用丁装置验证溴乙烷的消去产物是乙烯
32.(2021·天津高三二模)下列实验操作、现象和结论均正确的是
选
实验操作 现象 结论
项
未知溶液中含有 或
产生能使澄清石灰水变浑
A 向少量未知溶液中加入稀盐酸
浊的气体
在空气中点燃氢气,将导管伸入盛有氯气
B 集气瓶中产生白烟 生成
的集气瓶
C 向 溶液中滴入稀盐酸 溶液中出现凝胶 非金属性:
向 溶液中滴加少量稀硫酸,测
D 电导率减小 溶液中的离子浓度减小
电导率变化
33.(2021·广东汕头市·高三二模)芯片被誉为“现代工业粮食”,是新一代信息产业的基石。制备芯片材
料高纯硅的装置如下图所示(加热及夹持装置省略),利用SiHCl 与过量H 在1100~1200℃反应(SiHCl 沸
3 2 3
点为31.8℃,遇水会强烈水解),下列说法不正确的是
A.装置B中的试剂是浓硫酸
B.实验开始时先打开装置A中的K
1
C.装置C采用常温冷却水,目的是使SiHCl 与H 充分混合
3 2
D.石英管中发生反应SiHCl +H Si+3HCl
3 2
34.(2021·辽宁朝阳市·高三三模)下列实验过程可以达到实验目的的是
实验目的 实验过程
A 探究 的漂白性 向橙色的溴水中通入 ,观察溶液颜色变化B 探究 的还原性 将 通过炽热的 ,观察现象
C 探究 的氧化性 向 溶液中滴入 溶液,观察现象
向相同体积不同浓度的 和 溶液中分别滴入 滴相同浓度的
比较 与 的溶度积
D
大小 溶液
35.(2021·广东高三模拟)某小组在实验室中用下图所示装置(夹持装置已略去)制取碳酸镧[La (CO)],
2 3 3
制备原理为2LaCl+6NH+3CO +3H O=La (CO)↓+6NHCl。下列说法正确的是
3 3 2 2 2 3 3 4
A.干燥管的作用是增大反应物间的接触面积
B.试剂X为饱和NaCO 溶液,试剂Y为饱和NH Cl溶液
2 3 4
C.若用稀硫酸代替装置I中的稀盐酸,则实验时可以不用盛试剂X的装置
D.实验时一般先通入装置II产生的气体,再通入装置I产生的气体
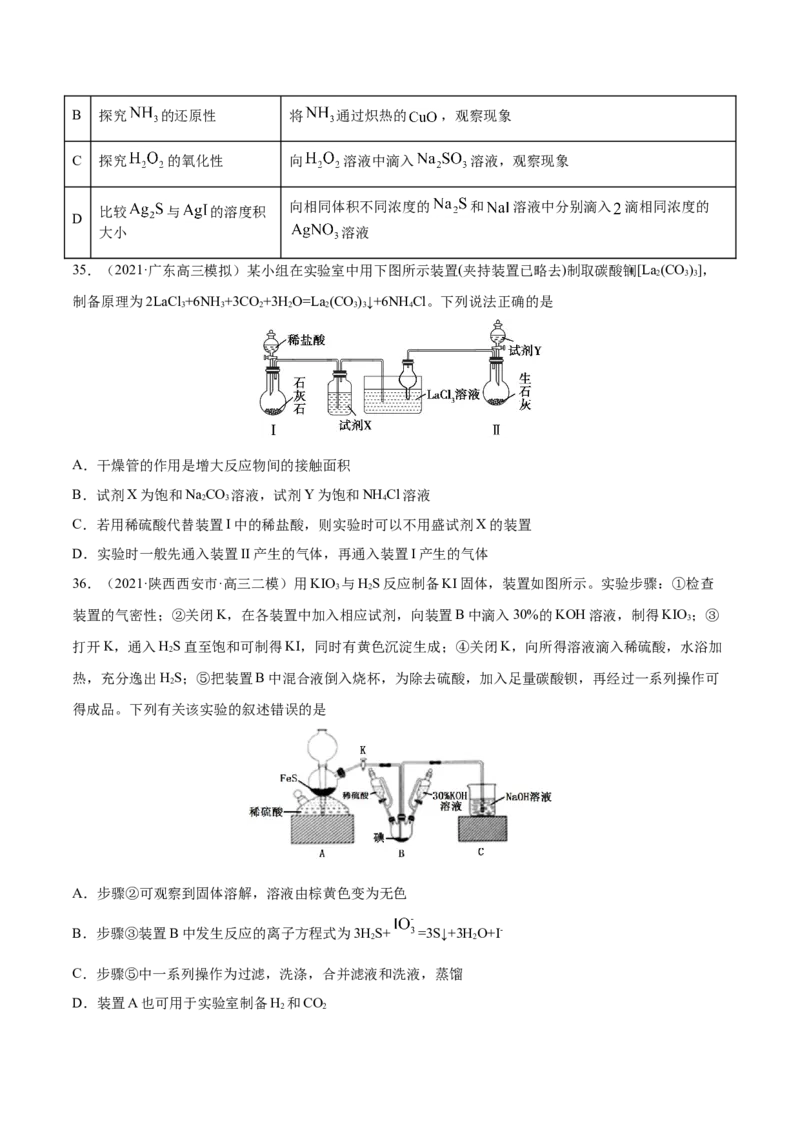
36.(2021·陕西西安市·高三二模)用KIO 与HS反应制备KI固体,装置如图所示。实验步骤:①检查
3 2
装置的气密性;②关闭K,在各装置中加入相应试剂,向装置B中滴入30%的KOH溶液,制得KIO ;③
3
打开K,通入HS直至饱和可制得KI,同时有黄色沉淀生成;④关闭K,向所得溶液滴入稀硫酸,水浴加
2
热,充分逸出HS;⑤把装置B中混合液倒入烧杯,为除去硫酸,加入足量碳酸钡,再经过一系列操作可
2
得成品。下列有关该实验的叙述错误的是
A.步骤②可观察到固体溶解,溶液由棕黄色变为无色
B.步骤③装置B中发生反应的离子方程式为3HS+ =3S↓+3H O+I-
2 2
C.步骤⑤中一系列操作为过滤,洗涤,合并滤液和洗液,蒸馏
D.装置A 也可用于实验室制备H 和CO
2 237.(2021·辽宁丹东市·高三二模)下列实验操作中,其现象、解释及结论均正确的是
序
实验操作 实验现象 解释或结论
号
试纸最终显蓝 NaClO在溶液中水解显
A 用pH试纸测定“84”消毒液pH
色 碱性
分别向两份相同的HO 溶液中滴入5滴等浓度的 前者产生气泡 CuSO 比KMnO 的催化
B 2 2 4 4
CuSO 溶液和KMnO 溶液率更快 速率更快 效果好
4 4
气体X一定具有强氧化
C 向BaCl 溶液中通入SO 和X气体 产生白色沉淀
2 2 性
分别向两份相同的蛋白质溶液中滴入饱和硫酸铵溶液和 前者是物理变化,后者
D 均有固体析出
醋酸铅溶液 是化学变化
38.(2021·山东泰安市·高三模拟)为达到实验目的,下列方案设计、现象和结论都正确的是
选项 实验目的 方案设计 现象和结论
检验某无色溶液
取少量该溶液于试管中,加入 若品红溶液褪色,则该
中是否含有
A 足量稀盐酸,将产生的气体通
溶液中含有
入品红溶液中
取少量固体溶于蒸馏水,然后
判断Fe(NO ) 固 若溶液变红,则
B 3 2 滴加少量稀硫酸,再滴入
体是否变质 Fe(NO ) 固体已变质
KSCN溶液 3 2
若硅酸钠溶液变浑浊,
探究酸性: 将稀硫酸与NaCO 混合后产生
C 2 3 则硫酸的酸性比硅酸的
HSO >H SiO 的气体直接通入硅酸钠溶液中
2 4 2 3 强
若产生疏松多孔的海绵
探究浓硫酸的性 向蔗糖中加入几滴蒸馏水,然 状炭,并放出刺激性气
D
质 后再加入浓硫酸 味的气体,则浓硫酸具
有脱水性和强氧化性