文档内容
专题 11 有机化学基础
考点01 官能团的结构与性质··············································································1
考点02 有机物的推断······················································································12
考点03 有机合成····························································································24
考点 01 官能团的结构与性质
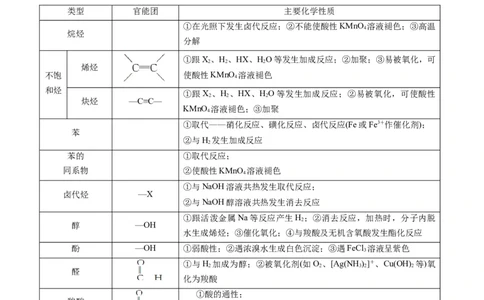
类型 官能团 主要化学性质
①在光照下发生卤代反应;②不能使酸性KMnO 溶液褪色;③高温
4
烷烃
分解
①跟X、H、HX、HO等发生加成反应;②加聚;③易被氧化,可
2 2 2
烯烃
不饱 使酸性KMnO 溶液褪色
4
和烃
①跟X 、H 、HX、HO等发生加成反应;②易被氧化,可使酸性
2 2 2
炔烃 —C≡C—
KMnO 溶液褪色;③加聚
4
①取代——硝化反应、磺化反应、卤代反应(Fe或Fe3+作催化剂);
苯
②与H 发生加成反应
2
苯的 ①取代反应;
同系物 ②使酸性KMnO 溶液褪色
4
①与NaOH溶液共热发生取代反应;
卤代烃 —X
②与NaOH醇溶液共热发生消去反应
①跟活泼金属Na等反应产生H ;②消去反应,加热时,分子内脱
2
醇 —OH
水生成烯烃;③催化氧化;④与羧酸及无机含氧酸发生酯化反应
酚 —OH ①弱酸性;②遇浓溴水生成白色沉淀;③遇FeCl 溶液呈紫色
3
①与H 加成为醇;②被氧化剂(如O 、[Ag(NH)]+、Cu(OH) 等)氧
2 2 3 2 2
醛
化为羧酸
①酸的通性;
羧酸
②酯化反应
酯 发生水解反应,生成羧酸(盐)和醇
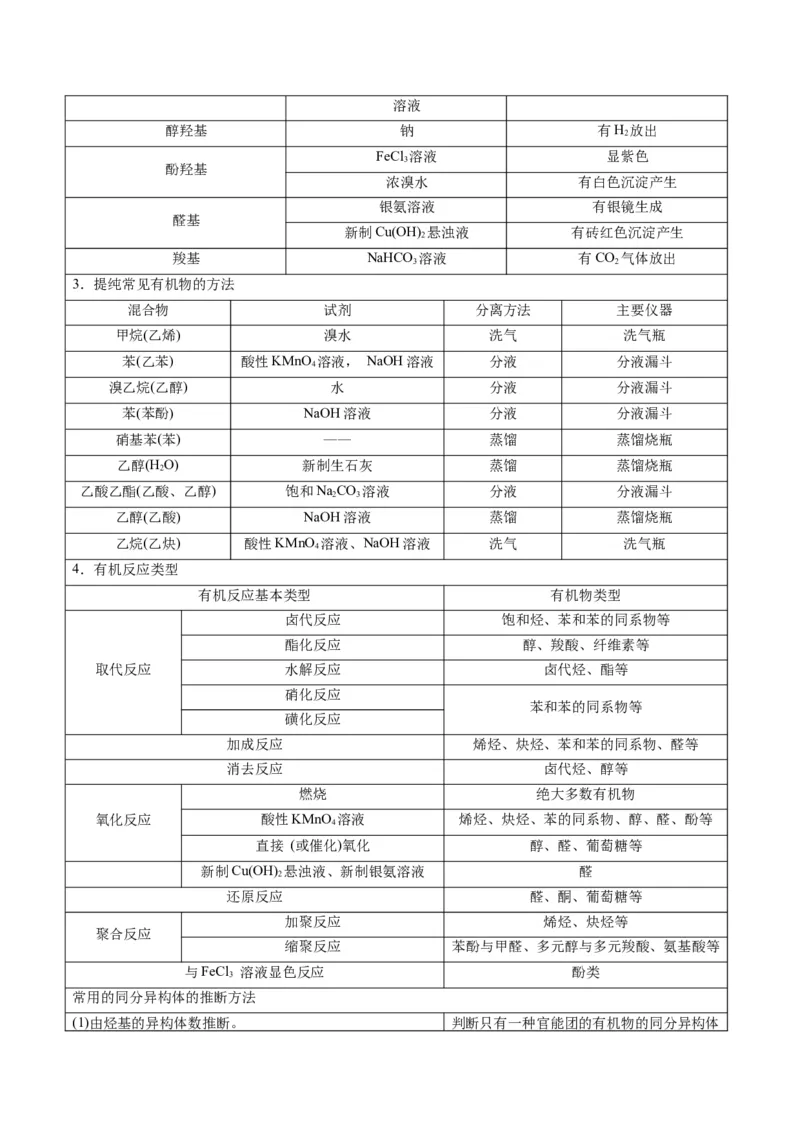
2.常见重要官能团的检验方法
官能团种类 试剂 判断依据
碳碳双键或 溴的CCl 溶液 橙红色褪去
4
碳碳三键 酸性KMnO 溶液 紫红色褪去
4
卤素原子 NaOH溶液、稀硝酸、AgNO 有沉淀生成
3溶液
醇羟基 钠 有H 放出
2
FeCl 溶液 显紫色
3
酚羟基
浓溴水 有白色沉淀产生
银氨溶液 有银镜生成
醛基
新制Cu(OH) 悬浊液 有砖红色沉淀产生
2
羧基 NaHCO 溶液 有CO 气体放出
3 2
3.提纯常见有机物的方法
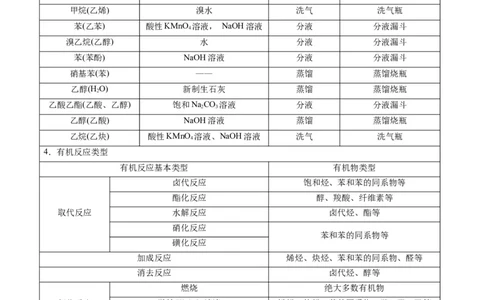
混合物 试剂 分离方法 主要仪器
甲烷(乙烯) 溴水 洗气 洗气瓶
苯(乙苯) 酸性KMnO 溶液, NaOH溶液 分液 分液漏斗
4
溴乙烷(乙醇) 水 分液 分液漏斗
苯(苯酚) NaOH溶液 分液 分液漏斗
硝基苯(苯) —— 蒸馏 蒸馏烧瓶
乙醇(H O) 新制生石灰 蒸馏 蒸馏烧瓶
2
乙酸乙酯(乙酸、乙醇) 饱和NaCO 溶液 分液 分液漏斗
2 3
乙醇(乙酸) NaOH溶液 蒸馏 蒸馏烧瓶
乙烷(乙炔) 酸性KMnO 溶液、NaOH溶液 洗气 洗气瓶
4
4.有机反应类型
有机反应基本类型 有机物类型
卤代反应 饱和烃、苯和苯的同系物等
酯化反应 醇、羧酸、纤维素等
取代反应 水解反应 卤代烃、酯等
硝化反应
苯和苯的同系物等
磺化反应
加成反应 烯烃、炔烃、苯和苯的同系物、醛等
消去反应 卤代烃、醇等
燃烧 绝大多数有机物
氧化反应 酸性KMnO 溶液 烯烃、炔烃、苯的同系物、醇、醛、酚等
4
直接 (或催化)氧化 醇、醛、葡萄糖等
新制Cu(OH) 悬浊液、新制银氨溶液 醛
2
还原反应 醛、酮、葡萄糖等
加聚反应 烯烃、炔烃等
聚合反应
缩聚反应 苯酚与甲醛、多元醇与多元羧酸、氨基酸等
与FeCl 溶液显色反应 酚类
3
常用的同分异构体的推断方法
(1)由烃基的异构体数推断。 判断只有一种官能团的有机物的同分异构体的种数时,根据烃基的异构体数判断较为快
捷。如判断丁醇的同分异构体时,根据组成
丁醇可写成C H—OH,由于丁基有4种结
4 9
构,故丁醇有4种同分异构体。
①同一种碳原子上的氢原子是等效的;
(2)由等效氢原子推 碳链上有几种不同的氢原子,其
②同一碳原子所连甲基上的氢原子是等效
断。 一元取代物就有几种同分异构
的;
体。一般判断原则:
③处于镜面对称位置上的氢原子是等效的。
如一个碳碳双键可以用环替换;碳氧双键可以用碳碳双键替换并将氧原子移到
他处;又如碳碳三键相当于两个碳碳双键,也相当于两个环。不同原子间也可
(3)用替换法推断。
以替换,如二氯苯C HCl 有3种同分异构体,四氯苯C HCl 也有3种同分异
6 4 2 6 2 4
构体。
(4)用定一移一法推 对于二元取代物同分异构体的判断,可固定一个取代基的位置,再改变另一个
断。 取代基的位置以确定同分异构体的数目。
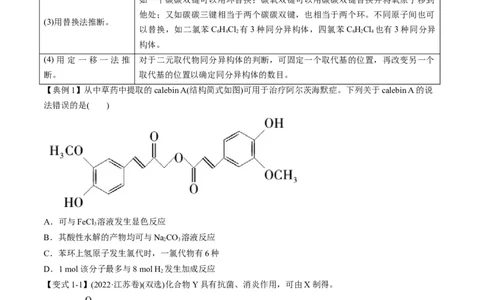
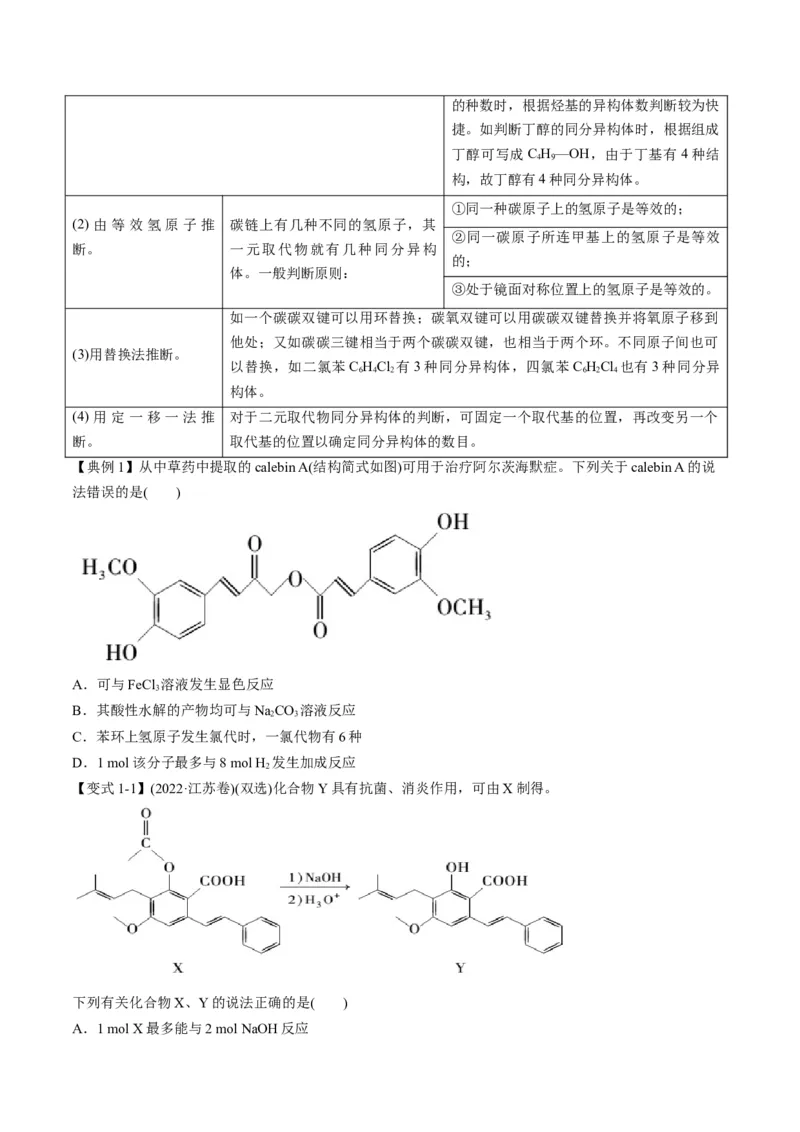
【典例1】从中草药中提取的calebin A(结构简式如图)可用于治疗阿尔茨海默症。下列关于calebin A的说
法错误的是( )
A.可与FeCl 溶液发生显色反应
3
B.其酸性水解的产物均可与NaCO 溶液反应
2 3
C.苯环上氢原子发生氯代时,一氯代物有6种
D.1 mol该分子最多与8 mol H 发生加成反应
2
【变式1-1】(2022·江苏卷)(双选)化合物Y具有抗菌、消炎作用,可由X制得。
下列有关化合物X、Y的说法正确的是( )
A.1 mol X最多能与2 mol NaOH反应B.Y与乙醇发生酯化反应可得到X
C.X、Y均能与酸性KMnO 溶液反应
4
D.室温下X、Y分别与足量Br 加成的产物分子中手性碳原子数目相等
2
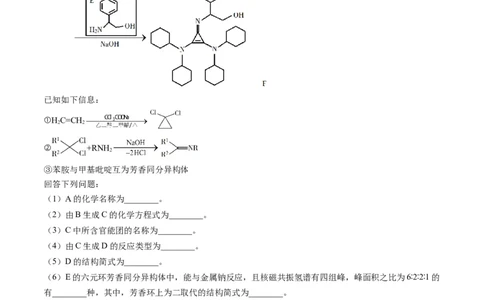
【变式1-2】有机碱,例如二甲基胺( )、苯胺( ),吡啶( )等,在有机合成中应用很普遍,目
前“有机超强碱”的研究越来越受到关注,以下为有机超强碱F的合成路线:
已知如下信息:
①HC=CH
2 2
② +RNH
2
③苯胺与甲基吡啶互为芳香同分异构体
回答下列问题:
(1)A的化学名称为________。
(2)由B生成C的化学方程式为________。
(3)C中所含官能团的名称为________。
(4)由C生成D的反应类型为________。
(5)D的结构简式为________。
(6)E的六元环芳香同分异构体中,能与金属钠反应,且核磁共振氢谱有四组峰,峰面积之比为6∶2∶2∶1的
有________种,其中,芳香环上为二取代的结构简式为________。
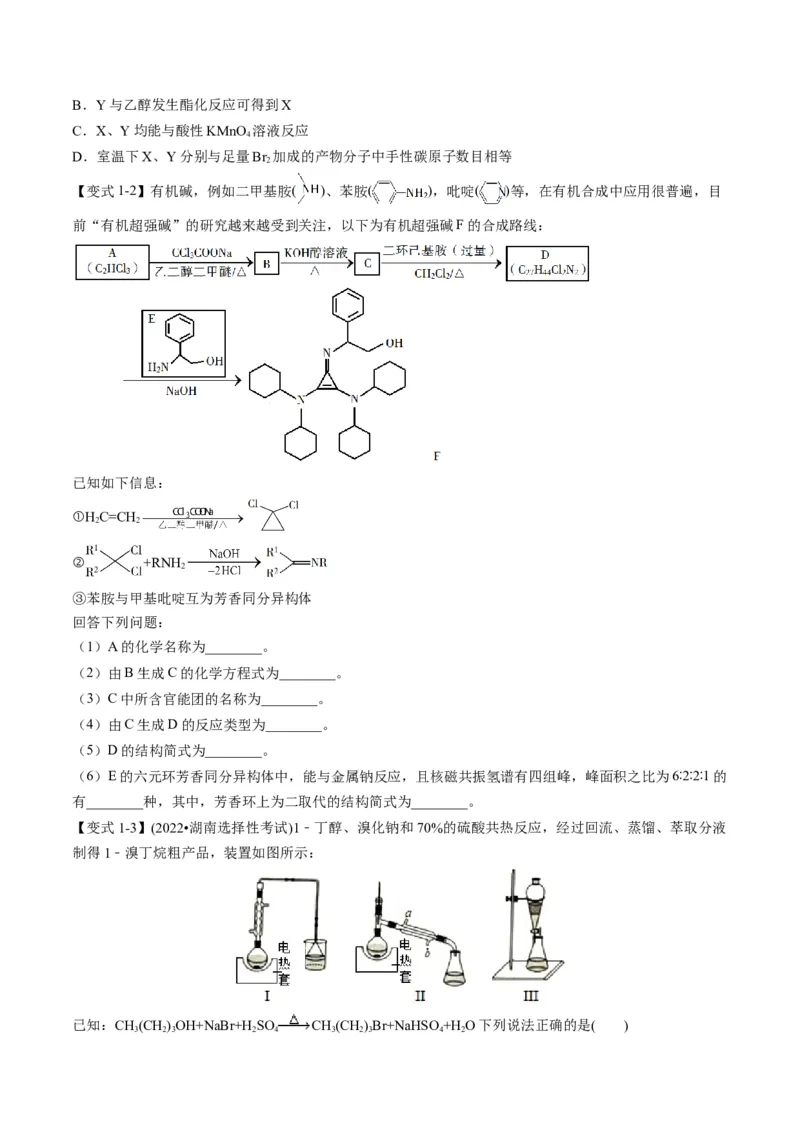
【变式1-3】(2022•湖南选择性考试)1﹣丁醇、溴化钠和70%的硫酸共热反应,经过回流、蒸馏、萃取分液
制得1﹣溴丁烷粗产品,装置如图所示:
已知:CH(CH)OH+NaBr+H SO CH(CH)Br+NaHSO +H O下列说法正确的是( )
3 2 3 2 4 3 2 3 4 2A.装置Ⅰ中回流的目的是为了减少物质的挥发,提高产率
B.装置Ⅱ中a为进水口,b为出水口
C.用装置Ⅲ萃取分液时,将分层的液体依次从下口放出
D.经装置Ⅲ得到的粗产品干燥后,使用装置Ⅱ再次蒸馏,可得到更纯的产品
【变式1-4】下列说法不正确的是( )
A.甘氨酸和丙氨酸混合,在一定条件下可生成4种二肽
B.乙酸、苯甲酸、乙二酸(草酸)均不能使酸性高锰酸钾溶液褪色
C.纤维素与乙酸酐作用生成的醋酸纤维可用于生产电影胶片片基
D.工业上通常用植物油与氢气反应生产人造奶油
【变式1-5】高分子材料在生产生活中应用广泛。下列说法错误的是( )
A.芦苇可用于制造黏胶纤维,其主要成分为纤维素
B.聚氯乙烯通过加聚反应制得,可用于制作不粘锅的耐热涂层
C.淀粉是相对分子质量可达几十万的天然高分子物质
D.大豆蛋白纤维是一种可降解材料
【变式1-6】苯并降冰片烯是一种重要的药物合成中间体,结构简式如图。关于该化合物,下列说法正确
的是( )
A.是苯的同系物
B.分子中最多8个碳原子共平面
C.一氯代物有6种(不考虑立体异构)
D.分子中含有4个碳碳双键
考点 02 有机物的推断
1、有机推断解题的一般模式
2、有机推断解题的方法
从基础原料入手,找出合成所需的直接或间接的中间体,逐步推向合成的目标有机
(1)正合成分析法:
物,
其合成示意图: 基础原料→中间体1→中间体2……→目标有机物。设计复杂有机物的合成路线时常用的方法。它是由目标有机物倒推寻找上一步反应
(2)逆合成分析法: 的中间体n,而中间体n又可以由中间体(n-1)得到,依次倒推,最后确定最适宜的
基础原料和最终的合成路线,
合成示意图: 目标有机物→中间体n→中间体(n-1)……→基础原料。
3、确定官能团的方法
①使溴水褪色,则表示该物质中可能含有“ ”或“ ”结构。
②使KMnO (H+)溶液褪色,则该物质中可能含有“ ”、“ ”
4
(1)根据试剂或特征 或“—CHO”等结构或为苯的同系物。
现象推知官能团的 ③遇FeCl 3 溶液显紫色,或加入溴水出现白色沉淀,则该物质中含有酚羟基。
种类 ④遇浓硝酸变黄,则表明该物质是含有苯环结构的蛋白质。
⑤遇I 变蓝则该物质为淀粉。
2
⑥加入新制的Cu(OH) 悬浊液,加热煮沸有红色沉淀生成或加入银氨溶液加热有银
2
镜生成,表示含有—CHO。
⑦加入Na放出H,表示含有—OH或—COOH。
2
⑧加入NaHCO 溶液产生气体,表示含有—COOH。
3
①
②2—OH(醇、酚、羧酸)――→H
2
③2—COOH――→CO,—COOH――→CO
2 2
④ ―――→ ,—C≡C—(或二烯、烯醛)――→—CHCH—
(2)根据数据确定官 2 2
能团的数目 ⑤某有机物与醋酸反应,相对分子质量增加42,则含有1个—OH;增加84,则含
有2个—OH。即—OH转变为—OOCCH 。
3
⑥由—CHO 转变为—COOH,相对分子质量增加 16;若增加 32,则含 2 个—
CHO。
⑦当醇被氧化成醛或酮后,相对分子质量减小2,则含有1个—OH;若相对分子质
量减小4,则含有2个—OH。
①若醇能氧化为醛或羧酸,则醇分子中应含有结构“—CHOH”;若能氧化成酮,
2
则醇分子中应含有结构“—CHOH—”。
(3)根据性质确定官
②由消去反应的产物可确定“—OH”或“—X”的位置。
能团的位置
③由一卤代物的种类可确定碳架结构。
④由加氢后的碳架结构,可确定“ ”或“—C≡C—”的位置。
4、有机反应类型的推断(1)有机化学反应类
型判断的基本思路
①在NaOH的水溶液中发生水解反应,可能是酯的水解反应或卤代烃的水解反应。
②在NaOH的乙醇溶液中加热,发生卤代烃的消去反应。
③在浓HSO 存在的条件下加热,可能发生醇的消去反应、酯化反应、成醚反应或
2 4
硝化反应等。
④能与溴水或溴的CCl 溶液反应,可能为烯烃、炔烃的加成反应。
4
⑤能与H 在Ni作用下发生反应,则为烯烃、炔烃、芳香烃、醛的加成反应或还原
2
(2)根据反应条件推
反应。
断反应类型
⑥在O、Cu(或Ag)、加热(或CuO、加热)条件下,发生醇的氧化反应。
2
⑦与O 或新制的Cu(OH) 悬浊液或银氨溶液反应,则该物质发生的是—CHO的氧
2 2
化反应。(如果连续两次出现O,则为醇―→醛―→羧酸的过程)
2
⑧在稀HSO 加热条件下发生酯、低聚糖、多糖等的水解反应。
2 4
⑨在光照、X(表示卤素单质)条件下发生烷基上的取代反应;在Fe粉、X 条件下发
2 2
生苯环上的取代反应。
1.化合物G是一种药物合成中间体,其合成路线如下:
回答下列问题:
(1)A中的官能团名称是________。
(2)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。用星号(*)标出B中的手性碳
________________________________________________________________________。
(3)写出具有六元环结构、并能发生银镜反应的B的同分异构体的结构简式:
_____________________________________________。(不考虑立体异构,只需写出3个)
(4)反应④所需的试剂和条件是_______________________________________。
(5)⑤的反应类型是________。
(6)写出F到G的反应方程式:__________________________________________________。(7)设计由甲苯和乙酰乙酸乙酯(CHCOCH COOC H)制备 的合成路线
3 2 2 5
_______________________________________________________(无机试剂任选)。
2.PBAT(聚己二酸/对苯二甲酸丁酯)可被微生物几乎完全降解,成为包装、医疗和农用薄膜等领域的新
兴材料,可由聚合物PBA和PBT共聚制得,一种合成路线如下:
已知:R—CH――→R—CN――→R—COOH
3
回答下列问题:
(1)B的化学名称为 ,C所含官能团的名称为 。
(2)H的结构简式为 。
(3)②、④的反应类型分别为 、 。
(4)⑤的化学方程式为________________________________________
____________________________________________________。
(5)写出所有的与D互为同分异构体且满足以下条件的结构简式 。
①能与NaHCO 溶液反应;
3
②能发生银镜反应;
③能发生水解反应;
④核磁共振氢谱四组峰,峰面积比为1∶6∶2∶1
(6)设计由丙烯为起始原料制备 的单体的合成路线(其他试剂任选)。
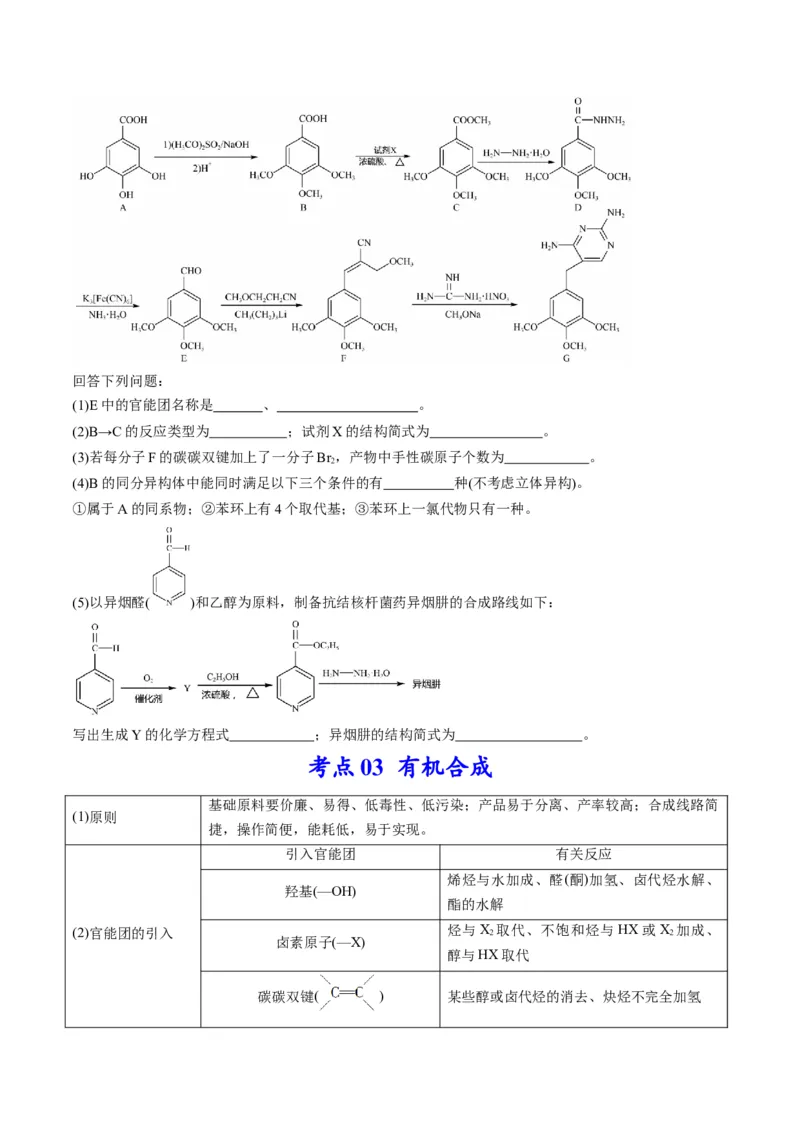
3.(2022•湖北选择性考试) (13分)甲基苄啶(G)是磺酸胺类抗菌药物的增效剂,其合成路线如下:回答下列问题:
(1)E中的官能团名称是 、 。
(2)B→C的反应类型为 ;试剂X的结构简式为 。
(3)若每分子F的碳碳双键加上了一分子Br ,产物中手性碳原子个数为 。
2
(4)B的同分异构体中能同时满足以下三个条件的有 种(不考虑立体异构)。
①属于A的同系物;②苯环上有4个取代基;③苯环上一氯代物只有一种。
(5)以异烟醛( )和乙醇为原料,制备抗结核杆菌药异烟肼的合成路线如下:
写出生成Y的化学方程式 ;异烟肼的结构简式为 。
考点 03 有机合成
基础原料要价廉、易得、低毒性、低污染;产品易于分离、产率较高;合成线路简
(1)原则
捷,操作简便,能耗低,易于实现。
引入官能团 有关反应
烯烃与水加成、醛(酮)加氢、卤代烃水解、
羟基(—OH)
酯的水解
(2)官能团的引入 烃与X 2 取代、不饱和烃与HX或X 2 加成、
卤素原子(—X)
醇与HX取代
碳碳双键( ) 某些醇或卤代烃的消去、炔烃不完全加氢醛基(—CHO) 某些醇(含有—CHOH)的氧化、烯烃的氧化
2
醛的氧化、酯的酸性水解、羧酸盐的酸化、
羧基(—COOH) 苯的同系物(侧链上与苯环相连的碳原子上有
氢原子)被强氧化剂氧化
酯基(—COO—) 酯化反应
①通过加成消除不饱和键(碳碳双键、碳碳三键等);
②通过加成或氧化等消除醛基(—CHO);
(4)官能团的消除
③通过消去、氧化或酯化反应等消除羟基(—OH);
④通过水解反应消除酯基、肽键、卤素原子。
①通过官能团之间的衍变关系改变。如:醇 醛 羧酸。
②通过某些 如:CHCHOH CH===CH XCH CHX
3 2 2 2 2 2
化学方法改 HOCH CHOH,CHCHCH===CH CHCHCHXCH
2 2 3 2 2 3 2 3
变官能团个 CHCH===CHCH 。
3 3
数或位置。
A、酚羟基的保护:因酚羟基易被氧化,所以在氧化其他基团前可以
先使其与NaOH(或羧酸)反应,把—OH变为—ONa(或酯基)将其保护
(5)官能团的改变
起来,待氧化后再酸化将其转变为—OH。
B、碳碳双键的保护:碳碳双键也容易被氧化,在氧化其他基团前可
③有机合成
以利用其与HCl等的加成反应将其保护起来,待氧化后再利用消去
中常见官能
反应转变为碳碳双键。
团的保护
C、氨基(—NH )的保护:如对硝基甲苯 对氨基苯甲酸的过程中
2
应先把—CH 氧化成—COOH之后,再把—NO 还原为—NH 。防止
3 2 2
当KMnO 氧化—CH 时,—NH (具有还原性)也被氧化。
4 3 2
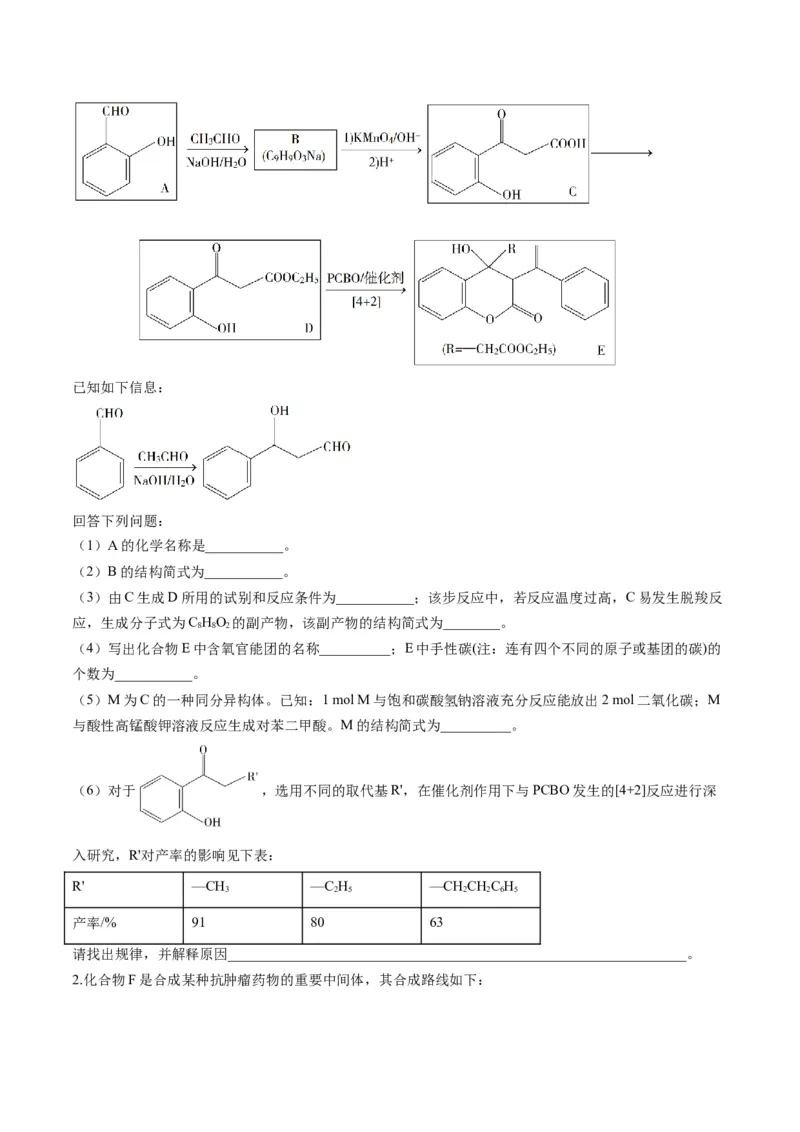
1.苯基环丁烯酮( PCBO)是一种十分活泼的反应物,可利用它的开环反应合成一系列多官
能团化合物。近期我国科学家报道用PCBO与醛或酮发生[4+2]环加成反应,合成了具有生物活性的多官能
团化合物(E),部分合成路线如下:已知如下信息:
回答下列问题:
(1)A的化学名称是___________。
(2)B的结构简式为___________。
(3)由C生成D所用的试别和反应条件为___________;该步反应中,若反应温度过高,C易发生脱羧反
应,生成分子式为C HO 的副产物,该副产物的结构简式为________。
8 8 2
(4)写出化合物E中含氧官能团的名称__________;E中手性碳(注:连有四个不同的原子或基团的碳)的
个数为___________。
(5)M为C的一种同分异构体。已知:1 mol M与饱和碳酸氢钠溶液充分反应能放出2 mol二氧化碳;M
与酸性高锰酸钾溶液反应生成对苯二甲酸。M的结构简式为__________。
(6)对于 ,选用不同的取代基R',在催化剂作用下与PCBO发生的[4+2]反应进行深
入研究,R'对产率的影响见下表:
R' —CH —C H —CHCHC H
3 2 5 2 2 6 5
产率/% 91 80 63
请找出规律,并解释原因_________________________________________________________________。
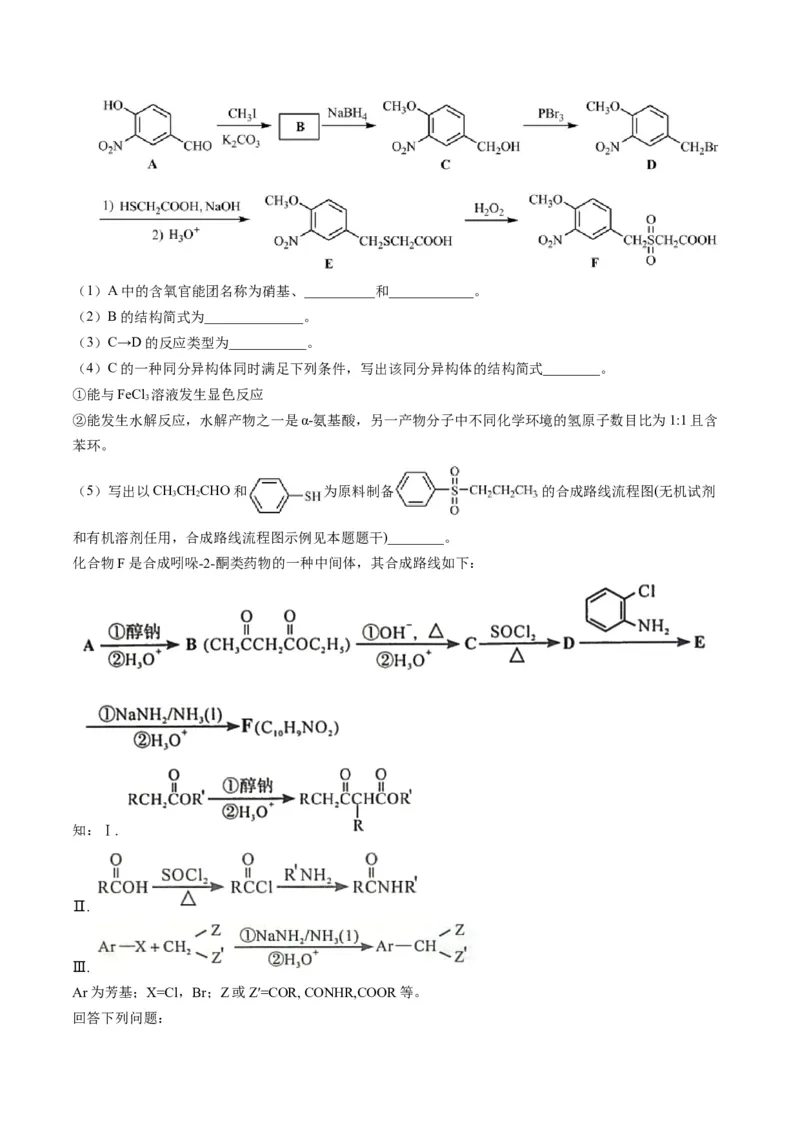
2.化合物F是合成某种抗肿瘤药物的重要中间体,其合成路线如下:(1)A中的含氧官能团名称为硝基、__________和____________。
(2)B的结构简式为______________。
(3)C→D的反应类型为___________。
(4)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式________。
①能与FeCl 溶液发生显色反应 。
3
②能发生水解反应,水解产物之一是α-氨基酸,另一产物分子中不同化学环境的氢原子数目比为1:1且含
苯环。
(5)写出以CHCHCHO和 为原料制备 的合成路线流程图(无机试剂
3 2
和有机溶剂任用,合成路线流程图示例见本题题干)________。
化合物F是合成吲哚-2-酮类药物的一种中间体,其合成路线如下:
知:Ⅰ.
Ⅱ.
Ⅲ.
Ar为芳基;X=Cl,Br;Z或Z′=COR, CONHR,COOR等。
回答下列问题:(1)实验室制备A的化学方程式为 ,提高A产率的方法是 ;A的某同分异构
体只有一种化学环境的碳原子,其结构简式为 。
(2)C→D的反应类型为 ;E中含氧官能团的名称为 。
(3)C的结构简式为 ,F的结构简式为 。
(4)Br 和 的反应与Br 和苯酚的反应类似,以 和 为原料合
2 2
成 ,写出能获得更多目标产物的较优合成路线(其它试剂任选)。
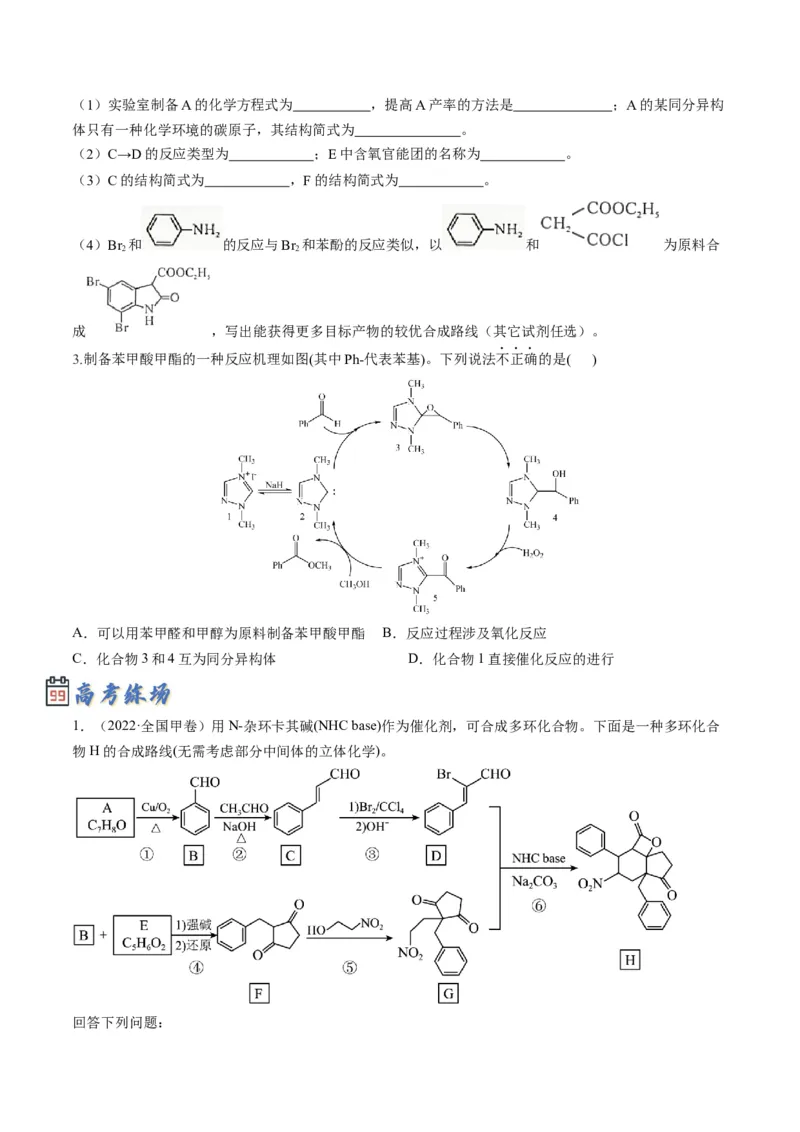
3.制备苯甲酸甲酯的一种反应机理如图(其中Ph-代表苯基)。下列说法不正确的是( )
A.可以用苯甲醛和甲醇为原料制备苯甲酸甲酯 B.反应过程涉及氧化反应
C.化合物3和4互为同分异构体 D.化合物1直接催化反应的进行
1.(2022·全国甲卷)用N-杂环卡其碱(NHC base)作为催化剂,可合成多环化合物。下面是一种多环化合
物H的合成路线(无需考虑部分中间体的立体化学)。
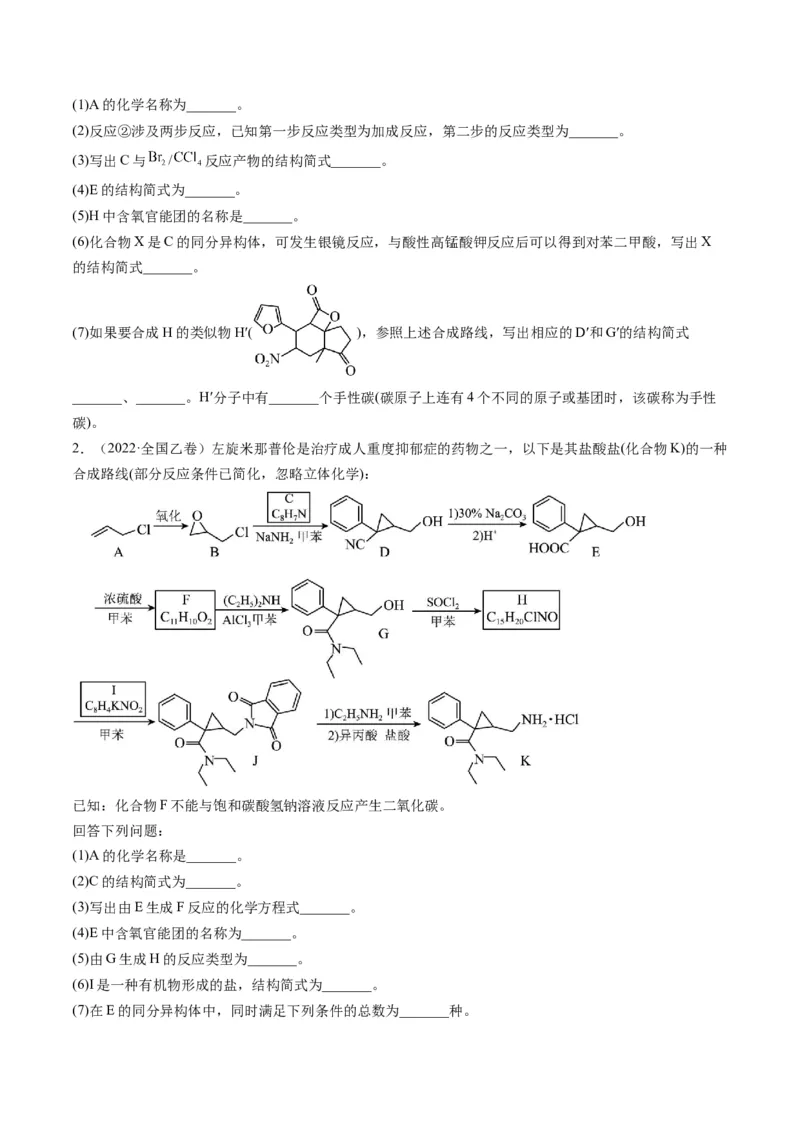
回答下列问题:(1)A的化学名称为_______。
(2)反应②涉及两步反应,已知第一步反应类型为加成反应,第二步的反应类型为_______。
(3)写出C与 / 反应产物的结构简式_______。
(4)E的结构简式为_______。
(5)H中含氧官能团的名称是_______。
(6)化合物X是C的同分异构体,可发生银镜反应,与酸性高锰酸钾反应后可以得到对苯二甲酸,写出X
的结构简式_______。
(7)如果要合成H的类似物H′( ),参照上述合成路线,写出相应的D′和G′的结构简式
_______、_______。H′分子中有_______个手性碳(碳原子上连有4个不同的原子或基团时,该碳称为手性
碳)。
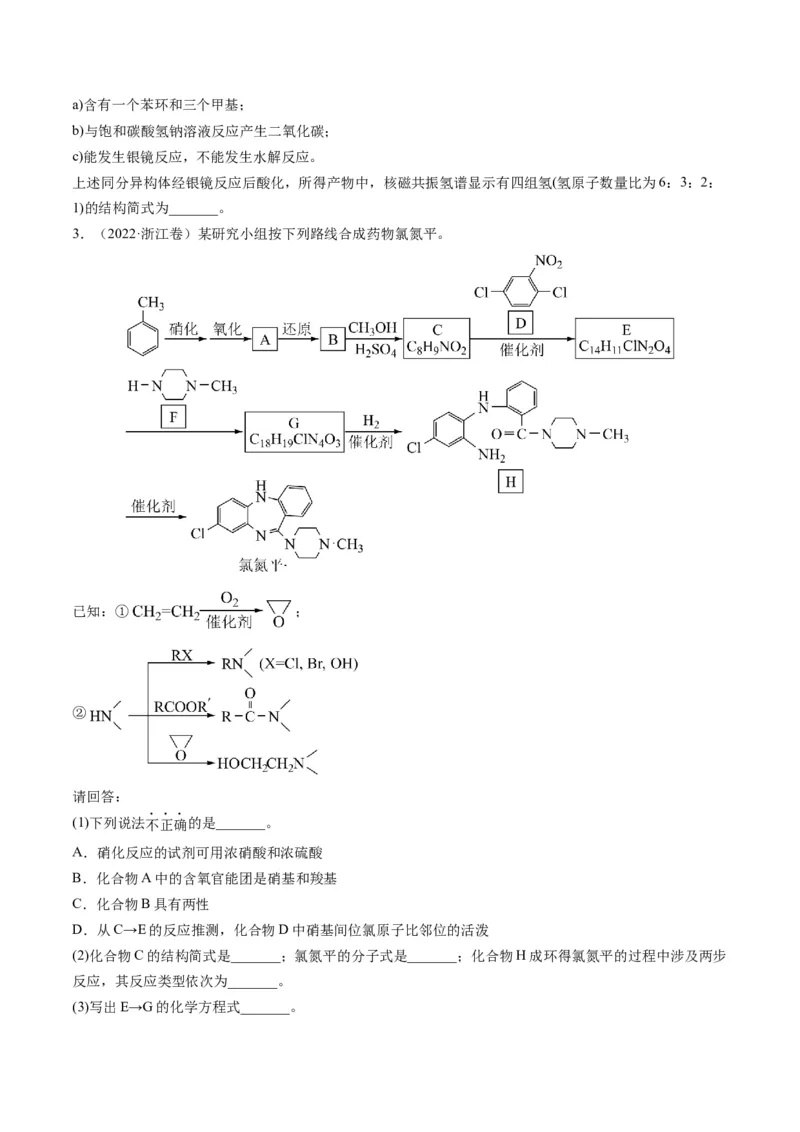
2.(2022·全国乙卷)左旋米那普伦是治疗成人重度抑郁症的药物之一,以下是其盐酸盐(化合物K)的一种
合成路线(部分反应条件已简化,忽略立体化学):
已知:化合物F不能与饱和碳酸氢钠溶液反应产生二氧化碳。
回答下列问题:
(1)A的化学名称是_______。
(2)C的结构简式为_______。
(3)写出由E生成F反应的化学方程式_______。
(4)E中含氧官能团的名称为_______。
(5)由G生成H的反应类型为_______。
(6)I是一种有机物形成的盐,结构简式为_______。
(7)在E的同分异构体中,同时满足下列条件的总数为_______种。a)含有一个苯环和三个甲基;
b)与饱和碳酸氢钠溶液反应产生二氧化碳;
c)能发生银镜反应,不能发生水解反应。
上述同分异构体经银镜反应后酸化,所得产物中,核磁共振氢谱显示有四组氢(氢原子数量比为6:3:2:
1)的结构简式为_______。
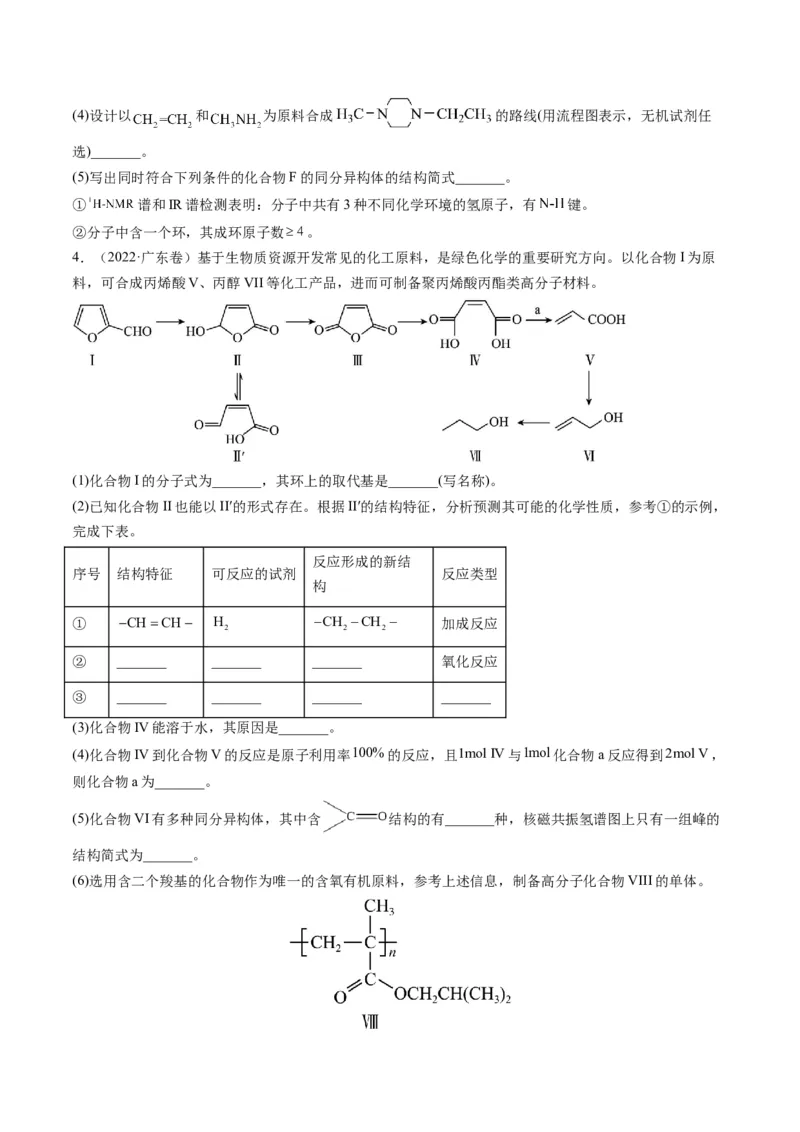
3.(2022·浙江卷)某研究小组按下列路线合成药物氯氮平。
已知:① ;
②
请回答:
(1)下列说法不正确的是_______。
A.硝化反应的试剂可用浓硝酸和浓硫酸
B.化合物A中的含氧官能团是硝基和羧基
C.化合物B具有两性
D.从C→E的反应推测,化合物D中硝基间位氯原子比邻位的活泼
(2)化合物C的结构简式是_______;氯氮平的分子式是_______;化合物H成环得氯氮平的过程中涉及两步
反应,其反应类型依次为_______。
(3)写出E→G的化学方程式_______。(4)设计以 和 为原料合成 的路线(用流程图表示,无机试剂任
选)_______。
(5)写出同时符合下列条件的化合物F的同分异构体的结构简式_______。
① 谱和IR谱检测表明:分子中共有3种不同化学环境的氢原子,有 键。
②分子中含一个环,其成环原子数 。
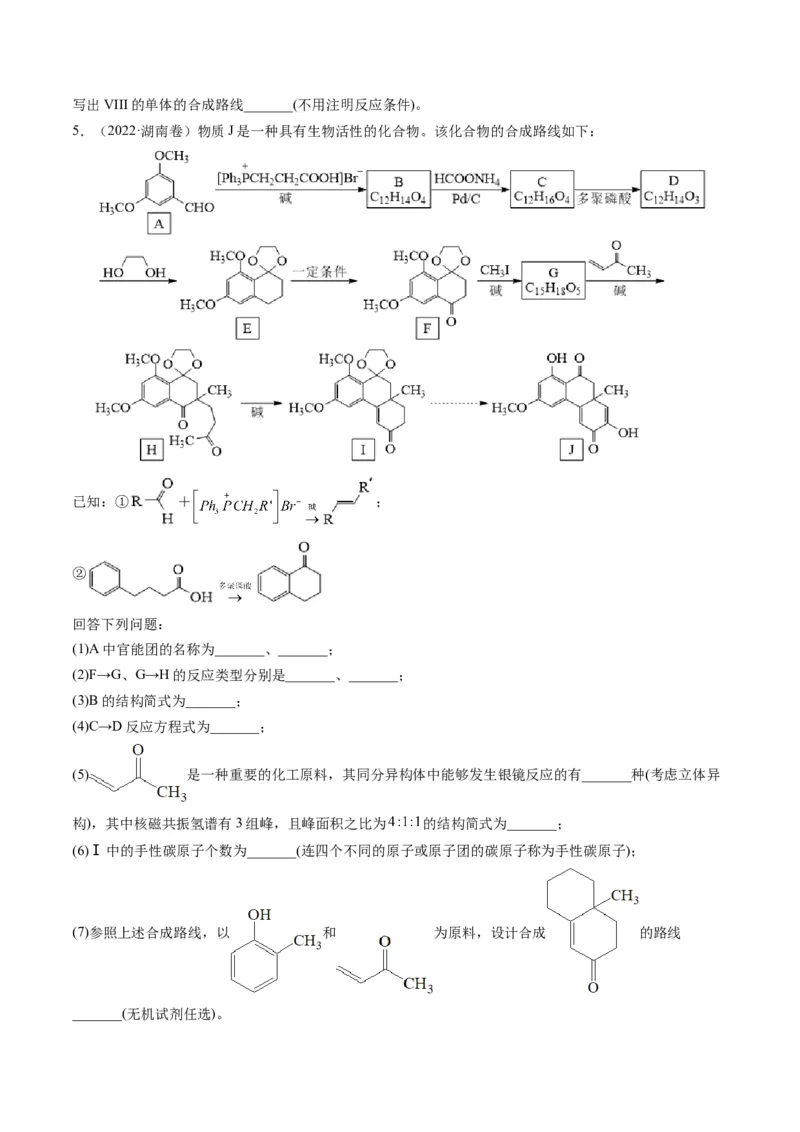
4.(2022·广东卷)基于生物质资源开发常见的化工原料,是绿色化学的重要研究方向。以化合物I为原
料,可合成丙烯酸V、丙醇VII等化工产品,进而可制备聚丙烯酸丙酯类高分子材料。
(1)化合物I的分子式为_______,其环上的取代基是_______(写名称)。
(2)已知化合物II也能以II′的形式存在。根据II′的结构特征,分析预测其可能的化学性质,参考①的示例,
完成下表。
反应形成的新结
序号 结构特征 可反应的试剂 反应类型
构
① CHCH H CH CH 加成反应
2 2 2
② _______ _______ _______ 氧化反应
③ _______ _______ _______ _______
(3)化合物IV能溶于水,其原因是_______。
(4)化合物IV到化合物V的反应是原子利用率100%的反应,且1mol IV与1mol化合物a反应得到2mol V,
则化合物a为_______。
(5)化合物VI有多种同分异构体,其中含 结构的有_______种,核磁共振氢谱图上只有一组峰的
结构简式为_______。
(6)选用含二个羧基的化合物作为唯一的含氧有机原料,参考上述信息,制备高分子化合物VIII的单体。写出VIII的单体的合成路线_______(不用注明反应条件)。
5.(2022·湖南卷)物质J是一种具有生物活性的化合物。该化合物的合成路线如下:
已知:① + ;
②
回答下列问题:
(1)A中官能团的名称为_______、_______;
(2)F→G、G→H的反应类型分别是_______、_______;
(3)B的结构简式为_______;
(4)C→D反应方程式为_______;
(5) 是一种重要的化工原料,其同分异构体中能够发生银镜反应的有_______种(考虑立体异
构),其中核磁共振氢谱有3组峰,且峰面积之比为 的结构简式为_______;
(6)Ⅰ中的手性碳原子个数为_______(连四个不同的原子或原子团的碳原子称为手性碳原子);
(7)参照上述合成路线,以 和 为原料,设计合成 的路线
_______(无机试剂任选)。