文档内容
专题 11 物质结构与元素周期律
目录
01 模拟基础练
【题型一】原子结构 核素
【题型二】元素周期表 元素周期律
【题型三】微粒间的相互作用力
【题型四】杂化轨道理论与分子空间构型
【题型五】简单晶体结构分析及晶胞计算
02 重难创新练
03 真题实战练
题型一 原子结构 核素
1.(2024·河南平顶山高三第一次质量检测)氚管是一种应用在深海夜光手表中的发光装置。其主要结
构是在一个密闭玻璃管中充入氚气,由氚在β衰变时释放出的电子射中涂在玻璃管内部的荧光粉,发出荧
光。下列说法错误的是( )
A.氚原子核内中子数为2 B.β衰变属于化学变化
C.H、D、T互为同位素 D.含有氚的废水具有放射性
2.“嫦娥五号”顺利将 月壤带回地球。科学家发现月壤中有地球土壤中没有的3He。3He是一
种优良的核反应原料,与氘发生核聚变反应,放出巨大的能量: ,下列有关说法正确
的是( )
A.D 和H 互为同位素 B.等质量的3He和2H具有相同的中子数
2 2
C.3He与 发生的核聚变反应属于化学变化 D.3He位于周期表的第1行、第18列
3.北斗导航系统上使用的原子钟是世界上最准确的原子钟——2000万年相差一秒,该原子钟上使用
的核素是 ,已知铯是第ⅠA族元素,下列说法错误的是( )
A.Cs元素的相对原子质量为137 B.CsOH溶液能溶解氧化铝C. 与 核外电子层结构相同 D.酚酞遇CsCO 溶液变红色
2 3
4.钋-210属于极毒性放射性元素,以相同重量来比较,钋-210的毒性是氰化物的2.5亿倍,只需
一颗尘埃大小就足以取人性命,而且没有解毒剂。下列有关210 P 说法正确的是( )
84 O
A. 与 互为同素异形体 B. 与 互为同位素
C. 的质子数为84,中子数为126 D.Po元素的相对原子质量为210
5.我国新一代“人造太阳”HL-2M“托卡马克”装置近日取得突破性进展,等离子体电流突破1兆安
培,距离可控核聚变点火又近了一步。“人造太阳”中的核聚变反应之一为 H+ H→ He+ n。下列说法
错误的是( )
A.常温同压下,等质量的3H、1H 体积之比为1∶3
1 2 1 2
B.2HO与1HO化学性质基本相同
1 2 1 2
C.1mol3H的中子数比1mol2H的多1mol
1 1
D.3HO能稳定存在于自然界中
1 2
题型二 元素周期表 元素周期律
6.元素X的原子,其M层与K层电子数相同;元素Y的原子,其L层上有5个电子。X和Y所形成
的稳定化合物的摩尔质量为( )
A.148 g·mol-1 B.100 g·mol-1 C.90 g·mol-1 D.38 g·mol-1
7.下列事实不能用元素周期律解释的是( )
A.HSO 的酸性强于HSiO B. 与热水能反应,Al与热水很难反应
2 4 2 3
C.HO的稳定性强于HS D.HI的沸点高于HBr
2 2
8.下列关于物质的结构与性质的叙述正确的是( )
A.Li、Na同主族, Na保存在煤油中,可推断Li也保存在煤油中
B.Be、Mg同主族,MgO不溶于强碱,可推断BeO也不溶于强碱
C.Ge、Pb同主族,Ge可作半导体材料,可推断Pb也可作半导体材料
D.O、S同主族,HO 有氧化性,可推断HS 也有氧化性
2 2 2 2
9.下列有关物质性质的比较正确的是( )
A.碱性:Ba(OH) <Ca(OH) <KOH B.离子半径:Mg2+<O2-<F--
2 2
C.还原性:SiH>PH >HCl D.热稳定性:CH>NH >HF
4 3 4 3
10.X、Y、Z、W、R五种前20号主族元素,原子序数依次增大。基态X原子中有3个未成对电子,Z是元素周期表中电负性最大的元素,Y和W同主族,常温下0.01mol·L-1R的最高价氧化物对应的水化物溶
液的pH=12。下列说法正确的是( )
A.简单离子半径:r(W) I (Y )> I (Z ) D.简单氢化物的键角:Y>W
1 1 1
11.W、X、Y、Z为原子序数依次增大的短周期主族元素,W的最高正价与最低负价代数和为0,X
的最高能级不同轨道都有电子且自旋方向相同,Y的最外层电子数为偶数,Z的核外电子数等于X与Y的
最外层电子数之和。下列说法不正确的是( )
A.第一电离能:X>Y B.W、X、Y可能形成离子晶体
C.原子半径:Z>Y>X D.W与Z形成的化合物中可能含有非极性键
12.某种天然硅酸盐矿石主要成分的化学式为R[Z WY ]•3X Y,其中X、Y、Z、W、R是主族元素,
2 3 10 2
原子序数依次增大,且处于四个不同周期。Y元素是地壳中含量最高的元素,化合物 RY在实验室中常用
作干燥剂。下列说法正确的是( )
A.原子半径:W>Z>Y B.工业制备Z单质采用热还原法
C.X和R形成的化合物,X显负价 D.W的最高价氧化物可溶于稀硝酸
题型三 微粒间的相互作用力
13.物质发生下列变化时,需克服的作用力不属于化学键的是( )
A.HCl溶于水 B.I 升华 C.HO电解 D.烧碱熔化
2 2
14.对下列物质溶于水时破坏的作用力描述错误的是( )
A.氯化钠,破坏了离子键 B.氯化氢,破坏了共价键
C.蔗糖,破坏了分子间作用力 D.二氧化碳,没有破坏作用力
15.下列各组物质的晶体中,化学键类型相同,熔化时所克服的作用力也完全相同的是
A.CO 和SiO B.NaCl和HCl C.(NH )CO 和CO(NH) D.NaH和KCl
2 2 4 2 3 2 2
16.下列各物质中,按熔点由高到低的顺序排列正确的是( )
A.CH>SiH >GeH>SnH B.KCl>NaCl>MgCl >MgO
4 4 4 4 2
C.Rb>K>Na>Li D.金刚石>Si>钠
17.NF 可由NH 和F 在Cu催化剂存在下反应直接得到:4NH +3F=====NF +3NH F,该化学方程
3 3 2 3 2 3 4
式中的5种物质不所含的晶体类型有( )
A.离子晶体 B.分子晶体 C.共价晶体 D.金属晶体
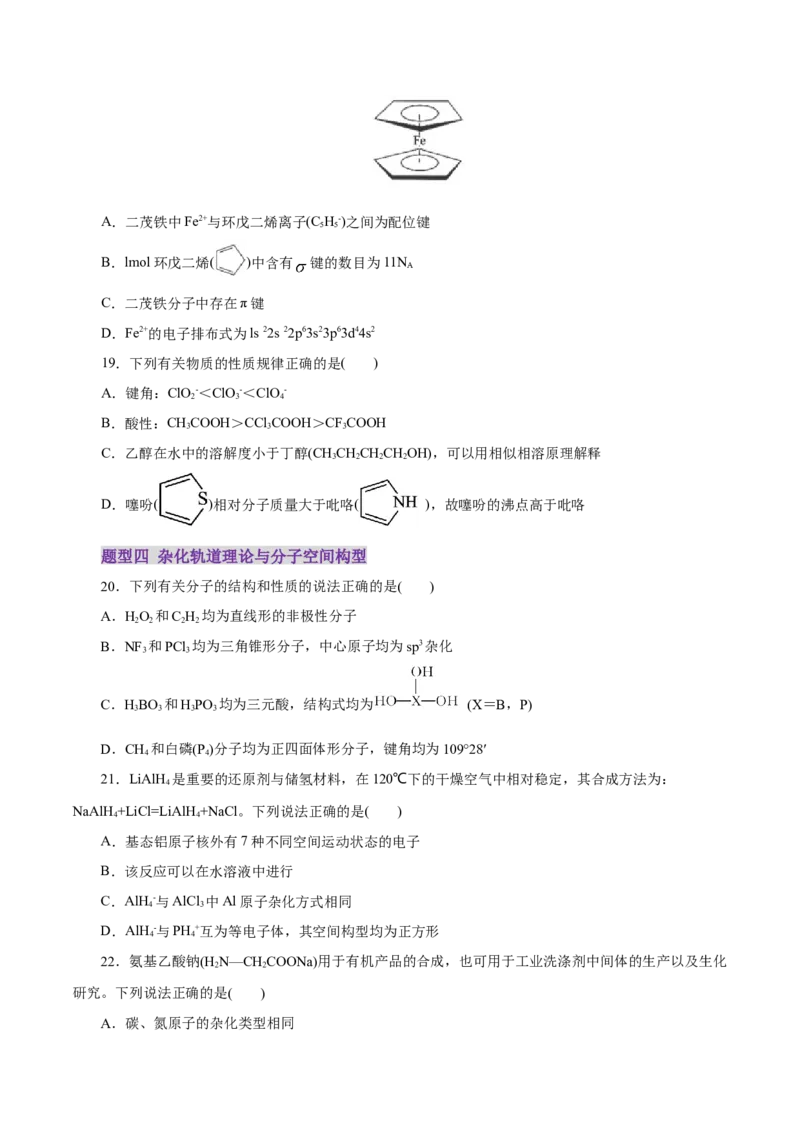
18.二茂铁[(C H)Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,
5 5 2
可作为导弹和卫星的涂料等。它的结构如图所示,下列说法不正确的是( )A.二茂铁中Fe2+与环戊二烯离子(C H-)之间为配位键
5 5
B.lmol环戊二烯( )中含有 键的数目为11N
A
C.二茂铁分子中存在π键
D.Fe2+的电子排布式为ls 22s 22p63s23p63d44s2
19.下列有关物质的性质规律正确的是( )
A.键角:ClO -<ClO -<ClO -
2 3 4
B.酸性:CHCOOH>CCl COOH>CFCOOH
3 3 3
C.乙醇在水中的溶解度小于丁醇(CHCHCHCHOH),可以用相似相溶原理解释
3 2 2 2
D.噻吩( )相对分子质量大于吡咯( ),故噻吩的沸点高于吡咯
题型四 杂化轨道理论与分子空间构型
20.下列有关分子的结构和性质的说法正确的是( )
A.HO 和C H 均为直线形的非极性分子
2 2 2 2
B.NF 和PCl 均为三角锥形分子,中心原子均为sp3杂化
3 3
C.HBO 和HPO 均为三元酸,结构式均为 (X=B,P)
3 3 3 3
D.CH 和白磷(P )分子均为正四面体形分子,键角均为109°28′
4 4
21.LiAlH 是重要的还原剂与储氢材料,在120℃下的干燥空气中相对稳定,其合成方法为:
4
NaAlH +LiCl=LiAlH +NaCl。下列说法正确的是( )
4 4
A.基态铝原子核外有7种不同空间运动状态的电子
B.该反应可以在水溶液中进行
C.AlH-与AlCl 中Al原子杂化方式相同
4 3
D.AlH-与PH +互为等电子体,其空间构型均为正方形
4 4
22.氨基乙酸钠(H N—CH COONa)用于有机产品的合成,也可用于工业洗涤剂中间体的生产以及生化
2 2
研究。下列说法正确的是( )
A.碳、氮原子的杂化类型相同B.氨基乙酸钠中N原子的价层电子对数为4
C.1 mol氨基乙酸钠分子中所含σ键的物质的量为10 mol
D.氮原子和与其成键的另外三个原子在同一平面内
23.CHOH、NH 和(CH)NNH 均为常见的燃料,关于这三者的结构与性质,下列说法不正确的是(
3 2 4 3 2 2
)
A.CHOH的电子式为
3
B.NH 空间结构为平面形
2 4
C.CHOH、NH 和(CH)NNH 都易溶于水
3 2 4 3 2 2
D.CHOH和(CH)NNH中C、O、N杂化方式均相同
3 3 2
24.一定条件下发生反应:Fe+6HCN+2KCO=K [Fe(CN) ]+H↑+2CO↑+2HO。下列说法正确的
2 3 4 6 2 2 2
是( )
A.K[Fe(CN) ]的中心原子的核外电子排布式为[Ar]3d5
4 6
B.该反应中只存在离子键和共价键的断裂和形成
C.HCN、CO、CO2-中碳的杂化方式和空间构型均相同
2 3
D.HCN 水溶液中存在 4 种氢键
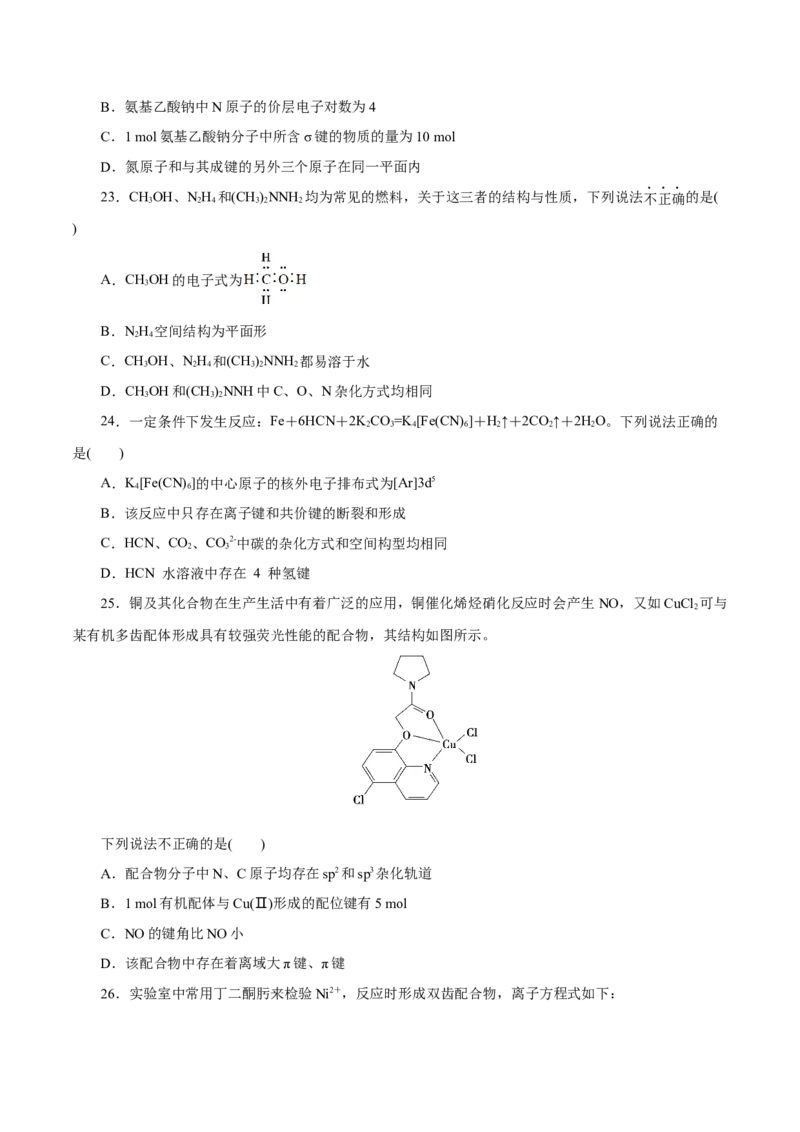
25.铜及其化合物在生产生活中有着广泛的应用,铜催化烯烃硝化反应时会产生NO,又如CuCl 可与
2
某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。
下列说法不正确的是( )
A.配合物分子中N、C原子均存在sp2和sp3杂化轨道
B.1 mol有机配体与Cu(Ⅱ)形成的配位键有5 mol
C.NO的键角比NO小
D.该配合物中存在着离域大π键、π键
26.实验室中常用丁二酮肟来检验Ni2+,反应时形成双齿配合物,离子方程式如下:下列说法不正确的是( )
A.基态Ni2+的电子排布式为1s22s22p63s23p63d8
B.丁二酮肟分子中碳原子与氮原子的杂化方式均为sp3
C.每个二(丁二酮肟)合镍(Ⅱ)含有32个σ键
D.二(丁二酮肟)合镍(Ⅱ)的中心原子的配体数目和配位数分别为2、4
题型五 简单晶体结构分析及晶胞计算
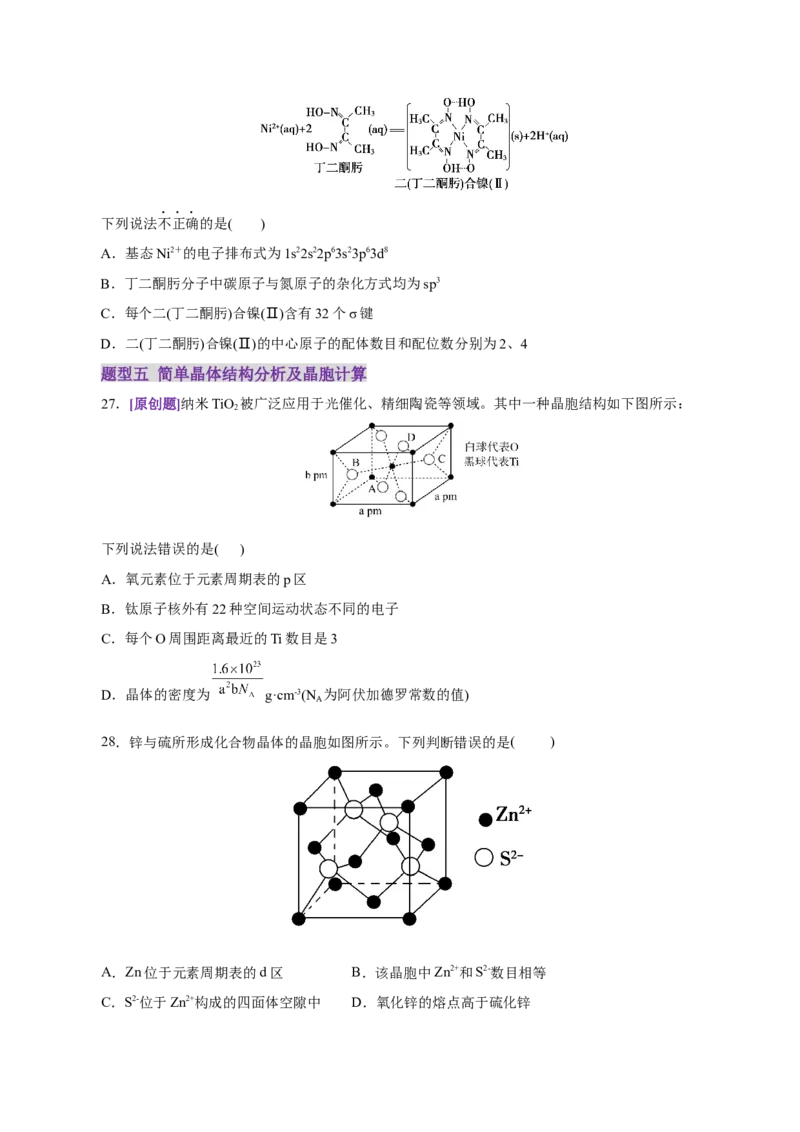
27.[原创题]纳米TiO 被广泛应用于光催化、精细陶瓷等领域。其中一种晶胞结构如下图所示:
2
下列说法错误的是( )
A.氧元素位于元素周期表的p区
B.钛原子核外有22种空间运动状态不同的电子
C.每个O周围距离最近的Ti数目是3
D.晶体的密度为 g·cm-3(N 为阿伏加德罗常数的值)
A
28.锌与硫所形成化合物晶体的晶胞如图所示。下列判断错误的是( )
A.Zn位于元素周期表的d区 B.该晶胞中Zn2+和S2-数目相等
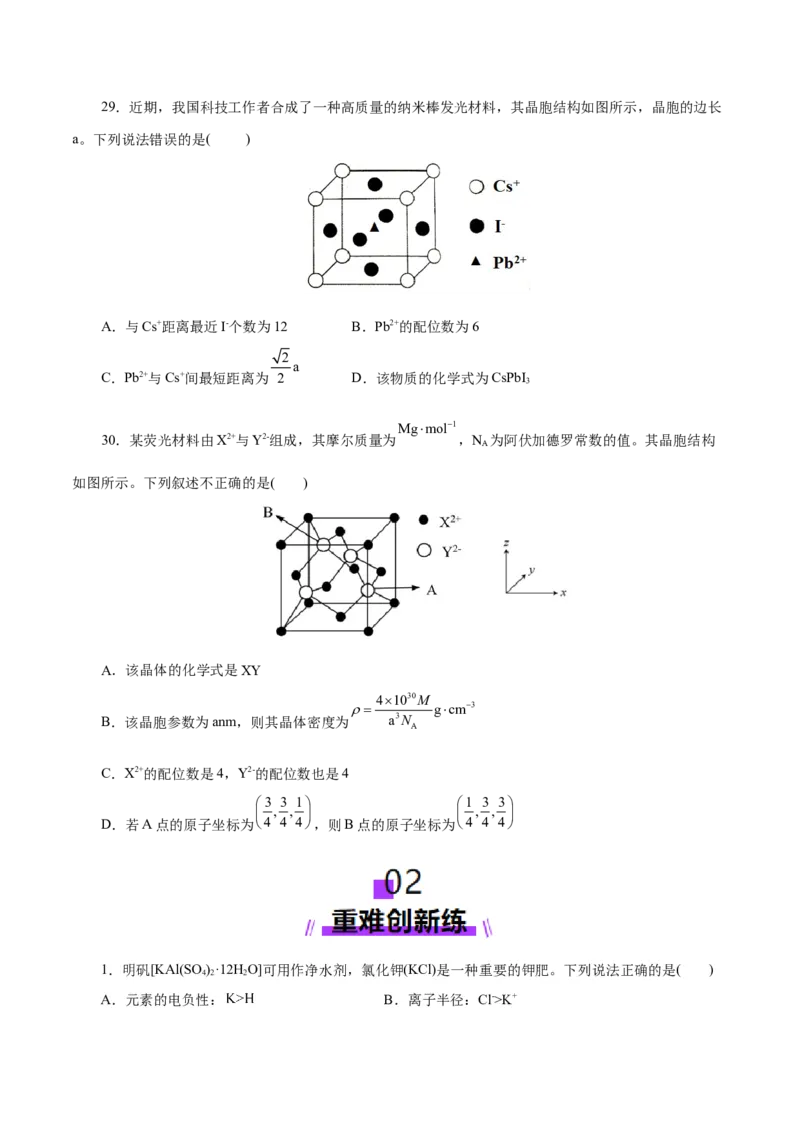
C.S2-位于Zn2+构成的四面体空隙中 D.氧化锌的熔点高于硫化锌29.近期,我国科技工作者合成了一种高质量的纳米棒发光材料,其晶胞结构如图所示,晶胞的边长
a。下列说法错误的是( )
A.与Cs+距离最近I-个数为12 B.Pb2+的配位数为6
2
a
C.Pb2+与Cs+间最短距离为 2 D.该物质的化学式为CsPbI
3
Mgmol1
30.某荧光材料由X2+与Y2-组成,其摩尔质量为 ,N 为阿伏加德罗常数的值。其晶胞结构
A
如图所示。下列叙述不正确的是( )
A.该晶体的化学式是XY
41030M
gcm3
B.该晶胞参数为anm,则其晶体密度为 a3N
A
C.X2+的配位数是4,Y2-的配位数也是4
3 3 1 1 3 3
, , , ,
D.若A点的原子坐标为4 4 4,则B点的原子坐标为4 4 4
1.明矾[KAl(SO)·12H O]可用作净水剂,氯化钾(KCl)是一种重要的钾肥。下列说法正确的是( )
4 2 2
A.元素的电负性: B.离子半径:Cl->K+C.元素的第一电离能:S>O D.碱性:Al(OH) >KOH
3
2.关于CHOH、NH 和(CH)NNH 的结构与性质,下列说法不正确的是( )
3 2 4 3 2 2
A.CHOH为极性分子
3
B.NH 空间结构为平面形
2 4
C.NH 的沸点高于(CH)NNH 的原因是NH 分子间氢键数目更多
2 4 3 2 2 2 4
D.CHOH和(CH)NNH 中C、O、N杂化方式均相同
3 3 2 2
3.SO 及其三聚体环状结构如图所示。下列说法不正确的是( )
3
A.SO 与CO2-、NO -互为等电子体,空间结构都为平面三角形
3 3 3
B.SO 为非极性分子,中心原子杂化类型sp3
3
C.三聚体环状结构中S与O形成的共价键的键长有a、b两类
D.该三聚体环状结构中含有12个σ键
4.二氧化氯(ClO )是一种黄绿色气体,易溶于水,在水中的溶解度约为Cl 的5倍,其水溶液在较高
2 2
温度与光照下会生成ClO -与ClO -。ClO 是一种极易爆炸的强氧化性气体,实验室制备ClO 的反应为
2 3 2 2
2NaClO +SO+H SO =2ClO +2NaHSO 下列关于ClO 、ClO -、ClO -的说法正确的是( )
3 2 2 4 2 4 2 2 3
A.ClO 分子是极性分子 B.ClO -中含有非极性键
2 2
C.ClO -的空间构型为平面三角形 D.ClO -与ClO -的键角相等
3 2 3
5.氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反
应为N(g)+3H(g) 2NH (g)ΔH=-92.4kJ·mol-1。实验室用加热NH Cl和Ca(OH) 固体混合物的方法制取
2 2 3 4 2
少量氨气;侯氏制碱法用氨气、二氧化碳,与饱和食盐水制备纯碱碳酸钠。下列有关NH 、NF 、NH +、
3 3 4
NO -、NO -等含氮粒子的说法正确的是( )
2 3
A.NH 中N-H键角比NH +中N-H键角大
3 4
B.NH 极易溶于水,主要原因是NH 分子间能形成氢键
3 3
C.NH 的水溶液能导电,但一水合氨不能完全电离,因此NH 属于弱电解质
3 3
D.NH 、NF 的空间构型都是三角锥型,NO -、NO -中的N都是sp2杂化
3 3 2 3
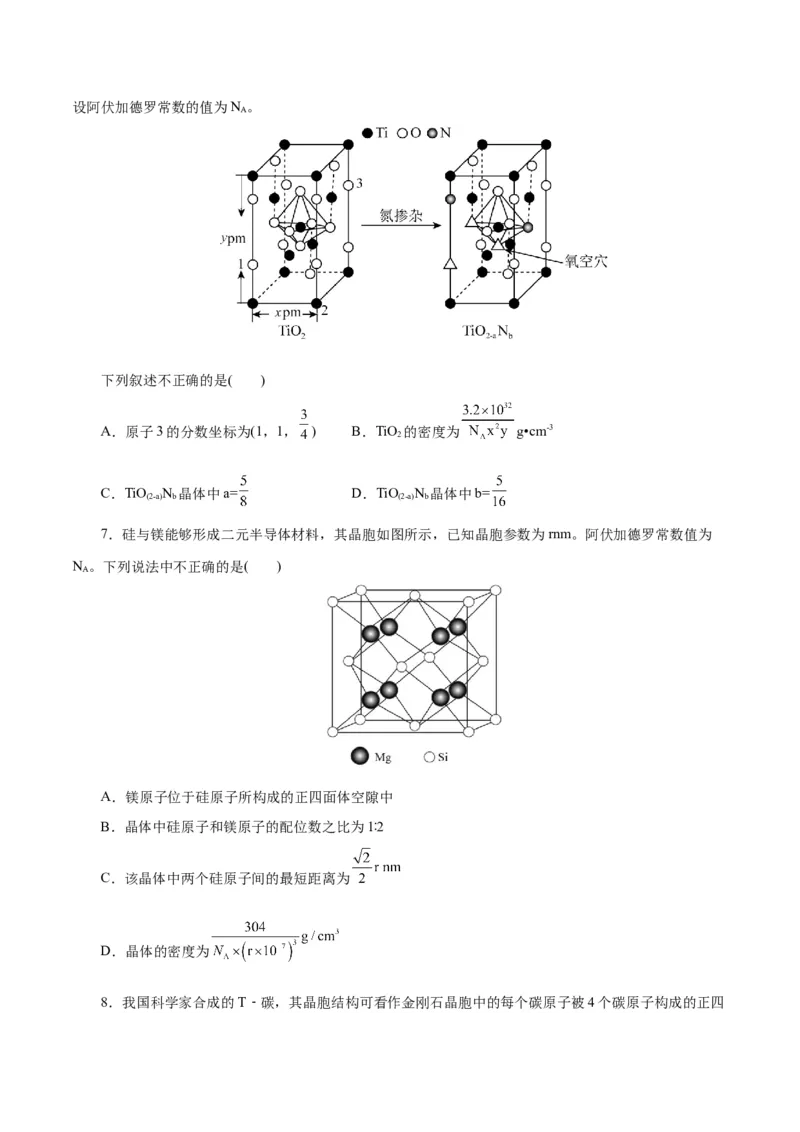
6.TiO 通过氮掺杂生成TiO N 的反应如图。已知原子1、2的分数坐标为(0,0, )和(1,0,0),
2 (2-a) b设阿伏加德罗常数的值为N 。
A
下列叙述不正确的是( )
A.原子3的分数坐标为(1,1, ) B.TiO 的密度为 g•cm-3
2
C.TiO N 晶体中a= D.TiO N 晶体中b=
(2-a) b (2-a) b
7.硅与镁能够形成二元半导体材料,其晶胞如图所示,已知晶胞参数为rnm。阿伏加德罗常数值为
N 。下列说法中不正确的是( )
A
A.镁原子位于硅原子所构成的正四面体空隙中
B.晶体中硅原子和镁原子的配位数之比为1∶2
C.该晶体中两个硅原子间的最短距离为
D.晶体的密度为
8.我国科学家合成的T﹣碳,其晶胞结构可看作金刚石晶胞中的每个碳原子被4个碳原子构成的正四面体单元替代,如图所示。T﹣碳的密度为金刚石的一半。下列说法不正确的是( )
A.每个T﹣碳晶胞中碳原子个数为32
B.T﹣碳与金刚石中碳原子的杂化方式相同
C.T﹣碳中碳原子数与共价键数之比为1:2
D.T﹣碳晶胞边长和金刚石晶胞边长之比为1:2
9.[Co(NH )]Cl 晶体的晶胞如下图所示(己知该立方晶胞的边长为 ,阿伏加德罗常数为N ,
3 6 2 A
[Co(NH )]Cl 的摩尔质量为 )。以下说法不正确的是( )
3 6 2
A.若规定A点原子坐标为 ,B点原子坐标为 ,则C点原子坐标为
B.离[Co(NH )]2+最近的 有8个
3 6
C.[Co(NH )]Cl 中,中心离子的配位数为8
3 6 2
D.[Co(NH )]Cl 晶体的密度为
3 6 2
1.(2024·北京卷,12,3分)下列依据相关数据作出的推断中,不正确的是( )
A.依据相同温度下可逆反应的Q与K大小的比较,可推断反应进行的方向B.依据一元弱酸的K,可推断它们同温度同浓度稀溶液的 大小
a
C.依据第二周期主族元素电负性依次增大,可推断它们的第一电离能依次增大
D.依据F、Cl、Br、I的氢化物分子中氢卤键的键能,可推断它们的热稳定性强弱
2.(2024·河北卷,8,3分)从微观视角探析物质结构及性质是学习化学的有效方法。下列实例与解释
不符的是( )
选项 实例 解释
A 原子光谱是不连续的线状谱线 原子的能级是量子化的
孤电子对与成键电子对的斥力大
B CO、CHO、CCl 键角依次减小
2 2 4 于成键电子对之间的斥力
CsCl晶体中Cs+与8个Cl-配位,而NaCl晶体中
C Cs+比Na+的半径大
Na+与6个Cl-配位
各步中的C-H键所处化学环境不
D 逐个断开CH 中 的C-H键,每步所需能量不同
4 同
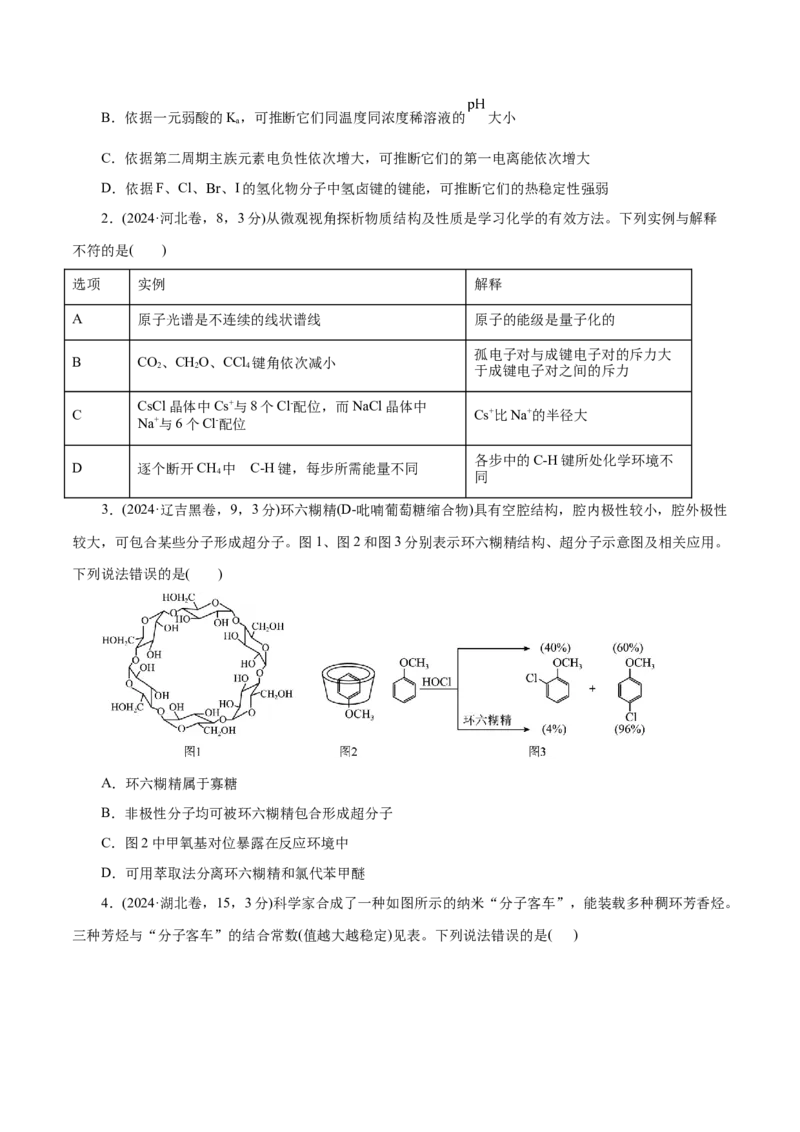
3.(2024·辽吉黑卷,9,3分)环六糊精(D-吡喃葡萄糖缩合物)具有空腔结构,腔内极性较小,腔外极性
较大,可包合某些分子形成超分子。图1、图2和图3分别表示环六糊精结构、超分子示意图及相关应用。
下列说法错误的是( )
A.环六糊精属于寡糖
B.非极性分子均可被环六糊精包合形成超分子
C.图2中甲氧基对位暴露在反应环境中
D.可用萃取法分离环六糊精和氯代苯甲醚
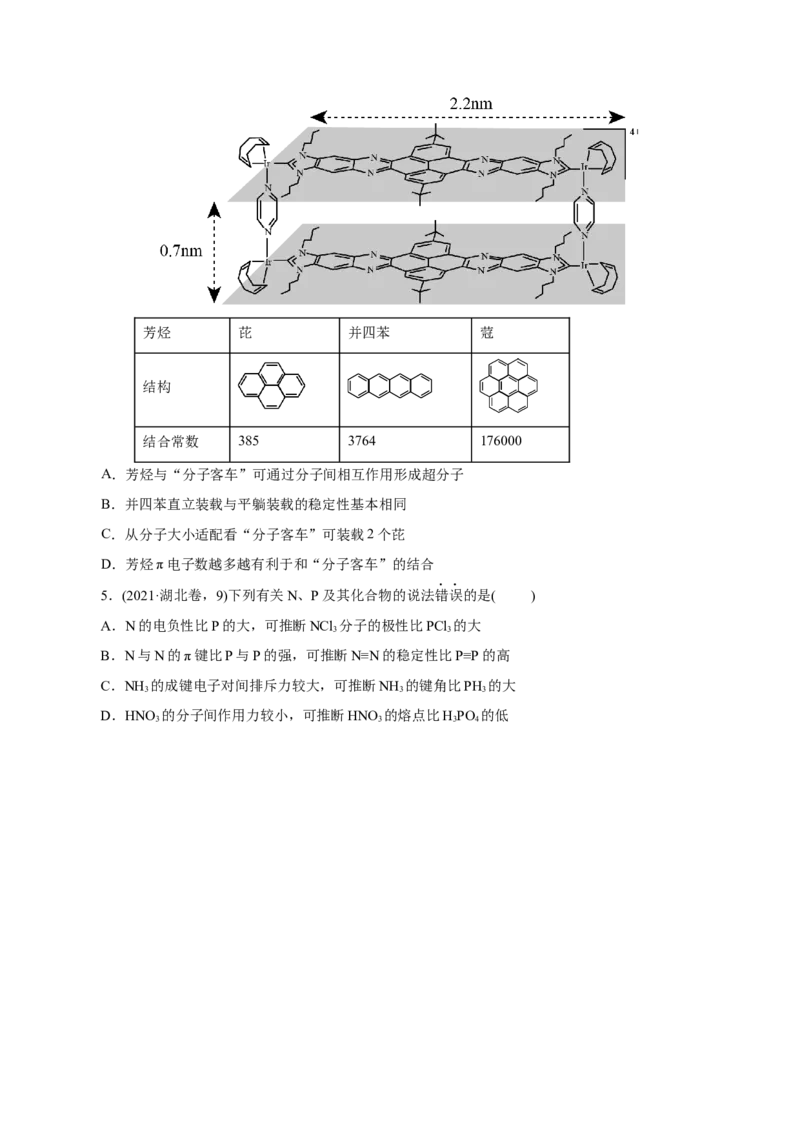
4.(2024·湖北卷,15,3分)科学家合成了一种如图所示的纳米“分子客车”,能装载多种稠环芳香烃。
三种芳烃与“分子客车”的结合常数(值越大越稳定)见表。下列说法错误的是( )芳烃 芘 并四苯 蒄
结构
结合常数 385 3764 176000
A.芳烃与“分子客车”可通过分子间相互作用形成超分子
B.并四苯直立装载与平躺装载的稳定性基本相同
C.从分子大小适配看“分子客车”可装载2个芘
D.芳烃π电子数越多越有利于和“分子客车”的结合
5.(2021·湖北卷,9)下列有关N、P及其化合物的说法错误的是( )
A.N的电负性比P的大,可推断NCl 分子的极性比PCl 的大
3 3
B.N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高
C.NH 的成键电子对间排斥力较大,可推断NH 的键角比PH 的大
3 3 3
D.HNO 的分子间作用力较小,可推断HNO 的熔点比HPO 的低
3 3 3 4