文档内容
1.下列装置能达到实验目的的是
选项 A B C D
实验
[来源:学科网
装置
ZXXK]
探究NaCO 和 用已知浓度的NaOH
实验 2 3 检验蔗糖与浓硫酸反应 验证镁和稀盐酸的反
NaHCO 溶解度的相对 溶液滴定未知浓度的
目的 3 产生的CO 应的热效应
大小 稀硫酸 2
【答案】A
2.下列实验方案不能达到实验目的的是
A.图A装置Cu和浓硝酸制取NO B.图B装置实验室制备Cl
2
C.图C装置实验室制取乙酸乙酯 D.图D装置实验室分离CO和CO
2
【答案】C
【解析】A.Cu和浓硝酸反应生成二氧化氮,二氧化氮和水反应生成一氧化氮,可制取NO,故A不符合题意;B.浓盐酸和高锰酸钾溶液生成氯气,氯气与氢氧化钠反应进行尾气吸收,故B不符合题意;C.乙酸乙酯在
NaOH溶液中水解,应选饱和碳酸钠溶液,故C符合题意;D.要将CO和CO 分离,足量纯碱溶液用来吸收
2
CO,先收集到干燥的CO;滴加稀硫酸,再将生成的CO 用浓硫酸干燥,收集到纯净的CO,故D不符合题意。
2 2 2
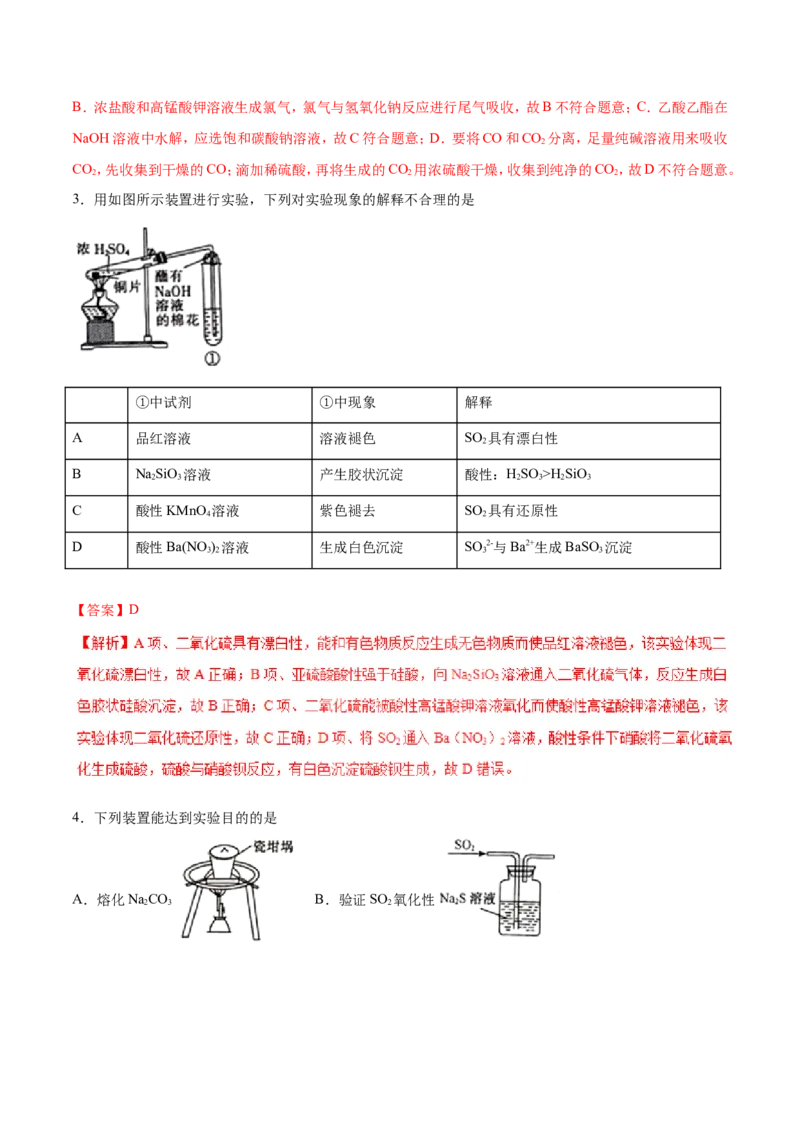
3.用如图所示装置进行实验,下列对实验现象的解释不合理的是
[来源:Zxxk.Com]
①中试剂 ①中现象 解释
A 品红溶液 溶液褪色 SO 具有漂白性
2
B NaSiO 溶液 产生胶状沉淀 酸性:HSO >H SiO
2 3 2 3 2 3
C 酸性KMnO 溶液 紫色褪去 SO 具有还原性
4 2
D 酸性Ba(NO ) 溶液 生成白色沉淀 SO 2-与Ba2+生成BaSO 沉淀
3 2 3 3
【答案】D
4.下列装置能达到实验目的的是
[来源:学_科_网Z_X_X_K]
A.熔化NaCO B.验证SO 氧化性
2 3 2C.实验室制取NH D.保存液溴
3
【答案】B
5.某化学学习小组用如图所示装置制备、收集Cl,并进行性质验证实验(夹持装置略去)。下列说法正确的是
2
A.用KMnO 和浓盐酸制备Cl 时,只选①
4 2
B.③用于Cl 收集时,a为进气口
2
C.④中加入NaBr溶液和CCl ,通入Cl 反应后振荡、静置,下层溶液呈橙红色
4 2
D.⑤中通入Cl 使品红溶液褪色后,取出溶液加热可恢复红色
2
【答案】C
【解析】A. KMnO 和浓盐酸反应制备Cl,①不可行,高锰酸钾可溶于水,氯气可以从长颈漏斗中逸出。选②可
4 2
达到实验目的,故A项错误;B. 排空气法收集氯气时,因氯气的密度比空气大,则应从b进气,故B项错误;
C. Cl 的氧化性比Br 大,通入NaBr溶液中,会发生氧化还原反应生成Br ,进而被CCl 萃取在下层溶液中,
2 2 2 4
显橙红色,故C项正确;D. Cl 能使品红溶液褪色,主要是发生了氧化还原反应,不可逆,因此取出溶液加热
2
不能恢复红色,故D项错误。
6.下列选用的仪器和药品能达到实验目的的是
[来源:学科网ZXXK]A.准确量取一定体积的
B.验证SO 漂白性 C.制NH 的发生装置 D.排空气法收集CO
KMnO 溶液 2 3 2
4
【答案】B
7.用下列实验装置进行相应的实验,能达到实验目的的是
A. 所示装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验
B. 所示装置验证二氧化硫的漂白性
C. 所示装置分离四氯化碳和苯的混合物D. 所示装置检验氯化铵受热分解生成的两种气体
【答案】D
8.实验室根据“侯氏制碱法”原理制备少量NaHCO :NH +CO +H O+NaCl=NaHCO ↓+NHCl。其实验包括
3 3 2 2 3 4
制取氨气→ 制取NaHCO →分离NaHCO →干燥NaHCO 四个步骤。下列实验必须选用的主要仪器正确的
3 3 3
是:
A.制取氨气,可选用②③
B.制取NaHCO ,可选用④⑦⑨
3
C.分离NaHCO ,可选用④⑤⑥⑦
3
D.干燥NaHCO ,可选用②③⑦⑧
3
【答案】A
【解析】A.实验室常用NH Cl和Ca(OH) ,固体加热,选择仪器②③,A项正确;B.制取NaHCO ,在饱和氯化钠
4 2 3
溶液中依次通入NH 和CO,只需要⑨,B项错误;C.分离NaHCO ,过滤,需要④⑤⑦,C项错误;
3 2 3
D.干燥NaHCO ,干燥固体,需要①②⑦⑧,D项错误。
3
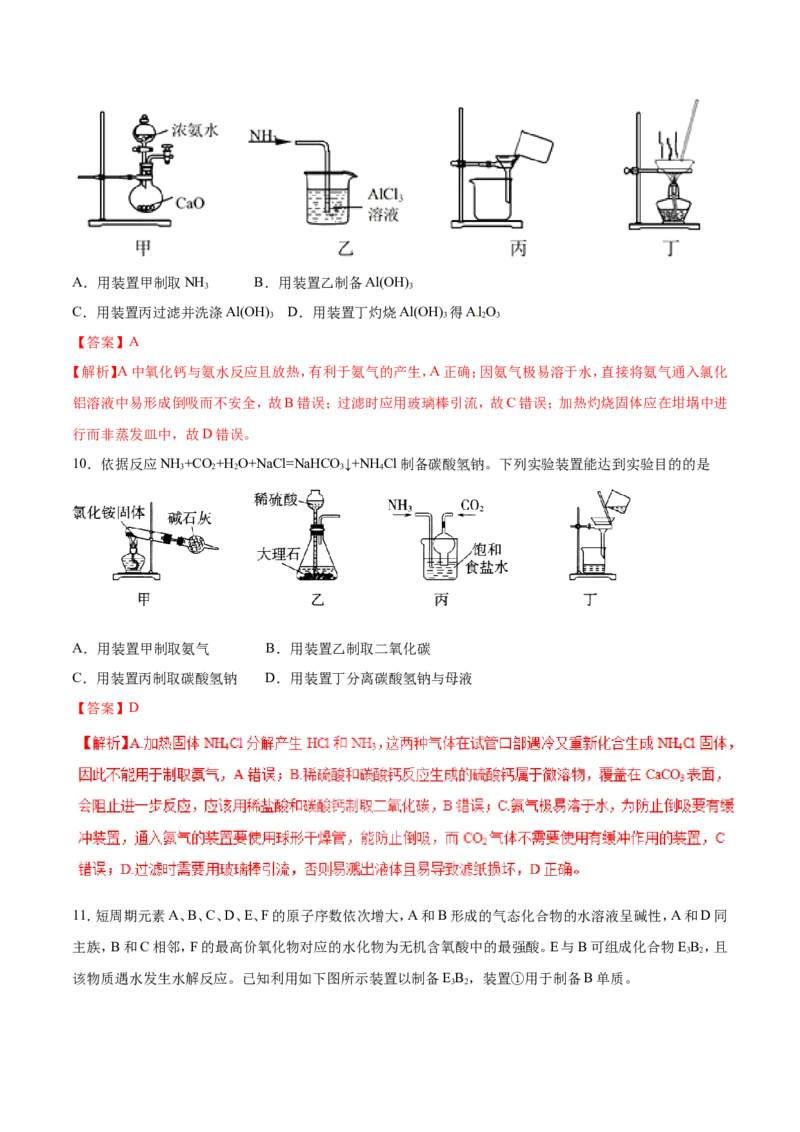
9.实验室将NH 通入AlCl 溶液中制备Al(OH) ,经过滤、洗涤、灼烧得Al O,下列图示装置和原理均能达到
3 3 3 2 3
实验目的是( )A.用装置甲制取NH B.用装置乙制备Al(OH)
3 3
C.用装置丙过滤并洗涤Al(OH) D.用装置丁灼烧Al(OH) 得AlO
3 3 2 3
【答案】A
【解析】A中氧化钙与氨水反应且放热,有利于氨气的产生,A正确;因氨气极易溶于水,直接将氨气通入氯化
铝溶液中易形成倒吸而不安全,故B错误;过滤时应用玻璃棒引流,故C错误;加热灼烧固体应在坩埚中进
行而非蒸发皿中,故D错误。
10.依据反应NH +CO +H O+NaCl=NaHCO ↓+NHCl制备碳酸氢钠。下列实验装置能达到实验目的的是
3 2 2 3 4
A.用装置甲制取氨气 B.用装置乙制取二氧化碳
C.用装置丙制取碳酸氢钠 D.用装置丁分离碳酸氢钠与母液
【答案】D
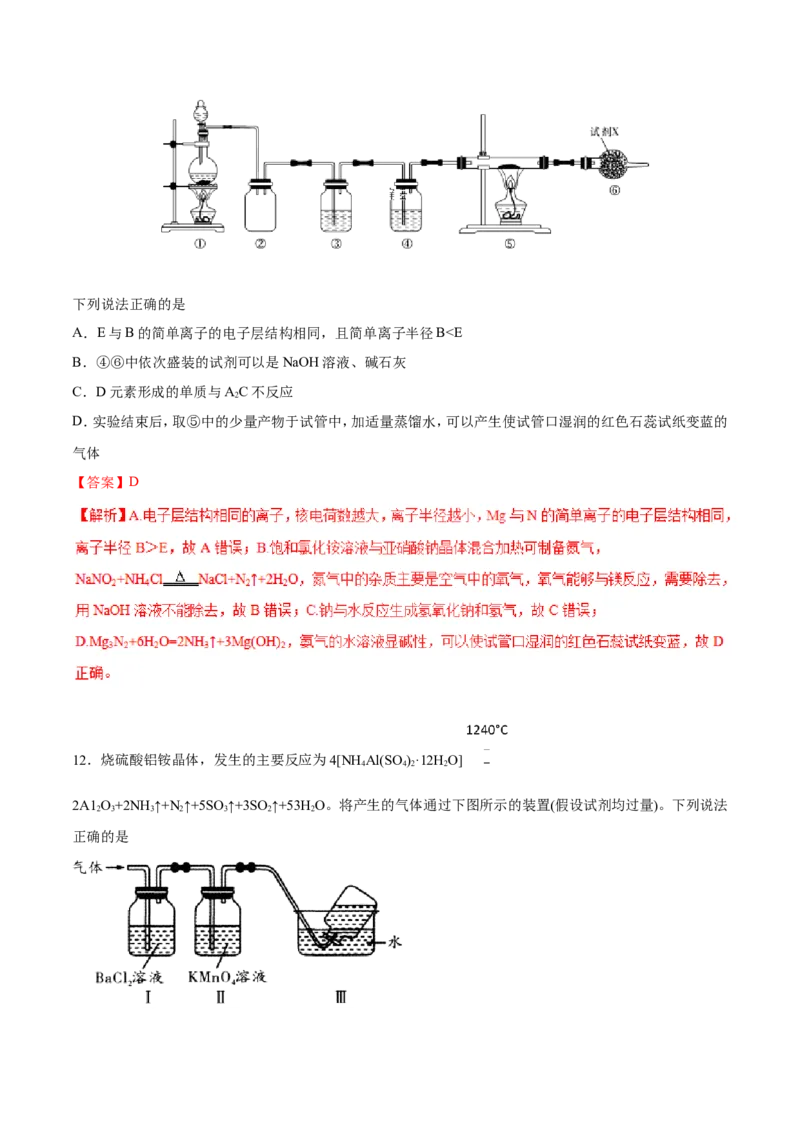
11.短周期元素A、B、C、D、E、F的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,A和D同
主族,B和C相邻,F的最高价氧化物对应的水化物为无机含氧酸中的最强酸。E与B可组成化合物EB ,且
3 2
该物质遇水发生水解反应。已知利用如下图所示装置以制备EB ,装置①用于制备B单质。
3 2下列说法正确的是
A.E与B的简单离子的电子层结构相同,且简单离子半径BC>Si B. “喷泉”实验
C. 制取并收集干燥纯净的NH D. 探究SO 的还原性和漂白性
3 2
【答案】B
【解析】A. 盐酸不是最高价氧化物对应水化物的含氧酸,且挥发出的盐酸能够使硅酸钠变浑浊,图示装置无
法达到实验目的,故A项错误;B. 图示装置中NaOH溶液与氯气反应,是瓶内气压骤降,可完成喷泉实验,故
B项正确;C. NH 的密度较小,应该采用向下排空气法收集,图中为向上排空气法,故C项错误;D. SO 与硫
3 2
化氢的反应中,二氧化硫的S元素化合价降低,表现的是氧化性,而不是还原性,故D项错误。
14.氮化铝(AlN)是一种新型无机非金属材料,常温下可与烧碱溶液发生反应:AlN+NaOH+3H O=NaA
2
l(OH) +NH↑。某课题小组利用甲图所示装置测定样品中AlN的含量(杂质不反应,量气管为碱式滴定管改造)。
4 3
下列说法正确的是
A.量气管中的液体应为水B.用长颈漏斗代替分液漏斗,有利于控制反应速率
C.反应结束时,a、b两管液面的差值即为产生气体的体积
D.若其它操作均正确,实验结束时按乙图读数,测得AlN含量偏高
【答案】D
15.用下列实验装置进行相应实验,能达到实验目的的是(夹持装置未画出)
A.用装置甲制取二氧化硫气体 B.用装置乙检验溶液中是否有钾离子
C.用装置丙验证氨气极易溶解于水 D.用装置丁加热氢氧化钠固体
【答案】C
【解析】A.浓硫酸与铜反应需要加热,该装置不能加热,故A错误;B.要透过蓝色钴玻璃观察钾的焰色反应,
故B错误;C.用装置丙进行实验时,挤压胶头滴管使少量水进入烧瓶,烧瓶内气体压强减小,气球明显变大,
说明NH 极易溶于水,故C正确;D.瓷坩埚中含有二氧化硅,高温条件下可与氢氧化钠反应,则用瓷坩埚加热
3
氢氧化钠,易导致坩埚炸裂,故D错误。
16.关于下列各实验或装置的叙述中,正确的是
A.实验①可用于制取氨气B.实验②中最后一滴NaOH标准液使溶液由无色变为红色,即达到滴定终点
C.装置③可用于吸收尾气中少量NH 或HCl,并防止倒吸
3
D.装置④可用于从酒精水溶液中制取无水乙醇
【答案】C
17.氮化锂(Li N)常作固体电解质和催化剂,遇水蒸气剧烈反应生成氢氧化锂和氨气。某实验小组用一瓶氮气
3
样品制备纯净的氮化锂的装置如图所示。
已知:连苯三酚碱性溶液能定量吸收少量O,氯化亚铜盐酸溶液能定量吸收少量CO生成Cu(CO)Cl·H O且
2 2
易被O 氧化;在加热条件下,CO 与锂发生剧烈反应。下列说法正确的是
2 2
A.干燥管e中试剂为无水CuSO ,用于检验氮气中的水蒸气
4
B.为了减少气体用量,先点燃酒精灯再通入氮气
C.a、c中试剂分别为连苯三酚碱性溶液、浓硫酸
D.a装置可以换成盛装赤热铜粉的硬质玻璃管
【答案】C
【解析】A.干燥管e主要作用是防止外界空气中的二氧化碳和水蒸气进入,干扰实验,应该装有碱石灰,故A
错误;B.未发生反应前,装置中有空气,空气中含有氧气和二氧化碳,会干扰实验,在加热以前,需要先通入一
段时间气体,排尽装置中的空气,故B错误;C. 原料气中干扰气体要依次除去,a中盛放连苯三酚碱性溶液除
去氧气,b中盛放氯化亚铜盐酸溶液除去一氧化碳,c中盛放浓硫酸干燥,故C正确;D. a装置若换成盛装赤
热铜粉的硬质玻璃管,可除去氧气,但同时生成的氧化铜可以和一氧化碳继续反应,生成二氧化碳,干扰实验,
故D错误。
18.某研究性小组为了探究石蜡油分解产物,设计了如下实验方案。下列说法错误的是A.石蜡油是石油减压蒸馏的产物
B.碎瓷片加快了石蜡油的分解
C.酸性高锰酸钾溶液褪色说明生成了乙烯
D.溴的四氯化碳溶液褪色是因为发生了加成反应
【答案】C
19.用下列实验装置和方法进行相应实验,能达到实验目的的是
A.用装置甲制备SO
2
B.用装置乙从碘水溶液中萃取碘
C.用装置丙除去粗盐溶液中混有的KCl杂质
D.用装置丁蒸干溶液获得(NH )CO 晶体
4 2 3
【答案】B
【解析】A.浓硫酸与铜在加热的条件下生成SO ,而装置甲中没有加热仪器,所以用装置甲不能达到实验目的,
2
A项错误;B.碘在苯中的溶解度比在水中的溶解度大且苯与水互不相溶,萃取剂和装置的选择都正确,所以
用装置乙可以达到实验目的,B项正确;C.KCl易溶于水,过滤操作无法除去粗盐溶液中的KCl杂质,所以用装置丙无法达到实验目的,C项错误;D.(NH )CO 受热易分解:(NH )CO 2NH ↑+CO ↑+H O,所以用装置丁
4 2 3 4 2 3 3 2 2
无法达到实验目的。D项错误。
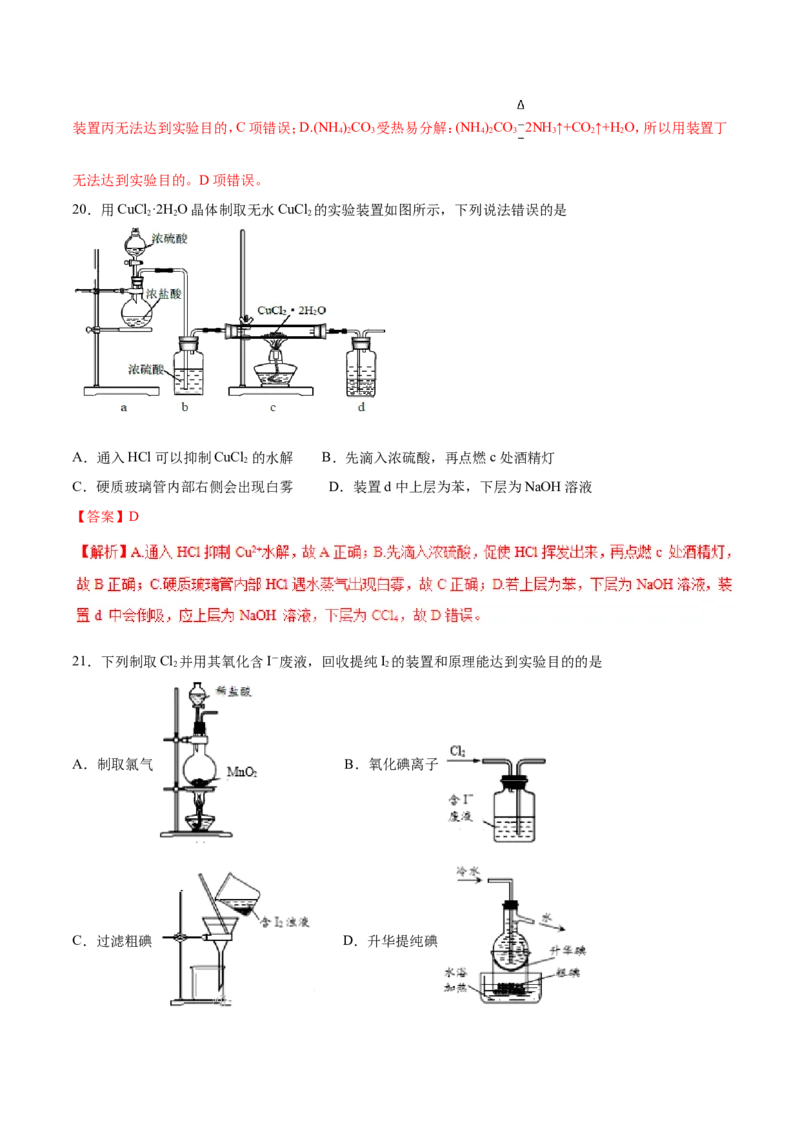
20.用CuCl ·2H O晶体制取无水CuCl 的实验装置如图所示,下列说法错误的是
2 2 2
A.通入HCl 可以抑制CuCl 的水解 B.先滴入浓硫酸,再点燃c 处酒精灯
2
C.硬质玻璃管内部右侧会出现白雾 D.装置d 中上层为苯,下层为NaOH 溶液
【答案】D
21.下列制取Cl 并用其氧化含I-废液,回收提纯I 的装置和原理能达到实验目的的是
2 2
A.制取氯气 B.氧化碘离子
C.过滤粗碘 D.升华提纯碘【答案】D
22.用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是
A.若A为浓盐酸,B为KMnO 晶体,C中盛有紫色石蕊溶液,则C中溶液最终呈红色
4
B.实验仪器D可以起到防止溶液倒吸的作用
C.若A为浓氨水,B为生石灰,C中盛有AlCl 溶液,则C中溶液中先产生白色沉淀,然后沉淀又溶解
3
D.若A为浓HSO ,B为Cu,C中盛有澄清石灰水,则C中溶液变浑浊
2 4
【答案】B
【解析】A.若A为浓盐酸,B为KMnO 晶体,二者反应生成氯气,把氯气通到紫色石蕊溶液中,氯气与水反应
4
生成HCl和HClO,HCl使紫色石蕊溶液变红,HClO具有漂白性,使溶液褪色,C中溶液最终呈无色,A错误;
B.D中球形干燥管中间部分较粗,盛放液体的量较多,倒吸的液体靠自身重量回落,因此可以防止液体倒吸,
B正确;C.若A为浓氨水,B为生石灰,滴入后反应生成氨气,氨气和铝离子反应生成氢氧化铝,但氢氧化铝
不溶于弱碱一水合氨,所以C中产生白色沉淀不溶解,C错误;D.若A为浓硫酸,B为Cu,反应需要加热才能
发生,如果不加热,则没有二氧化硫产生,所以C中溶液无变化,D错误。
D.若A为浓HSO ,B为Cu,C中盛有澄清石灰水,则C中溶液变浑浊
2 4
23.用制溴苯的废催化剂(主要含FeBr 及少量溴、苯)为原料,制取无水FeCl 和溴的苯溶液,选用的方法能
3 3
达到相应实验目的的是
A.用装置①及其试剂制取氯气
B.用装置②氧化FeBr 溶液中的溴离子
3C.用装置③分离出FeCl 溶液,不能选用装置④分离
3
D.用装置⑤将FeCl 溶液蒸发至干,可得无水FeCl
3 3
【答案】C
24.某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略)。实验开始前,
向装置中通入一段时间的N,排尽装置内的空气。
2
已知:在溶液中,FeSO +NO [Fe(NO)]SO(棕色),该反应可用于检验NO。下列对该实验相关描述错误
4 4
的是
A.装置F、I中的试剂依次为水,硫酸亚铁溶液
B.装置J收集的气体中不含NO
C.实验结束后,先熄灭酒精灯,再关闭分液漏斗的活塞
D.若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应
【答案】B25.光气(COC1 熔点为-118℃,沸点为8.2℃,微溶于水,易溶于甲苯等有机溶剂)可作为化学武器的成分,其
2
制备实验装置如图所示(夹持装置已省略)。
已知:3CCl +2H SO (浓) 3COCl ↑+4HCl+S OCl。下列说法正确的是
4 2 4 2 2 5 2
A.装置组装连接后,第一步操作通入冷凝水,然后才能加热
B.自来水从冷凝管的X口通入,且被冷凝的物质是CCl
4
C.装置乙中可收集到光气的甲苯溶液,装置丙、丁均可收集到液态光气
D.可将装置丁的尾气通过导管直接通入NaOH溶液中进行尾气处理
【答案】C
【解析】A、根据反应方程式,有气体生成,因此第一步操作是检验装置的气密性,故A错误;B、冷凝水应从下
口通入,上口出水,即从Y口进水,X口出水,被冷凝的物质是COCl ,故B错误;C、光气易溶于甲苯,因此挥
2
发出的光气被甲苯吸收,得到光气的甲苯溶液,根据光气的物理性质,装置丙、丁均可收集到液态光气,故C
正确;D、尾气中含有HCl,导管直接通入NaOH溶液,引起倒吸,应用倒扣的漏斗,故D错误。