文档内容
专题 12 化学反应机理
(本卷共19小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
第I卷 (选择题共100分)
一、选择题:本题共14个小题,每小题5分,共70分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
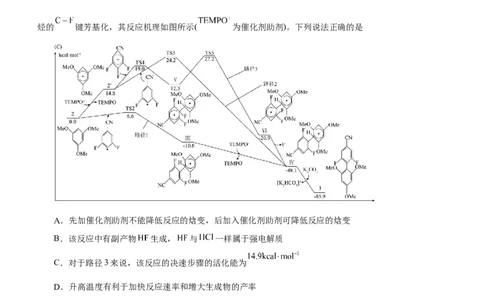
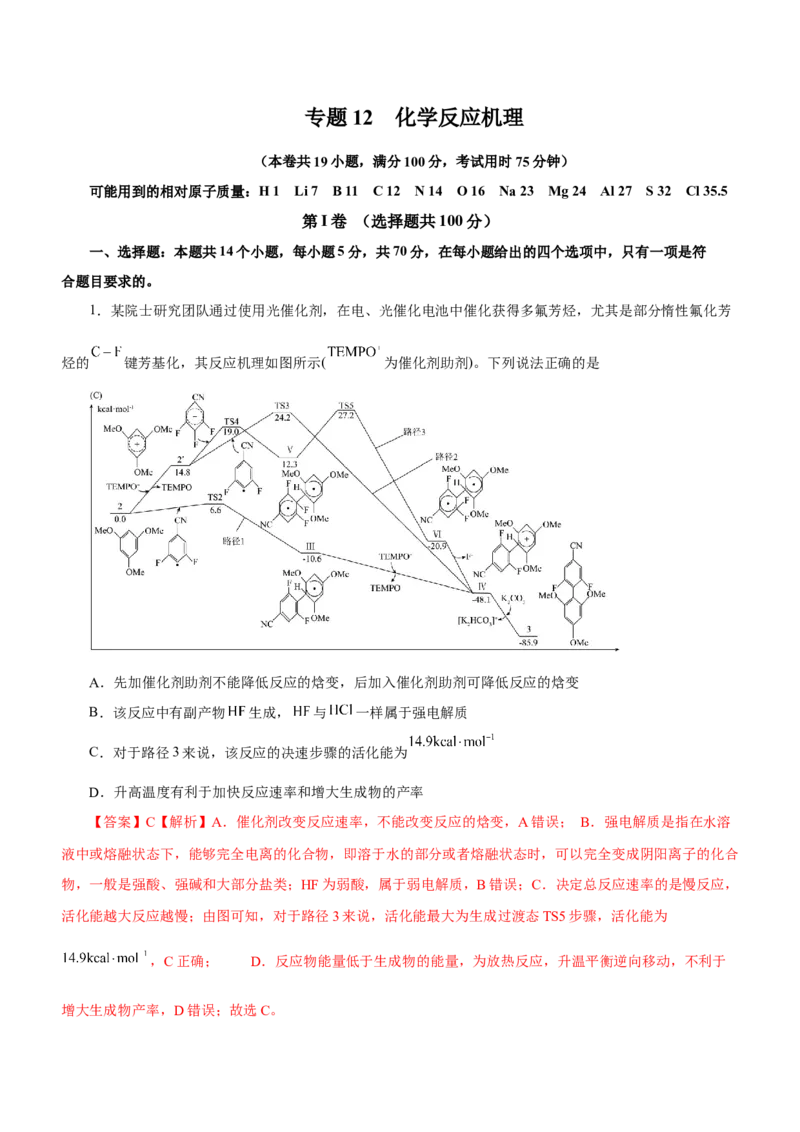
1.某院士研究团队通过使用光催化剂,在电、光催化电池中催化获得多氟芳烃,尤其是部分惰性氟化芳
烃的 键芳基化,其反应机理如图所示( 为催化剂助剂)。下列说法正确的是
A.先加催化剂助剂不能降低反应的焓变,后加入催化剂助剂可降低反应的焓变
B.该反应中有副产物 生成, 与 一样属于强电解质
C.对于路径3来说,该反应的决速步骤的活化能为
D.升高温度有利于加快反应速率和增大生成物的产率
【答案】C【解析】A.催化剂改变反应速率,不能改变反应的焓变,A错误; B.强电解质是指在水溶
液中或熔融状态下,能够完全电离的化合物,即溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合
物,一般是强酸、强碱和大部分盐类;HF为弱酸,属于弱电解质,B错误;C.决定总反应速率的是慢反应,
活化能越大反应越慢;由图可知,对于路径3来说,活化能最大为生成过渡态TS5步骤,活化能为
,C正确; D.反应物能量低于生成物的能量,为放热反应,升温平衡逆向移动,不利于
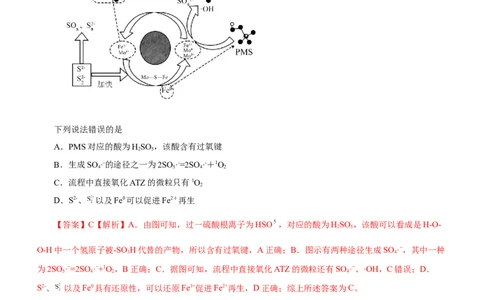
增大生成物产率,D错误;故选C。2.阿特拉津(ATZ)是农业中使用广泛且难以降解的除草剂,某科学组织研究发现,以FeS@MoS 为催化
x 2
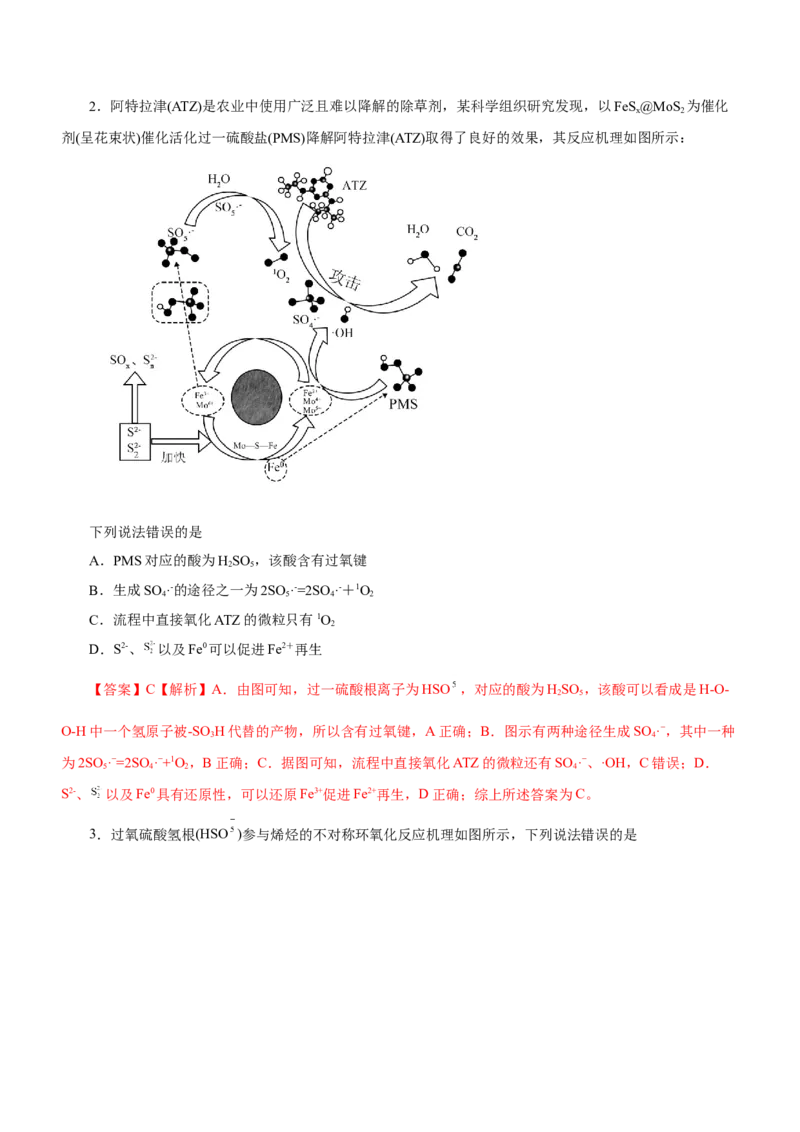
剂(呈花束状)催化活化过一硫酸盐(PMS)降解阿特拉津(ATZ)取得了良好的效果,其反应机理如图所示:
下列说法错误的是
A.PMS对应的酸为HSO ,该酸含有过氧键
2 5
B.生成SO ·-的途径之一为2SO ·-=2SO·-+1O
4 5 4 2
C.流程中直接氧化ATZ的微粒只有1O
2
D.S2-、 以及Fe0可以促进Fe2+再生
【答案】C【解析】A.由图可知,过一硫酸根离子为HSO ,对应的酸为HSO ,该酸可以看成是H-O-
2 5
O-H中一个氢原子被-SO H代替的产物,所以含有过氧键,A正确;B.图示有两种途径生成SO ·−,其中一种
3 4
为2SO ·−=2SO·−+1O,B正确;C.据图可知,流程中直接氧化ATZ的微粒还有SO ·−、·OH,C错误;D.
5 4 2 4
S2-、 以及Fe0具有还原性,可以还原Fe3+促进Fe2+再生,D正确;综上所述答案为C。
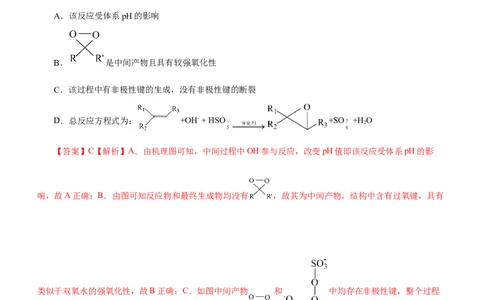
3.过氧硫酸氢根(HSO )参与烯烃的不对称环氧化反应机理如图所示,下列说法错误的是A.该反应受体系pH的影响
B. 是中间产物且具有较强氧化性
C.该过程中有非极性键的生成,没有非极性键的断裂
D.总反应方程式为: +OH- + HSO +SO +H O
2
【答案】C【解析】A.由机理图可知,中间过程中OH-参与反应,改变pH值即该反应受体系pH的影
响,故A正确;B.由图可知反应物和最终生成物均没有 ,故其为中间产物,结构中含有过氧键,具有
类似于双氧水的强氧化性,故B正确;C.如图中间产物 和 中均存在非极性键,整个过程
中存在非极性键断裂,故C错误;D.由图可知该反应的反应物有: 、OH- 、 HSO ,生成物为: 、SO 、HO,总反应方程式为: +OH- + HSO +SO
2
+H O,故D正确;故选C。
2
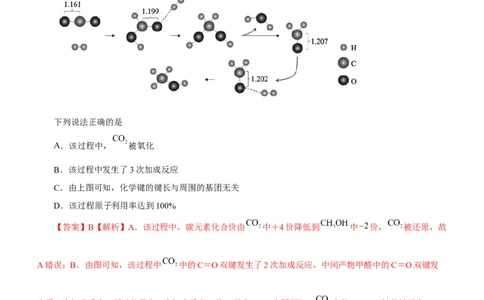
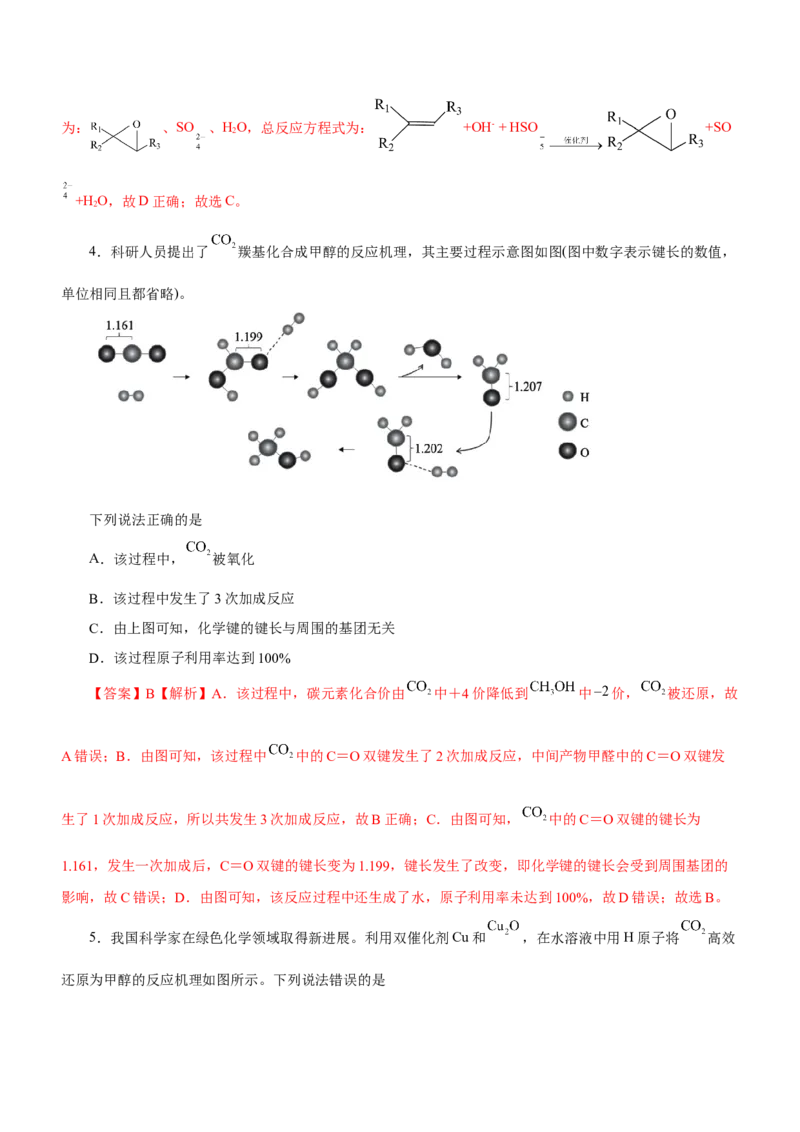
4.科研人员提出了 羰基化合成甲醇的反应机理,其主要过程示意图如图(图中数字表示键长的数值,
单位相同且都省略)。
下列说法正确的是
A.该过程中, 被氧化
B.该过程中发生了3次加成反应
C.由上图可知,化学键的键长与周围的基团无关
D.该过程原子利用率达到100%
【答案】B【解析】A.该过程中,碳元素化合价由 中+4价降低到 中 价, 被还原,故
A错误;B.由图可知,该过程中 中的C=O双键发生了2次加成反应,中间产物甲醛中的C=O双键发
生了1次加成反应,所以共发生3次加成反应,故B正确;C.由图可知, 中的C=O双键的键长为
1.161,发生一次加成后,C=O双键的键长变为1.199,键长发生了改变,即化学键的键长会受到周围基团的
影响,故C错误;D.由图可知,该反应过程中还生成了水,原子利用率未达到100%,故D错误;故选B。
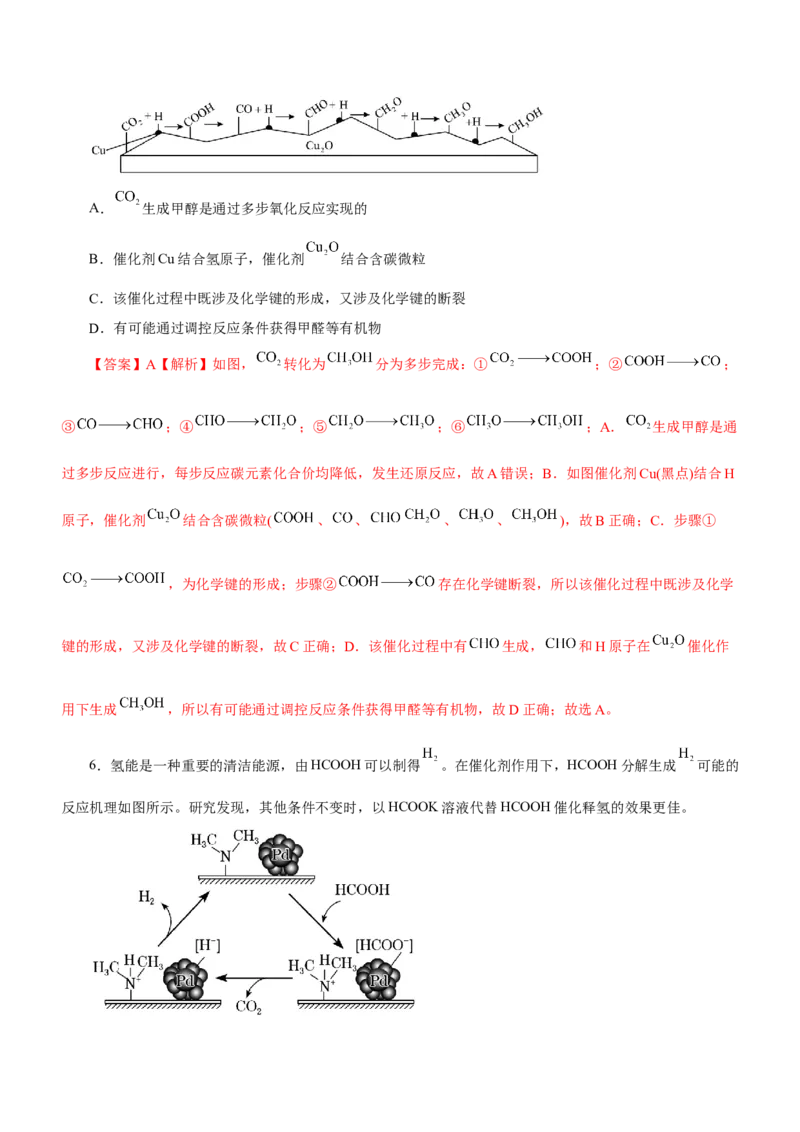
5.我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和 ,在水溶液中用H原子将 高效
还原为甲醇的反应机理如图所示。下列说法错误的是A. 生成甲醇是通过多步氧化反应实现的
B.催化剂Cu结合氢原子,催化剂 结合含碳微粒
C.该催化过程中既涉及化学键的形成,又涉及化学键的断裂
D.有可能通过调控反应条件获得甲醛等有机物
【答案】A【解析】如图, 转化为 分为多步完成:① ;② ;
③ ;④ ;⑤ ;⑥ ;A. 生成甲醇是通
过多步反应进行,每步反应碳元素化合价均降低,发生还原反应,故A错误;B.如图催化剂Cu(黑点)结合H
原子,催化剂 结合含碳微粒( 、 、 、 、 ),故B正确;C.步骤①
,为化学键的形成;步骤② 存在化学键断裂,所以该催化过程中既涉及化学
键的形成,又涉及化学键的断裂,故C正确;D.该催化过程中有 生成, 和H原子在 催化作
用下生成 ,所以有可能通过调控反应条件获得甲醛等有机物,故D正确;故选A。
6.氢能是一种重要的清洁能源,由HCOOH可以制得 。在催化剂作用下,HCOOH分解生成 可能的
反应机理如图所示。研究发现,其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳。下列说法正确的是
A.HCOOH催化释氢过程中,有非极性键的断裂与形成
B.HCOOD催化释氢反应除生成 外,还生成 、HD、
C.其他条件不变时,以HCOOK溶液代替HCOOH不能提高释放氢气的纯度
D.HCOOK溶液代替HCOOH时发生反应:
【答案】D【解析】在催化剂作用下,HCOOH分解生成CO 和H;若将HCOOH换成HCOOD或
2 2
HCOOK,也可按HCOOH分解的原理分析。A.转化涉及到N-H键的断裂和形成、O-H键的断裂以及H-H键
的形成,没有非极性键的断裂,A错误;B.若用HCOOD代替HCOOH,反应为HCOOD分解,除生成CO
2
外,还生成HD,没有H 、D,B错误;C.若用HCOOK溶液代替HCOOH,HCOOK分解生成CO 和KH,
2 2 2
KH与水反应生成KOH和H,KOH能吸收CO,所以最终所得气体中CO 的量会减少,提高释放氢气的纯
2 2 2
度,C错误;D.若用HCOOK溶液代替HCOOH,生成的KOH能吸收CO 转变为 ,离子反应为
2
,D正确;故选D。
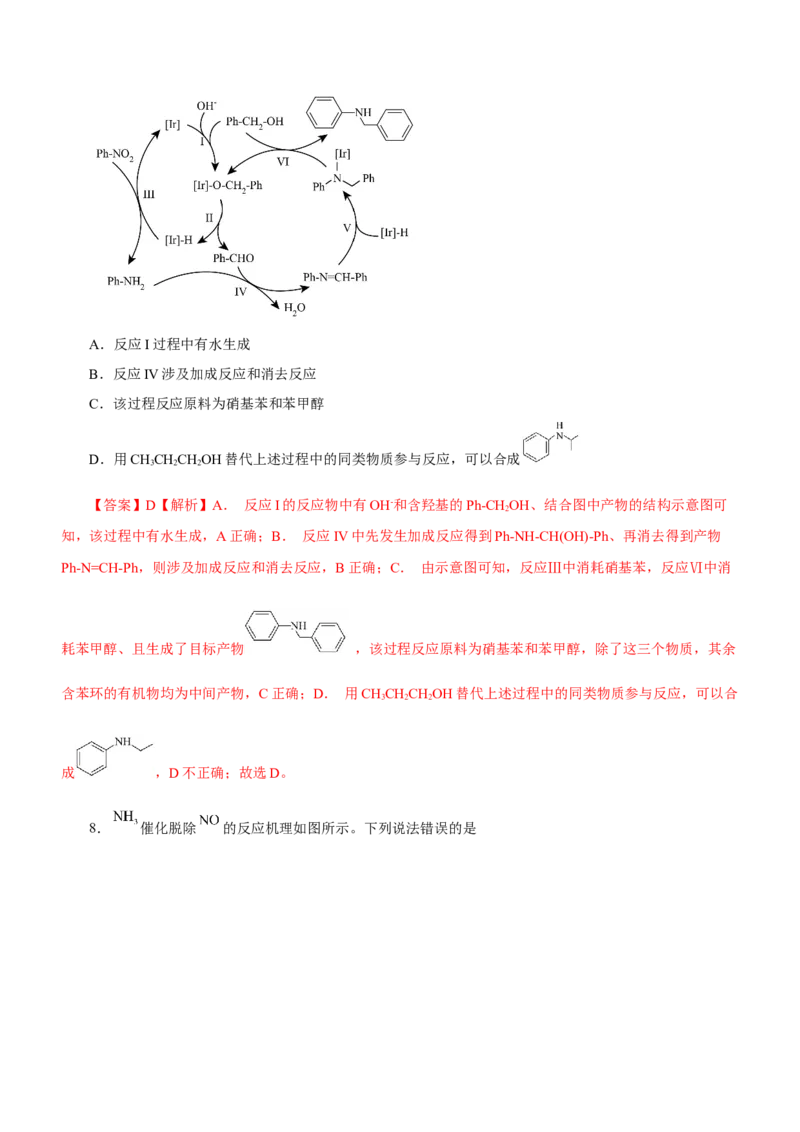
7. 可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其
中Ph-代表苯基,[Ir]代表 )下列说法不正确的是A.反应I过程中有水生成
B.反应IV涉及加成反应和消去反应
C.该过程反应原料为硝基苯和苯甲醇
D.用CHCHCHOH替代上述过程中的同类物质参与反应,可以合成
3 2 2
【答案】D【解析】A. 反应I的反应物中有OH-和含羟基的Ph-CH OH、结合图中产物的结构示意图可
2
知,该过程中有水生成,A正确;B. 反应IV中先发生加成反应得到Ph-NH-CH(OH)-Ph、再消去得到产物
Ph-N=CH-Ph,则涉及加成反应和消去反应,B正确;C. 由示意图可知,反应Ⅲ中消耗硝基苯,反应Ⅵ中消
耗苯甲醇、且生成了目标产物 ,该过程反应原料为硝基苯和苯甲醇,除了这三个物质,其余
含苯环的有机物均为中间产物,C正确;D. 用CHCHCHOH替代上述过程中的同类物质参与反应,可以合
3 2 2
成 ,D不正确;故选D。
8. 催化脱除 的反应机理如图所示。下列说法错误的是A.脱除 的反应中 作还原剂
B.反应过程中V元素的化合价发生变化
C.每脱除 消耗
D. 脱除 的化学方程式为:
【答案】D【解析】A.总反应为 ,NH 生成氮气中N元素化合价升高,则
3
NH 做还原剂,故A正确;B.从反应机理来看,前三步反应与第四步反应相比V元素所形成的化学键有所变
3
化,所以V的化合价发生变化,故B正确;C.总反应为 ,NO与O 的反应系
2
数比为4:1,每脱除 消耗 ,故C正确;D. 脱除 的化学方程式为:
,故D错误;故选D。
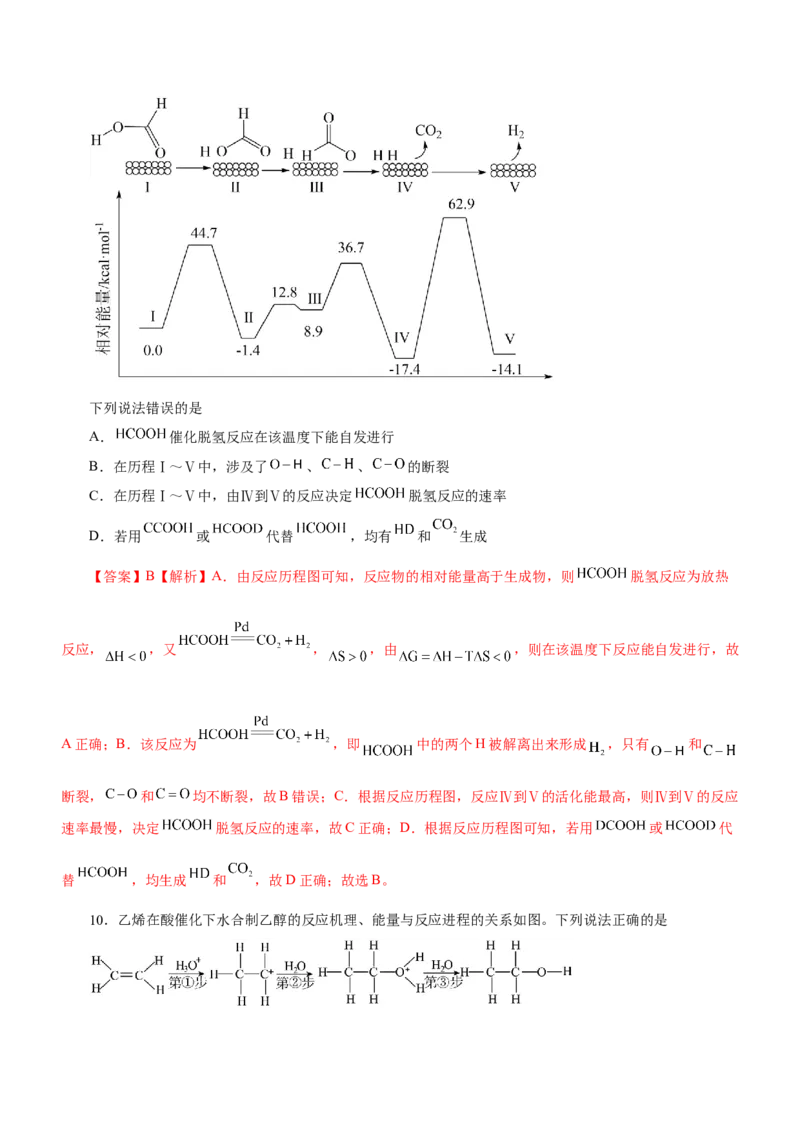
9.一定温度下, 在 催化剂表面脱氨的反应机理、反应历程与能量的关系如图所示:下列说法错误的是
A. 催化脱氢反应在该温度下能自发进行
B.在历程Ⅰ~Ⅴ中,涉及了 、 、 的断裂
C.在历程Ⅰ~Ⅴ中,由Ⅳ到Ⅴ的反应决定 脱氢反应的速率
D.若用 或 代替 ,均有 和 生成
【答案】B【解析】A.由反应历程图可知,反应物的相对能量高于生成物,则 脱氢反应为放热
反应, ,又 , ,由 ,则在该温度下反应能自发进行,故
A正确;B.该反应为 ,即 中的两个H被解离出来形成 ,只有 和
断裂, 和 均不断裂,故B错误;C.根据反应历程图,反应Ⅳ到Ⅴ的活化能最高,则Ⅳ到Ⅴ的反应
速率最慢,决定 脱氢反应的速率,故C正确;D.根据反应历程图可知,若用 或 代
替 ,均生成 和 ,故D正确;故选B。
10.乙烯在酸催化下水合制乙醇的反应机理、能量与反应进程的关系如图。下列说法正确的是A.由上图可知总反应一定不需加热就能进行B.第①步反应只有O-H键发生断裂
C.总反应速率由第①步反应决定 D.第①②③步反应都是放热反应
【答案】C【解析】A.虽然总反应是放热反应,但第①步反应是吸热反应,所以需加热才能进行,A不
正确;B.第①步反应中,断裂O-H键、碳碳双键中的一个键,形成碳氢键,B不正确;C.因第②③步反应
为放热反应,第①步反应为吸热反应,所以总反应速率由第①步反应决定,C正确;D.由图可知,第②③步
反应都是放热反应,但第①步反应为吸热反应,D不正确;故选C。
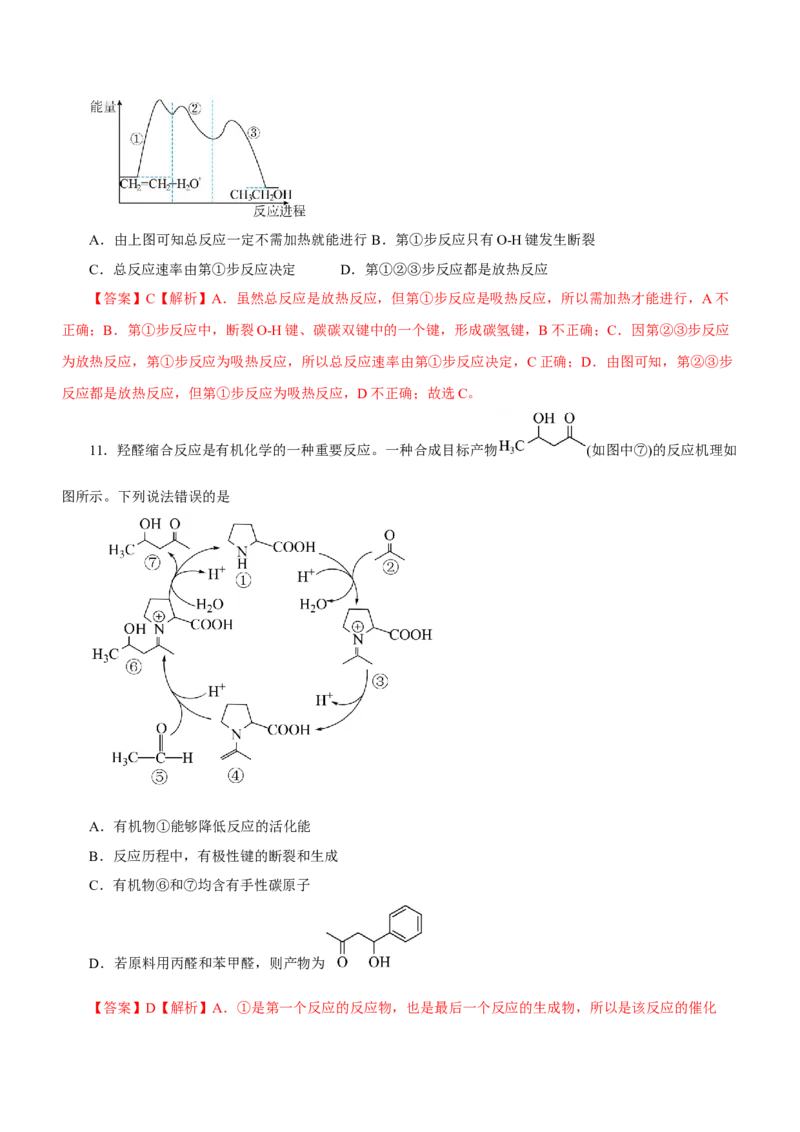
11.羟醛缩合反应是有机化学的一种重要反应。一种合成目标产物 (如图中⑦)的反应机理如
图所示。下列说法错误的是
A.有机物①能够降低反应的活化能
B.反应历程中,有极性键的断裂和生成
C.有机物⑥和⑦均含有手性碳原子
D.若原料用丙醛和苯甲醛,则产物为
【答案】D【解析】A.①是第一个反应的反应物,也是最后一个反应的生成物,所以是该反应的催化剂,能降低反应所需活化能,A正确;B.③到④的过程中,有C—N极性键的断裂和C—O极性键的生成,B
正确;C.手性碳原子是连接4个不同的原子或原子团的C原子,根据化合物⑤、⑥、⑦结构简式可知,⑥和
⑦均含有手性碳原子,C正确;D.按照图示流程反应可知,如果原料用丙醛和苯甲醛,则产物为
,D错误;故选D。
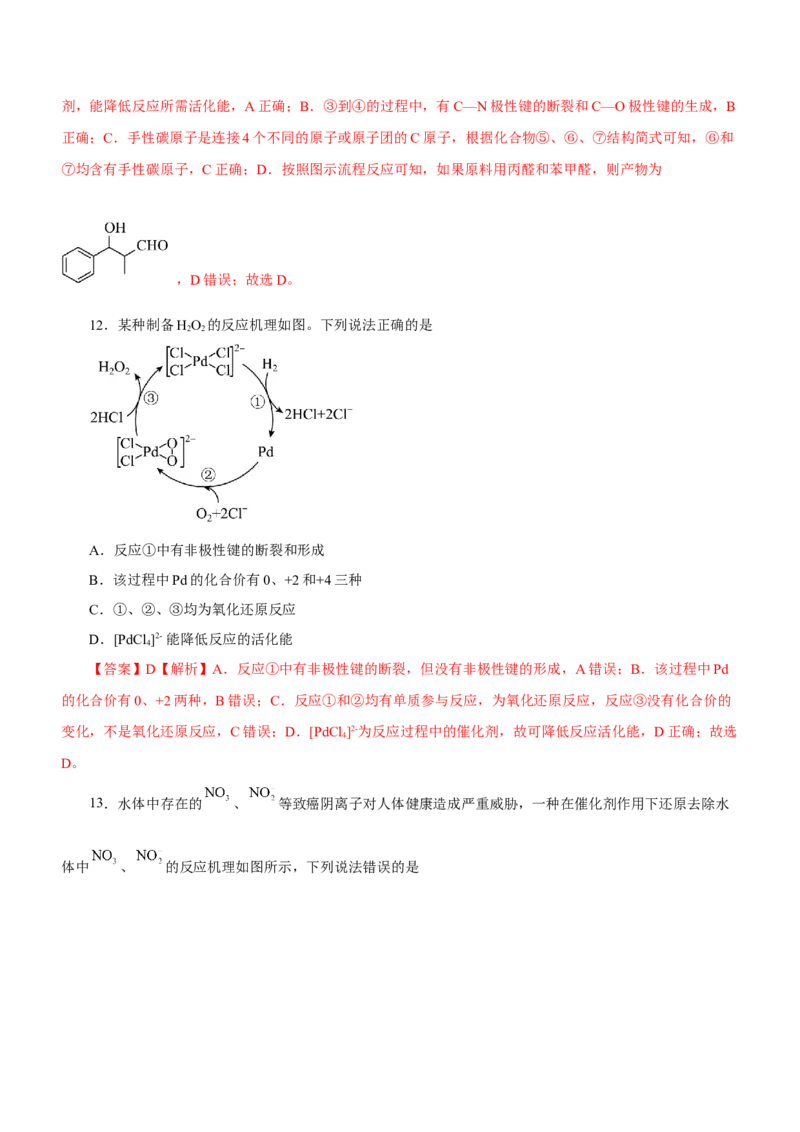
12.某种制备HO 的反应机理如图。下列说法正确的是
2 2
A.反应①中有非极性键的断裂和形成
B.该过程中Pd的化合价有0、+2和+4三种
C.①、②、③均为氧化还原反应
D.[PdCl ]2- 能降低反应的活化能
4
【答案】D【解析】A.反应①中有非极性键的断裂,但没有非极性键的形成,A错误;B.该过程中Pd
的化合价有0、+2两种,B错误;C.反应①和②均有单质参与反应,为氧化还原反应,反应③没有化合价的
变化,不是氧化还原反应,C错误;D.[PdCl ]2-为反应过程中的催化剂,故可降低反应活化能,D正确;故选
4
D。
13.水体中存在的 、 等致癌阴离子对人体健康造成严重威胁,一种在催化剂作用下还原去除水
体中 、 的反应机理如图所示,下列说法错误的是A.催化剂Cu只能将 转化为
B.亚硝酸根被氢气还原的离子方程式:
C. 转化为 的过程中氧化剂和还原剂的物质的量之比为5:2
D.用该法处理后水体的pH增大
【答案】C【解析】A. 、 在Cu、Pd催化作用下与 反应转化为 和2 ,由图可知,反
应中催化剂Cu只能将 转化为 ,A正确;B.亚硝酸根被氢气还原的离子方程式:
,B正确;C. 转化为 的总反应为:
,氧化剂为 ,还原剂为 ,氧化剂和还原剂的物质的量之比为2:5,C错误;D.催化剂作用下用氢气
还原去除水体中 、 的时,均生成 ,处理后水体的pH增大,D正确;故选C。
14.催化丙烯制醛的反应机理如图所示。下列说法错误的是A.上述循环过程中,Co的配位数发生了变化
B.上述循环过程中,有C-O键的形成,无C-O键的断裂
C.丙烯醛基化总反应为
D. 可降低丙烯醛基化反应的活化能
【答案】B【解析】A.由图可知,Co可以形成3个配位键,也可以形成4个配位键,A正确;B.由图
可知,在第二步有C-O键的断裂,B错误;C.由题干反应历程图可知,总反应式为
,C正确;D.由题千反应历程图可知, ,参与反应过
程,反应前后保持不变,是该反应的催化剂,可降低丙烯醛基化反应的活化能,D正确;故选B。
二、选择题:本题共5个小题,每小题6分,共30分。在每小题给出的四个选项中,只有一项或两项是
符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个
且正确的得5分,选两个且都正确的得6分,但只要选错一个,该小题得0分。
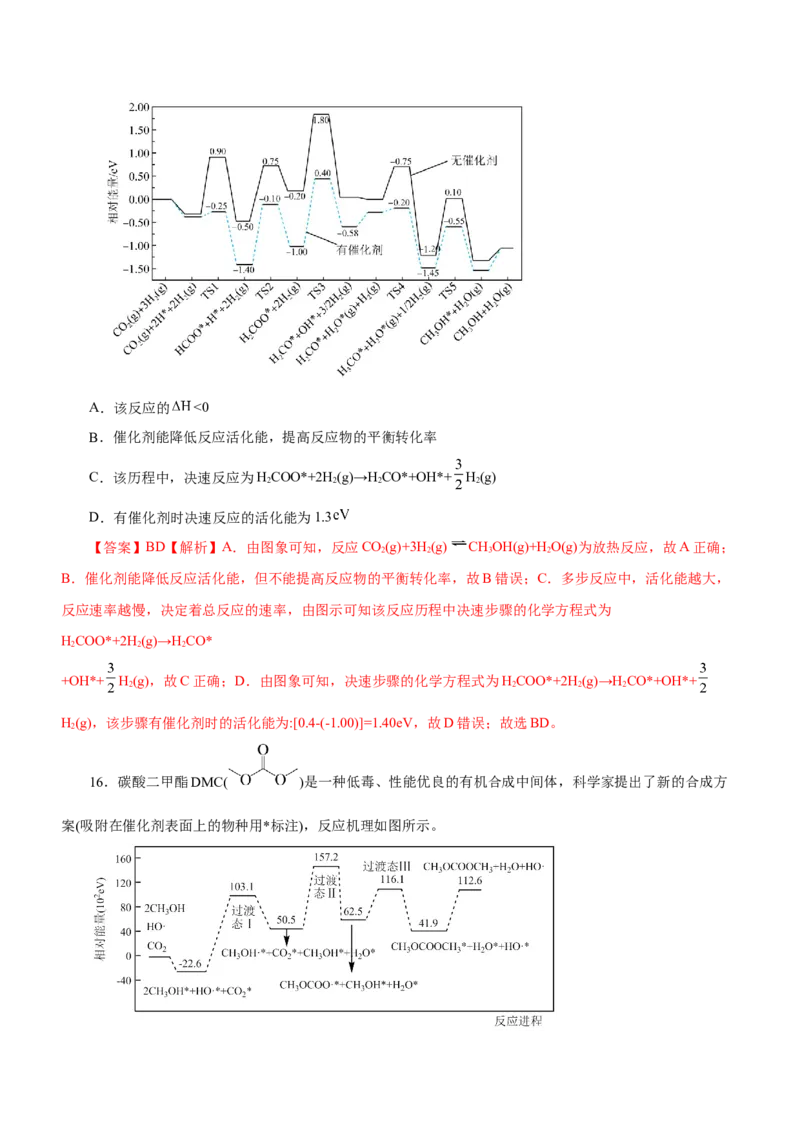
15.某反应在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*
标注,TS为过渡态)。下列有关说法错误的是A.该反应的 <0
B.催化剂能降低反应活化能,提高反应物的平衡转化率
C.该历程中,决速反应为HCOO*+2H (g)→H CO*+OH*+ H(g)
2 2 2 2
D.有催化剂时决速反应的活化能为1.3
【答案】BD【解析】A.由图象可知,反应CO(g)+3H(g) CHOH(g)+H O(g)为放热反应,故A正确;
2 2 3 2
B.催化剂能降低反应活化能,但不能提高反应物的平衡转化率,故B错误;C.多步反应中,活化能越大,
反应速率越慢,决定着总反应的速率,由图示可知该反应历程中决速步骤的化学方程式为
HCOO*+2H (g)→H CO*
2 2 2
+OH*+ H(g),故C正确;D.由图象可知,决速步骤的化学方程式为HCOO*+2H (g)→H CO*+OH*+
2 2 2 2
H(g),该步骤有催化剂时的活化能为:[0.4-(-1.00)]=1.40eV,故D错误;故选BD。
2
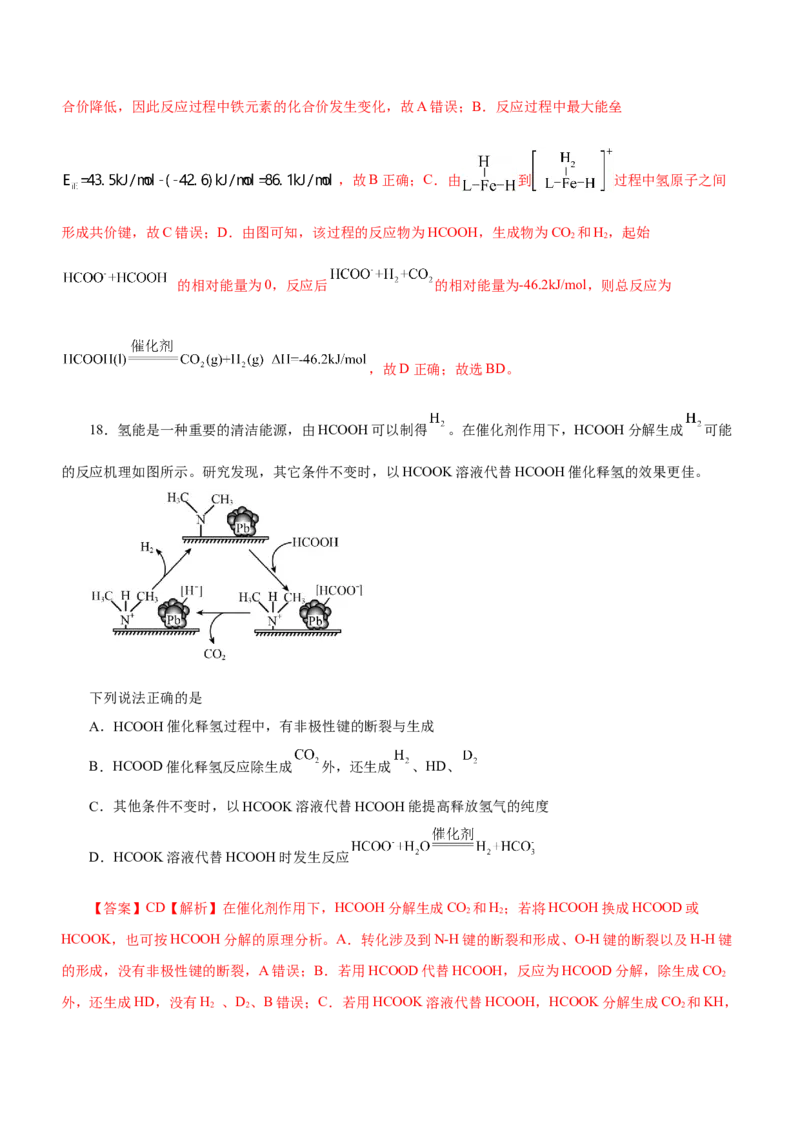
16.碳酸二甲酯DMC( )是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方
案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。下列说法错误的是
A.HO·提高了反应的活化能
B.过程CHOH*+HO·*=CH O·*+HO*是该反应的决速步骤
3 3 2
C.过程中既有H-O键的断裂,又有H-O键的形成
D.吸附和脱附过程中共吸收48.1eV的能量
【答案】AD【解析】A.HO·在反应前参与反应,反应后又生成,作催化剂,降低了反应的活化能,提高
化学反应速率,故A错误;B.决速步骤一般伴有的是能量的落差大,活化能大的步骤即决速步骤,由图示可
知生成过渡态I时的所需的活化能最大,所以CHOH*+HO·*=CH O·*+HO*是该反应的决速步骤,故B正确;
3 3 2
C.过程中甲醇反应时有H-O键的断裂,生成水时有H-O键的形成,故C正确;D.吸附和脱附过程中共吸收
的能量为终态减去始态的能量,始态相对能量为0eV,终态相对能量为112.6×102 eV,则吸附和脱附过程中共
吸收的能量为1.126×104 eV,故D错误;故选AD。
17.铁的某种络合物离子(用 表示)催化甲酸分解的反应机理及相对能量变化如图所示。下列
说法正确的是
A.反应过程中铁元素价态没有改变
B.反应过程中最大能垒
C.由 到 过程中形成了离子健
D.总反应为:
【答案】BD【解析】A. →CO+ 的过程中,碳的化合价从+2价升高为+4价,则铁的化
2合价降低,因此反应过程中铁元素的化合价发生变化,故A错误;B.反应过程中最大能垒
,故B正确;C.由 到 过程中氢原子之间
形成共价键,故C错误;D.由图可知,该过程的反应物为HCOOH,生成物为CO 和H,起始
2 2
的相对能量为0,反应后 的相对能量为-46.2kJ/mol,则总反应为
,故D正确;故选BD。
18.氢能是一种重要的清洁能源,由HCOOH可以制得 。在催化剂作用下,HCOOH分解生成 可能
的反应机理如图所示。研究发现,其它条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳。
下列说法正确的是
A.HCOOH催化释氢过程中,有非极性键的断裂与生成
B.HCOOD催化释氢反应除生成 外,还生成 、HD、
C.其他条件不变时,以HCOOK溶液代替HCOOH能提高释放氢气的纯度
D.HCOOK溶液代替HCOOH时发生反应
【答案】CD【解析】在催化剂作用下,HCOOH分解生成CO 和H;若将HCOOH换成HCOOD或
2 2
HCOOK,也可按HCOOH分解的原理分析。A.转化涉及到N-H键的断裂和形成、O-H键的断裂以及H-H键
的形成,没有非极性键的断裂,A错误;B.若用HCOOD代替HCOOH,反应为HCOOD分解,除生成CO
2
外,还生成HD,没有H 、D、B错误;C.若用HCOOK溶液代替HCOOH,HCOOK分解生成CO 和KH,
2 2 2KH与水反应生成KOH和H,KOH能吸收CO,所以最终所得气体中CO 的量会减少,提高释放氢气的纯
2 2 2
度,C正确;D.若用HCOOK溶液代替HCOOH,生成的KOH能吸收CO 转变为 ,离子反应为
2
,D正确;故选CD。
19.NO的治理是当前生态环境保护中的重要课题之一,Cu基催化剂是 技术脱除NO中性能较为
优异的新型催化剂,但 会造成Cu基催化剂的催化性能下降。加入 可抑制 对Cu基催化剂的影响
(含Ce化合物的比例系数均未标定),其作用机理如图所示。下列说法正确的是
A.NO可以造成臭氧空洞
B.在反应机理②中,Ce元素的化合价升高
C.整个反应的化学方程式为
D.改良催化剂可以提高合成反应的平衡转化率
【答案】AC【解析】A.NO具有还原性、臭氧具有氧化性,两者可以反应造成臭氧空洞,A正确;B.
在反应机理②中,硫、氧、氮、氢元素化合价没有改变,则Ce元素的化合价也不会改变,B错误;C.由图可
知,整个反应反应物为氨气、一氧化氮、氧气,三者在催化剂作用下生成氮气和水,化学方程式为
,C正确;D.催化剂可以提高反应速率,但是不能改变合成反应的平衡转化
率,D错误;故选AC。