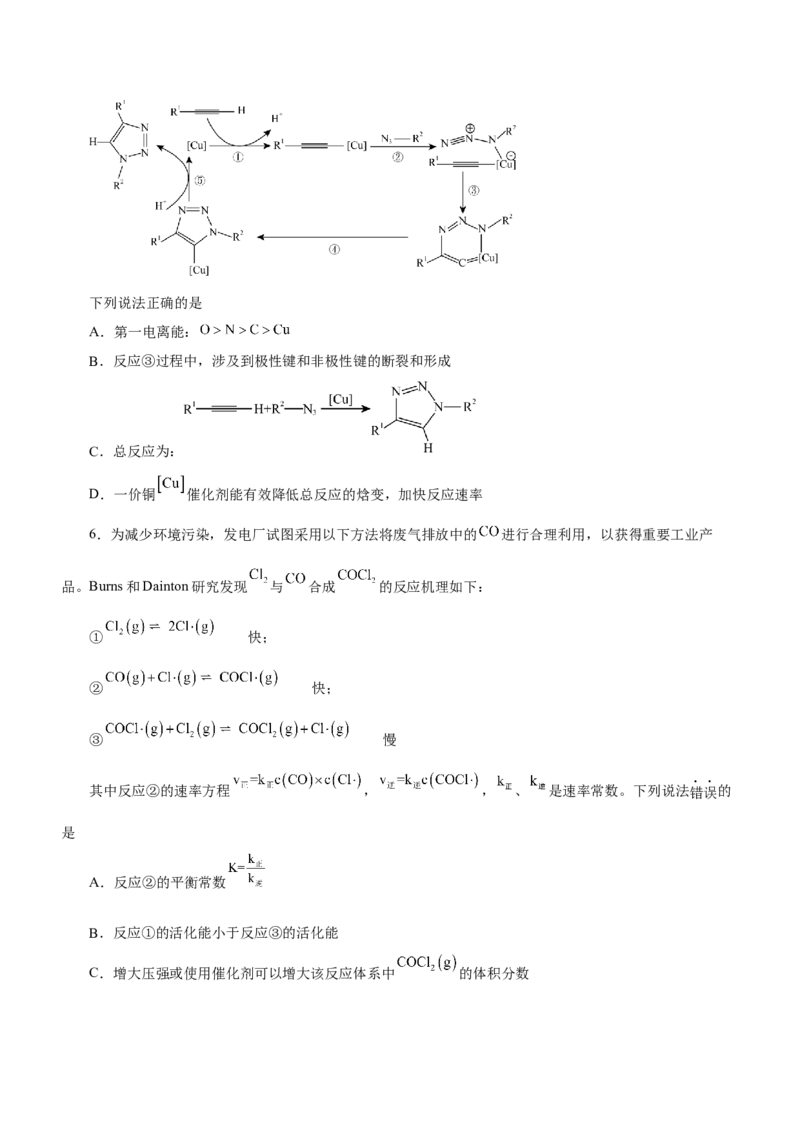文档内容
专题 12 化学反应机理
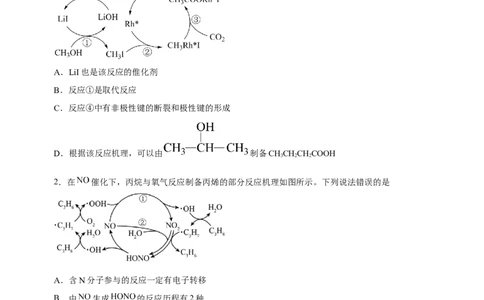
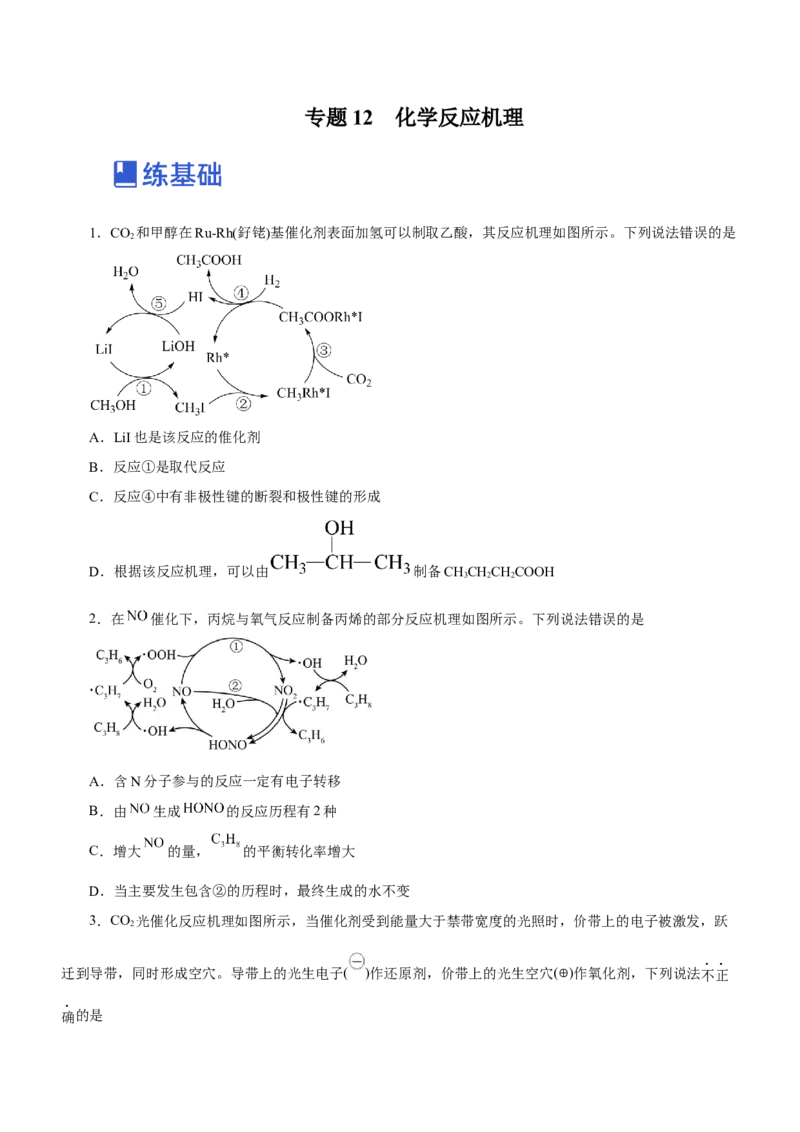
1.CO 和甲醇在Ru-Rh(釨铑)基催化剂表面加氢可以制取乙酸,其反应机理如图所示。下列说法错误的是
2
A.LiI也是该反应的倠化剂
B.反应①是取代反应
C.反应④中有非极性键的断裂和极性键的形成
D.根据该反应机理,可以由 制备CHCHCHCOOH
3 2 2
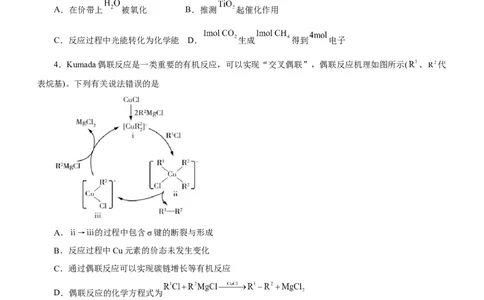
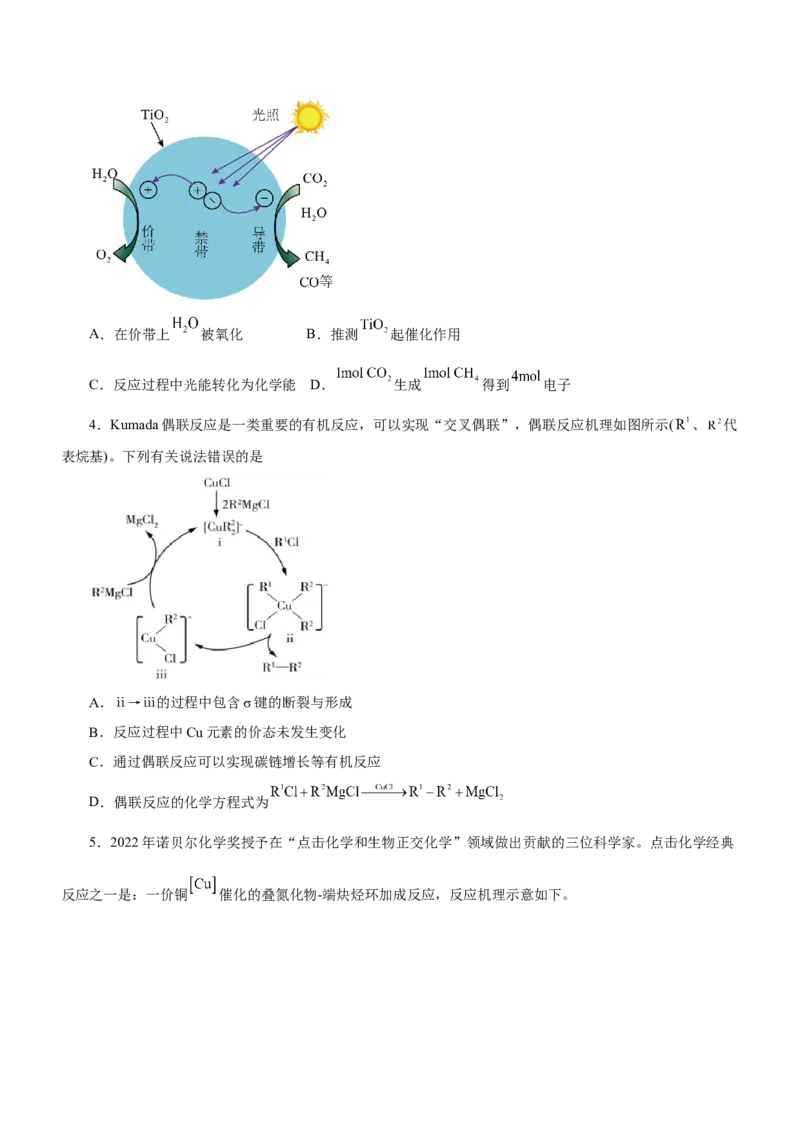
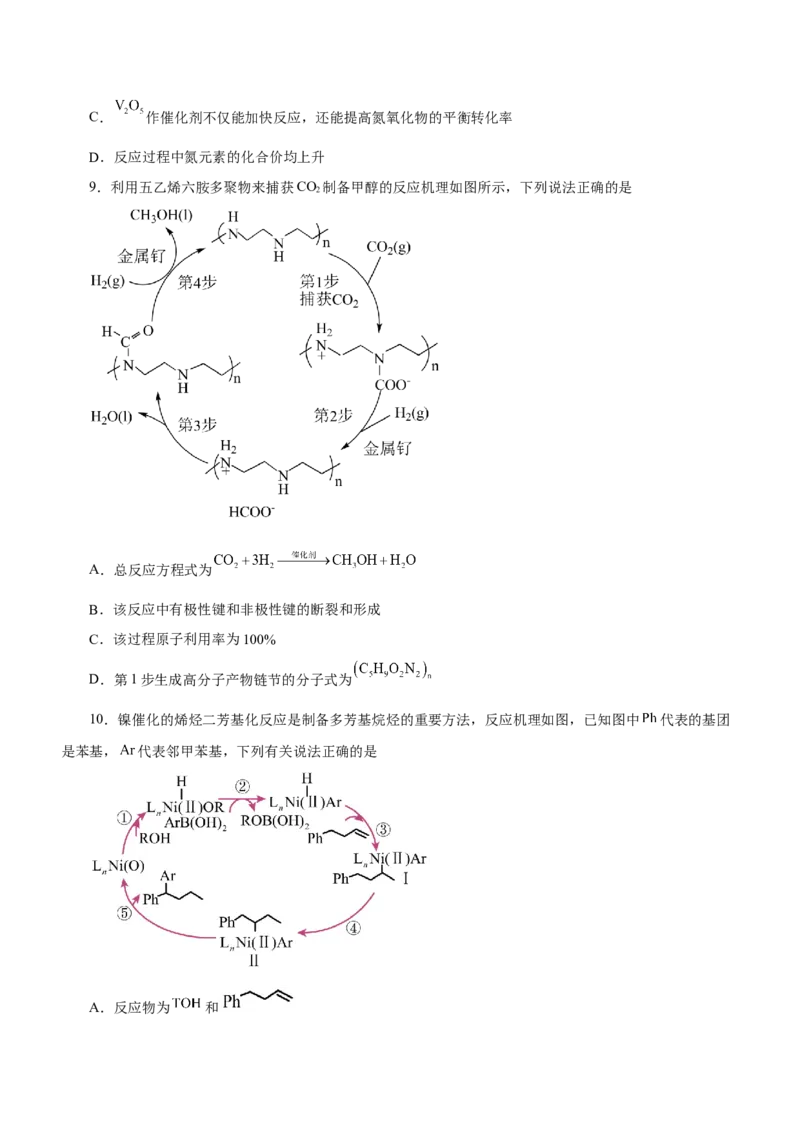
2.在 催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是
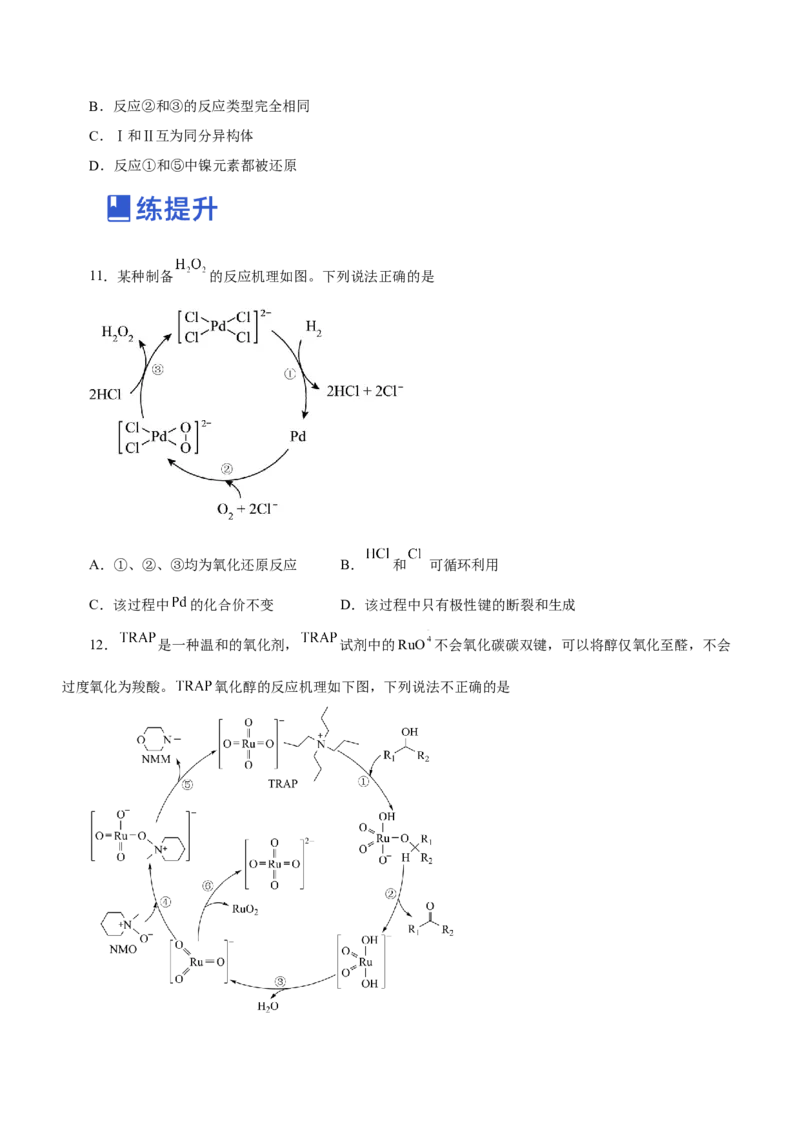
A.含N分子参与的反应一定有电子转移
B.由 生成 的反应历程有2种
C.增大 的量, 的平衡转化率增大
D.当主要发生包含②的历程时,最终生成的水不变
3.CO 光催化反应机理如图所示,当催化剂受到能量大于禁带宽度的光照时,价带上的电子被激发,跃
2
迁到导带,同时形成空穴。导带上的光生电子( )作还原剂,价带上的光生空穴(⊕)作氧化剂,下列说法不正
确的是A.在价带上 被氧化 B.推测 起催化作用
C.反应过程中光能转化为化学能 D. 生成 得到 电子
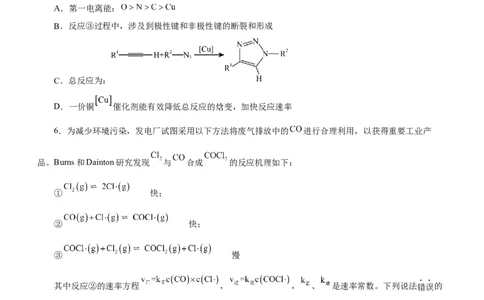
4.Kumada偶联反应是一类重要的有机反应,可以实现“交叉偶联”,偶联反应机理如图所示( 、 代
表烷基)。下列有关说法错误的是
A.ⅱ→ⅲ的过程中包含σ键的断裂与形成
B.反应过程中Cu元素的价态未发生变化
C.通过偶联反应可以实现碳链增长等有机反应
D.偶联反应的化学方程式为
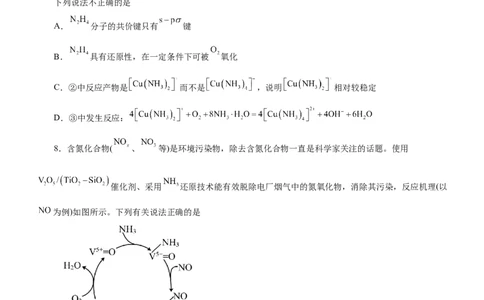
5.2022年诺贝尔化学奖授予在“点击化学和生物正交化学”领域做出贡献的三位科学家。点击化学经典
反应之一是:一价铜 催化的叠氮化物-端炔烃环加成反应,反应机理示意如下。下列说法正确的是
A.第一电离能:
B.反应③过程中,涉及到极性键和非极性键的断裂和形成
C.总反应为:
D.一价铜 催化剂能有效降低总反应的焓变,加快反应速率
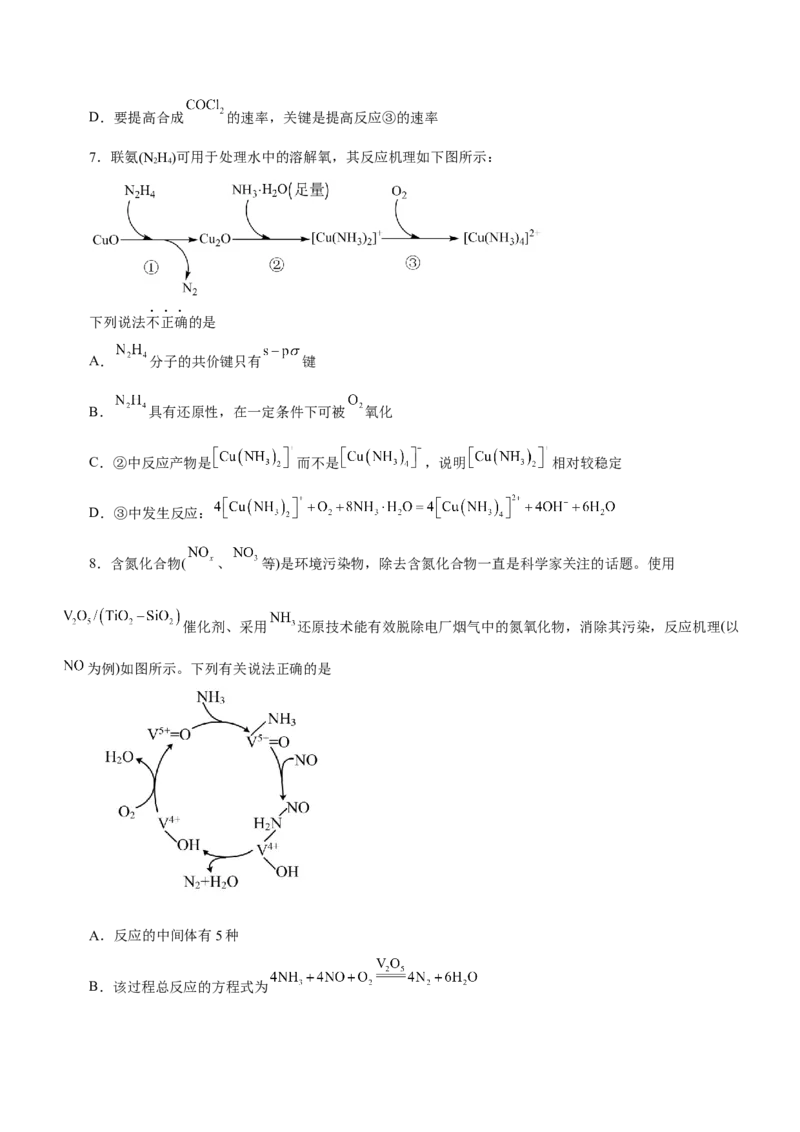
6.为减少环境污染,发电厂试图采用以下方法将废气排放中的 进行合理利用,以获得重要工业产
品。Burns和Dainton研究发现 与 合成 的反应机理如下:
① 快;
② 快;
③ 慢
其中反应②的速率方程 , , 、 是速率常数。下列说法错误的
是
A.反应②的平衡常数
B.反应①的活化能小于反应③的活化能
C.增大压强或使用催化剂可以增大该反应体系中 的体积分数D.要提高合成 的速率,关键是提高反应③的速率
7.联氨(N H)可用于处理水中的溶解氧,其反应机理如下图所示:
2 4
下列说法不正确的是
A. 分子的共价键只有 键
B. 具有还原性,在一定条件下可被 氧化
C.②中反应产物是 而不是 ,说明 相对较稳定
D.③中发生反应:
8.含氮化合物( 、 等)是环境污染物,除去含氮化合物一直是科学家关注的话题。使用
催化剂、采用 还原技术能有效脱除电厂烟气中的氮氧化物,消除其污染,反应机理(以
为例)如图所示。下列有关说法正确的是
A.反应的中间体有5种
B.该过程总反应的方程式为C. 作催化剂不仅能加快反应,还能提高氮氧化物的平衡转化率
D.反应过程中氮元素的化合价均上升
9.利用五乙烯六胺多聚物来捕获CO 制备甲醇的反应机理如图所示,下列说法正确的是
2
A.总反应方程式为
B.该反应中有极性键和非极性键的断裂和形成
C.该过程原子利用率为100%
D.第1步生成高分子产物链节的分子式为
10.镍催化的烯烃二芳基化反应是制备多芳基烷烃的重要方法,反应机理如图,已知图中 代表的基团
是苯基, 代表邻甲苯基,下列有关说法正确的是
A.反应物为 和B.反应②和③的反应类型完全相同
C.Ⅰ和Ⅱ互为同分异构体
D.反应①和⑤中镍元素都被还原
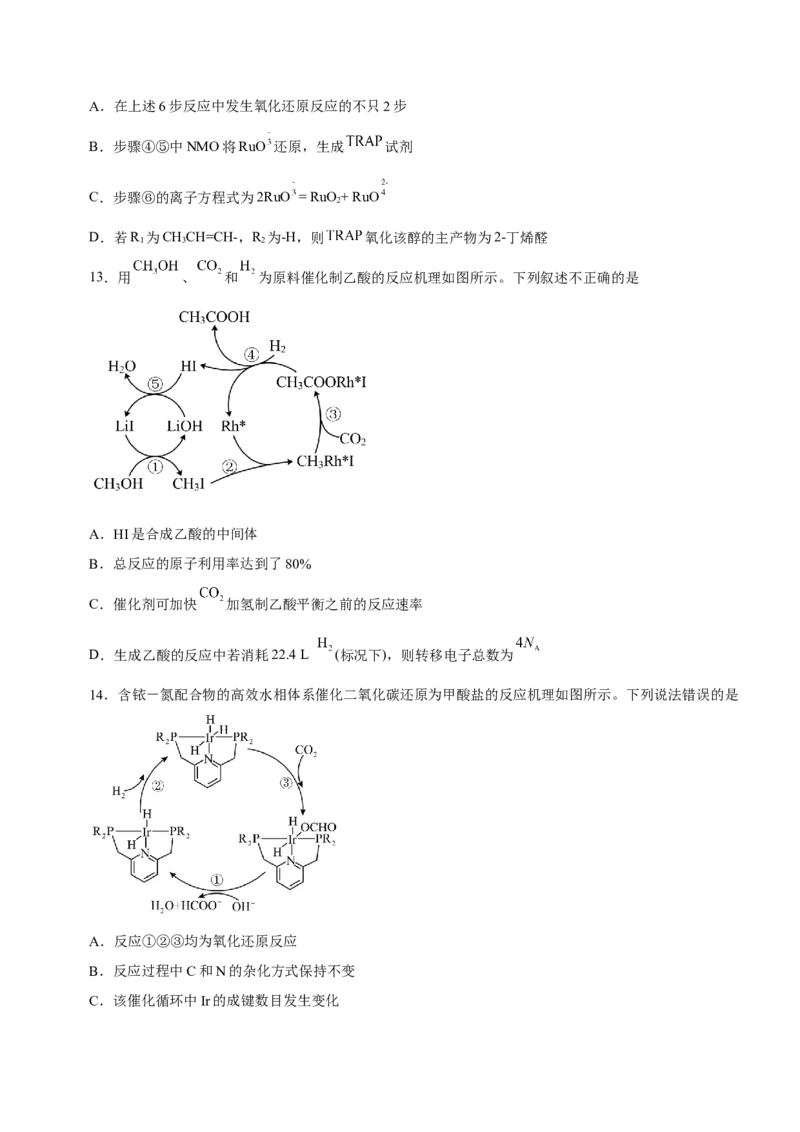
11.某种制备 的反应机理如图。下列说法正确的是
A.①、②、③均为氧化还原反应 B. 和 可循环利用
C.该过程中 的化合价不变 D.该过程中只有极性键的断裂和生成
12. 是一种温和的氧化剂, 试剂中的RuO 不会氧化碳碳双键,可以将醇仅氧化至醛,不会
过度氧化为羧酸。 氧化醇的反应机理如下图,下列说法不正确的是A.在上述6步反应中发生氧化还原反应的不只2步
B.步骤④⑤中NMO将RuO 还原,生成 试剂
C.步骤⑥的离子方程式为2RuO = RuO+ RuO
2
D.若R 为CHCH=CH-,R 为-H,则 氧化该醇的主产物为2-丁烯醛
1 3 2
13.用 、 和 为原料催化制乙酸的反应机理如图所示。下列叙述不正确的是
A.HI是合成乙酸的中间体
B.总反应的原子利用率达到了80%
C.催化剂可加快 加氢制乙酸平衡之前的反应速率
D.生成乙酸的反应中若消耗22.4 L (标况下),则转移电子总数为
14.含铱-氮配合物的高效水相体系催化二氧化碳还原为甲酸盐的反应机理如图所示。下列说法错误的是
A.反应①②③均为氧化还原反应
B.反应过程中C和N的杂化方式保持不变
C.该催化循环中Ir的成键数目发生变化D.该过程的总反应为H+CO +OH-=HCOO-+H O
2 2 2
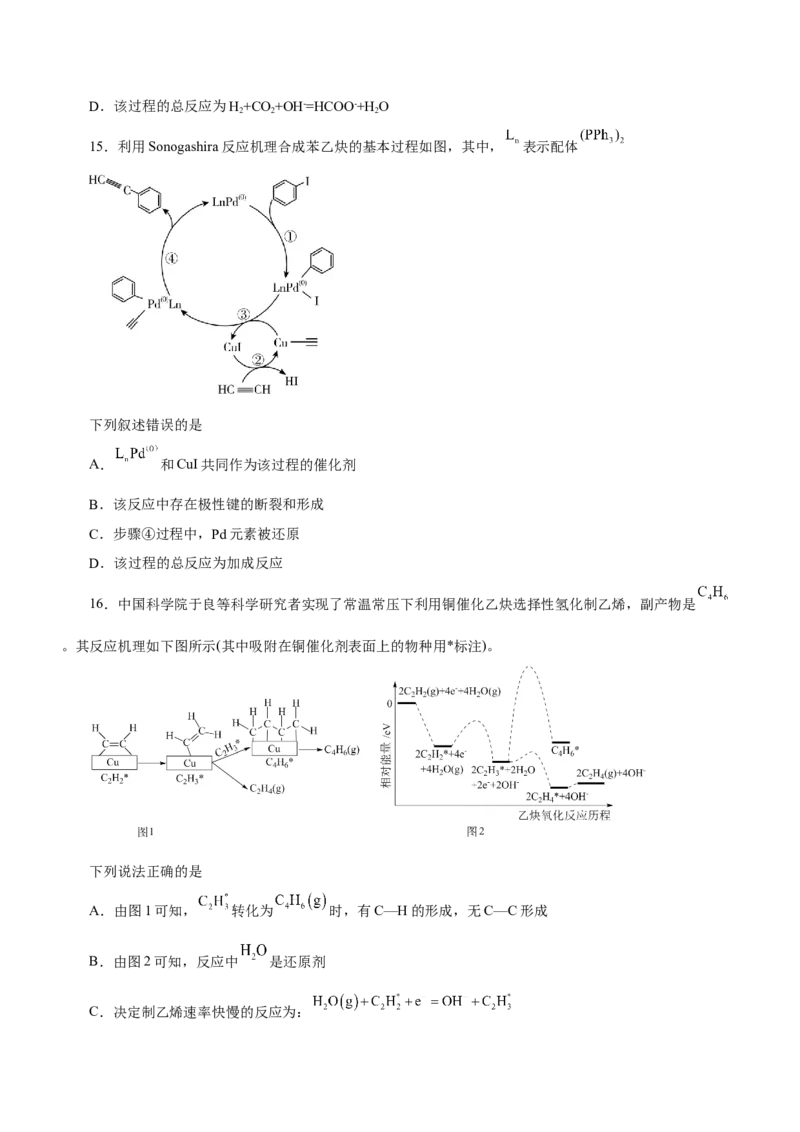
15.利用Sonogashira反应机理合成苯乙炔的基本过程如图,其中, 表示配体
下列叙述错误的是
A. 和CuI共同作为该过程的催化剂
B.该反应中存在极性键的断裂和形成
C.步骤④过程中,Pd元素被还原
D.该过程的总反应为加成反应
16.中国科学院于良等科学研究者实现了常温常压下利用铜催化乙炔选择性氢化制乙烯,副产物是
。其反应机理如下图所示(其中吸附在铜催化剂表面上的物种用*标注)。
下列说法正确的是
A.由图1可知, 转化为 时,有C—H的形成,无C—C形成
B.由图2可知,反应中 是还原剂
C.决定制乙烯速率快慢的反应为:D.生成 的速率比生成 的速率慢
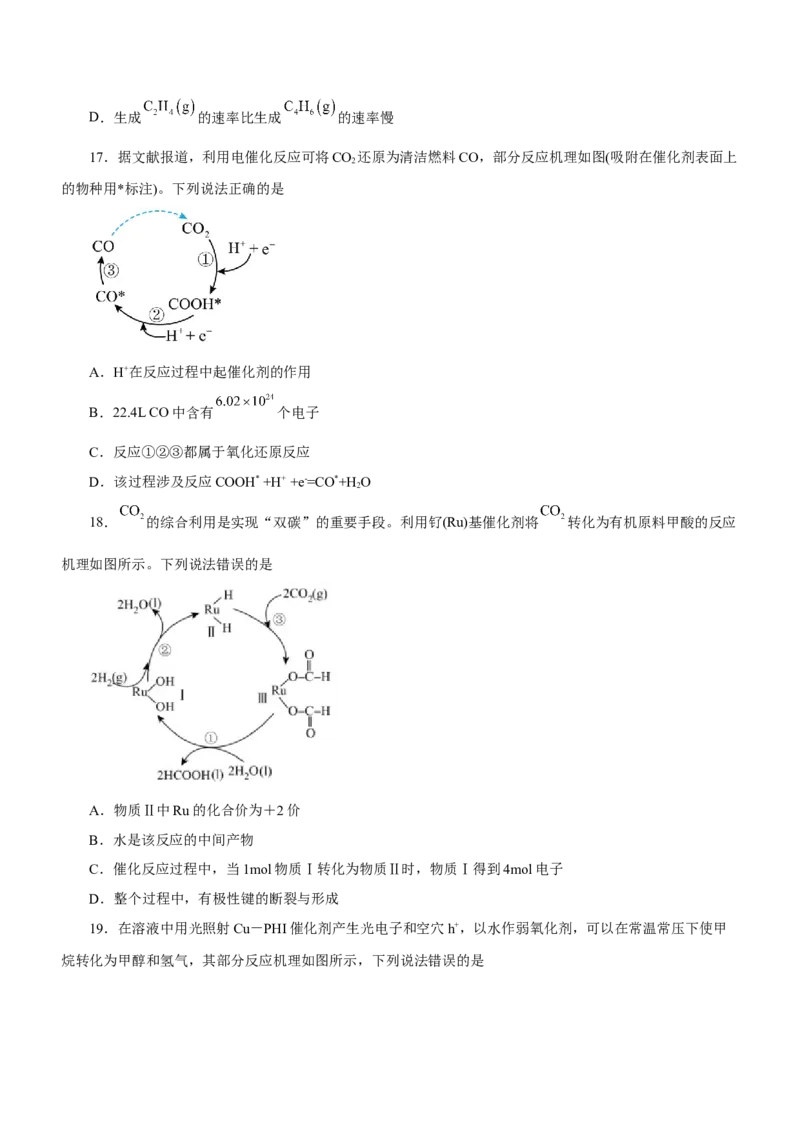
17.据文献报道,利用电催化反应可将CO 还原为清洁燃料CO,部分反应机理如图(吸附在催化剂表面上
2
的物种用*标注)。下列说法正确的是
A.H+在反应过程中起催化剂的作用
B.22.4L CO中含有 个电子
C.反应①②③都属于氧化还原反应
D.该过程涉及反应COOH* +H+ +e-=CO*+H O
2
18. 的综合利用是实现“双碳”的重要手段。利用钌(Ru)基催化剂将 转化为有机原料甲酸的反应
机理如图所示。下列说法错误的是
A.物质Ⅱ中Ru的化合价为+2价
B.水是该反应的中间产物
C.催化反应过程中,当1mol物质Ⅰ转化为物质Ⅱ时,物质Ⅰ得到4mol电子
D.整个过程中,有极性键的断裂与形成
19.在溶液中用光照射Cu-PHI催化剂产生光电子和空穴h+,以水作弱氧化剂,可以在常温常压下使甲
烷转化为甲醇和氢气,其部分反应机理如图所示,下列说法错误的是A.催化剂表面水转化为过氧化氢发生反应为2HO+2h+=H O+2H+
2 2 2
B.增加少量HO 可加快制备甲醇的速率
2 2
C.图中碳元素的化合价有两种
D.该反应的化学方程式为CH+H O CHOH+H
4 2 3 2
20.Burns和Dainton研究发现Cl 与CO合成COCl 的反应机理如下:
2 2
①Cl(g) 2Cl·(g) 快
2
②CO(g)+Cl·(g) COCl·(g) 快
③COCl·(g)+Cl(g) COCl (g)+Cl·(g) 慢
2 2
其中反应②存在v =k c(CO)c(Cl·)、v =k c(COCl·)k为速率常数,下列说法正确的是
正 正 逆 逆
A.反应②的平衡常数K=
B.反应①的活化能大于反应③的
C.要提高合成COCl 的速率,关键是提高反应①的速率
2
D.选择合适的催化剂能加快该反应的速率,并提高COCl 的平衡产率
2
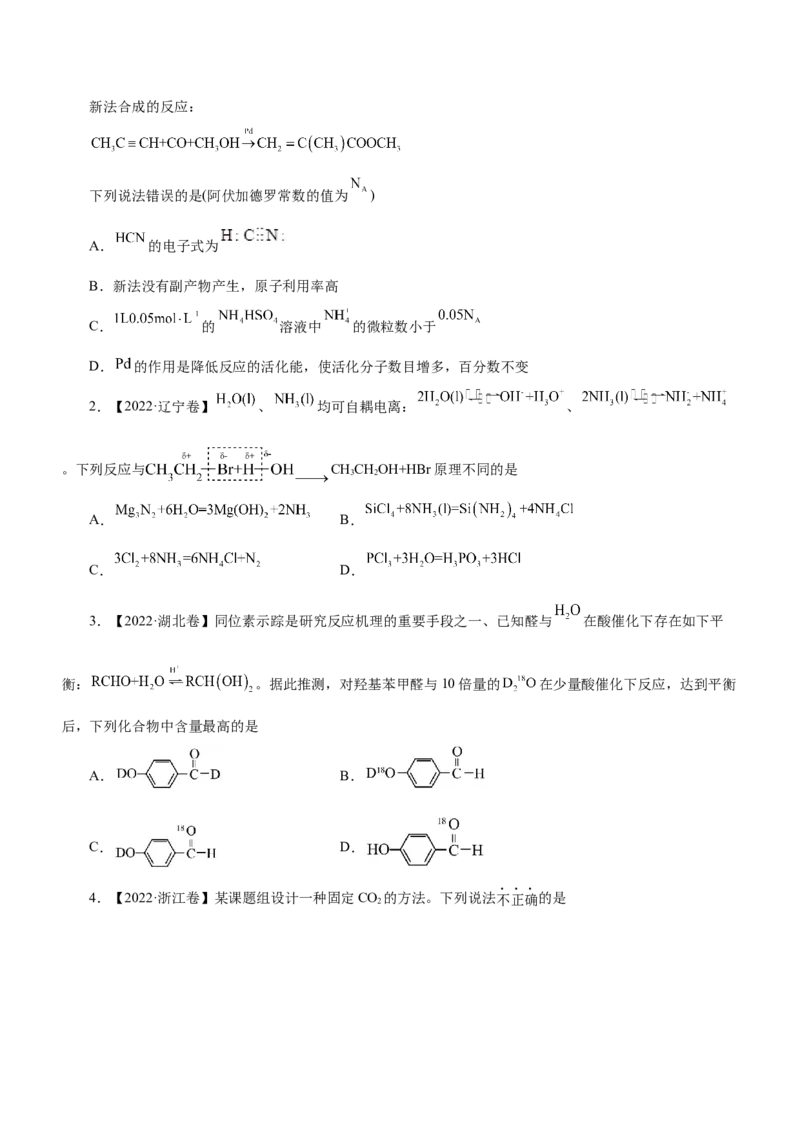
1.【2022·湖南卷】甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应:新法合成的反应:
下列说法错误的是(阿伏加德罗常数的值为 )
A. 的电子式为
B.新法没有副产物产生,原子利用率高
C. 的 溶液中 的微粒数小于
D. 的作用是降低反应的活化能,使活化分子数目增多,百分数不变
2.【2022·辽宁卷】 、 均可自耦电离: 、
。下列反应与 CHCHOH+HBr原理不同的是
3 2
A. B.
C. D.
3.【2022·湖北卷】同位素示踪是研究反应机理的重要手段之一、已知醛与 在酸催化下存在如下平
衡: 。据此推测,对羟基苯甲醛与10倍量的 在少量酸催化下反应,达到平衡
后,下列化合物中含量最高的是
A. B.
C. D.
4.【2022·浙江卷】某课题组设计一种固定CO 的方法。下列说法不正确的是
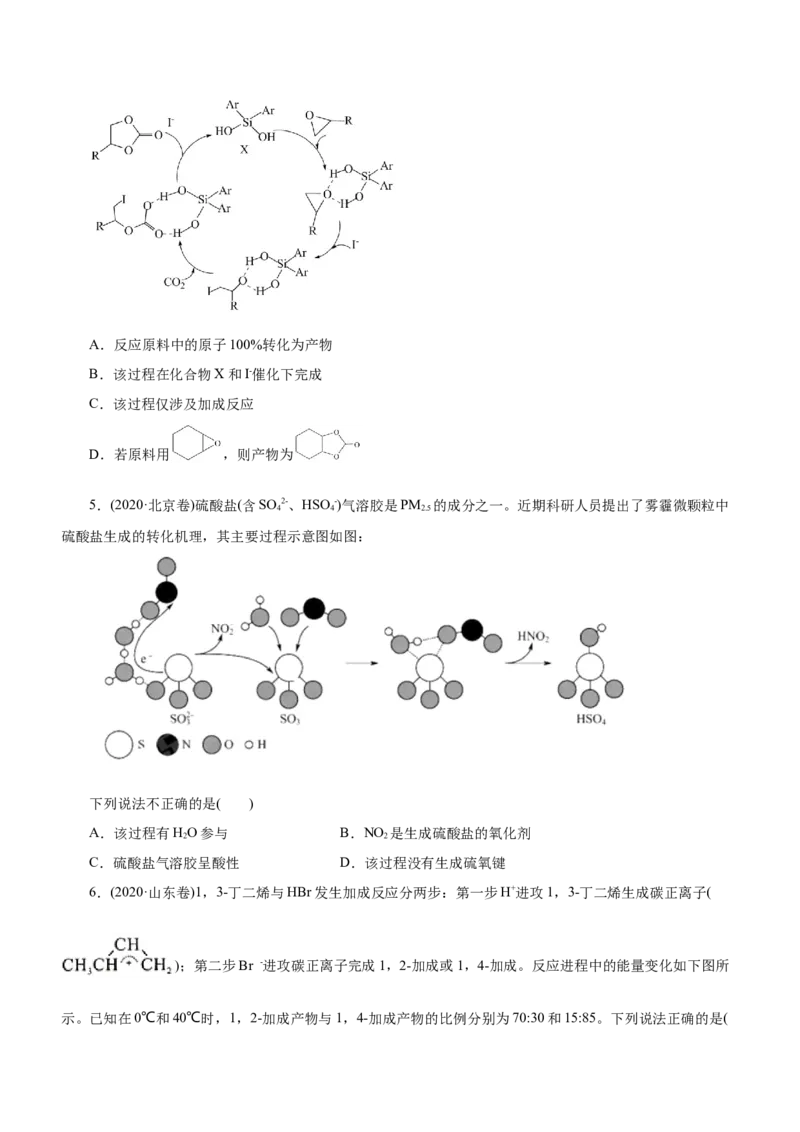
2A.反应原料中的原子100%转化为产物
B.该过程在化合物X和I-催化下完成
C.该过程仅涉及加成反应
D.若原料用 ,则产物为
5.(2020·北京卷)硫酸盐(含SO 2-、HSO -)气溶胶是PM 的成分之一。近期科研人员提出了雾霾微颗粒中
4 4 2.5
硫酸盐生成的转化机理,其主要过程示意图如图:
下列说法不正确的是( )
A.该过程有HO参与 B.NO 是生成硫酸盐的氧化剂
2 2
C.硫酸盐气溶胶呈酸性 D.该过程没有生成硫氧键
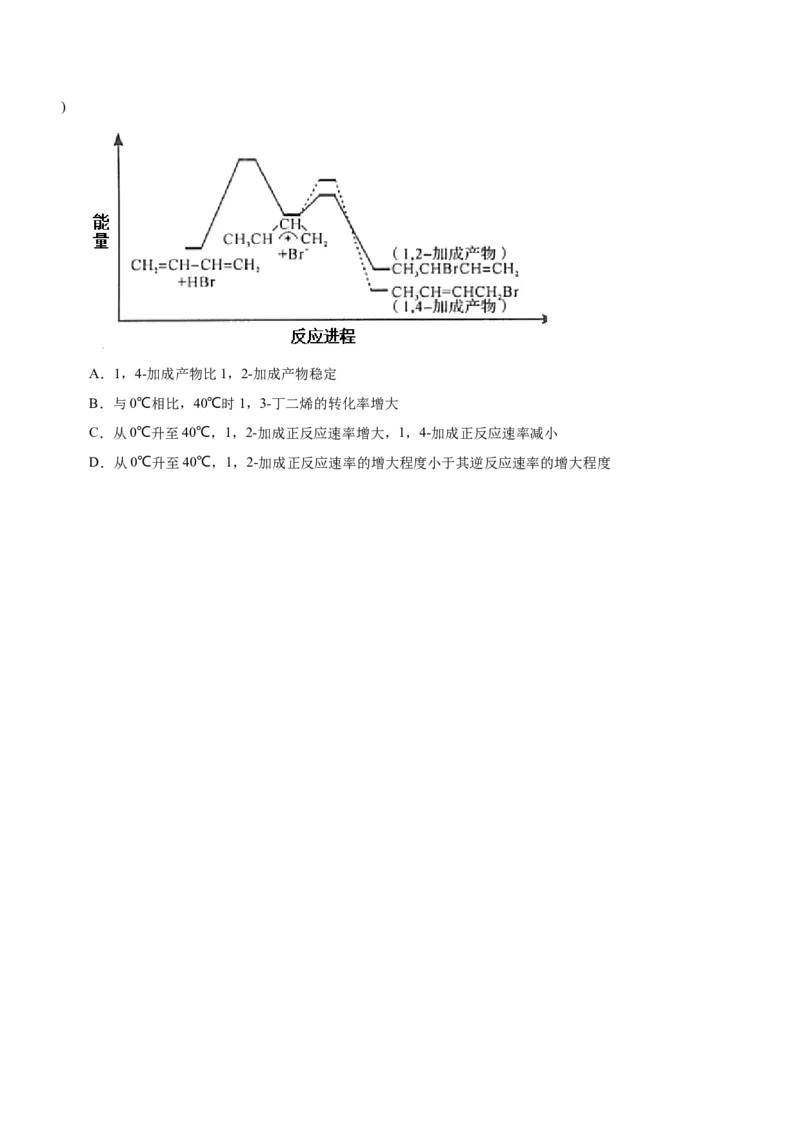
6.(2020·山东卷)1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正离子(
);第二步Br -进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所
示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是()
A.1,4-加成产物比1,2-加成产物稳定
B.与0℃相比,40℃时1,3-丁二烯的转化率增大
C.从0℃升至40℃,1,2-加成正反应速率增大,1,4-加成正反应速率减小
D.从0℃升至40℃,1,2-加成正反应速率的增大程度小于其逆反应速率的增大程度