文档内容
专题 16 化学实验综合(题型突破)
(考试时间:75分钟 试卷满分:100分)
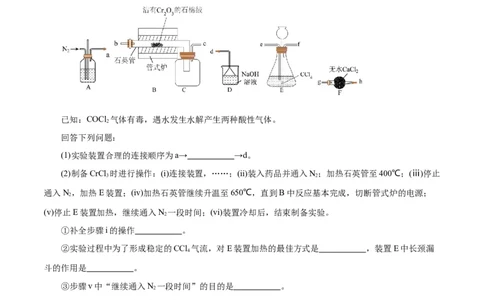
1.(14分)(2024·山东烟台高三期中)三氯化铬(CrCl )是常用的媒染剂和催化剂,易潮解,易升华,高温
3
下易被氧气氧化。实验室用Cr O 和CCl (沸点76.8℃)在高温下制备无水CrCl ,同时生成COCl 气体。实
2 3 4 3 2
验装置(加热及夹持装置略)如图所示。
已知:COCl 气体有毒,遇水发生水解产生两种酸性气体。
2
回答下列问题:
(1)实验装置合理的连接顺序为a→ →d。
(2)制备CrCl 时进行操作:(i)连接装置,……;(ii)装入药品并通入N;加热石英管至400℃;(ⅲ)停止
3 2
通入N,加热E装置;(iv)加热石英管继续升温至650℃,直到B中反应基本完成,切断管式炉的电源;
2
(v)停止E装置加热,继续通入N 一段时间;(vi)装置冷却后,结束制备实验。
2
①补全步骤i的操作 。
②实验过程中为了形成稳定的CCl 气流,对E装置加热的最佳方式是 ,装置E中长颈漏
4
斗的作用是 。
③步骤v中“继续通入N 一段时间”的目的是 。
2
(3)装置D中反应的离子方程式为 。
(4)测定CrCl 产品的纯度,实验如下:
3
①取mg CrCl 产品,在强碱性条件下,加入过量30%H O 溶液,小火加热使CrCl 完全转化为
3 2 2 3
CrO2-,继续加热一段时间;
4
②冷却后,滴入适量的稀硫酸和浓磷酸,使CrO2-转化为Cr O2-,加适量的蒸馏水配成250.00mL溶液;
4 2 7
③取25.00mL溶液,用新配制的 的NH )Fe(SO ) 标准溶液滴定至终点,重复3次,平均消耗
4 2 4 2
NH )Fe(SO ) 标准溶液VmL(已知Cr O2-被 还原为Cr3+)。
4 2 4 2 2 7则样品中CrCl (摩尔质量为M g·molˉ1)的质量分数为 %;若步骤③中所用标准溶液已变
3
质,将导致CrCl 质量分数测定值 (填“偏高”、“偏低”或“无影响”)。
3
【答案】(1)ef→bc→gh
(2) 检查装置气密性 (76.8°C以上)水浴加热 平衡压强(调节N 的气体流速、检验后面装置是
2
否堵塞) 将COCl 完全排入装置D被充分吸收
2
(3) COCl +4OH-=CO 2-+2Cl-+2H O
2 3 2
(4) 偏高
【解析】三氯化铬易潮解,易升华,高温下易被氧气氧化,所以实验过程中要确保装置内不能存在氧
气和水蒸气,A装置的作用是干燥N,E装置用N 将CCl 导入装置参与反应,F装置作用是防止水蒸气进
2 2 4
入反应装置,C装置作用是收集气体,D装置是处理COCl 尾气,B装置是发生装置。整个反应流程先用
2
干燥的N 排除装置内空气,然后再通入N 将CCl 气体带入装置,与B中的Cr O 反应,生成的COCl 有
2 2 4 2 3 2
毒气体用C装置收集,与D装置中NaOH溶液反应从而进行吸收处理,为防止D装置中水蒸气进入反应装
置,还有在C和D装置中间加一个干燥装置F。(1)实验装置合理的连接顺序为a→ef→bc→gh→d;(2)①有
气体参与或生成的实验,实验前必须先检查装置的气密性,故(i)连接装置,检查装置气密性;②实验过程
中为了形成稳定的CCl 气流,反应温度低于100°C,故对E装置加热的最佳方式是(76.8°C以上)水浴加热,
4
装置E中长颈漏斗的作用是平衡压强(调节N 的气体流速、检验后面装置是否堵塞);③COCl 有毒,结束
2 2
时用N 将COCl 完全排入装置D被充分吸收,防止污染空气;(3)装置D中可以看做是COCl 先与水反应
2 2 2
生成二氧化碳和氯化氢,二氧化碳和氯化氢再与氢氧化钠反应,故反应的离子方程式为COCl +4OH-=CO 2-
2 3
+2Cl-+2H O;(4)由得失电子守恒,原子守恒可知,测定过程中的物质的量的关系为:2CrCl ~2CrO2-~
2 3 4
Cr O2-~6(NH )Fe(SO ),产品中CrCl 的物质的量为: = ,产品中的CrCl 的质
2 7 4 2 4 2 3 3
量分数表达式为 ,产品中CrCl 的质量分数表达式为 %;若步骤③中所用标准溶
3
液已变质,则滴定时消耗的标准液体积偏大,将导致CrCl 质量分数测定值偏高。
3
2.(14分)(2024·黑龙江齐齐哈尔高三联考)四氮化四硫(S N)是重要的硫一氮二元化合物,室温下为橙
4 4
黄色固体,难溶于水,能溶于CCl 等有机溶剂,178~187℃熔化并分解,可用NH 与SCl 反应制备,某同
4 3 2
学利用如图装置(加热装置已略)制取SCl ,然后制取SN。
2 4 4已知:SCl 为红棕色液体,有刺激性臭味,熔点:−78℃,沸点:60℃,易水解。反应步骤如下:
2
①反应时先向C中通入干燥的氯气,使硫粉与氯气在50℃下反应生成SCl 。
2
②待C中的硫粉全部反应后,关闭B、C之间的止水夹,撤掉装置A、B。
③连接制氨的装置,通入氨,反应制得SN。
4 4
回答下列问题:
(1)仪器X的名称为 ,装置A中可用三氧化铬(还原产物中铬为+3价)与浓盐酸快速反应制
得氯气,写出反应的离子方程式: 。
(2)B装置中应选择的试剂为 ,装置D的作用为 。
(3)向制得的SCl 中通入NH ,生成SN 的同时还生成一种常见固体单质和一种盐,写出反应的化学方
2 3 4 4
程式: 。所得产物分离后,检验所得盐中阳离子的具体操作步骤和现象为 。
(4)S N 在碱性条件下发生水解反应氮元素转化为氨气,用硼酸吸收,滴定氨气释放量可进一步测定
4 4
SN 的纯度。称取1.100 g S N 样品,加入NaOH溶液,并加热,释放出的氨气用足量100 mL1 mol/L硼酸
4 4 4 4
吸收[反应方程式为2NH +4H BO=(NH)B O+5H O,假定反应过程中溶液体积不变]。反应后的溶液以
3 3 3 4 2 2 7 2
甲基红―亚甲蓝为指示剂,再用1 mol/L的盐酸[滴定反应方程式为(NH )B O+2HCl+5H O=2NH Cl+4
4 2 2 7 2 4
HBO]进行滴定,重复三次实验。实验数据记录如下表所示:
3 3
实验序号 初始读数(mL) 最终读数(mL)
Ⅰ 0.20 20.22
Ⅱ 0.40 24.85
Ⅲ 1.00 20.98
则制得的SN 的纯度为 (保留4位有效数字)。
4 4
【答案】(1) 分液漏斗 2CrO+12H++16Cl-=2Cr3++3Cl↑+6H O
3 2 2
(2)浓硫酸 防止空气中的水蒸气进入装置
(3) 6SCl +16NH=S N+2S↓+12NHCl 取少量固体粉末于试管中,加入NaOH溶液并加热,在试管
2 3 4 4 4
口放置湿润的红色石蕊试纸,若试纸变蓝色,则盐中的阳离子为NH +
4(4)83.64%
【解析】在装置A中用三氧化铬(还原产物中铬为+3价)与浓盐酸快速反应制得氯气,在装置B中用浓
硫酸干燥氯气,然后在装置C中用Cl、S反应制取SCl ,SCl 与NH 发生反应:
2 2 2 3
6SCl +16NH=S N+2S↓+12NHCl,最后尾气处理时,为防止水蒸气进入装置C,同时吸收多余的Cl,可
2 3 4 4 4 2
以使用盛有碱石灰的干燥管进行干燥处理。在滴定方法测定SN 的含量时,可根据反应中物质转化关系,
4 4
找到已知物与待求物之间关系,滤液关系式进行求解。(1)根据图示可知仪器X是分液漏斗;装置A中可用
三氧化铬(还原产物中铬为+3价)与浓盐酸快速反应制得氯气,根据电子守恒、电荷守恒、原子守恒,可得
反应的离子方程式为:2CrO+12H++16Cl-=2Cr3++3Cl↑+6H O;(2)装置B的作用是干燥氯气,由于Cl 是酸
3 2 2 2
性气体,与酸性干燥剂浓硫酸不反应,因此B装置中使用的干燥剂是浓硫酸;装置D的作用是防止空气中
的水蒸气进入装置C,同时进行尾气处理,吸收多余的Cl;(3)在装置C中Cl 与固体S发生反应制取得到
2 2
SCl ,SCl 又与通入的NH 发生反应制取得到SN,同时得到固体S单质及NH Cl,该反应的化学方程式
2 2 3 4 4 4
为:6SCl +16NH=S N+2S↓+12NHCl;反应产生的盐NH Cl中含有的阳离子是NH +,可根据其与强碱在
2 3 4 4 4 4 4
加热时反应产生有刺激性气味的NH ,NH 能够使湿润的红色石蕊试纸变为蓝色检验。故检验NH +的具体
3 3 4
操作步骤和现象为取少量固体粉末于试管中,加入NaOH溶液并加热,在试管口放置湿润的红色石蕊试纸,
若试纸变蓝色,则盐中的阳离子为NH +;(4)结合反应方程式和原子守恒可知反应的关系式:
4
SN~4NH~4HCl,分析实验数据:可知实验Ⅱ数据与其他两组相差较大,舍去,消耗盐酸溶液平均体积为
4 4 3
V(HCl)= ,所以n(S N) = n(HCl) = ×0.02 L× l mol/L=0.005 mo1,因此SN
4 4 4 4
的质量分数为: 。
3.(14分)(2024·广东广州高三联考)三氯化六氨合钴[Co(NH )]Cl ,在钴化合物的合成中是重要原料。
3 6 3
实验室以CoCl 为原料制备[Co(NH )]Cl ,步骤如下:
2 3 6 3
Ⅰ. CoCl 的制备。
2
CoCl 可以通过钴和氯气反应制得,实验室制备纯净CoCl 可用下图实验装置实现(已知:钴单质在
2 2
300℃以上易被氧气氧化,CoCl 易潮解)。
2(1)仪器Y的名称为 ,试剂Z为 。
(2)X中发生反应的化学方程式为 。
(3)装置的连接顺序为A→ →B(按气流方向,用大写字母表示,反应开始前应先点燃
处的酒精灯。
Ⅱ.三氯化六氨合钴(Ⅲ)的制备。
原理为:2CoCl +2NHCl+10NH +H O=2[Co(NH )]Cl +2H O
2 4 3 2 2 3 6 3 2
(4)水浴
温度不超过60℃的原因是 。
(5)加入浓盐酸,析出产品的离子方程式为 。
Ⅲ.测定[Co(NH )]Cl 中钴的含量。
3 6 3
(6)原理:利用 将KI氧化成 ,Co3+被还原为Co2+。然后用淀粉溶液作指示剂,
0.015mol·L-1NaSO 标准溶液滴定生成的 ,SO2-转化为SO2-。若称取样品的质量为0.27g,滴定 时,
2 2 3 2 3 4 6
达到终点消耗NaSO 标准溶液的平均体积为54.00mL。滴定终点的现象为 ,该样品中钴元素
2 2 3
的质量分数为 。
【答案】(1)直形冷凝管 碱石灰
(2)MnO +4HCl(浓) MnCl +Cl↑+2H O
2 2 2 2
(3) E→C→D A
(4)保证较快的反应速率,同时也可以减少氨气的挥发(或HO 的分解);由于双氧水易分解,所以水浴
2 2
温度不超过60℃的原因是防止双氧水分解
(5)[Co(NH )]3++3Cl-=[Co(NH )]Cl ↓
3 6 3 6 3
(6)当滴入最后一滴NaSO 标准溶液,溶液由蓝色褪为无色,并且半分钟内不再恢复蓝色 17.7%
2 2 3
【解析】A装置的作用是制取Cl,生成的Cl 中含有HCl和水蒸气,装置E的作用是除去Cl 中含有
2 2 2
的HCl,装置C的作用是除去Cl 中含有的水蒸气,装置D中氯气与金属Co加热反应生成CoCl ,CoCl 易
2 2 2
潮解,装置B中为碱石灰,其作用是防止空气中的水蒸气进入装置D中,同时吸收多余的Cl。(1)仪器Y
2
的名称为直形冷凝管;根据以上分析可知试剂Z是碱石灰;故装置的连接顺序为A→E→C→D→B;(2)X
中MnO 与浓盐酸反应加热生成Cl,发生的化学方程式为MnO +4HCl(浓) MnCl +Cl↑+2H O;(3)为排尽
2 2 2 2 2 2
装置中的空气,反应开始前应先点燃A处的酒精灯。(4)由于温度过高会导致氨气的挥发(或HO 的分解),
2 2
而温度较低时反应速率又太慢,不利于反应的发生,保持温度为60℃时,能够保证较快的反应速率,同时也可以减少氨气的挥发(或HO 的分解),则目的为保证较快的反应速率,同时也可以减少氨气的挥发(或
2 2
HO 的分解);(5)[Co(NH )]Cl 溶液中加入浓HCl,氯离子浓度增大,根据沉淀溶解平衡理论,平衡向生成
2 2 3 6 3
[Co(NH )]Cl 晶体的方向移动,所以加入浓HCl的目的是有利于[Co(NH )]Cl 析出,提高产率,则析出产
3 6 3 3 6 3
品的反应方程式为[Co(NH )]3++3Cl-=[Co(NH )]Cl ↓。(6)碘遇淀粉显蓝色,所以滴定至终点的现象是当滴
3 6 3 6 3
入最后一滴NaSO 标准溶液,溶液由蓝色褪为无色,并且半分钟内不再恢复蓝色;碘量法测定
2 2 3
[Co(NH )]Cl 中钴的含量,故用淀粉溶液作为指示剂;涉及反应方程式为2Co3++2I-=2Co2++I ,I+2S O2-
3 6 3 2 2 2 3
=2I-+S O2-,反应的关系式为2Co3+~I~2NaSO,硫代硫酸钠的物质的量为(0.015×0.054)mol=0.81×10-
4 6 2 2 2 3
3mol,则样品中钴元素的质量分数= =17.7%。
4.(14分)(2024·河南省部分学校高三第二次联考)硫化锂(Li S)广泛地应用于电池行业中。实验室可用
2
多种方法制备LiS。回答下列问题:
2
(1)以碳酸锂粉末与HS在600~700℃条件下制备LiS,实验装置如图所示(夹持仪器已省略):
2 2
1.HPO 溶液 2.NaS溶液 3.磁子 4.加热炉 5.反应管 6.石墨舟 7.NaOH溶液
3 4 2
①仪器X的名称为 ,写出X中发生反应的离子方程式: [已知
K (H PO )>K (H S)>K (H PO )]。
a1 3 4 a1 2 a2 3 4
②能否用稀硝酸代替HPO 溶液? (填“能”或“不能”),简述理由: (语言
3 4
叙述)。
③石墨舟中反应生成LiS的化学方程式为 。
2
(2)研究表明,高温下,LiSO 与焦炭反应也可以制备LiS。有同学认为气体产物中可能含有CO、CO
2 4 2 2
及SO ,为验证气体成分,选用下图所示的部分装置(可以重复选用)进行实验。
2①实验装置连接的合理顺序为气体产物→ →G→H→C。
②若F中品红未褪色,H中黑色粉末变为红色,G前的C中澄清石灰水不变浑浊,H后的C中澄清石
灰水变浑浊,则LiSO 与焦炭反应的化学方程式为 。
2 4
(3)测定产品LiS的纯度取产品ag于锥形瓶中,加入V mL c mol·L-1的硫酸(足量),充分反应后排尽
2 1 1
产生的气体,滴入2滴酚酞,用cmol·L-1的NaOH标准溶液进行滴定,达到滴定终点时,消耗NaOH标准
2
溶液的体积为VmL。
2
①达到滴定终点的现象是 。
②产品中LiS的质量分数为 。
2
【答案】(1) 三颈烧瓶 2HPO +S2-=2H PO -+H S↑ 不能 硝酸具有强氧化性会氧化S2-而
3 4 2 4 2
不能生成HS Li CO+H S LiS+ H O+CO↑
2 2 3 2 2 2 2
(2) F→E→F→C→D Li SO +4C LiS+4CO↑
2 4 2
(3)滴入最后半滴氢氧化钠溶液,溶液变浅红色,且半分钟内不变化
【解析】(1)①仪器X的名称为三颈烧瓶;已知K (H PO )>K (H S)>K (H PO ),可知HPO 溶液和
a1 3 4 a1 2 a2 3 4 3 4
NaS溶液反应的离子方程式为:2HPO +S2-=2 H PO -+H S↑;②不能用稀硝酸代替HPO 溶液,因为硝酸具
2 3 4 2 4 2 3 4
有强氧化性会氧化S2-而不能生成HS;③碳酸锂粉末与HS在600~700℃条件下制备LiS,石墨舟中反应
2 2 2
的化学方程式为:LiCO+H S LiS+ H O+CO↑;(2)①根据分析,实验装置连接的合理顺序为
2 3 2 2 2 2
气体产物→F→E→F→C→D→G→H→C;②若F中品红未褪色,H中黑色粉末变为红色,G前的C中澄清
石灰水不变浑浊,H后的C中澄清石灰水变浑浊,说明没有二氧化硫和二氧化碳生成,气体产物只有
CO,则LiSO 与焦炭反应的化学方程式为LiSO +4C LiS+4CO↑;(3)①达到滴定终点的现象是滴入最
2 4 2 4 2
后半滴氢氧化钠溶液,溶液变浅红色,且半分钟内不变化;②产品中LiS与硫酸反应生成硫化氢,剩余硫
2酸用氢氧化钠溶液滴定,可知LiS消耗的硫酸为 mol,则产品中LiS的物质的量为
2 2
mol,LiS的质量分数为 = 。
2
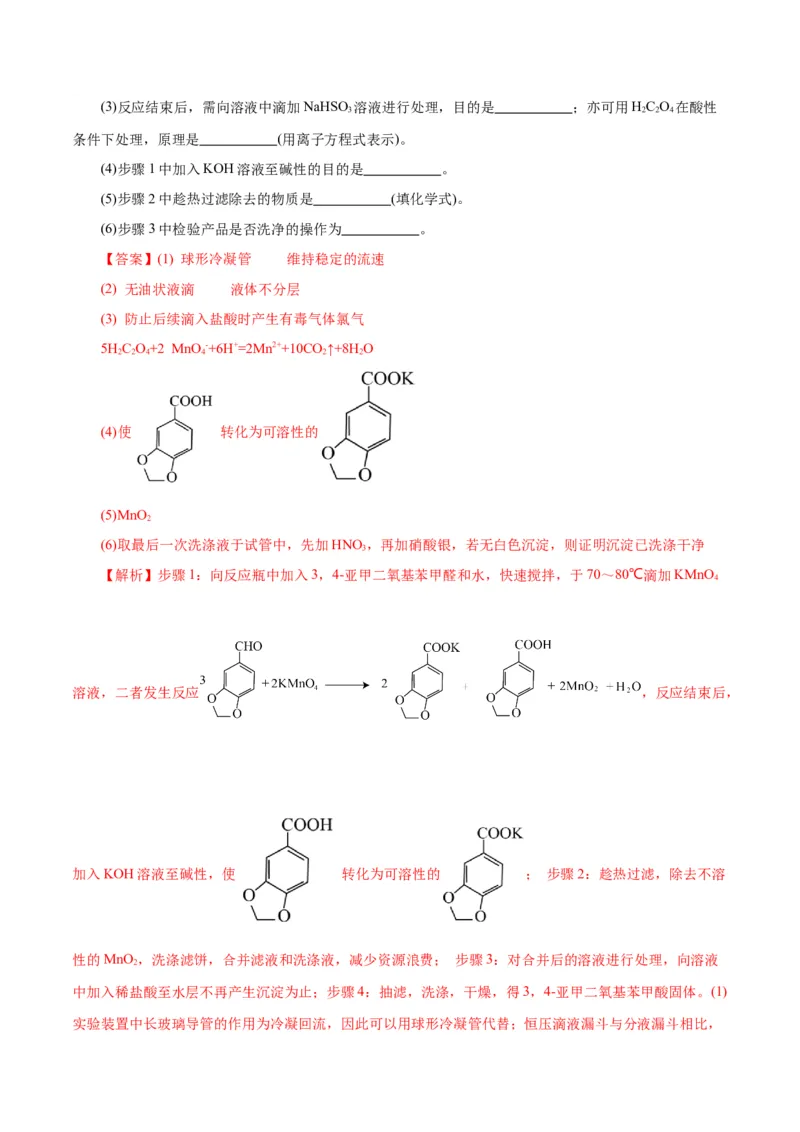
5.(14分)(2024·云南昆明五华高三教学质量检测)3,4-亚甲二氧基苯甲酸是一种用途广泛的有机合成
中间体,微溶于水,实验室可用KMnO 氧化3,4-亚甲二氧基苯甲醛(油状液体)制备,其反应方程式为:
4
实验步骤如下:
步骤1:向三颈烧瓶中加入一定量3,4-亚甲二氧基苯甲醛和水,快速搅拌,于70~80℃滴加稍过量的
酸性KMnO 溶液。缓慢开启搅拌器并加热。反应结束后,加入KOH溶液至碱性。
4
步骤2:趁热过滤,洗涤滤饼。合并滤液和洗涤液,向其中加入盐酸至水层不再产生沉淀。
步骤3:抽滤,洗涤,干燥,得3,4-亚甲二氧基苯甲酸固体。
回答下列问题:
(1)实验装置中长玻璃导管可用 代替(填仪器名称)。恒压滴液漏斗与分液漏斗相比,其优点
除平衡气压,使液体顺利流下之外,还有 。
(2)步骤1中观察到回流液中无 、 时,可判断制备反应已初步完成。(3)反应结束后,需向溶液中滴加NaHSO 溶液进行处理,目的是 ;亦可用HC O 在酸性
3 2 2 4
条件下处理,原理是 (用离子方程式表示)。
(4)步骤1中加入KOH溶液至碱性的目的是 。
(5)步骤2中趁热过滤除去的物质是 (填化学式)。
(6)步骤3中检验产品是否洗净的操作为 。
【答案】(1) 球形冷凝管 维持稳定的流速
(2) 无油状液滴 液体不分层
(3) 防止后续滴入盐酸时产生有毒气体氯气
5HC O+2 MnO -+6H+=2Mn2++10CO ↑+8H O
2 2 4 4 2 2
(4)使 转化为可溶性的
(5)MnO
2
(6)取最后一次洗涤液于试管中,先加HNO,再加硝酸银,若无白色沉淀,则证明沉淀已洗涤干净
3
【解析】步骤1:向反应瓶中加入3,4-亚甲二氧基苯甲醛和水,快速搅拌,于70~80℃滴加KMnO
4
溶液,二者发生反应 ,反应结束后,
加入KOH溶液至碱性,使 转化为可溶性的 ; 步骤2:趁热过滤,除去不溶
性的MnO ,洗涤滤饼,合并滤液和洗涤液,减少资源浪费; 步骤3:对合并后的溶液进行处理,向溶液
2
中加入稀盐酸至水层不再产生沉淀为止;步骤4:抽滤,洗涤,干燥,得3,4-亚甲二氧基苯甲酸固体。(1)
实验装置中长玻璃导管的作用为冷凝回流,因此可以用球形冷凝管代替;恒压滴液漏斗与分液漏斗相比,其优点除平衡气压,使液体顺利流下之外,由于其配备了压力控制装置,因此还可以维持稳定的流速;(2)
由于3,4-亚甲二氧基苯甲醛为油状液体且与水不相溶,因此当回流液中无油状液滴或液体不分层时,可
判断反应初步完成;(3)由于步骤1中滴加稍过量的酸性KMnO 溶液,因此反应后KMnO 剩余,若不将其
4 4
除掉,则后续滴入盐酸时产生有毒气体氯气;亦可用HC O 在酸性条件下处理,原理是5HC O+2 MnO -
2 2 4 2 2 4 4
+6H+=2Mn2++10CO ↑+8H O;(4)反应结束后,加入KOH溶液至碱性,目的使 转化为可溶
2 2
性的 ;(5)步骤2中,趁热过滤除去的物质难溶性的物质为MnO ;(6)由题意可知,产品中可
2
能混有的杂质为含氯离子的物质,因此只需取最后一次洗涤液于试管中,先加HNO,再加硝酸银,若无
3
白色沉淀,则证明沉淀已洗涤干净。
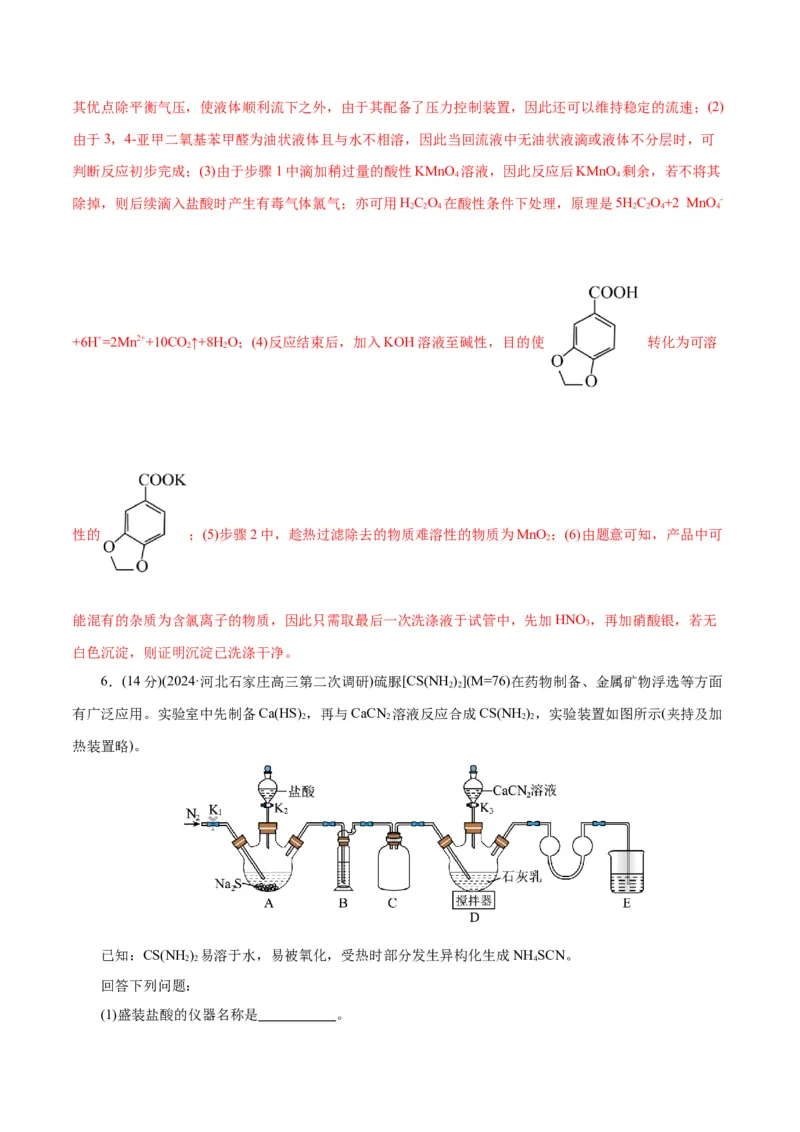
6.(14分)(2024·河北石家庄高三第二次调研)硫脲[CS(NH )](M=76)在药物制备、金属矿物浮选等方面
2 2
有广泛应用。实验室中先制备Ca(HS) ,再与CaCN 溶液反应合成CS(NH ),实验装置如图所示(夹持及加
2 2 2 2
热装置略)。
已知:CS(NH ) 易溶于水,易被氧化,受热时部分发生异构化生成NH SCN。
2 2 4
回答下列问题:
(1)盛装盐酸的仪器名称是 。(2)实验前先检查装置气密性,操作:
①在E中加水至浸没导管末端,……;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整 。
(3)检查装置气密性后加入药品,打开K 装置B中盛装的试剂为 。
2.
(4)关闭K,撤走搅拌器,打开K3,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见
2
的碱。控制温度不高于80℃的原因是 ,D处合成硫脲的化学方程式为 。
(5)将装置D中液体过滤后,结晶得到粗产品。
①称取mg产品,加水溶解配成500mL溶液。在锥形瓶中加入足量氢氧化钠溶液和n×10-3mol单质碘,
发生反应:6NaOH+3I =NaIO+5NaI+3H O,量取25.00mL硫脲溶液加入锥形瓶,发生反应:
2 3 2
NaIO +3CS(NH )=3HOSC(NH)NH +NaI。
3 2 2 2
②充分反应后加稀硫酸至酸性,发生反应:NaIO +5NaI+3H SO =3I +3Na SO +3H O,滴加两滴淀粉溶
3 2 4 2 2 4 2
液,用cmol/LNa SO 标准溶液滴定,发生反应:I+2Na SO=2NaI+Na SO 至终点时消耗标准溶液VmL。
2 2 3 2 2 2 3 2 4 6.
粗产品中硫脲的质量分数为 (用含“m、n、C、V的式子表示);若滴定时加入的稀硫酸量
不足,会导致所测硫脲的质量分数 (填“偏高”、“偏低”或“不变”)。(已知:
4NaIO +3Na SO+6NaOH=4NaI+6Na SO +3H O。)
3 2 2 3 2 4 2
【答案】(1)分液漏斗
(2)关闭开关K、K、K
1 2 3
(3)饱和硫氢化钠(NaHS)溶液
(4)硫脲[(CSNH )]受热时部分发生异构化生成NH SCN,故温度不能过高 Ca(HS) +2CaCN +6H O
2 2 4 2 2 2
2CS(NH )+3Ca(OH)
2 2 2
(5) 偏高
【解析】(1)盛装盐酸的仪器名称是分液漏斗;(2)实验前先检查装置的气密性,在E中加水至浸没导管
末端,关闭K、K、K 形成一个封闭体系,热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒
1 2 3
精灯,一段时间后,E处导管末端形成一段水柱,且高度不变,说明装置气密性良好。(3)反应生成硫化氢
气体含有挥发的氯化氢气体,装置B中盛装的实际为饱和硫氢化钠溶液,可以除去硫化氢气体;(4)已知:
CS(NH ) 易溶于水,易被氧化,受热时部分发生异构化生成NH SCN,故温度不能高于80℃,D处合成硫
2 2 4
脲的化学方程式为Ca(HS) +2CaCN +6H O 2CS(NH )+3Ca(OH) ;(5)反应关系式为3I~NaIO ,所以
2 2 2 2 2 2 2 3,可得到 ,则质量分数为
;若滴定时加入的稀硫酸量不足,会导致所测硫脲的质量分
数偏高。
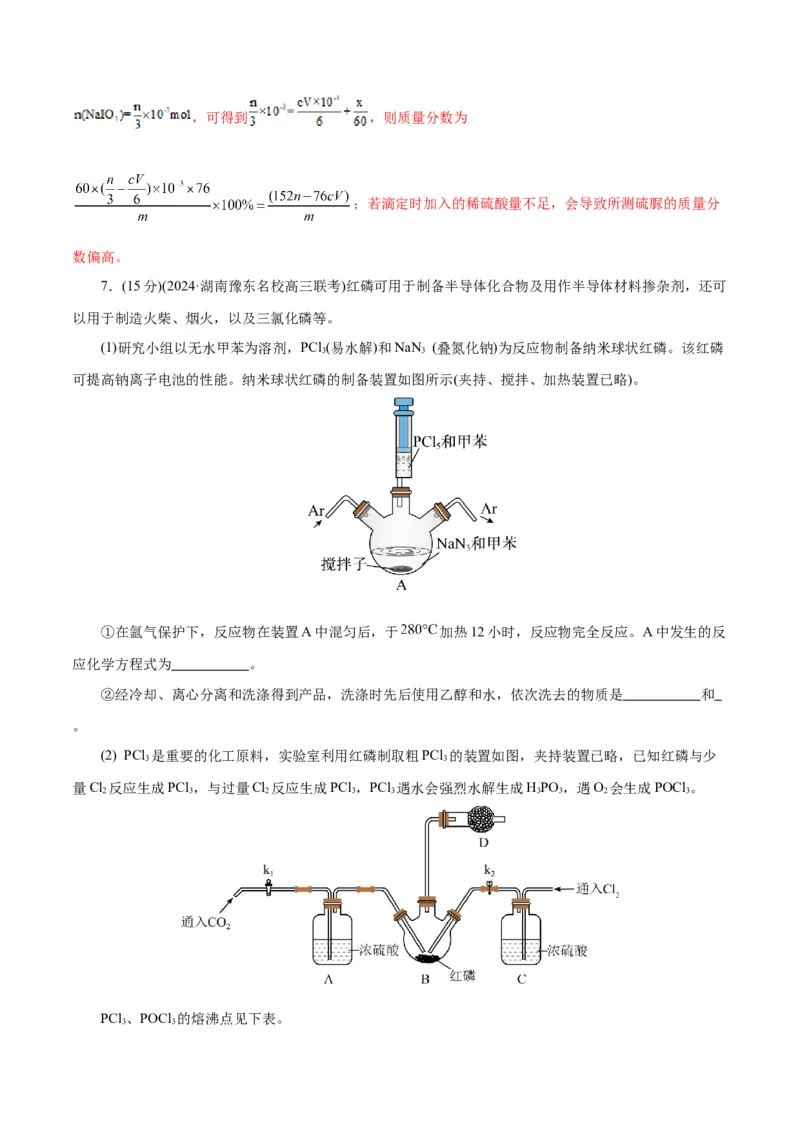
7.(15分)(2024·湖南豫东名校高三联考)红磷可用于制备半导体化合物及用作半导体材料掺杂剂,还可
以用于制造火柴、烟火,以及三氯化磷等。
(1)研究小组以无水甲苯为溶剂,PCl (易水解)和NaN (叠氮化钠)为反应物制备纳米球状红磷。该红磷
3 3
可提高钠离子电池的性能。纳米球状红磷的制备装置如图所示(夹持、搅拌、加热装置已略)。
①在氩气保护下,反应物在装置A中混匀后,于 加热12小时,反应物完全反应。A中发生的反
应化学方程式为 。
②经冷却、离心分离和洗涤得到产品,洗涤时先后使用乙醇和水,依次洗去的物质是 和
。
(2) PCl 是重要的化工原料,实验室利用红磷制取粗PCl 的装置如图,夹持装置已略,已知红磷与少
3 3
量Cl 反应生成PCl ,与过量Cl 反应生成PCl ,PCl 遇水会强烈水解生成HPO ,遇O 会生成POCl 。
2 3 2 3 3 3 3 2 3
PCl 、POCl 的熔沸点见下表。
3 3熔点
物质 沸点
PCl 75.5
3
POCl 1.3 105.3
3
回答下列问题:
①装置B中的反应需要 ,较适合的加热方式为 。
②制备Cl 可选用的仪器是 (填标号),其反应离子方程式为 。
2
③实验结束后,装置B中制得的PCl 粗产品中常混有POCl 、PCl 等。加入过量红磷加热可将PCl 转
3 3 3 5
化为PCl ,通过 (填操作名称),即可得到较纯净的PCl 产品。
3 3
④PCl 纯度测定
3
步骤I:取wg上述所得PCl 产品,置于盛有蒸馏水的水解瓶中摇动至完全水解,将水解液配成
3
溶液;
步骤II:取 上述溶液于锥形瓶中,先加入足量稀硝酸,一段时间后再加VmLc mol·L-1
1 1
AgNO 溶液(过量),使Cl-完全转化为AgCl沉淀(Ag PO 可溶于稀硝酸);
3 3 4
步骤III:以硫酸铁溶液为指示剂,用c mol·L-1KSCN溶液滴定过量的AgNO 溶液(AgSCN难溶于水),
2 3
达到滴定终点时,共消耗VmLKSCN溶液。
2
滴定终点的现象: ;产品中PCl 的质量分数为 %。
3
【答案】(1)10NaN +2PCl 2P+15N↑+10NaCl 甲苯 NaCl
3 5 2
(2) ①水浴加热 ②c 2MnO -+10Cl-+16H+= 2Mn2++5Cl↑+8H O
4 2 2
③蒸馏 ④当滴入最后半滴标准液后,溶液变成红色,且半分钟内不褪色
【解析】(1)①在氧气保护下,反应物在装置A中完全反应,PCl 和NaN 反应生成红磷、N 和NaCl,
3 3 2
其反应的化学方程式为10NaN +2PCl 2P+15N↑+10NaCl;②根据反应可知,得到的产物上站有甲苯
3 5 2和NaCl,用乙醇洗去甲苯,用水洗去NaCl;(2)①装置B中的反应需要65~70℃,不能用酒精灯直接加热,
则较适合的加热方式为水浴加热;②a、b适合块状固体和液体在常温下反应生成气体的反应,应选用高锰
酸钾和浓盐酸制取氯气,用c装置,其反应的离子方程2MnO -+10Cl-+16H+= 2Mn2++5Cl↑+8H O;③实验
4 2 2
结束后,装置B中制得的PCl 粗产品中常混有POCl 、PCl 等,加入过量红磷加热可将PCl 转化为PCl ,
3 3 3 3 3
根据PCl 和POCl 的沸点相差较大,则通过蒸馏方法得到较纯净的PCl 产品;④根据PCl 遇水会强烈水解
3 3 3 3
生成HPO ,则步骤Ⅰ中发生反应的化学方程式为PCl +3H O=HPO +3HCl,产品中PCl 的质量分数为
3 3 3 2 3 3 3
。